Comunicaciones
TAMIZAJE Y CUANTIFICACIÓN DE FITOQUÍMICOS EN Vanilla pompona BAJO DOS AMBIENTES
SCREENING AND QUANTITATION OF PHYTOCHEMICALS OF VANILLA POMPONA UNDER TWO ENVIRONMENTS
TRIAGEM E QUANTIFICAÇÃO DE FITOQUÍMICOS EM VANILLA POMPONA SOB DOIS AMBIENTES
TAMIZAJE Y CUANTIFICACIÓN DE FITOQUÍMICOS EN Vanilla pompona BAJO DOS AMBIENTES
Interciencia, vol. 44, núm. 10, pp. 571-578, 2019
Asociación Interciencia
Recepción: 02 Mayo 2019
Aprobación: 07 Noviembre 2019
Resumen: Las plantas producen fitoquímicos que sirven de protección ante factores bióticos y abióticos. Esta investigación tuvo como objetivo detectar y cuantificar la concentración de compuestos fenólicos totales (CFT), flavonoides totales (FLAVT), triterpenos totales (TRIT) y saponinas totales (SAPT) en hoja, tallo, flor y fruto de Vanilla pompona provenientes de las localidades de Cazuelas, Veracruz y de Morelos, Oaxaca, México. Los fitoquímicos se detectaron por cromatografía en capa fina (CCF) y la cuantificación se realizó por métodos espectrofotométricos. Las pruebas por CCF revelaron presencia de saponinas, flavonoides y ácidos fenólicos principalmente en extractos de metanol y de terpenos en el extracto de hexano de las estructuras analizadas de V. pompona en las dos localidades. Las estructuras procedentes de la localidad de Morelos tuvieron la concentración mayor de CFT (0,382 ±0,152g·100g-1) y de FLAVT (0,989 ±0,150g·100g-1), y aquellas de Cazuelas presentaron la concentración mayor de TRIT (7,054 ±5,721g·100g-1) y SAPT (3,310 ±1,106g·100g-1). Por estructura, los frutos tuvieron la concentración mayor de CFT (0,501 ±0,133g·100g-1) y TRIT (19,790 ±2,662g·100g-1), mientras que la hoja y flor destacaron por presentar la concentración mayor de FLAVT (1,101 ±0,136 y 1,033 ±0,078g·100g-1). Los dos primeros factores del análisis de correlaciones canónicas explicaron 99,72% de la varianza total, lo cual mostró que a mayor temperatura y humedad del suelo el contenido de TRIT y SAPT aumenta. Los resultados permitieron conocer que la concentración de los fitoquímicos de V. pompona varió en función de ambiente, localidad y tipo de tejido.
Palabras clave: Estructuras Reproductivas , Estructuras Vegetales , Metabolitos Secundarios , Vanilla pompona .
Resumo: As plantas produzem fitoquímicos que servem de proteção diante de fatores bióticos e abióticos. Esta investigação teve como objetivo detectar e quantificar a concentração de compostos fenólicos totais (CFT), flavonóides totais (FLAVT), triterpenos totais (TRIT) e saponinas totais (SAPT) em folha, caule, flor e fruto de Vanilla pompona provenientes das localidades de Cazuelas, Veracruz e de Morelos, Oaxaca, México. Os fitoquímicos foram detectados por cromatografia em camada fina (CCF) e a quantificação foi realizada por métodos espectrofotométricos. As provas por CCF revelaram presença de saponinas, flavonóides e ácidos fenólicos principalmente em extratos de metanol e de terpenos no extrato de hexano das estruturas analisadas de V. pompona nas duas localidades. As estruturas procedentes da localidade de Morelos tiveram concentração maior de CFT (0,382 ±0,152g·100g-1) e de FLAVT (0,989 ±0,150g·100g-1), e aquelas de Cazuelas apresentaram concentração maior de TRIT (7,054 ±5,721g·100g-1) e SAPT (3,310 ±1,106g·100g-1). Por estrutura, os frutos tiveram concentração maior de CFT (0,501 ±0,133g·100g-1) e TRIT (19,790 ±2,662g·100g-1), enquanto que a folha e flor destacaram-se por apresentar concentração maior de FLAVT (1,101 ±0,136 e 1,033 ±0,078g·100g-1). Os dois primeiros fatores da análise de correlações canónicas explicaram 99,72% da variância total, o qual mostrou que enquanto maior temperatura e umidade do solo, maior o conteúdo de TRIT e SAPT. Os resultados permitiram conhecer que a concentração dos fitoquímicos de V. pompona variou em função do ambiente, localidade e tipo de tecido.
Abstract: Plants produce phytochemicals that help protect against biotic and abiotic factors. This research aimed to detect and quantify the concentration of total phenolics compounds (TPC), total flavonoids (TFLAV), total triterpenes (TTRI) and total saponins (TSAP) present in leaf, stem, flower and fruit of Vanilla pompona from the localities of Cazuelas, Veracruz and of Morelos, Oaxaca, Mexico. Phytochemicals were detected by thin layer chromatography (TLC) and quantification was carried out by spectrophotometric methods. TLC tests revealed the presence of saponins, flavonoids and phenolic acids mainly in methanol extracts and terpenes in the hexane extract of the analyzed structures of V. pompona in the two localities. Plant structures from the locality of Morelos had the highest concentration of TPC (0.382 ±0.152g·100g-1) and TFLAV (0.989 ±0.150g·100g-1), while Cazuelas stood out for having the highest concentration of TTRI (7.054 ±5.721g·100g-1) and TSAP (3.310 ±1.106g·100g-1). By structure, the fruits had the highest concentration of TPC (0.501 ±0.133g·100g-1) and TTRI (19.790 ±2.662g·100g-1), while the leaf and flower stood out for having the highest concentration of TFLAV (1.101 ±0.136 and 1.033 ±0.078g·100g-1). The first two factors of the canonical correlation analysis explained 99.72% of the total variance, which shows that at higher temperature and soil moisture the content of TTRI and TSAP increases. The results revealed that the concentration of phytochemicals of V. pompona varied depending on the environment, location and type of tissue.
Introducción
En México se reconocen nueve especies de Vanilla (Soto-Arenas, 2009) de las cuales, por el desarrollo de sabor y aroma característico del fruto beneficiado (curado y deshidratado), tienen importancia comercial tres especies: Vanilla planifolia Jacks. ex Andrews, V. tahitensis J.W. Moore, y V. pompona Schiede (Ramachandra y Ravishankar, 2000). En el contexto general, V. pompona se registra como la tercera especie en importancia comercial, atrás de V. planifolia y V. tahitensis, porque se cultiva en menor escala, aunque tiene uso en preparaciones farmacéuticas y perfumería, por la presencia de compuestos característicos y diferenciales de las otras especies (Ehlers y Pfister, 1997). En México se ha reportado la presencia de V. pompona en condiciones silvestres, así como pequeñas plantaciones cultivadas en los estados de Oaxaca, Nayarit, Michoacán, Guerrero, Veracruz y Jalisco (Herrera-Cabrera et al., 2017).
La mayoría de los estudios que han generado información sobre el aroma y otros fitoquímicos del género Vanilla se enfocan en los frutos beneficiados de V. planifolia (Ranadive, 1992; Pérez-Silva et al., 2006;Salazar-Rojas et al., 2012). Recientemente, también se han descrito diferencias en la concentración de los fitoquímicos (fenólicos totales, flavonoides, saponinas, triterpenos, taninos totales, condensados e hidrolizables) de plantas de V. planifolia procedentes de la Huasteca Potosina, en San Luis Potosí (Andradre-Andrade et al., 2018) y de la región del Totonacapan, en Puebla-Veracruz (Ibarra-Cantún et al., 2018), atribuidas al manejo del cultivo y a las condiciones ambientales en que se desarrolla la planta.
Los fitoquímicos son sintetizados a partir del metabolismo secundario y no se relacionan directamente con los procesos primarios del desarrollo y crecimiento de las plantas (Mazid et al., 2011). Su biosíntesis se estimula por la interacción con el medio ambiente; como agentes alelopáticos, relaciones de mutualismo en la atracción de polinizadores, funciones defensivas al causar toxicidad como mecanismo de defensa ante herbívoros, entre otras funciones. Por lo que, en especies vegetales, los metabolitos secundarios son utilizados para adaptarse a condiciones tales como temperatura, humedad, salinidad, radiación UV y estrés químico (Akula y Ravishankar, 2011). En los últimos años ha cobrado importancia el uso de compuestos de origen natural para su aplicación en la industria farmacéutica, perfumería, insecticidas y como saborizantes (Teoh, 2016).
V. pompona es una especie prioritaria dentro del acervo genético secundario de V. planifolia (Soto-Arenas y Dressler, 2010) por poseer características sobresalientes a los principales problemas que se enfrenta esta última, tales como resistencia a antracnosis (Collectotrichum sp.), pudrición de raíz (Fusarium oxysporum Schltdl) y climas xerofitos (Soto-Arenas, 1999; Hernández-Hernández y Lubinsky, 2011). Por ello, dada la limitada información sobre V. pompona, es de interés analizar y conocer el tipo de fitoquímicos que presentan las diferentes estructuras de la planta. En la especie se ha descrito en particular a los compuestos del aroma en el fruto beneficiado (Ehlers y Pfister, 1997;Galeas et al., 2015, 2016) y a compuestos químicos de frutos de diferentes etapas de madurez (Maruenda et al., 2013). Sin embargo, no se ha documentado en la literatura el tipo de fitoquímicos presentes en las estructuras vegetales y florales de V. pompona y se han omitido los estudios donde se consideren las condiciones ambientales en las que crece.
Bajo la hipótesis que la presencia de fitoquímicos en hojas, tallos, flores y frutos de V. pompona varía en relación con la estructura y la localidad de recolecta, el trabajo tuvo como objetivo detectar mediante pruebas cualitativas los grupos de fitoquímicos (saponinas, alcaloides, taninos, ácidos fenólicos, flavonoides, y terpenos) presentes en extractos de diferente polaridad y conocer la concentración de los compuestos fenólicos, flavonoides, terpenos y saponinas totales en hoja, tallo, flor y fruto de V. pompona. Además, se determinó la influencia de la condición ambiental en la que crecen las plantas con relación a la concentración de fitoquímicos, mediante la evaluación de dos sitios de recolecta: Cazuelas Papantla, Veracruz y Morelos Santa Cruz Itundujia, Oaxaca, México.
Materiales y Métodos
Durante el periodo de floración se recolectaron esquejes de V. pompona de 1m de longitud, de la base a la punta, para obtener hojas, tallos y flores (mayo 2016). Los frutos se recolectaron 31 semanas después de la polinización. Las muestras se obtuvieron de dos plantaciones contrastantes: la primera de una plantación cultivada (introducida) teniendo como tutores arboles de cedro blanco (Cedrela odorata L.), sin manejo agronómico y con 10 años de antigüedad en la localidad de Cazuelas, municipio de Papantla, Veracruz, México; y la segunda una población silvestre de V. pompona dentro de un bosque de árboles de pino (Pinus patula Schiede) y encino (Quercus sp.) en la localidad de Morelos, municipio de Santa Cruz Itundujia, Oaxaca, México (Soto-Arenas y Dressler, 2010).
Para describir las características climáticas se empleó la ubicación geográfica de las localidades y las capas temáticas de clima (CONABIO, 1998a), precipitación (CONABIO, 1998b), temperatura media anual (CONABIO, 1998c), régimen de humedad (Maples-Vermeersch, 1992) y zonas ecológicas (Toledo y Ordoñez, 2009). Las principales características de las localidades se muestran en la Tabla I.
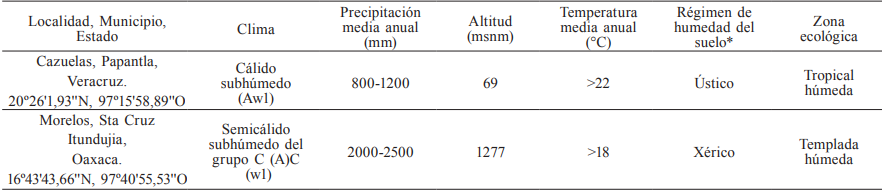
Fuente: CONABIO (1998a, b, c).* Ústico: 180 a 270 días de humedad; Xérico: 90 a 180 días de humedad.
Análisis cualitativo
Estudio por cromatografía en capa fina (CCF)
Las estructuras vegetales utilizadas se almacenaron de una a dos semanas a una temperatura de -20ºC antes de la preparación de los extractos.
Preparación de extractos
Se utilizaron disolventes de diferente polaridad (metanol y hexano). Las estructuras vegetales (hoja y tallo) y reproductivas (flor y fruto) se cortaron en pequeñas porciones y se les agregó disolvente hasta cubrirlas totalmente de manera individual. Las muestras se colocaron en un baño ultrasónico (Ultrasonic Cleaner AS5150B) durante 30min a temperatura ambiente. Posteriormente, los extractos (200mg·ml-1) se dejaron en maceración por 12h a 4ºC y se almacenaron a -20ºC hasta su uso.
Identificación de los grupos de compuestos
En placas de gel de sílice 60, F254 (Sigma-Aldrich; No. Cat. Z193275) se aplicaron de 15 a 20µl de los extractos en forma de punto, dejando 0,5cm de separación entre cada punto de aplicación. Los eluyentes y agentes cromogénicos fueron específicos para la detección de cada grupo de metabolitos (Wagner y Bladl, 1996) y la determinación se realizó por duplicado. En el caso de flavonoides las placas se visualizaron con luz ultravioleta (UVLMS-38 series 3UVTM Lamp) a 254 y 365nm.
Análisis cuantitativo
Preparación de extractos
Previo al análisis de fitoquímicos, a todos los tejidos se les determinó el contenido de humedad en termobalanza (Ohaus MB45), para expresar la concentración de los metabolitos secundarios con base en materia seca (MS).
Compuestos fenólicos totales (CFT) y flavonoides totales (FLAVT)
De cada tejido fresco (hoja, tallo, flor y fruto) se prepararon extractos en metanol a una concentración inicial de 500mg·ml-1, posteriormente se realizaron diluciones que dependían de la estructura vegetal y reproductiva de V. pompona. Las muestras se colocaron en un baño ultrasónico (Ultrasonic Cleaner AS5150B) durante 30min a temperatura ambiente. Después los extractos se dejaron en maceración por 12h a 4ºC, y se almacenaron a -20ºC hasta su uso.
Saponinas totales
De cada estructura se prepararon extractos en agua (200mg·ml-1). Las muestras se colocaron en un baño ultrasónico (Ultrasonic Cleaner AS5150B) por un lapso de 30min a temperatura ambiente. Posteriormente, los extractos se maceraron por 12h a 4ºC y se filtraron y almacenaron en viales de vidrio a -20oC hasta su análisis.
Triterpenos totales
Se pesó 1g de muestra fresca, se añadió 10ml de etanol 75% y se dejó reposar a temperatura ambiente por 10h. La muestra se sometió a baño ultrasónico (Ultrasonic Cleaner AS5150B) por 40min a 60°C, se centrifugó a 2350g durante 5min a 4°C. El sobrenadante se evaporó en rotaevaporador (Heidolph, Laborota 4000). La solución se guardó a 4°C durante 12h, y se centrifugó a 2350g por 5min. Posterior-mente el etanol se evaporó por completo. El residuo se extrajo cuatro veces con butanol:agua (1:1; v/v). La fase acuosa se descartó y la fase orgánica se evaporó en rotaevaporador. Al residuo se le añadió éter etílico y se almaceno a 4°C por 12h, se centrifugo y se descartó el disolvente. Con el residuo sólido se preparó una solución muestra a una concentración de 0,5mg·ml-1 disuelto en etanol a 100%. Los extractos se almacenaron en viales de vidrio a -20oC hasta su análisis (Zhong-Cheng et al., 2014).
Cuantificación de fitoquímicos
Compuestos fenólicos totales
Se utilizó el método colorimétrico de Folin-Ciocalteau (Herald et al., 2012) con algunas modificaciones (se utilizó agua desionizada, se leyó la absorbancia a 725nm, y hubo un tiempo de reposo de 60min). Se registró la absorbancia a 725nm en un espectrofotómetro de microplaca (UV-Vis; Thermo Scientific Varioskan Flash). Se obtuvo una curva estándar (y= 0,0089x+0,0002; r2= 0,99) con ácido gálico (Sigma Aldrich, No Cat. G7384). Los resultados se expresaron en mg equivalentes de ácido gálico por 100g de materia seca (MS).
Flavonoides totales
Su contenido se obtuvo con base en el método de Silva-Beltrán et al. (2015) con una modificación (lectura de la absorbancia a 415nm). Se determinó la absorbancia a 415nm en el espectrofotómetro de microplaca UV-Vis (Thermo Scientific Varioskan Flash). Se obtuvo una curva estándar (y= 0.001x+0.0209; r2= 0.99) con quercetina (Sigma Aldrich, No Cat. Q4951). El contenido de flavonoides totales se expresó en equivalentes de quercetina en g·100g-1 MS.
Triterpenos totales
Se utilizó el método colorimétrico basado en Chang y Lin (2012) con una modificación (lectura de la absorbancia a 550nm). La absorbancia fue medida a 550nm en un espectrofotómetro UV/Vis (Evolution 300, Thermo Scientific). La curva estándar (y= 0,0011x+0,0107; r2= 0,99) se preparó con ácido oleanólico (Sigma Aldrich, No Cat. 05504). El contenido de triterpenos totales se expresó en equivalentes de ácido oleanólico en g·100 g-1 MS.
Saponinas totales
Se analizaron de acuerdo al método de Ahmed y Wang (2015), con la modificación de utilizar ácido sulfúrico 72%. La absorbancia fue medida a 544nm en un espectrofotómetro UV/Vis (Evolution 300, Thermo Scientific). Los resultados se expresaron en g·100g-1 MS de acuerdo con la ecuación de la curva estándar (y= 0,0003x+0,0059; r2= 0,99) realizada con saponina quillaje (Sigma Aldrich, No Cat. 57900).
Análisis estadístico
Para los resultados de número de bandas de las pruebas cualitativas por cromatografía en capa fina, se realizaron tablas de contingencia mediante el programaSPSS (ver. 19). La concentración de los compuestos fenólicos totales, flavonoides totales, saponinas totales y triterpenos totales, de nueve repeticiones de hoja y tallo, y cuatro repeticiones para flor y fruto de cada localidad de recolecta, fueron analizados bajo un modelo equivalente al diseño completamente al azar. Se realizó un análisis de varianza y comparación de medias mediante la prueba de Tukey (α=0,05) con el paquete estadístico SAS versión 9.0 (SAS, 2002). Para corroborar si el ambiente tuvo efecto en la producción de fitoquímicos, se procedió a identificar asociaciones entre variables ambientales (altitud, precipitación media anual, temperatura media anual y régimen de humedad del suelo) y concentración de fitoquímicos mediante un análisis de correlaciones canónicas por medio del procedimiento PROC CANCORR (SAS, 2002).
Resultados y Discusión
Análisis cualitativo de fitoquímicos por cromatografía en capa fina (CCF)
Los grupos de fitoquímicos que fueron identificados por CCF presentaron diferente número de bandas y variación entre los tejidos (Tabla II). Las saponinas, compuestos de naturaleza triterpenicas o esteroidal, se revelaron en mayor cantidad de bandas (21 a 23 bandas) entre los fitoquímicos estudiados; su abundancia se puede considerar como una respuesta a factores ambientales y como parte de una estrategia de adaptación ambiental que conduce a tolerancia a estrés abiótico (Akula y Ravishankar, 2011). Datos similares se reportaron en Panax ginseng, especie perenne, donde las saponinas se detectaron en raíz, bulbo, hoja, tallo, flor y fruto y su acumulación dependió de factores abióticos ambientales (Szakiel et al., 2011). También se han detectado en V. planifolia primordialmente en hoja, tallo y flor (Andrade-Andrade et al., 2018), donde su presencia varió en relación con el tejido y la localidad de recolecta.
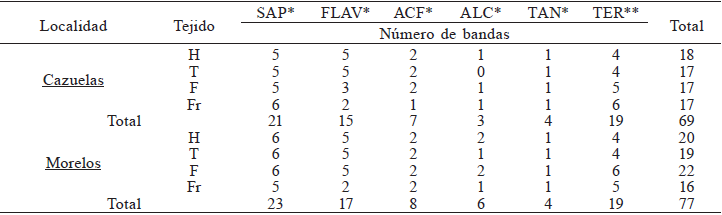
H: hoja, T: tallo, F: flor, Fr: fruto; SAP: saponinas, FLAV: flavonoides, ACF: ácidos fenólicos, ALC: alcaloides, TAN: taninos, TER: terpenos. *Extractos de metanol de saponinas, flavonoides, ácidos fenólicos, alcaloides y taninos. **Extracto de hexano de terpenos.
Los terpenoides, que fueron el segundo grupo de fitoquímicos de mayor abundancia (19 bandas), se sintetizan en el citosol y el retículo endoplásmatico, y su función es originar sustancias como aceites esenciales, fragancias florales que sirven para atraer a polinizadores (García, 2004). En el caso de V. pompona, estos metabolitos pueden estar asociados a la fragancia del labelo de la flor, que actúa como atrayente de las abejas (Euglossine) que polinizan por recompensa (Soto-Arenas, 2009); aunque también diferentes estructuras de terpenos generan algunas toxinas que actúan como defensa ante depredadores (Mazid et al., 2011). En V. planifolia, los terpenos fueron los fitoquímicos que se detectaron en mayor abundancia por CCF (Andrade-Andrade et al., 2018).
Los flavonoides (15 a 17 bandas) generalmente intervienen en las plantas para protección contra hongos, bacterías e insectos, y para proteger a las células de flores y hojas de los rayos UV (Mazid et al., 2011), debido a que ayudan a reducir el estrés oxidativo y actúan además como reguladores del crecimiento (Kumar y Pandey, 2013).
Los ácidos fenólicos (7 a 8 bandas) tienen la función de proveer color y aroma a las plantas y en la vainilla tienen una participación importante en el sabor y aroma de los frutos (Sharma et al., 2007). El metabolismo de estos compuestos se activa ante el estrés biótico y abiótico como defensa para la planta ante herbívoros, insectos, y también tienen actividad antimicrobiana y antifúngica (Mazid et al., 2011).
Los alcaloides (3 a 6 bandas) generalmente se presentan en mayor abundancia en plantas dicotiledóneas que en monocotiledóneas (Mazid et al., 2011), como lo es V. pompona. Recientemente se documentó que en el género Vanilla no hay presencia de alcaloides (Teoh, 2016), lo que explica la baja detección de estos fitoquímicos en V. pompona. Los taninos tuvieron poca presencia (4 bandas); son metabolitos que tienen la capacidad de enlazar proteínas que generan toxinas y actúan de protección ante depredadores de las plantas (Mazid et al., 2011).
La hoja (18-20 bandas) junto con la flor (17-22) fueron los tejidos que presentaron diversidad mayor de metabolitos, debido posiblemente a que la principal función de estos está asociada a la defensa de las plantas contra herbívoros, y al papel que tienen en las interacciones planta-polinizador (Stevenson et al., 2017).
Análisis cuantitativo de fitoquímicos
Los valores promedio obtenidos en la concentración de fitoquímicos por localidad y por tejido (Tabla III) mostraron diferencias altamente significativas (P<0,0001), con excepción de compuestos fenólicos totales que tuvieron solo diferencias significativas (P<0,05). Los grupos de fitoquímicos tuvieron coeficientes de variación entre 11 y 22%; el mayor correspondió a las saponinas, lo cual revela consistencia en la información con el modelo estadístico empleado.
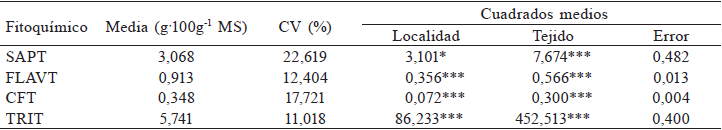
*** P<0,0001; * P<0,05. CFT: compuestos fenólicos totales; FLAVT: flavonoides totales; TRIT: triterpenos totales; SAPT: saponinas totales.
La concentración de los componentes fitoquímicos varió entre las localidades de recolecta y por el tipo de tejido (Tabla IV). Las estructuras de la planta de V. pompona de la localidad de Cazuelas presentaron la concentración mayor de saponinas totales y de triterpenos totales, mientras que las de Morelos tuvieron mayor cantidad de flavonoides totales y compuestos fenólicos totales. Las diferencias entre localidades de recolecta pueden atribuirse a las condiciones ambientales de cada localidad. Cazuelas tiene un clima cálido subhúmedo (Aw1), precipitación media anual de 800-1200mm, altitud de 69msnm, temperatura media anual >22°C, se ubica en la zona ecológica tropical húmeda y tiene un régimen de humedad del suelo ústico (Tabla I). Por su parte, la localidad de Morelos tiene un clima semicálido subhúmedo (A)C (w1), precipitación media anual de 2000-2500mm, temperatura media anual >18°C, altitud de 1277msnm, pertenece a la zona ecológica templada húmeda y presenta un régimen de humedad del suelo xérico (Tabla I). De manera similar a como se documentó en Bacopa monnieri, donde el contenido mayor de saponinas en plantas cultivadas se obtuvo debido a la alta temperatura y humedad en la estación lluviosa (Phrompittayarat et al., 2011), mientras que en V. pompona, la temperatura y el régimen de humedad del suelo en la localidad de Cazuelas propiciaron la acumulación mayor de saponinas.
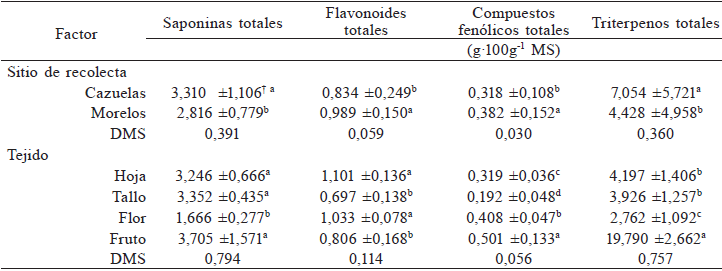
†Media ±desviación estándar. Medias con la misma letra dentro de cada columna por sitio o tejido no difieren estadísticamente (Tukey, P≤0,05).
En este estudio la concentración de metabolitos fue diferente en relación con la estructura de la planta, como lo describen King y Young (1999); los fitoquímicos se acumulan en diferentes partes de las plantas, como en raíces, hojas, tallos, flores, frutos o semillas, y su concentración puede variar en función de la estructura, edad del tejido, especie y condiciones de crecimiento. La hoja mostró concentración alta de SAPT (3,246g·100g-1) y FLAVT (1,101g·100g-1). El tallo tuvo una concentración alta de SAPT (3,352g·100g-1), la flor de FLAVT (1,033g·100g-1) y el fruto acumuló principalmente CFT (0,501g·100g-1) y TRIT (19,79g·100g-1).
En la interacción de localidad por tejido, en Cazuelas la concentración mayor de SAPT se mostró en el fruto (4,924g·100g-1), no así en la localidad de Morelos donde la hoja (2,849g·100g-1) y el tallo (3,515g·100g-1) tuvieron la acumulación mayor de estos metabolitos (Figura 1a). Se sabe que frutos inmaduros tienen mayor contenido de fitoquímicos como las saponinas, que sirven para proteger a los frutos de los depredadores (Kreuger y Potter, 1994). De ahí que, antes de la cosecha, en semillas de soya (Glycine max L.) la concentración de estos metabolitos varió de 4 a 6g·100g-1 (Berhow et al., 2006), y en hojas de Ginkgo biloba L. se obtuvieron concentraciones de saponinas de 5,914 a 11,155g·100g-1 (Qian et al., 2009).
Respecto a la concentración de FLAVT (Figura 1b), en las dos localidades la hoja y la flor tuvieron la acumulación más alta y mostraron concentraciones similares en un rango de 1,031 a 1,131g·100g-1. En la localidad de Cazuelas, los CFT (Figura 1c) mostraron la concentración mayor en el fruto (0,404g·100g-1) y en la flor (0,394g·100g-1), mientras que en Morelos estos compuestos se acumularon principalmente en el fruto (0,645g·100g-1). En frutales, la concentración de compuestos fenólicos, flavonoides y otros fitoquímicos pueden variar debido a cambios en las condiciones climáticas como temperatura, radiación UV, humedad, salinidad y precipitación (Xu et al., 2011; Chandra et al., 2014), y son precisamente las hojas y frutos en V. pompona los órganos más expuestos ante factores externos. Los TRIT (Figura 1d) tuvieron una concentración 6 a 10 veces más alta en los frutos que en las demás estructuras, y en la localidad de Cazuelas tuvieron aún una concentración mayor (22,091g·100g-1) que en Morelos (17,49g·100g-1). Si se parte de que en general los terpenos actúan como agentes de protección de la planta ante depredadores, estrés abiótico como alta temperatura, alta intensidad de luz, contaminación atmosférica entre otros factores (Vickers et al., 2009), es muy probable que la temperatura de la localidad de Cazuelas (>22°C) pudo propiciar una acumulación mayor de triterpenos en comparación con la localidad de Morelos (>18°C).
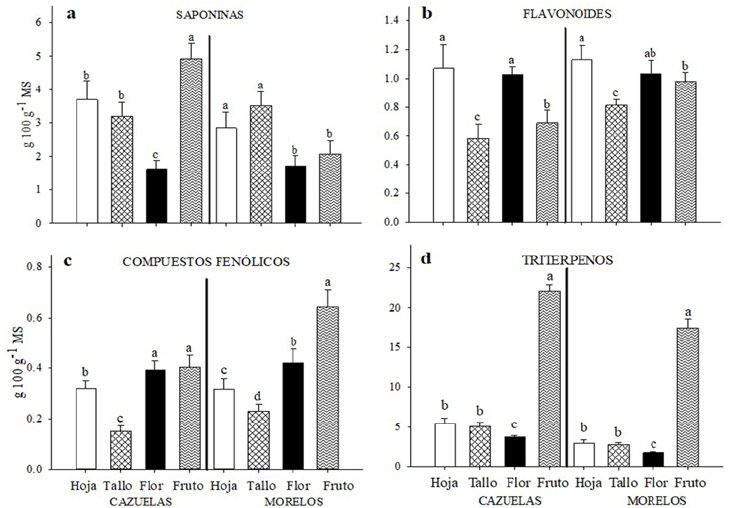
Figura 1
Concentración de a) saponinas, b) flavonoides, c) compuestos fenólicos y d) triterpenos en hoja, tallo, flor y fruto de V. pompona recolectados en la localidad de Cazuelas y Morelos, México. Medias con la misma letra por localidad no difieren estadísticamente (Tukey, P≤0,05).
En general las saponinas tienen propiedades antifúngicas, antiinflamatorias, antibacteriales, antioxidantes y antimicrobianas (Cheok et al., 2014), y como triterpenoides pueden modular la producción de especies reactivas de oxígeno para acelerar el proceso de reparación de tejidos, a través de inducir la migración celular, la proliferación celular y la deposición de colágeno, entre otras propiedades (Agra et al., 2015). Por ello, la presencia de concentraciones altas de estos metabolitos en V. pompona refieren a esta especie como una fuente promisoria para realizar estudios más detallados, a fin de conocer la naturaleza química de las saponinas (triterpenicas o esteroidales) y el tipo de triterpenos. Algunos estudios han mencionado que dentro de los compuestos volátiles detectados en frutos beneficiados de V. pompona se han encontrado terpenos, principalmente limoneno que pertenece al grupo de los limonoides y monoterpenos (α-terpineno, p-cimeno), compuestos que son utilizados en la industria como saborizantes y como aromatizantes (Galeas et al., 2016).
Correlación canónica de las variables del ambiente con la concentración de fitoquímicos de V. pompona
Los dos primeros factores del análisis de correlaciones canónicas explicaron 99,72% de la varianza total (Figura 2). La correlación estructural de las variables ambientales y los fitoquímicos estudiados muestra que a mayor temperatura y humedad del suelo aumenta el contenido de TRIT y SAPT. En el caso de altitud y precipitación, se observó una correlación baja no significativa con FLAVT y CFT (Tabla V), lo que sugiere que es poco probable que la altitud y la precipitación afecten el contenido de estos fitoquímicos en V. pompona.
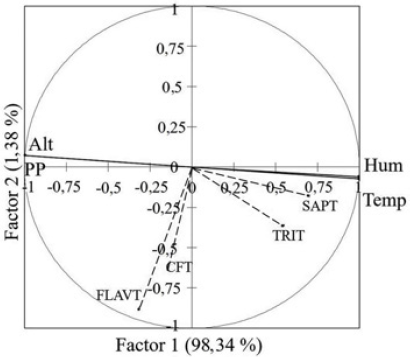
Figura 2
Representación gráfica de los coeficientes de correlación estructural de los dos primeros factores en la interacción de variables ambientales (—) y fitoquímicos (---) de los tejidos de V. pompona. Temp: Temperatura media anual >18 y >22ºC; Hum: Régimen de humedad del suelo (Ústico: 180 a 270 días de humedad, Xérico: 90 a 180 días de humedad); PP: precipitación media anual 800-1200 y 2000-2500mm; Alt: 69 y 1277msnm; CFT: compuestos fenólicos totales; SAPT: saponinas totales; FLAVT: flavonoides; TRIT: triterpenos totales.
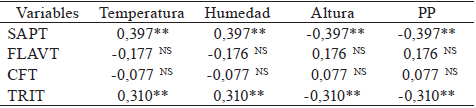
**: P<0,01, NS: estadísticamente no significativo. Temp: Temperatura media anual >18 y >22 oC; Hum: Régimen de humedad del suelo; Ústico: 180 a 270 días de humedad; Xérico 90 a 180 días de humedad; PP: precipitación media anual (800-1200 y 2000-2500mm). Altitud: 69 y 1277msnm; SAPT: saponinas totales; FLAVT: flavonoides totales; CFT: compuestos fenólicos totales; TRIT: triterpenos totales.
Para los parámetros de humedad del suelo y temperatura media anual (Tabla V), ambas mostraron correlaciones positivas significativas con la concentración de TRIT (0,310**) y SAPT (0,397**), lo cual coincide con las condiciones ambientales de las localidades de estudio. En Cazuelas, Veracruz la humedad del suelo y la temperatura media anual fueron mayores en relación a Morelos, Oaxaca (Tabla I), de ahí que por sitio de colecta se cuantificaron los valores más altos de estos metabolitos (Tabla IV), y en particular para triterpenos totales en todos los tejidos de la planta (Figura 1d), mientras que no fue así para saponinas totales, donde solo fue en hoja y fruto (Figura 1a).
Conclusiones
El perfil de fitoquímicos que mostraron las estructuras de la planta de V. pompona fue primordialmente de saponinas, terpenos, flavonoides y ácidos fenólicos, observados bajo el análisis cualitativo por cromatografía en capa fina. La concentración de los fitoquímicos en V. pompona varió en función del ambiente y el tipo de tejido. Por localidad, Morelos tuvo la concentración mayor de compuestos fenólicos totales y flavonoides totales, y Cazuelas tuvo un contenido mayor de saponinas totales y triterpenos totales principalmente en frutos. En Cazuelas, la temperatura media anual y el régimen de humedad del suelo tuvieron efecto directo en la acumulación de triterpenos totales y saponinas totales.
REFERENCIAS
Agra LC, Ferro JNS, Barbosa FT, Barreto E (2015) Triterpenes with healing activity: A systematic review. J. Dermatol. Treat. 26: 465-470.
Ahmed HOA, Wang C (2015) Determination of tea saponin in Camellia seed oil with UV and HPLC analysis. WJET 3: 30-37.
Akula R, Ravishankar GA (2011) Influence of abiotic stress signals on secondary metabolites in plants. Plant Signal Behav. 6: 1720-1731.
Andrade-Andrade G, Delgado-Alvarado A, Herrera-Cabrera BE, Arévalo-Galarza L, Caso-Barrera L (2018) Variación de compuestos fenólicos totales, flavonoides y taninos en Vanilla planifolia jacks. ex andrews de la Huasteca Hidalguense, México. Agrociencia 52: 55-66.
Berhow MA, Kong SB, Vermillion KE, Duval SM. (2006). Complete quantification of group A and group B soyasaponins in soybeans. J. Agric. Food Chem. 54: 2035-2044.
Chandra S, Khan S, Avula B, Lata H, Yang MH, ElSohly MA, Khan IA (2014) Assessment of total phenolic and flavonoid content, antioxidant properties, and yield of aeroponically and conventionally grown leafy vegetables and fruit crops: A comparative study. Evid. Bas. Complem. Altern. Med. 2014: 1-9.
Chang CL, Lin CS (2012) Phytochemical composition, antioxidant activity, and neuroprotective effect of Terminalia chebula Retzius extracts. Evid. Bas. Complem. Altern. Med. 2012: 1-7.
Cheok CY, Salman HAK, Sulaiman R (2014) Extraction and quantification of saponins: A review. Food Res. Int. 59: 16-40.
CONABIO (1998a) Climas (clasificación de Koppen, modificado por García). Escala 1:1000000. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. México. http://www.conabio.gob.mx/informacion/gis/ (Cons. 20/11/2017).
CONABIO (1998b) Precipitación total anual. Escala 1: 1000000. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. México. http://www.conabio.gob.mx/informacion/gis/
CONABIO (1998c) Isotermas Medias Anuales. Escala 1:1000000. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. México. http://www.conabio.gob.mx/informacion/gis/ (Cons. 20/11/2017).
Ehlers D, Pfister M (1997) Compounds of vanillons (Vanilla pompona Schiede). J. Essent. Oil Res. 9: 427-431.
Galeas M, Lin J, Hartman T (2015) Chemical Characterization of Vanilla pompona Schiede, Part I. Perfum. Flavor. 40: 16-28.
Galeas M, Lin J, Hartman T (2016) Chemical Characterization of Vanilla pompona Schiede, Part II. Perfum. Flavor. 41: 26-34.
García DE (2004) Los metabolitos secundarios de las especies vegetales. Pastos Forrajes 27: 1-13.
Herald JT, Gadgil P, Tilley M (2012) High-throughput micro plate assays for screening flavonoid content and DPPH-scavenging activity in sorghum bran and flour. J. Sci. Food Agric. 92: 2326-2331.
Hernández-Hernández J, Lubinsky P (2011) Vanilla Diseases. En Havkin-Frenkel D, Belanger FC (Eds.) Handbook of Vanilla Science and Technology. Wiley-Blackwell. pp 26-38.
Herrera-Cabrera BE, Hernández M, Vega M, Wegier A (2017) Vanilla pompona. The IUCN Red List of Threatened Species 2017. http://dx.doi.org/10.2305/IUCN.UK.2017-3.RLTS.T105878897A105878899 (Cons. 27/02/2018).
Ibarra-Cantún D, Delgado-Alvarado A, Herrera-Cabrera BE, Soto-Hernández RM, Salazar-Rojas VM, Aguilar MI (2018) Effect of the environmental condition of Vanilla planifolia Jacks. ex Andrews cultivation on phytochemical concentration. Rev. Chapingo Ser. Hort. 24: 152-165.
King A, Young G (1999) Characteristics and occurrence of phenolic phytochemicals. J. Am. Diet. Assoc. 24: 213-218.
Kreuger B, Potter DA (1994) Changes in saponins and tannins in ripening holly fruits and effects of fruit consumption on non-adapted insect herbivores. Am. Midl. Nat. 132: 183-191.
Kumar S, Pandey AK (2013) Chemistry and biological activities of flavonoids: An overview. Scient. World J. 2013: 1-16.
Maples-Vermeersch M (1992) Regímenes de humedad del suelo en Hidrogeografía IV.6.2 Atlas Nacional de México. Vol. II. Escala 1:4000000. Instituto de Geografía, UNAM. México. http://www.conabio.gob.mx/informacion/metadata/gis/rehsu4mgw.xml?_httpcache=yes& _xsl=m/db/metadata/xsl/fgdc_html.xsl&_indent=no (Cons. 20/02/2018).
Maruenda H, Del Lujan Vico M, Householder JE, Janovec JP, Cañari C, Naka A, González AE (2013) Exploration of Vanilla pompona from the Peruvian Amazon as a potential source of vanilla essence: Quantification of phenolics by HPLC-DAD. Food Chem. 138:161-167.
Mazid M, Khan TA, Mohammad F (2011) Role of secondary metabolites in defense mechanisms of plants. Biol. Med. 3: 232-249.
Pérez-Silva A, Odoux E, Brat P, Ribeyre F, Rodriguez-Jimenez G, Robles-Olvera V, García-Alvarado MA, Günata Z (2006) GC-MS and GC olfactometry analysis of aroma compounds in a representative aroma extract from cured vanilla (Vanilla planifolia G. Jackson) beans. Food Chem. 99: 728-735.
Phrompittayarat W, Jetiyanon K, Wittaya-areekul S, Putalun W, Tanaka H, Khan I, Ingkaninan K (2011) Influence of seasons, different plant parts, and plant growth stages on saponin quantity and distribution in Bacopa monnieri. Songklanakarin J. Sci. Technol. 33: 193-199.
Qian ZM, Lu J, Gao QP, Li SP (2009) Rapid method for simultaneous determination of flavonoid, saponins and polyacetylenes in Folium Ginseng and Radix Ginseng by pressurized liquid extraction and high-performance liquid chromatography coupled with diode array detection and mass spectrometry. J. Chromatogr. A. 1216(18): 3825-3830.
Ramachandra RS, Ravishankar GA (2000) Vanilla flavour: Production by conventional and biotechnological routes. J. Sci. Food Agric. 80: 289-304.
Ranadive AS (1992) Vanillin and related flavor compounds in vanilla extracts made from beans of various global origins. J. Agric. Food Chem. 40: 1922-1924.
Salazar-Rojas VM, Herrera-Cabrera BE, Delgado-Alvarado A, Soto-Hernández M, Castillo-González F, Cobos-Peralta M (2012) Chemotypical variation in Vanilla planifolia Jack. (Orchidaceae) from the Puebla-Veracruz Totonacapan region. Genet. Resour. Crop Evol. 59: 875-887.
SAS (2002) SAS/STAT 9.0. User’s guide. SAS Institute Inc. Cary, NC, EEUU. 421 pp.
Sharma UK, Sharma N, Gupta AP, Kumar V, Sinha AK (2007) RP-HPTLC densitometric determination and validation of vanillin and related phenolic compounds in accelerated solvent extract of Vanilla planifolia. J. Sep. Sci. 30: 3174-3180.
Silva-Beltrán NP, Ruiz-Cruz S, Cira-Chávez LA, Estrada-Alvarado MI, Ornelas-Paz JDJ, López-Mata MA, Márquez-Ríos E (2015) Total phenolic, flavonoid, tomatine, and tomatidine contents and antioxidant and antimicrobial activities of extracts of tomato plant. Int. J. Anal. Chem. 2015: 1-10.
Soto-Arenas M (1999) Filogeografía y Recursos Genéticos de las Vainillas de México. Informe Final SNIB-CONABIO Proyecto No. J101. Instituto Chinoín, A.C. - Herbario de la Asocia-ción Mexicana de Orquideo-logía, A.C. México.
Soto-Arenas MA (2009) Recopilación y Análisis de la Información Existente sobre las Especies Mexicanas del Género Vanilla. Reporte Intermedio. CONACYT. México. 76 pp.
Soto-Arenas M, Dressler R (2010) A revision of the Mexican and Central American species of Vanilla plumier ex Miller with a characterization of their its region of the nuclear ribosomal DNA. Lankesteriana 9: 285-354.
SPSS (2010) Statistical Package for Social Sciences. User’s Manual (Versión 19).
Stevenson PC, Nicolson SW, Wright GA (2017) Plant secondary metabolites in nectar: impacts on pollinators and ecological functions. Funct. Ecol. 31: 65-75.
Szakiel A, Paczkowski C, Henry M (2011) Influence of environmental abiotic factors on the content of saponins in plants. Phytochem. Rev. 10: 471-491.
Teoh ES (2016) Medicinal Orchids of Asia. Springer. Basel, Switzerland. 752 pp.
Toledo VM, Ordóñez MJ (2009) Zonas Ecológicas de México. Extraído de los proyectos A006 y E021: ‘Diagnostico de los escenarios de la biodiversidad en México’ fases 1 y 2. Escala 1:1 000 000. Centro de Ecología, UNAM. Proyecto financiado por la Comisión Nacional para el Conocimiento y Uso de la Biodiversidad (CONABIO), México.
Vickers CE, Gershenzon J, Lerdau MT, Loreto F (2009) A unified mechanism of action for volatile isoprenoids in plant abiotic stress. Nature Chem. Biol. 5: 283-291.
Wagner H, Bladt S (1996) Plant Drug Analysis: A Thin Layer Chromatography Atlas. 2a ed. Springer. Nueva York, EEUU. 384 pp.
Xu C, Zhang Y, Zhu L, Huang Y, Lu J (2011) Influence of growing season on phenolic compounds and antioxidant properties of grape berries from vines grown in subtropical climate. J. Agric. Food Chem. 59: 1078-1086.
Zhong-Cheng K, Zhi-Ping Z, Zhi-Yuan X, Fang C, Shang-Qing H (2014) Response surface optimized extraction of total triterpene acids from Eriobotrya japonica (Thunb) Lindl (Loquat) leaf and evaluation of their in vitro antioxidant activities. Trop. J. Pharm. Res. 13: 787-792.
Notas de autor
adah@colpos.com