COMUNICACIONES
Recepção: 22 Agosto 2017
Corrected: 08 Abril 2019
Aprovação: 15 Abril 2019
Financiamento
Fonte: Os autores agradecem ao apoio financeiro da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES); à CODEVASF e o Centro Integrado de Recursos Pesqueiros e Aquicultura do Betume, 4ª/CIB, 4ªSR, Neópolis-SE, pelo auxílio no desenvolvimento deste trabalho.
Beneficiário: DESENVOLVIMENTO EMBRIONÁRIO E O EFEITO DE DIFERENTES DIETAS NO DESEMPENHO DE PÓS-LARVAS DE TAMBAQUI
Resumo: Objetivou-se acompanhar o desenvolvimento embrionário do tambaqui (Colossoma macropomum) e o desempenho pós-larval alimentadas com diferentes dietas. As espécies foram submetidas à reprodução induzida para posterior observação e descrição dos estágios de desenvolvimento embrionário. Após a fertilização, na primeira hora os ovos foram observados a cada 10min, e subsequente a cada 30min, até a eclosão. As observações e capturas das imagens foram em microscopia trinocular, com câmera digital. No experimento de desempenho, 6000 larvas, comprimento total de 5,70 ±0,2894mm e peso médio inicial de 0,0012 ±0,0010mg foram mantidos em 12 incubadoras de 25L e quatro de 75L, estocando 10 larvas/L distribuídas ao acaso em quatro tratamentos e quatro repetições, avaliando pasta de branchoneta, leite em pó, albumina e cistos de Artêmia salina descapsulados. No desenvolvimento embrionário as características observadas foram: aumento do espaço perivitelínico, clivagens, mórula, blástula, gástrula, desenvolvimento da região cefálica, caudal, vesícula óptica, aparecimento dos somitos, e eclosão aos 774min após fertilização. As larvas alimentadas com cisto de Artêmia salina descapsulados apresentaram peso e comprimento superiores aos observados nos demais tratamentos. Não houve diferença significativa na taxa de sobrevivência nos diferentes tratamentos. O desenvolvimento embrionário do tambaqui foi de 12h e 54min ou 360h/grau, na temperatura de incubação de 28,7 ±0,5°C. O cisto de Artêmia salina descapsulado foi mais eficiente nas variáveis peso, comprimento e taxa sobrevivência. Desta forma, essa dieta pode ser utilizada na alimentação de pós-larva de tambaqui.
Palavras-chave: Fertilização, Larva, Nutrição, Peixe, Vitelo.
Abstract: The objective of this work was to monitor the embryonic development of ‘tambaqui’ (Colossoma macropomum) and the post-larval performance, fed with different diets. The species were submitted to induced spawning for further observation and description of embryonic development stages. After fertilization, in the first hour the eggs were observed every 10min and, subsequently, every 30min until hatching. The observations and captured images were made by tri-ocular microscope with digital camera. In the performance trial, 6000 larvae, with total length of 5.70 ±0.2894mm and average weight of 0.0012 ±0.0010mg were kept in 12 incubators of 25L and four of 75L, stocking 10 larvae/L randomly allocated to four treatments and four repetitions. Branchoneta folder, powdered milk, albumin and decapsulated Artemia salina cysts were evaluated. The following characteristics were observed during embryo development: increased perivitelline space, rifts, morula, blastula, gastrula, development of the cephalic and caudal regions, optic vesicle, appearance of somites, and hatching at 774min after fertilization. The larvae fed with decapsulated cysts of A. salina, presented higher weight and length than those in the other treatments. There was no significant difference in survival rate between different treatments. The embryonic development of the tambaqui took 12h 54min or 360 h/degree in the incubation temperature of 28.7 ±0.5°C. The decapsulated cysts of A. salina were more efficient in the weight, length and survival rate variables; thus, such a diet can be utilized in post-larval tambaqui feeding.
Resumen: Se estudió el efecto de diferentes dietas sobre el desarrollo embrionario del ‘tambaqui’ (Colosoma macropomum) y el desempeño post-larval. Las especies fueron sometidas a la reproducción inducida para la posterior observación y descripción de las etapas de desarrollo embrionario. Durante la primera hora después de la fertilización los huevos fueron observados cada 10min y posteriormente cada 30min, hasta eclosión. Las observaciones y capturas de imágenes se realizaron con microscopia triocular y cámara digital. En el experimento de rendimiento, 6000 larvas con longitud total de 5,70 ±0,2894mm y peso medio inicial de 0,0012 ±0,0010mg se mantuvieron en 12 incubadoras de 25L y cuatro de 75L, distribuyendo al azar 10 larvas/L en cuatro tratamientos: pasta de branchoneta, leche en polvo, albumina y quistes descapsulados de Artemia salina, con cuatro repeticiones. Las características observadas durante el desarrollo embrionario fueron: aumento del espacio perivitelínico, clivajes, mórula, blástula, gástrula, desarrollo de la región cefálica y caudal, vesícula óptica, aparición de somitas, y eclosión a los 774min después de la fertilización. Las larvas alimentadas con quiste de A. salina descapsulados presentaron peso y longitud superiores a los observados en los demás tratamientos. No hubo diferencia significativa en la tasa de supervivencia en los diferentes tratamientos. El desarrollo embrionario del tambaqui fue de 12h 54min o 360 h/grado, a temperatura de incubación de 28,7 ±0,50C. El quiste de A. salina descapsulado fue más eficiente en las variables peso, longitud y tasa de supervivencia; de esta forma, esta dieta puede ser utilizada en la alimentación postlarval de tambaqui.
Introdução
O Brasil possui grande potencial hídrico e climático para aquicultura (Rocha et al. 2013), bem como a fauna mais rica em peixes do globo terrestre, sendo enquadrado como um dos países mais promissores para a expansão desta atividade (Buzollo et al., 2011). Apesar dos avanços, a piscicultura tem seu potencial de crescimento reduzido, sendo um dos entraves para este crescimento o pouco conhecimento biológico das espécies nativas de valor comercial (Godinho, 2007).
O tambaqui (Colossoma macropomum) é uma espécie onívora (Souza et al., 2014) de alto potencial produtivo pelo fato de apresentar boa aceitação de ração artificial (Santos et al., 2010), crescimento rápido e resistência ao manuseio. Além disso, o tambaqui é uma espécie de peixe que possui alto valor comercial e grande importância econômica e social na América Latina (Silva et al., 2007). A produção comercial do tambaqui vem crescendo cada vez mais no Brasil e vários são os cuidados relacionados ao cultivo dessa espécie, principalmente nos estágios iniciais de seu desenvolvimento, larvicultura e alevinagem (Affonso et al., 2009).
Segundo Maciel (2006), pesquisas sobre o estudo do desenvolvimento embrionário de peixes têm fornecido dados às pesquisas de grande repercussão e inovação no meio científico, pois gera informações básicas necessárias para a identificação de possíveis alterações do padrão do desenvolvimento, qualidade e viabilidade dos embriões causados pela aplicação de novas tecnologias, como a utilização de sêmen criopreservado. Reynalte-Tataje et al. (2004) e Ninhaus-Silveira et al. (2006) relataram que a descrição dos estágios embrionários em teleósteos traz informações importantes para a produção em grande escala de peixes em laboratório, além de contribuir com a sistemática e inventário ambiental.
A nutrição ainda é considerada um dos principais entraves encontrados na piscicultura, pois os gastos com o arraçoamento podem representar até 60% dos custos de produção (Boscolo et al., 2001). A alimentação reflete diretamente no desempenho, sobrevivência e crescimento dos peixes. Uma alimentação deficiente pode resultar em uma das principais causas de mortalidade nas fases iniciais de vida; contudo, esse problema pode ser minimizado, quando alimento apropriado são fornecidos para cada espécie (Diemer et al., 2012). Embora tenham ocorrido avanços no desenvolvimento de dietas inertes para larvicultura, a maior parte delas ainda estão baseadas na utilização de alimentos vivos como estratégia de alimentação (Conceição et al., 2010). Baseado nisso, é importante o estudo de fontes alternativas de alimentação com o intuito de tornar a atividade mais atrativa e rentável, sem prejuízo ao crescimento e a saúde dos animais (Palma et al., 2010; Lemos et al., 2011).
Este estudo teve como objetivo acompanhar o desenvolvimento embrionário de pós-larvas do tambaqui (Colossoma macropomum) e a utilização de diferentes dietas sobre o desenvolvimento na fase inicial.
Material e Métodos
Desenvolvimento embrionário
O experimento foi realizado no Centro Integrado de Recursos Pesqueiros do Betume da (CODEVASF 4ª/CIB), localizada no perímetro irrigado de Betume, no município de Neópolis-SE, Brasil, e teve duração de três dias. Os animais utilizados no experimento foram obtidos no plantel do próprio centro. Para minimizar o estresse da manipulação, os animais foram sedados mediante imersão em tanque contendo óleo de cravo (eugenol) diluído em álcool absoluto 1:10:1000 (eugenol:álcool:água).
Para a reprodução induzida, a fêmea recebeu tratamento hormonal com duas doses de acetato de buserelina, sendo a primeira de 0,20µl·kg-1 de peso vivo, e a segunda de 0,50µl·kg-1 de peso vivo, com intervalo de 7h 30min entre as aplicações. No macho foi administrada dose única de 0,08µl·kg-1 de peso vivo simultaneamente à segunda aplicação da fêmea. Para evitar a liberação dos ovócitos de forma espontânea no tanque realizou-se uma sutura sobre abertura urogenital da fêmea e 9h 20min após a segunda dose hormonal foi realizada a coleta dos gametas.
Após a extrusão, os ovócitos foram acondicionados em bacias plásticas e, em seguida, foram misturados com sêmen. Posteriormente, foram acrescentados 1000ml de água do tanque (28,4°C), que foi homogeneizado suavemente permanecendo por 5min para a ativação dos espermatozoides e hidratação dos ovos. O momento de adição da água foi anotado e considerado como início da fertilização (tempo zero). Após a hidratação, os ovos foram transferidos para incubadoras cônicas de fibra de vidro, com capacidade de 250 litros.
Para o acompanhamento do desenvolvimento embrionário, amostras de ovos foram periodicamente removidos das incubadoras com auxílio de uma pipeta graduada e foram depositados em lâmina milimetrada. Na primeira hora após a fertilização, as observações foram feitas a cada 10min, e posteriormente a cada 30min, até a eclosão dos ovos. As observações e as capturas das imagens foram realizadas em estereomicroscópio trinocular acoplado à câmera digital. A câmera digital foi programada para capturar as imagens de 30 em 30s até o momento de eclosão das larvas que ocorreu com 12h 54min após a fertilização.
Para este estudo foi utilizada a classificação de Faustino et al. (2011), ou seja, a expressão ‘ovócito’ refere-se ao gameta feminino, antes da fertilização. O termo ‘ovo’ referiu se aos estágios compreendidos entre a fertilização e o final da gastrulação, quando então ocorre a formação do eixo embrionário passando a ser denominado ‘embrião’. A denominação ‘larva’ foi utilizada desde o momento da eclosão até a absorção total do vitelo.
Experimento de desempenho
Foram utilizadas 6000 larvas de tambaqui, obtidas por indução hormonal, e transferidas para as unidades experimentais com idade de 4 dias com comprimento total de 5,70 ±0,3mm e peso médio inicial de 0,0012 ±0,0010mg. Os animais foram transferidos aleatoriamente para as unidades experimentais durante um período de 8 dias. Foram utilizadas 12 incubadoras modelo cilindro cônico de 25 litros e quatro de 75 litros com fluxo aberto (3,0 L/min), na densidade de estocagem de 10 larvas/L, sem aeração constante e com fotoperíodo natural.
Os alimentos avaliados foram: pasta de branchoneta, leite em pó, albumina e cisto de Artêmia salina descapsulados. Para o processo de descapsulação dos cistos de Artêmia salina seguimos a metodologia proposta por Takata (2007).
Para produção da pasta de branchoneta, as mesma foram capturadas nos viveiros da própria estação de piscicultura com rede de plâncton de malha de 25mm. Posteriormente as branchonetas foram lavadas em água corrente para retirada das impurezas e trituradas em liquidificador até a formação de uma pasta homogênea que foi acondicionada na geladeira e retirada somente na hora da alimentação.
A quantidade de cada alimento fornecido nos trata- mentos foram 24g/dia por incubadoras de 25 litros e 72g/dia por incubadoras de 75 litros, distribuídos em oito refeições diárias, cada 3h durante as 24h. A exigência nutricional de proteína das pós-larvas de tambaqui é em torno de 42%. A composição química das dietas utilizadas estão expressas na Tabela I. Antes do fornecimento da alimentação o fluxo de água das incubadoras era cessado para evitar a perda de alimento. Uma vez por dia, uma hora após a alimentação, era feito a sifonagem das incubadoras para retirada de excretas e sobras de alimento. Em cada sifonagem retirava-se 50% do volume total da incubadora, e posteriormente, o fluxo de água era aberto.
COMPOSIÇÃO QUÍMICA DAS DIFERENTES DIETAS UTILIZADAS NA ALIMENTAÇÃO DE LARVAS DE TAMBAQUI (Colossoma macropomum)
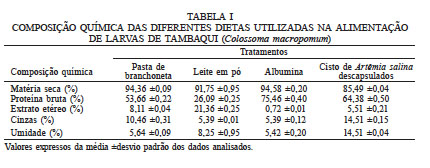
V Valores expressos da média ±desvio padrão dos dados analisados.
A cada dois dias e ao final do experimento foram coletados aleatoriamente de cada incubadora 10% do total de indivíduos os quais foram fixados em formol 4% tamponado para a determinação do peso e comprimento. Para determinação do peso e do comprimento as larvas foram retiradas do formol e colocadas sobre papel absorvente para a retirada do excesso de líquidos, medindo-se seu comprimento padrão, da ponta do focinho até o início da inserção da nadadeira caudal. Decorridos oito dias, as larvas restantes foram contadas para a determinação da taxa de sobrevivência.
As medições das larvas foram realizadas sob estereomicroscópio trinocular, equipado com uma câmera digital com aumento 1,5x. Posteriormente, foram pesadas em uma balança analítica de precisão de 0,0001g.
Os parâmetros temperatura (ºC) e o oxigênio dissolvido (mg·L-1), foram monitorados diariamente às 6:00 e 18:00, por meio de aparelho eletrônico portátil (YSI 550A), assim como o pH (pHmetro HANNA HELP 5).
Os animais foram distribuídos em um delineamento inteiramente casualizado com quatro tratamentos e quatro repetições. Os dados foram submetidos à análise de variância e, no caso de diferenças estatísticas, aplicou-se o teste Tukey a 5% de probabilidade, por meio do programa computacional estatístico Sisvar (versão 5.3).
Resultados e Discussão
O desenvolvimento embrionário de tambaqui apresentou as sequências de eventos, expressos em minutos após a fertilização (MAF). Quando incubados a temperatura média de 28,7 ±0,5ºC foi observado que aos cinco MAF, o citoplasma tornou-se mais evidente no polo animal, formando um disco de citoplasma conhecido como blastodisco, disposto sob uma porção rica em vitelo no polo vegetal, destacando um aumento do espaço perivitelínico (Figura 1A). Estes eventos também foram observados em ovos de tambaqui (Colossoma macropomum), por Leite et al. (2013) após 10min de fertilização com a temperatura de 25,0ºC e 27,5ºC respectivamente, e por Valbuena-Villarreal et al. (2012) em ovos de capaz (Pimelodus Grosskopffi) após 15min de fertilização com temperatura de 27 ±1,0ºC.
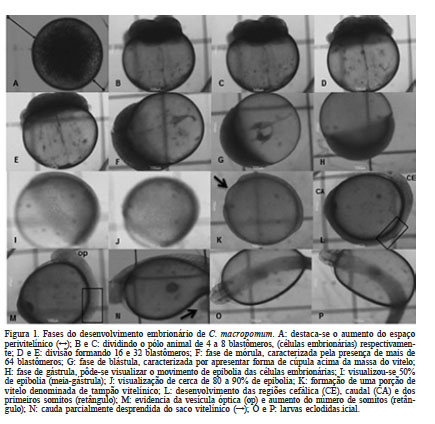
Figura 1
Fases do desenvolvimento embrionário de C. macropomum. A: destaca-se o aumento do espaço perivitelínico (↔); B e C: dividindo o pólo animal de 4 a 8 blastômeros, (células embrionárias) respectivamente; D e E: divisão formando 16 e 32 blastômeros; F: fase de mórula, caracterizada pela presença de mais de 64 blastômeros; G: fase de blástula, caracterizada por apresentar forma de cúpula acima da massa do vitelo; H: fase de gástrula, pôde-se visualizar o movimento de epibolia das células embrionárias; I: visualizou-se 50% de epibolia (meia-gástrula); J: visualização de cerca de 80 a 90% de epibolia; K: formação de uma porção de vitelo denominada de tampão vitelínico; L: desenvolvimento das regiões cefálica (CE), caudal (CA) e dos primeiros somitos (retângulo); M: evidencia da vesícula óptica (op) e aumento do número de somitos (retângulo); N: cauda parcialmente desprendida do saco vitelínico (→); O e P: larvas eclodidas.icial.
As clivagens ocorreram entre 25 e 60 MAF, dividindo o polo animal de 4 a 8 blastômeros de igual tamanho (Figuras 1B e 1C) que, em seguida, sofreram divisão formando 16 blastômeros, e assim sucessivamente até a formação de 32 células (Figuras 1D e 1E). Os eventos iniciais das clivagens corroboram com os resultados observados por Sividanes et al. (2012), que trabalharam com ovos de jundiá (Rhamdia voulezi) com temperatura de 27,0 ±0,5ºC e Sividanes et al. (2013), que incubaram ovos de piau vermelho Leporinus copelandii com temperatura da água de 27,7 ±0,8ºC.
Devido ao aumento da segmentação celular, foi observado uma diminuição gradativa no tamanho dos blastômeros, o que foi observado em outros experimentos, corroborando os relatos de Marques et al. (2008) e Leite et al. (2013). Por isso, a partir dessa fase, não foi possível quantificar o número de blastômeros.
Posteriormente, com 87 MAF, foi observado o estágio de mórula, caracterizada pela presença de mais de 64 blastômeros. A Figura 1F mostra a mórula em seu estágio final, em que os blastômeros formaram um maciço celular semelhante a uma ‘meia amora’. Resultados semelhantes foram encontrados por Faustino et al. (2010), onde observaram os estágios de mórula em híbridos de surubim (Pseudoplatystoma spp.) com 90 MAF e temperatura entre 27 e 29ºC; Sividanes et al. (2013) relataram que o estágio de mórula para L. copellandii foi observado aos 92 MAF e 27,7 ±0,8ºC.
Foi observado com 140 MAF o estágio de blástula, que se caracteriza por apresentar forma de cúpula acima da massa do vitelo (Figura 1G). Esse formato é resultante da primeira clivagem no sentido horizontal, dividindo o embrião em duas camadas de células com uma cavidade entre elas chamada de blastocele (Salmito-Vanderley e Santana, 2010). Resultados semelhantes foram encontrados por Sividanes et al. (2012), que verificaram a fase de blástula em R. voulezi, aos 128 MAF com 27,0 ±0,5ºC. Buzollo et al. (2011) observaram a formação da blástula em mandi amarelo (Pimelodus maculatus) aos 120min em de 29ºC.
Na fase de gástrula, pode ser visualizado o movimento de epibolia das células embrionárias, as quais realizaram um movimento de divergência (epibolia) do pólo animal em direção ao pólo vegetativo. O início desta fase foi observado com 167 MAF, quando ~30% do vitelo foi recoberto (Figura 1H). Com 206 MAF visualizou-se 50% de epibolia (meia-gástrula, Figura 1I), aos 292 MAF cerca de 80 a 90% de epibolia (Figura 1J) e, com 325 MAF, o final do movimento, que se completou com a formação de uma porção de vitelo não recoberta pelo blastoderme após os movimentos celulares, denominada de tampão vitelínico (Figura 1K). Resultados semelhantes com R. voulezi foram verificados por Sividanes et al. (2012), que verificaram o processo de gastrulação com 172 MAF e temperatura de 27,0 ±0,5ºC. Também foi relatado por De Alexandre et al. (2010), com matrinxã (Brycon cephalus), onde observou-se 90% da epibolia com 360 MAF com 26,8oC. A sequência de eventos também foi relatado por Leite et al. (2013) com C. macropomum, onde a epibolia alcançou 50% da região vitelínica com 180 MAF e a gástrula final ou fechamento do blastóporo com 240 MAF e 27,5ºC.
No início da fase de histogênese e organogênese, com 370 MAF, notou-se o desenvolvimento das regiões cefálicas, caudal e desenvolvimento dos primeiros somitos (Figura 1L). Resultados semelhantes foram encontrados por Buzollo et al. (2011), onde notou esses desenvolvimentos em P. maculatus aos 360 MAF e temperatura de 29ºC. Leite et al. (2013) relataram esses desenvolvimentos com 420 MAF trabalhando com C. macropomum) na temperatura de 27,5oC.
A vesícula óptica tornou se mais evidente 440 MAF, ocorrendo simultaneamente ao aumento no número de somitos (Figura 1M). Nessa fase, a cauda do embrião apresentou-se completamente aderida ao saco vitelínico. Resultados também foram observados por De Alexandre et al. (2010) e Leite et al. (2013), onde observaram esses desenvolvimentos em B. cephalus com 420 MAF e 26,8ºC e com C. macropomum, onde a vesícula óptica evidenciou-se com 480 MAF e 27,5ºC.
Quando a cauda demonstrou-se parcialmente desprendida do saco vitelínico, em 550 MAF, foi observada a expansão do saco de vitelo na zona caudal, acompanhando o formato larval (Figura 1N). Resultados semelhantes foram observados por Leite et al. (2013) quem relataram esses eventos com 570 MAF e 27,5ºC com C. macropomum e Faustino et al. (2010) em híbridos de Pseudoplatystoma spp., após 540min e temperatura entre 27 e 29ºC.
O tempo decorrente do desenvolvimento embrionário varia de acordo com a espécie, tamanho do ovo e com a temperatura da água. Espécies que realizam migração, com desova total, com fecundação externa e que não realizam cuidado parental possuem ovos menores, fecundação maior e embriogênese mais rápida (Godinho, 2007).
Os movimentos se tornaram mais intensos à medida que a cauda soltava-se do saco vitelínico (Figura 1O). O embrião apresentou movimento de natação dentro da membrana coriônica, até o momento em que a larva eclodiu e tornou-se livre (Figura 1P). A eclosão das larvas ocorreu na temperatura de incubação de 28,7 ±0,5ºC, a 774 MAF (12h 54min), o equivalente a 360 horas-grau.
Leite et al. (2013) observaram com C. macropomum resultados semelhantes onde essas movimentações ocorreram e 780 MAF ocorreu sua eclosão com temperatura de 27,5oC. Buzollo et al. (2011) relatam em P. maculatus movimentação constante para ruptura da membrana coriônica aos 780 MAF e 29ºC.
Os valores médios para as variáveis físico-químicas da água obtidos no período experimental (Tabela II) estiveram dentro dos limites considerados satisfatórios para a criação da espécie.
PARÂMETROS FÍSICO-QUÍMICOS DA ÁGUA OBTIDOS DURANTE O EXPERIMENTO COM LARVAS DE TAMBAQUI (Colossoma macropomum) SUBMETIDAS A DIFERENTES DIETA
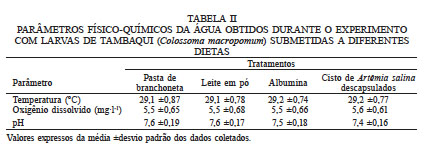
Valores expressos da média ±desvio padrão dos dados coletados. Valores expressos da média ±desvio padrão dos dados coletados.
Foram observadas diferenças significativas (P<0,05) entre os diferentes tratamentos para o peso e comprimento das larvas de tambaqui. Os valores médios de peso (g), comprimento (mm) e sobrevivência (%) das larvas de tambaqui submetidas a diferentes dietas estão apresentados na Tabela III.
As larvas de tambaqui alimentadas com cisto de Artêmia salina descapsulados, apresentaram peso e comprimento superior (P<0,05) ao observado nos demais tratamentos (Tabela III). Isso indica que os cistos de Artêmia salina descapsulados demonstraram ser bem atrativos e proteicos, sendo bem aceitos pelas pós-larvas de tambaqui, provavelmente isso ocorreu devido a sua alta capacidade de flutuação e demora no afundamento no tanque de cultivo facilitando a sua captura. Segundo García et al. (2011), o melhor desempenho obtido em larvas de peixes alimentadas com cistos descapsulados pode estar relacionada com uma maior quantidade de alimentos (matéria seca) consumidas e, portanto, maior quantidade de proteínas, lipídios, carboidratos e energia. Esses resultados corroboram com os encontrados por Lombardi e Gomes (2008), que alimentaram larvas de tambacu com cistos de A. salina descapsulado. Que também foi observado por Baboli et al. (2012), alimentando larva de truta marrom (Salmo trutta caspius) com cistos de Artemia descapsulados durante 35 dias.
VALORES MÉDIOS (±DESVIO PADRÃO) DE COMPRIMENTO (MM) E SOBREVIVÊNCIA (%) DE LARVAS DE TAMBAQUI (Colossoma macropomum) SUBMETIDAS A DIFERENTES DIETAS
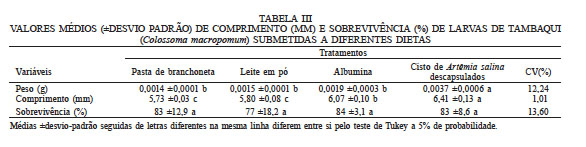
Médias ±desvio-padrão seguidas de letras diferentes na mesma linha diferem entre si pelo teste de Tukey a 5% de probabilidade Médias ±desvio-padrão seguidas de letras diferentes na mesma linha diferem entre si pelo teste de Tukey a 5% de probabilidade
As larvas alimentadas com albumina apresentaram peso e comprimento inferiores ao registrado com cistos de A. salina descapsulados, porém o peso e comprimento foram superiores (P<0,05) ao obtido nos tratamentos com leite em pó e pasta de branchoneta, nos quais as larvas apresentaram o menor peso e comprimento. Nagel et al. (2012), obtiveram bom resultado substituindo a farinha de peixe pela albumina com nível de 50% em experimento com juvenis de truta arco-íris (Oncorhynchus mykiss W.). Resultados inferiores de peso e comprimento também foram encontrados por Tronco et al. (2007) em experimento, alimentando larva de jundiá (Rhamdia quelen) com uma dieta de 100% de albumina.
Os resultados de peso e comprimento foram inferiores no tratamento com leite em pó; isso pode estar relacionado com o valor proteico do leite que foi de 9% de proteína em uma porção de 26g, sendo inferior aos demais tratamentos. Segundo Dairiki e Silva (2011) a quantidade de proteína ingerida diminui conforme o crescimento do peixe. Em larvas, a exigência está em torno de 42% e decresce para até 20% quando o peixe alcança a idade adulta. De acordo com Kubitza (2003), diversas pisciculturas alimentam as pós-larvas ainda nas incubadoras com ração, leite em pó, gema de ovo crua ou cozida, levedura e diversos outros produtos. A maioria das pós-larvas não são capazes de aproveitar diretamente os nutrientes presentes nestes alimentos. O desenvolvimento que se observa nas pós-larvas recebendo estes alimentos se deve à ingestão indireta das bactérias aderidas às micropartículas de alimento e dos protozoários que se proliferam na água das incubadoras graças ao aumento na população bacteriana e à presença das partículas de alimento em suspensão.
Os resultados obtidos para utilização de pasta de branchoneta não se diferiram significativamente dos obtidos para dieta com leite em pó. Mesmo a pasta de branchoneta possuindo um valor proteico superior, acredita-se que o fornecimento na forma de pasta não seja tão atrativo, pelo fato do tamanho das partículas não serem adequadas ao tamanho da boca das larvas de tambaqui. Song et al. (2005) citaram que é muito importante, na primeira alimentação, analisar o tamanho da boca que possui uma relação positiva com o diâmetro do alimento, sendo importante dimensionar o tamanho do alimento proporcionalmente à dimensão da boca. Resultados inferiores também foram encontrados por Marinho (2007), ao alimentar larva de surubim (Pseudo-platystoma corruscans) com branchoneta em pó durante 10 dias, foi atribuído ao diâmetro das partículas do alimento. Yflaar e Olivera (2003), alimentando larva de camarão cinza com náuplios de branchoneta congelados, também obteve resultados inferiores de peso e comprimento até o estágio de PL10, o que foi atribuído ao processo de limpeza dos cistos de branchoneta e armazenamento inadequado.
Não houve diferença significativa (P>0,05) na taxa de sobrevivência das larvas nos diferentes tratamentos (Tabela III). Resultados inferiores e superiores de sobrevivência foram encontrados por Lombardi Gomes (2008), na primeira e segunda fase de seu experimento com sobrevivência em torno de 62 e 97% de sobrevivência, respectivamente, alimentando larva de tambacu com cisto de A. salina descapsulado. Tronco et al. (2007), encontraram resultados inferiores, com 76,67% de sobrevivência em seu experimento II com 14 dias de criação, onde alimentou larva de R. quelen com uma dieta de 100% de albumina. Resultados superiores foram encontrados por Morais (2005) quem, utilizando uma dieta à base de ovo cru e cozido de galinha, obteve um ótimo resultado com Symplysodon sp. alcançando uma sobrevivência de 91,98%.
Neste trabalho foi observado que mesmo leite em pó tendo um valor proteico bem inferior quando comparado com os outros tratamentos não foi um fator decisivo na variável sobrevivência, sendo que não foi observada diferença significativa entre os tratamentos. Resultado inferior de sobrevivência foi encontrado por Marinho (2007) alimentando larva de P. corruscans com branchoneta em pó durante 10 dias onde obteve sobrevivência média de 13,75%.
Conclusão
O conhecimento dos estágios de desenvolvimento do tambaqui Colossoma macropomum é de grande importância para o conhecimento biológico da espécie. A utilização de cisto de Artêmia salina descapsulado é indicada na dieta de pós-larva de tambaqui por ter promovido melhoras nas variáveis: peso, comprimento e taxa sobrevivência larval.
Gratidão
Os autores agradecem ao apoio financeiro da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES); à CODEVASF e o Centro Integrado de Recursos Pesqueiros e Aquicultura do Betume, 4ª/CIB, 4ªSR, Neópolis-SE, pelo auxílio no desenvolvimento deste trabalho.
DESENVOLVIMENTO EMBRIONÁRIO E O EFEITO DE DIFERENTES DIETAS NO DESEMPENHO DE PÓS-LARVAS DE TAMBAQUI
Affonso EG, Barros FP, Brasil EM, Tavares-Dias M, Ono EA (2009) Indicadores fisiológicos de estresse em peixes expostos ao peróxido de hidrogênio (H2O2). Em Tavares-Dias M (Org.) Manejo e Sanidade de Peixes em Cultivo. Embrapa Amapá. Macapá, Brasil. pp. 346-360.
Baboli MJ, Roozbehfar R, Biria M (2012) Use of decapsulated artemia cysts for the growth and survival of caspian salmon (Salmo trutta caspius) fry. Int. J. Biosci. 2: 110-115.
Boscolo WR, Hayashi C, Soares CM, Furuya WM, Meurer F. (2001) Desempenho e características de carcaça de machos revertidos de tilápias do Nilo (Oreochromis niloticus), linhagens tailandesa e comum, nas fases inicial e de crescimento. Rev. Bras. Zootec. 30: 1391-1396.
Buzollo H, Veríssimo-Silveira R, Oliveira-Almeida IR, Alexandre JS, Okuda HT, Ninhaus-Silveira A (2011) Structural analysis of the Pimelodus maculatus (Lacépède, 1803) embryogenesis (Siluriformes: Pimelodidae). Neotrop. Ichthyol. 9: 601-616.
Conceição LEC, Yúfera M, Makridis P, Morais S, Dinis MT (2010) Live feed for early stages of fish rearing. Aquacult. Res. 41: 613-640.
Dairiki JK, Da Silva TBA (2011) Revisão de Literatura: Exigências Nutricionais do Tambaqui - Compilação de Trabalhos, Formulação de Ração Adequada e Desafios Futuros. Embrapa Amazônia Ocidental. Manaus, Brasil. 44 pp.
De Alexandre JS, Ninhaus-Silveira A, Veríssimo-Silveira R, Buzollo H, Senhorini JA, Chaguri MP (2010). Structural analysis of the embryonic development in Brycon cephalus (Gunther, 1869). Zygote 18: 173-183.
Diemer O, Neu DH, Sary C, Finkler JK, Boscolo WR, Feiden A (2012) Artemia sp. na alimentação de larvas de jundiá (Rhamdia quelen). Ciênc. Anim. Bras. 13: 175-179.
Faustino F, Nakaghi LSO, Marques C, Ganeco LN, Makino LC (2010) Structural and ultrastructural characterization of the embryonic development of Pseudoplatystoma spp. hybrids. Int. J. Dev. Biol. 54: 723-730.
Faustino F, Nakaghi LSO, Neumann E (2011) Brycon gouldingi (Teleostei, Characidae): aspects of the embryonic development in a new fish species with aquaculture potential. Zygote 19: 351-363.
García V, Celada JD, Carral JM, González R, González A, Sáez-Royuela MA (2011) Comparative study of different preparations of decapsulated Artemia cysts as food for tench (Tinca tinca L.) larvae. Anim. Feed Sci. Tech. 70: 72-77
Godinho H (2007) Estratégias reprodutivas de peixes aplicadas à aquicultura: bases para o desenvolvimento de tecnologias de produção. Rev. Bras. Reprod. Anim. 31: 351-360.
Kubitza F (2003) Larvicultura de peixes nativos. Panorama Aquicult. (maio-junho): 47-56.
Leite LV, Melo MAP, Oliveira FCE, Pinheiro JPS, Campello CC, Nunes JF, Salmito-Vanderley CSB (2013) Determinação da dose inseminante e embriogênese na fertilização artificial de tambaqui (Colossoma macropomum). Arq. Bras. Med. Vet. Zootec. 65: 421-429.
Lemos MVA, Guimarães IG, Miranda EC (2011) Farelo de coco em dietas para o tambaqui (Colossoma macropomum). Rev. Bras. Saúde e Prod. Anim. 12: 188-198.
Lombardi DC, Gomes LC (2008) Substituição de alimento vivo por alimento inerte na larvicultura intensiva do tambacu (♀Colossoma macropomum × ♂Piaractus mesopotamicus). Acta Sci. Anim. Sci. 30: 467-472.
Maciel CMRR (2006) Ontogenia de Larvas De Piracanjuba, Brycon orbignyanus Valenciennes (1849) (Characiformes, Characidae, Bryconinae). Tese. Universidade Federal de Viçosa. Brasil. 229 pp.
Marinho SAM (2007) Sobrevivência e Crescimento de Larvas de Surubim Pseudoplatystoma corruscans (Spix & Agassiz, 1829) sob Diferentes Condições Alimentares. Tese. Universidade Federal Rural de Pernambuco. Brasil. 66 pp.
Marques C, Nakaghi LSO, Faustino F, Ganeco LN, Senhorini JA (2008) Observation of the embryonic development in Pseudoplatystoma coruscans (Siluriformes: Pimelodidae) under light and scanning electron microscopy. Zygote 16: 333-342.
Morais FB (2005) Sistema Intensivo de Incubação e Manejo de Cria de Acará Disco, Symphysodon spp. Tese. Universidade Federal Rural de Pernambuco. Brasil. 54pp.
Nagel F, Slawski H, Adem H, Tressel RP, Wysujack K, Schultz C (2012). Albumin and globulin rapeseed protein fractions as fish meal alternative in diets fed to rainbow trout (Oncorhynchus mykiss W.). Aquaculture 354-355: 121-127.
Ninhaus-Silveira A, Foresti F, Azevedo A (2006) Structural and ultrastructural analysis of embryonic development of Prochilodus lineatus (Valenciennes, 1836) (Characiforme; Prochilodontidae). Zygote 14: 217-229.
Palma EH, Takahashi LS, Dias LTS, Gimbo RY, Kojima JT, Nicodemo D (2010) Estratégia alimentar com ciclo de restrição e alimentação no desempenho produtivo de juvenis de tilápia do Nilo da linhagem GIFT. Ciênc. Rural 40: 391-396.
Reynalte-Tataje D, Zaniboni-Filho E, Esquivel JR (2004) Embryonic and larvae development of piracanjuba, Brycon orbignyanus Valenciennes, 1849 (Pisces, Characidae). Acta. Sci. Biol. Sci. 26: 67-71.
Rocha CMC, Resende EK, Routledge EAB, Lundstedt LM (2013) Avanços na pesquisa e no desenvolvimento da aquicultura brasileira. Pesq. Agropec. Bras. 48: iv-vi.
Rodrigues APO (2014) Nutrição e alimentação do tambaqui (Colossoma macropomum). Bol. Inst. Pesca 40: 135-145.
Salmito-Vanderley CSB, Santana ICH (2010) Histologia e Embriologia Animal Comparada. Desenvolvimento de Peixes. 1ª ed. Fortaleza, Brasil.
Santos L, Filho MP, Sobreira C, Ituassú D, Fonseca FAL (2010) Exigência proteica de juvenis de tambaqui (Colossoma macropomum) após privação alimentar. Acta Amaz. 40: 597-604.
Silva JAM, Pereira Filho M, Cavero BAS, Oliveira-Pereira MI (2007) Digestibilidade aparente dos nutrientes e energia de ração suplementada com enzimas digestivas exógenadas para jevenis de tambaqui (Colossoma macropomum Cuvier, 1818). Acta Amaz. 37: 157-164.
Sividanes VP, Fries EM, Decarli JA, Feiden A, Hermes CA (2013) Desenvolvimento embrionário do piau vermelho Leporinus copelandii (Steindachner, 1875). Cultivando o Saber 6: 85-94.
Sividanes VP, Decarli JA, Feiden A, Boscolo WR, Signor A, Signor AA, Diemer O (2012) Desenvolvimento embrionário do jundiá Rhamdia voulezi. Rev. Acad. Cs. Agr. Amb. 10: 403-408.
Song YB, Oh SR, Seo JP, Ji BG, Lim BS, Lee YD (2005) Larval development and rearing of longtooth grouper Epinephelus bruneus in Jeju Insland, Korea. J. World Aquacult. Soc. 36: 209-215.
Takata R (2007) Produção de Juvenis de Artemia franciscana e Análise da Utilização de Dietas Vivas e Inertes na Larvicultura Intensiva do Pintado Pseudoplatystoma coruscans. Tese. Universidade Estadual Paulista. Brasil. 117 pp.
Tronco AP, Radunz Neto J, Medeiros TS, Lima RL (2007) Alimentação de larvas de jundiá (Rhamdia quelen) com dietas semipurificadas e fontes lipídicas. Bol. Inst. Pesca 33: 9-17.
Valbuena-Villarreal RD, Zapata-Berruecos BE, David-Ruales C, Cruz-Casallas PE (2012) Desarrollo embrionario del capaz Pimelodus grosskopfii (Steindachner, 1879). Int. J. Morphol. 30: 150-156.
Yflaar BZ, Oliveira A (2003) Utilização de náuplios de “branchoneta” Dendrocephalus brasiliensis (Pesta, 1921) na alimentação de larvas do "camarão cinza" Litopenaeus vannamei (Boone, 1931). Acta Sci. Biol. Sci. 25: 299-307.
Autor notes
vitorzoo@hotmail.com
