COMUNICACIONES
Recepção: 04 Abril 2017
Corrected: 03 Maio 2018
Aprovação: 04 Maio 2018
Resumo: Avaliou-se o crescimento inicial de Handroanthus serratifolius (Vahl) S.O. Grose. (ipê-amarelo amazônico) e Handroanthus ochraceus (Cham.) Mattos (ipe-amarelo de cerrado), cultivados sob telas de sombreamento pretas e coloridas. O delineamento utilizado foi inteiramente casualizado em esquema fatorial 2×5 (espécies × coberturas) com 16 repetições, em dois experimentos: o primeiro com os tratamentos pleno sol e telas pretas com 37,89; 57,57; 71,17 e 85,66% de retenção da radiação global; e o segundo com as telas de ~60% de sombreamento nas cores vermelha, azul, verde, prata e preta. As variáveis altura, diâmetro do coleto e número de folhas e folíolos, foram mensuradas a cada 20 dias. Uma análise destrutiva com sete das repetições foi realizada ao final do período experimental para obtenção das massas seca de folhas, caule e raiz, assim como, a área foliar. Os dados foram submetidos à análise de variância, regressões e teste Tukey a 5%. H. serratifolius e H. ochraceus diferiram para todas as variáveis. As condições pleno sol e tela preta de 37,89% proporcionaram as melhores respostas de crescimento em todas as variáveis e nas mudas sob sombreamento >57,57% as piores. O uso da tela colorida vermelha proporcionou maior crescimento vegetativo das espécies, enquanto o crescimento sob tela azul foi inibido. Conclui-se que a intensidade e a qualidade da radiação global retida e transmitida influenciam o crescimento inicial de mudas de H. serratifolius e H. ochraceus.
Palavras-chave: Ecofisiologia, Handroanthus serratifolius, Handroanthus ochraceus, Produção de Mudas, Radiação Solar.
Resumen: Se evaluó el crecimiento inicial de Handroanthus serratifolius (Vahl) S.O. Grose. (Lapacho-amarillo amazónico) y Handroanthus ochraceus (Cham.) Mattos (Lapacho-amarillo de la Savana), cultivados bajo pantallas de sombreado negras y coloridas. El delineamiento utilizado fue completamente al azar en esquema factorial 2×5 (especies × coberturas) con 16 repeticiones, en dos experimentos: el primero con los tratamientos de pleno sol y pantallas negras con 37,89; 57,57; 71,17 y 85,66% de retención de la radiación global; y el segundo con las pantallas de ~60% de sombreado en los colores rojo, azul, verde, plata y negro. Las variables altura, diámetro del colecto y número de hojas y folíolos, se midieron cada 20 días. Un análisis destructivo con siete de las repeticiones fue realizado al final del período experimental para la obtención de las masas secas de hojas, tallo y raíces, así como el área foliar. Los datos fueron sometidos al análisis de varianza, regresiones y test Tukey al 5%. H. serratifolius. H. ochraceus difirieron para todas las variables. Las condiciones pleno sol y pantalla negra del 37,89% proporcionaron las mejores respuestas de crecimiento en todas las variables y en los vástagos bajo sombreado >57,57% las peores. El uso de la pantalla en color rojo permitió mayor crecimiento vegetativo de las especies, mientras que el crecimiento bajo la pantalla azul fue inhibido. Se concluye que la intensidad y la calidad de la radiación global retenida y transmitida influencian el crecimiento inicial de los vástagos de H. serratifolius y H. ochraceus.
Abstract: The initial growth of Handroanthus serratifolius (Vahl) S.O. Grose. (Amazon yellow ipe) and Handroanthus ochraceus (Cham.) Mattos (Brazilian Cerrado yellow ipe), cultivated under black and colored shading net, was evaluated. The experimental design was completely randomized in a 2×5 factorial scheme (species × coverings) with 16 replications, in two experiments: the first one with the treatments of full sun and black nets with 37.89, 57.57, 71.17 and 85.66% retention of global radiation; and the second with nets of ~60% shading in red, blue, green, silver and black colors. The variables height, stem diameter and number of leaves and leaflets were measured every 20 days. A destructive analysis with 7 of the replicates was done at the end of the experimental period to obtain the dry masses of leaves, stem and root, as well as the leaf area. Data were submitted to analysis of variance, regressions and Tukey test at 5%. H. serratifolius and H. ochraceusdiffered for all variables. The full sun and black net conditions of 37.89% led to the best growth responses in all variables and the plants shaded by more than 57.57% the worst. The use of the red colored net permitted greater vegetative growth of the species, while growth under blue net was inhibited. It is concluded that the intensity and the quality of the retained and transmitted global radiation influence the initial growth of H. serratifolius and H. ochraceus seedlings.
Introdução
Dentre os fatores físicos do ambiente, a luz desempenha papel relevante na regulação da produção primária, contribuindo de forma efetiva para o crescimento das plantas. As respostas morfofisiológicas dos vegetais, contudo, não dependem apenas da presença, atenuação ou ausência da luz, mas também da qualidade espectral da luz incidente (Klein et al., 2016), visto que, o espectro e dispersão da radiação, possui influência no crescimento das plantas, podendo ocasionar mudanças em várias características anatômicas, morfológicas e bioquímicas (Brant et al., 2009).
As espécies florestais podem ser classificadas em dois grandes grupos segundo as necessidades luminosas, as pioneiras e as tardias no processo de sucessão. A alta intensidade luminosa é um fator que favorece o crescimento vigoroso das espécies pioneiras, podendo, contudo, causar danos às plântulas de espécies tardias. Todavia, o sombreamento excessivo pode causar o estiolamento e desenvolvimento insatisfatório de espécies pioneiras e favorecer o crescimento inicial de espécies tardias (Longhi et al., 2006).
Durante a fase de viveiro (desenvolvimento inicial), as características ambientais como umidade e temperatura do ar, intensidade e qualidade da luz, podem ser manipuladas de forma a favorecer ecofisiologicamente a produção vegetal. Por essa razão, tem sido cada vez mais comum a utilização de telados de forma a promover alterações diretas na intensidade e no espectro da radiação, e indiretas na temperatura e umidade relativa do ar, visando o aumento da qualidade e produtividade das mudas (Henrique et al., 2011).
Handroanthus serratifolius e Handroanthus ochraceus são duas espécies de Ipê amarelo nativas do Brasil, pertencentes a família Bignoniaceae, com distribuição entre os diversos domínios fitogeográficos, sendo, contudo, comumente encontrados nos domínios da Amazônia e Cerrado, respectivamente (Zappi et al., 2015). Devido ao aspecto ornamental, principalmente durante a floração, as espécies vêm sendo largamente utilizada para fins de arborização, assim como, em virtude da resistência a ambientes xerófitos com baixa fertilidade química e pH, também são empregadas na recuperação de áreas degradadas (Lorenzi, 1992).
A falta de informações técnicas que permitam a obtenção de mudas vigorosas, aliadas a deficiência de conhecimento sobre a ecofisiologia, morfologia e anatomia de espécies florestais, principalmente durante a fase inicial, são alguns dos fatores que limitam a produção de mudas de qualidade de muitas espécies como os ipês. Assim esse trabalho teve por objetivo avaliar o crescimento e o desenvolvimento inicial das espécies de ipê-amarelo amazônico (Handroanthus serratifolius) e ipê-amarelo do cerrado (Handroanthus ochraceus), propagadas por sementes, em diferentes níveis de luminosidade e qualidade espectral da radiação proporcionados por telas poliefinas pretas e coloridas, na região de transição Cerrado-Amazônia.
Materiais e Métodos
O experimento foi instalado no Setor de Produção Vegetal da Universidade Federal de Mato Grosso, Campus Universitário de Sinop, localizado nas coordenadas 11,85°S e 55,56°O e com altitude média de 371m. Segundo a classificação de Koppen, o tipo climático predominante na região é o Aw - clima tropical úmido, com estação seca bem definida (maio a setembro) e precipitação média anual em torno de 1970mm (85% desse total concentrada entre outubro e março), e com temperatura média anual de 24,70°C (Souza et al., 2013).
As sementes das duas espécies de ipês-amarelo (H. serratifolius e H. ochraceus), foram germinadas em câmara de germinação sob temperatura constante de 30°C e fotoperíodo de 12h, até o aparecimento da raiz primária e das folhas cotiledonares. Após a germinação as plântulas foram acondicionadas em bandejas de poliestireno, contendo substrato comercial (Holambra) por um período de 25 dias. Com a constatação do surgimento do primeiro par de folhas verdadeiras e estabilização do sistema radicular as mudas foram transplantadas para vasos com volume de 8 litros contendo substrato, composto pela mistura de 30% de substrato comercial (Holambra) e 70% de terra de vegetal, e incorporado formulação 1,5% de fertilizante químico NPK (5-30-10).
As bandejas com as plântulas e posteriormente os vasos contendo as mudas foram mantidos sob as telas de sombreamento (tratamentos) alinhadas no sentido norte-sul com as dimensões de 3,0×1,0×1,5m (comprimento, largura e altura). Os tratamentos testados foram (Tabela I): pleno sol, telas poliefinas pretas a 37,89; 57,57, 71,17 e 85,66% de atenuação da radiação global e telas coloridas chromatinet vermelha (54,15%) e azul (66,05%), frontinet verde (65,48%) e aluminet prata (61,88%).
PERCENTUAL DE TRANSMISSIVIDADE DE DIFERENTES COMPONENTES DA RADIAÇÃO SOLAR PARA AS TELA DE SOMBREAMENTO,QUANDO COMPARADAS COM A CONDIÇÃO DE PLENO SOL

As avaliações de crescimento não destrutivas foram realizadas, a cada 20 dias, entre 06/07/2015 (data do transplantio) e 15/04/2016, em 16 mudas por espécie em cada condição de sombreamento. Para avaliar o crescimento das plantas foram mensuradas as variáveis: altura das mudas (cm), medida do colo da planta até a gema apical (com régua graduada); diâmetro do caule (mm), medida no colo da muda com auxílio de paquímetro digital; número de folhas, consideradas apenas as folhas totalmente expandidas; e número de folíolos, considerando o tipo de folha em cada fase do desenvolvimento (folhas simples, trifoliada e digitada).
Na última avaliação, aos 281 dias após o transplantio para os vasos (DAT), realizou-se a análise destrutiva de sete mudas de cada espécie por cada tratamento. Foram obtidos os valores da massa seca das raízes (MSR), da parte aérea (MSPA), considerada pela soma da massa seca do caule (PMSC) e da massa seca das folhas (MSF); e a área foliar total da muda (cm.) determinada pelo integralizador fotoelétrico de área modelo Li-3100 (LI-COR). Com base nos dados de área foliar e da massa seca foram obtidos o índice de área foliar (IAF), razão de área foliar (RAF) e área foliar específica (AFE), segundo Benincasa (2003).
O monitoramento meteorológico nas condições de pleno sol foi realizado em uma estação próxima a área experimental (distante 50m), sendo medidas diariamente a evaporação do tanque classe A, precipitação pluvial, temperatura do ar (Tar), umidade relativa do ar (UR), radiação global e insolação. No interior dos viveiros (telados), para medidas de rotina com intervalos de 10min da temperatura e a umidade relativa do ar foram instalados termohigrômetros KlimaLogg Pro (TFA Dostmann GmbH, Alemanha).
A irrigação das mudas foi realizada diariamente com base na evapotranspiração da cultura, dada pelo produto entre a evapotranspiração referência do dia (ETo) obtida pelo método do tanque Classe A (coeficiente de tanque de 0,7795 (Souza et al., 2015) e o coeficiente de cultivo (Kc) de 0,78 (Monteiro et al., 2016).
Para obtenção dos graus-dias acumulados (GDA) empregou-se a metodologia de Ometto (1981), considerando as temperaturas basais mínimas (Tb) de 14,52 e 15,77°C, e basais máximas (TB) de 34,42 e 34,80°C, para H. serratifolius e H. ochraceus, respectivamente, determinadas por meio de regressões lineares entre as temperaturas mínimas e máximas diárias e o índice de área foliar, na fenofase de mudança das folhas de folíolos simples para trifólios (Figura 1).
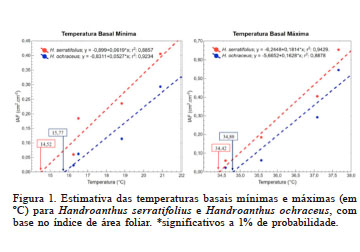
Figura 1
Estimativa das temperaturas basais mínimas e máximas (em ºC) para Handroanthus serratifolius e Handroanthus ochraceus, com base no índice de área foliar. *significativos a 1% de probabilidade.
A análise estatística foi realizada de maneira isolada, considerando-se parcelas subdivididas no tempo, em esquema fatorial 2×5 (espécies × coberturas). No primeiro caso, analisou-se as diferentes intensidades de sombreamento, por meio das telas pretas de 37,89; 57,57; 71,17 e 85,66% e a condição de pleno sol. No segundo caso, avaliou-se as variações espectrais da radiação solar por meio das telas coloridas (vermelha, verde, azul, prata e preta, todas consideradas comercialmente com retenção de 50% da luz). Para as análises não destrutivas foram consideradas 16 repetições (sendo cada vaso uma repetição), enquanto que nas análises destrutivas foram consideradas sete repetições. Os dados foram submetidos a análise de variância, pelo teste F, e quando significativas, foram realizadas comparações de médias pelo teste Tukey a 5% de significância, com o software Sisvar 5.6 (Ferreira, 2011) ou ajustadas regressões para as variáveis quantitativas com o software Statistica 13.3 Basic Academic Blunde.
Resultados e Discussão
As precipitações ocorreram entre 93 e 281 DAT, com acúmulos de 1237mm (Figura 2). A temperatura média do ar (Tar) no período experimental, na condição pleno sol, foi de 26,8°C. A umidade relativa do ar (UR) aumentou após o período de estiagem, passando de 58,2 para 79,3%, com UR mínimas e máximas diárias de 50,78 e 97,21%, respectivamente. Para a radiação global (H.) observou-se pequenas alterações na estação seca, com médias diárias de 21,2MJ·m-2/dia, todavia nota-se grandes variações na transmissividade atmosférica na estação chuvosa (Souza et al., 2016). Por conseguinte, ocorreu decréscimo na insolação diária entre os períodos de estiagem (8,87h/dia) e chuvoso (5,84h/dia).
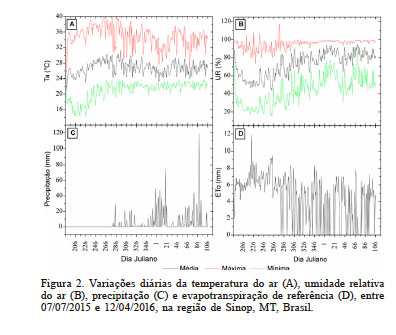
Figura 2
Variações diárias da temperatura do ar (A), umidade relativa do ar (B), precipitação (C) e evapotranspiração de referência (D), entre 07/07/2015 e 12/04/2016, na região de Sinop, MT, Brasil.
Os valores médios diários da Tar registradas sob as telas poliefinas pretas apresentaram sazonalidade semelhante a condição de pleno sol, com pequenas reduções de Tar com o aumento do percentual de sombreamento, com médias diárias de 26,39 e 26,02°C para as telas pretas 37,89 e 85,66% (Figura 3). Contudo, UR sofreu maiores atenuações, com médias diárias de 65% em pleno sol e de 80 a 83,90% de sombreamento.
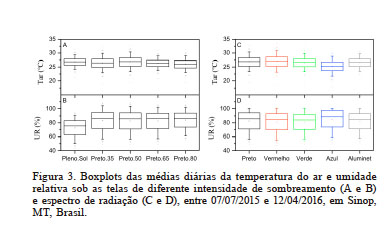
Figura 3
Boxplots das médias diárias da temperatura do ar e umidade relativa sob as telas de diferente intensidade de sombreamento (A e B) e espectro de radiação (C e D), entre 07/07/2015 e 12/04/2016, em Sinop, MT, Brasil.
O uso das telas poliefinas coloridas também promoveu alterações no microambiente, com menor Tar e maior UR na tela azul (25,27°C e 85,59%) e maior Tar na tela vermelha (27,0°C), com UR semelhante (81,39%) ao observado nas telas verde (81,20%) e prata (82,17%).
O uso das telas de sombreamento, com exceção da tela de 71,17%, possibilitou o crescimento em altura e diâmetro das mudas de H. serratifolius, com maior incremento a partir de 1500 GDa, quando submetidas as menores intensidades de radiação solar (Figura 4). Para H. ochraceus, independentemente do tipo de tela (pretas ou coloridas), o sombreamento inibiu o crescimento em altura e diâmetro das mudas.
O aumento do número de folhas (NF) para ambas as espécies ocorreu até 2500 GDa, atingindo médias de 13,42 e 10,47 folhas por planta para H. ochraceus e H. serratifolius. Acima dos 2500 GDa notou-se a estabilização do lançamento de novas folhas, com reduções de NF aos 3500 GDa para 11,14 e 8,95 folhas por planta para H. serratifolius e H. ochraceus, respectivamente (Figura 4). Nos diferentes tipos de sombreamentos (coloridas e pretas) não foram observadas diferenças no número de folhas até 1000 GDa. Todavia, acima dessa soma térmica, ocorreu uma tendência de redução de NF com o aumento do nível de sombreamento com as telas pretas.

Figura 4.
Superfícies de resposta para altura de planta (A), diâmetro de coleto (B), número das folhas (C) e dos folíolos (D) para mudas de duas espécies de ipê-amarelo, em função da soma térmica acumulada (X) e da tela de sombreamento (Y - decimal da transmissividade global da tela (Figura 1)), em Sinop-MT, Brasil.
Observou-se também que, o número dos folíolos que compuseram as folhas das duas espécies, diminuiu com o aumento do bloqueio da radiação global (telas pretas). Contudo, foi crescente ao longo do tempo de avaliação para H. serratifolius em todas as condições de sombreamento e para H. ochraceus submetidas a pleno sol e telas pretas de 37,89% (Figura 4).
As diferentes fenofases no desenvolvimento das folhas ocorrem devido à característica genética das espécies. Em algumas espécies do gênero Handroanthus, pertencentes a família Bignoniaceae, após a emissão do par de folhas cotiledonares, as mudas emitem inicialmente um par de folhas simples verdadeiras. Em uma fase intermediária, as plantas passam a emitir pares de folhas compostas com três folíolos. Posteriormente, desde que não ocorram perturbações no crescimento do ramo, são emitidas folhas compostas por cinco folíolos, indicando que estas podem ser consideradas como folhas adultas e fontes da planta (Figura 5).

Figura 5
Desenvolvimento foliar de Handroanthus serratifolius: A1- folha simples, A2 – folha trifoliolada (3 folíolos) e A3 - folha digitada (5 folíolos); e Handroanthus ochraceus: A1- folha simples, A2 – folha trifoliolada (3 folíolos) e A3 - folha digitada (5 folíolos).
Nesse sentido, a soma térmica necessária para que ocorra o processo de diferenciação entre folhas simples e folhas trifolioladas foi de ~1500 GDa para ambas as espécies, enquanto que, para o aparecimento das folhas digitadas (cinco folíolos) exigiu-se ~2300 GDa para H. serratifolius e ~3000 GDa para H. ochraceus.
Do total da massa seca (MST) da planta, para as duas espécies de ipê observou-se maiores acúmulos nas raízes, sendo em torno de 40,50 e 52,70% para H. serratifolius e H. ochraceus, respectivamente. Sequencialmente, as folhas foram os órgãos com maior alocação de biomassa, compreendendo 32,46 e 27,17% da MST em H. serratifolius e H. ochraceus (Tabela II). Em H. serratifolius, para as partições de massa seca de caule (MSC) e folhas (MSF) não foram observas diferenças em função do sombreamento, com exceção para a tela preta de 71,17%. Já para H. ochraceus, aos maiores percentuais de MSC e MSF foram obtidos nas maiores intensidades de radiação (pleno sol e preta 37,89%).
VARIÁVEIS DE CRESCIMENTO DE MUDAS DE DUAS ESPÉCIES DE IPÊ-AMARELO CULTIVADAS SOB TELAS DE DIFERENTE INTENSIDADE DE SOMBREAMENTO E ESPECTRO DE RADIAÇÃO, AOS 281 DAT
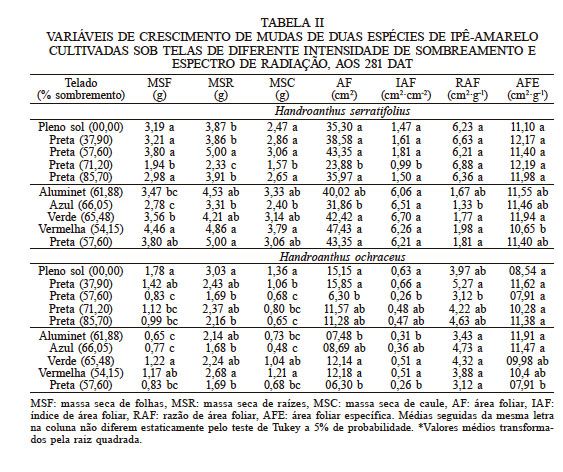
MSF MSF: massa seca de folhas, MSR: massa seca de raízes, MSC: massa seca de caule, AF: área foliar, IAF: índice de área foliar, RAF: razão de área foliar, AFE: área foliar específica. Médias seguidas da mesma letra na coluna não diferem estaticamente pelo teste de Tukey a 5% de probabilidade. *Valores médios transformados pela raiz quadrada.
Semelhante a massa seca, para H. serratifolius a área foliar (AF) e seus índices (IAF, RAF e AFE) não variaram significativamente com os incrementos das intensidades de luminosidade, com exceção do tratamento com tela de 71,17% (Tabela II). Contudo, para H. ochraceus, observou-se que as variáveis dependentes da área foliar apresentaram redução com o aumento do nível de sombreamento.
O uso de telas de sombreamento de diferentes colorações influenciou no crescimento de ambas as espécies de ipê. Para altura, diâmetro, NF e número de folíolos, a tela vermelha 54,15% propiciou os maiores valores, enquanto que a tela azul 66,05% gerou os menores incrementos.
Semelhante aos resultados encontrados nas telas monocromáticas, nas telas coloridas, a maior alocação de carboidratos ocorreu nas raízes (54,70 e 39,40% da MST), seguido das folhas (24,20 e 32,40% da MST), para H. ochraceus e H. serratifolius, respectivamente. Em geral, o uso da tela vermelha 54,15% e azul 66,05%, para ambas as espécies, proporcionou as maiores e menores alocações da massa seca em todos os órgãos. Esse mesmo comportamento também foi observado para a área foliar e seus índices (IAF, RAF e AFE).
As variações morfométricas avaliadas nas plantas (altura, diâmetro, NF e número de folílios) em função da soma térmica acumulada (GDa) foram descritas por regressões polinomiais de segunda ordem (Figura 6), com coeficientes lineares e angulares significativos a 5% de probabilidade (Tabela III). Para H. serratifolius, não foi possível determinar pontos máximos para nenhuma variável morfométrica. Já para H. ochraceus, definiu-se como GDa que permite o maior número de folhas (NF) os valores de 2220, 2133, 2088 e 2023 GDa, que permitiu obter 14,93; 13,37; 12,89; e 12,61 folhas por planta, para pleno sol e telas pretas de 37,89; 57,57 e 85,66% de sombreamento, respectivamente.
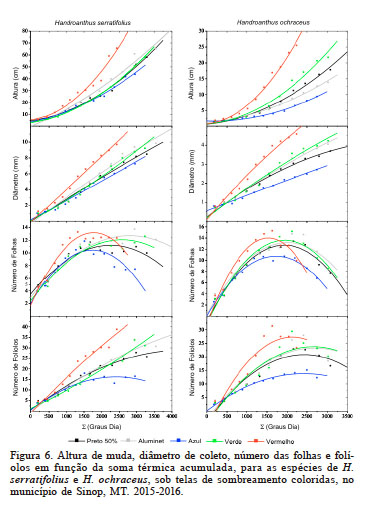
Figura 6
Altura de muda, diâmetro de coleto, número das folhas e folíolos em função da soma térmica acumulada, para as espécies de H. serratifolius e H. ochraceus, sob telas de sombreamento coloridas, no município de Sinop, MT. 2015-2016.
MODELOS POLINOMIAIS AJUSTADOS (y= a+bx+cx2) E COEFICIENTES DE DETERMINAÇÃO (R2) PARA VARIÁVEIS DE MORFOMÉTRICAS DE MUDAS DE DUAS ESPÉCIES DE IPÊ-AMARELO, CULTIVADAS SOB TELAS DE SOMBREAMENTO EM DIFERENTES COMPRIMENTOS DE ONDA
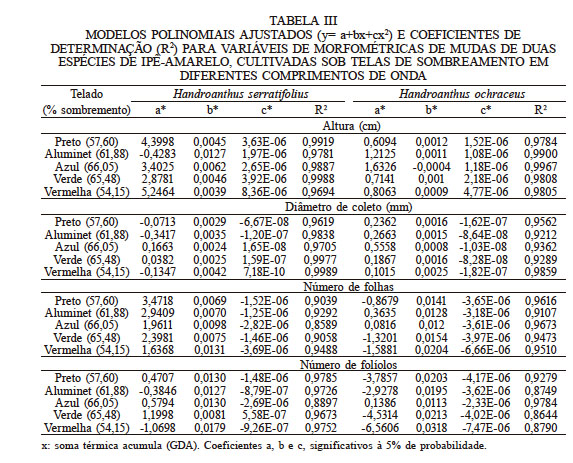
x x: soma térmica acumula (GDA). Coeficientes a, b e c, significativos à 5% de probabilidade.
O uso das telas de sombreamento pretas e coloridas permitiu alterações no comportamento das variáveis do crescimento para as duas espécies. Nesse contexto, infere-se que H. ochraceus e H. serratifolius são sensíveis às mudanças na intensidade e qualidade do espectro de radiação solar durante sua fase inicial de desenvolvimento. As diferenças de crescimento foram notadas, de forma mais expressiva, após os 87 DAT (correspondente ao final da estação seca), em função das modificações microclimáticas no ambiente de cultivo, com maior UR e diminuições de Tar (média diária e da amplitude térmica), da insolação e dos níveis de radiação global incidente (Figura 2).
Como a função das telas de sombreamento é diminuir parte da radiação global incidente (por absorção ou reflexão), pode-se indicar que as diferenças não significativas no crescimento das mudas obtidas até 87 DAT (estação seca), são justificadas pelo fato de que, atenuações >57,57% de sombreamento ainda permitem o suprimento da demanda de fótons utilizados durante a etapa fotoquímica da fotossíntese. Associa-se ainda, que as modificações nas condições do ambiente, como a redução da amplitude térmica diurna e noturna e o aumento de UR, podem favorecer o crescimento das mudas, pois diminuem as chances de estresse hídrico e térmico na estação chuvosa.
As mudas de H. serratifolius apresentaram aumento de altura quando submetidas às menores intensidades de radiação. Esses resultados são semelhantes aos encontrados na literatura para espécies como Simanrouba amara Aulb (Azevedo et al., 2010), Caesalpinia ferrea (Lima et al., 2008), Mimosa caesalpiniifolia Benth e Sterculia foetida (Camera e Endres, 2008), nas quais, o crescimento superior em altura, das plantas sombreadas, aconteceu como uma resposta de fuga ao déficit de luz, ocasionando estiolamento ainda na fase de muda.
As respostas das plantas ao sombreamento variam de forma intra e interespecífica, conferindo vantagens seletivas à adaptação de diferentes ambientes (Franklin, 2008). Ciolfi et al. (2013) relataram duas estratégias dos vegetais em resposta a competição por luz: a tolerância e a fuga ao sombreamento. Em dicotiledôneas, o fenômeno mais marcante como resposta das plantas para evitar o sombreamento é o rápido alongamento do caule de forma a elevar o aparato fotossintético acima da copa das plantas competidoras (Franklin e Quail, 2010). Além do alongamento do caule, as plantas do grupo intolerante ao sombreamento, inicialmente exibem outras respostas sob condições de baixa radiação, como aumento da área foliar e reduções no diâmetro do coleto e incorporação da biomassa (Markesteijn e Poorter, 2009;Caron et al., 2007;Ciolfi et al., 2013;Legner et al., 2013).
A redução de 50% da intensidade de radiação solar pode causar decréscimo de até 60% na assimilação líquida de CO. em espécies sensíveis ao sombreamento (Cassol et al., 2007) devido a redução da atividade fotossintética (Oliveira et al., 2016). Dessa forma, plantas sombreadas tendem a aumentar a área foliar para maximizar a absorção de energia (Teixeira et al., 2013). Contudo, o custo de investimento no órgão foliar somente é possível devido a realocação dos fotoassimilados de outras partes da planta, o que tende a proporcionar menores diâmetros de caule.
Nas mudas de H. serratifolius observou-se que apesar da altura ter sido maior nas menores intensidades luminosas, o diâmetro do coleto não diferiu entre plantas sob pleno sol e telas pretas de 57,57 e 85,66% de sombreamento, indicando que essa espécie pode ser considerada como pouco tolerante ao sombreamento, uma vez que, o crescimento do caule, quando sombreado, ocorreu preferencialmente em altura.
Além do crescimento desigual do caule, H. serratifolius exibiu ainda menores números de folhas e folíolos quando cultivado a 85,66% de sombreamento após 258 DAT (2500 GDa). Contudo, observou-se que essa condição, propiciou os maiores valores de número de folhas e folíolos até os 131 DAT (1000 GDa), indicando que nas fases iniciais, as mudas investiram o material orgânico produzido no próprio aparato fotossintético e no crescimento em altura como tentativa de evitar o sombreamento.
Em espécies crescendo sob sombreamento, comumente observa-se maior alocação dos fotoassimilados para produção e modificação das folhas (Legner et al., 2013; Giertych et al., 2015). Esse efeito ocorre para a otimização da partição de fotoassimilados (Thornley, 1972;Bloom et al., 1985), na qual as plantas investem na produção dos componentes que facilitem a aquisição do recurso limitante no ambiente (Giertych et al., 2015). Nas espécies que compõem o grupo das intolerantes, o gradiente de alocação da biomassa ocorre preferencialmente para o órgão folhas, permitindo o aumento da exploração de luz para a fotossíntese (Markesteijn e Poorter, 2009).
O decréscimo do número de folhas indica que a quantidade de energia na forma de carboidrato disponível para a planta, pode ser insuficiente para suprir o investimento em novos tecidos foliares por longos períodos no ponto de compensação lumínica. Assim, o sombreamento com tela preta de 85,66% por períodos maiores do que quatro meses pode ser considerado prejudicial em mudas de H. serratifolius.
Por conseguinte, plantas crescendo sob alta intensidade de radiação solar (pleno sol), em contrapartida, apresentam alta taxa de assimilação de CO. (Oliveira et al., 2016). Contudo, sob tais condições, as plantas estão expostas a alta temperatura foliar, o que pode acarretar no fechamento estomático e consequentemente na diminuição da absorção de CO. durante parte do dia (Hamerlynck e Knapp, 1996; Cui et al., 2006). Limitações na assimilação de CO. impostas pelo fechamento estomático podem promover desbalanço na cadeia de transferência de elétrons, levando a superexcitação e consequentemente fotoinibição e, ainda, danos ao centro de reação dos fotossistemas (Li et al., 2009). Esse processo poderá, portanto, induzir o consumo de parte dos produtos da fotossíntese para a recuperação do aparelho fotossintético pré-existente, e diminuir a alocação dos produtos orgânicos para o processo respiratório celular, que por sua vez resultaria no incremento em altura e/ou diâmetro por meio da divisão celular.
As mudas de H. serratifolius sob tela preta de 57,57% de sombreamento também apresentaram alocação menor de biomassa para o crescimento do diâmetro do coleto e número de folhas, entretanto, nesta condição, a área foliar e a biomassa total da planta, das folhas e do caule apresentaram os maiores valores médios. Portanto, infere-se que as mudas da espécie, apesar de sofrer certo nível de estiolamento a 57,57% de sombreamento, conseguem se desenvolver de maneira satisfatória com metade da radiação incidente.
As modificações no microclima sob tela preta de 37,89% de sombreamento proporcionaram reduções de Tar e aumento de UR do ambiente de cultivo, favorecendo o crescimento sem, contudo, reduzir a intensidade da radiação disponível aos níveis mínimos necessários para que o processo fotossintético e outros processos metabólicos ocorram de forma satisfatória para H. serratifolius. Essa espécie é comumente classificada, na sucessão ecológica, como uma espécie secundária inicial (Lorenzi, 1992); ou seja, apresenta alta capacidade de se desenvolver em ambientes abertos, com alta luminosidade. Contudo, é adaptada, ainda, a certo nível de sombreamento, geralmente causado pela presença de espécies heliófilas iniciais.
A espécie de ipê amarelo do cerrado (H. ochraceus) exibiu decréscimo de todas as variáveis analisadas com o aumento do sombreamento (Figura 4). Observou-se até os 65 DAT respostas típicas de fuga ao sombreamento, como o aumento em altura e número de folhas das mudas submetidas a condições >71,17% de sombreamento. Em acréscimo foi observado reduções do incremento em crescimento sob as malhas, evidente após 65 DAT, demonstrando pouca adaptabilidade das mudas a condição de baixa intensidade de radiação.
A alocação da biomassa seca, indiferente da condição de sombreamento, ocorreu preferencialmente nas raízes (45,76 e 70,85% da MST para o ipê-amarelo amazônico e do cerrado; Tabela II). A distribuição da massa seca entre os órgãos de um vegetal é uma característica inerente a cada espécie (Benincasa, 2003) sendo comumente influenciadas por alterações no ambiente (Costa et al., 2010). Muitas espécies intolerantes ao sombreamento apresentam alta demanda de água e nutrientes para suprir sua elevada taxa fotossintética e crescimento rápido. Essas espécies quando encontradas em ambientes xéridos (Schenk e Jackson, 2002) ou com longos períodos de seca (Paz, 2003) investem parte da biomassa produzida no aprofundamento das raízes, aumentando a probabilidade de encontrar nutrientes e água (Markesteijn e Poorter, 2009).
As duas espécies avaliadas, em especial H. ochraceus, apesar de apresentar ampla distribuição de ocorrência são encontradas com frequência em ambientes perturbados e ecossistemas com baixa disponibilidade hídrica em grande parte do ano (características do bioma Cerrado). Assim, a alocação de biomassa nas raízes pode ser considerada uma estratégia da espécie as condições típicas desses ambientes.
Todas as variáveis biométricas não destrutivas (altura, diâmetro, número de folhas e número de folíolos) em H. serratifolius e H. ochraceus foram afetadas significativamente pelas telas coloridas (Figura 6). As alterações no microambiente causadas pelos telados com coloração vermelha (54,15%) proporcionaram os maiores níveis de crescimento. Em contrapartida, os efeitos do telado com coloração azul (66,05%) foram observados de maneira mais significativa nas alterações fenológicas das folhas, com tendência ao retardo do desenvolvimento vegetativo das mudas.
As relações entre os efeitos da qualidade da radiação no desenvolvimento do vegetal ainda não são claras. De forma geral, as modificações no espectro da radiação são fatores importantes no crescimento vegetal por causar alterações morfoanatômicas (Gomes et al., 2009). Alguns autores, cujos resultados não corroboram com os deste estudo, relatam não terem encontrado influência do comprimento de onda no desenvolvimento de diversas espécies de plantas superiores (Melo et al., 2009; Costa et al., 2010; Henrique et al., 2011). Contudo, os mesmos autores, notaram diferenças como aumento dos incrementos das variáveis biométricas e acumulo de carboidratos em mudas crescendo sob telas com coloração vermelha.
No presente estudo, considerando as telas com 57,57% de sombreamento, o uso do telado na cor vermelha (54,15%) conferiu diferenças significativas ao crescimento das mudas do ipê-amarelo quando comparadas com as telas azul (66,05%) e preta para H. ochraceus; e azul (66,05%) e prata (61,88%) para H. serratifolius. Porém, de forma semelhante as observações de Oren-Shamir et al. (2001), a distribuição da biomassa nas mudas não ficou restrita ao crescimento em altura, não permitindo dessa forma atribuir o desempenho da tela unicamente a resposta dos fitocromos ao sombreamento, mas sim a um provável aumento de vigor vegetal causado pela exposição a este comprimento de onda.
As variáveis relativas à área foliar são utilizadas pela sua relação com a capacidade fotossintética do vegetal. Assim, o menor desenvolvimento observado nas mudas sob telado azul (66,05%) pode estar relacionado com redução das variáveis foliares como o número de folhas e folíolos, área foliar e razão de área foliar.
A plasticidade fenotípica observada nas taxas foliares, em geral, está associada com o regime de intensidade luminosa, sendo a redução da área foliar normalmente relatada em plantas submetidas a pleno sol (Camera e Endres, 2008; Lima et al., 2008; Azevedo et al., 2010). Por outro lado, a redução na razão de luz vermelha/azul, causada pelo ambiente sob condição do telado vermelho, conforme Costa (2010), também é responsável pelo aumento da área foliar; assim como sob tela azul, onde a relação de azul/vermelho é alta, pode ocorrer a inibição do desenvolvimento.
Os comprimentos de onda na faixa espectral do azul são considerados vitais para o desenvolvimento das plantas superiores por participar de uma série de eventos fotomorfogénicos, bem como dos processos de abertura estomática, formação de clorofilas, cloroplastos e do ciclo circadiano (Matsuda et al., 2004; Kang et al., 2008; Demarsy e Frankhauser, 2009), estando assim diretamente ligada a fixação de carbono pela fotossíntese.
A luz azul, contudo, também é reconhecida por causar inibição do alongamento do caule e expansão da área foliar (Saebo et al., 1995; Dougher e Bugbee, 2004), principalmente pela sua deficiência, visto que ambientes com baixos níveis desse comprimento de onda causam o alongamento dos internós (Runkle e Heins, 2001). Plantas crescendo sob luz azul, segundo Leite et al. (2008), podem manter os estômatos abertos mesmo em condições não ideais (como instantes com alta temperatura do ar), prejudicando o crescimento das plantas. Além disso, os processos de alongamento do caule e alocação de biomassa que ocorrem preferencialmente na ausência da luminosidade (Myster, 1999) são inibidos em plantas expostas ao comprimento de onda da luz azul, mesmo por períodos curtos nos horários antecedentes ao anoitecer, devido, provavelmente, a redução das formas ativas dos fitocromos (Fraszczak, 2013).
Conclusão
O uso de telas de sombreamento pretas em diferentes intensidades altera o crescimento das mudas de ipê-amarelo amazônico e de cerrado, tanto por variáveis morfométricas (altura, diâmetro, número de folhas e número de folíolos) quanto pela alocação de massa seca e área foliar.
As telas poliefinas pretas de 37,89% de sombreamento produziram mudas de melhor qualidade. O uso de telas pretas com sombreamento >57,57% causa o estiolamento das mudas de H. serratifolius e reduz o crescimento de mudas de H. ochraceus.
H. serratifolius e H. ochraceus são sensíveis às mudanças na qualidade do espectro da radiação, sendo que tela poliefina vermelha permite produzir mudas de melhor qualidade, enquanto que tela poliefina azul proporciona menores incrementos em todas as variáveis biométricas.
O período máximo de permanência das mudas das duas espécies em viveiro é de 2500 GDa, ocorrendo após esse período a estabilização do crescimento em diâmetro e o decréscimo do número de folhas e folíolos. A época de transplantio para as duas espécies depende das condições climáticas regionais, sendo recomendada preferencialmente no início da estação chuvosa, permitindo assim o estabelecimento inicial com a menor taxa de mortalidade por deficiência hídrica, aliado ao menor custo com suplementação hídrica.
CRESCIMENTO INICIAL DE IPÊ-AMARELO AMAZÔNICO E DE CERRADO CULTIVADOS SOB DIFERENTES INTENSIADADES DE SOMBREAMENTO E COMPRIMENTO ESPECTRAL DE ONDA
Azevedo IMG, Alencar RM, Barbosa AP, Almeida NO (2010) Estudo do crescimento e qualidade de mudas de marupá (Simarouba amara Aubl.) em viveiro. Acta Amaz. 40: 157-164.
Barber J (2009) Photosynthetic energy conversion: natural and artificial. Chem. Soc. Rev. 38: 185-196.
Brant RSI, Pinto JEB, Rosa LF, Albuquerque CJ, Ferri PH, Corrêa RM (2009) Crescimento, teor e composição do óleo essencial de melissa cultivada sob malhas fotoconversoras. Ciênc. Rural 39: 1401-1407.
Benincasa MMP (2003) Análise de Crescimento de Plantas: Noções Básicas. 2ª ed. Funep. Jaboticabal, Brasil. 41 pp.
Bloom AJ, Chapin FS, Mooney HA (1985) Resource limitation in plants an economic analogy. Annu. Rev. Ecol. Evol. Systemat. 16: 363-392.
Câmara C, Endres L (2008) Desenvolvimento de mudas de duas espécies arbóreas: Mimosa caesalpiniifolia Benth. e Sterculia foetida L. sob diferentes níveis de sombreamento em viveiro. Floresta 38: 43-51.
Caron BO, de Souza VQ, Cantarelli EB, Manfron PA, Behling A, Cassol D, Falqueto AR, Bacarin EMA (2007) Fotossíntese em Mentha piperita e Melissa officinalis sob sombreamento. Rev. Bras. Biociênc. 5: 576-578.
Cassol D, Falqueto AR, Bacarin EMA (2007). Fotossíntese em Mentha piperita e Melissa officinalis sob sombreamento. Rev. Bras. Biociênc. 5: 576-578.
Ciolfi A, Sessa G, Sassi M, Possenti M, Salvucci S, Carabelli M, Morelli G, Ruberti I (2013) Dynamics of the shade-avoidance response in Arabidopsis. Plant Physiol. 163: 331-353
Costa LCDB, Pinto JEBP, Castro EMD, Alves E, Bertolucci SKV, Rosal LF (2010) Effects of coloured shade netting on the vegetative development and leaf structure of Ocimum selloi. Bragantia 69: 349-359.
Cui L, LI J, Fan Y, Xu S, Zhang Z (2006) High temperature effects on photosynthesis, PSII functionality and antioxidant activity of two Festuca arundinacea cultivars with different heat susceptibility. Bot. Stud. 47: 61-69.
Demarsy E, Fankhauser C (2009) Higher plants use LOV to perceive blue light. Curr. Opin. Plant Biol. 12: 69-74.
Dougher T, Bugbee B (2004) Long-term blue light effects on the histology of lettuce and soybean leaves and stems. J. Am. Soc. Hort. Sci. 129: 467-472.
Ferreira DF (2011) Sisvar: computer statistical analysis system. Ciênc. Agrotecnol. 35: 1039-1042.
Fraszczak B (2013) Effect of short-term exposure to red and blue light on dill plants growth. Hort. Sci. 40: 177-185.
Franklin KA (2008) Shade avoidance. New Phytol. 179: 930-944.
Franklin KA, Quail PH (2010) Phytochrome functions in Arabidopsis development. J. Exp. Bot. 61: 11-24.
Giertych MJ, Karolewski P, Oleksyn J (2015) Carbon allocation in seedlings of deciduous tree species depends on their shade tolerance. Acta Physiol. Plant. 37(10): 1-15.
Gomes IAC, Castro EM De, Soares AM, Alves JD, Alvarenga MIN, Melo AAM, Alvarenga AD (2009) Sombreamento de plantas de Catharanthusroseus (L.) G. Don ‘Pacifica White’por malhas coloridas: desenvolvimento vegetativo. Ciênc. Agrotecnol. 33: 514-520.
Hamerlynck E, Knapp AK (1996) Photosynthetic and stomatal responses to high temperature and light in two oaks at the western limit of their range. Tree Physiol. 16: 557-565.
Henrique PC, Alves JD, Deuner S, Goulart PFP, Livramento DE (2011) Aspectos fisiológicos do desenvolvimento de mudas de café cultivadas sob telas de diferentes colorações. Pesq. Agropec. Bras. 45: 458-465.
Kang B, Grancher N, Koyffmann V, Lardemer D, Burney S, Ahmad M (2008) Multiple interactions between cryptochrome and phototropin blue-light signalling pathways in Arabidopsis thaliana. Planta 227: 1091-1099.
Klein J, Rampim L, Kestring D, Guimarães VF, Rodrigues JD (2016) Influência de protetores físicos coloridos nas trocas gasosas em mudas de canafístula [Peltophorumdubium (Spreng.) Taub.]. Ciênc. Flor. 26: 797-809.
Legner N, Fleck S, Leuschner C (2013). Low light acclimation in five temperate broad-leaved tree species of different successional status: the significance of a shade canopy. Ann. For. Sci. 70: 557-570.
Leite CA, Ito RM, Lee GTS, Ganelevin R, Fagnani MA (2008) Light spectrum management using colored nets to control the growth and blooming of Phalaenopsis. Acta Hort. 770: 177-184.
Li Z, Wakao S, Fischer BB, Niyogi KK (2009) Sensing and responding to excess light. Annu. Rev. Plant Biol. 60: 239-260.
Lima JD, Silva BMS, Moraes WS, Dantas VAV, Almeida CC (2008) Efeitos da luminosidade no crescimento de mudas de Caesalpinia ferrea Mart. ex Tul. (Leguminosae, Caesalpinoideae). Acta Amaz. 38: 5-10.
Longhi SJ, Brena DA, Gomes JF, DA Silva Narvaes I, Berger G, Soligo AJ (2006) Classificação e caracterização de estágios sucessionais em remanescentes de Floresta Ombrófila Mista na Flona de São Francisco de Paula, RS, Brasil. Ciênc. Flor. 16: 113-125.
Lorenzi H (1992) Árvores Brasileiras: Manual de Identificação e Cultivo de Plantas Arbóreas Nativas do Brasil. Plantarum. Nova Odessa, Brasil. 352 pp.
Markesteijn L, Poorter L (2009) Seedling root morphology and biomass allocation of 62 tropical tree species in relation to drought and shade tolerance. J. Ecol. 97: 311-325.
Matsuda R, Ohashi-Kaneko K, Fujiwara K, Goto E, Kurata K (2004) Photosynthetic Characteristics of Rice Leaves Grown under Red Light with or without Supplemental Blue Light. Plant Cell Physiol. 45: 1870-1874.
Monteiro EB, Silva ACD, Souza AP, Tanaka AA, Ferneda BG, Martim CC (2016) Water requirements and crop coefficients of tropical forest seedlings in different shading conditions. Rev. Bras. Eng. Agríc. Amb. 20: 709-715.
Myster J (1999) The effects of temperature alternations, irradiance level, photoperiod, and day extension light quality on morphogenesis, growth, and flowering of Begonia x hiemalis Fotsch. Gartenbauwissenschaft 64: 206-213.
Oliveira GC, Vieira WL, Bertolli SC, Pacheco AC (2016) Photosynthetic behavior, growth and essential oil production of Melissa officinalis L. cultivated under colored shade nets. Chil. J. Agric. Res. 76: 123-128.
Ometto JC (1981) Bioclimatologia Vegetal. Agronômica Ceres. São Paulo, Brasil. 440 pp.
Oren-Shamir M, Gussakovsky EE, Shpiegel E, Nissim-Levi A, Ratner K, Ovadia R, Giller YE, Shahak Y (2001) Coloured shade nets can improve the yield and quality of green decorative branches of Pittosphorumvariegatum. J. Hort. Sci. Biotechnol. 76: 353-361.
Paz H (2003) Root/shoot allocation and root architecture in seedlings: variation among forest sites, microhabitats, and ecological groups. Biotropica 35: 318-332.
Runkle ES, Heins RD (2001) Specific functions of red, far red, and blue light in flowering and stem extension of long-day plants. J. Am. Soc. Hort. Sci. 126: 275-282.
Saebo A, Krekling T, Appelgren M (2002) Light quality affects photosynthesis and leaf anatomy of birch plantlets in vitro. Plant Cell Tiss. Org. Cult. 41: 177-185.
Schenk HJ, Jackson RB (2002) Rooting depths, lateral root spreads and below-ground/above-ground allometries of plants in water-limited ecosystems. Ecology 90: 480-494.
Souza AP, Zamadei T, Monteiro E B, Casavecchia BH (2016) Transmissividade atmosférica da radiação global na região amazônica de Mato Grosso. Rev. Bras. Meteorol. 31: 639-648.
Souza AP, De Almeida FT, Arantes KR, Martim CC, Da Silva JO (2015) Coeficientes de Tanque Classe A para estimativa da evapotranspiração de referência diária na região de transição Cerrado-Amazônica. Sci. Plena 11(5): 1-13.
Souza AP, Mota LL, Zamadei T, Martin CC, Almeida FT, Paulino J (2013) Classificação climática e balanço hídrico climatológico no estado de Mato Grosso. Nativa 1(1): 34-43.
Teixeira WF, Fagan EB, Silva JO, Da Silva PG, Silva FH, Sousa MC, De Carvalho Canedo S (2013) Atividade da enzima nitrato redutase e crescimento de Swietenia macrophylla king sob efeito de sombreamento. Flor. Amb. 20: 91-98.
Thornley JHA (1972) Balanced quantitative model for root: shoot ratios in vegetative plants. Ann. Bot. 36: 431-441.
Zappi DC, Filardi FLR, Leitman P, Souza VC, Walter BM, Pirani JR, Morim MP, Queiroz LP, Cavalcanti TB, Mansano VF, Forzza RC (2015) Growing knowledge: an overview of seed plant diversity in Brazil. Rodriguésia 66: 1085-1113.
Autor notes
pachecoufmt@gmail.com
