COMUNICACIONES
Recepción: 26 Abril 2021
Corregido: 22 Julio 2021
Aprobación: 23 Julio 2021
Resumen: En el año 2013 el 12% de los bosques de pino de México presentaron brotes de escarabajos descortezadores; la mayor incidencia ocurrió en el eje neovolcánico transversal, zona que coincide con la mayor diversidad de pinos. El género Dendroctonus Erichson contiene las especies de descortezadores consideradas como plagas primarias de los bosques mexicanos de coníferas, generan grandes pérdidas en la masa forestal y con ello impactos ecológicos y económicos de gran magnitud. El objetivo del trabajo fue identificar nematodos nativos con potencial para el manejo de Dendroctonus frontalis. El muestreo de suelo se realizó en abril de 2014 y septiembre de 2015, utilizando larvas de Galleria mellonella como trampa. Se aislaron tres cepas de nematodos (TMA2, GMA6, CGA7), siendo los tres aislados identificados como Pristionchus americanus Herrmann 2006, por sus características morfológicas y morfométricas. Se corroboró la identificación mediante análisis filogenéticos con una similitud del 99% con la especie. La patogenicidad de los nematodos se probóin vitro sobre adultos de D. Frontalis aplicando dosis de 1000 juveniles infectivos (JI) de los tres aislamientos realizados y se contabilizó la mortalidad a las 48 y 96h. Los datos fueron procesados con el modelo lineal generalizado (GLM) con distribución cuasibinomial. Los análisis indicaron que el aislamiento TMA2 obtuvo mejores resultados con un porcentaje de mortalidad de 92,25%, mientras que la cepa CGA7 y GMA6 no presentaron diferencias, con mortalidad de 76,54 y 63% respectivamente.
Palabras clave: Control Biológico, Descortezadores, Nematodos Entomopatógenos, Pristionchus americanus .
Abstract: In 2013, 12% of pine forests in Mexico had outbreaks of bark beetles; the highest incidence occurred in the Trans-Mexican Volcanic Belt, an area that coincides with the highest diversity of pine trees. The genus Dendroctonus Erichson contains the species of bark beetles considered as primary pests of Mexican coniferous forests, which generate large losses in the forest mass ecological and economic impacts of high magnitude. The objective of this work was to identify native nematodes with potential for the management ofDendroctonus frontalis. Soil sampling was carried out in April 2014 and September 2015, using Galleria mellonellalarvae as traps. Three nematode strains (TMA2, GMA6, GA7) were isolated, and based on morphological and morphometric characteristics, the three isolates were identified as Pristionchus americanus Herrmann 2006. Identification was corroborated by phylogenetic analysis with 99% similarity to the species. The pathogenicity of the nematodes was tested in vitro in adults of D. frontalis, doses of 1000 infective juveniles (JI) of the three isolates were applied and mortality was tested at 48 and 96h. The data were processed with a generalized linear model (GLM) with quasi-binomial distribution. The analyses indicated that isolate TMA2 had the best results with a mortality percentage of 92.25%, while strains CGA7 and GMA6 showed no differences, with mortality of 76.54% and 63%, respectively.
Resumo: Em 2013, 12% dos pinhais de México apresentavam focos de escaravelhos; a maior incidência ocorrendo no faixa neovulcânica transversal, área que coincide com a maior diversidade de pinheiros. O gênero Dendroctonus Erichson contém as espécies de escaravelhos considerados pragas primárias de florestas de coníferas mexicanas, gerando grandes perdas na massa florestal e com isso impactos ecológicos e econômicos de grande magnitude. O objetivo do studio foi identificar nematóides nativos com potencial para o manejo de Dendroctonus frontalis. A amostragem do solo foi realizada em abril de 2014 e setembro de 2015, usando larvas da Galleria mellonella como armadilha. Três linhagens de nematóides (TMA2, GMA6, CGA7) foram isoladas, o nematóide Pristionchus americanus Herrmann 2006 foi identificado nos três isolados por características morfológicas e morfométricas e a identificação foi corroborada por análise filogenética com 99% de similaridade com as espécies. A patogenicidade dos nematóides foi testada in vitro em adultos de D. frontalis, doses de 1000 juvenis infecciosos (JI) dos três isolados foram aplicadas e a mortalidade foi registrada em 48 e 96h. Os dados foram processados com o modelo linear generalizado (GLM) com distribuição quasibinomial. As análises indicaram que o isolado TMA2 obteve melhores resultados com percentual de mortalidade de 92,25% enquanto as cepas CGA7 e GMA6 não apresentaram diferenças, com mortalidades de 76,54 e 63% respectivamente.
Introducción
Los escarabajos descortezadores del género Dendroctonus (Coleóptera: Curculionidae: Scolytinae) son las principales plagas de los bosques de coníferas de México, de los cuales forman parte natural y desempeñan una función primordial en su dinámica al promover el recambio de especies vegetales. Sin embargo, algunas especies bajo ciertas condiciones incrementan sus densidades poblaciones y su capacidad de infestación, lo que ocasiona la muerte de extensiones grandes de arbolado (Díaz-Núñez et al., 2006;Del-Val y Sáenz-Romero, 2017).
En el año 2013 el 12% de los bosques de pinos del país presentaron brotes de descortezadores. La mayor incidencia ocurrió en el eje neovolcánico transversal, zona que coincide con la mayor diversidad de pinos (Salinas-Moreno et al., 2010; Cibrián et al., 2014; Del-Val y Sáenz-Romero, 2017). Dendroctonus frontalis Zimmerman es considerada una de las plagas primarias más importantes del país, ya que ocasiona la muerte de miles de árboles, lo que provoca un desequilibrio ecológico y pérdidas económicas de gran magnitud (Reséndiz-Martínez et al., 2016).
En el estado de Querétaro se ha incrementado el índice de infestación por descortezadores en bosques de pino, donde D. frontalis es una de las especies con mayor actividad (Gijón-Hernández et al., 2015). El control de estos insectos está regulado por la Norma Oficial Mexicana NOM-019-SEMARNAT-2006, que establece medidas de control mecánico y químico (DOF, 2008). Una alternativa de control biológico que ha sido poco explorada en el área forestal es el uso de organismos patógenos, como lo son los nematodos entomopatógenos, que poseen un alto potencial para el control de insectos plaga debido a que mantienen una relación simbiótica con bacterias que inducen la muerte por septicemia del huésped (Merino y France, 2009).
Este tipo de nematodos tienen características que le brindan potencial para ser agentes de control biológico, buscar activamente a sus hospederos y matarlos rápidamente al entrar en él y liberar bacterias simbiontes (Liu y Poinar, 2000); además son letales a un amplio rango de insectos de importancia económica (Bathon, 1996). El objetivo de esta investigación fue aislar e identificar nematodos entomopatógenos, así como evaluar in vitro su potencial para el manejo de insectos descortezadores.
Metodología
Muestreo de suelo
Los muestreos se realizaron, de abril a agosto 2014 y de abril a septiembre 2015, en los parajes La Gachupina, El Tejamanil y Campo Santo, municipio Pinal de Amoles, Querétaro. Las muestras de suelo fueron tomadas al azar de la periferia de árboles de pino con síntomas y signos de descortezadores (grumos de resina en el fuste y presencia de galerías e insectos). Se obtuvieron muestras compuestas de 1kg que contenían 24 submuestras, tomadas de 0 a 30cm de profundidad con una pala recta desinfectada con hipoclorito de sodio al 5% (Stock et al., 1999). Las muestras se depositaron en bolsas negras plásticas y fueron transportadas al laboratorio de Sanidad forestal del CENID-COMEF-INIFAP para su procesamiento.
Aislamiento de nematodos de suelo
Cada muestra de suelo fue tamizada con la ayuda de tamices analíticos; posteriormente se humedeció y se homogenizó (Campos-Herrera et al., 2006). Los nematodos fueron obtenidos de las muestras de suelo usando la técnica de ‘Cebo de Galleria’ (Bedding y Akhurst, 1975), para lo que se colocaron 10 cajas de Petri por muestra, depositando cuatro larvas de último instar de Galleria mellonella L. (Lepidóptera: Pyralidae). Las cajas fueron incubadas durante 15 días en una cámara bioclimática a 24 ±3°C en oscuridad (Campos-Herrera et al., 2006).
Las larvas muertas se recolectaron y se desinfestaron con hipoclorito de sodio al 1% y se colocaron individualmente en trampas White (White, 1927). Las larvas se incubaron a 25°C y fueron examinadas cada 24h por 10 días. Los juveniles infectivos que emergieron se lavaron con agua potable estéril y se colectaron en tubos de centrifuga (Campos-Herrera et al., 2006).
Identificación morfológica y morfométrica
Los nematodos aislados se deshidrataron por el método descrito por Seinhorst (1959) y fueron utilizados en el análisis morfológico y morfométrico (n=15) de machos y hembras. El análisis fue comparado con las descripciones de Herrmann et al. (2006a). Con el propósito de observar la región caudal de los machos y la presencia y disposición de las papilas genitales, los ejemplares se deshidrataron utilizando la técnica descrita por Zhao et al. (2006) para ser observados en un microscopio electrónico de barrido (JEOL JSM-6390® Tokyo, Japón).
Identificación molecular
Para la extracción del ADN de los nematodos aislados se utilizó la técnica descrita por SENASICA (2013).
La PCR se realizó en mezclas de reacción de 20µl que contenían 2µl de ADN (20ng·µl-1), 10µl SsoAdvanced ™ Universal Probes Supermix (2X) de Biorad., 6µl de agua libre de nucleasas y 1µl de cada uno de los cebadores (10nmol) SSUF07 (5’AAAGATTAAGCCATGCATG 3’) y SSUR26 (5’CATTCTTGGCAAATGCTTTCG 3’) del 18S ribosomal. Se utilizó un termociclador T100 (Biorad.) con el siguiente programa: desnaturalización inicial 95ºC por 6min, 35 ciclos con desnaturalización de 94ºC por 30s, anillamiento de 55ºC por 30s, extensión de 72ºC por 1min y una extensión final de 72ºC por 10min (Pedram, 2008). El fragmento esperado es de aproximadamente 1000 pb. Los productos de PCR se visualizaron en gel de agarosa al 1% en un fotodocumentador (Infinity-ST5 Vilber Loumat) y enviados a secuenciar a Macrogen Inc., Korea.
Las secuencias obtenidas se editaron en el programa BioEdit Sequence Alignment Editor versión 7.2.5. Dichas secuencias se compararon por alineamiento con la información disponible en la base de datos del GenBank (NCBI; National Center for Biotechnology Information), mediante el método BLAST (http://www.ncbi.nlm.nih.gov/BLAST/).
Análisis filogenético
Se descargaron de la base de nucleótidos del GenBank las secuencias de la región SSU. Se utilizó el programa MEGA7 (Tamura et al., 2011), con el que se realizó el análisis de máxima parsimonia con el método Bootstrap con 1000 repeticiones.
Pruebas de patogenicidad in vitro
Para realizar los bioensayos se colectaron descortezadores en campo, para lo cual se ubicó un área con brotes activos en el municipio Pinal de Amoles, Querétaro; se seleccionó un árbol >15cm de diámetro, con follaje verde y grumos frescos, se derribó y cortó en pequeños tocones que fueron sellados con parafina con el objetivo de mantener la humedad del material, se depositaron en bolsas negras que fueron transportadas al área de Sanidad Forestal del CENID-COMEF. Los tocones se descortezaron, se colectaron adultos maduros y se colocaron en frascos estériles. Se llevó a cabo la identificación taxonómica del 10% de la colecta total para corroborar que la especie fuera D. frontalis (Wood, 1985; Cibrián et. al, 1995).
Para el estudio de patogenicidad se realizó un diseño experimental en bloques aleatorios con dos factores de tratamientos: cepa de nematodo y tiempo. Para ello se prepararon cajas de Petri con papel filtro Whatman N° 1 y se añadieron cuatro tratamientos que consistieron en 3ml de una suspensión con 1000 JI de las cepas TMA2 (El Tejamanil), GMA6 (La Gachupina), CGA7 (Campo Santo) y un testigo (3ml de agua estéril), con tres repeticiones cada uno. Una vez humedecido el papel filtro, se colocaron en cada caja 20 adultos de D. frontalis sin síntomas de enfermedad y con alta movilidad; posteriormente se incubaron a 25 ±2°C. A las 48 y 96h se contaron y separaron los escarabajos muertos, los cuales posteriormente fueron desinfestados con hipoclorito de sodio al 1% durante 10s, se enjuagaron tres veces con agua destilada estéril y se disectaron bajo microscopio estereoscopio con el objetivo de verificar la muerte por nematodos (Fan et al., 2000). La cantidad de ejemplares muertos de cada observación fue sumada para registrar y calcular el porcentaje de mortalidad final.
Análisis estadístico
Antes de realizar el análisis de los datos se aplicó la corrección de la mortalidad con la fórmula de Abbott (1925) para cada una de las cepas de nematodos a partir de la mortalidad registrada para el testigo. Para probar el efecto del tratamiento, el tiempo y su interacción sobre la mortalidad de los descortezadores, se compararon los datos mediante un modelo lineal generalizado (GLM) con distribución quasibinomial y función logarítmica en el programa R-project. Para aquellos factores que fueron significativos estadísticamente se realizaron pruebas de Tukey (p≤0,05) con el paquete STATISTICA 7.
Resultados y Discusión
Se obtuvieron tres aislamientos de nematodos con características de entomopatógenos, a los cuales se les asigno el código de muestra TMA2, GMA6 y CGA7. Dichos aislamientos se encuentran depositados en el laboratorio de Sanidad Forestal en el Centro Nacional de Investigación Disciplinaria en Conservación y Mejoramiento de Ecosistemas Forestales del INIFAP.
Se procedió a la identificación morfológica y morfométrica de los tres aislados de nematodos entomopatógenos (TMA2, GMA6 y CGA7), arrojando las características siguientes:
Medidas
La morfometría de los tres aislados es similar (Tabla I). Para el caso de las hembras la máxima longitud del cuerpo (L) se observó en la población CGA7 con 1719,4µm, seguido de la cepa GMA6 que presentó 1608µm y el aislado TMA 1508,3µm; siendo este último el que presento menor longitud. Con respecto a la distancia del extremo anterior al poro excretor (PE), el aislado GMA6 con una distancia de 146,7µm, 144,3µm para la población CGA7, y TMA2 142,5µm (Tabla I). En relación al ancho de la cola a nivel del ano la población GMA6 presento el mayor valor con 55,9µm; 54,9μm para CGA7, y GMA6 con 54,6μm.
MORFOMETRÍA DE SEGUNDA GENERACIÓN DE LAS CEPAS
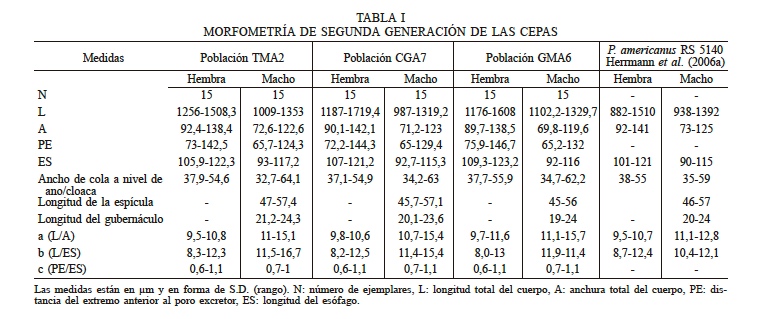
Las Las medidas están en µm y en forma de S.D. (rango). N: número de ejemplares, L: longitud total del cuerpo, A: anchura total del cuerpo, PE: distancia del extremo anterior al poro excretor, ES: longitud del esófago.
Descripción
Macho. La cutícula es anillada, con estrías longitudinales. La cabeza es ligeramente redondeada y presenta seis papilas labiales (Figura 1a). El estoma es ancho y asimétrico, en el metastoma se observa una elevación dorsal sobre la que se asienta un diente en forma de garra. El esófago presenta un procorpus cilíndrico y musculoso que ocupa dos tercios del diámetro del cuerpo, el metacorpus es muscular de forma ovoide, el istmo es alargado, estrecho y no muscular, el bulbo basal es de forma glandular, el anillo nervioso está rodeando el istmo a media región. El poro excretor se ubica en la porción media del esófago. Presenta una espícula en forma de hoz estrecha y el gubernáculo es delgado y similar en su forma a la espícula (Figura 1b). Se observan siete pares de papilas genitales distribuidas en la siguiente forma: dos pares precloacales y seis post cloacales. La cola es de forma cónica que se adelgaza progresivamente hasta terminar en forma de látigo (Figura 1c).
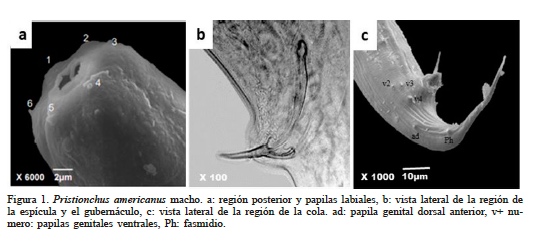
Figura 1
Pristionchus americanus macho. a: región posterior y papilas labiales, b: vista lateral de la región de la espícula y el gubernáculo, c: vista lateral de la región de la cola. ad: papila genital dorsal anterior, v+ numero: papilas genitales ventrales, Ph: fasmidio.
Hembra. El cuerpo es largo y grueso. Son similares al macho, pero son más grandes en longitud. La cutícula es delgada y finamente anillada, presentan estriación longitudinal a lo largo de todo el cuerpo. La cabeza es ligeramente redondeada, la región anterior tiene seis papilas labiales (Figura 2a), cuatro papilas cefálicas y una abertura anfidial elíptica. El estoma ancho y asimétrico, en el metastoma se asienta un diente en forma de garra. El poro excretor se ubica en la parte media del esófago (Figura 2b). Son didélficas, anfidélficas, presentan endotoquía matricida. La vulva se encuentra entre el 45-52% de la longitud total del cuerpo (Figura 2c). La cola es de forma cónica que se adelgaza progresivamente hasta terminar en forma de látigo (Figura 2d).
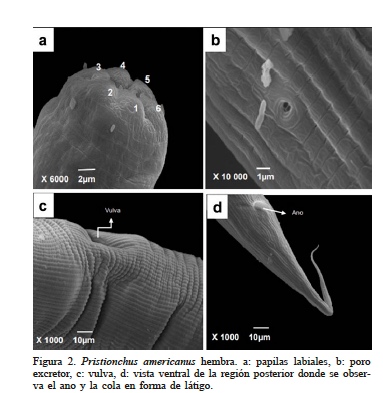
Figura 2
Pristionchus americanus hembra. a: papilas labiales, b: poro excretor, c: vulva, d: vista ventral de la región posterior donde se observa el ano y la cola en forma de látigo.
De acuerdo con los trabajos de Andrássy (1984) y Herrmann et al. (2006b) la descripción morfológica y morfométrica de los aislamientos coincide con la especie Pristionchus americanus Herrmann, 2006. Los aislamientos TMA2, CGA7 y GMA6 mostraron alta similitud morfométrica entre sí, no se presentaron variaciones representativas en el tamaño ni en la forma de las espículas y gubernáculo, ni en la presencia y disposición de papilas genitales por lo que se consideró que pertenecen a la misma especie.
Identificación molecular
Las secuencias obtenidas de la región SSU de los aislados TMA2, CGA7 y GMA6 mostraron un porcentaje de identidad del 99% con P. americanus 18S ribosomal RNA gene (número de accesión: KJ704995). Las secuencias de los aislamientos se encuentran depositados en la base de datos de nucleótidos del GenBank del National Center of Biotechnology Information con los números de accesión: TMA2 (KX382830), CGA7 (KX382831) y GMA6 (KX382832).
Análisis filogenético
El análisis filogenético basado en la región SSU (Figura 3) mostró que las secuencias se agruparon entre las especies P. americanus y P. maupasi, pero esta última fue descartada por las características morfológicas como la disposición de las papilas genitales. A además, la especie P. maupasi es un nematodo que presenta hermafroditas (Herrnann, 2006b) a diferencia de las cepas de este estudio que presentan sexos separados; por lo que se confirmó la identidad de la especie.
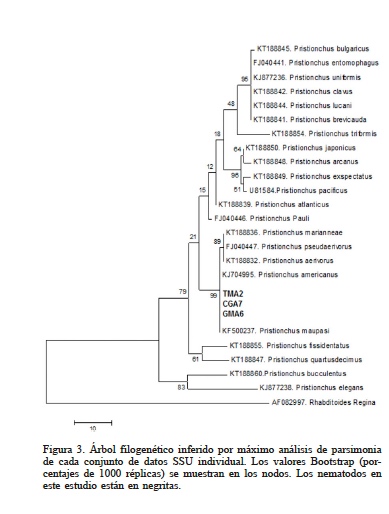
Figura 3
Árbol filogenético inferido por máximo análisis de parsimonia de cada conjunto de datos SSU individual. Los valores Bootstrap (porcentajes de 1000 réplicas) se muestran en los nodos. Los nematodos en este estudio están en negritas.
Pruebas de patogenicidad
Debido a que en el control se obtuvo un 17% de mortalidad, se realizó una corrección del porcentaje de mortalidad con la fórmula de Abbot. El análisis estadístico registró un efecto significativo del tiempo, la especie de nematodo y de la interacción tiempo × especie de nematodo sobre la mortalidad de D. frontalis (P<0,0001).
El tratamiento que obtuvo mejores resultados en cuanto a la mortalidad de descortezadores corresponde a la suspensión con 1000 JI del aislamiento TMA2 con un porcentaje de mortalidad de 92,25% a las 96 horas, mientras que las cepas CGA7 y GMA6 no presentaron diferencias significativas, con mortalidades de 76,54 y 63% respectivamente (Figura 4). Los resultados permiten ser comparados con otros medios de control biológico del descortezador, como lo reportado por Gijón-Hernández et al. (2015) en donde el aislamiento del hongo nativo Trichoderma sp. demostró una efectividad del 100% en la muerte de los insectos descortezadores a nivel de laboratorio.
El análisis estadístico indicó un efecto significativo entre la especie del nematodo y su interacción con el tiempo sobre la mortalidad de D. frontalis, con lo cual se puede observar que los aislamientos TMA2 y GMA6 presentaron diferencias significativas sobre la mortalidad a las 48 y 96h, en cambio el aislamiento CGA7 presentó similitud en ambas horas (Figura 4).
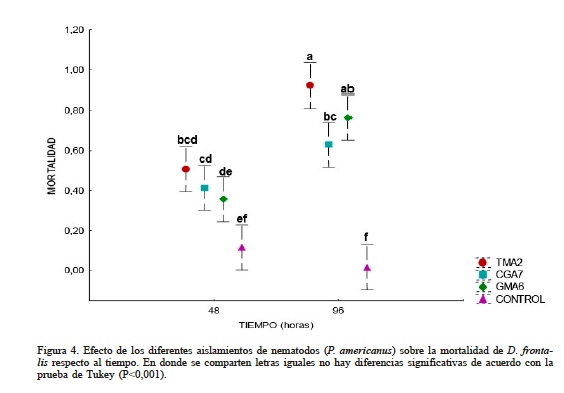
Figura 4
Efecto de los diferentes aislamientos de nematodos (P. americanus) sobre la mortalidad de D. frontalis respecto al tiempo. En donde se comparten letras iguales no hay diferencias significativas de acuerdo con la prueba de Tukey (P<0,001).
Los aislamientos GMA6, CGA7 y TMA2 pertenecen a un grupo de nematodos que presentan una interacción con otros organismos conocida como necromenica, en donde los nematodos no se alimentan activamente, sino que invaden al huésped y permanecen detenidos en etapa dauer hasta la muerte del huésped y es entonces cuando se reanuda su desarrollo dentro del cadáver (Dieterich et al., 2008). Esta característica les ha permitido vivir en estrecha asociación con los escarabajos (Ragsdale et al., 2015).
Durante el estudio de nematodos entomopatógenos realizado por Ye et al. (2015) en Carolina del Norte, EEUU, se aisló la especie Pristionchus aerivorus de larvas de G. mellonella, que murieron dentro de las primeras 48h, y donde se recuperó un alto número de nematodos cinco días más tarde. Se ha demostrado que especies pertenecientes al género Pristionchus presentan asociaciones con bacterias entomopatógenas, un ejemplo de ello es P. entomophagus del cual se aisló la bacteria Proteus vulgaris, una bacteria que es patógena en insectos (Rae et al., 2008).
El alto porcentaje de patogenicidad de los nematodos de las cepas P. americanus TMA2, CGA7 y GMA6 evaluados en este estudio sobre D. frontalis, revelan que son capaces de infectar a este insecto y que podrían estar asociadas a bacterias entomopatógenas, lo cual requiere estudios adicionales para determinar a las bacterias asociadas de estos nematodos. Este estudio es el primer reporte de P. americanus en México que se propone como potencial agente de control biológico contra D.frontalis bajo condiciones de laboratorio.
IDENTIFICACIÓN DE NEMATODOS ENTOMOPATÓGENOS CON POTENCIAL PARA EL MANEJO DE Dendroctonus frontalis (CURCULIONIDAE: SCOLYTINAE)
Abbott WS (1925) A method of computing the effectiveness of an insecticide. J. Econ. Entomol. 18: 265-267.
Andrássy I (1984) Klase Nematoda. (Ordnungen Monhysterida, Desmoscolecida, Araeolaimida, Chromadorida, Rhabditida). Fischer. Stuttgart, Alemania. 509 pp.
Bathon H (1996) Impact of entomopathogenic nematodes on non-target host. Biocontr. Sci. Technol. 6: 421- 434.
Bedding RA, Akhurst RJ (1975) A simple technique for the detection of insect parasitic rhabditids nematodes in soil. Nematologica 21: 109-110.
Campos-Herrera R, Escuer M, Labrador S, Gutiérrez C (2006) Aislamiento, identificación y caracterización ecológica de nematodos entomopatógenos de la Rioja. Zubía 23-24: 27-58.
Cibrián TD, Quiñonez FSA, Morales BJ (2014) Diagnóstico de la Situación Actual de Insectos en los Bosques Templados de México. Universidad Autónoma Chapingo. México. 313 pp.
Cibrián-Tovar D, Méndez-Montiel JT, Campos-Bolaños R, Yates OH, Flores-Lara J (1995) Insectos Forestales de México. Universidad Autónoma Chapingo, Secretaría de Agricultura y Recursos Hidráulicos, United States Departament of Agriculture, Natural Resources Canadá y Comisión Forestal de América del Norte. 455 pp.
Del-Val E, Sáenz-Romero C (2017) Insectos descortezadores (Coleóptera: Curculionidae) y cambio climático: problemática actual y perspectivas en los bosques templados. TIP Rev. Espec. Cs. Quím. Biol. 20(2): 53-60.
Díaz-Núñez V, Sánchez-Martínez G, Gillette NE (2006) Respuesta de Dendroctonus mexicanus (Hopkins) a dos isómeros ópticos de verbenona. Agrociencia 40: 349-354.
Dieterich C, Clifton SW, Schuster LN, Chinwalla A, Delehaunty K, Dinkelacker I, Fulton L, Fulton R, Godfrey J, Minx P (2008) The Pristionchus pacificus genome provides a unique perspective on nematode lifestyle and parasitism. Nature Genet. 40: 1193-1198.
DOF (2008) Norma Oficial Mexicana NOM-019-SEMARNAT-2006, que Establece los Lineamientos Técnicos de los Métodos para el Combate y Control de Insectos Descortezadores. Diario Oficial de la Federación. México.
Fan X, Maggiorani A, Gudiño S (2000) Uso de entomopatógenos como una alternativa en el control de polilla (Tecia solanivora), importante plaga de la papa (Solanum tuberosum). Mérida-Venezuela. Rev. Forest. Venez. 44: 115-118.
Gijón-Hernández AR, Trejo-Sandoval Z, López-Guzmán CM, Ramírez-Huerta L, Arriola- Padilla VJ, Pérez-Gálvez IM (2015) Caracterización y efectividad de Trichoderma spp., sobre insectos descortezadores de pino. Entomol. Mex. 2: 293-299.
Herrmann M, Mayer WE, Sommer RJ (2006a) Nematodes of the genus Pristionchus are closely associated with scarab beetles and the Colorado potato beetle in Western Europe. Zoology 109: 96-108.
Herrmann M, Mayer WE, Sommer RJ (2006b) Sex, bugs and Haldanes rule: the nematode genus Pristionchus in the United States. Front. Zool. 3: 14.
Liu J, Poinar GO (2000) Control of insect pest with entomopathogenic nematodes: the impact of molecular biology and phylogenetic reconstruction. Annu. Rev. Entomol. 45: 287-306.
Merino LM, France IA (2009) Nematodos entomopatógenos: Control biológico de insectos plaga de importancia económica. Tierra Adentro 84: 24-25.
Pedram M (2008) Longidorus kheirii n. sp. (Nematoda: Longidoridae) from Iran. Systemat. Parasitol. 71: 199-211.
Rae R, Riebesell M, Dinkelacker I, Wang Q, Herrmann M, Weller MA, Dieteric C, Sommer RJ (2008) Isolation of naturally associated bacteria of necromenic Pristionchus nematodes and fitness consequences. J. Exp. Biol. 211: 1927-1936.
Ragsdale EJ, Kanzaki N, Herrmann M (2015) Taxonomy and natural history: the genus Pristionchus. En Sommer RJ (Ed.) Pristionchus pacificus. A nematode model for comparative and evolutionary biology. Nematology Monographs and Perspectives 11. Brill. Leiden, Holanda. pp. 77-120.
Reséndiz-Martínez JF, Torres-Huerta B, López-Gómez V, Gijón-Hernández AR, Sánchez-Martínez G (2016) Enemigos naturales de Dendroctonus frontalis Zimmerman, 1868 y Dendroctonus mexicanus Hopkins, 1915 (Coleóptera: Scolytinae), capturados mediante semioquímicos en la reserva de la biosfera sierra gorda de Querétaro. Entomol. Mex. 3: 626-632.
Salinas-Moreno Y, Ager A, Vargas CF, Hayes JL, Zuñiga G (2010) Determining the vulnerability of Mexican pine forests to bark beetles of the genus Dendroctonus Erichson (Coleopter: Curculionidae: Scolytinae). Forest Ecol. Manag. 260: 52-61.
Seinhorst JW (1959) A rapid method for the transfer of nematodes from fixative to anhydrous glycerin. Nematologica 4: 67-69.
SENASICA (2013) Nematodos en Papa de Importancia Cuarentenaria en México. Protocolos de Diagnóstico. Centro Nacional de Referencia Fitosanitaria. México. 76 pp.
Stock SP, Pryory SB, Kaya HK (1999) Distribution of entomophatogenic nematodes (Steinernematidae: Heterorhabditidae) in natural hábitats in California, USA.Biodivers. Conserv. 8: 535-549.
Tamura K, Peterson D, Peterson N, Stecher G, Nei M, Kumar S (2011) MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods. Molec. Biol. Evol. 28: 2731-2739.
White GF (1927) A method for obtaining infective nematode larvae from cultures. Science 66(1709): 302-303.
Wood SL (1985) Aspectos taxonómicos de los Scolytidae. En Memoria de los Simposio Nacionales de Parasitología Forestal II y III. Publicación especial No. 46. México. pp. 170-174.
Ye W, Yu Q, Kanzaki N, Adams PR, Cardoza YJ (2015) Characterisation of, and entomopathogenic studies on, Pristionchus aerivorus (Cobb in Merrill & Ford, 1916) Chitwood, 1937 (Rhabditida: Diplogastridae) from North Carolina, USA. Nematology 17: 567-580.
Zhao Z, Davies K, Riley I, Nobbs J (2006) Laimaphelenchus australis sp. Nov. (Nematoda: Aphelenchina) from exotic pines, Pinus radiata and P. pinaster, in Australia. Zootaxa 1248: 35-44.
Notas de autor
gijonhadrianar207001@gmail.com
