Revisión
Eliminación de complejos antibiótico-metal en aguas residuales mediante métodos electroquímicos: una revisión
Removal of Antibiotic-Metal Complexes in Wastewater by Electrochemical Methods: A Review
Eliminación de complejos antibiótico-metal en aguas residuales mediante métodos electroquímicos: una revisión
TecnoLógicas, vol. 28, núm. 63, pp. 1-21, 2025
Instituto Tecnológico Metropolitano

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 06 Diciembre 2024
Aprobación: 24 Abril 2025
Publicación: 31 Mayo 2025
Resumen: La presencia de antibióticos y metales en aguas residuales provoca la modificación de genes con resistencia bacteriana (ARG). Se han encontrado concentraciones de ambas especies en decenas de µg/L en aguas residuales municipales, lo que promueve la formación de complejos antibiótico-metal, generando así compuestos más estables y peligrosos para el ecosistema que sus entes individuales. El objetivo de esta revisión fue analizar los complejos antibiótico-metal presentes en aguas residuales, sus propiedades fisicoquímicas y efectos toxicológicos, así como evaluar las técnicas electroquímicas utilizadas para su eliminación o recuperación y su integración con otros tratamientos. Para ello se realizó una revisión de la literatura existente en la temática en las principales bases de datos científicas, como Science Direct, Scopus, ACS Publications, PubMed y Web of Science, seleccionado los 111 trabajos más representativos. Los resultados mostraron que los métodos electroquímicos se presentan como una herramienta prometedora para el tratamiento eficiente de aguas contaminadas con estos complejos, ya que tienen la ventaja de lograr la degradación del antibiótico y la recuperación del metal, lo que no logran otros tratamientos convencionales. De los tratamientos revisados, se puede concluir que el método fotoelectrocatalítico resulta ser el más eficiente por mostrar altos porcentajes de degradación de los antibióticos en cortos tiempos de tratamiento. Esto se debe a la sinergia entre la acción de la luz en un ánodo semiconductor y la corriente eléctrica aplicada que provoca la generación de oxidantes fuertes.
Palabras clave: Contaminantes emergentes, degradación de medicamentos, fotoelectrocatálisis, recuperación de metales.
Abstract: The presence of antibiotics and metals in wastewater leads to alteration of antibiotic resistance genes (ARGs). Concentrations of both species have been detected in municipal wastewater in the range of tens of µg/L, promoting the formation of antibiotic–metal complexes. These complexes are more stable and hazardous to the ecosystem than their individual components. The objective of this review was to analyze antibiotic-metal complexes present in wastewater, their physicochemical properties, and toxicological effects, as well as to evaluate the electrochemical techniques used for their removal or recovery, and their integration with other treatment methods. A comprehensive literature review was conducted using major scientific databases such as Science Direct, Scopus, ACS Publications, PubMed, and Web of Science, selecting the 111 most representative studies. The results showed that electrochemical methods represent a promising tool for the efficient treatment of water contaminated with these complexes, as they offer the advantages of both antibiotic degradation and metal recovery, benefits not achieved by conventional treatments. Among the treatments reviewed, photoelectrocatalysis emerged as the most efficient method, showing high rates of antibiotic degradation within short treatment times. This efficiency is attributed to the synergy between light activation of a semiconductor anode and applied electric current, which leads to the generation of strong oxidizing agents.
Keywords: Emerging pollutants, drug degradation, photoelectrocatalysis, metal recovery.
Highlights
-
Esta revisión integra el conocimiento actual sobre el tratamiento de aguas contaminadas con complejos antibiótico-metal mediante procesos electroquímicos.
Se presentan de forma sistemática las propiedades fisicoquímicas de los antibióticos, su complejación con iones metálicos y los principios de los tratamientos electroquímicos.
Se discuten las limitaciones, perspectivas en la aplicación de procesos electroquímicos para el tratamiento de aguas.
Highlights
-
This review integrates current knowledge on the treatment of water contaminated with antibiotic-metal complexes through electrochemical processes.
The physicochemical properties of antibiotics, their complexation with metal ions, and the principles of electrochemical treatments are presented systematically.
The limitations and prospects for the application of electrochemical processes in water treatment are discussed.
1. INTRODUCCIÓN
La contaminación por residuos farmacéuticos, específicamente por antibióticos, ha generado una preocupación ambiental global debido a su capacidad para persistir en los ecosistemas y promover el desarrollo de resistencia bacteriana [1]. Muestra de ello es que se han detectado una gran variedad de antibióticos en las aguas residuales, tanto hospitalarias como domésticas. En algunos países como Australia se han encontrado 28 tipos de antibióticos diferentes en efluentes hospitalarios, plantas de tratamiento de aguas residuales, ríos y en cuencas de almacenamiento de agua potable [2], mientras que en China se identificaron 22 fármacos psiquiátricos en aguas residuales hospitalarias y en tres plantas de tratamiento de aguas municipales [3]. De igual manera, en Corea del Sur se encontraron 12 tipos de fármacos en el río Han, que se considera la fuente más importante de agua potable para los habitantes de Seúl y la provincia de Gyeonggi [4]. Por otra parte, en Costa Rica se detectaron 14 tipos de fármacos en aguas residuales agrícolas alrededor de las granjas de producción lechera, incluyendo áreas rurales y urbanas [5]. Para el caso particular de Colombia, en las principales ciudades de Bogotá y Medellín se lograron cuantificar 19 fármacos diferentes en aguas residuales, agua potable y efluentes después del tratamiento de aguas, observando la presencia de antibióticos en cada matriz [6].
Por otro lado, las aguas residuales, principalmente las industriales, contienen en su mayoría diversos metales pesados como el Cu, Ni, Cr, Cd, As, entre otros [7]. También se han encontrado metales pesados como el Cu, Cd y V en las aguas de lluvia en el norte de Colombia, en concentraciones promedio de 23.47 µgL-1, 4.72 µg/L y 11.25 µg/L, respectivamente [8]. Los metales pesados en forma iónica son tóxicos y pueden acumularse o absorberse con facilidad en los organismos vivos, trayendo consigo problemas en la salud humana [9].
Cabe destacar que la coexistencia de metales pesados con antibióticos resultantes de la centralización de aguas residuales trae como consecuencia la formación de complejos antibiótico-metal, lo que hace más complicado tratarlas debido a la estabilidad de dicho complejo. Es posible encontrar iones de metales pesados complejados en los efluentes acuosos incluso después de pasar por las diferentes etapas de las plantas de tratamiento de aguas residuales, debido a su no biodegradación y a la resistencia que tienen los metales pesados a la precipitación química convencional, que se lleva a cabo con iones OH- o S-2, o a otros tratamientos como intercambio iónico [10]. Además, la coexistencia de los antibióticos y metales pesados pueden generar un riesgo para la salud humana y el ambiente, debido a que la permanencia del complejo antibiótico-metal en el ambiente genera el desarrollo de genes con resistencia a los antibióticos (ARG) [11]. Para tratar este tipo de contaminantes se han estudiado varias tecnologías para el tratamiento de aguas residuales con contenido de complejos metálicos como adsorción [12], coprecipitación, separación por membranas, entre otras [10], [13], aunque la mayoría de estos métodos no considera la recuperación de los metales.
Por otro lado, es conocido que los métodos electroquímicos tienen como ventaja principal la posibilidad de recuperación de los metales provenientes de las aguas residuales, además de la disminución de formación de lodos, la versatilidad, la alta eficiencia energética, la facilidad de automatización y la seguridad de sus procesos [14]. Entre los métodos electroquímicos se destacan la electrocoagulación [15], y procesos electroquímicos de oxidación avanzada [16], [17], como la electrólisis [18] y fotoelectrocatálisis [19].
A la fecha, la información sobre el tratamiento por métodos electroquímicos de aguas residuales contaminadas con complejos metálicos se encuentra poco centralizada. Por este motivo, el presente artículo tuvo como objetivos (1) realizar una revisión bibliográfica sobre los complejos antibiótico-metal, describiendo qué factores intervienen en el enlace de coordinación y cómo varia su toxicidad; (2) los fundamentos de las técnicas electroquímicas usadas para la eliminación y/o recuperación de los metales pesados que forman complejos; y (3) una comparación entre los diferentes tratamientos electroquímicos utilizados para la recuperación del metal y su combinación con otras técnicas, como fotocatálisis o el uso de membranas de intercambio iónico, entre otras.
2. METODOLOGÍA
Se desarrolló una búsqueda bibliográfica de publicaciones científicas relacionadas en dos ejes fundamentales: 1) la formación de los complejos antibiótico-metal y 2) la degradación de complejos antibiótico-metal por métodos electroquímicos. Para esto, se utilizaron las bases de datos Scopus, Science Direct, American Chemical Society (ACS) y Web of Science. Los resultados de ambas búsquedas se presentan en la Tabla 1.
| No. | Ecuación de búsqueda | Scopus | Science Direct | Web of Science | ACS |
| 1 | complex AND metal AND (antibiotic OR ciprofloxacin OR tetracycline OR ofloxacin) | 4648 | 132562 | 3556 | 81 |
| 2 | complex AND metal AND (antibiotic OR ciprofloxacin OR tetracycline OR ofloxacin) AND electrochem) AND (degradation OR advanced AND oxidation AND processes) | 76 | 437 | 59 | 52 |
En el caso de la ecuación de búsqueda No 1, se realizaron filtros para limitar el número de artículos, por lo que se limitó la búsqueda al área de química y a las siguientes palabras claves: “antibiotics”, “metal complexes”, “ligands”, “metal ions”, esto con el fin de encontrar información directamente relacionada con la formación del ligando y de los factores que afectan la estabilidad del complejo formado. Una vez filtrada la información se analizaron artículos repetidos en todas las bases de datos.
3. COMPLEJOS ANTIBIÓTICO-METAL
La formación de complejos se da por la interacción de un metal catiónico con una molécula, denominada ligando, que tiene pares de electrones libres y que puede ocupar una o varias posiciones en la esfera de coordinación del catión metálico [20]. A su vez, los ligandos que se unen a los cationes metálicos a través de varios sitios de coordinación (átomos donadores de electrones) se conocen como quelantes. Los agentes complejantes o quelantes son usados ampliamente en la industria química, alimentaria y farmacéutica, entre otras [21].
Por otro lado, en diversas industrias como la galvánica, textil y química se emplea una gran variedad de metales [22], especialmente metales pesados como el Cu en la agricultura [23], Cr en los colorantes [24], Pb en baterías [25], etc. Esto provoca que en la centralización de aguas residuales estos metales se combinen con agentes complejantes o quelantes, formando compuestos mucho más estables que tienen efectos negativos en la salud y medio ambiente [26].
La concentración de los complejos antibiótico-metal en las aguas residuales está limitado por las concentraciones del fármaco, estos pueden estar entre los ng/L hasta unos pocos µg/L [27]. La co-existencia de antibióticos y metales se ha detectado en aguas residuales municipales, en el que antibióticos como la ciprofloxacina (CIP) y clortetraciclina se encuentran en concentraciones entre 0.5 µg/L y 22 µg/L en y metales como Cr, Cu, Pb se encuentran en decenas y centenas de µg/L. Por ende, la concentración de los complejos antibiótico metal se encontrarán en cantidades traza siendo este tipo de contaminante un desafío para la química analítica, el cual se encuentra aún en desarrollo [28].
3.1 Formación y estabilidad de los complejos antibiótico-metal
Los antibióticos son una clase importante de medicamentos que han sido ampliamente utilizados para tratar infecciones bacterianas, tanto en humanos como en animales [29]. El uso extensivo de estos compuestos en sectores como la ganadería, la avicultura o la medicina ha despertado preocupación ambiental, ya que su presencia ha sido identificada en distintos cuerpos de agua, incluyendo agua potable, aguas superficiales y descargas de plantas de tratamiento. Esto ha llevado a clasificarlos como contaminantes emergentes, debido a que la mayoría de las infraestructuras actuales de tratamiento de aguas no están preparadas para eliminarlos eficazmente [30]. En adición, la presencia de los antibióticos en los diversos sistemas acuáticos puede generar resistencia bacteriana [31].
Por otro lado, como se ha explicado anteriormente, debido a sus diferentes propiedades, los metales están presentes en la mayoría de las industrias, incluyendo la industria textil, agroquímica, galvanoplástica, entre otros [32]. Estos metales son tóxicos y peligrosos para el ecosistema, y debido a su amplio uso se ha evidenciado su bioacumulación en suelos, lo que tiene graves efectos negativos tanto en la flora como en la fauna y los seres humanos [32]-[34].
Debido a su naturaleza química, los antibióticos poseen átomos con pares de electrones libres, y forman complejos con diferentes metales, ya sean monovalentes o quelatos dependiendo del número de átomos enlazados con el catión metálico central [34]. Por ejemplo, las quinolonas (Q), un grupo específico de antibióticos, tienen dos grupos carboxilos que actúan como sitios de coordinación, debido a su capacidad de quelación y a su carga negativa, permite la ionización de los grupos funcionales, atrayendo al ion metálico para formar un complejo estable [35]. Además, se han registrado diferentes investigaciones acerca de la degradación del antibiótico y recuperación del metal, comprendiendo primero su interacción y demás factores que pueden afectar en la formación de dicho complejo [35], [36].
Los antibióticos tienen diferentes grupos funcionales, como ácidos carboxilos, cetonas, aminas y amidas, los cuales están asociados a su posibilidad de aceptar o donar protones dependiendo en el pH que se encuentren. Otro aspecto importante de los antibióticos es su constante de disociación ácida (pKa), ya que esta puede cambiar de acuerdo con las condiciones del pH y afectar la unión con el ion metálico [37]. Así, cuanto más alta sea la lpKa, los ligandos formarán enlaces de coordinación más estables con el metal [38]. En adición, como los metales son considerados ácidos de Lewis, se alcanzará una mayor afinidad entre el antibiótico y el metal, dando como resultado un compuesto con mayor estabilidad [39]. En la Tabla 2 se muestra un resumen de las características más importantes de algunos antibióticos, como la estructura, la solubilidad en agua y la constante de acidez. (Error 1: La referencia: Tabla 2 está ligada a un elemento que ya no existe)
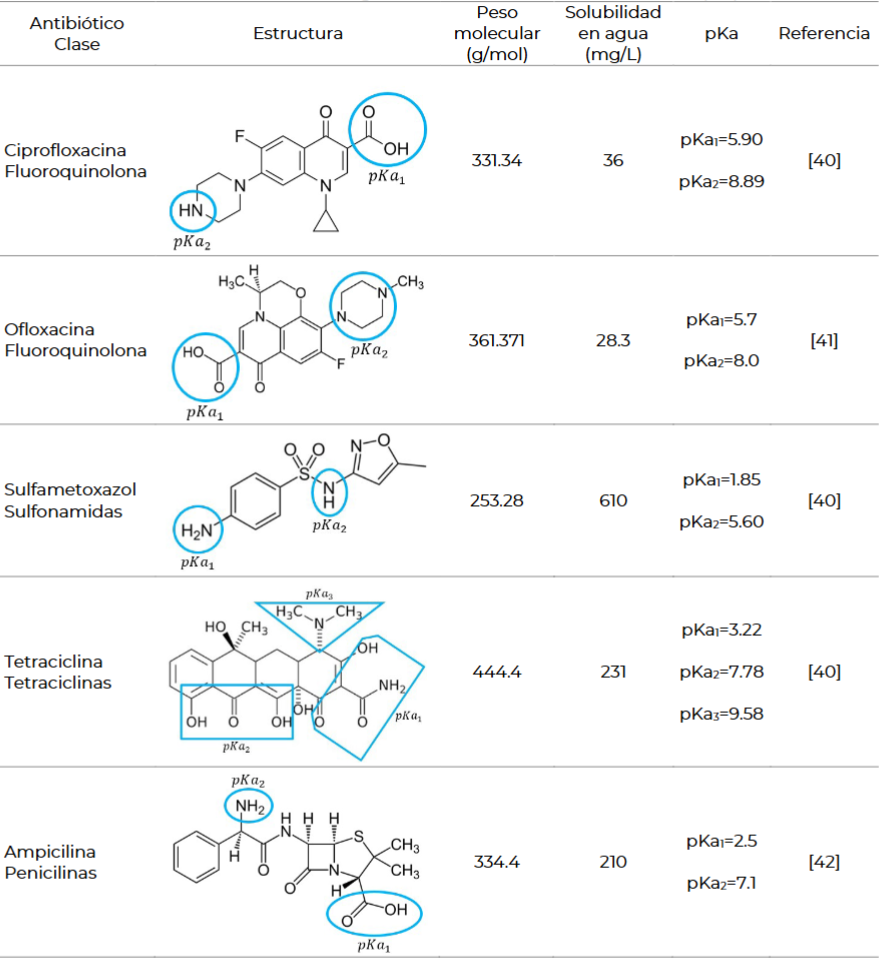
Tabla 2.
Características de algunos antibióticos
Fuente: elaboración propia.
Adicionalmente, la solubilidad del antibiótico está relacionada con la pKa, puesto que esta indica qué tan fácil se disocia un compuesto en el medio. De esta manera, cuando se tiene un pKa bajo, el antibiótico se disocia fácilmente, y tendrá una mayor solubilidad, mientras que pKa altas indican menor solubilidad del fármaco en el agua.
En términos de estabilidad de los complejos antibiótico-metal, es importante señalar que la constante de formación β (1) indica la estabilidad del complejo formado, por lo que un mayor valor de β implica mayor estabilidad del complejo.
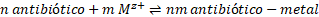 (1)
(1)donde M representa al catión metálico, z la carga del ion, n y m los coeficientes estequiométricos. En la Tabla 3 se presentan las constantes de formación de algunos complejos antibiótico-metal, algunas características importantes del metal y la relación estequiométrica de ambas especies.
| Catión metálico | Tipo metal | Número de coordinación | Radio Iónico (Å) | Antibiótico, log β y (M:antibiótico) | Referencias | |||
| CIP | OFL | NOR | LEVO | |||||
| Cobre (II) | M. Transición | 4 6 | 0.53 0.73 | 14.89 (1:1) 29.06 (1:2) | 14.21 (1:1) 26.25 (1:2) | 14.75 (1:1) 28.45 (1:2) | 13.74 (1:1) 26.25 (1:2) | [26], [43] |
| Hierro (III) | 6(hs) 6(ls) | 0.55 0.65 | 18.86 (1:1) 48.63 (1:3) | 20.32 (1:1) 48.32 (1:3) | 15.80 (1:1) 47.80 (1:3) | 18.98 (1:1) 46.92 (1:3) | ||
| Zinc (II) | 4 6 | 0.60 0.74 | 12.74 (1:1) 24.84 (1:2) | 12.90 (1:1) 25.35 (1:2) | 12.90 (1:1) 25.35 (1:2) | 12.90 (1:1) 23.87 (1:2) | ||
| Calcio (II) | M. alcalino-térreos | 6 | 1 | - | 2.3 | 2.2 | - | |
| Magnesio (II) | 6 | 0.72 | - | 2.9 | 2.9 | 11.88 | [26], [44] | |
| Bario (II) | 6 8 | 1.35 1.42 | - | 1.1 | 1.1 | 1.1 | ||
| Estroncio (II) | 6 8 | 1.18 1.26 | - | 1.1 | 1.2 | - | ||
El tipo de metal también influye en la estructura y en la estabilidad del complejo antibiótico-metal, ya que características como radió iónico, carga superficial y densidad de carga pueden afectar al complejo. Cuando un catión metálico tiene mayor densidad de carga y, por lo tanto, un radio atómico pequeño, su carga iónica es mayor, obteniéndose un complejo con mejor estabilidad [26], [45]. En cuanto a la carga iónica, se ha encontrado que las quinolonas forman quelatos más estables con ácidos de Lewis duros, como los cationes trivalentes (Al3+, Fe3+). Por ejemplo, los valores de la constante de formación para los quelatos de ciprofloxacina (CIP) disminuyen en el siguiente orden: Al3+ > Fe3+ > Cu2+ > Zn2+ > Mn2+ > Mg2+ y una tendencia parecida presentan los quelatos de norfloxacina [45]. Por otro lado, se forman quelatos menos estables con los cationes del grupo 2A (Mg2+, Ca2+, Ba2+) [46].
3.2 Efecto del pH, la temperatura y la fuerza iónica
El pH modifica la estequiometría de los complejos antibiótico-metal, esto se debe a la forma en cómo se encuentran los ligandos (antibióticos) a diferentes valores de pH. Por ejemplo, en condiciones básicas, las Q actúan como ligando en su forma desprotonada (Q−). En un medio neutro, ligeramente ácido o básico, pueden actuar en su forma zwitteriónica (QH±). En un medio fuertemente ácido, forman complejos iónicos en su forma catiónica (QH2+) [47]. En el caso específico del complejo Cu2+- CIP, a pH ácido (2.45) donde predomina la forma desprotonada de la CIP, la relación estequiométrica es 1:1, mientras que a pH más alto (5.52), donde la molécula es zwitteriónica, permite una relación estequiométrica de 1:2, es decir, el ion cobre se coordina con dos moléculas de CIP [26].
Por otra parte, en diferentes investigaciones se ha demostrado que la temperatura puede influir en la variación de la constante de formación β de los complejos. Un incremento en la temperatura disminuye dicha constante [48], [49]. Por ejemplo, cuando se analiza el efecto de la temperatura sobre los complejos de CIP con Al3+, Cu2+ y Co2+, la constante de formación disminuyó una, dos y catorce veces, respectivamente, al comprar un sistema de 18 °C y 4 °C [50].
También se evidencia que la fuerza iónica puede afectar en la formación de los complejos. Hay un aumento en su estabilidad del complejo cuando se disminuye la fuerza iónica, [51]. Es por esto que, para la mayoría de los estudios de estabilidad de complejos, se establece un valor constante de fuerza iónica de la solución.
3.3 Toxicidad de los antibióticos, metals y sus complejos
La presencia de los antibióticos en diferentes medios acuáticos ha generado una gran preocupación por sus efectos toxicológicos y la producción de ARG. Esto se puede ver reflejado en [52], donde se abarcó más de 200 tipos de antibióticos y se demostró que alrededor de un 44 % de ellos generaron toxicidad a un crustáceo de agua dulce (Daphnia magna). Además, se evidencia que los antibióticos pueden afectar el proceso de fotosíntesis en las plantas acuáticas y en la tasa de supervivencia de los embriones de pez cebra por las deformidades en el embrión, específicamente por la presencia de sulfametoxazol [53].
Por otra parte, los metales pesados son compuestos tóxicos y nocivos para la salud del ser humano (Tabla 4). Además, se reporta el límite máximo permitido de descarga según la legislación colombiana, la Agencia de Protección Ambiental (EPA, por sus siglas en inglés) de Estados Unidos y el Ministerio de Ecología y Medio Ambiente de China.
| Metal pesado | Efectos tóxicos | Límite máximo permitido en (mg/L) | |||
| Colombia [62] | EE. UU. [63] | China [64] | |||
| Cu (II) | Enfermedades hepáticas, cáncer en el tracto respiratorio, falta de sangre, irritación del estómago e intestino, enfermedad de Wilson e insomnio. | 1.00 | 0.25 | 0.5 | |
| Ni (II) | Dermatitis, náuseas, asma crónica, tos, anafilaxia, cáncer de pulmón, caída del cabello, destrucción de los glóbulos rojos, enfermedades hepáticas, y enfermedades nefrotóxicas. | 0.50 | 0.20 | 0.05 | |
| Zn (II) | Mareos, depresión, letargo, signos neurológicos como convulsiones y ataxia y aumento de la sed. | 3.00 | 1.00 | 1.0 | |
| Cr (VI) | Dolor de cabeza, náuseas, diarrea, vómitos y es cancerígeno para humanos. | 0.50 | 0.05 | 0.05 | |
| Cd (II) | Insuficiencia renal, carcinógeno humano, osteomalacia, debilidad en los huesos enfermedades respiratorias, enfermedades gastrointestinales, defectos de nacimiento, anemia, e inhibe el control del calcio en los sistemas biológicos | 0.10 | 0.01 | 0.01 | |
| Hg | Pérdida de la memoria, muerte por intoxicación, inflamación de encías, afecta las articulaciones del cuerpo humano, dolor en las extremidades, enfermedades renales, vasculares y neuronales, inconsciencia, muerte de células cutáneas en humanos, aborto, pérdida de la memoria, afecta la visión y nerviosismo. | 0.02 | 0.001 | 0.001 | |
| Pb | Teratogenicidad cerebral, enfermedades vasculares y neuronales, daña el cerebro infantil en desarrollo, insuficiencia renal, afecta los órganos de los sentidos y el sistema circulatorio y genera pérdida de la función muscular voluntaria | 0.50 | 0.01 | 0.1 | |
A su vez, los complejos antibiótico-metal en donde los ligandos se enlazan con el ion metálico donando sus electrones, puede desencadenar una serie de graves consecuencias en el ecosistema acuático permaneciendo tiempo en el ambiente por tiempos prolongados [54]. Además, estos compuestos afectan la estructura microbiana, debido a que genera así una destrucción celular, provocando así un alertamiento en el crecimiento de microbiano [55].
También se ha investigado la gran variedad de complejos antibióticos-metal, que se pueden formar en las aguas residuales, debido a la gran variedad de efectos toxicológicos diferentes, como es el ejemplo de oxitetraciclina y tetraciclina con diferentes iones metálicos como el Cu2+ y Cd2+, en donde se utilizó el mismo microrganismo y se obtuvo que cada complejo tuvo un efecto diferente en la bacteria [54].
Con base en lo anterior y al contrastar algunas investigaciones [56], [57], se ha evidenciado que la interacción del antibiótico con los iones de metales pesados, promueven la generación de ARG. Al estudiarse diferentes iones de metales (Cu, Zn, Cd, Pb, As, Mn, Cr, Ni y Fe) con varios tipos de antibióticos (sulfonamidas, macrólidos, β-lactamas, quinolonas y tetraciclinas) se observó que el sistema antibiótico-cobre obtuvo una mayor respuesta a la generación de ARG [58]. Además, en otros estudios se menciona que el Cu2+ produce una mayor transferencia en la membrana celular, permitiendo así la movilidad de elementos genéticos que causan el incremento en la generación de los ARG [59], [60]. Es por esto que se hacen necesarias las investigaciones alrededor de tratamientos de aguas con presencia de los complejos antibiótico-metal.
Es bien conocido que los métodos convencionales de tratamientos de aguas tales como absorción, filtración por membrana, entre otros, tienen la finalidad de eliminar diferentes contaminantes presentes en las aguas residuales. Sin embargo, suelen ser poco eficientes en la degradación de antibióticos [6] y esto se debe a las propiedades químicas de los fármacos anteriormente mencionados. Además, como se ha logrado ver, la unión entre antibiótico-metal aumenta la estabilidad del compuesto.
En consecuencia, la interacción de antibióticos con iones de metales pesados en aguas residuales ha mostrado efectos toxicológicos variados y la preocupación radica en su permanencia en el ambiente por tiempos prolongados, afectando la estructura microbiana y promoviendo la generación de ARG. Por lo tanto, es crucial investigar tratamientos de aguas que aborden la presencia de estos complejos. Los métodos convencionales de tratamiento de aguas son insuficientes para degradar antibióticos, lo que subraya la necesidad de alternativas viables y eficientes como los métodos electroquímicos y procesos de oxidación avanzada para la simultánea degradación del antibiótico y recuperación de los metales provenientes de los complejos [61].
4. MÉTODOS ELECTROQUÍMICOS
Los tratamientos electroquímicos son útiles para la remoción, recuperación o degradación de diferentes contaminantes, ya sean orgánicos e inorgánicos presentes en las aguas residuales de diferentes tipos de industria, por ejemplo, de industria textil [65], alimentaria [66], galvánica, entre otras. Por ello, estas técnicas electroquímicas son ampliamente usadas para el tratamiento de aguas residuales [67].
Los procesos electroquímicos se llevan a cabo en celdas, las cuales están constituidas por conductores electrónicos (electrodos) en los que ocurren reacciones de oxidación y reducción, además cuentan con un conductor iónico en solución (electrolito) [68]. En estos procesos, un contaminante puede degradarse o recuperarse mediante su oxidación o reducción en un electrodo adecuado, dentro de una celda electrolítica, gracias a la aplicación de un voltaje o a la corriente utilizada. Por lo tanto, como el potencial al que se oxida o reduce un analito depende de su naturaleza, se puede conseguir selectividad en los métodos electrolíticos si se elige adecuadamente el potencial. Estás reacciones se dan por transferencia de electrones entre la solución electrolítica y los electrodos, el cual es un proceso útil para el tratamiento de aguas residuales, donde la solución electrolítica contiene las aguas residuales a tratar [67].
Sin embargo, la eficiencia de la celda electroquímica va a depender del material de los electrodos y de los parámetros relacionados a la celda, tales como: densidad de corriente, temperatura, agitación y la composición del electrolito; es decir el pH, la concentración y tipo de contaminantes del agua residual a tratar [69].
Además, una de las ventajas de los tratamientos electroquímicos es que se utilizan los electrones, evitando así la adición de compuestos químicos en su mayoría peligrosos, ayudando a la disminución de costos y de subproductos resultantes de las reacciones entre los agentes contaminantes y los reactivos usados para tratarlos [70]. Otro aspecto importante es que cuando se realizan tratamientos convencionales a las aguas residuales, es muy común la generación de altos volúmenes de lodos. Con la aplicación de la mayoría de las técnicas electroquímicas, este problemático subproducto se ve reducido [71].
A continuación, se presentarán el principio de las técnicas electroquímicas más comunes para el tratamiento de aguas residuales de acuerdo con el tipo de contaminante.
4.1 Electrocoagulación
La electrocoagulación (ECQ) es una técnica de tratamiento alternativo usado para la depuración de aguas residuales, principalmente de efluentes provenientes de las industrias. Esta técnica se puede definir como un proceso en el cual, al aplicar una corriente eléctrica a través de dos electrodos sumergidos en la celda electrolítica, se desestabilizan las partículas de los contaminantes que se encuentran en suspensión, emulsión o en estado coloidal en las aguas residuales [72].
Para esta técnica se usa una corriente con una intensidad tal que pueda disolver los llamados ánodos de sacrificio, para los cuales comúnmente se usan el Fe o Al. Cuando el proceso inicia, en la celda se da la formación de iones de Fe2+, Fe3+ o Al3+[73], como se muestra en (2), los cationes obtenidos pueden neutralizar las cargas negativas de los iones contenidos en el efluente y además pueden formar hidróxidos del metal, debido a la presencia de los iones OH- como producto de la reacción catódica (3). Estos hidróxidos juegan un papel importante, ya que son capaces de coagular los contaminantes contenidos en las aguas residuales, los cuales forman un conglomerado (flocs) con las sustancias disueltas en las aguas contaminadas al desestabilizar las partículas suspendidas presentes [74]. Cuando ya se da este proceso, los contaminantes presentes forman compuestos hidrofóbicos que por acción de la gravedad se precipitan o por métodos de aireación flotan en la superficie del agua y luego pueden ser extraídos por técnicas de separación [75].
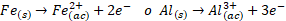 (2)
(2)
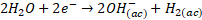 (3)
(3)El proceso de electrocoagulación presenta mayor eficiencia para remover contaminantes orgánicos y compuestos aniónicos que iones metálicos, debido a que la materia orgánica y los aniones son más susceptibles al cambio de estabilidad por la presencia de los cationes de hierro y aluminio [76].
Para el caso específico de los complejos antibiótico-metal, se evaluó la remoción del antibiótico TTC complejado con Ni2+ usando ECQ. Para este complejo se observó que la relación molar TTC-Ni tuvo influencia en los rendimientos de remoción. Una relación 1:1 tuvo una eliminación de ambos contaminantes en la solución acuosa de un 100 % en 10 min, mientras que para la relación 2:1 TTC-Ni, la eliminación fue del 90 % en 20 min Para la relación 1:2, la eliminación fue del 99.6 % en 20 min [77].
Aunque la ECQ logra altos porcentajes de remoción en tiempos relativamente cortos de proceso, tiene la desventaja de generar lodos y dado la composición de los contaminantes estudiados, dichos lodos tendrán en su composición metales pesados.
4.2 Electrólisis
El tratamiento mediante electrólisis (ECL) o también conocido como electrodeposición ha ganado interés en los últimos tiempos, sobre todo en el tratamiento de aguas residuales con presencia de metales, ya que con este método no sólo se puede remover los diferentes cationes de metales pesados presentes en los efluentes, sino que también pueden ser recuperados para darles reutilización en procesos industriales [78].
La electrólisis consiste en la aplicación de corriente eléctrica a una celda en la cual el electrolito contiene los iones de los metales pesados los cuales pueden ser reducidos y separados dependiendo de su potencial de reducción. Cuando los iones del metal logran ser separados, estos son electrodepositados en la superficie del cátodo en su estado elemental en el cual presentan una valencia de cero [77], lo que resulta en la recuperación de metales nocivos del agua residual, mientras que en el ánodo ocurren reacciones de oxidación que resultan útiles cuando las aguas residuales contienen materia orgánica o agentes complejantes los cuales pueden ser oxidados [80].
Los parámetros más influyentes en el proceso de electrólisis son la densidad de corriente que puede alterar las películas formadas en el cátodo dándole diferente morfología y microestructura [81], la temperatura que influye directamente en las propiedades del recubrimiento como en su composición y estructura, además influye en la cinética de reacción [73], y las constantes de equilibrio, dado que afecta la energía libre de Gibbs del sistema [82].
El pH juega un papel importante en el proceso de electrodeposición debido a que la velocidad de migración de los iones H+ y OH- es más rápida que cualquier otra especie iónica bajo el mismo campo eléctrico. Esto da como resultado la producción de gas de hidrógeno en el cátodo a pH bajo con el consumo de grandes cantidades de electricidad. Del mismo modo, a pH alto, el oxígeno se produce en el ánodo, lo que resulta en una baja eficiencia de corriente [83]. Por eso, un buen manejo del pH contribuye a un aumento en el porcentaje de recuperación del metal. La agitación es muy importante para homogeneizar los iones del metal a separar en la solución, ya que mejora la convección y el transporte de masa. Un aumento o disminución de la velocidad de agitación conduciría a un transporte más rápido o lento de iones desde el seno de la solución a la superficie del electrodo, lo que afecta directamente la tasa de reacción [84].
Entre los tratamientos electroquímicos, el proceso de electrólisis ha generado interés dado que aparte de remover los diferentes cationes metálicos de las aguas residuales, estos pueden ser recuperados para un posterior uso, lo que convierte este en un proceso que tiene tanto valor ambiental como económico [78]. Para el caso de metales complejados con compuestos orgánicos como Ni-amonio [85], Cu-EDTA o Ni-EDTA [86], la ECL ha sido ampliamente usada. Sin embargo, ante la emergente preocupación de los contaminantes antibiótico-metal, no se registra ningún artículo en el que se use solamente esta técnica, pues se centra en la recuperación del metal. La ECL ha resultado ser especialmente útil en combinación con otras técnicas como se presentará en el apartado 4.5.
4.3 Electrodiálisis
La técnica de electrodiálisis (ED) consiste en un proceso de separación de membranas en las que los iones de una solución se transportan a través de membranas de intercambio aniónico y catiónico, que son láminas delgadas de materiales plásticos y se les aplica un potencial eléctrico como fuerza impulsora. Las membranas están distribuidas alternadamente entre dos electrodos [87].
Las membranas pueden considerarse resinas de intercambio iónico en forma de película. Estas poseen una alta densidad de grupos iónicos ligados a ella y permiten que sea posible el transporte selectivo de iones dependiendo de la carga que estos posean. Existen dos tipos de membranas y, en ambos casos, los grupos de iones permanecen fijos a la matriz del polímero. La primera es una membrana de intercambio catiónico, la cual está constituida por grupos cargados negativamente. La segunda es una membrana de intercambio aniónico, la cual está constituida por grupos cargados positivamente [78], [79]. En las membranas se da el paso de contra-iones (de carga opuesta) de manera que se le impida el paso a lo que serían los co-iones (de misma carga) debido a la repulsión electrostática que se da entre ambos tipos de iones. El movimiento de estos iones es generado por la presencia de un campo eléctrico interpuesto por dos electrodos [88]-[90].
La ED se ha estudiado para el tratamiento del complejo entre el ion Cr y un residuo farmacéutico en cantidades traza, acetilacetona (acac), el complejo cargado positivamente Cr(acac)n(3−n)+ es tratado a través de una membrana de intercambio aniónico logrando una remoción de ambos contaminantes por encima del 97 % con la ventaja que la solución acuosa restante queda desalinizada [91].
LA ED presenta limitación en la eliminación de compuestos orgánicos neutros o no polares, además de posibles saturaciones en las membranas debido a la presencia de complejos orgánico-metálicos.
4.4 Electrocatálisis (oxidación anódica)
Este tipo de técnicas ha mostrado ser muy eficiente en cuanto al tratamiento de aguas residuales con presencia de contaminantes emergentes como los compuestos farmacéuticos y también para tratar diferentes compuestos orgánicos [64].
La oxidación anódica (EC) es la técnica más usada en los procesos electroquímicos de oxidación avanzada. Este método de tratamiento se basa en que el sistema electrolítico degrade la materia orgánica (MO). El proceso se da en dos etapas: I) transferencia directa del electrón a la superficie del ánodo (M) en donde se da oxidación heterogénea que corresponde a las ecuaciones (4) a (6); y II) formación de especies reactivas de oxígeno (ROS) en la superficie del ánodo a partir de la oxidación del agua o iones OH- presentes en el agua residual, siendo esta una oxidación homogénea representada en (7) y (8)[92].
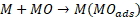 (4)
(4)
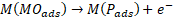 (5)
(5)
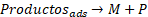 (6)
(6)
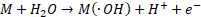 (7)
(7)
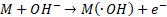 (8)
(8)La producción de ROS, específicamente del radical hidroxilo (. 0H) es muy importante para la degradación de moléculas orgánicas debido a que este presenta un potencial redox de 2.8 V, lo que significa que es un agente oxidante muy fuerte, permitiendo que tengan tendencia a reaccionar con cualquier molécula orgánica produciendo una mineralización de los contaminantes emergentes [92].
La técnica EC se ha empleado para el estudio de degradación de diferentes antibióticos, algunos de estos se presentan en la Tabla 5. La eficiencia de oxidación depende del tipo de ánodo utilizado, mostrando un mayor porcentaje de remoción los ánodos de diamante dopado con boro (BDD) y IrO2. Sin embargo, es importante resaltar que para dichos trabajos también se usaron electrolitos clorados, los cuales generan especies reactivas de cloro que también son consideradas especies oxidantes fuertes y co-ayudan a la oxidación de los medicamentos estudiados [93].
| Ánodo | Cátodo | Antibiótico o familia | % remoción de los antibióticos | Electrolito soporte | Tiempo (min) | Ref. |
| BDD | Ti | Ofloxacina | 100 | NaCl | 10 | [94] |
| PbO2/Pb | PbO2/Pb | Ofloxacina | 85 | Na2SO4 | 120 | [27] |
| Ti/SnO2-Sb | Ti | Tetraciclina | 88.8-95.8 | Na2SO4 | 40 | [95] |
| Ti/IrO2 | Zr | Fluoroquinolonas Penicilinas cefalosporinas | 100 100 90 | NaCl | 10 20 25 | [93] |
Aunque la EC ha mostrado altos porcentajes de remoción de contaminantes orgánicos, su aplicación no se ha extendido a los complejos antibiótico-metal, pues este tipo de estudios requieren abordar tanto el ánodo (oxidación del antibiótico) como el cátodo (recuperación del metal. Es por esto que la EC se desarrolla especialmente combinada con otro tipo de técnicas como se mostrará en las siguientes secciones.
4.5 Fotoelectrocatálisis
La fotoelectrocatálisis (PEC) es la combinación de dos técnicas distintas: la fotocatálisis y la electroquímica, y ha sido usada regularmente para eliminar compuestos orgánicos y metales pesados de las aguas residuales [96].
En principio, el sistema fotoelectrocatalítico promueve la oxidación de los contaminantes orgánicos presentes en aguas residuales cuando estos reaccionan en el fotoánodo, siendo estos por lo general óxidos, ya que se necesitan semiconductores para que se produzcan el par e-/h+. Sin embargo, al aplicar un potencial o corriente al sistema, este permite que no se recombinen, permitiendo así una mayor eficiencia en la degradación del contaminante, asimismo, algunos de los electrones que son fotogenerados se ven impulsados por el potencial de polarización del cátodo logrando reducir los metales pesados [97].
Por lo tanto, en PEC se tienen las reacciones de fotocatálisis, mostradas en las ecuaciones (9) a (13), y las reacciones de la electrocatálisis, correspondientes a las ecuaciones (14) a (17), donde en ambas reacciones se producirán ROS, permitiendo así una mejor degradación del antibiótico, como se observa en (18)[64].
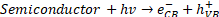 (9)
(9)
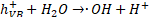 (10)
(10)
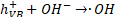 (11)
(11)
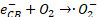 (12)
(12)
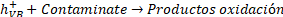 (13)
(13)
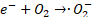 (14)
(14)
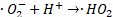 (15)
(15)
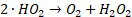 (16)
(16)
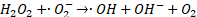 (17)
(17)
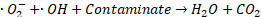 (18)
(18)Al igual que en la EC, en la PEC se presentan parámetros importantes que pueden afectar el rendimiento en la degradación de contaminantes emergentes. Uno de los más importantes es el tipo de semiconductor que se utilice, ya que este puede tener una variación en la producción de ROS [98]. Por ello, en diversas investigaciones suelen utilizar óxidos de titanio, ya que presenta un alto porcentaje de degradación por la producción ROS que genera [41].
Otro factor importante es el tipo de luz que se implemente en el sistema, ya que este va a permitir la excitación del e- para generar el salto del band gap. Por lo tanto, se ha visto que en diferentes estudios utilizan diferentes fuentes de luz. La degradación de la ofloxacina por EC a partir del complejo Cu2+- ofloxacina fue del 90.10 % en 120 min usando una fuente de luz UV 254 nm [99]. Mientras que para la degradación de CIP usando una luz led azul de 460 nm, tuvo una degradación del 80 % en 360 min [98]. Por lo tanto, un tipo de luz más energética de tipo UV genera mayor velocidad de degradación, aunque tiene un mayor impacto económico comparada con luces led o luz visible.
Además, el electrolito puede jugar un papel muy importante en la degradación de los contaminantes emergentes, ya que al utilizar NaCl en la celda fotoelectroquímica se podrán producir especies reactivas de cloro, que a su vez ayudará en la degradación del antibiótico. En algunos estudios donde se comparan electrolitos soportes como el Na2SO4 y NaCl, la degradación de la CIP resulta ser más rápida y eficiente con NaCl [100].
En la Tabla 6 se encuentran resultados de algunas investigaciones relacionadas con la simultánea degradación y recuperación de los complejos antibióticos-metales, en donde se encuentran algunas técnicas electroquímicas combinadas.
| Tratamiento | Ánodo | Cátodo | Complejo | % remoción del ligando | % recuperación del metal | Tiempo | Ref. |
| Fotoelectrocatálisis | TiO2- nanotubos | Placa de Ti | OFL-Cu | 90.1 | 76.8 | 120 min | [99] |
| Electroquímico | 54.6 | 61.8 | |||||
| Celda de combustible microbiológica | Grafito | Grafito | Cloranfenicol-Ag | 98.8 | 99.8 | 24 h | [101] |
| Fotoelectrocatálisis | Bi2S3 @CoO | Bi2S3@CoO | TTC- Cr (VI) | 91 | 92 | 180 min | [102] |
| Electrocoagulación | Al | Fe | TTC-Ni | 100 | 100 | 20 min | [77] |
| Electrocoagulación con electro-Fenton | Grafito | N-Co/Fe-PC | CIP-Cu | 96.40 TOC 83.62 | 99.69 | 120 min | [103] |
| Fotoelectrocatálisis | Bi/Bi2O3/TiO2 NTs | Placa de Ti | OTC-Cu | 96.5 | 76.1 | 5 h | [104] |
Es importante mencionar que, algunos estudios reportan el porcentaje de disminución del carbono orgánico total (TOC), para representar la eficiencia de la mineralización del antibiótico, ya que las medidas que realizan la mayoría de las investigaciones es cuantificar la degradación por medio de cromatografía líquida de alta eficacia (HPLC). Sin embargo, esta metodología no tiene en cuenta los productos intermediarios que pueden generarse en dicha degradación, mientras que el TOC tiene en cuenta la materia orgánica presente [105], por ello adquiere mayor importancia al igual que la demanda química de oxígeno (COD) [106].
Con base en la Tabla 6 se puede observar que la fotoelectrocatálisis es la técnica electroquímica más estudiada en comparación de las otras técnicas, en donde se exploran diferentes variables como variación en los electrolitos soportes con diferentes concentraciones, pH ácidos y básicos, entre otros [16], [96], [97], [102], [107], [109]. Además, Los ánodos comúnmente utilizados son de TiO2 debido a sus propiedades semiconductoras [95], aunque otros estudios exploran la oportunidad de modificar los fotoánodos, con la finalidad de producir mayor cantidad de ROS y obtener una mayor eficiencia en la degradación de los antibióticos [96].
| Tratamiento | Ánodo | Cátodo | Complejo | % remoción del ligando | % recuperación del metal | Tiempo | Ref. |
| Fotoelectrocatálisis | TiO2- nanotubos | Placa de Ti | OFL-Cu | 90.1 | 76.8 | 120 min | [99] |
| Electroquímico | 54.6 | 61.8 | |||||
| Celda de combustible microbiológica | Grafito | Grafito | Cloranfenicol-Ag | 98.8 | 99.8 | 24 h | [101] |
| Fotoelectrocatálisis | Bi2S3 @CoO | Bi2S3@CoO | TTC- Cr (VI) | 91 | 92 | 180 min | [102] |
| Electrocoagulación | Al | Fe | TTC-Ni | 100 | 100 | 20 min | [77] |
| Electrocoagulación con electro-Fenton | Grafito | N-Co/Fe-PC | CIP-Cu | 96.40 TOC 83.62 | 99.69 | 120 min | [103] |
| Fotoelectrocatálisis | Bi/Bi2O3/TiO2 NTs | Placa de Ti | OTC-Cu | 96.5 | 76.1 | 5 h | [104] |
5. RETOS Y PERSPECTIVAS
Teniendo en cuenta la versatilidad, selectividad y eficiencia de los procesos electroquímicos, este artículo hace un aporte a la síntesis y análisis de la literatura existente en tratamiento de aguas con presencia de metales pesados complejados con antibióticos. Es así como la revisión de la literatura presentada muestra una integración en el conocimiento y una descripción general de las propiedades de los antibióticos, complejación con iones metálicos, además de los principios y ejemplos. A continuación, se presentan algunas limitaciones de los diferentes métodos electroquímicos aplicados y trabajos futuros en este tema para el tratamiento de aguas.
Los métodos electroquímicos y sus combinaciones presentan algunos retos frente al tratamiento de complejos antibiótico-metal. Uno de estos retos está relacionado con el escalado de dichos procesos dado que tienen una alta dependencia a variables como el pH, potencial o corriente aplicada, fuerza iónica, concentraciones de contaminantes y electrolitos soportes en las aguas a tratar, por lo que se haría necesario un seguimiento riguroso a cada una de las variables en la planta de tratamiento.
Si bien muchos de los estudios analizados evalúan el carbono orgánico total, demanda química de oxígeno y la actividad antimicrobiana después de los tratamientos, se hacen necesarias también evaluaciones de citotoxicidad dado que los subproductos generados de procesos de oxidación avanzada pueden ser tóxicos [110].
Aunque los procesos electroquímicos presentan retos importantes para su aplicación, también presenta perspectivas como alternativas prometedoras para el tratamiento simultáneo de metales pesados complejados con antibióticos, donde pueden lograrse altos porcentajes de degradación de antibióticos y la recuperación de los metales pesados en cortos tiempos de tratamiento.
El tratamiento combinado de fotoelectrocatálisis es una estrategia prometedora dado que es un método eficaz y permite el uso de fuente de luz solar UV o visible como auxiliar para la descontaminación de aguas [111]. El desarrollo de materiales para fotoánodos es una de las mayores tendencias en este campo de estudio. Las condiciones que se buscan en estos materiales fotocatalíticos es que presenten separaciones de bandas de conducción y de valencia eficientes que eviten la recombinación de electrones, además de altas áreas superficiales para aumentar sitios activos y favorecer la adsorción y degradación de los antibióticos, sin perder sus propiedades conductoras al tratarse de procesos electroquímicos.
6. CONCLUSIONES
El tratamiento de las aguas residuales sigue siendo un campo de investigación que se encuentra en continuo crecimiento. La presencia de contaminantes emergentes representa un reto para los tratamientos de aguas existentes. La centralización de aguas residuales hospitalarias, domesticas, industriales, entre otras, permite la formación de complejos estables de antibiótico-metal, los cuales provocan la persistencia en el ambiente y la generación de ARG. La eliminación o recuperación de los metales iónicos complejados se hace difícil a través de los métodos convencionales como la precipitación.
La estabilidad y estequiometría de los complejos antibiótico-metal depende de la naturaleza química del antibiótico, la presencia de grupos funcionales con heteroátomos con pares de electrones libres favorece la complejación metálica. Dicha estabilidad depende también del ion metálico, su carga, radio iónico o densidad de carga favorece la interacción con el antibiótico.
Los métodos electroquímicos adquieren una mayor importancia en el proceso de tratamiento de aguas residuales con presencia de complejos metálicos, dado que, comparado con otras tecnologías, se puede obtener una simultánea degradación del antibiótico en el ánodo y recuperación del metal en el cátodo. Dentro de las técnicas electroquímicas, la fotoelectrocatálisis resulta comprometedora para el tratamiento de metales complejados con antibióticos y al mismo tiempo genera oportunidades de nuevas investigaciones enfocadas a la modificación de los ánodos, el efecto del pH, la densidad de corriente o voltaje, la fuente de luz y otros factores que pueden variar en el sistema.
La eficiencia de la degradación del complejo antibiótico-metal no solo depende de parámetros eléctricos como densidad de corriente, el potencial eléctrico y materiales de electrodos, sino también del electrolito, el pH, la fuerza iónica, la temperatura y en gran medida el electrolito soporte juega un rol importante en la oxidación de los antibióticos, pues se pueden formar intermediarios en el ánodo como el radical hidroxilo, el cual es un agente oxidante fuerte que promueve la mineralización del antibiótico.
Agradecimientos
Los autores agradecen el apoyo económico del Instituto Tecnológico Metropolitano de Medellín a través del proyecto con código P23205. A.F.S-M. agradece la financiación del Programa “Jóvenes Investigadores e Innovadores ITM 2024” del Instituto Tecnológico Metropolitano de Medellín.
REFERENCIAS
[1] A. Kotwani, J. Joshi, and D. Kaloni, “Pharmaceutical effluent: a critical link in the interconnected ecosystem promoting antimicrobial resistance,” Environ. Sci. Pollut. Res., vol. 28, pp. 32111–32124, Jul. 2021. https://doi.org/10.1007/s11356-021-14178-w
[2] A. J. Watkinson, E. J. Murby, D. W. Kolpin, and S. D. Costanzo, “The occurrence of antibiotics in an urban watershed: From wastewater to drinking water,” Sci. Total Environ., vol. 407, no. 8, pp. 2711–2723, Apr. 2009. https://doi.org/10.1016/j.scitotenv.2008.11.059
[3] S. Yuan, X. Jiang, X. Xia, H. Zhang, and S. Zheng, “Detection, occurrence and fate of 22 psychiatric pharmaceuticals in psychiatric hospital and municipal wastewater treatment plants in Beijing, China,” Chemosphere, vol. 90, no. 10, pp. 2520–2525, Mar. 2013. https://doi.org/10.1016/j.chemosphere.2012.10.089
[4] J. Kwon Im, M. Young Hwang, E. Hee Lee, H. Ran Noh, and S. Ju Yu, “Pharmaceutical compounds in tributaries of the Han River watershed, South Korea,” Environ. Res., vol. 188, p. 109758. Sep. 2020. https://doi.org/10.1016/j.envres.2020.109758
[5] D. Ramírez-Morales et al., “Pharmaceuticals, hazard and ecotoxicity in surface and wastewater in a tropical dairy production area in Latin America,” Chemosphere, vol. 346, p. 140443. Jan. 2024. https://doi.org/10.1016/j.chemosphere.2023.140443
[6] A. M. Botero-Coy et al., “‘An investigation into the occurrence and removal of pharmaceuticals in Colombian wastewater,” Sci. Total Environ., vol. 642, pp. 842–853, Nov. 2018. https://doi.org/10.1016/j.scitotenv.2018.06.088
[7] S. Khan, I. Ahmad, M. Tahir Shah, S. Rehman, and A. Khaliq, “Use of constructed wetland for the removal of heavy metals from industrial wastewater,” J. Environ. Manage, vol. 90, no. 11, pp. 3451–3457, Aug. 2009. https://doi.org/10.1016/j.jenvman.2009.05.026
[8] C. Doria-Argumedo, “Metales pesados (Cd, Cu, V, Pb) en agua lluvia de la zona de mayor influencia de la mina de carbón en La Guajira, Colombia,” Rev. Colomb. Quim., vol. 46, no. 2, pp. 37–44, May. 2017. https://doi.org/10.15446/rev.colomb.quim.v46n2.60533
[9] J.-G. Yu et al., “Graphene nanosheets as novel adsorbents in adsorption, preconcentration and removal of gases, organic compounds and metal ions,” Sci. Total Envirom., vol. 502, pp. 70-79, Jan. 2015. https://doi.org/10.1016/j.scitotenv.2014.08.077
[10] R.-S. Juang and S.-W. Wang, “Electrolytic recovery of binary metals and EDTA from strong complexed solutions,” Water Res., vol. 34, no. 12, pp. 3179–3185, Aug. 2000. https://doi.org/10.1016/S0043-1354(00)00061-0
[11] Q. Yan, Z. Zhong, X. Li, Z. Cao, X. Zheng, and G. Feng, “Characterization of heavy metal, antibiotic pollution, and their resistance genes in paddy with secondary municipal-treated wastewater irrigation,” Water Res., vol. 252, p. 121208, Mar. 2024. https://doi.org/10.1016/j.watres.2024.121208
[12] I. Ijaz et al., “Simultaneous adsorption of sulfamethoxazole and neodymium from wastewater by a MXene-, α-aminophosphonate-, and sulfated fucan-based ternary composite based on anion-synergistic interactions,” RSC Adv., vol. 15, no. 7, pp. 5042–5059, Feb. 2025. https://doi.org/10.1039/D4RA08766F
[13] Y. Zhu, W. Fan, T. Zhou, and X. Li, “Removal of chelated heavy metals from aqueous solution: A review of current methods and mechanisms,” Sci. Total Environ., vol. 678, pp. 253–266, Aug. 2019. https://doi.org/10.1016/j.scitotenv.2019.04.416
[14] E. Elsayed, “The Role of Electrochemistry and Electrochemical Technology in Environmental Protection, a review,” Int. J. Mater. Tech. Innov., vol. 3, no. 2, pp. 37–63, Jun. 2023. https://ijmti.journals.ekb.eg/article_304724.html
[15] W. Guan, B. Zhang, S. Tian, and X. Zhao, “The synergism between electro-Fenton and electrocoagulation process to remove Cu-EDTA,” Appl. Catal. B., vol. 227, pp. 252–257, Jul. 2018. https://doi.org/10.1016/j.apcatb.2017.12.036
[16] J. A. Byrne, B. R. Eggins, W. Byers, and N. M. D. Brown, “Photoelectrochemical cell for the combined photocatalytic oxidation of organic pollutants and the recovery of metals from waste waters,” Appl. Catal. B., vol. 20, no. 2. pp. L85-L89, Feb. 1999. https://doi.org/10.1016/S0926-3373(98)00103-9
[17] J. L. Wilkinson et al., “Pharmaceutical pollution of the world’s rivers,” Proc. Natl. Acad. Sci. U.S.A., vol. 119, no. 8, p. e2113947119, Feb. 2022. https://doi.org/10.1073/pnas.2113947119
[18] M. Li, X. Xi, Z. Nie, L. Ma, and Q. Liu, “Recovery of tungsten from WC-Co hard metal scraps using molten salts electrolysis,” J. Mater. Res. Techn., vol. 8, no. 1, pp. 1440–1450, Jan-Mar. 2019. https://doi.org/10.1016/j.jmrt.2018.10.010
[19] O. V. Nkwachukwu, C. Muzenda, B. A. Koiki, and O. A. Arotiba, “Perovskites in photoelectrocatalytic water treatment: Bismuth ferrite - graphite nanoparticles composite photoanode for the removal of ciprofloxacin in water,” J. Photochem. Photobiol. A Chem., vol. 434, p. 114275. Jan. 2023. https://doi.org/10.1016/j.jphotochem.2022.114275
[20] A. Mattheew Wilson, P. J. Bailey, P. A. Tasker, J. R. Turkington, R. A. Grant, and J. B. Love, “Solvent extraction: The coordination chemistry behind extractive metallurgy,” Chem. Soc. Rev., vol. 43, no. 1, pp. 123-134, Oct. 2013. https://doi.org/10.1039/C3CS60275C
[21] D. Kołodyńska, “Complexing Agents,” in Kirk-Othmer Encyclopedia of Chemical Technology. Hoboken, New Jersey, USA: Wiley, 2019, pp. 1–26. https://doi.org/10.1002/0471238961.0308051208152301.a01.pub3
[22] A. A. Azmi, J. Jai, N. A. Zamanhuri, and A. Yahya, “Precious Metals Recovery from Electroplating Wastewater: A Review,” in IOP Conf. Ser.: Mater. Sci. Eng., vol. 358, 3rd Int. Conf. Glob. Sustain. Chem. Eng. (ICGSCE), Bristol, Eng: Institute of Physics Publishing, 2018, p. 012024. https://iopscience.iop.org/article/10.1088/1757-899X/358/1/012024
[23] F. C. Coelho et al., “Agricultural use of copper and its link to Alzheimer’s disease,” Biomolecules, vol. 10, no. 6, p. 897, Jun. 2020. https://doi.org/10.3390/biom10060897
[24] E. Kyung Choe, Y.-Z. Kim, Y. Dal Cho, and S. Hwan Son, “Study on analytical scheme for human ecological quality control of chromium-complex acid dyes,” Text. Res. J., vol. 86, no. 17, pp. 1847–1858, Nov. 2015. https://doi.org/10.1177/004051751561742
[25] P. Bača, and P. Vanýsek, “Issues Concerning Manufacture and Recycling of Lead,” Energies (Basel), vol. 16, no. 11, p. 4468, Jun. 2023. https://doi.org/10.3390/en16114468
[26] P. Khurana, R. Pulicharla, and S. Kaur Brar, “Antibiotic-metal complexes in wastewaters: fate and treatment trajectory,” Environ. Int., vol. 157, p. 106863, Dec. 2021. https://doi.org/10.1016/j.envint.2021.106863
[27] S. Sharan, P. Khare, and R. Shankar, “Electrochemical degradation of ofloxacin using PbO2/Pb-based lead acid battery electrode: Parametric optimization and kinetics study,” Mater. Today Proc., vol. 78, part 1, pp. 128–137, 2023. https://doi.org/10.1016/j.matpr.2022.12.195
[28] P. Khurana, R. Pulicharla, and S. Kaur Brar, “Analytical challenges of antibiotic-metal complexes in wastewaters: A mini-review,” Environ. Nanotechnol. Monit. Manag., vol. 18, p. 100747, Dec. 2022. https://doi.org/10.1016/j.enmm.2022.100747
[29] J. Lu, J. Wu, C. Zhang, Y. Zhang, Y. Lin, and Y. Luo, “Occurrence, distribution, and ecological-health risks of selected antibiotics in coastal waters along the coastline of China,” Sci. Total Environ., vol. 644, pp. 1469–1476, Dec. 2018. https://doi.org/10.1016/j.scitotenv.2018.07.096
[30] X. Liu, S. Lu, W. Guo, B. Xi, and W. Wang, “Antibiotics in the aquatic environments: A review of lakes, China,” Sci. Total Environ., vol. 627, pp. 1195-1208, Jun. 2018. https://doi.org/10.1016/j.scitotenv.2018.01.271
[31] R. E. Fernández Rodríguez, H. Bolívar Anillo, C. Hoyos Turcios, L. Carrillo García, M. Serrano Hernández, and E. Abdellah, “Antibiotic resistance: the role of man, animals and the environment,” Salud Uninorte, vol. 36, no. 1, pp. 298–324, Jan-Apr. 2020. http://dx.doi.org/10.14482/sun.36.1.615
[32] K.-J. Appenroth, “Definition of ‘Heavy Metals’ and Their Role in Biological Systems,” in Soil Biology, Berlin, Heidelberg: Springer Berlin Heidelberg, 2010, pp. 19–29. https://doi.org/10.1007/978-3-642-02436-8_2
[33] H. Ali, and E. Khan, “Trophic transfer, bioaccumulation, and biomagnification of non-essential hazardous heavy metals and metalloids in food chains/webs—Concepts and implications for wildlife and human health,” Human and Ecogical Risk Assessment: An International Journal, vol. 25, no. 6, pp. 1353–1376, Aug. 2019. https://doi.org/10.1080/10807039.2018.1469398
[34] M. Kumar, K. Kaur Sodhi, P. Singh, P. Kumar Agrawal, and D. Kumar Singh, “Synthesis and characterization of antibiotic-metal complexes [FeCl3(L1)2H2O and Ni(NO3)2(L2)2H2O] and enhanced antibacterial activity,” Environ. Nanotechnol. Monit. Manag., vol. 11, p. 100209, May 2019. https://doi.org/10.1016/j.enmm.2019.100209
[35] G. Psomas, and D. P. Kessissoglou, “Quinolones and non-steroidal anti-inflammatory drugs interacting with copper(ii), nickel(ii), cobalt(ii) and zinc(ii): Structural features, biological evaluation and perspectives,” Dalton Trans., vol. 42, no. 18, pp. 6252-6276, Feb. 2013. https://doi.org/10.1039/C3DT50268F
[36] R. Puicharla, D. P. Mohapatra, S. K. Brar, P. Drogui, S. Auger, and R. Y. Surampalli, “A persistent antibiotic partitioning and co-relation with metals in wastewater treatment plant - Chlortetracycline,” J. Environ. Chem. Eng., vol. 2, no. 3, pp. 1596–1603, Sep. 2014. https://doi.org/10.1016/j.jece.2014.06.001
[37] Q. Wang, X. He, H. Xiong, Y. Chen, and L. Huang, “Structure, mechanism, and toxicity in antibiotics metal complexation: Recent advances and perspectives,” Sci. Total. Environ., vol. 848, p. 157778, Nov. 2022. https://doi.org/10.1016/j.scitotenv.2022.157778
[38] P. Lu, Y. Wu, H. Kang, H. Wei, H. Liu, and M. Fang, “What can pKaand NBO charges of the ligands tell us about the water and thermal stability of metal organic frameworks?,” J. Mater. Chem. A, vol. 2, no. 38, pp. 16250–16267, Aug. 2014. https://doi.org/10.1039/C4TA03154G
[39] B. P. Hay, A. Chagnes, and G. Cote, “On the Metal Ion Selectivity of Oxoacid Extractants,” Solvent Extr. Ion Exch., vol. 31, no. 1, pp. 95–105, Dec. 2012. https://doi.org/10.1080/07366299.2012.709452
[40] Z. Qiang, and C. Adams, “Potentiometric determination of acid dissociation constants (pK a) for human and veterinary antibiotics,” Water Res., vol. 38, no. 12, pp. 2874–2890, Jul. 2004. https://doi.org/10.1016/j.watres.2004.03.017
[41] R. Li, S. E. Williams, Q. Li, J. Zhang, C. Yang, and A. Zhou, “Photoelectrocatalytic Degradation of Ofloxacin Using Highly Ordered TiO2 Nanotube Arrays,” Electrocatalysis, vol. 5, no. 4, pp. 379–386, Oct. 2014. https://doi.org/10.1007/s12678-014-0204-3
[42] J. W. Peterson, L. J. Petrasky, M. D. Seymour, and R. S. Bergmans, “Laboratory Investigation of Antibiotic Interactions with Fe2O3 Nanoparticles in Water,” J. Environ. Engin., vol. 142, no. 5, Jan. 2016. https://doi.org/10.1061/(ASCE)EE.1943-7870.0001090
[43] A. Cuprys, R. Pulicharla, S. Kaur Brar, P. Drogui, M. Verma, and R. Y. Surampalli, “Fluoroquinolones metal complexation and its environmental impacts,” Coord. Chem. Rev., vol. 376, pp. 46-61, Dec. 2018. https://doi.org/10.1016/j.ccr.2018.05.019
[44] H. R. Park, G. Y. Jeong, H. C. Lee, J. G. Lee, and G. M. Baek, “Ionization and Divalent Cation Complexation of Quinolone Antibiotics in Aqueous Solution,” Bull. Korean Chem. Soc., vol. 21, no. 9, pp. 849-854, Sep. 2000. https://koreascience.kr/article/JAKO200013464477305.page
[45] V. Uivarosi, “Metal complexes of quinolone antibiotics and their applications: An update,” Molec., vol. 18, no. 9, pp. 11153-11197, Sep. 2013. https://doi.org/10.3390/molecules180911153
[46] I. Turel, N. Bukovec, and E. Farkas, “Complex formation between some metals and a quinolone family member (ciprofloxacin),” Polyhedron, vol. 15, no. 2, pp. 269–275, Jan. 1996. https://doi.org/10.1016/0277-5387(95)00231-G
[47] K. Siddappa, S. B. Mane, and D. Manikprabhu, “Spectral characterization and 3D molecular modeling studies of metal complexes involving the O, N-donor environment of quinazoline-4(3H)-one Schiff base and their biological studies,” Sci. World J., p. 817365, Feb. 2014. https://doi.org/10.1155/2014/817365
[48] A. T. Abdelkarim, W. H. Mahmoud, and A. A. El-Sherif, “Potentiometric, thermodynamics and coordination properties for binary and mixed ligand complexes of copper (II) with cephradine antibiotic and some N- and O-bound amino acids (α-alanine and β-alanine),” J. Mol. Liq., vol. 328, p. 115334. Apr. 2021. https://doi.org/10.1016/j.molliq.2021.115334
[49] H. Kaur, J. K. Puri, and A. Singla, “Metal ion interactions with drugs: Electrochemical study of complexation of various bivalent metal ions with nimesulide and ibuprofen,” J. Mol. Liq., vol. 182, pp. 39–42, Jun. 2013. https://doi.org/10.1016/j.molliq.2013.03.005
[50] A. Cuprys, R. Pulicharla, J. Lecka, S. K. Brar, P. Drogui, and R. Y. Surampalli, “Ciprofloxacin-metal complexes –stability and toxicity tests in the presence of humic substances,” Chemosphere, vol. 202, pp. 549–559, Jul. 2018. https://doi.org/10.1016/j.chemosphere.2018.03.117
[51] S. Rakshit, D. Sarkar, E. J. Elzinga, P. Punamiya, and R. Datta, “Surface Complexation of Oxytetracycline by Magnetite: Effect of Solution Properties,” Vadose Zone Journal, vol. 13, no. 2, pp. 1–10, Feb. 2014. https://doi.org/10.2136/vzj2013.08.0147
[52] L. Zhu, X. Lin, Z. Di, F. Cheng, and J. Xu, “Occurrence, Risks, and Removal Methods of Antibiotics in Urban Wastewater Treatment Systems: A Review,” Water, vol. 16, no. 23, p. 3428, Nov. 2024. https://doi.org/10.3390/w16233428
[53] N. Iftikhar et al., “Sulfamethoxazole (SMX) Alters Immune and Apoptotic Endpoints in Developing Zebrafish (Danio rerio),” Toxics, vol. 11, no. 2, p. 178, Feb. 2023. https://doi.org/10.3390/toxics11020178
[54] J. Hao, X. Wang, Y. Wang, Y. Wu, and F. Guo, “Optimizing the Leaching Parameters and Studying the Kinetics of Copper Recovery from Waste Printed Circuit Boards,” ACS Omega, vol. 7, no. 4, pp. 3689–3699, Jan. 2022. https://doi.org/10.1021/acsomega.1c06173
[55] H. Guo, S. Xue, M. Nasir, J. Gu, and J. Lv, “Impacts of cadmium addition on the alteration of microbial community and transport of antibiotic resistance genes in oxytetracycline contaminated soil,” J. Environ. Sci., vol. 99, pp. 51–58, Jan. 2021. https://doi.org/10.1016/j.jes.2020.04.015
[56] A. A. Roberto, J. B. Van Gray, J. Engohang-Ndong, and L. G. Leff, “Distribution and co-occurrence of antibiotic and metal resistance genes in biofilms of an anthropogenically impacted stream,” Sci. Total Environ., vol. 688, pp. 437–449, Oct. 2019. https://doi.org/10.1016/j.scitotenv.2019.06.053
[57] J. C. Thomas et al., “Co-occurrence of antibiotic, biocide, and heavy metal resistance genes in bacteria from metal and radionuclide contaminated soils at the Savannah River Site,” Microb. Biotechnol., vol. 13, no. 4, pp. 1179–1200, Jul. 2020. https://doi.org/10.1111/1751-7915.13578
[58] J. Hao, X. Wang, Y. Wang, F. Guo, and Y. Wu, “Study of gold leaching from pre-treated waste printed circuit boards by thiosulfate‑cobalt-glycine system and separation by solvent extraction,” Hydrometallurgy, vol. 221, p. 106141, Aug. 2023. https://doi.org/10.1016/j.hydromet.2023.106141
[59] N. Li, J. Chen, C. Liu, J. Yang, C. Zhu, and H. Li, “Cu and Zn exert a greater influence on antibiotic resistance and its transfer than doxycycline in agricultural soils,” J. Hazardous Mater., vol. 423, no. Part. B, p. 127042, Feb. 2022. https://doi.org/10.1016/j.jhazmat.2021.127042
[60] X. Wang, B. Lan, H. Fei, S. Wang, and G. Zhu, “Heavy metal could drive co-selection of antibiotic resistance in terrestrial subsurface soils,” J. Hazardous Mater., vol. 411, p. 124848, Jun. 2021. https://doi.org/10.1016/j.jhazmat.2020.124848
[61] I. Lozano, C. J. Pérez-Guzmán, A. Mora, J. Mahlknecht, C. López Aguilar, and P. Cervantes-Avilés, “Pharmaceuticals and personal care products in water streams: Occurrence, detection, and removal by electrochemical advanced oxidation processes,” Sci. Total Environ., vol. 821, p. 154348, Jun. 2022. https://doi.org/10.1016/j.scitotenv.2022.154348
[62] Ministerio de Ambiente y Desarrollo Sostenible, “Resolución 0631 de 2015,” 17 Mar. 2015. https://www.minambiente.gov.co/wp-content/uploads/2021/11/resolucion-631-de-2015.pdf
[63] T. Austiono Kurniawan, G. Y. S. Chan, W.-H. Lo, and S. Babel, “Physico-chemical treatment techniques for wastewater laden with heavy metals,” Chem. Eng. J., vol. 118, no. 1–2, pp. 83–98, May. 2006. https://doi.org/10.1016/j.cej.2006.01.015
[64] Y. Zhou et al., “Determining discharge characteristics and limits of heavy metals and metalloids for wastewater treatment plants (WWTPs) in China based on statistical methods,” Water (Switz.), vol. 10, no. 9, p. 1248, Sep. 2018. https://doi.org/10.3390/w10091248
[65] P. Kaur, J. Prakash Kushwaha, and V. Kumar Sangal, “Electrocatalytic oxidative treatment of real textile wastewater in continuous reactor: Degradation pathway and disposability study,” J. Hazardous Mater., vol. 346, pp. 242–252, Mar. 2018. https://doi.org/10.1016/j.jhazmat.2017.12.044
[66] J. Pinedo-Hernández, Y. Núñez, I. Sánchez, and J. Marrugo-Negrete, “Treatment of meat industry wastewater using electrochemical treatment method,” Port. Electrochim. Acta, vol. 33, no. 4, pp. 223–230, Nov. 2015. https://doi.org/10.4152/pea.201504223
[67] N. B. Singh, and A. B. H. Susan, “Polymer nanocomposites for water treatments,” in Polymer-based Nanocomposites for Energy and Environmental Applications: A volume in Woodhead Publishing Series in Composites Science and Engineering, M. Jawaid, and M. Mansoob Khan, Eds., Ottawa, Canadá: University of Ottawa Press-Woodhead Publishing, 2018, pp. 569–595. https://doi.org/10.1016/B978-0-08-102262-7.00021-0
[68] A. J. Bard, and L. R. Faulkner, Electrochemical Methods, Fundamentals and Applications, Hoboken, New Jersey, USA: Wiley, 1983. https://www.wiley.com/en-us/Electrochemical+Methods%3A+Fundamentals+and+Applications%2C+2nd+Edition-p-9780471043720
[69] H. M. Zelada Romero, and C. Vásquez, “Evaluation of the Efficiency of an Electrocoagulation Cell for the Treatment of Wastewater coming from the Textile Industry,” in Proc. LACCEI Int. Multi-conference Engin., Educ. Techn., Boca Raton, FL, USA, 2023. https://doi.org/10.18687/LACCEI2023.1.1.1530
[70] Y. Feng, L. Yang, J. Liu, and B. E. Logan, “Electrochemical technologies for wastewater treatment and resource reclamation,” Environ. Sci. Water Res. Technol., vol. 2, no. 5, pp. 800-831, May. 2016. https://doi.org/10.1039/C5EW00289C
[71] J. Rumky, A. Deb, M. Joon Shim, E. Laakso, and E. Repo, “A review on the recent advances in electrochemical treatment technologies for sludge dewatering and alternative uses,” J. Hazardous Mater., vol. 11, p. 100341, Aug. 2023. https://doi.org/10.1016/j.hazadv.2023.100341
[72] A. Shahedi, A. K. Darban, F. Taghipour, and A. Jamshidi-Zanjani, “A review on industrial wastewater treatment via electrocoagulation processes,” Curr. Opin. Electrochem., vol. 22, pp. 154-169, Aug. 2020. https://doi.org/10.1016/j.coelec.2020.05.009
[73] C. Femina Carolin, P. Senthil Kumar, A. Saravanan, G. Janet Joshiba, and M. Naushad, “Efficient techniques for the removal of toxic heavy metals from aquatic environment: A review,” J. Environ. Chem. Engin., vol. 5, no. 3, pp. 2782-2799, Jun. 2017. https://doi.org/10.1016/j.jece.2017.05.029
[74] C. A. Martínez-Huitle, and E. Brillas, “Decontamination of wastewaters containing synthetic organic dyes by electrochemical methods: A general review,” Appl. Catal. B: Environ., vol. 87, no. 3-4., pp. 105-145, Apr. 2009. https://doi.org/10.1016/j.apcatb.2008.09.017
[75] N. Yasri, J. Hu, M. G. Kibria, and E. P. L. Roberts, “Electrocoagulation Separation Processes,” in Multidisciplinary Advances in Efficient Separation Processes, I. Chernyshova, S. Ponnurangam, and Q. Liu, Eds., Washington, USA: American Chemical Society, 2020, pp. 167–203. https://pubs.acs.org/doi/abs/10.1021/bk-2020-1348.ch006
[76] D. Sharma, P. Kumar Chaudhari, S. Dubey, and A. Kumar Prajapati, “Electrocoagulation Treatment of Electroplating Wastewater: A Review,” J. Environ. Engin., vol. 146, no. 10, Jul. 2020. https://doi.org/10.1061/(ASCE)EE.1943-7870.0001790
[77] A. Adeyemi Oladipo, F. Suleiman Mustafa, O. Nestor Ezugwu, and M. Gazi, “Efficient removal of antibiotic in single and binary mixture of nickel by electrocoagulation process: Hydrogen generation and cost analysis,” Chemosphere, vol. 300, p. 134532, Aug. 2022. https://doi.org/10.1016/j.chemosphere.2022.134532
[78] L. Yang et al., “Electrochemical recovery and high value-added reutilization of heavy metal ions from wastewater: Recent advances and future trends,” Environ. Int., vol. 152, p. 106512, Jul. 2021. https://doi.org/10.1016/j.envint.2021.106512
[79] F. Fu, and Q. Wang, “Removal of heavy metal ions from wastewaters: A review,” J. Environ. Manage., vol. 92, no. 3, pp. 407-418, Mar. 2011. https://doi.org/10.1016/j.jenvman.2010.11.011
[80] Y. Zhu, W. Fan, T. Zhou, and X. Li, “Removal of chelated heavy metals from aqueous solution: A review of current methods and mechanisms,” Sci. Total Environ., vol. 678, pp. 253-266, Aug. 2019. https://doi.org/10.1016/j.scitotenv.2019.04.416
[81] W. Wang, and K. Sun, “Influence of current density on the microstructure of carbon-based cathode materials during aluminum electrolysis,” Appl. Sci. (Switz.), vol. 10, no. 7, p. 2228, Apr. 2020. https://doi.org/10.3390/app10072228
[82] O. V. Ogechi, and O. A. Ikejiofor, “A Review of the Essence of Stability Constants in the Thermodynamic Assessments of Chemical Compounds,” International Journal of Anesthesiology and Practice, vol. 1, no. 1, Dec. 2022. https://doi.org/10.58489/2994-2624/002
[83] J.-H. Chang, A. V. Ellis, C.-T. Yan, and C.-H. Tung, “The electrochemical phenomena and kinetics of EDTA-copper wastewater reclamation by electrodeposition and ultrasound,” Sep. Purif. Technol., vol. 68, no. 2, pp. 216–221, Aug. 2009. https://doi.org/10.1016/j.seppur.2009.05.014
[84] H. I. Maarof, W. M. A. Wan Daud, and M. Kheireddine Aroua, “Recent trends in removal and recovery of heavy metals from wastewater by electrochemical technologies,” Rev. Chem. Engin., vol. 33, no. 4, pp. 359–386, 2017. https://doi.org/10.1515/revce-2016-0021
[85] W. Guan, S. Tian, D. Cao, Y. Chen, and X. Zhao, “Electrooxidation of nickel-ammonia complexes and simultaneous electrodeposition recovery of nickel from practical nickel-electroplating rinse wastewater,” Electrochim. Acta, vol. 246, pp. 1230–1236, Aug. 2017. https://doi.org/10.1016/j.electacta.2017.06.121
[86] L. Wu, S. Garg, J. Xie, C. Zhang, Y. Wang, and T. David Waite, “Electrochemical Removal of Metal-Organic Complexes in Metal Plating Wastewater: A Comparative Study of Cu-EDTA and Ni-EDTA Removal Mechanisms,” Environ. Sci. Technol., vol. 57, no. 33, pp. 12476–12488, Aug. 2023. https://doi.org/10.1021/acs.est.3c02550
[87] M. del M. Cerrillo-Gonzalez, M. Villen-Guzman, J. M. Rodriguez-Maroto, and J. M. Paz-Garcia, “Metal Recovery from Wastewater Using Electrodialysis Separation,” Metals, vol. 14, no. 1, p. 38, Dec. 2024. https://doi.org/10.3390/met14010038
[88] N. Pismenskaya et al., “A review on ion-exchange membranes fouling during electrodialysis process in food industry, part 2: Influence on transport properties and electrochemical characteristics, cleaning and its consequences,” Membranes (Basel), vol. 11, no. 11, p. 811, Oct. 2021. https://doi.org/10.3390/membranes11110811
[89] H. Strathmann, “Electrodialysis, a mature technology with a multitude of new applications,” Desalination, vol. 264, no. 3, pp. 268–288, Dec. 2010. https://doi.org/10.1016/j.desal.2010.04.069
[90] L. Gurreri, A. Tamburini, A. Cipollina, and G. Micale, “Electrodialysis applications in wastewater treatment for environmental protection and resources recovery: A systematic review on progress and perspectives,” Membranes, vol. 10, no. 7, p. 146, Jul. 2020. https://doi.org/10.3390/membranes10070146
[91] C. Jiang et al., “Complexation Electrodialysis as a general method to simultaneously treat wastewaters with metal and organic matter,” Chem. Engin. J., vol. 348, pp. 952–959, Sep. 2018. https://doi.org/10.1016/j.cej.2018.05.022
[92] S. Oladejo Ganiyu, C. A. Martínez-Huitle, and M. A. Oturan, “Electrochemical advanced oxidation processes for wastewater treatment: Advances in formation and detection of reactive species and mechanisms,” Curr. Opin. Electrochem., vol. 27, p. 100678, Jun. 2021. https://doi.org/10.1016/j.coelec.2020.100678
[93] E. A. Serna-Galvis, K. E. Berrio-Perlaza, and R. A. Torres-Palma, “Electrochemical treatment of penicillin, cephalosporin, and fluoroquinolone antibiotics via active chlorine: evaluation of antimicrobial activity, toxicity, matrix, and their correlation with the degradation pathways,” Environ. Sci. Pollut. Res., vol. 24, no. 30, pp. 23771–23782, Oct. 2017. https://doi.org/10.1007/s11356-017-9985-2
[94] H. Ren et al., “Removal of ofloxacin from wastewater by chloride electrolyte electro-oxidation: Analysis of the role of active chlorine and operating costs,” Sci. Total Environ., vol. 850, p. 157963, Dec. 2022. https://doi.org/10.1016/j.scitotenv.2022.157963
[95] D. Zhi, J. Qin, H. Zhou, J. Wang, and S. Yang, “Removal of tetracycline by electrochemical oxidation using a Ti/SnO2–Sb anode: characterization, kinetics, and degradation pathway,” J. Appl. Electrochem., vol. 47, no. 12, pp. 1313–1322. Dec. 2017. https://doi.org/10.1007/s10800-017-1125-7
[96] M. Hosseini, H. Rasoulzadeh, H. Akbari, H. Akbari, and A. Adibzadeh, “Photo-electrocatalytic degradation of remdesivir from aqueous solutions using Ni-doped ZnO nanocomposite: Kinetic, degradation pathway, toxicity reduction and reusability,” J. Photochem. Photobiol. A. Chem., vol. 450, p. 115416, May 2024. https://doi.org/10.1016/j.jphotochem.2023.115416
[97] S. Ye, Y. Chen, X. Yao, and J. Zhang, “Simultaneous removal of organic pollutants and heavy metals in wastewater by photoelectrocatalysis: A review,” Chemosphere, vol. 273, p. 128503, Jun. 2021. https://doi.org/10.1016/j.chemosphere.2020.128503
[98] K. Changanaqui, E. Brillas, P. L. Cabot, H. Alarcón, and I. Sirés, “Complete abatement of the antibiotic ciprofloxacin from water using a visible-light-active nanostructured photoanode,” Chemosphere, vol. 352, p. 141396, Mar. 2024. https://doi.org/10.1016/j.chemosphere.2024.141396
[99] L. Liu, R. Li, Y. Liu, and J. Zhang, “Simultaneous degradation of ofloxacin and recovery of Cu(II) by photoelectrocatalysis with highly ordered TiO2 nanotubes,” J. Hazardous Mater., vol. 308, pp. 264–275, May. 2016. https://doi.org/10.1016/j.jhazmat.2016.01.046
[100] H. He et al., “Photoelectrocatalytic coupling system synergistically removal of antibiotics and antibiotic-resistant bacteria from aquatic environment,” J. Hazardous Mater., vol. 424, no. part C, p. 127553, Feb. 2022. https://doi.org/10.1016/j.jhazmat.2021.127553
[101] D. Wu, D. Lu, F. Sun, and Y. Zhou, “Process optimization for simultaneous antibiotic removal and precious metal recovery in an energy neutral process,” Sci. Total Environ., vol. 695, p. 133914, Dec. 2019. https://doi.org/10.1016/j.scitotenv.2019.133914
[102] L. Yang, Y. Hu, and L. Zhang, “Architecting Z-scheme Bi2S3@CoO with 3D chrysanthemums-like architecture for both photoeletro-oxidization and -reduction performance under visible light,” Chem. Engin. J., vol. 378, p. 122092, Dec. 2019. https://doi.org/10.1016/j.cej.2019.122092
[103] C. Sun, J. Wang, C. Gu, C. Wang, S. Sun, and P. Song, “MOF-derived N-Co/Fe-PC composite as heterogeneous electro-Fenton catalysis combined with electrocoagulation process for enhanced degradation of Cu-CIP complexes from wastewater,” Chem. Engin. J., vol. 452, no. Part 4, p. 139592, Jan. 2023. https://doi.org/10.1016/j.cej.2022.139592
[104] J. Qin, S. Ye, K. Yan, and J. Zhang, “Visible light-driven photoelectrocatalysis for simultaneous removal of oxytetracycline and Cu (II) based on plasmonic Bi/Bi2O3/TiO2 nanotubes,” J. Colloid Interface Sci., vol. 607, pp. 1936–1943, Feb. 2022. https://doi.org/10.1016/j.jcis.2021.10.008
[105] C. Volk, L. Wood, B. Johnson, J. Robinson, H. W. Zhu, and L. Kaplan, “Monitoring dissolved organic carbon in surface and drinking waters,” J. Environ. Monit., vol. 4, no. 1, pp. 43–47, Jan. 2002. https://doi.org/10.1039/B107768F
[106] X. Zhu, X. Li, Y. Shan, and X. Zhao, “Treatment of catalyst wastewater through an environmentally friendly electrodeposition-precipitation-electrooxidation coupling process: Recovery of copper and silicate, and removal of COD,” Sep. Purif. Technol., vol. 317, p. 123858, Jul. 2023. https://doi.org/10.1016/j.seppur.2023.123858
[107] T. Paul, P. L. Miller, and T. J. Strathmann, “Visible-light-mediated TiO2 photocatalysis of fluoroquinolone antibacterial agents,” Environ. Sci. Technol., vol. 41, no. 13, pp. 4720–4727, Jun. 2007. https://doi.org/10.1021/es070097q
[108] A. Kurnia Asih, R. Desni Yetti, and B. Chandra, “Photodegradation of Antibiotic Using TiO2 as a Catalyst: A Review,” Int. J. Pharm. Sci. Med., vol. 6, no. 2, pp. 37–43, Feb. 2021. https://ijpsm.com/Publish/Feb2021/V6I205.pdf
[109] B. A. Koiki, B. O. Orimolade, B. N. Zwane, D. Nkosi, N. Mabuba, and O. A. Arotiba, “Cu2O on anodised TiO2 nanotube arrays: A heterojunction photoanode for visible light assisted electrochemical degradation of pharmaceuticals in water,” Electrochim. Acta, vol. 340, p. 135944, Apr. 2020. https://doi.org/10.1016/j.electacta.2020.135944
[110] H. Zeng, S. Tian, H. Liu, B. Chai, and X. Zhao, “Photo-assisted electrolytic decomplexation of Cu-EDTA and Cu recovery enhanced by H2O2 and electro-generated active chlorine,” Chem. Engin. J., vol. 301, pp. 371–379, Oct. 2016. https://doi.org/10.1016/j.cej.2016.04.006
[111] K. H. Hama Aziz, and F. S. Mustafa, “Advanced oxidation processes for the decontamination of heavy metal complexes in aquatic systems: A review,” Case Studies Chem. Environ. Engin., vol. 9, p. 100567, Jun. 2024. https://doi.org/10.1016/j.cscee.2023.100567
Notas
Los autores declaran que no existe conflictos de interés de tipo financiero, profesional o personal, que hayan afectado de manera directa o indirecta al desarrollo de la presente revisión.
Andrés F. Sánchez-Medina: metodología, redacción, revisión y edición.
Manuel Romero-Sáez: financiación, metodología, redacción, revisión y edición.
Carolina Ramírez-Sánchez: financiación, metodología, redacción, revisión y edición.
Notas de autor
carolinaramirezs@itm.edu.co
Información adicional
Cómo citar / How to cite: A. F. Sánchez-Medina, M. Romero-Sáez, and C. Ramírez-Sánchez, “Eliminación de complejos antibiótico-metal en aguas residuales mediante métodos electroquímicos: una revisión,” TecnoLógicas, vol. 28, no. 63, e3344, 2025. https://doi.org/10.22430/22565337.3344
Información adicional
redalyc-journal-id: 3442
Enlace alternativo
https://revistas.itm.edu.co/index.php/tecnologicas/article/view/3344 (html)
