Investigación
Efecto del secado en la concentración de compuestos bioactivos y la actividad antioxidante de plantas forrajeras
Effect of Drying on the Concentration of Bioactive Compounds and Antioxidant Activity of Forage Plants
Efecto del secado en la concentración de compuestos bioactivos y la actividad antioxidante de plantas forrajeras
TecnoLógicas, vol. 28, núm. 63, pp. 1-17, 2025
Instituto Tecnológico Metropolitano

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 13 Enero 2025
Aprobación: 27 Junio 2025
Publicación: 04 Agosto 2025
Resumen: Las especies forrajeras contienen compuestos bioactivos con propiedades beneficiosas para la salud; sin embargo, su concentración varía según la especie y puede verse afectada por el proceso de secado. Este estudio evaluó cinco especies: botón de oro (Tithonia diversifolia (Hemsl.) A.Gray), colla negra (Smallanthus pyramidalis (Triana) H.Rob.), dalia silvestre (Dahlia imperialis Roezl ex Ortgies), morera (Morus alba L.) y saúco (Sambucus nigra L.), con el objetivo de determinar su contenido de compuestos bioactivos y actividad antioxidante, así como el efecto de tres métodos de secado: horno, deshidratación solar y ventana refractiva. La metodología empleada consistió en la aplicación de técnicas espectrofotométricas específicas como cloruro de aluminio para la cuantificación de flavonoides, Folin-Ciocalteu para fenoles totales, vainillina para taninos condensados y DPPH para evaluar la actividad antioxidante. Los resultados obtenidos fueron los siguientes: antes del secado, la colla negra presentó la mayor concentración de fenoles totales, la dalia silvestre el mayor contenido de flavonoides, y el botón de oro los niveles más altos de taninos condensados y actividad antioxidante. El secado por ventana refractiva fue el método más eficiente para preservar estos compuestos, destacándose el saúco con 1282.46 mg de ácido gálico equivalente para fenoles totales, 637.94 mg de catequina equivalente para flavonoides y 257.83 mg de catequina equivalente para taninos condensados, todas las unidades en 100 g de materia seca. Asimismo, el botón de oro alcanzó la mayor actividad antioxidante, con 2374.90 µmol de equivalentes Trolox por 100 g de materia seca. En contraste, la deshidratación solar también mostró buenos resultados, especialmente en botón de oro y saúco, mientras que el secado en horno fue el menos favorable, aunque la morera presentó una actividad antioxidante relativamente alta. En conclusión, la ventana refractiva se posiciona como la mejor alternativa para preservar y potenciar los compuestos bioactivos en especies forrajeras deshidratadas.
Palabras clave: Actividad antioxidante, compuestos fenólicos, flavonoides, horno de secado, sambucus nigra L.
Abstract: Forage species contain bioactive compounds with health-promoting properties; however, their concentration varies depending on the species and can be affected by the drying process. This study evaluated five species: button of gold (Tithonia diversifolia (Hemsl.) A.Gray), black colla (Smallanthus pyramidalis (Triana) H.Rob.), wild dahlia (Dahlia imperialis Roezl ex Ortgies), mulberry (Morus alba L.), and elderberry (Sambucus nigra L.), with the aim of determining their bioactive compound content and antioxidant activity, as well as the effect of three drying methods: oven drying, solar dehydration, and refractive window drying. The methodology employed consisted of the application of specific spectrophotometric techniques such as aluminum chloride for the quantification of flavonoids, Folin-Ciocalteu for total phenols, vanillin for condensed tannins, and DPPH for evaluation of antioxidant activity. The results obtained were as follows: before drying, black colla presented the highest concentration of total phenols, wild dahlia the highest flavonoid content, and button of gold the highest levels of condensed tannins and antioxidant activity. Drying by refractive window was the most efficient method to preserve these compounds, highlighting the elderberry with 1282.46 mg of gallic acid equivalents for total phenols, 637.94 mg of catechin equivalents for flavonoids, and 257.83 mg of catechin equivalents for condensed tannins, all units in 100 g of dry matter. Additionally, button of gold achieved the highest antioxidant activity, with 2374.90 µmol Trolox equivalents per 100 g of dry matter. In contrast, solar dehydration also showed good results, especially in button of gold and elderberry, while oven drying was the least favorable method, although the mulberry showed relatively high antioxidant activity. In conclusion, refractive window drying is the best alternative for preserving and enhancing bioactive compounds in dehydrated forage species.
Keywords: Antioxidant activity, phenolic compounds, flavonoids, drying oven, sambucus nigra L.
Highlights
-
La ventana refractiva conservó mejor los compuestos bioactivos y la actividad antioxidante.
El secado en horno causó pérdidas de más del 79 % en bioactivos y 77 % en actividad antioxidante.
Botón de oro tuvo la mayor actividad antioxidante antes del secado (13796.18 µmol ET/100 gMS).
Dalia silvestre tuvo el mayor contenido de flavonoides antes del secado (4575.34 mg EC/100 gMS).
Las pérdidas de compuestos bioactivos y antioxidantes variaron según especie y método aplicado.
Highlights
-
Refractive window drying better preserved bioactive compounds and antioxidant activity.
The oven drying caused losses of more than 79% in bioactive compounds and 77% in antioxidant activity.
The button of gold had the highest antioxidant activity before drying (13,796.18 µmol TE/100 g DM).
Wild dahlia had the highest flavonoid content before drying (4,575.34 mg CE/100 g DM).
Losses of bioactive compounds and antioxidants varied according to the species and the drying method used.
1. INTRODUCCIÓN
A nivel mundial, la disponibilidad de recursos está disminuyendo debido a factores como el calentamiento global, el crecimiento poblacional, la deforestación, la pérdida de biodiversidad, entre otros. Estos factores ponen en riesgo la alimentación humana, la producción animal y la sostenibilidad de la población [1]. En este contexto, es fundamental encontrar alternativas para mejorar la gestión de los recursos naturales, especialmente aquellos que provienen de la biodiversidad.
Gracias a su ubicación geográfica, Colombia es un país extremadamente rico en recursos naturales, sin embargo, estos no son aprovechados de manera óptima y se desconoce su valor potencial, es por esto que el estudio de este tipo de recursos es de vital importancia para satisfacer las diferentes necesidades generadas por el constante desarrollo y crecimiento económico del país [2].
Por su parte, el departamento de Nariño posee una gran variedad de flora y fauna gracias a sus diversos ecosistemas como bosques secos, montañas y páramos, diferenciables por su nivel altitudinal y pisos térmicos que hacen que tenga un gran potencial para la producción de variedad de especies vegetales de interés para la elaboración de forrajes [3].
Los forrajes son plantas que crecen, se desarrollan en un terreno, se cosechan y se suministran al animal en forma de heno o ensilaje para su alimentación. Estos no solo aportan fibra, sino que también contienen compuestos bioactivos de gran interés en áreas como farmacología, química y cosmética, debido a sus propiedades benéficas para la salud [4], [5].
Dentro de los compuestos bioactivos más ampliamente reconocidos y presentes en mayores concentraciones se encuentran las vitaminas, los minerales y los líganos, los cuales tienen como principales fuentes de obtención a las frutas y hortalizas [6]. Además, existen otros compuestos, como los fenoles, los carotenoides, los compuestos organosulfurados y los fitoesteroles, que, aunque están presentes en concentraciones bajas, tienen funciones biológicas importantes en el cuerpo humano y ejercen efectos como antimicrobianos antioxidantes, antinflamatorios y agentes inmunomoduladores [6], [7].
Diversas investigaciones han demostrado que los parámetros de secado, como la temperatura, el tiempo de exposición y la técnica empleada, influyen directamente en la estabilidad y concentración de los compuestos bioactivos. Por ejemplo, en un estudio realizado con frutos de saúco (Sambucus peruviana HBK) en diferentes estados de maduración, sometidos a secado en horno de convección a tres temperaturas distintas (50°C, 60°C y 70°C) y con una velocidad de aire de 2.5 m/s, se encontró que los frutos maduros en estado fresco presentaban un contenido más elevado de los parámetros evaluados, como resultado de la mayor biosíntesis de compuestos bioactivos en esa etapa. Además, se observó que el secado a 50°C permitió una mejor conservación de estos compuestos, dado que muchos de ellos son sensibles al calor y tienden a degradarse durante el proceso de deshidratación [8].
De igual manera, en un estudio realizado con hojas de Moringa oleifera, se evidenció que el secado convectivo a 50°C permitió conservar mejor los polifenoles y la capacidad antioxidante en comparación con temperaturas más elevadas (60–80°C), donde se observó una degradación significativa de los compuestos [9]. Asimismo, el secado de frutos de níspero a 50°C permitió retener en mayor proporción los compuestos fenólicos totales y los carotenoides, mejorando la calidad funcional del producto [10].
En relación con los métodos alternativos de secado, la técnica de ventana refractiva ha despertado interés por su capacidad para preservar las propiedades funcionales de productos vegetales. Esta tecnología ha demostrado ser eficaz en la conservación de compuestos bioactivos durante el proceso de deshidratación. Diversos autores [11] señalan que esta tecnología permite una menor pérdida de metabolitos secundarios, como los fenoles, y un incremento en el contenido de flavonoides, especialmente cuando se aplican tiempos de secado más cortos en comparación con otros métodos convencionales.
En consonancia con lo anterior, un estudio [12], comparó la ventana refractiva con el secado por horno al vacío en muestras de sábila suplementadas con polifenoles de chontaduro. Aunque ambas técnicas permitieron conservar las propiedades funcionales del producto, la ventana refractiva a 60°C logró una mayor retención de compuestos fenólicos y capacidad antioxidante, lo que evidencia su superioridad frente a otros métodos térmicos.
Por otro lado, el secado solar representa una alternativa de bajo costo y fácil implementación en regiones con alta disponibilidad de radiación solar. No obstante, su eficiencia en la preservación de biocompuestos puede verse comprometida debido a la falta de control sobre variables críticas como la temperatura y la humedad. En un estudio en el que se evaluó la pérdida de compuestos bioactivos y la actividad antioxidante de Ficus carica durante el secado solar directo, se encontró que este método redujo significativamente el contenido de antocianinas, fenoles totales y la actividad antioxidante, y provocó una disminución total de los flavonoides y flavonoles [13].
En vista de lo anterior, es claro que la técnica y los parámetros del secado son determinantes para garantizar la calidad funcional de los forrajes. No obstante, existe un vacío en la literatura respecto al efecto de estas tecnologías de secado en especies forrajeras nativas o adaptadas al ecosistema del departamento de Nariño.
Por ello, el objetivo de esta investigación fue evaluar el efecto de tres técnicas de secado: horno convectivo, ventana refractiva y secado tradicional, sobre la concentración de compuestos bioactivos y la actividad antioxidante en forrajes presentes en el departamento de Nariño, Colombia.
2. METODOLOGÍA
2.1 Obtención de las muestras
Las muestras de forraje utilizadas fueron recolectadas de forma manual en la Granja Botana de la Universidad de Nariño, ubicada en Pasto, Colombia, (latitud 1.1576180° N, 77.275734° O, altitud aproximada de 2827.32 m.s.n.m.). El método de cosecha consistió en el corte manual de las plantas, siguiendo prácticas tradicionales que permitieron preservar la integridad de las especies. Se recolectaron aproximadamente 250 gramos de muestra fresca por cada planta. La recolección se realizó en el mes de junio de 2024, coincidiendo con la temporada seca de la región altoandina.
Las especies recolectadas incluyeron el botón de oro (Tithonia diversifolia (Hemsl.) A. Gray), colla negra (Smallanthus pyramidalis (Triana) H. Rob.), dalia silvestre (Dahlia imperialis Roezl ex Ortgies), la morera (Morus alba L.) y el saúco (Sambucus nigra L.), todas en estado de prefloración con una edad aproximada de cuatro meses. Las plantas se cultivaron bajo condiciones climáticas típicas de región andina, con temperaturas promedio de 15°C, humedad relativa alta y distribución de lluvias que favoreció un desarrollo vegetativo óptimo. La cosecha se realizó sin almacenamiento posterior; es decir, el material vegetal se llevó directamente a los procesos de secado inmediatamente después del corte evitando posibles alteraciones en su composición química.
2.2 Secado de las muestras
Se utilizaron 83 gramos de muestra fresca por cada método de secado, con tres repeticiones experimentales por tratamiento. Los métodos evaluados fueron: horno eléctrico de aire forzado (T1), deshidratación solar (T2) y secado por ventana refractiva (T3). En el T1, se utilizó un horno Biobase modelo BOV-V45F, fabricado en Shandong, China, con una velocidad del aire de 2.5 m/s y a una temperatura de 60°C durante 3 horas. En T2, las hojas se colocaron en bandejas dentro de un invernadero que recibía radiación solar, donde se mantuvieron condiciones térmicas controladas con una temperatura diurna promedio de 28°C y nocturna de 18°C, logrando el secado en un periodo de 360 horas. En T3, se utilizó un secador de refractancia Cei Robots, modelo HS-50XL, fabricado en Cali, Colombia, a 60°C, alcanzando la reducción de humedad en 4 horas.
En los tres métodos, las muestras iniciaron con una humedad promedio de 79.70 % y se secaron hasta un rango de humedad de 7-12 %. Esta humedad fue determinada utilizando una balanza de humedad por infrarrojos SHIMADZU MOC63u, fabricada en Kioto, Japón, en modo rápido, programada a 120°C. El forraje se deshidrató hasta que su peso permaneció constante, momento en el cual el equipo registró automáticamente la medición al detectar una mínima variación entre mediciones de peso consecutivas, señalando que la muestra había logrado el equilibrio [14].
Luego, las hojas secas de las plantas se pulverizaron utilizando un procesador de alimentos IMUSA AD6018CO, fabricado en Copacabana, Colombia. El polvo resultante fue envasado en bolsas metalizadas herméticas, resistentes a la luz y la humedad, para protegerlo de la oxidación y la degradación. Las muestras se almacenaron en un lugar fresco, seco y oscuro, con el fin de conservar sus propiedades fisicoquímicas en condiciones óptimas hasta su análisis.
2.3 Obtención de extractos
Para la obtención de los extractos, se pesaron 5 g del material vegetal fresco o seco de cada planta, según el tipo de extracto a preparar. Posteriormente, se maceraron en metanol acuoso al 80 % en una relación 1:20. La mezcla se colocó en un baño ultrasónico a 37 kHz y 30°C durante 30 minutos. Luego, se centrifugó a 10000 rpm a 15°C por 15 minutos y se filtró para separar los sólidos del extracto líquido. A continuación, se evaporó la mayor parte del disolvente en un rotaevaporador a una temperatura de 35°C y 70 rpm. Se registró el volumen final de cada uno de los extractos y se almacenó en frascos ámbar bajo refrigeración a 4°C [15].
2.4 Determinación del contenido de fenoles totales (CPT)
Para determinar el contenido de fenoles totales de los extractos, se empleó el método Folin-Ciocalteu. Para ello, se utilizó una curva de calibración de ácido gálico en concentraciones de 25 mg/L a 800 mg/L, con un R² de 0.998. Para la preparación de la solución de prueba, se tomaron 100 μL de muestra y se mezclaron con 7.9 mL de agua destilada. Luego, se agregaron 500 μL de reactivo de Folin-Ciocalteu y 1.5 mL de solución saturada de carbonato de sodio a una concentración de 200 g/L. La mezcla se incubo durante 2 horas y posteriormente se midió la absorbancia a 760 nm en un espectrofotómetro MAPADA Single Beam UV-Vis, modelo P4, fabricado en Shanghái, China. El contenido se expresó en miligramos de equivalentes de ácido gálico por 100 gramos de materia seca (mg EAG/100 g MS), de acuerdo con (1) [8],[6].
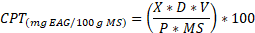 (1)
(1)Dónde: X = Equivalentes de ácido gálico (mg/mL); D = factor de dilución; V= Volumen de extracción (mL); P= peso de la muestra (g) y MS= materia seca.
2.5 Determinación del contenido de flavonoides (CFT)
El contenido total de flavonoides se estimó mediante una curva de calibración utilizando catequina como patrón, en concentraciones de 25 mg/L a 600 mg/L y un R² de 0.9927. Para ello, se tomaron 250 µL de la muestra y se mezclaron con 1.25 mL de agua ultrapura. Luego, se añadieron 75 µL de nitrito de sodio al 5 %, 150 µL de cloruro de aluminio al 10 % y 500 µL de hidróxido de sodio 1 M, dejando transcurrir 5 minutos entre la adición de cada solución. Posteriormente, se agregó 775 µL de agua hasta completar un volumen total de 3 mL y se agitó para homogeneizar la mezcla. Finalmente, se midió la absorbancia de las muestras a 510 nm en un espectrofotómetro MAPADA Single Beam UV-Vis, modelo P4, fabricado en Shanghái, China. El contenido se expresó en miligramos de equivalente de catequina por 100 gramos de materia seca (mg EC/100 g MS), según (2)[16]. (Error 1: La referencia [16]. debe estar ligada) (Error 2: El tipo de referencia [16]. es un elemento obligatorio) (Error 3: No existe una URL relacionada)
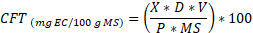 (2)
(2)Dónde: X = Equivalentes de catequina (mg/mL); D = factor de dilución; V= Volumen de extracción (mL); P= peso de la muestra (g) y MS= materia seca.
2.6 Determinación del contenido de taninos condensados (CTC)
El contenido de taninos condensados se determinó mediante el método de vainillina. Para ello, se construyó una curva de calibración utilizando catequina disuelta en metanol como estándar, en concentraciones de 25 mg/L a 1300 mg/L, con un R² de 0.9863. La solución de prueba se preparó tomando 240 µL de extracto y mezclándolos con 1200 µL de una solución recién preparada de vainillina al 1 % y HCl 8 % en metanol, en una relación 1:1. La mezcla se incubó a 30°C durante 20 minutos. Posteriormente, se midió la absorbancia a 492 nm en un espectrofotómetro MAPADA Single Beam UV-Vis, modelo P4, fabricado en Shanghái, China. Los resultados se expresaron en miligramos de equivalentes de catequina por 100 gramos de materia seca (mg EC/100 g MS), de acuerdo con (3) [17].
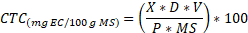 (3)
(3)Dónde: X = Equivalentes de catequina (mg/mL); D = factor de dilución; V= Volumen de extracción (mL); P= peso de la muestra (g) y MS= materia seca.
2.7 Determinación de la actividad antioxidante (CA)
La actividad antioxidante de las muestras se estimó mediante el procedimiento de 2,2-difenil-1-picrilhidrazilo (DPPH). Para ello, se realizó una curva de calibración utilizando trolox como patrón, en concentraciones de 25 µM a 1300 µM, con un R² de 0.9894. Para la medición, se preparó previamente una solución metanólica de 60 µM del radical DPPH, en un balón aforado completamente cubierto de aluminio. Luego, se tomaron 50 µL del extracto y se añadieron 1950 µL de la solución de DPPH en metanol. La mezcla se agitó y se incubó en la oscuridad a temperatura ambiente durante 30 minutos. Posteriormente, se midió la absorbancia a 517 nm en un espectrofotómetro MAPADA Single Beam UV-Vis, modelo P4, fabricado en Shanghái, China. Los resultados se expresaron en micromol de equivalentes de trolox por cada 100 gramos de materia seca (µmol ET/100 g MS), utilizando (4) [8], [16], [18].
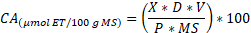 (4)
(4)Dónde: X = Equivalentes Trolox (µmol/mL); D = factor de dilución; V= Volumen de extracción (mL); P= peso de la muestra (g) y MS= materia seca.
2.8 Análisis estadístico
Se evaluó la concentración de compuestos bioactivos y la actividad antioxidante en muestras vegetales, tanto en estado fresco como después de aplicar diferentes métodos de secado. En ambos casos, se aplicó un diseño completamente al azar (DCA) con un solo factor categórico, el cual correspondió al tipo de forraje o al método de secado. Para el análisis por tipo de forraje, el factor tuvo cinco niveles con tres repeticiones, correspondientes a las especies estudiadas; en el análisis por método de secado, el factor tuvo tres niveles, también con tres repeticiones. Para ambas situaciones, las variables de respuesta fueron el contenido de fenoles totales, los flavonoides, los taninos condensados y la actividad antioxidante. Los datos, expresados como promedio ± desviación estándar, fueron sometidos a un análisis de varianza (ANOVA) con un nivel de significancia de p ≤ 0.05, previa verificación del cumplimiento de los supuestos de normalidad (prueba de Shapiro- Wilk) y homogeneidad de varianzas (prueba de Levene). Para la comparación de medias entre tratamientos se empleó la prueba de Tukey de rangos múltiples (p ≤ 0.05).
3. RESULTADOS Y DISCUSIÓN
3.1 Determincación de la concentración de compuestos bioactivos y la actividad antioxidante de plantas forrajeras en estado fresco
La Tabla 1 indica los resultados del contenido de compuestos fenólicos totales, flavonoides, taninos condensados y capacidad antioxidante de las plantas de saúco, morera, botón de oro, dalia y colla negra. De acuerdo con el análisis de varianza (ANOVA), el tipo de forraje tiene un efecto significativo sobre cada una de las variables de respuesta evaluadas, con un nivel de significancia (p ≤ 0.05).
| Tipo de forraje | Fenoles totales (mg EAG/100 g MS) | Flavonoides (mg EC/100 g MS) | Taninos condensados (mg EC/100 g MS) | Actividad antioxidante (µmol ET/100 g MS) |
| Saúco | 4144.88 ± 12.4 | 3700.00 ± 19.6 | 816.34 ± 11.3 | 10952.61 ± 16.3 |
| Morera | 1541.80 ± 10.8 | 1193.34 ± 10.9 | 377.42 ± 7.5 | 7259.86 ± 16.5 |
| Botón de oro | 3800.27 ± 5.9 | 3411.86 ± 16.3 | 1471.57 ± 14.1 | 13796.18 ± 23.6 |
| Dalia | 5030.49 ± 20.3 | 4575.34 ± 20.4 | 438.21 ± 14.0 | 13678.18 ± 11.7 |
| Colla negra | 5150.66 ± 28.2 | 3757.19 ± 4.3 | 873.07 ± 13.0 | 12748.90 ± 10.8 |
El análisis de comparación múltiple realizado para cada tipo de forraje mediante la prueba de Tukey reveló diferencias significativas en el contenido de compuestos fenólicos totales entre las especies de forraje evaluadas. Los forrajes con mayor contenido de fenoles fueron la colla negra y dalia, mientras que la morera y el botón de oro presentaron los niveles más bajos. Esta variación en el contenido de fenoles entre las distintas especies se debe a que los polifenoles comprenden fracciones extraíbles y no extraíbles. Los estudios se centran en analizar la fracción extraíble, la cual, al igual que la fracción no extraíble, se encuentra en diferentes proporciones en cada especie vegetal [19]. En este sentido, se ha observado que en muchas matrices vegetales el contenido de compuestos fenólicos no extraíbles puede incluso superar al de los extraíbles, ya que incluyen estructuras poliméricas complejas y compuestos asociados a componentes estructurales de la planta, como polisacáridos y proteínas, lo que influye notablemente en la cuantificación total de estos metabolitos en cada especie [20].
De acuerdo con los datos bibliográficos, el contenido de fenoles en el saúco es de 4757.93 ± 1.31 mg EAG/100 g MS [8]. Este valor es un 12.88 % superior al que se expone en el presente estudio. Con referencia a la morera, algunos estudios informaron un contenido superior al observado en esta investigación, con una concentración de 2688 ± 1.76 mg EAG/100 g MS [21]. Por otro lado, el contenido de fenoles en el botón de oro y la dalia superó los valores reportados en la literatura, donde se indicó que las hojas de botón de oro tienen una concentración de 1764 ± 1.5 mg EAG/100 g MS, mientras que en flores de dalia de la variedad Yaretzi se encontró un contenido de 3152 ± 16.67 mg EAG/100 g MS [22], [23].
Respecto al contenido de flavonoides fue mayor en dalia y menor en morera. La concentración de flavonoides difiere de manera significativa entre los tipos de forrajes estudiados. Se observó que la concentración de estos compuestos en cuanto a materia fresca, en sauco, fue considerablemente inferior a la obtenida en algunos estudios [24]. Esta variación puede deberse a que la síntesis y la composición fitoquímica de una planta, incluso dentro de la misma especie, puede verse afectada por diversas condiciones de estrés. Estos factores incluyen tanto estreses bióticos (ataques de insectos potencialmente plagas, enfermedades fúngicas y bacterianas), como abióticos (temperatura, sequía, salinidad y radiación UV) [25], [26].
Por su parte, los taninos condensados mostraron una mayor concentración en botón de oro y una menor en morera, con una diferencia del 74.35 % entre ambas especies. Las medias de las concentraciones de taninos condensados presentaron diferencias estadísticamente significativas entre los diferentes forrajes evaluados. Según algunas investigaciones, el botón de oro tiene una concentración de taninos 26.05 % superior a la observada en este estudio, con un valor de 1990 ± 0.48 mg EC/100 g MS [27]. En cuanto a las demás especies evaluadas, la bibliografía no proporcionó información suficiente. Sin embargo, algunos autores reportaron concentraciones de taninos en hojas de otras plantas como cosmos amarillo, manayupa, rosa china y moringa, de 68.70, 868, 970 y 2900 EC/100 g MS, respectivamente [27], [29]. Esto demuestra que existe variación en el contenido de taninos entre las distintas especies vegetales. Este contenido está influenciado por diversos factores como la genética, el entorno de desarrollo de la planta, la especie vegetal, la fertilidad del suelo, el órgano o parte de la planta, la estación de crecimiento, así como los tipos de solventes utilizados y la metodología de extracción empleada [30], [31].
En cuanto a la actividad antioxidante, se evidenció diferencias significativas entre las medias de los tratamientos. Se observó que todos los forrajes presentaron una alta actividad antioxidante, siendo superior en botón de oro y menor en morera. El saúco presentó una actividad antioxidante 29.20 % inferior a la reportada en la literatura, en la cual se encontró un valor de 15470 ± 5.7 µmol ET/100 g MS, en su fruto [8]. De manera similar, en otra investigación, se reportó una concentración 78.13 % menor en un extracto en metanol de hojas de botón de oro [32]. Es importante destacar que esta última especie presentó una mayor cantidad de taninos condensados, compuestos que pueden contribuir de forma significativa en actividad antioxidante de la planta.
Por otro lado, es fundamental considerar que existen compuestos diferentes a los evaluados, que también tienen actividad antioxidante y pueden estar presentes en los forrajes. Aunque la actividad antioxidante predominante es la de los polifenoles, también hay compuestos como carotenoides, tocoferoles, tocotrienoles, así como algunos aminoácidos y péptidos que poseen esta propiedad [33]. Un ejemplo de esto se observó en extractos de Euphorbia echinus, donde de identifico una relación inversa entre la cantidad de compuestos fenólicos y la capacidad antioxidante [34]. Esto ayuda a entender por qué la actividad antioxidante no siempre es mayor en los forrajes con una mayor concentración de los compuestos bioactivos evaluados.
3.2 Comparación del efecto del secado en la concentración de compuestos bioactivos y la actividad antioxidante de plantas forrajeras
3.2.1Contenido de fenoles totales después del secado
En la Figura 1 se puede observar el comportamiento de la concentración de fenoles totales en las especies sometidas a los diferentes tipos de secado. Según el análisis de varianza, el método de secado tiene un efecto significativo sobre el contenido de fenoles totales en todas las plantas, con un nivel de significación para p ≤ 0.05. La prueba de comparación múltiple de medias reveló que existen diferencias significativas en la concentración de fenoles totales entre los distintos métodos de secado para cada planta evaluada. Es importante tener en cuenta que, la retención de polifenoles depende en gran medida de las tasas de deshidratación, la exposición a la radiación solar, y las temperaturas medias y máximas durante el secado. Estas condiciones varían según el método de secado utilizado, lo que da lugar a una concentración variable de polifenoles entre las muestras sometidas a los diferentes tratamientos [35].
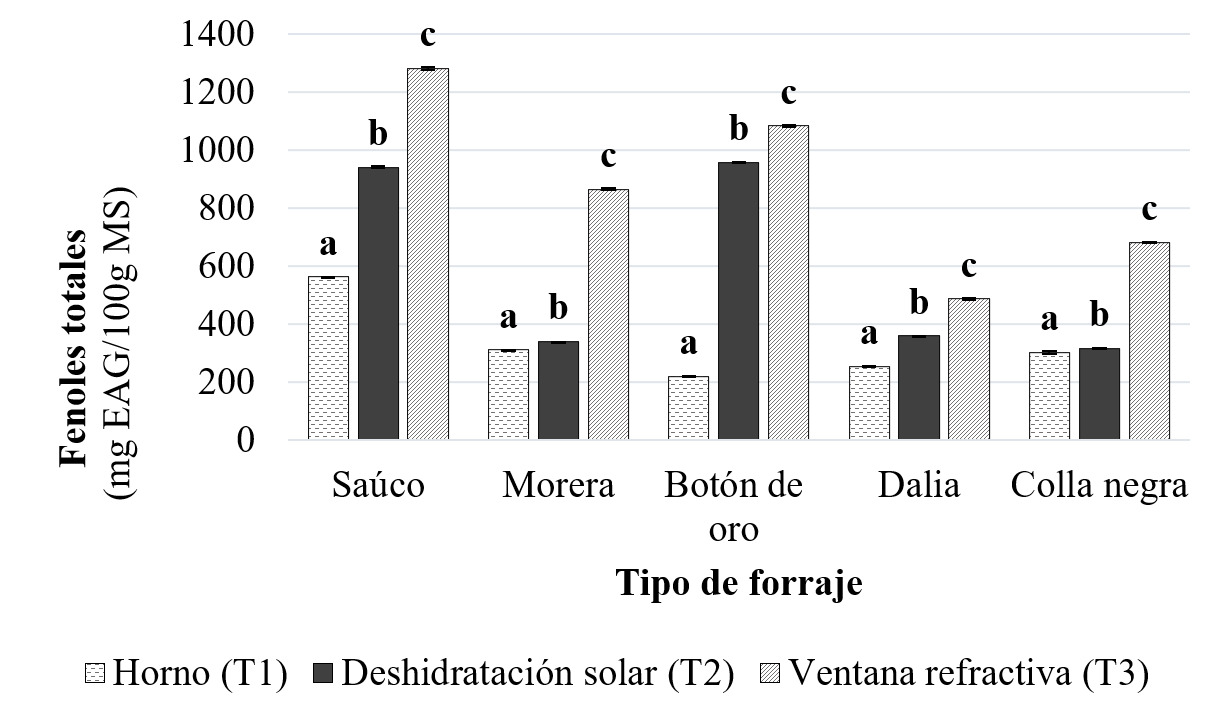
Figura 1.
Contenido de fenoles totales de los forrajes sometidos a diferentes tipos de secado
Fuente: elaboración propia.
La planta que mostró un mayor contenido de compuestos fenólicos utilizando los métodos de secado T3 y T1, fue el saúco, con un contenido de 1282.46 ± 5.12 y 561.98 ± 0.53 mg EAG/100 g MS, respectivamente. Estos valores representan un porcentaje de pérdida respecto al contenido fresco de las mismas especies de 69.06 % y 86.44 %. Los valores obtenidos en estos tratamientos estuvieron, en algunas plantas, dentro del rango y, en otras, por encima del registrado para Aloe vera suplementado con polifenoles de residuos agroindustriales, que fue de 260 - 670 mg EAG/100 g MS para el secado por ventana refractiva y 150 -240 mg EAG/100 g MS para el secado por horno [12].
Por su parte, el tratamiento T2 presentó una mayor concentración de fenoles en el forraje del botón de oro, con un valor de 957.30 ± 2.82 mg EAG/100 g MS, lo que representa una pérdida del 74.81 % respecto a su contenido inicial. Las concentraciones de fenoles en el secado solar superaron los valores reportados para chile de agua, el cual presento un contenido de 255.72 ± 10.40 mg EAG/100 g MS [36].
Se observó que, en general, el contenido de fenoles fue más elevado en las muestras vegetales secadas por T3 y más bajo en las secadas por T1. Esta misma tendencia se constató en otros estudios, donde el secado por ventana refractiva arrojó una concentración más elevada de fenoles en comparación con otros métodos de secado [37]. Este patrón podría deberse al tipo de secado, ya que se conoce que en el secado por ventana refractiva la energía térmica proveniente del fluido calentado se transmite a través de la película por conducción y radiación [38]. Esta transferencia de calor, que ocurre de manera indirecta y principalmente por radiación infrarroja, favorece la retención de compuestos y nutrientes.
A su vez, se observa una mayor fluctuación en el contenido de fenoles de los forrajes secados con el método T2, donde, en algunos casos, los valores son más cercanos a los obtenidos con T1 y, en otros, a los obtenidos con T3. Esto podría deberse a que las condiciones de secado en el método T2, como temperatura, flujo de aire y humedad relativa, son menos controladas en comparación con los otros dos métodos, que permiten un mayor control de las mencionadas variables.
Asimismo, es importante destacar que, aunque en el tratamiento T2 se observó un comportamiento fluctuante en el contenido de fenoles, la pérdida de estos compuestos no fue tan alta en comparación con la registrada en los forrajes secados por el método T1. Esto puede atribuirse a que en el secado solar las muestras se exponen a temperaturas moderadas (ambientales), lo que genera un menor estrés térmico, a pesar de que este secado se desarrolla durante un periodo más prolongado [35]. Por otro lado, en el caso del secado por horno de convección, los compuestos bioactivos como los fenoles y flavonoides reaccionan fácilmente con el oxígeno a altas temperaturas. La velocidad de esta reacción acelera su degradación, debido a la alta susceptibilidad de estos compuestos a la oxidación, lo que contribuye a una mayor pérdida de su contenido durante tratamientos térmicos intensos [39].
3.2.2Contenido de flavonoides después del secado
La Figura 2 muestra la concentración de flavonoides en los forrajes evaluados sometidos a los diferentes métodos de secado. El tratamiento T3 permitió conservar una mayor cantidad de flavonoides en comparación con los tratamientos T1 y T2, que mostraron una menor concentración. El análisis de varianza indicó que el tipo de secado influyó significativamente en el contenido de flavonoides de cada uno de los forrajes evaluados, con una significación para p ≤ 0.05. Algunos autores [40] señalan que, aunque las técnicas de secado se han utilizado ampliamente para mejorar la vida útil de varios productos, como por ejemplo la de los forrajes, estos métodos tienen efectos negativos sobre los compuestos bioactivos, generando cambios físicos y químicos, como degradación, volatilización e isomerización, debido a la exposición del producto a temperaturas elevadas.
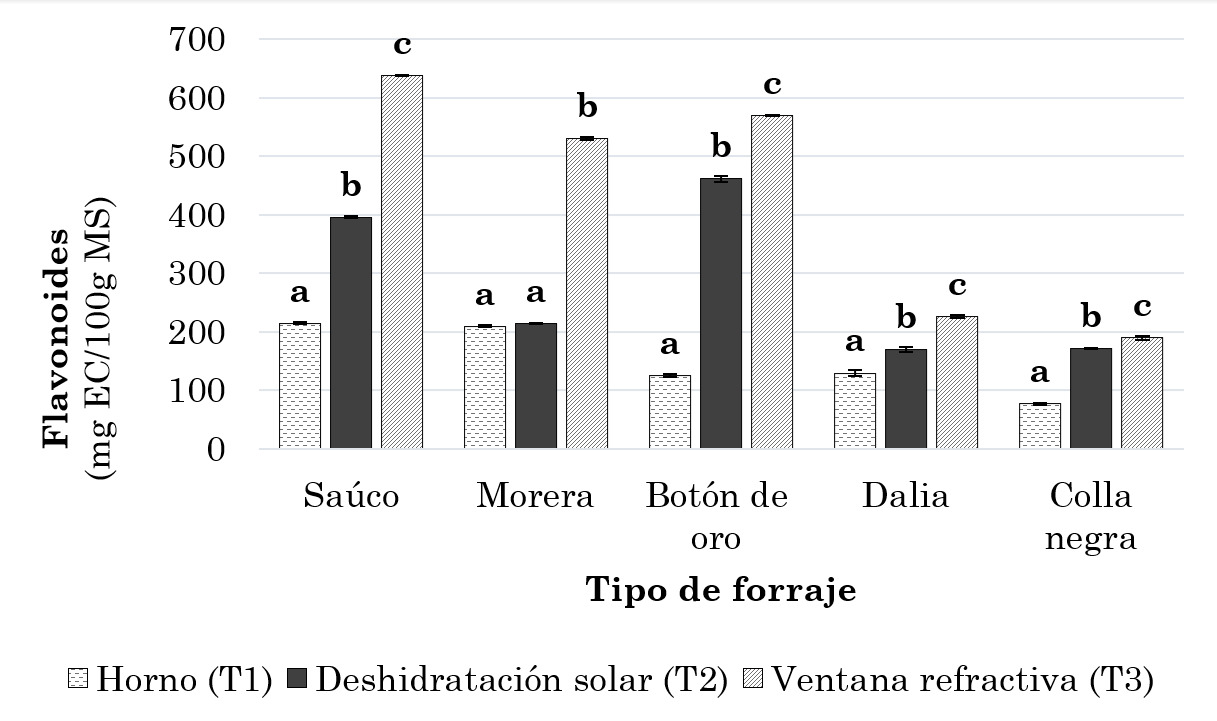
Figura 2.
Contenido de flavonoides de los forrajes sometidos a diferentes tipos de secado
Fuente: elaboración propia.
Adicionalmente, la prueba de múltiples rangos reveló que, respecto a la morera, no hubo diferencias significativas en los niveles de flavonoides entre los métodos de secado T1 y T2, lo que pudiera sugerir que la degradación de flavonoides fue equivalente en ambos métodos, a pesar de las diferencias en temperatura y en su duración. Esto puede ser atribuido al hecho de que, aunque la temperatura en el secado T2 fue menor que en T1, el tiempo de exposición fue más prolongado, lo que favoreció un mayor contacto de los flavonoides de la morera con agentes de deterioro, como el oxígeno y las enzimas, a los que posiblemente son más susceptibles. Estos agentes pudieron generar oxidación aérea y degradación enzimática y junto con la temperatura tuvieron un efecto compensatorio en la degradación de los compuestos [35].
En contraste, los métodos de secado si tuvieron influencia en la variación del contenido de flavonoides en las demás plantas. Puesto que los flavonoides y taninos condensados son un subgrupo de los polifenoles, los factores que afectaron estos compuestos en el proceso de secado son los mismos que influyeron en la degradación de polifenoles, lo que puede que explique las diferencias encontradas.
Es relevante mencionar que la concentración más elevada de flavonoides en los forrajes secados mediante los métodos T3 y T1 fue en saúco, con valores de 637.94 ± 1.13 y 214.46 ± 2.20 mg EC/100 g MS, respectivamente. Estos valores representan una pérdida del 82.76 % y del 94.20 % en comparación con el forraje fresco de la misma especie. El contenido de flavonoides en los forrajes secados mediante ventana refractiva fue superior al reportado para rodajas de betabel y al igual que en este estudio, fue el tratamiento que logró preservar mejor los flavonoides en comparación con otros tipos de secado [28]. En relación con el secado por horno, el contenido registrado para chile jalapeño rojo estuvo por encima de los valores obtenidos en esta investigación, exhibiendo una concentración de 545 ± 0.08 mg EC/100 g MS [41].
Por otro lado, entre los forrajes secados por el método T2, el botón de oro logró conservar una mayor concentración de estos compuestos, con un valor de 460.83 ± 4.43 mg EC/100 g MS, lo que resulta en una pérdida del 86.49 % respecto a su concentración inicial. En comparación, la concentración de flavonoides en chile de agua secado por el sistema de deshidratación solar estuvo dentro del rango obtenido en este trabajo, la cual fue de 481.71 ± 23.50 mg EC/100 g MS [36].
Es importante destacar que los forrajes de dalia y colla negra presentaron, antes de los procesos de secado, la mayor concentración de fenoles totales y flavonoides. Sin embargo, tras ser sometidos a los diferentes métodos de secado, mostraron la menor concentración de dichos compuestos. Esto puede que sugiera que los fenoles y flavonoides presentes en estas dos especies son más termolábiles en comparación con los de las demás plantas evaluadas. La estabilidad de los flavonoides a temperaturas elevadas depende de la estructura química de cada compuesto. Algunos de estos compuestos son la quercetina, ácido gálico, cianidina 3-O-glucosido y la mirecitina, entre otros [40], [42]. Considerando que los compuestos presentes en estas plantas pueden tener una estructura que favorece el deterioro térmico, se puede atribuir a ello la pérdida de los mismos.
3.2.3Contenido de taninos condensados después del secado
En la Figura 3 se muestra la concentración de taninos condensados en los forrajes deshidratados. Se evidenció que los diferentes métodos de secado tuvieron una influencia significativa sobre el contenido de taninos condensados, con una significación para p ≤ 0.05. Además, la prueba de Tukey reveló diferencias significativas entre las medias de la concentración de estos compuestos en cada tipo de forraje, tras ser sometidos a los tratamientos de secado T1, T2 y T3.
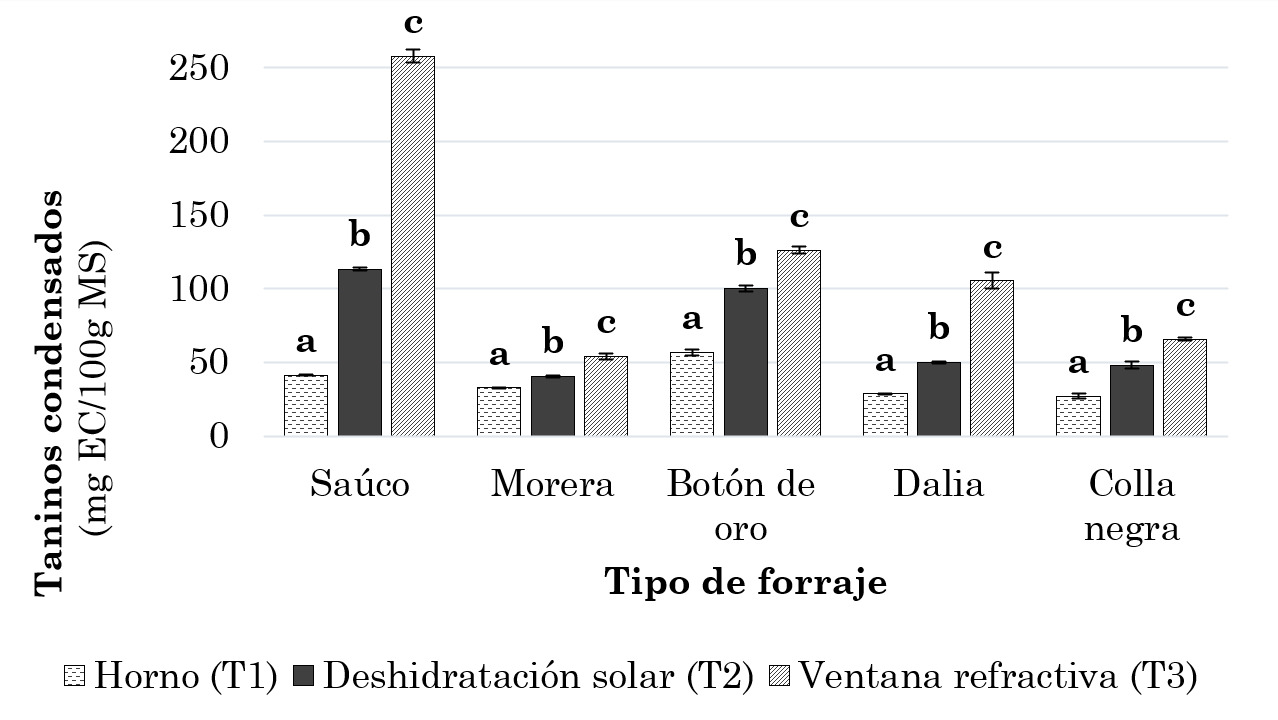
Figura 3.
Contenido de taninos condensados de los forrajes sometidos a diferentes tipos de secado
Fuente: elaboración propia.
La concentración más elevada de taninos se obtuvo mediante el método de secado T3, específicamente en el forraje de saúco, con un valor de 257.83 ± 4.32 mg EC/100 g MS. Este valor es un 68.42 % inferior al obtenido en el forraje fresco de la misma especie. El saúco también logró preservar un nivel más alto de taninos con el secado T2 en comparación con las demás especies de forrajes, con una pérdida del 86.12 % respecto a su contenido en fresco. Por su parte, en el método T1, el forraje que presentó la cifra más alta fue el de botón de oro, con una pérdida del 96.15 %. Algunos investigadores reportaron un contenido de taninos condensados en frutos de chile secados por el sistema de deshidratación solar, superiores a los registrados en el presente estudio, esto puede que se deba a que el contenido de taninos depende de diferentes factores como la variedad, la especie, el estado de la planta y las condiciones ambientales durante su crecimiento [43], [44]. También se observó que, aunque el forraje botón de oro fue la segunda especie deshidratada con mayor concentración de taninos, sufrió un impacto significativo debido a los métodos de secado. A pesar de su alta concentración de taninos en estado fresco, se visualizó una pérdida del 91.43 % en el secado T3.
Además, se pudo evidenciar que en los métodos de secado en los que hubo un ascenso brusco de temperatura, como en el caso del tratamiento T1, se observó una mayor pérdida de taninos condensados. En algunos estudios, se encontró que, utilizando el secado convectivo a diferentes temperaturas, los taninos, los fitatos y los oxalatos presentaron una tendencia descendente con el aumento de la temperatura y el acortamiento del tiempo. Sin embargo, notaron también que la temperatura tuvo una mayor influencia en la degradación que la duración del secado, lo que explica el comportamiento del contenido de taninos reportado en el presente estudio para el secado T2. Aunque este tratamiento duró más tiempo, su temperatura fue menor, lo que permitió preservar un mayor contenido de taninos condensados [45].
Es importante tener en cuenta que los resultados obtenidos tienen implicaciones significativas según el objetivo del uso de las plantas. Por un lado, si se busca utilizar la planta como alimento para animales, el método de secado T1 es preferible, ya que reduce significativamente el contenido de taninos y presenta una mayor eficiencia en el tiempo de secado. Esto es relevante, ya que, durante mucho tiempo, los metabolitos secundarios presentes en las plantas, como los taninos, han sido considerados compuestos perjudiciales para los animales y se les ha denominado factores antinutricionales [46]. Esto se debe a que niveles altos de estos compuestos pueden provocar reacciones astringentes y dañar la flora intestinal bacteriana de los animales, lo que puede desencadenar una digestión incompleta de los alimentos y una absorción mínima de proteínas y otros nutrientes [47].
Por otro lado, si el objetivo es la extracción y el aprovechamiento de estos compuestos con fines farmacológicos e industriales, el método de secado T3 es el adecuado, ya que preserva estos valiosos compuestos. Es relevante destacar que los taninos poseen un gran poder antioxidante al secuestrar radicales libres, como el hidroxilo (OH), y actuar como inhibidores de la enzima xantina oxidasa, la principal generadora de radicales libres. También se señala que estos compuestos ofrecen efectos positivos para la salud, ya que presentan propiedades antibacterianas, anticarcinogénicas, así como la capacidad de inhibir la peroxidación de lípidos y la agregación de plaquetas, procesos vinculados a la formación de trombos en el sistema circulatorio [48]. Adicionalmente, debido a su alto contenido de grupos aromáticos y fenólicos, los taninos condensados han sido empleados en la producción de biocombustibles y de moléculas aromáticas. Asimismo, gracias a sus propiedades de absorción UV se han aprovechado en el desarrollo de materiales con funciones anti- UV [49].
3.2.4Actividad antioxidante después del secado
La Figura 4, muestra la actividad antioxidante de los forrajes evaluados sometidos a los diferentes métodos de secado. El análisis de varianza efectuado demuestra que los métodos de secado tienen una influencia significativa sobre la actividad antioxidante en cada uno de los forrajes, con un nivel de confianza del 95 %. Por otra parte, las medias de la actividad antioxidante de cada uno de los forrajes entre métodos de secado fueron significativamente diferentes. Se puede inferir que esto puede estar relacionado principalmente con la degradación de los compuestos bioactivos presentes en las plantas, dado que estos son en gran medida los responsables de dicha capacidad.
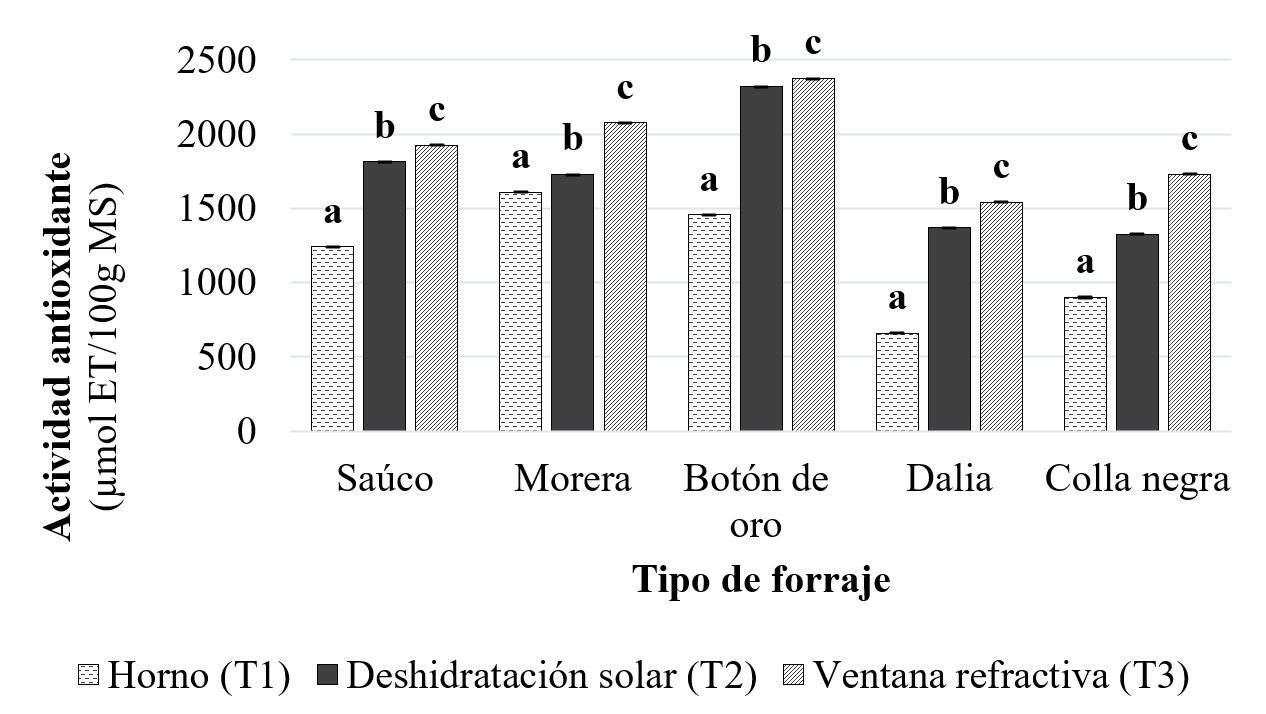
Figura 4.
Actividad antioxidante de los forrajes sometidos a diferentes tipos de secado
Fuente: elaboración propia.
La mayor actividad antioxidante de los forrajes secados por los tratamientos T3 y T2 se obtuvieron en el forraje botón de oro, con valores de 2374.90 ± 2.03 y 2320.91 ± 2.13 µmol ET/100 g MS respectivamente. Estos valores representaron una pérdida de 82.79 % y 83.18 % con respecto a la actividad antioxidante del forraje en estado fresco. La revisión bibliográfica no arrojó información acerca de la actividad antioxidante en el secado por ventana refractiva en este forraje; sin embargo, para el secado por deshidratación solar, en comparación con los valores reportados en este estudio en unidades de peso fresco, se reportó una actividad antioxidante inferior en uvilla deshidratada [35].
Por otro lado, en el tratamiento T1 se obtuvo una mayor actividad antioxidante en el forraje morera con un valor de 1606.92 ± 3.63 µmol ET/100 g MS y una pérdida del 77.87 %. Los valores de esta investigación están por debajo de los registrados para hojas de huazontle secadas con el mismo método, las cuales presentaron un contenido de 6922 µmol ET/100 g MS. Esta diferencia se debe a que el poder antioxidante varía, al igual que los compuestos bioactivos, entre especies y variedades de plantas [48].
De igual forma, se observó que hubo una mayor actividad antioxidante en el método T3 en comparación con los otros métodos estudiados. Este mismo comportamiento fue registrado en otro estudio, donde el secado por ventana refractiva arrojó mejores resultados que el secado por horno. Esta tendencia se explica por el hecho de que la ventana refractiva tiene la capacidad de deshidratar de manera adecuada las muestras sensibles a altas temperaturas, reteniendo los atributos de calidad de los materiales biológicos y conservando sus propiedades bioactivas. Además, involucra la transferencia de calor por conducción, convección y radiación, lo que le otorga un gran potencial para su uso en la deshidratación de muestras termosensibles con alto contenido de humedad [12].
Además, es importante recalcar que, el forraje botón de oro en estado fresco también presentó la mayor actividad antioxidante en relación con los demás forrajes evaluados. Lo anterior indica que los compuestos presentes en esta especie tienen un gran potencial para prevenir o reducir la oxidación de otras moléculas, protegiéndolas contra los daños causados por los radicales libres. Esta planta posee compuestos como los taninos libres y condensados, fenoles, flavonoides, lignina y alcaloides que son los responsables de la acción antioxidante [50]. Asimismo, esta planta tiene un destacado valor en la medicina tradicional, donde se le atribuyen propiedades antipalúdicas, antidiabéticas, anticancerígenas y antibacterianas [51].
4. CONCLUSIONES
En estado fresco, los forrajes que presentaron los niveles más altos de compuestos bioactivos fueron la dalia, el botón de oro y la colla negra, con concentraciones significativamente superiores al resto de especies analizadas. Estas plantas también mostraron la mayor actividad antioxidante, lo que las posiciona como candidatas idóneas para ser aprovechadas en sistemas productivos que buscan alternativas con propiedades funcionales. En contraste, el sauco y la morera presentaron los contenidos más bajos de dichos compuestos, lo cual sugiere un menor valor antioxidante en su forma natural.
Al evaluar el efecto de los métodos de secado (ventana refractiva, horno y deshidratación solar), se observó una reducción importante en la concentración de compuestos bioactivos y en la capacidad antioxidante. El método de secado por horno de convección resultó ser el más agresivo, generando pérdidas superiores al 79 % en el contenido de compuestos bioactivos y una disminución de la actividad antioxidante por encima del 77 %, lo que pone en evidencia la sensibilidad de estos compuestos al calor. Por tanto, este método resulta poco recomendable para la conservación de las propiedades funcionales de los forrajes.
En contraste, El secado por ventana refractiva demostró ser el método más eficiente en la preservación de los compuestos bioactivos, especialmente en el caso del sauco, que mostró una mejor estabilidad frente a los efectos de la temperatura y tiempo de duración del proceso. Este hallazgo sugiere que, si bien algunas especies presentan bajos niveles en estado fresco, su resistencia al secado podría hacerlas viables en procesos industriales si se aplica un tratamiento térmico adecuado.
El análisis realizado evidenció que los forrajes evaluados fueron una fuente significativa de compuestos bioactivos con elevada actividad antioxidante, especialmente en su estado fresco. Además, estos hallazgos son una base para escoger de manera adecuada el método de secado, ya que este factor resulto determinante para conservar las propiedades funcionales y garantizar la calidad de los forrajes. Estos hallazgos aportan información fundamental para la toma de decisiones en el diseño de procesos que incorporen técnicas de secado y promuevan el aprovechamiento de los recursos vegetales locales.
Agradecimientos
Agradecimientos a Minciencias y al SGR por su apoyo presupuestal al proyecto “Innovación en los procesos de alimentación, sacrificio y transformación de carne de Cuy (Cavia porcellus) como herramienta para el fortalecimiento de la actividad cuyícola del departamento de Nariño” con código BPIN 2021000100086 y al Grupo de Apoyo a la Investigación y Desarrollo Agroalimentario (GAIDA) de la Universidad de Nariño.
REFERENCIAS
[1] J. Ramírez de la Ribera et al., “El clima y su influencia en la producción de los pastos,” Rev. Electr. Veter., vol. 18, no. 6, pp. 1–12, Jun. 2017. https://www.redalyc.org/pdf/636/63651420007.pdf
[2] J. D. Montoya, “Los principales recursos naturales de Colombia,” desarrollosustentable.co, 2023. Accessed: Dec. 28, 2024. [Online]. Available: https://www.desarrollosustentable.co/recursos-naturales-de-colombia/
[3] A. S. Candamil, “Biodiversidad y medio ambiente en Nariño,” Wix.com, 2019. Accessed: Dec. 28, 2024. [Online]. Available: https://asuazac2833.wixsite.com/misitio-1/post/fauna-y-flora-de-nari%C3%B1o#:~:text=Tambi%C3%A9n%20encontramos%20en%20Nari%C3%B1o%%202053,g%C3%A9neros%20de%20Ericaceae%2C%20como%20Befaria
[4] C. F. Aguilar Pérez, and R. Santos Ricalde, “Pastos y forrajes para alimentación en caballos,” Bioagrociencias, vol. 15, no. 2, pp. 60–67, 2022. https://doi.org/10.56369/bac.4523
[5] R. León, N. Bonifaz, and F. Gutiérrez, “Generalidades”, in Pastos y forrajes del Ecuador Siembra y producción de pasturas, 1ra ed. Quito, Ecuador: Universidad Politécnica Salesiana, 2018, pp. 1-622. https://dspace.ups.edu.ec/handle/123456789/19019
[6] S. Hurtado Barroso, “Efecto de la dieta mediterránea y sus compuestos bioactivos en la prevención y prognosis de enfermedades crónicas,” Tesis doctoral, Universitat de Barcelona, Barcelona, España, 2019. https://hdl.handle.net/2445/144469
[7] J. I. Alvarez-Leite, “The Role of Bioactive Compounds in Human Health and Disease,” Nutrients, vol. 17, no. 7, p. 1170, Mar. 2025. https://doi.org/10.3390/nu17071170
[8] M. Garay Veliz, “Evaluación de bioactivos y actividad antioxidante en el secado de sauco (Sambucus peruviana HBK) por espectrofotometria y antocianinas por HPLC,” Tesis de grado, Universidad Nacional del Centro del Perú, Huancayo, Perú, 2019. https://repositorio.uncp.edu.pe/bitstream/handle/20.500.12894/5401/T010_4115725%208_T.pdf?sequence=1&isAllowed=y
[9] S. Zapata Giraldo, “Evaluación del efecto de la temperatura de deshidratación sobre la capacidad antioxidante y el contenido de metabolitos antioxidantes en hojas de Moringa Oleifera e incorporación en una bebida lactea,” Tesis de maestría, Universidad Nacional de Colombia, Medellín, Colombia, 2022. https://repositorio.unal.edu.co/handle/unal/87302
[10] S. Tobar Barrientos, “Efecto de la temperatura de secado en los compuestos bioactivos y capacidad antioxidante del nispero (Mespilus germánica L.),” Tesis de grado, Universidad Nacional del Centro del Perú, Huancayo, Perú, 2018. http://hdl.handle.net/20.500.12894/4787
[11] M. Espinoza et al., “Thermal impact of Refracting WindowTM drying on the antioxidant metabolites of quince peels (Cydonia oblonga L.),” Agroind. Sci., vol. 5, no. 2, pp. 143–151, Jan. 2016. https://doi.org/10.17268/agroind.science.2015.02.06
[12] K. Peña Anchico, “Evaluación del secado sobre la conservación del contenido fenólico y capacidad antioxidante del aloe vera suplementado con polifenoles,” Trabajo de grado, Universidad ICESI, Cali, Colombia, 2022. https://repository.icesi.edu.co/server/api/core/bitstreams/59256449-fb9c-4847-b760-46327ff31d5c/content
[13] H. Barrientos Garcia, “Cinética de pérdida de humedad, compuestos bioactivos, actividad antioxidante y estabilidad en Ficus carica, durante el secado solar directo,” Tesis de grado, Universidad Nacional de San Cristóbal de Huamanga, Ayacucho, Perú, 2023. https://repositorio.unsch.edu.pe/handle/UNSCH/5678
[14] J. M. De la Vega Camalle, “Caracterización nanoscópica superficial de películas de almidón extraído de tubérculos andinos,” Tesis de pregrado, Universidad Técnica de Ambato, Ambato, Ecuador, 2023. https://repositorio.uta.edu.ec/handle/123456789/37941
[15] F. H. Ruíz Espinoza, A. C. Rosales Nieblas, F. A. Beltrán Morales, S. Zamora Salgado, and J. G. Loya Ramírez, “Capacidad antioxidante de tomate orgánico y convencional, determinado con dos métodos fotométricos: estudio preliminar / Organic and conventional tomato antioxidant capacity, determined with two photometric methods: preliminary study,” Braz. J. Anim. Environ. Res., vol. 4, no. 3, pp. 3456–3464, Jul. 2021. https://doi.org./10.34188/bjaerv4n3-052
[16] V. Vallejo-Castillo, J. Muñoz-Mera, M. F. Pérez-Bustos, and A. Rodriguez-Stouvenel, “Recovery of antioxidants from papaya (Carica papaya L.) peel and pulp by microwave–assisted extraction,” Rev. Mex. Ingen. Quim., vol. 19, no. 1, pp. 85–98, Jun. 2020. https://doi.org/10.24275/rmiq/Alim593
[17] A. Kuri-García, A. Vargas-Madriz, A. Mendoza-Juárez, O. Roldán-Padrón, and J. Chávez-Servín, “Efecto térmico del blanqueado culinario en el perfil fenólico de ocho diferentes quelites presentes en la dieta tradicional mexicana,” Digit. Cienc. UAQ., vol. 14, no. 1, pp. 80–94, Jul. 2021. https://revistas.uaq.mx/index.php/ciencia/article/view/115
[18] N. Echegaray et al., “Total phenol content and antioxidant activity of different celta pig carcass locations as affected by the finishing diet (Chestnuts or commercial feed),” Antiox., vol. 10, no. 1, p. 5, Dec. 2020. https://doi.org/10.3390/antiox10010005
[19] C. J. Vargas Fajardo, “Determinación y cuantificación de compuestos fenólicos en flores de Taraxacum officinale, mediante HPLC-DAD-MS y ensayos colorimétricos UV-VIS,” Tesis de grado, Universidad de los Andes, Bogotá, Colombia, 2020. https://repositorio.uniandes.edu.co/entities/publication/a89b28a0-f819-47a9-86e1-e83ceca6c4f4
[20] Y. Zeng et al., “By-Products of Fruit and Vegetables: Antioxidant Properties of Extractable and Non-Extractable Phenolic Compounds,” Antiox., vol. 12, no. 2, p. 418, Feb. 2023. https://doi.org/10.3390/antiox12020418
[21] J. Tongmai, C. Chupeeruch, U. Suttisansanee, R. Chamchan, C. Khemthong, and N. On-Nom, “Development of anthocyanin-rich jelly by Thai mulberry (Morus alba) fruit powder,” Walailak Proced., vol. 2019, no. 1, Mar. 2019. https://wjst.wu.ac.th/index.php/wuresearch/article/view/6577
[22] J. De la Cruz-López, M. M. Hernández-Villegas, M. E. Aranda-Ibáñez, G. I. Bolio-López, M. A. Velázquez-Carmona, and S. Córdova-Sánchez, “Potencial nutricional y fitohelmíntico de los extractos acuosos de Tithonia diversifolia Hemsl. (Asteraceae) en pequeños rumiantes en el trópico mexicano,” Inform. Tec. Econ. Agrar., vol. 118, no.1, pp. 69-81, Mar. 2022. https://doi.org/10.12706/itea.2021.016
[23] J. A. Lopéz Santiz, “Descripción morfológica y fitoquímica de dalia variedad Yaretzi [Dahlia x hortorum (Willd.)],” Tesis de maestría, Universidad Autónoma de Chapingo, Chapingo, México, 2024. https://repositorio.chapingo.edu.mx/handle/123456789/3470
[24] L. López Salgado, and S. Torres Pacheco, “Diseño de productos funcionales derivados del fruto y la hoja del sauco,” Tesis de grado, Universidad de los Andes, Bogotá, Colombia, 2020. http://hdl.handle.net/1992/51641
[25] W. Zárate-Martínez, S. González-Morales, F. Ramírez-Godina, A. Robledo-Olivo, and A. Juárez-Maldonado, “Efecto de los ácidos fenólicos en el sistema antioxidante de plantas de tomate (Solanum lycopersicum Mill.),” Agron. Mesoamer., vol. 32, no. 3, pp. 854–868, Sep. 2021. https://doi.org/10.15517/am.v32i3.45101
[26] R. Jan, S. Asaf, M. Numan, Lubna, and K.-M. Kim, “Plant secondary metabolite biosynthesis and transcriptional regulation in response to biotic and abiotic stress conditions,” Agronomy, vol. 11, no. 5, p. 968, May. 2021. https://doi.org/10.3390/agronomy11050968
[27] V. F. Díaz Echeverría et al., “Valoración nutricional y fermentación in vitro de mezclas de follaje de árboles con harina de yuca en dietas para borregos,” Acta Univ., vol. 33, pp. 1–18, Feb. 2023. https://doi.org/10.15174/au.2023.3558
[28] R. J. Ortega-Medrano, L. F. Ceja-Torres, M. Vázquez-Sánchez, G. C. G. Martínez-Ávila, and J. R. Medina-Medrano, “Characterization of Cosmos sulphureus Cav. (Asteraceae): Phytochemical Screening, Antioxidant Activity and Chromatography Analysis,” Plants, vol. 12, no. 4, p. 896, Feb. 2023. https://doi.org/10.3390/plants12040896
[29] G. C. Gordillo Rocha, “Efecto analgésico y antiinflamatorio de la administración de Desmodium molliculum (manayupa) en el tratamiento de dismenorreas primarias,” Tesis de doctorado, Universidad Nacional Mayor de San Marcos, Lima, Perú, 2022. https://core.ac.uk/download/pdf/499734223.pdf
[30] K. Flores-Manzano, “Evaluación de contenido de taninos de cinco ecotipos de tara (Caesalpinia spinosa),” Tesis de grado, Universidad Nacional de Moquegua, Moquegua, Perú, 2022. https://alicia.concytec.gob.pe/vufind/Record/UNAM_cb0094b747fa2f0d177100b7edbe5fd4
[31] N. Iqbal, and P. Poór, “Plant Protection by Tannins Depends on Defence-Related Phytohormones,” J. Plant Growth Regul., vol. 44, no. 1, pp. 22–39, Mar. 2024. https://doi.org/10.1007/s00344-024-11291-1
[32] G. Juárez Juárez, “Actividad antioxidante de la hoja de Tithonia diversifolia (Hemls.) A. Gray,” Tesis de maestría, Institución de enseñanza e investigación en ciencias agrícolas, Montecillo, Texcoco, México, 2020. http://colposdigital.colpos.mx:8080/xmlui/handle/10521/4981
[33] J. J. Serra Bisbal, J. Melero Lloret, G. Martínez Lozano, and C. Fagoaga, “Especies vegetales como antioxidantes de alimentos,” Nereis. Interdisc. Ibero-American J. Meth., Modell. Simul., vol. 1, no. 12, pp. 71–90, May. 2020. https://doi.org/10.46583/nereis_2020.12.577
[34] R. Benjamaa et al., “Comparative evaluation of antioxidant activity, total phenolic content, anti-inflammatory, and antibacterial potential of Euphorbia-derived functional products,” Front. Pharmacol., vol. 15, Feb. 2024. https://doi.org/10.3389/fphar.2024.1345340
[35] O. N. Cabascango Molina, “Evaluación del efecto de tres métodos de secado sobre la actividad antioxidante y fenoles totales de la uvilla Physalis peruviana L,” Tesis de grado, Universidad Técnica del Norte, Ibarra, Ecuador, 2019. https://repositorio.utn.edu.ec/handle/123456789/9230
[36] G. de J. Pérez González, “Comparativo del proceso de secado y la calidad funcional del chile de agua (Capsicum annuum L.) usando un secador de charolas versus un secador solar mixto,” Tesis de grado, Universidad Tecnológica de la Mixteca, Huajapan de León, México, 2021. http://jupiter.utm.mx/~tesis_dig/14334.pdf
[37] M. S. Torres Niño, “Evaluación de la eficiencia energética y parámetros de calidad mediante el secado con ventana refractiva del betabel (Beta vulgaris),” Tesis de maestría, Instituto Tecnológico de Tuxtepec, Tuxtepec, Oaxaca, México, 2022. https://rinacional.tecnm.mx/jspui/handle/TecNM/5637
[38] N. C. Silva, A. O. Santos, C. R. Duarte, and M. A. S. Barrozo, “Refractance Window Drying as an Alternative Method for Brewer’s Spent Grain Preservation,” Appl. Biosci., vol. 3, no. 1, pp. 71–86, Feb. 2024. https://doi.org/10.3390/applbiosci3010005
[39] R. ElGamal, C.Song, A. M. Rayan, C. Liu, S. Al-Rejaie, and G. ElMasry, “Thermal Degradation of Bioactive Compounds during Drying Process of Horticultural and Agronomic Products: A Comprehensive Overview,” Agronomy, vol. 13, no. 6, p. 1580, Jun. 2023. https://doi.org/10.3390/agronomy13061580
[40] T. Belwal et al., “Effects of different drying techniques on the quality and bioactive compounds of plant-based products: a critical review on current trends,” Drying Technol., vol. 40, no. 8, pp. 1539–1561, May. 2022. https://doi.org/10.1080/07373937.2022.2068028
[41] E. Alvarez-Parrilla, F. Contreras-Muñiz, J. Rodrigo-García, L. A. De la Rosa, J. A. García-Fajardo, and J. A. Núñez-Gastélum, “Cinética de secado y efecto de la temperatura sobre las características físicas y compuestos fenólicos de chile jalapeño rojo (Capsicum annuum L.),” Biotecnia, vol. 21, no. 1, pp. 139–147, Jan. 2019. https://doi.org/10.18633/biotecnia.v21i1.877
[42] F. Navarrete Osorio, “Efecto de la temperatura del secado al vacío sobre la cinética de secado, compuestos bioactivos y actividad antioxidante de flores de fucsia (Fuchsia magellanica),” Tesis de maestría, Universidad de Chile, Santiago, Chile, 2024. https://doi.org/10.58011/w25c-h707
[43] M. D. Herrera, J. Mena-Covarrubias, A. C. Menchaca-Valdéz, N. M. Ortíz-Rodríguez, and O. García-Valladares, Calidad física y nutracéutica de chile secado por diferentes métodos, 1ra ed., Zacatecas, México: Campo Experimental Zacatecas, 2019, p. 37. http://zacatecas.inifap.gob.mx/publicaciones/secadoChile.pdf
[44] A. Quispe-Romero, G. Ticona-Tito, A. Viza-Salas, R. Quispe-Tello, and S. Cervantes-Alagón, “Capacidad antioxidante y taninos de la planta altoandina Jinchu Jinchu (Usuchjata Gistapama): Un estudio in vitro,” Rev. Acciones Méd., vol. 2, no. 3, pp. 67–75, Sep. 2023. https://doi.org/10.35622/j.ram.2023.03.005
[45] N. P. Minh, and N. M. Chanh, “Effect of varying processing methods (optimal conditions) on chemical properties of herbal leaf tea produced from ‘Voi’ (Syzygium nervosum) leaves,” Food Res., vol. 6, no. 2, pp. 191–201, Apr. 2022. https://www.myfoodresearch.com/uploads/8/4/8/5/84855864/_26__fr-2021-741_minh.pdf
[46] X. Niu et al., “Effects of Caragana korshinskii tannin on fermentation, methane emission, community of methanogens, and metabolome of rumen in sheep,” Front. Microbiol., vol. 15, p. 1334045, Feb. 2024. https://doi.org/10.3389/fmicb.2024.1334045
[47] S. M. Bermudez Guevara, and M. C. Calderón Jiménez, “Evaluación de la composición de Poli-Fenoles Totales Y Taninos condensados en las hojas de la planta Mussaenda erythrophylla para el uso como alternativa en la alimentación bovina,” Tesis de grado, Universidad de Los Llanos, Villavicencio, Colombia, 2021. https://repositorio.unillanos.edu.co/handle/001/3296
[48] P. A. Jiménez Oliver, “Efecto del tipo de secado (horno y liofilización) y la forma de preparación (crudo y hervido) en el perfil fenólico y la capacidad antioxidante de la hoja e inflorescencia de Chenopodium berlandieri,” Tesis de maestría, Universidad Autónoma de Querétaro, Querétaro, México, 2022. https://ri-ng.uaq.mx/handle/123456789/3702
[49] F. Seidi, Y. Liu, Y. Huang, H. Xiao, and D. Crespy, “Chemistry of lignin and condensed tannins as aromatic biopolymers,” Chem. Soc. Rev., vol. 54, no. 6, pp. 3140–3232, Feb. 2025. https://doi.org/10.1039/D4CS00440J
[50] G. A. Castaño-Jiménez, W. A. Barragán-Hernández, L. Mahecha-Ledesma, and J. Angulo-Arizala, “Revisión de la calidad nutricional de botón de oro y de afrecho de yuca para la producción de ensilajes en ganadería de leche,” Vet. Mex. OA, vol. 10, no. 1, pp. 1–23, Oct. 2023. https://doi.org/10.22201/fmvz.24486760e.2023.1201
[51] M. F. Madrid Mendoza et al., “Ethanolic extract from leaves of tithonia diversifolia induces apoptosis in HCT-116 cells through oxidative stress,” J. Toxicol. Environ. Health A, vol. 87, no. 7, pp. 275–293, Jan. 2024. https://doi.org/10.1080/15287394.2024.2308256
Notas
Los autores declaran que no existe ningún conflicto de intereses económicos, profesionales o personales que puedan influir de forma inapropiada en los resultados obtenidos en este artículo.
Jonathan David Granja-Cabrera: desarrollo del experimento, evaluación del diseño de experimentos, análisis de resultados y redacción del manuscrito.
Robinson Timaná: diseño de la investigación, experimentación, redacción y revisión del manuscrito.
Oswaldo Osorio Mora: experimentación, análisis bibliográfico, estructuración y revisión final del manuscrito.
Karen Paredes: desarrollo de las pruebas espectrofotométricas, análisis de resultados y redacción del manuscrito.
Notas de autor
jdgranja19A@udenar.edu.co
Información adicional
Cómo citar / How to cite: J. Granja-Cabrera, R. Timaná, O. Osorio, and K. Paredes, “Efecto del secado en la concentración de compuestos bioactivos y la actividad antioxidante de plantas forrajeras,” TecnoLógicas, vol. 28, no. 63, e3379, 2025. https://doi.org/10.22430/22565337.3379
Información adicional
redalyc-journal-id: 3442
Enlace alternativo
https://revistas.itm.edu.co/index.php/tecnologicas/article/view/3379 (html)
