Resumen:
El propósito de esta investigación fue precisar diferencias significativas en el flujo de CO. generado por microorganismos en suelos desnudos (sd), comparado con el de suelos dominados por Avicennia germinans .Ag) y Conocarpus erectus .Ce). Se realizó un trabajo de campo en la laguna de Unare, colectando 72 muestras de suelo superficial: 36 de sd, 18 de suelo con Ag y 18 de suelos de Ce. Se determinó respiración basal. Los datos obtenidos fueron tratados estadísticamente a partir de las pruebas . y .. Se reconoce que los sd produjeron 3,74 mg C-CO. g/24h, mientras que los dominados por manglar en su superficie, arrojaron 12,25 mg C-CO. g/24h; la prueba . indica una significancia de 0,01 evidenciando la diferencia significativa entre ambos grupos. Los suelos con Ag registraron 10,61 mg C-CO2 g/24h, y los dominados por Ce 13,88 mg C-CO2 g/24h. La prueba . corrobora las diferencias significativas en el flujo de CO. liberado por los tres grupos analizados.
Palabras clave:respiración basalrespiración basal,microorganismosmicroorganismos,Laguna de UnareLaguna de Unare.
Abstract: The purpose of this research was to know significant differences in CO2 flow genera- ted by microorganisms in bare soils (bs), compared to those dominated by Avicennia germinans (Ag) and Conocarpus erectus (Ce). For this purpose, a field experiment was carried out in the Unare Lagoon, 72 samples of topsoil were collected, distributed in: 36 bs, 18 Ag-soil and 18 Ce-soil; basal respiration was determined. Data obtained were treated statistically by U-test and H-test. It is recognized that bs presented an average of 3.74 mg C-CO2 g/24h, while those dominated by mangrove on its surface, without considering the dominant species, showed an average of 12.25 mg C-CO2 g/24h, U-test indicates significance of 0.01 evidencing significant difference between both sample groups. Ag-soils recorded an average of 10.61 mg C-CO2 g/24h, and soils dominated by Ce 13.88 mg C-CO2 g/24h.
Keywords: basal respiration, microorganisms, Unare Lagoon.
2.- Artículos / Papers
Flujo de CO2 en suelos dominados por manglares Avicennia germinans y Conocarpus erectus
CO2 flow in soils dominated by mangroves Avicennia germinans and Conocarpus erectus
Universidad de los Andes

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 3.0 Internacional.
Recepción: 01 Noviembre 2017
Aprobación: 01 Septiembre 2021
El estudio del CO2 en el suelo constituye un pa- rámetro útil no solamente para comprender el comportamiento de la actividad microbiológica, sino además para analizar sus posibles incidencia en algunas propiedades edáficas fundamentales para determinar la calidad de los suelos (Carter, 2002; Krebs, 2003; Palma, 2011; Guerrero et al., 2012; Bogado, 2013; Núñez, 2013, 2014; Núñez et al., 2017), su potencialidad de aprovechamiento (Carter, 2002; FAO, 2002; Verhulst et al., 2015), así como la vinculación sistémica con la atmósfera, en lo concerniente al calentamiento global (De Benito y Sombrero, s/f; Sandoval et al., 2003; Ver- hulst et al., 2015).
Peris (2013) refiere como necesario para que el almacenamiento de este gas se produzca en la estructura del suelo, la existencia de la cobertura vegetal, ya que las plantas, en su proceso fotosin- tético, captan directamente el Dióxido de carbono de la atmósfera, lo metabolizan y almacenan C en su tejido.
Otra fuente de suministro indirecto de CO2 a la estructura del suelo se vincula con la respira- ción de microorganismos edáficos, raíces, hifas micorrícicas, y en menor proporción, a la oxida- ción bioquímica de los compuestos de carbono (Lloyd y Taylor, 1994); de este modo, la actividad metabólica que realizan, fundamentalmente, los microorganismos durante el proceso de descompo- sición de la hojarasca y la materia orgánica (MO), puede ser cuantificado mediante la medición de la producción de CO2 (Alef, 1995).
Siendo, además, un parámetro proporcional a la Productividad Primaria Neta (PPN) del ecosistema, entendida como el flujo de carbono procedente de la atmósfera, presentes en las plantas verdes por unidad de tiempo determinada (Wang y Polglase, 1995); constituyendo el segundo flujo de carbono más importante en el balance global, después de la Productividad Primaria Bruta (PPB) o la energía total fijada por el proceso de fotosíntesis en las plantas (Schimel, 1995).
De allí que, investigadores como Jandl (1981), Zambrano et al. (2004), Peris (2013) entre otros, coinciden en destacar la importancia de la captura del CO2 en el suelo, ya que en la medida en que este gas invernadero es retenido en la estructura edá- fica, su disponibilidad disminuye en la atmósfera.
En efecto, se ha estimado que el C orgánico en suelos del mundo es de 1500 Pg, cerca de 2,1 veces más que en la atmósfera y cerca de 2,7 veces más que la reserva biótica que comprende a las plantas de la tierra (Neill et al., 1998). En las zonas forestales, se estima que CO2 almacenado en los suelos, representa el 36% del total del carbono a un metro de profundidad (Zambrano et al., 2004). En el caso particular de los ecosistemas de manglar, suelen ser reconocido su elevado proce- samiento de materia orgánica, por lo que tienen un alto potencial de impacto en el ciclo global de carbono (Dittmar et al., 2006).
Es oportuno destacar que el término manglar proviene de la lengua Guaraní y se traduce al es- pañol como ‘árbol retorcido’ (Comisión Nacional Forestal, 2009). Estos individuos son clasificados como formaciones halófilas arbustivas o arbóreas que crecen en superficies planas y suelos fangosos, profundos, de color oscuro, próximos a la influencia de aguas relativamente tranquilas y salinas; con raíces aéreas y respiratorias, las cuales penetran el suelo en un sistema radicular que además sirve como órgano de ventilación (Monkhouse, 1978; Font Quer, 2001).
En el caso particular del género de mangle negro, mangle prieto o Avicennia, es una especie de la familia Acanthaceae, que suelen ser reco- nocidos como árboles con raíces respiratorias o neumorrizas, las cuales crecen con geotropismo negativo: la parte que crece de manera vertical se extienden por el pantano absorbiendo oxígeno para la planta, mientras que el resto del sistema radicular se encuentra hundido en el fango en condiciones aeróbicas deficientes. Las hojas son opuestas, co- riáceas y persistentes, los pedúnculos terminales y dicotomearios, ternados y multiflorales; las flores son pequeñas de corola casi coriácea (Ronquillo, 1851; Lindorf et al., 2006). De este género, se han identificado en el mundo once (11) especies, de las cuales, como ya se mencionó, cuatro (4) han sido reportadas en el continente americano: A. bicolor, A. tonduzii, A. tomentosa y A. germinans (Unión Internacional para la Conservación de la Naturaleza y Recursos Naturales- Comisión de Ecología, 1983).
Esta última especie del género Avicennia, pre- senta glándulas de secreción salina, ubicadas la epidermis superior e inferior de la hoja, con una estructura pluricelular globosa que constituye la cabeza, así como, un pie formado por varias células colectoras. Estas son las encargadas de liberar a la planta de importantes cantidades de sal que si acumularan serían perjudiciales o letales (Lindorf et al., 2006).
En relación con el mangle Zaragoza, botoncillo o C. erectus, es una especie de la familia Combre- taceae, reconocido como un arbusto endémico de América, caracterizado por presentar múltiples troncos tortuosos, con corteza estriada de color gris oscuro. Puede encontrársele con dos variantes, distinguibles entre sí por sus hojas con presencia o no de una cubierta de tricomas. De allí que al- gunos botánicos la distinguen como una variedad taxonómica llamada Conocarpus erectus var. Seri- ceus (Trejo, 2009). Este género, también presenta glándulas secretoras de sal en ambas epidermis (Lindorf et al., 2006).
Ahora bien, las cantidades de CO2 absorbidas por el suelo como sumidero, especialmente en las zonas boscosas, pueden volver a la atmósfera si la cobertura vegetal desaparece a consecuencia de las plagas, las enfermedades, las formas de aprove- chamiento antrópico como extracción de madera o recogida de cosecha, así como los incendios fo- restales (Ministerio de Medio Ambiente y Medio Rural y Marino del gobierno de España, 2015).
Para los bosques de manglar, Armentano (1981) determinó que a principios de los años 80, en la zona intertropical, 230.000 ha de manglares habían sido convertidos en estanques piscícolas. Con esa tasa de destrucción, se estimó que después de 10 a 20 años esos depósitos habrían liberado a la atmós- fera de cuatro a nueve millones de toneladas de C. En el caso particular de Venezuela, los man- glares se ubican en el borde costero que separa tierra firme del mar, comprendiendo una exten- sión discontinua de aproximadamente 1.100 km de la línea costera, ocupando aproximadamente el 29% es ésta. Estos bosques se caracterizan por la presencia de distintas especies de manglares, entre las que destacan: Rhizophora mangle, Avicennia germinans, Laguncularia racemosa y el Conocarpus erectus (Pannier y Pannier, 1989).
Éstos han sido objeto de diversas investigacio- nes, orientadas fundamentalmente a estudiar: su estructura (De Olivares, 1988; Cumana et al., 2000; Medina y Barboza, 2003; Barboza et al., 2006, Del Mónaco et al., 2010; López et al., 2011), así como, la actividad microbiana y almacenamiento de carbono (Sánchez et al., 2010; Rodríguez y Gómez, 2016). Sin embargo, en ninguna de estas investigaciones se ha indagado sobre las potencialidades asociadas a las especies de manglar, no solamente para capturar CO2 en el suelo que ocupa, sino como hábitat que favorece el desarrollo de la microflora y microfau- na edáfica, y su consecuente producción de CO2. Desde esta perspectiva, el propósito de la pre- sente investigación fue precisar las diferencias significativas en el flujo de CO2, generado por la acción de los microorganismos edáficos en suelos desnudos así como los dominados en superficie por Avicennia germinans y Conocarpus erectus, en la laguna de Unare, Venezuela.
La laguna de Unare es un humedal, ubicado entre los 10°04’–10°08’N y 65°12’–65°75’O, en el estado An- zoátegui de Venezuela. Colinda al norte con el mar Caribe y por el sur con una planicie y una serie de colinas relativamente bajas, cuya altura máxima es de 600 metros, denominada cerro El Morro (Roa 1990), mientras que al este tiene como límite el rio Unare y al oeste con Boca de Uchire (FIGURA 1).
Esta laguna cubre una superficie aproximada de 47,5 km2 y, de acuerdo con lo referido por, Ojeda (2004) durante la estación seca, que se prolonga de diciembre a mayo, reduce su extensión hasta aproximadamente 44 km2; hacia los bordes, prin- cipalmente en sus sectores norte y oeste, las aguas llegan a retirarse hasta 2 km de la barra que las separa del mar.
Esta barra es un cordón arenoso de unos 22 km de longitud y un ancho de 200-600m, unido al continente en el oeste en Boca de Uchire, y al este en el delta del río Unare, y presenta tres bocas: Unare, La Mora y Nueva, las cuales tienden a ce- rrarse por influencia de la dinámica sedimentaria del borde costero o por construcción de vías de comunicación (Suárez, 1991).
El principal aporte de agua continental, du- rante la época de lluvia, corresponde a los ríos Cautaro, Chávez y Unare, siendo este último el que mantiene parte de su caudal en el período seco. Generalmente, el aporte de agua dulce ocu- rre en la época de lluvia, confiriendo a la laguna una condición hiposalina (Senior y Ocando, s/f). El cierre de las bocas durante buena parte del año imposibilita el ingreso del agua del mar y promueve el estancamiento de las aguas al in- terior de la laguna, lo cual es un factor que no solo contribuye con la eutrofización, sino además con la contaminación relacionada con el aumento del suministro de nutrientes provenientes de la actividad agrícola, desarrollada aguas arriba en la cuenca del río Unare (Gómez et al., 2006).
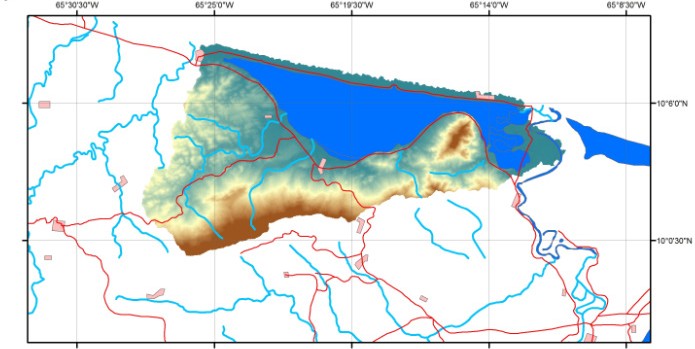
FIGURA 1.
Mapa de localización de la laguna de Unare
De acuerdo con lo referido por Marín (2000), la laguna es un centro de notoria actividad pesquera artesanal, basada en la extracción de camarones y peces, en las zonas próximas al manglar, esti- mando que entre 30.000 personas provenientes de los pueblos y caseríos ubicados en su entorno, viven directa e indirectamente de esta actividad El origen de los manglares en la zona se estima que se ubica en la década de los 70 del siglo XX por lo que, según Roa (1990), el manglar se desplazó del litoral, por acción del oleaje hacia la zona más interna de la laguna. Aun cuando, en la actualidad no se conoce la densidad del manglar en la zona, se reconoce su existencia hacia la zona norte y oeste de la laguna, desarrollados en parches de bosques abiertos o en algunos casos, individuos aislados (FIGURA 2).
Lo anterior permite suponer que se trata de un manglar joven, con una ocupación de poco menos de 5 décadas, lo cual resulta de interés para esta investigación, ya que se reconoce que éstos suelen ser mejores fijadores de carbono, en contraposición a los bosques maduros que presentan balances en el cual, la captura iguala la emisión.
La investigación, en atención a su propósito, se desarrolló en tres fases:
El trabajo de campo se llevó a cabo entre el 15 y 17 de junio de 2017, en el inicio de la estación lluviosa para la localidad, esto considerando que las precipitaciones favorecen la humedad edáfica y “un porcentaje de humedad más alto favorece la actividad de los microorganismos en el suelo” (Ramos y Zuñiga, 2008: 125), sin llegar a la anoxia genera- da por la inundación o saturación por agua de la estructura del suelo, que ocurre como consecuen- cia del extendido período lluvioso. En efecto, la inundación del suelo, como consecuencia de las precipitaciones, inhibe la actividad de enzimas como la β-D-glucosidasa y la fosfatasa, involucradas en el ciclo del carbono (Xiao-Chang y Qin, 2006) Por tratarse de un área donde los manglares crecen en una cobertura abierta o sin contacto entre el dosel de los individuos, en campo se pro- cedió a la colecta de suelo superficial (0-20 cm de profundidad) considerando: a) para zonas con presencia de A. germinans. o C. erectus, se tomó la muestra en el área más próxima a la base del individuo arbóreo, y b) para la zona desprovista de manglar, se asumió el área próxima a la del individuo muestreado en el criterio ‘a’, con una distancia no menor a 5 metros lineales, contados a partir del área cubierta por el dosel del referido individuo.

FIGURA 2.
Manglares en la laguna de Unare.
Nótese en los detalles: (A) en el centro de la imagen, el bosque de manglar con presencia de A. germinans, en cobertura dispersa, hacia el extremo inferior-derecho de la imagen el dosel de un individuo de la especie C. erectus, y al fondo, las últimas estribaciones de la serranía del Interior del sistema montañoso de la costa; (B) espécimen de A. germinans con sus características neumorrizas sobre la superficie del suelo, y (C) espécimen de C. erectus
Bajo el criterio antes descrito, se colectaron 72 muestras de suelo, distribuidas de la siguiente manera: a) 18 muestras de suelo dominados por A. germinans, b) 18 muestras de suelo dominados por C. erectus., y c) 36 muestras de suelo desnu- do o desprovisto de manglar, clasificadas en dos subgrupos, según su proximidad a un individuo de A. germinas o C. erectus.
Las muestras fueron resguardadas en bolsas de polietileno denso, identificadas con etiqueta contentiva de la siguiente información: clave única de identificación, coordenadas del punto de mues- treo, fecha y hora de la colecta. Las mismas fueron preservadas para su transporte al laboratorio, en una cava con una temperatura controlada entre 4 ºC a 6 ºC.
Para determinar el CO2 liberado, se empleó el pro- tocolo reportado por Anderson (1982), con objeto de conocer la respiración basal (RB). Para esto, las muestras de suelo conservadas a humedad de campo y cernidas en el tamiz de 2 mm, fueron pre-acondicionadas a temperatura ambiente (24°C) a fin de lograr su estabilización.
Posteriormente, se colocaron 50 g de cada muestra de suelo en frascos de vidrio color ám- bar de 500 ml de capacidad. Adicionalmente, se suspendió un trampa de álcali: frasco de vidrio color ámbar, contentivo de 5 ml de una solución de NaOH (0,1 M). Transcurridas 24 horas, se retiró la trampa de álcali, se adicionó 2 mL de BaCl2 y 2 gotas de Fenolftaleína. El CO2 absorbido fue titu- lado con HCl (0,1 M). El resultado fue expresado en: mg C-CO2 g/24 h.
También se emplearon frascos sin muestras de suelo con trampas de álcali como blancos, a fin de establecer un patrón de comparación.
Para determinar el efecto de la fuente de variación: la presencia de manglar así como la posible inci- dencia de la especie dominante, en comparación con el suelo desnudo; se realizó el análisis esta- dístico a partir del programa IBM SPSS Statistics versión 23.0.
Los datos fueron analizados mediante: a) la prueba de U de Mann-Whitney para determinar las diferencias significativas entre los grupos de muestras, al comparar el promedio de CO2 liberado, asociado a la condición de cobertura de la especie dominante: suelo sin cobertura de manglar en contraste con el suelo cubierto por cada una de las dos especies en estudio; y b) la prueba H de Kruskal-Wallis, para determinar el efecto interactivo entre las condiciones: sin manglar, dominado por Avicennia g. y dominado por C. erectus., conside- radas como parte de la investigación.
El suelo desprovisto de manglar presentó un flujo de CO2 que oscila entre 0,44 y 7,48 C-CO2 g/24 h, para un promedio de 3,74 mg C-CO2 g/24h. Los datos correspondientes a este grupo de muestra presentaron una desviación típica de 1,98; varianza de 3,92 y coeficiente de variación de 52,96%. Esto último estimador permite suponer una mediana homogeneidad entre los valores obtenidos para las unidades de análisis en este grupo de muestra (CUADRO 1).
Al contrastar los dos subgrupos de muestras de suelo sin manglar, la prueba U de Mann-Whitney, presentó un nivel de significancia de 0,34 lo que permite suponer que no existen diferencias signi- ficativas en el flujo de CO2 entre estas muestras. Es por ello que se asume que el suelo desprovisto de manglar presenta valores similares de flujo de CO2. El análisis del suelo con manglar en su superfi- cie, sin considerar la especie dominante, presentó un flujo de CO2 que oscila entre 9,24 y 15,84 C-CO2 g/24h, para un promedio de 12,25 mg C-CO2 g/24h, esto supone un incremento en la emisión de CO2 de más del 220% en contraposición al grupo de muestras de suelo sin manglar en superficie.
La desviación típica estimada para este grupo arrojó un valor de 2,11; la varianza de 4,45 y el coeficiente de variación de 17,22%, indicando que existe homogeneidad entre los valores obtenidos para las unidades de análisis en estas muestras (CUADRO 1).
El contraste entre las muestras de suelo des- provistas de manglar y aquellas que presentan al menos un individuo en su superficie, arrojó un nivel de significancia en la prueba U igual a 0,01 lo que permite afirmar que el flujo de CO2 es significativamente diferente entre ambos grupos de muestras.
En el caso específico de los suelos dominados en superficie por A. germinans registraron valores de CO2 entre 9, 24 y 11,88 mg C-CO2 g/24h, para un promedio de 10,61 mg C-CO2 g/24h, lo que repre- senta un incremento de aproximadamente 150% en comparación con el valor promedio estimado para las muestras sin manglar próximos al área ocupada por esta especie (CUADRO 1).
Este grupo de muestras arrojó valores de desviación típica y varianza de 0,99, así como un coeficiente de variación de 9,38%, lo que advierte la homogeneidad de los valores obtenidos para las unidades de análisis en este grupo (CUADRO 1). La prueba U de Mann-Whitney ratifica la po- tencialidad forestal de los suelos cubiertos con A. germinans como sumidero de CO2, en contraste con los suelos desnudos, al arrojar un nivel de significancia de 0,001.
Flujo de CO2 (mg C-CO2 g/24h) en el suelo de la laguna de Unare, según la dominancia en superficie
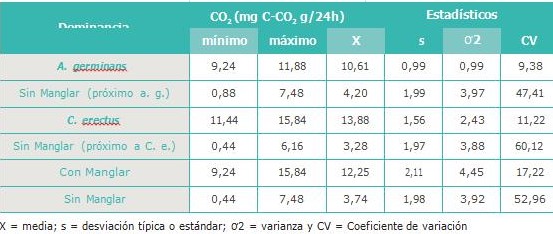
Las muestras de suelo dominado en superficie por C. erectus presentaron valores de liberación de CO2 entre 11,44 y 15,84 mg C-CO2 g/24h, para un promedio de13,88 mg C-CO2 g/24h. Lo anterior representa un incremento de, aproximadamente, 323% si se considera el valor promedio de CO2 esti- mado para las muestras de suelo sin cobertura de manglar en superficie, próximas al área ocupada por esta especie (CUADRO 1).
Este grupo de muestras arrojó una desviación típica de 1,56; varianza de 2,43 así como un coefi- ciente de variación de 11,22%, lo que advierte la homogeneidad de los valores obtenidos para las unidades de análisis (CUADRO 1).
La prueba U de Mann-Whitney ratifica la po- tencialidad forestal de los suelos cubiertos con C. erectus como sumidero de CO2, en contraste con los suelos desnudos, al arrojar un nivel de signi- ficancia de 0,010.
La prueba H de Kruskal-Wallis arrojó un valor p igual a 0,000 evidenciando que existen diferencia significativas en el CO2 liberado en los tres grupos de muestras (CUADRO 2), lo cual ratifica lo antes referido sobre la potencialidad del manglar para generar condiciones de producción y captura de este gas, pero además advierte, de una aparente superioridad del C. erectus con relación a A. ger- minans (FIGURA 3), como agente regulador de las condiciones para el flujo de CO2 del suelo.
Los resultados anteriormente expuestos eviden- cian la potencialidad forestal de los manglares, no solo para generar condiciones que favorecen la proliferación de microorganismos, y con ello la producción de CO2 asociado a su respiración, sino además, su captura en la estructura del suelo, con- virtiéndolos en verdaderos sumideros del este gas. Tal como reseña Botero (s/f), el detritus pro- veniente del manglar: las hojas y madera muerta son atacadas por bacterias, hongos y protozoarios, que la descomponen en materia orgánica más fina y finalmente las mineralizan, dejando como par- tes de sus aportes nutrientes inorgánicos y CO2 disponible en el suelo.
Si bien la referida potencialidad forestal no ha sido lo suficientemente reportada para el flujo de carbono por respiración de microflora y microfauna en suelos dominados por manglar, es importante resaltar que ha sido reconocida en otras variantes de captura de carbono para zonas de este tipo en: Florida-Estados Unidos de América (Lugo y Sne- daker, 1974), Malasia (Putz y Chan, 1986), México (Moreno et al., 2002; Sánchez et al., 2011), China ( Xiaonan er al., 2008), Panamá (Universidad de Sevilla et al., 2012; Herrera et al., 2016) entre otros. Por otra parte, a pesar que los estudios vincula- dos a las condiciones detonantes de la proliferación de microorganismos en suelos de manglar resultan escasos, son válidos los aportes generados por Reth et al. (2005), quienes determinaron correla- ciones positivas entre la temperatura del suelo y la producción de CO2 proveniente de la actividad de bacterias heterótrofas; en contraposición con lo reportado por González et al. (2006), quienes precisaron la correlación negativa entre la tem- peratura del agua y la proliferación de bacterias heterotróficas, siendo que a mayor temperatura las poblaciones de bacteria disminuían. Como se evidencia, no ha sido posible establecer tal corre- lación lineal, ya que existen otros factores como el pH o la humedad del suelo, que pueden disminuir la actividad metabólica de los microrganismos, si los valores se encuentran fuera del rango óptimo para las bacterias (Voroney, 2007).
Prueba H de Kruskal-Wallis de CO2 liberado en suelos sin manglar y suelos cubiertos por A. germinans o C. erectus
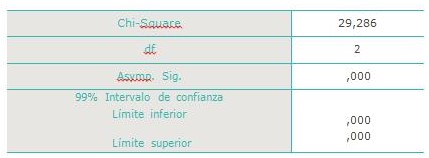
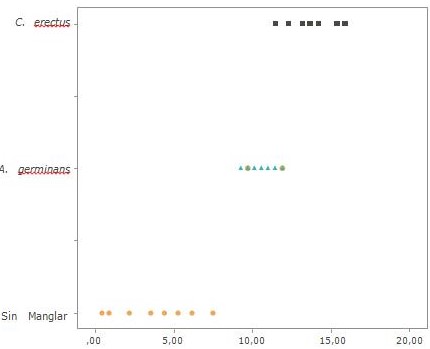
FIGURA 3.
Distribución del flujo de CO2 (mg C-CO2 g/24h) en suelos sin manglar, dominados por A. germinans o C. erectus
No obstante, el efecto sombra sobre el suelo, generado por la estructura del manglar y especí- ficamente la producida por el dosel de la planta, posiblemente propicie condiciones microclimá- ticas, caracterizadas entre otros elementos, por el leve descenso de la temperatura en su área de dominio. Ya que la planta es capaz de filtrar y ab- sorber parte de la radiación solar, reduciendo su efecto y regulando térmicamente la superficie del suelo y el agua circundante, generando en éstas las condiciones óptimas de temperatura para la proliferación de microrganismos edáficos y sus consecuentes procesos metabólicos.
Lo anterior genera, a su vez, aportes al man- glar, ya que la proliferación óptima de ciertos mi- croorganismos, en opinión de Holguin et al. (2007), contribuye mediante tres mecanismos, para que la actividad bacteriana tribute al sostenimiento de las diversas especies: a) favorecen la minera- lización de la materia orgánica bajo condiciones principalmente anaerobias y microaerofílicas. Esto, fundamentalmente, por la intervención de bacterias sulfato reductoras, cuya área de influencia se ubica en las capas anaerobias de los sedimentos de manglar; b) incrementa las tasas de fijación biológica de nitrógeno, lo que contribuyen con un 40 a 60% de los requerimientos del ecosiste- ma, y c) la presencia de bacterias de la rizósfera, brindan a la planta nutrientes y otras sustancias necesarias para su crecimiento.
La notable captura de CO2 en suelos cubiertos por A. germinas tiene efectos positivos sobre esta especie de manglar, ya que de acuerdo con lo refe- rido por Lovelock et al. (2016), contribuye con un posible aumento en la productividad del nivel de la hoja, así como en su índice del área, considerando que esto último pudiese compensar la reducción en el uso de agua por hojas individuales.
De acuerdo con Reef et al. (2015; 2016), es pro- bable que las altas concentraciones recientes de CO2, tengan un efecto positivo significativo en la tasa de crecimiento de A. germinans durante el próximo siglo, cambiando y expandiendo su nicho, especialmente en áreas donde la disponibilidad de nutrientes sea alta.
La efectividad del C. erectus para generar con- diciones que favorezcan la emisión y/o captura de CO2 en el suelo que ocupan no ha sido suficiente- mente estudiado; no obstante, El Mahrouky et al. (2014) reportan, en un estudio cuyo propósito fue reconocer el efecto de enmendar con desechos de C. erectus un suelo calcáreo arenoso, que la adición de restos de estas especie llevó a una disminución significativa en el pH del suelo, la tasa de emisión de CO2 fue mayor en los primeros días de incuba- ción que cuando este progresó; sin embargo, la emisión acumulada se incrementó de 3 a 6 veces más que la del grupo control.
La investigación permitió establecer diferencias significativas en la captura de CO2 en suelos domi- nados por manglar, en contraposición de aquellos que no evidencian la presencia de esta especie en su superficie. Siendo significativamente más alto la producción de este gas invernadero en el primero de los dos grupos de muestras referidos. Ahora bien, es importante destacar que los sue- los dominados en superficie por individuos de C. erectus emitieron significativamente más CO2 que los dominados por A. germinans.
Si bien se reconoce la efectividad de los eco- sistemas de manglar en la captura del CO2, es necesario la promoción de investigaciones vin- culadas a estudiar la correlación directa entre el almacenamiento del referido gas invernadero y las distintas especies de manglar, a fin de precisar posibles escenarios de captura del dióxido de car- bono en suelos cubiertos por manglar, así como determinar la efectividad de las especies como agentes reguladores de este elemento en el suelo.
6. Agradecimientos
La investigación fue financiada por FONDEIN-UPEL, con la aprobación de la Subdirección de Investiga- ción y Postgrado del IPC, la Coordinación General de Investigación y el Centro de Investigaciones de Estudios del Medio Físico Venezolano. Muy especialmente, agradecemos el apoyo durante el trabajo de campo y de laboratorio de los Ba- chilleres Yohana Moreno, Javier Pérez, Génesis Gómez, Gabriel Sojo, Gabriela López y Williams Castro, estudiantes del curso ‘Seminario de Inves- tigación en Geografía’ del Programa de Geografía e Historia del IPC.

FIGURA 1.
Mapa de localización de la laguna de Unare

FIGURA 2.
Manglares en la laguna de Unare.
Nótese en los detalles: (A) en el centro de la imagen, el bosque de manglar con presencia de A. germinans, en cobertura dispersa, hacia el extremo inferior-derecho de la imagen el dosel de un individuo de la especie C. erectus, y al fondo, las últimas estribaciones de la serranía del Interior del sistema montañoso de la costa; (B) espécimen de A. germinans con sus características neumorrizas sobre la superficie del suelo, y (C) espécimen de C. erectus
Flujo de CO2 (mg C-CO2 g/24h) en el suelo de la laguna de Unare, según la dominancia en superficie

Prueba H de Kruskal-Wallis de CO2 liberado en suelos sin manglar y suelos cubiertos por A. germinans o C. erectus


FIGURA 3.
Distribución del flujo de CO2 (mg C-CO2 g/24h) en suelos sin manglar, dominados por A. germinans o C. erectus
