Investigación
Evidencias biofísicas de la formación del heterómero entre el receptor de oxitocina y el receptor de serotonina 1A
Biophysical evidences for receptor heteromer formation between the oxitocin and the serotonin 1A receptors
Evidencias biofísicas de la formación del heterómero entre el receptor de oxitocina y el receptor de serotonina 1A
Investigación Clínica, vol. 58, núm. 4, pp. 352-364, 2017
Universidad del Zulia
Recepción: 03 Marzo 2017
Aprobación: 19 Octubre 2017
Resumen.: En la actualidad, tanto la formación de homodímeros y heterodímeros, así como la regulación alostérica que tiene lugar en las interacciones receptor-receptor en estas estructuras macromoleculares, representan importantes blancos terapéuticos para el tratamiento de enfermedades psiquiátricas. También, se ha descrito que la señalización celular a través del receptor de oxitocina y del receptor de serotonina 1A está relacionada con la etiología y el tratamiento de enfermedades mentales. Por ello, el objetivo de este estudio fue demostrar la formación de un heterodímero entre estos receptores. En este trabajo, se utilizaron células HeLa para la expresión transciente de los receptores marcados con fluorescencia. Los análisis de microscopia demostraron que el receptor de oxitocina y el receptor de serotonina 1A fueron capaces de colocalizar en zonas discretas de la membrana citoplasmática, lo que sugiere la formación de un heterodímero entre estas proteínas. También, los experimentos de internalización revelaron que la activación del receptor de serotonina 1A indujo la internalización específica del receptor de oxitocina, lo que sugiere una posible regulación alostérica en la interacción receptor-receptor. Los resultados obtenidos han proporcionado las primeras evidencias experimentales de la formación del heteroreceptor entre estas proteínas y de una posible modulación alostérica en la interacción receptor-receptor. Estos hallazgos se podrían convertir en un punto de partida para explorar el uso de este heteroreceptor como una nueva estrategia para el tratamiento de los trastornos de ansiedad.
Palabras clave: Receptor de oxitocina, receptor de serotonina 1A, heterómeros, heteroreceptor, heterodímero, ansiedad, depresión.
Abstract.: Currently, it is considered that both, the formation of homodimers and heterodimers and the allosteric regulation of receptor-receptor interactions within these macromolecular structures, represent important therapeutic targets for the treatment of psychiatric diseases. Also, it has been reported that cell signaling through the oxytocin receptor and the serotonin 1A receptor are related with the etiology and treatment of mental illness. Therefore, the aim of this study was to demonstrate the formation of a heterodimer between these receptors. In this work, HeLa cells were used for the transient expression of fluorescent-tagged receptors. The microscopic analysis demonstrated that the oxytocin receptor and serotonin 1A receptor were able to colocalize in discrete areas of the cytoplasmic membrane, suggesting the formation of a heterodimer containing these proteins. Additionally, internalization experiments revealed that activation of the serotonin 1A receptor induced specific internalization of the oxytocin receptor, suggesting a possible allosteric regulation in the receptor-receptor interaction. Herein, the results obtained have provided the first experimental evidences of the heteroreceptor formation between these receptors and a possible existence of allosteric modulation in the receptor-receptor interaction. These findings could become a starting point for exploring the use of this heteroreceptor as a new strategy for the treatment of anxiety disorders.
Keywords: Oxytocin receptor, serotonin 1A receptor, heteromer, heteroreceptor, anxiety, depression.
INTRODUCCIÓN
La Organización Mundial de la Salud ha informado que cada año más de 300 millones de personas en todo el mundo experimentan episodios de ansiedad, y que entre el 10 y el 15% de la población global ha experimentado algún tipo de trastorno de ansiedad durante su vida (1).
Estudios recientes han demostrado que la oxitocina desempeña un papel importante en la fisiología y la fisiopatología de la ansiedad (2). Existen evidencias experimentales que muestran que la administración de oxitocina en animales de experimentación tiene efecto ansiolítico (3) y suprime el estrés inducido por la corticosterona (4). Además, ratones “knock-out” para el receptor de oxitocina (OxTR) al ser sometidos a factores estresantes exhiben un comportamiento similar a la ansiedad y un incremento en el nivel de corticosterona (5). Por el contrario, la sobreexpresión de OxTR en la amígdala de ratas reduce la ansiedad (6).
También, se ha descrito que el sistema serotoninérgico (5-HT), y en especial el receptor de serotonina 1A (5-HT1AR) juega un papel relevante en la etiología y el tratamiento de enfermedades mentales (7-9). La depleción del sistema 5-HT, similar a los niveles reportados en pacientes con trastornos emocionales, incrementa la expresión de receptores de glutamato y mejora la actividad glutamatérgica en el núcleo lateral de la amígdala lo que conduce a potenciar el miedo y la ansiedad (10).
Se ha señalado que los mecanismos moleculares de respuesta a la ansiedad son complejos y podrían involucrar la interacción de varios sistemas de neurotransmisores. Los novedosos trabajos de Fuxe y col. han demostrado in vitro y ex vivo que los receptores no solo se encuentran en la superficie de las células en forma de monómeros sino que pueden formar dímeros (homodímeros y heterodímeros) e incluso establecer mosaicos de interacciones (interacción entre más de dos receptores) (11-14). De hecho, se ha llegado a describir que estas estructuras macromoleculares se pueden formar en el retículo endoplasmático durante la síntesis proteica (15, 16). Se ha subrayado que la existencia de heterómeros y de regulación alostérica en la interacción receptor-receptor dentro de estos complejos multiproteicos, incrementan notablemente la diversidad de reconocimiento, tráfico y señalización mediada por los receptores de membrana (12, 13). En este sentido, se conoce que el OxTR forma un heterodímero con el receptor dopamina D2 (17), un receptor implicado en diversos desórdenes neuropsiquiátricos (18), y que el neuropéptido oxitocina a través de una regulación alostérica positiva en la interacción receptor-receptor, incrementa la señalización dopaminérgica (17).
Resulta interesante que la administración de 3,4-metilendioximetanfetamina (MDMA) eleva los niveles plasmáticos de oxitocina en ratas y que este incremento pueda ser bloqueado por un antagonista específico de 5-HT1AR (19). Este mismo estudio, reveló que al administrar un agonista específico de 5-HT1AR (8-OH-DPAT), las ratas manifestaron un comportamiento social similar al obtenido con el tratamiento con MDMA (19).
Dado que el incremento de los niveles plasmáticos de oxitocina inducido por MDMA y 8-OH-DPAT parece estar asociado con el 5-HT1AR y la importancia del OxTR para la fisiopatología de la ansiedad y su tratamiento, el objetivo este trabajo ha sido estudiar si estos receptores pueden formar un heterómero y si existe regulación alostérica dentro de la interacción receptor-receptor.
MATERIALES Y MÉTODOS
Cultivo celular y transfección de las células HeLa
Las células HeLa (ATCC®CCL-2™), (cedidas por la Dra. Mileidys Pérez Alea del Instituto de Investigación Vall d’Hebron, Barcelona, España), fueron cultivadas sobre cubreobjetos en placas de 6 pocillos (1x105 células/pocillo), en medio DMEM suplementado con 2 mM L-glutamina, 100 U/mL penicilina, 100 µg/mL estreptomicina y 10% (v/v) de suero fetal bovino (FBS) a 37oC en una atmósfera húmeda de 5% de CO2-95% aire. Todos los reactivos utilizados para los cultivos, subcultivos y transfecciones de las células HeLa fueron adquiridos de Thermo Fisher Scientific (EE. UU).
Como marcaje de los receptores a estudiar se empleó la proteína verde fluorescente (GFP) para el OxTR y la proteína amarillo fluorescente (YFP) para el 5-HT1AR. Los plásmidos pcMV6-OxTR-GFP y pcDNA3.1-5-HT1AR-YFP que codifican para los receptores de interés marcados con las correspondientes proteínas fluorescentes, fueron proporcionados por el Dr. Dasiel Oscar Borroto-Escuela del Karolinska Institutet, Suecia.
Las células se transfectaron de forma individual (1 µg total de ADN) o se co-transfectaron (2 µg totales de ADN) con los plásmidos pcMV6-OxTR-GFP y pcDNA3.1-5-HT1AR-YFP por el método de la Lipofectamina™2000 (Thermo Fisher Scientific, EE.UU) (relación 1:1) según lo recomendado por la casa comercial.
Ensayos de colocalización e internalización
A las 48 horas de las transfecciones se analizaron las expresiones transcientes de las proteínas fluorescentes. Las células HeLa, que expresaban de forma individual el OxTR-GFP o el 5-HT1AR-YFP, y que co-expresaban el OxTR-GFP y el 5-HT1AR-YFP, fueron lavadas, fijadas y montadas sobre portaobjetos. Para la tinción de los núcleos se utilizó un medio de montaje con DAPI (Thermo Fisher Scientific, EE.UU). Para la obtención de las imágenes de las expresiones individuales y dobles se empleó un microscopio de fluorescencia Leica DMi8 (Leica Microsystems, Alemania).
Para los ensayos de internalización las células en crecimiento que co-expresaban el OxTR-GFP y el 5-HT1AR-YFP fueron tratadas con 10 nM de 8-OH-DPAT (Santa Cruz Biotechnology, EE.UU) por 5 minutos a temperatura ambiente. Luego, las células fueron lavadas, fijadas, montadas sobre portaobjetos y visualizadas a través de un microscopio de fluorescencia como se ha descrito anteriormente. Como control se utilizaron células en crecimiento que expresaban de forma individual el OxTR-GFP o el 5-HT1AR-YFP y células que co-expresaban el OxTR-GFP y el 5-HT1AR sin marca fluorescente. Estas células fueron incubadas con 10 nM de 8-OH-DPAT por 5 minutos a temperatura ambiente y se procedió como se ha descrito anteriormente.
RESULTADOS
Los resultados obtenidos muestran la correcta expresión transciente e independiente del OxTR marcado con proteína fluorescente GFP (verde) y del 5-HT1AR marcado con proteína fluorescente YFP (rojo) (Fig. 1), y revelan que, a las 48 horas después de las transfecciones, una considerable porción de los receptores se localizó en la membrana citoplasmática de las células HeLa (B y 1D). Se debe señalar que en las transfecciones con más de 2 µg totales de ADN se encontró que una considerable señal fluorescente se localizó en el citoplasma celular. También, se halló que las relaciones ADN/ Lipofectamina superiores a 1:3 produjeron una considerable muerte celular. En algunos experimentos se observó una notable señal fluorescente en el citoplasma de las células (Fig. 1D).
Los resultados de las superposiciones de los espectros de emisión de los fluoróforos en las células HeLa que co-expresaron el 5-HT1AR-YFP (Fig. 2A) y el OxTR-GFP (Fig. 2B) indicaron que las proteínas marcadas con fluorescencia fueron capaces de colocalizar en zonas discretas de la membrana citoplasmática (Fig. 2C). La formación de zonas de color amarillo producto de la superposición de los espectros de emisión del OxTR marcado con la proteína fluorescente GFP (verde) con el 5-HT1AR marcado con proteína fluorescente YFP (rojo) podría sugerir la formación del heteroreceptor OxTR/5-HT1AR. Los resultados de los experimentos de internalización realizados para explorar la posible regulación alostérica producto de la interacción receptor-receptor dentro del heteroreceptor OxTR/5-HT1AR, han sugerido que existe una modulación alostérica ya que la activación del 5-HT1AR indujo la internalización del OxTR.
La especificidad de la internalización obtenida se analizó en células que expresaban solo el OxTR-GFP o solo el 5-HT1AR-YFP tratadas con el agonista específico del 5-HT1AR (Fig. 3). Los resultados demostraron que el agonista promovió de manera específica la formación de vesículas de internalización del 5-HT1AR-YFP (Figs. 3B y 3C), sin embargo, no causó la internalización del OxTR-GFP en células que solo expresaban el receptor de oxitocina (Figs. 3E y 3F).
También, la señal no específica, producto del espectro de emisión de los marcadores fluorescentes seleccionados, se evaluó en células que co-expresaban ambos receptores, con la particularidad que solo el OxTR-GFP estuvo marcado con fluorescencia. Estas células fueron tratadas con el agonista específico del 5-HT1AR y se comprobó la internalización del OxTR-GFP (Fig. 4). Los resultados revelaron que no hubo señal no especifica producto de las limitaciones de la técnica empleada y que el agonista condujo a la formación de los endosomas de internalización del OxTR-GFP que al parecer estaban formando parte del heterodímero OxTR-GFP/5-HT1AR, y que se observaron en verde/amarillo por la ausencia de marcaje fluorescente del receptor de serotonina5-HT1AR (Figs. 4A y 4B). En estos mismos experimentos, se observó que una porción considerable del OxTR-GFP no internalizó y se mantuvo localizada en la membrana celular (Fig. 4B).
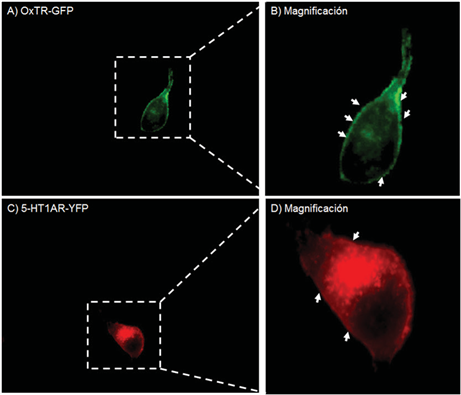
Fig.1.
Expresión de los receptores marcados con proteínas fluorescente en la membrana citoplasmática de células HeLa. A) Expresión transciente del OxTR marcado con GFP. B) Magnificación de A, las fechas indican la expresión del OxTR en la membrana citoplasmática (verde). C) Expresión transciente del 5-HT1AR marcado con YFP. D) Magnificación de C, las fechas indican la expresión del 5-HT1AR en la membrana citoplasmática (rojo). Las imágenes son representativas de tres experimentos realizados de forma independiente. Las imágenes fueron adquiridas en un solo plano z
Finalmente, los resultados obtenidos en células que co-expresaban el OxTR marcado con proteína fluorescente GFP y el 5-HT1AR marcado con proteína fluorescente YFP tratadas con el agonista del receptor de serotonina mostró diferentes posibilidades de la señal fluorescente (Fig. 5). Se observó la formación de los endosomas de co-internalización de OxTR-GFP y el 5-HT1AR-YFP (Figs. 5C y 5D). También, se encontró solo vesículas de color rojo producto de la internalización del 5-HT1AR-YFP (Figs. 5C y 5D). Además, se halló una parte del OxTR-GFP no se localizó en las vesículas de internalización y permaneció en la superficie celular (Figs. 5C y 5D).
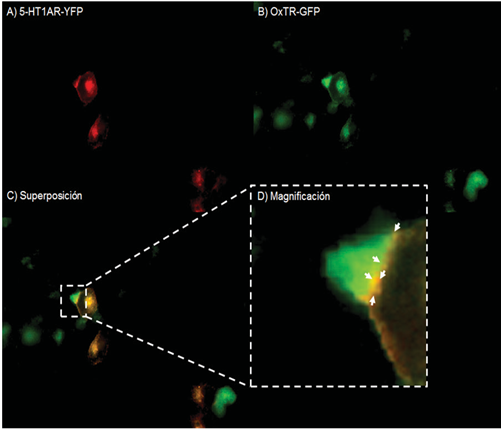
Fig.2.
Colocalización de los receptores de oxitocina y los receptores de serotonina 5-HT1A en la superficie de células HeLa. A) Expresión transciente del 5-HT1AR marcado con YFP (rojo). B) Expresión transciente del OxTR marcado con GFP (verde). C) Superposición de los espectros de emisión de GFP y YFP. D) Magnificación de C, las flechas indican las regiones específicas de la membrana citoplasmática donde colocaliza la señal fluorescente (amarillo) de OxTR-GFP y 5-HT1AR-YFP. Las imágenes son representativas de tres experimentos realizados de forma independiente. Todas las imágenes fueron adquiridas en un solo plano z.
DISCUSIÓN
Los inhibidores de la recaptación de serotonina, son uno de los ansiolíticos y antidepresivos más prescritos a nivel mundial. El efecto terapéutico de la mayoría de estos medicamentos como la fluoxetina y la buspirona (20, 21), es inhibir la recaptación de serotonina presináptica, lo que podría incrementar en alguna medida, la neurotransmisión serotoninérgica a través de los 5-HT1AR postsinápticos; por ejemplo, los localizados en las dendritas de las neuronas glutamatérgicas del hipocampo (22, 23). Sin embargo, se ha cuestionado el uso de estos compuestos por sus numerosos efectos secundarios y la demora de su acción antidepresiva, lo que provoca el abandono del tratamiento por los pacientes (24-26).
Por lo anterior, ha sido necesario explorar y establecer nuevas estrategias para el tratamiento de los trastornos de ansiedad y depresión. En este sentido, se ha subrayado que tanto la formación de homodímeros y heterodímeros como la regulación alostérica que tiene lugar en la interacción receptor-receptor abren una nueva visión para comprender la fisiología y fisiopatología de estos trastornos mentales (12, 27). De hecho, en la actualidad los heteroreceptores representan importantes dianas terapéuticas para el tratamiento de estas patologías (13, 27, 28).
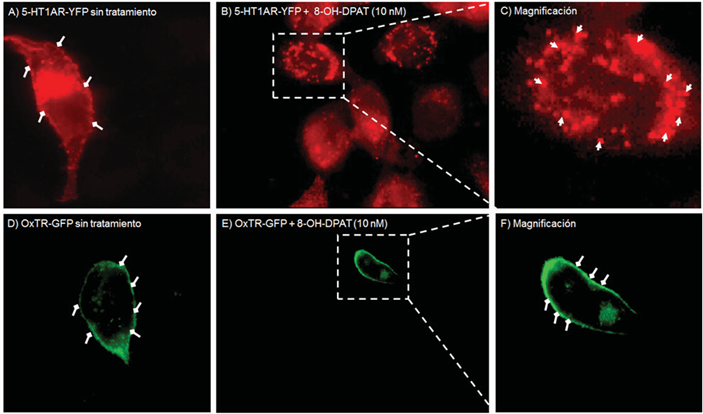
Fig.3.
El agonista del receptor de serotonina induce la internalización del 5-HT1AR, pero no del OxTR, en células HeLa que expresan de forma independiente estos receptores. A) Expresión del 5-HT1AR-YFP en la membrana celular de células sin tratamiento (flechas con terminación cuadrada). B) El agonista indujo la internalización del 5-HT1AR-YFP en células que solo expresan 5-HT1AR-YFP. C) Magnificación de B, las flechas con terminación triangular indican la formación de los endosomas de internalización del 5-HT1AR-YFP. D) Expresión del OxTR-GFP en la membrana celular de células sin tratamiento (flechas con terminación cuadrada). E) El agonista no provocó la internalización del OxTR-GFP en células que solo expresan OxTR-GFP. F) Magnificación de E, las flechas con terminación cuadrada indican la localización del OxTR-GFP en la membrana celular. Todas las imágenes son representativas de tres experimentos realizados de forma independiente. Todas las imágenes fueron adquiridas en un solo plano z.
Este trabajo ha proporcionado las primeras evidencias que demuestran una interacción física entre el OxTR y el 5-HT1AR, lo que sugiere la formación del heteroreceptor OxTR/5-HT1AR. Ha quedado demostrado que el OxTR-GFP y el 5-HT1A-YFP co-expresados de forma transciente en células HeLa, colocalizan en regiones discretas de la membrana citoplasmática, lo que podría confirmar la capacidad del receptor de oxitocina de establecer heterodímeros con otros miembros de la familia A de receptores de membrana acoplados a proteínas G, tales como el receptor de dopamina D2 (17), vasopresina (29), alfa-adrenérgico (30) o el receptor beta-adrenérgico (31). Sin embargo, se ha descrito que el OxTR es incapaz de formar estas complejas estructuras con el receptor de bradiquinina (32). Incrementar el conocimiento sobre la capacidad diferencial de formar heterómeros por parte del receptor de oxitocina sin duda será relevante a la hora de proponer su uso para el tratamiento de patologías mentales.
Numerosos estudios han confirmado que existe regulación alostérica dentro de los heteroreceptores, donde uno de los protómeros puede modular el reconocimiento y la señalización del otro protómero (23, 33, 34). Los hallazgos obtenidos en este estudio muestran que el tratamiento con el agonista del 5-HT1AR induce la internalización específica del OxTR, lo que sugiere que existe una regulación alostérica en la interacción proteína-proteína dentro el heteroreceptor OxTR/5-HT1AR.
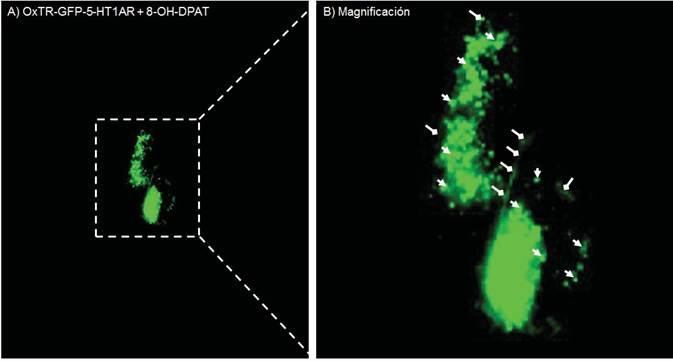
Fig.4.
Una porción del OxTR-GFP expresado en la membrana celular no internaliza con el receptor de serotonina 5-HT1AR. A) Células HeLa expresando el OxTR-GFP y el 5-HT1AR sin marca fluorescente tratadas con el agonista de 5-HT1AR. B) Magnificación de A, las fechas con terminación triangular indican la formación de los endosomas de internalización del heterodímero OxTR-GFP/5-HT1AR y las flechas con terminación cuadrada indican la porción de OxTR-GFP que permaneció ubicado en la membrana citoplasmática. Todas las imágenes son representativas de tres experimentos realizados de forma independiente. Todas las imágenes fueron adquiridas en un solo plano z.
Aunque en este trabajo se han aportado las primeras evidencias que sugieren la formación del heteroreceptor OxTR/5-HT1AR se debe tener en cuenta las limitaciones de la técnica empleada. Una porción de la colocalización podría deberse a la cercanía del espectro de emisión de los fluoruros utilizados. Sin embargo, en todos los experimentos realizados se comprobó que no existe un cien por ciento de colocalización. En algunos ensayos se observó que en las células HeLa que expresaban OxTR-GFP/5-HT1AR-YFP tratadas con el agonista de 5-HT1AR, una porción del OxTR-GFP se mantuvo en la membrana citoplasmática. Al parecer esta fracción de OxTR no interactuó con el 5-HT1AR-YFP y podría corresponder a receptores que se encontraban en forma de entidades individuales (monómeros), formando homodímeros o heteroreceptores con otras proteínas de la membrana celular. Estas evidencias podrían confirmar que parte de la colocalización obtenida ha sido específica, producto de la interacción proteína-proteína entre estos receptores.
Sin embargo, será imprescindible emplear otras técnicas como transferencia de energía de fluorescencia de Förster, transferencia de energía de bioluminiscencia, co-inmunoprecipitación y ensayos de proximidad de ligando para corroborar la formación del heteroreceptor OxTR/5-HT1AR. De igual forma, será necesario evaluar la señalización a través de segundos mensajeros para confirmar la naturaleza de la modulación alostérica que tiene lugar en este heterodímero.
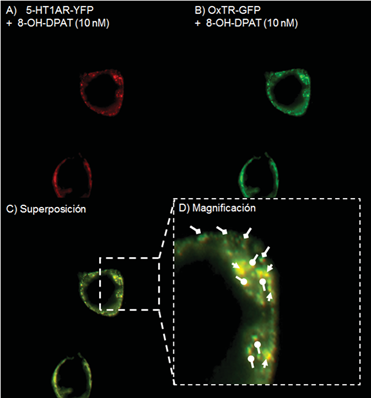
Fig.5.
La internalización de OxTR-GFP en células HeLa que co-expresan ambos receptores inducida por el tratamiento con el agonista del receptor de serotonina 5-HT1AR, es específica a la formación del heterodímero. A y B) Células HeLa que expresan el OxTR-GFP y el 5-HT1AR-YFP tratadas con el agonista de 5-HT1AR. C) Superposición de los espectros de fluorescencia de GFP y YFP. D) Magnificación de C, las flechas con terminación triangular indican la formación de los endosomas de co-internalización de color amarillo, producto de la superposición de la fluorescencia del OxTR-GFP (verde) y el 5-HT1AR-YFP (rojo), las flechas con terminación circular indican los endosomas de internalización del 5-HT1AR-YFP (rojo) y las flechas con terminación cuadrada indican el OxTR-GFP (verde) localizado en la membrana celular (verde).Todas las imágenes son representativas de tres experimentos realizados de forma independiente. Todas las imágenes fueron adquiridas en un solo plano z.
Varias investigaciones han confirmado que el OxTR y el 5-HT1AR, de forma individual, juegan un papel crítico en la fisiología y fisiopatología de la ansiedad, por lo que, los resultados que demuestran la formación del heterodímero entre estas dos proteínas y de regulación alostérica en la interacción receptor-receptor resultan novedosos y se podrían convertir en un punto de partida para continuar los estudios dirigidos a explorar el uso de este heteroreceptor en el tratamiento de los trastornos de ansiedad.
Por ejemplo, se ha demostrado que el receptor 1 del factor de crecimiento de fibroblastos es capaz de formar homodímeros (35) y heterodímeros (23). Se ha encontrado que el heteroreceptor FGFR1/5-HT1AR está involucrado en la regulación de la neuroplasticidad del hipocampo de ratas (23) y que la administración aguda de los agonistas FGF-2 y 8-OH-DPAT de los receptores de FGFR1 y 5-HT1A respectivamente, producen un efecto antidepresivo sinérgico en animales de experimentación (23). De esta misma forma, podría ser interesante valorar si un co-tratamiento con los agonistas del OxTR y el 5-HT1AR tiene un efecto antidepresivo similar al encontrado con la activación simultánea de los protómeros del heteroreceptor FGFR1/5-HT1AR, y comparar su rapidez y eficacia con respecto a un tratamiento con los inhibidores de recaptación de serotonina.
Otro aspecto que se deriva de este trabajo, consiste que en los últimos años se ha discutido sobre el uso de compuestos bivalentes que activen o inhiban a uno o a ambos protómeros dentro de un heteroreceptor y que de esta forma regulen la actividad del otro protómero en función de la regulación alostérica de la interacción receptor-receptor (27, 36, 37), por lo que sería interesante estudiar la señalización celular inducida por un compuesto bivalente que de forma sinérgica active ambos protómeros en el heteroreceptor OxTR/5-HT1AR y comparar esta señalización con los efectos ansiolíticos regulados por la acción individual de los receptores de oxitocina y serotonina 1A. También, sería interesante explorar si existe una capacidad diferencial de los receptores de oxitocina de interactuar con los diferentes miembros de la familia de los receptores serotoninérgicos.
Sin duda, los resultados obtenidos en el presente estudio podrían dirigir la atención al heteroreceptor OxTR/5-HT1AR y exhortar a incrementar los estudios enfocados en la interacción receptor-receptor para su posible uso como diana terapéutica en el desarrollo de nuevos tratamientos de los trastornos de ansiedad.
AGRADECIMIENTOS
Este trabajo ha sido financiado por la Universidad Técnica de Ambato (Resoluciones 1243-CU-P-2014, 0912-CU-P-2016 y 0932-CU-P-2016) y el Programa “Becas Prometeo” de la Secretaria de Educación Superior, Ciencia, Tecnología e Innovación del Gobierno de Ecuador para Wilber Romero-Fernandez. Los autores agradecen al Dr. Dasiel Oscar Borroto Escuela por ceder los plásmidos empleados y a la Dra. Mileidys Pérez Alea por proporcionar las células HeLa.
REFERENCIAS
1. Wittchen HU, Jacobi F, Rehm J, Gustavsson A, Svensson M, Jonsson B, Olesen J, Allgulander C, Alonso J, Faravelli C, Fratiglioni L, Jennum P, Lieb R, Maercker A, van Os J, Preisig M, Salvador-Carulla L, Simon R, Steinhausen HC. The size and burden of mental disorders and other disorders of the brain in Europe 2010. Eur Neuropsychopharmacol 2011; 21(9): 655-679.
2. Neumann ID. Brain oxytocin: a key regulator of emotional and social behaviours in both females and males. J Neuroendocrinol 2008; 20(6): 858-865.
3. Ring RH, Malberg JE, Potestio L, Ping J, Boikess S, Luo B, Schechter LE, Rizzo S, Rahman Z, Rosenzweig-Lipson S. Anxiolytic-like activity of oxytocin in male mice: behavioral and autonomic evidence, therapeutic implications. Psychopharmacology 2006; 185(2): 218-225.
4. Windle RJ, Shanks N, Lightman SL, Ingram CD. Central oxytocin administration reduces stress-induced corticosterone release and anxiety behavior in rats. Endocrinology 1997; 138(7): 2829-2834.
5. Amico JA, Mantella RC, Vollmer RR, Li X. Anxiety and stress responses in female oxytocin deficient mice. J Neuroendocrinol 2004; 16(4): 319-324.
6. Bosch OJ W, M, Nair HP, Hermanth PJ, Young LJ, Neumann ID. Viral-vector mediated expression of oxytocin receptors in the amygdala of vorgin rats increases aggression and reduces anxiety. Front Neuroendocrinol 2006; 27: 124-1215.
7. Dawson LA, Watson JM. Vilazodone: a 5-HT1A receptor agonist/serotonin transporter inhibitor for the treatment of affective disorders. CNS Neurosci Ther 2009; 15(2): 107-117.
8. Harvey BH, Naciti C, Brand L, Stein DJ. Serotonin and stress: protective or malevolent actions in the biobehavioral response to repeated trauma? Ann N Y Acad Sci 2004; 1032: 267-272.
9. Savitz J, Lucki I, Drevets WC. 5-HT(1A) receptor function in major depressive disorder. Prog Neurobiol 2009; 88(1): 17-31.
10. Tran L, Lasher BK, Young KA, Keele NB. Depletion of serotonin in the basolateral amygdala elevates glutamate receptors and facilitates fear-potentiated startle. Transl Psychiatry 2013; 3: e298.
11. Fuxe K, Dahlstrom A, Hoistad M, Marcellino D, Jansson A, Rivera A, Diaz-Cabiale Z, Jacobsen K, Tinner-Staines B, Hagman B, Leo G, Staines W, Guidolin D, Kehr J, Genedani S, Belluardo N, Agnati LF. From the Golgi-Cajal mapping to the transmitter-based characterization of the neuronal networks leading to two modes of brain communication: wiring and volume transmission. Brain Res Rev 2007; 55(1): 17-54.
12. Fuxe K, Borroto-Escuela DO, Marcellino D, Romero-Fernandez W, Frankowska M, Guidolin D, Filip M, Ferraro L, Woods AS, Tarakanov A, Ciruela F, Agnati LF, Tanganelli S. GPCR heteromers and their allosteric receptor-receptor interactions. Curr Med Chem 2012; 19(3): 356-363.
13. Fuxe K, Borroto-Escuela DO, Romero-Fernandez W, Palkovits M, Tarakanov AO, Ciruela F, Agnati LF. Moonlighting proteins and protein-protein interactions as neurotherapeutic targets in the G protein-coupled receptor field. Neuropsychopharmacology 2014; 39(1): 131-155.
14. Borroto-Escuela DO, Brito I, Romero-Fernandez W, Di Palma M, Oflijan J, Skieterska K, Duchou J, Van Craenenbroeck K, Suarez-Boomgaard D, Rivera A, Guidolin D, Agnati LF, Fuxe K. The G protein-coupled receptor heterodimer network (GPCR-HetNet) and its hub components. Int J Mol Sci 2014; 15(5): 8570-8590.
15. Van Craenenbroeck K, Borroto-Escuela DO, Romero-Fernandez W, Skieterska K, Rondou P, Lintermans B, Vanhoenacker P, Fuxe K, Ciruela F, Haegeman G. Dopamine D4 receptor oligomerization--contribution to receptor biogenesis. FEBS J 2011; 278(8): 1333-1344.
16. Van Craenenbroeck K, Borroto-Escuela DO, Skieterska K, Duchou J, Romero-Fernandez W, Fuxe K. Role of dimerization in dopamine D(4) receptor biogenesis. Curr Protein Pept Sci 2014; 15(7): 659-665.
17. Romero-Fernandez W, Borroto-Escuela DO, Agnati LF, Fuxe K. Evidence for the existence of dopamine D2-oxytocin receptor heteromers in the ventral and dorsal striatum with facilitatory receptor-receptor interactions. Mol Psychiatry 2013; 18(8): 849-850.
18. Fuxe K, Borroto-Escuela DO, Tarakanov AO, Romero-Fernandez W, Ferraro L, Tanganelli S, Perez-Alea M, Di Palma M, Agnati LF. Dopamine D2 heteroreceptor complexes and their receptor-receptor interactions in ventral striatum: novel targets for antipsychotic drugs. Prog Brain Res 2014; 211: 113-139.
19. Thompson MR, Callaghan PD, Hunt GE, Cornish JL, McGregor IS. A role for oxytocin and 5-HT(1A) receptors in the prosocial effects of 3,4 methylenedioxymethamphetamine (“ecstasy”). Neuroscience 2007; 146(2): 509-514.
20. Wong DT, Bymaster FP, Engleman EA. Prozac (fluoxetine, Lilly 110140), the first selective serotonin uptake inhibitor and an antidepressant drug: twenty years since its first publication. Life Sci 1995; 57(5): 411-441.
21. Robinson DS, Rickels K, Feighner J, Fabre Lf, Jr., Gammans RE, Shrotriya RC, Alms DR, Andary JJ, Messina ME. Clinical effects of the 5-HT1A partial agonists in depression: a composite analysis of buspirone in the treatment of depression. J Clin Psychopharmacol 1990; 10(3 Suppl): 67S-76S.
22. Riad M, Zimmer L, Rbah L, Watkins KC, Hamon M, Descarries L. Acute treatment with the antidepressant fluoxetine internalizes 5-HT1A autoreceptors and reduces the in vivo binding of the PET radioligand [18F]MPPF in the nucleus raphe dorsalis of rat. J Neurosci 2004; 24(23): 5420-5426.
23. Borroto-Escuela DO, Romero-Fernandez W, Mudo G, Perez-Alea M, Ciruela F, Tarakanov AO, Narvaez M, Di Liberto V, Agnati LF, Belluardo N, Fuxe K. Fibroblast growth factor receptor 1-5-hydroxytryptamine 1A heteroreceptor complexes and their enhancement of hippocampal plasticity. Biol Psychiatry 2012; 71(1): 84-91.
24. Fournier JC, Derubeis RJ, Hollon SD, Dimidjian S, Amsterdam JD, Shelton RC, Fawcett J. Antidepressant drug effects and depression severity: a patient-level meta-analysis. JAMA 2010; 303(1): 47-53.
25. Segraves RT, Balon R. Antidepressant-induced sexual dysfunction in men. Pharmacol Biochem Behav 2014; 121: 132-137.
26. Taylor MJ, Freemantle N, Geddes JR, Bhagwagar Z. Early onset of selective serotonin reuptake inhibitor antidepressant action: systematic review and meta-analysis. Arch Gen Psychiatry 2006; 63(11): 1217-1223.
27. Tena-Campos M, Ramon E, Rivera D, Borroto-Escuela DO, Romero-Fernandez W, Fuxe K, Garriga P. G-protein-coupled receptors oligomerization: emerging signaling units and new opportunities for drug design. Curr Protein Pept Sci 2014; 15(7): 648-658.
28. Fuxe K, Marcellino D, Borroto-Escuela DO, Frankowska M, Ferraro L, Guidolin D, Ciruela F, Agnati LF. The changing world of G protein-coupled receptors: from monomers to dimers and receptor mosaics with allosteric receptor-receptor interactions. J Recept Signal Transduct Res 2010; 30(5): 272-283.
29. Terrillon S, Durroux T, Mouillac B, Breit A, Ayoub MA, Taulan M, Jockers R, Barberis C, Bouvier M. Oxytocin and vasopressin V1a and V2 receptors form constitutive homo- and heterodimers during biosynthesis. Mol Endocrinol 2003; 17(4): 677-691.
30. Diaz-Cabiale Z, Petersson M, Narvaez JA, Uvnas-Moberg K, Fuxe K. Systemic oxytocin treatment modulates alpha 2-adrenoceptors in telencephalic and diencephalic regions of the rat. Brain Res 2000; 887(2): 421-425.
31. Wrzal PK, Devost D, Petrin D, Goupil E, Iorio-Morin C, Laporte SA, Zingg HH, Hebert TE. Allosteric interactions between the oxytocin receptor and the beta2-adrenergic receptor in the modulation of ERK1/2 activation are mediated by heterodimerization. Cell Signal 2012; 24(1): 342-350.
32. Devost D, Zingg HH. Homo- and hetero-dimeric complex formations of the human oxytocin receptor. J Neuroendocrinol 2004; 16(4): 372-377.
32. Borroto-Escuela DO, Romero-Fernandez W, Tarakanov AO, Marcellino D, Ciruela F, Agnati LF, Fuxe K. Dopamine D2 and 5-hydroxytryptamine 5-HT((2)A) receptors assemble into functionally interacting heteromers. Biochem Biophys Res Commun 2010; 401(4): 605-610.
33. Borroto-Escuela DO, Ravani A, Tarakanov AO, Brito I, Narvaez M, Romero-Fernandez W, Corrales F, Agnati LF, Tanganelli S, Ferraro L, Fuxe K. Dopamine D2 receptor signaling dynamics of dopamine D2-neurotensin 1 receptor heteromers. Biochem Biophys Res Commun 2013; 435(1): 140-146.
34. Romero-Fernandez W, Borroto-Escuela DO, Tarakanov AO, Mudo G, Narvaez M, Perez-Alea M, Agnati LF, Ciruela F, Belluardo N, Fuxe K. Agonist-induced formation of FGFR1 homodimers and signaling differ among members of the FGF family. Biochem Biophys Res Commun 2011; 409(4): 764-768.
35. Daniels DJ, Kulkarni A, Xie Z, Bhushan RG, Portoghese PS. A bivalent ligand (KDAN-18) containing delta-antagonist and kappa-agonist pharmacophores bridges delta2 and kappa1 opioid receptor phenotypes. J Med Chem 2005; 48(6): 1713-1716.
36. Le Naour M, Akgun E, Yekkirala A, Lunzer MM, Powers MD, Kalyuzhny AE, Portoghese PS. Bivalent ligands that target mu opioid (MOP) and cannabinoid1 (CB1) receptors are potent analgesics devoid of tolerance. J Med Chem 2013; 56(13): 5505-5513.
Notas de autor
Autor de correspondencia: Wilber Romero Fernández, Universidad Técnica de Ambato, Facultad de Ciencias de la Salud, Ingahurco, Ambato 180150, Ecuador. Tel: + 59 3 33730268 ext. 5239. Fax: + 59 3 2521134 ext.103. Correo electrónico: wromfdez@uta.edu.ec