Original articles
Recepción: 15 Agosto 2016
Aprobación: 23 Mayo 2018
DOI: https://doi.org/10.22209/IC.v59n3a01
Resumen: Debido a su versatilidad y facilidad de producción, los fragmentos variables de cadena sencilla (scFvs) derivados de anticuerpos constituyen una herramienta atractiva para una diversidad de aplicaciones. Entre ellas se encuentran la producción de insumos para inmunodetección, la inmunoterapia, el diagnóstico por imagenología, entre otras. En el presente trabajo desarrollamos una línea celular capaz de producir una proteína de fusión en la que se combinan un scFv humano dirigido contra el antígeno tumoral HER2 y la porción Fc de la IgG1 humana (scFv-Fc anti-HER2). Para su producción se emplearon células CHO, las cuales fueron transfectadas usando la técnica de lipofección, con un plásmido derivado del vector comercial pSecTag A que ha sido modificado con la secuencia de ADN anti-HER2 de interés. Los transfectomas resultantes produjeron la proteína scFv-Fc anti-HER2, la cual se encontró en el sobrenadante de cultivo en la forma de un homodímero. Mediante ensayos de citometría de flujo se demostró la capacidad de la proteína scFv-Fc anti-HER2 de enlazarse de manera específica a la molécula HER2 expresada en la superficie de células de cáncer de mama, así como también a los receptores humanos para Fcγ expresados en la línea celular THP-1. Esta nueva línea celular servirá de base para la producción y purificación de la proteína de fusión scFv-Fc anti-HER2, cuya utilidad será ensayada en modelos de inmunodiagnóstico y/o inmunoterapia.
Palabras clave: anticuerpos, biotecnología, proteínas recombinantes.
Abstract: Due to their versatility and simplicity of production, single chain Fv fragments (scFvs) derived from antibodies have become popular tools for a variety of applications. Among these applications are the immunodetection of specific targets, imaging diagnostics and immunotherapy. In this work, we developed a stable cell line capable of producing a human scFv directed against the tumor antigen HER2 fused to the Fc of the human IgG1 (scFv-Fc anti-HER2). This cell line derives from CHO cells and has been stably transfected using a modified version of the commercial vector pSecTag A, which contains the sequence of interest. The resulting transfectants produced the scFv-Fc anti-HER2 fusion protein, which is present as a homodimeric molecule in culture supernatants. By using flow cytometry assays, it was shown that the scFv-Fc anti-HER2 molecules bind specifically to HER2 on the surface of SKBR-3 cancer cells, as well as to the FcγR receptors expressed on human leukemic monocytes (THP-1). This new cell line provides the starting material for the production and purification of the scFv-Fc anti-HER2 fusion protein, which will be tested in animal models as a novel tool for immunodiagnosis and/or breast cancer immunotherapy.
Keywords: antibodies, biotechnology, recombinant proteins.
INTRODUCCIÓN
Los fragmentos de anticuerpo de cadena sencilla (ScFv) representan una de los productos biotecnológicos de mayor desarrollo en esta década. Solo en el año 2017, hay decenas de reportes en la literatura especializada donde se describen nuevas moléculas con una gran diversidad de funciones que abarcan la inmunodetección de moléculas de interés académico e industrial (1,2), el diagnóstico y tratamiento de enfermedades crónicas (3-6) e infecciosas (7,8), entre otras.
Actualmente, hay al menos 18 anticuerpos monoclonales aprobados para uso terapéutico en cáncer, la mayoría de ellos obtenidos por tecnología de ADN recombinante y producidos en sistemas de expresión de células de mamíferos, tales como las células CHO (del inglés Chinese hamster ovary) (9,10). Las células CHO constituyen un sistema de expresión conveniente debido a su capacidad para generar de manera eficiente modificaciones post-traduccionales, tales como la glicosilación, preservando las funciones efectoras de los anticuerpos recombinantes y prolongando su tiempo de vida media en suero. La principal desventaja de este sistema de expresión es su alto costo relativo, tanto a pequeña como a gran escala. Sin embargo, este sistema de expresión continúa siendo el más popular para la producción de anticuerpos terapéuticos contra el cáncer (10,11).
Los anticuerpos recombinantes o sus moléculas derivadas que tienen aplicabilidad en el diagnóstico, detección o terapia del cáncer están comúnmente dirigidos a antígenos específicos que son expresados de manera casi exclusiva o de forma exacerbada en las células tumorales. Los receptores de factores de desarrollo epidérmico constituyen blancos importantes para varias de estas moléculas. Estos receptores forman parte de una familia de moléculas que están involucradas en la promoción de eventos de proliferación y sobrevivencia celular. Entre los receptores de factores de desarrollo epidérmico destaca el de tipo 2 (llamado HER2 en el humano), para el que ya se han comercializado dos anticuerpos terapéuticos: Trastuzumab (Herceptin, Genentech) y Pertuzumab (Perjeta, Roche) (9,12). A pesar de las notables mejoras en las respuestas clínicas obtenidas con la aplicación de los anticuerpos terapéuticos, algunas de sus propiedades deben ser modificadas para incrementar su capacidad de penetración al tumor, aumentar su internalización por parte de las células tumorales y/o evitar el desarrollo de resistencia al tratamiento. Además, se requiere del desarrollo nuevos reactivos con mayor poder de predicción de la respuesta al tratamiento, de manera de emplearlos solo en aquellos casos donde exista mayor probabilidad de éxito. Por otra parte, resulta imperativo el desarrollo local de este tipo de tecnologías para promover su producción, validación y comercialización a nivel nacional y regional. Con la finalidad de contribuir con estos objetivos, hemos diseñado mediante tecnología de ADN recombinante un scFv-Fc anti-HER2 para expresarlo en células CHO. Los scFv tienen un gran potencial biotecnológico ya que, en comparación con los anticuerpos completos, pueden ser producidos con mayor facilidad debido a su pequeño tamaño, lo que a su vez les confiere una mayor capacidad de penetración en tumores sólidos y presentan, además, una menor posibilidad de inducir una respuesta inmunitaria que promueva su eliminación (13). Al acoplar el fragmento Fc de la IgG1 al scFv, se promueve que éste pueda mediar funciones efectoras de células del sistema inmunitario, las cuales son de gran importancia para la actividad antitumoral de los anticuerpos (14), prolongando además su vida media en suero gracias a la interacción con el receptor neonatal para Fc (FcRn).
MATERIALES Y MÉTODOS
Construcciones genéticas
Para la construcción del vector de expresión que porta la fusión genética de interés se emplearon los vectores tipo plásmido pSecTag A y pSYN (gentilmente donados por el Dr. Bruno Roberts y la Dra. Marie-Alix Poul, respectivamente, ambos del Instituto de Investigación de Cáncer de Montpellier, Francia). La versión de pSecTag A utilizada contiene una secuencia que codifica un scFv anti-CEA (Antígeno Carcinoembrionario) fusionado a los dominios constantes CH2 y CH3 de la cadena pesada de la IgG humana del isotipo γ1 provenientes del vector comercial pFUSE-hIgG1-Fc (Invivogen). El plásmido pSYN contiene la secuencia correspondiente a la especificidad anti-HER2. El ADN plasmídico de ambos vectores fue digerido de forma secuencial empleando las enzimas SfiI y NotI (Thermo Fisher Scientific), siguiendo las recomendaciones del fabricante. Los fragmentos resultantes se separaron mediante electroforesis en gel de agarosa y se aislaron dos fragmentos de ADN: uno de aproximadamente 700 pares de bases (bp), proveniente del vector pSYN y otro de aproximadamente 6 000 bp, proveniente del vector pSecTag A modificado. Estos fragmentos fueron ligados empleando Ligasa T4 (New England Biolabs, RU), siguiendo las recomendaciones de la casa comercial. Posteriormente, los productos del ligamiento fueron clonados en bacterias E. coli de la cepa DH5-, purificados empleando un estuche comercial de minipreparaciones (Clontech, EUA) y secuenciados en el Servicio de Secuenciación de ácidos nucléicos del IVIC (15).
Transfección
El ADN plasmídico del vector de expresión construido fue producido a mayor escala e introducido en células CHO Pro-5. Se empleó la técnica de lipofección (Lipofectamine 2000, Invitrogen), siguiendo las recomendaciones del fabricante. La eficiencia de transfección se evaluó mediante microscopía de fluorescencia empleando un plásmido reportero (pMMP-mIL-12.IRES.eGFP, gentilmente donado por el Dr. Jesús Páez, Universidad de Harvard, EUA) que contiene la secuencia que codifica la proteína fluorescente verde. Posteriormente, se añadió la droga de selección (Zeocina) a la concentración óptima (0,25 μg/mL) previamente determinada y las placas se mantuvieron en la incubadora bajo observación continua hasta detectar la presencia de transfectomas resistentes. Para evidenciar la producción de la proteína de fusión se realizó un escrutinio del sobrenandante de los cultivos donde crecían células resistentes a la droga de selección, empleando para ello ensayos de Dot Blot y ELISA específicos para la IgG humana.
Dot blot específico para IgG
En una membrana de nitrocelulosa se repartieron alícuotas de 100 μL de cada sobrenadante cosechado de los cultivos de células productoras de la proteína recombinante, a través de un Bio-dot (Bio-rad, EUA). Posteriormente, la membrana fue sometida a vacío por 15 minutos y se dejó secar al aire por unos minutos más. Esta membrana se incubó luego con una solución tampón TBS (0,9% NaCl; 100 mM Tris; pH 7,5) con albúmina sérica bovina (BSA) al 5% (TBS-BSA 5%) a temperatura ambiente y en agitación durante 1 hora. A continuación, la membrana se lavó con TBS y se incubó en agitación y a temperatura ambiente con el anticuerpo específico para la porción Fc de la inmunoglobulina G humana conjugado a peroxidada (Sigma A-0170) durante 1 hora. Finalmente, la membrana se lavó 3 veces con TBS al que se le añadió Tween 20 al 0,1% (TBS-Tween 0,1%) para, posteriormente, incubarla a temperatura ambiente en solución de revelado DAB (650 μg/mL diaminobencidina; 0,01% H2O2 y 0,03% cloruro de cobalto, diluidos en tampón Tris-HCl 100 mM; pH 7) durante 30 minutos.
ELISA específico para IgG
Para realizar el ensayo de determinación de la concentración de proteína recombinante en los sobrenadantes de cultivo, se revistió una placa de ELISA con 100 μL/pozo de un anticuerpo de captura (Fab2 anti-Fc, Sigma I-9885) diluido a una concentración de 0,5 μg/mL en tampón PBS (5 mM Na2H-PO4, 1,5 mM KH2PO4, 2,7 mM KCl; 0,85% NaCl; pH 7,2), incubándola a 4ºC durante la noche. Después de 2 lavados con PBS frío, la placa se bloqueó con BSA diluido al 3% en PBS (PBS-BSA 3%) a 37ºC durante 1 hora. Al finalizar dicha incubación, los pozos de la placa se lavaron con PBS-Tween 0,05% y se colocaron 100 μL/pozo de los sobrenadantes de cultivo o diluciones seriadas de un patrón comercial de IgG humana de concentración conocida por duplicados. La placa se incubó a temperatura ambiente durante 90 minutos y se lavó 6 veces con PBS/Tween 0,05%. A continuación, se colocaron 100 μL/pozo del anticuerpo anti-IgG humana conjugado a peroxidada (Sigma A-0170) diluido en PBSBSA 3% y se realizó una nueva incubación a temperatura ambiente durante 90 minutos. Luego de lavar 4 veces con PBS-Tween 0,05% y una vez con PBS, se añadieron 50 μL/pozo de sustrato TMB (0,1 mg/mL tetrametilbencidina y 0,01% H2O2, diluidos en 20 mM ácido cítrico; 150 mM fosfato de sodio, pH 5,2) recién preparado, se incubó a temperatura ambiente durante 15 minutos y se detuvo la reacción con ácido sulfúrico 0,5 N. Finalmente, se procedió a registrar los valores de absorbancia a 450 nm de cada pozo, empleando para ello un lector de ELISA (Bioteck Instruments, Burlington, EUA). Los valores de absorbancia obtenidos para la curva patrón se utilizaron para generar una recta de regresión que permitió la estimación cuantitativa de las concentraciones de proteína de fusión en los sobrenadantes.
Clonación
La clonación se realizó mediante el método de dilución al límite. Una suspensión de 100 células/mL de cada transfectoma en estudio fue diluida seriadamente (1:2) hasta alcanzar la dilución que corresponde teóricamente a una concentración 6,25 células/mL. Cada dilución fue entonces repartida en una placa de cultivo celular de 96 pozos (a razón de 100 μL/pozo) en presencia de la droga de selección Zeocina (Invitrogen) y las placas resultantes fueron incubadas a 37°C, 5% CO2 durante aproximadamente 1 mes. Aquellas placas que presentaron colonias en menos de 30% de los pozos fueron sometidas a escrutinio mediante el ELISA específico para IgG, descrito en la sección anterior para determinar cuáles clones produjeron la mayor cantidad de proteína de fusión.
Producción de sobrenadantes que contienen la proteína de fusión scFv-Fc anti-HER2
Se realizaron cultivos estacionarios de los transfectomas productores de la proteína recombinante scFv-Fc anti-HER2. Dichas células fueron cultivadas hasta alcanzar confluencia empleando medio IMDM (Gibco, EUA) enriquecido con suero fetal bovino al 5%, 100 unidades/mL de penicilina, 100 ug/ mL de streptomicina, 250 ng/mL de anfotericina y 2 mM L-glutamina. Para ello, se inició el cultivo partiendo de frascos de 25 cm2, los cuales fueron expandidos hasta llegar a frascos de mayor volumen (175 cm2). En este punto se realizó el conteo de las células vivas en cámara de Neubauer, utilizando azul de tripano (0,4%) y ajustando el número de células viables a 1 x 107 para cada frasco de cultivo. La viabilidad celular siempre fue mayor a 95%. Luego que dichos cultivos alcanzaron confluencia, se sustituyó el medio por uno idéntico pero libre de suero fetal bovino. Al cabo de 96 horas, se colectaron los sobrenadantes de cultivo y se centrifugaron durante 10 minutos a 5000 g en una centrífuga de mesa (Thermo IEC, Needham Heights, MA, EUA). Seguidamente, los sobrenadantes se almacenaron a -20°C hasta su uso.
Caracterización bioquímica de la proteína de fusión scFv-Fc anti-HER2
Los sobrenadantes de cultivo fueron analizados mediante electroforesis en gel de poliacrilamida al 10% en condiciones no reductoras (Tricina SDS-PAGE). Para ello, se utilizó una cámara de electroforesis (Fisher Biotech electrophoresis systems. Fisher Scientific, Pittsburg, PA, EUA), en la que se cargaron 20 uL/carril de sobrenadante. Posterior a la separación electroforética, el gel se incubó en solución fijadora (50% etanol, 10% ácido acético) con agitación constante en un balancín de plataforma (Bellco Glass, INC. Vineland, NJ, EUA) durante toda la noche. Luego, se realizó la tinción del gel empleando para ello una solución de azul de Coomassie (0,1% azul de Coomassie R350, 20% metanol, 10% ácido acético) a temperatura ambiente y en agitación durante 3 horas. Seguidamente, el gel se decoloró mediante cambios sucesivos de solución decolorante (50% metanol, 10% ácido acético) hasta que solo las bandas proteicas presentaran coloración. Finalmente, se procedió al secado manual, para lo cual cada gel de poliacrilamida se incubó en una solución 20% glicerol con un movimiento de rotación suave por 2 horas. Al cabo de este tiempo, los geles se envolvieron en papel celofán y se dejaron secar en estufa a 37°C durante 48 horas.
Identificación de la proteína de fusión scFv-Fc anti-HER2 mediante la técnica de inmunoblot
En primer lugar, se realizó una electroforesis en gel de poliacrilamida con aproximadamente 1 μg de proteína recombinante/ carril y se empleó la IgG1 humanizada trastuzumab (5 μg) como control positivo. El gel fue equilibrado en tampón de transferencia (25 mM Trisma base, 192 mM glicina, pH 8,3) durante 30 minutos. Luego, se realizó la electro-transferencia a una membrana de nitrocelulosa igualmente equilibrada con tampón de transferencia. Para ello, se utilizó una cámara “Fisher biotech electrophoresis systems” (Fisher Scientific, Pittsburg, PA, EUA) con un voltaje de 250 mA (60 V) a una temperatura de 4ºC durante 2 horas. Para comprobar que la transferencia fue exitosa se realizó una tinción reversible de la membrana con una solución de rojo Ponceau (0,5% rojo Ponceau diluido en 0,1% ácido acético). Esta tinción fue revertida realizando varios lavados con TBS. Seguidamente, para evitar las uniones inespecíficas, se bloqueó la membrana con TBS-Tween 0,1% al 3% de leche descremada (TBSL), a temperatura ambiente y en agitación durante 2 horas. Posterior a un enjuague con TBS-Tween 0,1%, la membrana se incubó con el anticuerpo de detección anti-IgG humana acoplado a peroxidasa (Sigma A-0170) diluido 1/1000 en TBSL) a temperatura ambiente y en agitación por 2 horas. Luego, la membrana se lavó 4 veces con TBS/Tween 0,1% y 1 vez con TBS antes de colocar la solución de revelado DAB (6% Diaminobencidina, 0,015% H2O2, 0,03% cloruro de cobalto, diluidos en Tris-HCl 0,01 M, pH 7,6); esta solución permaneció en contacto con la membrana en oscuridad hasta que se observó un precipitado que puso en evidencia las bandas proteicas. Finalmente, la reacción se detuvo lavando la membrana con TBS.
Enlace al antígeno HER2
Para comprobar la unión de la proteína recombinante scFv-Fc anti-HER2 a su antígeno, se utilizaron células de cáncer de mama SKBR-3 (American Type Culture Collection, EEUU), las cuales sobre-expresan el receptor HER2. Dichas células fueron despegadas de los frascos de cultivo mediante tratamiento con 0,05% Tripsina-EDTA (Gibco, EUA) a 37ºC durante 5 minutos. Luego de un lavado con PBS, se procedió al contaje celular en cámara de Neubauer utilizando azul de tripano (0,4%). La suspensión se ajustó a una densidad de 106 células/mL en PBS-BSA 0,1% y se trató con suero de rata en hielo durante 10 minutos. Transcurrido ese tiempo, se añadieron alícuotas de 100 μL de la suspensión celular a 500 μL de sobrenadante de cultivo de un transfectoma productor de la proteína recombinante, de medio de cultivo o de una solución de Trastuzumab (500 ng/mL) en medio de cultivo. Las células así tratadas fueron incubadas en agitación a 4ºC durante 1 hora. Una vez finalizada la incubación, las células fueron lavadas con PBS-BSA 0,1%, suspendidas en 500 μL de PBS-BSA 0,1% y luego se les añadió 1 μL de una dilución 1/5 de un conjugado anti-Ig humana/isotiocianato de fluoresceína (FITC) (Wellcome Research Laboratories, Inglaterra), incubándose nuevamente a 4°C durante 1 hora. Al finalizar la incubación y luego de otro lavado con PBS-BSA 0,1%, las células se suspendieron en 0,2 mL de PBS-BSA 0,1%. Finalmente, cada una de las muestras se analizó mediante citometría de flujo (FACScalibur, Becton Dickinson, San Diego, CA, EUA) para determinar el número de células positivas a la unión de la proteína recombinante scFv-Fc anti-HER2.
Especificidad del enlace a HER2
La especificidad de la unión de la proteína recombinante scFv-Fc anti-HER2 al antígeno HER2 se comprobó de la manera descrita en la sección anterior, pero empleando la línea celular de adenocarcinoma mamario MDA-MB-231 (American Type Culture Collection, EEUU), la cual no expresa el receptor HER2.
Enlace a receptores para Fcγ
La unión de la proteína recombinante a los receptores FcγR presentes en células THP-1 (American Type Culture Collection, EEUU) (16) se determinó mediante el bloqueo de la unión al receptor de una preparación de IgG1 marcada con FITC. Para ello, 2 mg de trastuzumab fueron acoplados a FITC (Sigma, EUA) siguiendo el protocolo recomendado por el fabricante. Las células THP-1 fueron previamente contadas para ajustar su concentración a 106 células/mL en PBSBSA 0,1%. Seguídamente, alícuotas de 100 μL de esta suspensión celular fueron tratadas añadiéndoles 500 μL de sobrenadante (libre de suero fetal bovino) cosechado de los cultivos de las células productoras de la proteína recombinante, de medio de cultivo o de una dilución 1/500 de suero humano. Una vez finalizada la incubación, se realizó un lavado con PBS-BSA 0,1% y las células se centrifugaron para luego añadirles 2 μL de una dilución 1/10 del conjugado trastuzumab/FITC e incubar nuevamente a 4ºC durante 1 hora. Finalmente, las muestras se analizaron mediante citometría de flujo.
RESULTADOS
Digestión diagnóstica y secuenciación de ADN
A partir de las manipulaciones de biología molecular realizadas para la construcción y clonación del ADN recombinante que contiene la secuencia que codifica la proteína scFv-Fc anti-HER2, se obtuvieron colonias de E. coli resistentes al marcador de selección. Para corroborar que la resistencia era una consecuencia de la presencia del ADN plasmídico que contenía la secuencia construída, se procedió a purificar ADN plasmídico a partir de las colonias transformantes y realizar una digestión diagnóstica con la enzima de restricción SacI. La secuencia construída introduce un sito de corte único para esta enzima en el ADN del plásmido original a 819 bases del origen de replicación y aumenta su peso molecular a aproximadamente 6000 bp. En la Fig. 1 se observa que el ADN plasmídico, purificado a partir de cuatro colonias escogidas para el diagnóstico (carriles SD, sin digerir), migró en la separación electroforética de la forma esperada (a aproximadamente 6000 bp) luego de la digestión (carriles D, digerido).
Luego de su producción a mayor escala en bacterias y previo a la transfección de las células eucariotas, se procedió a la secuenciación y análisis de la región del plásmido que contenía la secuencia donde se realizó el cambio de especificidad. Dicho análisis reveló que el cambio de especificidad no resultó en alteración alguna de la secuencia en los sitios de corte de las enzimas de restricción ni en el marco de lectura. La secuencia anti-HER2 introducida se encuentra protegida por la patente No. WO 1999055367.
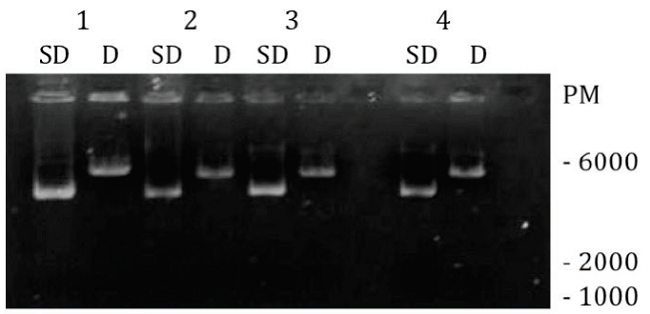
Fig. 1
Análisis de restricción. Gel de agarosa al 0,8% empleado para la identificación del ADN plasmídico de interés. El ADN plasmídico fue digerido con la enzima de restricción SacI (New England Biolabs, Inglaterra). En los carriles identificados con las letras SD se colocó ADN plasmídico, purificado de cuatro colonias transformantes de E. coli, sin digerir y en los carriles identificados con la letra D, se colocó el mismo ADN plasmídico digerido.
Escrutinio de transfectomas positivos para la producción de la proteína scFv-Fc anti-HER2
El escrutinio de los sobrenadantes de las colonias de transfectomas obtenidos se realizó mediante la técnica de “Dot blot”. En la Fig. 2 se muestra una imagen de la membrana de nitrocelulosa a la cual se adsorbieron las muestras de sobrenadante de cada uno de los cultivos. Se observa que, con excepción de las células transfectadas con el plásmido control (pMMP-mIL-12.IRES. eGFP, columna 1), en todos los transfectomas se detectó la presencia de la porción Fc de la IgG1 humana, lo cual es sugestivo de la presencia de la proteína de fusion scFv-Fc anti-HER2 en estos sobrenadantes. Aun cuando se aprecian diferencias aparentes en la intensidad de la señal entre los distintos sobrenadantes analizados, ello no puede ser tomado como una indicación de mayor o menor producción pues los cultivos no se encontraban sincronizados para la producción.

Fig. 2
Producción de scFv-Fc anti-HER2 por parte de los transfectomas seleccionados. Membrana de nitrocelulosa analizada mediante la técnica de dot blot. Las letras A, B, C, D, E, F, G, H corresponden a cada una de las filas de una placa de cultivo. La columna 1 contiene sobrenadantes de colonias de células CHO tranfectadas con un ADN plasmídico control. Las columnas 2, 3, 4 y 5 contienen sobrenadantes de células CHO transfectadas con el ADN plasmídico que codifica la proteína scFv-Fc anti-HER2.
Concentración relativa de la proteína de fusión en los sobrenadantes de cultivo
La concentración de proteína de fusión en los sobrenadantes de cultivo obtenidos de los transfectomas positivos para el dot blot se determinó mediante el cultivo sincronizado de los distintos transfectomas y el posterior análisis de los sobrenadantes mediante la técnica de ELISA tipo sándwich. Los resultados obtenidos se muestran en la Tabla I, donde puede apreciarse que los sobrenadantes examinados contienen entre 99 y 189 g/L de proteína de fusión scFv-Fc anti-HER2, destacándose los clones G12 y B9 como mejores productores bajo las condiciones estudiadas. Sin embargo, es de hacer notar que el clon G12, además de presentar una buena producción, tuvo una tasa de proliferación inferior a la del clon B9 (datos no mostrados), lo que sugiere que es más eficiente, ya que requiere de menos recursos para su cultivo.
Determinación del peso molecular de la proteína scFv-Fc anti HER2 mediante electroforesis en gel de poliacrilamida e inmunoblot
Con la finalidad de determinar el peso molecular aparente de la proteína de fusión obtenida y tener una imagen cualitativa de su concentración relativa en cada uno de los sobrenadantes de los cultivos sincronizados de los transfectomas, se utilizó la técnica de electroforesis en geles de poliacrilamida en condiciones desnaturalizantes, no reductoras (SDS-PAGE). En la Fig. 3 se muestra el resultado de la separación electroforética. Se observan varias bandas por carril, destacándose principalmente dos: una de aproximadamente 00.000 de peso molecular, la cual se encuentra por debajo de la banda correspondiente al peso de trastuzumab, y otra de aproximadamente 60.000. El peso molecular aparente del dímero de proteína de fusión, de acuerdo a la secuencia de aminoácidos esperada, es de 100.000, mientras que el monómero tendría un peso aproximado de 50.000.
CONCENTRACIÓN DE ScFv-Fc ANTI-HER2 EN LOS SOBRENADANTES DE LOS TRANSFECTOMAS PRODUCTORES

Con el fin de dilucidar si las bandas observadas en los geles de poliacrilamida correspondían al dímero y/o al monómero de proteína de fusión, se realizaron ensayos de inmunoblot (western blot). Este ensayo pone en evidencia la identidad de la proteína recombinante mediante el reconocimiento de la porción Fc de la IgG humana usando un anticuerpo específico. Como puede observarse en la Fig. 4, los resultados revelaron la presencia de una única proteína reactiva con el anticuerpo anti-IgG, de aproximadamente 100.000 de peso molecular aparente. Este tamaño es compatible con una conformación homodimérica de la proteína recombinante scFv-Fc anti-HER2. Se evidencia además una banda de aproximadamente 150.000 de peso molecular en el carril correspondiente al anticuerpo trastuzumab (IgG1) empleado como control positivo.

Fig. 3
Peso molecular aparente y concentración relativa de la proteína recombinante scFv-Fc anti-HER2 en los sobrenadantes de cultivo. Imagen del resultado de la separación electroforética en geles de poliacrilamida al 10% en condiciones no reductoras de los sobrenadantes obtenidos a partir de los diferentes cultivos de células CHO, productoras de la proteína recombinante scFv-Fc anti-HER2. Se señala con una flecha el tamaño esperado para la proteína recombinante. Código de identificación de transfectomas ensayados: D8, B12, B9, H10, H12, H11, H10, G7, G8, G9, G12 y F10.
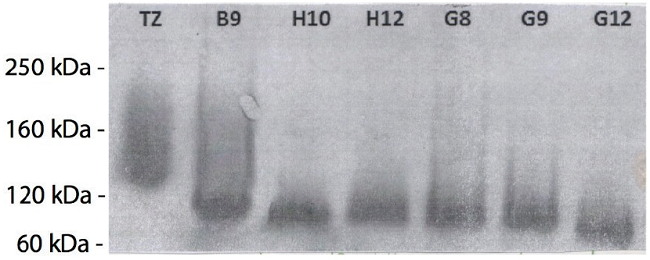
Fig. 4
Inmunoblot de sobrenadantes de cultivo de transfectomas productores de scFv-Fc anti HER2. Membrana de nitrocelulosa revelada con un anticuerpo anti-IgG humana acoplado a peroxidasa. Las bandas de color oscuro corresponden al precipitado generado por la detección de la porción Fc de las inmunoglobulinas G humanas. Tz=trastuzumab (IgG1 humanizada usada como control positivo). Código de identificación de transfectomas ensayados: B9, H10, H12, G8, G9 y G12.
Enlace de la proteína scFv-Fc anti HER2 al antígeno HER2
La unión de la proteína recombinante scFv-Fc anti-HER2 a su antígeno se estudió mediante citometría de flujo, empleando para ello células de adenocarcinoma mamario SKBR3, las cuales sobre-expresan el receptor HER2 (Fig. 5). El anticuerpo comercial anti-HER2 Trastuzumab (TZ) fue empleado como control positivo, mientras que el medio de cultivo IMDM se empleó como control negativo. A la par, se emplearon diluciones seriadas del sobrenadante de cultivo de uno de los transfectomas productores de la proteína scFv-Fc anti-HER2. Las células incubadas con TZ resultaron positivas al marcaje en un 99,24% con una intensidad media de fluorescencia (IMF) de 182,41 comparado con un marcaje del 1,70% de las células del control negativo (IMF de 12,74) (Panel A, Fig. 5). La incubación de las células SKBR3 con las diferentes diluciones de sobrenadante también resultó en el marcaje de las mismas, lo cual sugiere que la proteína recombinante scFv-Fc anti-HER2 es capaz de unirse a su antígeno. La proporción de células marcadas fue dependiente de la concentración de la proteína en cuestión, ya que ésta disminuyó considerablemente al aumentar el factor de dilución. Esto se evidenció, además, como una disminución de la IMF. El sobrenadante de cultivo que contiene la proteína recombinante diluida 1/10 marcó al 99,72% de las células con una IMF= 88,98. Estos valores disminuyeron en las muestras de células incubadas con las diluciones 1/100 (84,30% e IMF= 47,72) y 1/1000 (76,60% e IMF= 22,67) (Panel B, Fig. 5).
Especificidad del enlace de la proteína scFv-Fc anti-HER2 a HER2
Con la finalidad de probar la especificidad de unión de la proteína recombinante scFv-Fc anti-HER2 al antígeno HER2, se procedió a realizar el experimento descrito en la sección anterior, pero esta vez empleando la línea celular de adenocarcinoma mamario MDA-MB-231, la cual no expresa el receptor HER2. En este ensayo no se observó marcaje positivo con este tipo celular (Fig. 6), obteniéndose valores de IMF de 2,87 y 2,64 para el control negativo (suero humano) y el sobrenadante respectivamente, a diferencia de la IMF de 92,83 obtenida con la línea celular SKBR3 la cual presentó nuevamente un marcaje positivo al emplear sobrenadante. Se comprueba así que la proteína recombinante scFv-Fc anti-HER2 presente en el sobrenadante de cultivo se une de manera específica a su antígeno sobreexpresado en la línea celular de adenocarcinoma mamario SKBR3.
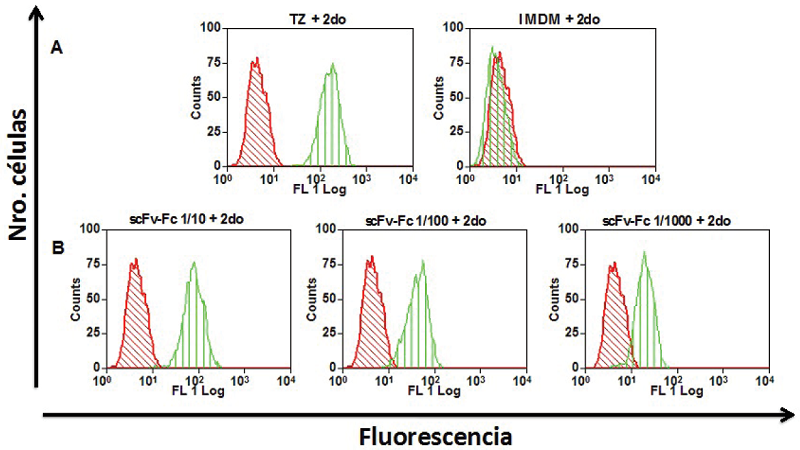
Fig. 5
Enlace de la proteína recombinante scFv-Fc anti-HER2 a células que sobre expresan el antígeno HER2. Análisis por citometría de flujo de células SKBR3 incubadas con diferentes diluciones del sobrenadante de cultivo del transfectoma B9 productor del scFv-Fc anti-HER2 (Panel B) o el anticuerpo comercial trastuzumab (Panel A). IMDM corresponde al control negativo (células pre-incubadas con medio de cultivo). El enlace fue revelado empleando un anticuerpo secundario (2do) anti-IgG humana conjugado a fluoresceína. El histograma rojo contiene los datos correspondiente a las células teñidas con anticuerpo secundario solamente. El histograma verde contiene los datos correspondiente a las células teñidas bajo las distintas condiciones experimentales empleadas.
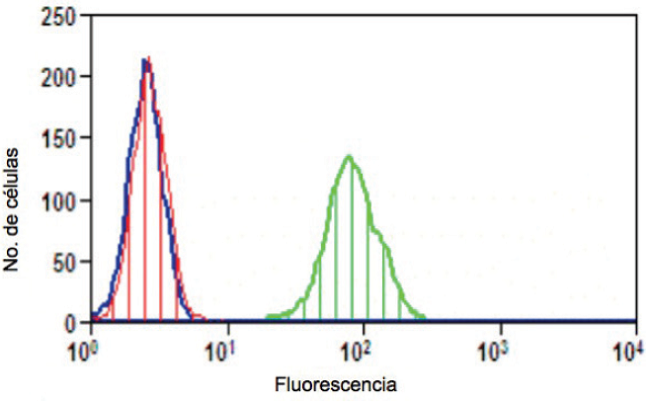
Fig. 6
Especificidad de unión de la proteína recombinante scFv-Fc anti-HER2 empleando células MDA-MB-231. Análisis por citometría de flujo de células MDA-MB-231 incubadas con sobrenadante de cultivo del transfectoma B9 productor del scFv-Fc anti-HER2. El enlace fue revelado empleando un anticuerpo anti-Ig humana conjugado a fluoresceína. El histograma rojo representa las células MDA-MB-231 incubadas con anticuerpo secundario solamente, el histograma azul representa las células MDA-MB-231 incubadas con sobrenadante de cultivo del transfectoma B9, y el histograma verde representa el marcaje de células SKBR3 con sobrenadante de cultivo del transfectoma B9.
Enlace de la proteína scFv-Fc anti HER2 a receptores para Fcγ
La unión de la proteína recombinante scFv-Fc anti-HER2 a los receptores FcγR se estudió mediante citometria de flujo, empleando la línea celular monocítica THP-1. Para ello, se procedió a realizar ensayos de bloqueo de la unión de un anticuerpo IgG1 humano conjugado a FITC utilizando como bloqueante el sobrenadante de cultivo de los transfectomas productores de la proteína scFv-Fc anti-HER2. Cuando se permitió el enlace directo del conjugado IgG1-FITC a las células THP-1 se obtuvo una IMF= 53,05. Como control negativo del bloqueo se empleó el medio de cultivo IMDM. Como control positivo del bloqueo se empleó suero humano (SH). Con estos controles las IMF resultantes fueron 51,44 y 9,94, respectivamente (Panel A, Fig. 7). A la par, se realizaron diluciones seriadas del sobrenadante de cultivo de uno de los transfectomas productores del scFv-Fc anti-HER2 y se comprobó la capacidad del mismo para bloquear la unión del conjugado IgG1-FITC. El bloqueo de esta unión fue dependiente de la concentración de la proteína recombinante, observándose que al aumentar el factor de dilución, la capacidad de bloquear la unión del conjugado fue menor. Al utilizar el sobrenadante puro, la IMF= 9,12; ésta aumentó al diluir el sobrenadante 1/10 (IMF= 14,52) ó 1/100 (IMF= 37,67) (Panel B, Fig. 7). El bloqueo de la unión del conjugado IgG1-FITC a las células THP-1, mediado por el scFv-Fc antiHER2, fue similar al ejercido por el SH cuando el primero fue usado puro. Esto pudo comprobarse al comparar los valores de IMF obtenidos para cada condición, siendo de 9,12 para el primer caso y 9,94 para el segundo. Además, a pesar de diluir el sobrenadante 1/100, el bloqueo de la IgG1-FITC fue eficiente, ya que la IMF obtenida fue aún menor (37,67) que cuando se empleó el control negativo de bloqueo (51,44).
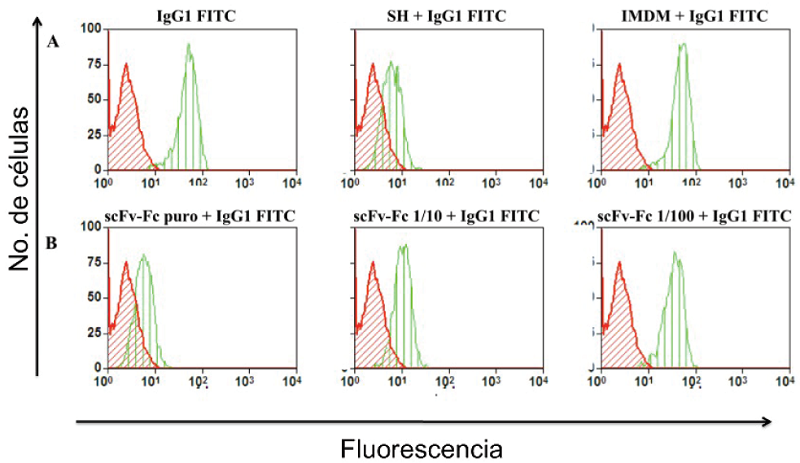
Fig. 7
Interferencia en el enlace de un conjugado IgG1-FITC a los receptores FcγR por parte del sobre nadante de cultivo del transfectoma B9 productor de la proteína scFv-Fc anti-HER2. En la figura se muestra el resultado del análisis por citometría de flujo de células THP-1 incubadas con el sobrenadante de cultivo de uno de los transfectomas productores del scFv-Fc anti-HER2 y sus respectivos controles y posteriormente marcadas con el conjugado IgG1-FITC. Se observa claramente el efecto inhibitorio que ejerció el sobrenadante sobre la unión del conjugado IgG1-FITC. El histograma rojo representa la auto-fluorescencia de las células THP-1. El histograma verde representa las células THP1 incubadas con el conjugado IgG1-FITC bajo las condiciones experimentales indicadas.
DISCUSIÓN
Los fragmentos de anticuerpo dirigidos contra el antígeno HER2 muestran un gran potencial de aplicación en el área biomédica. En la actualidad, están siendo probados en la detección, el diagnóstico y el tratamiento del cáncer de mama y otros tipos de cáncer que sobreexpresan HER2. Por ejemplo, estos fragmentos han sido conjugados a diversos soportes para darles más especificidad hacia el tumor en ensayos de detección por fotoacústica (17), resonancia magnética (18) e imagenología (19,20). Además, se han combinado con radionucleótidos (21), ARNasas (22), toxinas (23), ARN de interferencia (24), como posibles terapias para el tratamiento del cáncer de mama (25,26) y ovario (27).
El fragmento de anticuerpo scFv-Fc anti-HER2 diseñado y producido en este trabajo mediante tecnología de ADN recombinante presentó la mayoría de las características estructurales esperadas a partir de su diseño teórico. Esto pudo confirmarse inicialmente mediante la secuenciación del plásmido portador de la secuencia de ADN correspondiente y posteriormente, gracias a la caracterización estructural realizada, en la cual se determinó el peso molecular aparente de la proteína producida. El peso molecular de 100.000 se corresponde con el de una proteína homodimérica, en la que dos moléculas de scFv-Fc se combinan para formar un complejo molecular de valencia y propiedades similares a las de un anticuerpo del tipo IgG, pero de dimensiones reducidas. El reducido tamaño de esta proteína recombinante podría resultar ventajoso para su actividad biológica, permitiéndole un mayor poder de penetración a tumores, una mejor capacidad de unión a otras moléculas o nanopartículas, sin perder las propiedades citotóxicas características de la IgG1. En tal sentido, cabe mencionar que un anticuerpo compacto con una especificidad muy similar y del mismo tamaño producido por De Lorenzo y col. (28) resultó más eficiente que el anticuerpo comercial trastuzumab en la erradicación de tumores HER2 positivos en un modelo múrido, probablemente debido a su menor tamaño y mayor capacidad de penetración y difusión extravascular.
La secuencia del plásmido comercial pFUSE-hIgG1-Fc, a partir del cual se produjo la proteína scFv-Fc anti-HER2 solo posee 9 de los 16 aminoácidos que componen la región bisagra de la IgG1. Dado que esta porción faltante participa activamente en la formación de puentes disulfuros que mantienen a la molécula de IgG en conformación dimérica, llama la atención que la proteína scFv-Fc anti-HER2 conserve las interacciones necesarias para la formación de dímeros. Es posible que el homodímero scFv-Fc antiHER2 sea menos estable y pueda separarse en monómeros dependiendo de las condiciones en las que se encuentre. No obstante, una buena cantidad de otros fragmentos de este tipo preparados a partir del mismo plásmido comercial poseen estas mismas características en su región bisagra, sin presentar limitaciones aparentes en este sentido. Por ejemplo, Hu y col. produjeron un fragmento de anticuerpo o “minibody”, fusionando un scFv anti-CEA (del inglés Carcinoembryonic Antigen) a la región bisagra y el domino CH3 de una IgG1. Adicionalmente, produjeron una versión alternativa de esta molécula, sin región bisagra (29). La caracterización estructural de estas proteínas mediante cromatografía líquida de alta resolución (HPLC) reveló que ambas exhiben una conformación homodimérica, con un peso molecular de 80.000. Sin embargo, el análisis electroforético reveló la existencia de diferencias entre ambas. En el caso de la versión que contenía la región bisagra se observó un patrón de migración correspondiente al homodímero, con bandas de 41.000 en condiciones reductoras y de 82.000 en condiciones no reductoras. Por su parte, la versión del scFv-Fc anti-CEA que no poseía región bisagra se observó en forma de monómero tanto en condiciones reductoras como no reductoras, con una masa molecular aproximada de 40.000. Es posible que nuestro dímero, que también contiene un segmento truncado de la región bisagra, se comporte de manera análoga al producido por Hu y col. (29).
Otras proteínas recombinantes del tipo scFv-CH3 con especificidad anti-HER2 fueron obtenidas por el grupo de Olafsen en el año 2004 (30). Estas proteínas fueron producidas en dos versiones, con y sin región bisagra, y presentaron un peso molecular aparente de 80.000 en el análisis electroforético bajo condiciones no reductoras. Esto, junto al estudio mediante HPLC, demostró que estas proteínas se encontraban en forma dimérica en sus dos versiones (30). Tanto para el caso de las proteínas de fusión anti-CEA como para el caso de las proteínas de fusión anti-HER2, los investigadores argumentan que la versión sin región bisagra del anticuerpo compacto se puede mantener en forma dimérica gracias a interacciones hidrofóbicas que ocurren entre los dos dominios CH3, siendo éste el único componente del Fc que conforma a estas proteínas recombinantes (30,31).
La proteína scFv-Fc anti-HER2 fue capaz de unirse a la superficie de células de cáncer de mama que expresan el antígeno HER2 y a la superficie de la línea celular monocítica THP-1, la cual expresa receptores para la región Fcγ de la IgG humana. También se demostró la naturaleza específica de estas interacciones. La proteína scFv-Fc anti-HER2 no fue capaz de unirse a células tumorales de cáncer de mama que no expresan el antígeno HER2, mientras que su enlace a los receptores FcγR sobre las células THP-1 ocasionó el bloqueo de la unión de una IgG1. Es pertinente comentar que diferentes autores han documentado la existencia de regiones específicas presentes en las cadenas pesadas de la IgG, las cuales son reconocidas por el receptor FcγRI humano. Una de estas regiones es conocida como “lower hinge” (baja bisagra), la cual corresponde a una secuencia de aminoácidos que se encuentra al comienzo del dominio CH2, justo donde finaliza la región bisagra. Dicha secuencia se extiende, en la IgG1, desde la posición 231 hasta la posición 236 y está compuesta por los aminoácidos Glu-LeuLeu-Gly-Gly-Pro. Se ha reportado que los dos residuos de leucina consecutivos en las posiciones 234-235 son esenciales para el reconocimiento de la IgG1 por el receptor FcγRI y que su sustitución puede ocasionar una disminución de la afinidad por dicho receptor (32-34).
Otro elemento importante para el reconocimiento de la IgG por los receptores FcγR es la glicosilación de la IgG. Se ha descrito que la presencia de un motivo de N-glicosilación conservado que se encuentra en el dominio CH2 a partir de la posición 297 y cuya secuencia consenso es Asp-X-Ser/Thr (donde X es cualquier aminoácido excepto prolina) es esencial para la ocurrencia de esta interacción, para la lisis mediada por complemento y también para la activación de las tres clases de receptor FcγR (34,35). La información estructural acerca del Fc solo o en complejos con otras proteínas como proteína A o G ha mostrado que los dominios que componen el Fc adquieren una conformación tipo herradura, en la cual los azúcares enlazados a la asparagina sobresalen de la cavidad central (35). La presencia de estos azúcares es determinante para las funciones efectoras de la IgG; es por esto que la ausencia o las variaciones en los mismos pueden tener una profunda influencia sobre la mediación de sus actividades biológicas (34). Resta por definir si la proteína de fusión scFv-Fc anti-HER2 producida se encuentra glicosilada.
A pesar de que la producción de la proteína recombinante scFv-Fc anti-Her2 resultó exitosa, los niveles de producción podrían mejorarse empleando diferentes estrategias relacionadas con el mantenimiento de los cultivos de las células productoras. Por ejemplo, una de estas estrategias sería la detención del ciclo celular en la fase G1, ya que en esta fase se expresan altamente los genes involucrados en la biogénesis de los ribosomas y la traducción de proteínas. Adicionalmente, las células que se encuentran en la fase G1 son metabólicamente más activas y de mayor tamaño que las que no lo están. Por tal razón, la fase G1 del ciclo celular se considera como la ideal para la producción incrementada de proteínas recombinantes. La detención en dicha fase se ha empleado para aumentar la productividad en diferentes líneas celulares de uso comercial tales como las células CHO (36,37).
Los abordajes empleados para inducir la detención del ciclo celular son variados, pero actualmente hay dos que se han estudiado ampliamente. La primera estrategia consiste en el cambio de temperatura a una condición de hipotermia leve. Esta condición genera una respuesta celular que produce una disminución de la actividad metabólica (consumo de glucosa, captación de oxígeno y producción de lactato y amonio), retardo de la apoptosis y ayuda a extender la duración de la fase de producción (fase estacionaria). En tipos celulares como células CHO transfectadas para producir proteínas recombinantes, se ha observado incrementos en los niveles de ARNm recombinante ya sea debido al aumento en la transcripción del gen recombinante de interés o a una estabilidad incrementada del ARNm. Este proceso de cultivo consiste en dos fases: una en la cual se obtiene la mayor biomasa posible a 37°C, seguida de una fase extendida de producción con reducción de la temperatura (28-33°C), durante la cual las células permanecen en desarrollo detenido, mientras la producción de proteínas heterólogas se mantiene estable y en alto nivel (36-38). Otra estrategia comúnmente empleada para la detención del ciclo celular en fase G1 en el cultivo de células CHO productoras de proteínas recombinantes es la adición de dimetilsulfóxido (DMSO) a bajas concentraciones. Este compuesto químico es capaz de inducir una detención eficiente y reversible del ciclo celular en fase G1 en células CHO (90% de la población celular), empleándose a concentraciones de 1-2% (36). Al igual que el DMSO, el butirato de sodio se ha empleado exitosamente en la modulación del ciclo celular de células CHO. Ambos compuestos han sido asociados con la modulación de las ciclinas dependientes de quinasas y la inhibición de las histonas desacetilasas, induciendo así la detención del crecimiento celular y ocasionando, adicionalmente, un aumento en la expresión de proteínas heterólogas (37). Estas estrategias podrían emplearse para aumentar la producción del scFv-Fc anti-HER2 del mismo y así contar con mayor cantidad de proteína de la que hasta el momento ha sido obtenida, lo que permitiría realizar ensayos funcionales, no solo in vitro sino también in vivo.
En conclusión, este trabajo aporta el material de partida para producir un insumo biotecnológico que se une al antígeno HER2. Se requieren estudios de enlace y eficacia en la inducción de actividad anti-células cancerosas y definir su utilidad en diagnóstico y/o terapias antineoplásicas.
AGRADECIMIENTOS
El presente trabajo fue financiado por FONACIT proyecto No. 2012000808. Agradecemos al Servicio de Secuenciación de Ácidos Nucleicos del IVIC, así como al Laboratorio de Cultivo Celular del CBB, IVIC. También, al Dr. Bruno Roberts y la Dra. Marie-Alix Poul, y al personal del Laboratorio de Terapia Dirigida y Radiobiología del Instituto de Investigación de Cáncer de Montpellier, Francia.
REFERENCIAS
1. Liu Y, Lin M, Zhang X, Hu X, Lin J, Hao J, He D, Zhang X, Xu C, Zhong J, Xie Y, Zhang C, Liu, X. Development of competitive ELISA for the detection of bovine serum albumin using single-chain variable fragments. Anal Biochem 2017; 525:89-91.
2. Brofelth M, Städe LW, Ekstrand AI, Edfeldt LP, Kovacic R, Nielsen TT, Larsen KL, Duroux L, Wingren C. Site-specific photocoupling of pBpa mutated scFv antibodies for use in affinity proteomics. Biochim Biophys Acta Proteins Proteomics 2017; 1865:985-996.
3. Sebollela A, Cline EN, Popova I, Luo K, Sun X, Ahn J, Barcelos MA, Bezerra VN, Lyra e Silva NM, Patel J, Pinheiro NR, Qin LA, Kamel JM, Weng A, DiNunno N, Bebenek AM, Velasco PT, Viola KL, Lacor PN, Ferreira ST, Klein WL. A human scFv antibody that targets and neutralizes high molecular weight pathogenic amyloid-ß oligomers. J Neurochem 2017; 142:934-947.
4. Agha Amiri S, Shahhosseini S, Zarei N, Khorasanizadeh D, Aminollahi E, Rezaie F, Zargari M, Azizi M, Kalaj V. A novel antiCD22 scFv-apoptin fusion protein induces apoptosis in malignant B-cells. AMB Express 2017; 7:112.
5. Sokolowska-Wedzina A, Chodaczek G, Chudzian J, Borek A, Zakrzewska M, Otlewski J. High-affinity internalizing human scFv-Fc antibody for targeting FGFR1overexpressing lung cancer. Mol Cancer Res 2017; 15:1040-1050.
6. Liu Q, Pang H, Liu Q, Zhou J, Liu Y. Preparation of human single-chain variable fragment antibodies against anaplastic thyroid carcinoma, and single photon emission-computed tomography/computed tomography imaging in tumor-bearing nude mice. Oncol Rep 2017; 37:2980-2986.
7. Ahangarzadeh S, Bandehpour M, Kazemi B. Selection of single-chain variable fragments specific for Mycobacterium tuberculosis ESAT-6 antigen using ribosome display. Iran J Basic Med Sci 2017; 20:327-333.
8. Khan L, Kumar R, Thiruvengadam R, Parray HA, Makhdoomi MA, Kumar S. Crossneutralizing anti-HIV-1 human single chain variable fragments(scFvs) against CD4 binding site and N332 glycan identified from a recombinant phage library. Sci Rep 2017; 7:45143.
9. Scott AM, Allison JP, Wolchok JD. Monoclonal antibodies in cancer therapy. Cancer Immun 2012; 12:14.
10. Birch JR, Racher AJ. Antibody production. Adv Drug Deliv Rev 2006; 58:671-685.
11. Roque AC, Lowe C, Taipa AM. Antibodies and genetically engineered related molecules: production and purification. Biotechnol Prog 2008; 20(3):639-654.
12. Hudis CA. Trastuzumab - Mechanism of action and use in clinical practice. New Engl J of Med Rev 2007; 357:39-51.
13. Ahmad ZA, Yeap SK, Ali AM, Ho WY, Alitheen NBM, Hamid M. ScFv antibody: principles and clinical application. Clin Dev Immunol 2012; 2012:982050.
14. Gennari R, Menard S, Fagnoni F, Ponchio L, Scelsi M, Tagliabue E, Castiglioni F, Villani L, Magalotti C, Gibelli N, Oliviero B, Ballardini B, Da Prada G, Zambelli A. Pilot study of the mechanism of action of preoperative trastuzumab in patients with primary operable breast tumors overexpressing HER2. Clin Cancer Res 2004; 10: 5650-5655.
15. Fuenmayor J. Fusión molecular de un anticuerpo anti-HER2 a C5a o C5adesArg: potenciación de su efecto sobre cultivos de células tumorales SKbr-3. [Tesis Doctoral]. Caracas: Instituto Venezolano de Investigaciones Científicas; 2007.
16. Fleit H, Kobasiuk C. The human monocytelike cell line THP-1 expresses Fc gamma RI and Fc gamma RII. J Leukoc Biol 1991; 49: 556-565.
17. Kanazaki K, Sano K, Makino A, Shimizu Y, Yamauchi F, Ogawa S, Ding N, Yano T, Temma T, Ono M, Saji H. Development of anti-HER2 fragment antibody conjugated to iron oxide nanoparticles for "in vivo" HER2-targeted photoacoustic tumor imaging. Nanomedicine Nanotechnology, Biol Med 2018; 11: 2051-2060.
18. Yamada H, Hasegawa Y, Suzuki Y, Imai H, Matsuda T, Kimura Y, Toshimitsu A, Aoyama Y, Kondo T. Magnetic resonance imaging of tumor with a self-traceable polymer conjugated with an antibody fragment. Bioorg Med Chem Lett 2015; 25: 2675- 2678.
19. Kim H-Y, Wang X, Wahlberg B, Edwards WB. Discovery of hapten-specific scFv from a phage display library and applications for HER2-positive tumor imaging. Bioconjug Chem 2014; 25: 1311-1322.
20. Ueda M, Hisada H, Temma T, Shimizu Y, Kimura H, Ono M, Shimizu Y, Kimura H, Ono M, Nakamoto Y, Togashi K, Saji H. Gallium-68-labeled anti-HER2 single-chain Fv fragment: development and in vivo monitoring of HER2 expression. Mol Imaging Biol 2015; 17: 102-110.
21. D'Huyvetter M, Vincke C, Xavier C, Aerts A, Impens N, Baatout S, De Raeve H, Muyldermans S, Caveliers V, Devoogdt N, Lahoutte T. Targeted radionuclide therapy with A 177Lu-labeled anti-HER2 nanobody. Theranostics 2014; 4: 708-720.
22. D'Avino C, Paciello R, Riccio G, Coppola M, Laccetti P, Maurea N, Raines RT, De Lorenzo C. Effects of a second-generation human anti-ErbB2 ImmunoRNase on trastuzumab-resistant tumors and cardiac cells. Protein Eng Des Sel 2014; 27: 83-88.
23. Sokolova EA, Zdobnova TA, Stremovskiy OA, Balalaeva IV, Deyev SM. Novel recombinant anti-HER2/neu immunotoxin: design and antitumor efficiency. Biochem (Mosc) 2014; 79: 1376-1381.
24. Dou S, Yang X-Z, Xiong M-H, Sun C-Y, Yao Y-D, Zhu Y-H, Wang J. ScFv-decorated PEG-PLA-based nanoparticles for enhanced siRNA delivery to Her2+ breast cancer. Adv Healthc Mater 2014; 3: 1792-1803.
25. Leung K-M, Batey S, Rowlands R, Isaac SJ, Jones P, Drewett V, Carvalho J, Gaspar M, Weller S, Medcalf M, Wydro MM, Pegram R, Mudde GC, Bauer A, Moulder K, Woisetschläger M, Tuna M, Haurum JS, Sun, H. A HER2-specific modified Fc fragment (Fcab) induces antitumor effects through degradation of HER2 and apoptosis. Mol Ther 2015; 23: 1722-1733.
26. Nejatollahi F, Jaberipour M, Asgharpour M. Triple blockade of HER2 by a cocktail of anti-HER2 scFv antibodies induces high antiproliferative effects in breast cancer cells. Tumor Biol 2014; 35: 7887-7895.
27. Bull-Hansen B, Berstad MB, Berg K, Cao Y, Skarpen E, Fremstedal AS, Rosenblum M, Peng Q, Weyergang A. Photochemical activation of MH3-B1/rGel: a HER2-targeted treatment approach for ovarian cancer. Oncotarget 2015; 6: 12436-12451.
28. De Lorenzo C, Cozzolino R, Carpent ieri A, Pucci P, Laccetti P, D'Alessio G. Biological properties of a human compact anti-ErbB2 antibody. Carcinogenesis 2005; 26: 1890-1895.
29. Hu S, Shively L, Raubitschek A, Sherman M, Williams LE, Wong JYC, Shively JE, Wu AM . Minibody: a novel rngineered anti-carcinoembryonic antigen antibody fragment (Single-Chain Fv-CH3) which exhibits rapid, high-level targeting of xenografts. Cancer Res 1996; 56: 3055-3061.
30. Olafsen T, Tan GJ, Cheung C, Yazaki PJ, Park JM, Shively JE, Williams LE, Raubitschek AA, Press MM, Wu AM. Characterization of engineered anti-p185HER-2 (scFv-CH3)2 antibody fragments (minibodies) for tumor targeting. Protein Eng Des Sel 2004; 17: 315-323.
31. Yao-Ming H, WeiWei H, Eddie R, Kevin C, Helena Y, Thomas R. Maximizing productivity of CHO cell-based fed-batch culture using chemically defined media conditions and typical manufacturing equipment. Biotechnol Prog 2010; 26: 1400-1410.
32. Duncan AR, Woof JM, Partridge LJ, Burton DR, Winter G. Localization of the binding site for the human high-affinity Fc receptor on IgG. Nature 1988; 332: 563-564.
33. Canfield S, Morrison SL. The binding affinity of human IgG for its high affinity Fc receptor is determined by multiple amino acids in the CH2 domain and is modulated by the hinge region. J Exp Med 1991; 173: 1483-1491.
34. Clark M. IgG effector mechanisms. Chem Immunol 1997; 65: 88-110.
35. Nimmerjahn F, Ravetch JV. Fc? receptors as regulators of immune responses. Nat Rev Immunol 2008; 8: 34-47.
36. Kumar N, Gammell P, Clynes M. Proliferation control strategies to improve productivity and survival during CHO based production culture: A summary of recent methods employed and the effects of proliferation control in product secreting CHO cell lines. Cytotechnology 2007; 53: 33-46.
37. Sunley K, Butler M. Strategies for the enhancement of recombinant protein production from mammalian cells by growth arrest. Biotechnol Adv 2010; 28: 385-394.
38. hant RJ, Carden MJ, Smales CM. The coldshock response in cultured mammalian cells: harnessing the response for the improvement of recombinant protein production. Biotechnol Bioeng 2005; 93: 829-835.
Notas de autor
Autor de correspondencia: Jaheli Fuenmayor, Centro de Medicina Experimental, Instituto Venezolano de Investigaciones Científicas, Caracas, Venezuela. Teléfono: 0058-212-5041158. Correo electrónico: jfuenmay@ivic.gob.ve
