Originales
Recepción: 15 Septiembre 2018
Aprobación: 15 Enero 2019
Resumen:
Objetivo: Conocer la frecuencia de osteoporosis en hombres mayores de 50 años y sus factores de riesgo, en la parroquia Juan Rodríguez Suarez del Municipio Libertador del Estado Mérida, Venezuela.
Métodos: Se realizó un estudio observacional, transversal, aleatorizado. A cada sujeto se le realizó una historia clínica, incluyendo el test para hipogonadismo. Se midieron niveles de testosterona total y globulina transportadora de hormonas sexuales (SHBG), y se realizó densitometría ósea de cuello femoral y columna lumbar.
Resultados: Se estudiaron 75 hombres, con edad promedio de 61,15 ± 7,78 años, el valor máximo se ubicó en 84 años y el mínimo en 50 años. Según los resultados de la densitometría ósea: 44% era normal (Grupo 1), 42,3% tenía osteopenia (Grupo 2) y 13,3% osteoporosis (Grupo 3). El peso, el índice masa corporal (IMC) y la circunferencia de cintura estuvieron significativamente más bajos en los grupos 2 y 3 en comparación con el grupo 1 (p<0,05 y p<0,001, respectivamente). El hábito tabáquico, el sedentarismo y el consumo de alcohol fueron los factores de riesgo predominantes en todos los pacientes estudiados.
Conclusión: En el grupo estudiado se observó una frecuencia de 13,3% de osteoporosis y 42,3% de osteopenia. No hubo asociación con factores de riesgo clásicos de osteoporosis, excepto por una menor adiposidad entre aquellos hombres afectados con osteopenia y osteoporosis. No se observaron causas de osteoporosis secundaria.
Palabras clave: Osteoporosis en hombres, osteopenia, testosterona, densitometría ósea.
Abstract:
Objective: To know the frequency of osteoporosis in men older than 50 years old and its risk factors, in the Juan Rodríguez Suarez parish of the Libertador Municipality of the Mérida State, Venezuela.
Methods: An observational, cross-sectional, randomized study was conducted. Each subject underwent a medical history, including the test for hypogonadism. Levels of total testosterone and sex hormone binding globulin (SHBG) were measured, and bone densitometry of the femoral neck and lumbar spine was performed.
Results: Seventy-five men, with an average age of 61.15 ± 7.78 years were studied, the maximum value was 84 years old and the minimum was 50 years. According to the results of bone densitometry: 44% was normal (Group 1), 42.3% had osteopenia (Group 2) and 13.3% osteoporosis (Group 3). Weight, body mass index (BMI) and waist circumference were significantly lower in groups 2 and 3 compared to group 1 (p< 0.05 and p< 0.001, respectively). Smoking, sedentary lifestyle and alcohol consumption were the prevalent risk factors in all the studied patients.
Conclusion: In the group studied, a frequency of 13.3% of osteoporosis and 42.3% of osteopenia was observed. There was no association with classic risk factors for osteoporosis, except for a lower adiposity among men affected with osteopenia and osteoporosis. No causes of secondary osteoporosis were observed.
Keywords: Male osteoporosis, testosterone, bone densitometry, osteopenia.
INTRODUCCIÓN
La osteoporosis es una enfermedad sistémica caracterizada por disminución de la masa ósea, deterioro de la microarquitectura del tejido óseo y aumento en el riesgo de fractura1,2. En el hombre, la tasa de pérdida de la densidad mineral ósea (DMO) es de hasta 1% por año en la edad avanzada, y uno de cada ocho hombres por encima de los 50 años experimentará una fractura relacionada con osteoporosis2,3. La pérdida de masa ósea en hombres se acelera después de los 70 años y es más progresiva cuando hay déficit de esteroides sexuales4,5. A diferencia de la osteoporosis de la mujer en la menopausia, donde hay pérdida del hueso trabecular, en los hombres, se produce un adelgazamiento del hueso trabecular secundario a la reducción de la formación ósea4, preservándose el número de trabéculas, lo que explica su menor riesgo de fracturas, aunado al mayor tamaño de los huesos largos2,3,4.
Un tercio de las fracturas de cadera en el mundo ocurre en hombres, con una mayor mortalidad que en la mujer, de 37,5%. El 20% de los hombres con fracturas de cadera presentan una segunda fractura6. En el estudio de Rotterdam se observó que los sitios de mayor frecuencia de fractura en la población mayor de 55 años son el fémur proximal, el antebrazo y el húmero, con riesgo similar de fractura de cadera y otras entre ambos sexos1. La incidencia de fracturas en el sexo masculino tiene un repunte bimodal, en la adolescencia asociada a la actividad física y la alta frecuencia de traumatismos por el deporte y ejercicios extremos, y en la tercera edad, vinculado a la osteoporosis7,8. En ambos géneros existe una elevación exponencial en la incidencia de fracturas después de los 75 años, particularmente fracturas de cadera; sin embargo, la incidencia absoluta tiende a ser más baja en el sexo masculino7,8. En el estudio multicéntrico Canadiense de osteoporosis (CAMOS)9, las deformidades vertebrales, comúnmente asociadas a fractura, se ven tan frecuentes en hombres como en mujeres, reportándose una prevalencia en mayores de 50 años de 21,5% y 23,5% respectivamente.
El diagnóstico de osteoporosis en hombres mayores de 50 años de edad, se realiza cuando el valor del T-score es menor de - 2,5 desviaciones estándar (DS), de acuerdo con el criterio de la Organización Mundial de la Salud (OMS). En hombres menores de 50 años, se recomienda la utilización del Z-score, considerando un estado de osteoporosis cuando éste muestra 2 DS por debajo de lo normal para la edad, relacionando ese valor con la media para la población de la misma edad. La osteopenia no debería ser considerada como un diagnóstico. En su lugar, pacientes sobre 50 años de edad con T-score entre -2,5 y -1,5 deberían ser catalogados como “densidad ósea reducida”, y un diagnóstico de osteoporosis, con esos valores de T-score, solo ante la presencia de fractura. Es importante hacer notar que los pacientes con DMO reducida pueden no ser necesariamente considerados en riesgo incrementado de fractura, tales pacientes deberían ser analizados con su estratificación para riesgo de fractura a través de algún instrumento validado incluso en la población venezolana, como por ejemplo, “Fracture Risk Assessment Tool” (FRAX)1,5,6,10,11.
Las razones por las cuales las mujeres presentan mayor tasa de fractura que los hombres obedece a que estos alcanzan un pico de masa ósea más alto, experimentan una tasa más baja de pérdida ósea a medida que progresan en años, carecen de un equivalente a la fase menopáusica de la mujer y, por último, tienen una expectativa de vida más corta. Las diferencias en el patrón de la pérdida de hueso sobre el tiempo, también contribuyen a la ventaja biomecánica en los hombres con la edad, ya que aunque también experimentan una resorción ósea endocortical aumentada con la edad, la formación del periostio en el hombre es mayor2,3,7,12,13,14.
En el estudio prospectivo de osteoporosis en hombres en Montceau les Mines (MINOS), el aumento de la edad se relacionó con deformidad vertebral y disminución de la DMO en cadera15. El estudio europeo de osteoporosis (EPOS), con un registro de 29 centros y un total de 14.011 individuos mayores de 50 años, reportó una incidencia de fracturas vertebrales de 6,8% en hombres y 12,1% en mujeres, siendo la ubicación más frecuente en T12 y L116. Adicionalmente, en el estudio europeo de osteoporosis de columna vertebral (EVOS), que reclutó 15.570 hombres y mujeres con edades entre 50 y 79 años, en 36 centros de 19 países, se determinó que la prevalencia estandarizada de deformidad vertebral fue de 12% para los hombres y de 20,2% para las mujeres, utilizando el criterio de Eastell, y del 12% utilizando el de Mc Closkey17.
De acuerdo a los criterios de la OMS, se estima que de 1 a 2 millones de hombres en los Estados Unidos tienen osteoporosis y entre 8 a 13 millones tienen osteopenia18. Las cifras de prevalencia respectivas ajustadas por edad son impresionantes, 6% para osteoporosis y 47% para osteopenia19,20. En el NHANES III, la prevalencia de osteoporosis en hombres fue del 6% y del 19% estimada por riesgo de fractura21. En el estudio CAMOS, la identificación de riesgo absoluto de fractura integrando a los factores de riesgo, tales como la edad, la DMO, el diagnóstico de fracturas previas, antecedentes familiares de fracturas, el uso de glucocorticoides, el tabaquismo y el sedentarismo, entre los más importantes, demostró una asociación negativa en pacientes con fracturas por osteoporosis y su calidad de vida9.
Las principales causas de osteoporosis secundaria en el varón son el hipogonadismo, la administración de corticoides y el alcoholismo crónico; entre otras causas se destacan la baja ingesta de calcio y el déficit de vitamina D, la gastrectomía, la enfermedad pulmonar obstructiva crónica y la hipercalciuria22,23,24,25. Moro y cols observaron una frecuencia de 15 a 30% de hipogonadismo en su serie. Los niveles de testosterona sérica disminuyen con la edad, ocasionando un déficit estrogénico que favorece la fragilidad ósea14. Kelly y cols en pacientes ancianos con fracturas vertebrales encontraron bajos niveles de testosterona en el 59% comparado con un 18% del grupo control. Asimismo, se ha descrito que este déficit androgénico puede disminuir la síntesis de 1,25-dihidroxivitamina D, provocando una reducción de la absorción intestinal de calcio y de la formación ósea26.
En nuestro país se han realizado pocos estudios sobre osteoporosis en la población masculina, debida a esto, se decidió evaluar la frecuencia de osteoporosis en hombres mayores de 50 años, así como los factores de riesgo relacionados con la enfermedad, en una muestra del Municipio Libertador del Estado Mérida.
MATERIALES Y MÉTODOS
Sujetos:
Se realizó un estudio observacional, transversal y aleatorizado para determinar la frecuencia de osteoporosis en hombre mayores de 50 años en la parroquia Juan Rodríguez Suárez del Municipio Libertador del estado Mérida en Venezuela, durante el período comprendido entre agosto 2010 y agosto del 2011. Tomando como base el censo del año 2011, se realizó el calculó de la muestra y se utilizó una tabla de números aleatorios en los sectores de dicha población siendo seleccionados los sujetos de las casas que correspondieron a números pares según la tabla. Cada sujeto fue informado verbalmente sobre los objetivos y beneficios de la investigación y antes de ingresar al estudio dio su consentimiento por escrito.
Procedimiento:
A cada sujeto se le llenó una historia clínica, se le realizó una anamnesis para obtener los antecedentes sobre patologías personales (diabetes, hipogonadismo, enfermedad tiroidea, cáncer de próstata, hipercortisolismo), factores de riesgo de osteoporosis y fracturas (hábito tabáquico, alcohol, uso de esteroides, anticomiciales, y otros fármacos que alteren el metabolismo óseo); además se interrogó sobre antecedentes personales y familiares de fracturas previas. Se consideró consumo de alcohol la ingesta de 2 o más copas diarias; tabaquismo al individuo que fuma diariamente en la actualidad. Se realizó un examen clínico integral y se tomaron las variables de edad, peso, talla, presión arterial, frecuencia cardíaca, índice de masa corporal (IMC) y circunferencia de cintura (CC). El IMC fue calculado por la fórmula de Quetelet donde IMC= Peso (Kg)/Talla2 (m2)27.
Cada sujeto fue citado en ayunas de 12 horas para la toma de muestra de sangre venosa periférica, y se llenó el cuestionario de la escala de puntuación de síntomas de hipogonadismo de los varones de edad avanzada o AMSS por sus siglas en inglés Aging Males Symptoms; éste incluye una escala de puntuación de síntomas de hipogonadismo, en un cuestionario de 17 preguntas que valora la intensidad de los síntomas en una escala de 1 a 5, y permite categorizar a los pacientes en una escala de síntomas inexistentes cuando alcanza menos de 26 puntos, síntomas leves 25 a 36 puntos, síntomas moderados 27 a 49 puntos y síntomas severos mayores de 50 puntos28. A todos los sujetos se le realizó la densitometría ósea de cuello femoral y columna lumbar con un equipo HOLOGIC DISCOVERY QDR utilizando la técnica de absorciometría dual por emisión de Rx. Se obtuvieron valores que se expresaron en densidad mineral ósea (gr/cm2), contenido mineral óseo (g) y pérdida porcentual (%) con respecto a la población hispánica de referencia adulto joven. La conclusión diagnóstica se realizó de acuerdo a la clasificación recomendada por la OMS en hombres mayores de 50 años de edad; se consideró osteoporosis un valor de T-score menor de - 2,5 DS, masa ósea baja u osteopenia T-score entre -2,5 y -1,5, y normal un T score mayor de -1,5. A todos los pacientes se les aplicó la herramienta para el calculó de riesgo de fractura FRAX en general y para cadera (FRAX HIP), herramienta accesible online para población latina, la cual evalúa una seria de factores de riesgo clínico adicional a la DMO, que permite el cálculo de riesgo absoluto de fractura osteoporótica global y de fractura de cadera en los próximos 10 años en la población en estudio.
La muestra de sangre venosa periférica se centrifugó y se obtuvo el suero, el cual se almacenó a -70 grados centígrados hasta el momento que se realizó el análisis; se determinó el nivel de testosterona total y de globulina transportadora de hormonas sexuales (SHBG). La testosterona total se midió con el método de quimioluminiscencia, IMMULITE/IMMULITE 1000, de laboratorio Siemens Healthcare Diagnostics, Erlangen, Alemania, el cual es un inmunoensayo enzimático quimioluminiscente competitivo de fase sólida; los rangos de referencia para hombres ≥50 años son de 181-758 ng/dL, con una mediana de 427 e intervalo absoluto 181-772. La SHBG fue medida por quimioluminiscencia, con el método de IMMULITE/ IMMULITE 1000, de laboratorio Siemens Healthcare Diagnostics, Erlangen, Alemania, el cual es un ensayo inmunométrico quimioluminiscente de fase sólida; los rangos de referencia para muestras del hombre adulto con niveles normales de testosterona son de 13-71 nmol/l, con una mediana de 32 nmol/l.
Análisis Estadístico
Las variables continuas se presentan en promedio ± desviación estándar y las categóricas en número absoluto y porcentajes. Se estableció el número y porcentaje de pacientes que cumplieron con los criterios diagnósticos de osteopenia y osteoporosis, y se compararon con los sujetos normales mediante la aplicación del Chi2 o test de Fisher. Para la comparación de promedios se aplicó el t-student y el ANOVA. Se aplicó una matriz de correlación de Pearson entre las variables cuantitativas. Se utilizó el programa SPSS versión 19 para Windows. El nivel de significancia empleado fue una p <0,05.
RESULTADOS
Se estudiaron 75 hombres mayores de 50 años, residentes en el Municipio Libertador. El promedio de edad fue 61,15 ± 7,78 años, el valor máximo se ubicó en 84 años y el mínimo en 50 años. De acuerdo a los resultados de la densitometría ósea, según los criterios de la OMS, el 44% presentó densitometría ósea normal (Grupo 1), el 42,7% osteopenia (Grupo 2) y el 13,3% osteoporosis (Grupo 3). Dentro del grupo con osteoporosis, el 60% presentó osteoporosis de columna lumbar, el 30% mixta, tanto de columna lumbar como femoral, y el 10% osteoporosis a nivel de cuello femoral. En la tabla I, se describen las variables demográficas y clínicas de los pacientes estudiados, divididos según diagnóstico por DMO. La circunferencia abdominal, el peso y el IMC en los hombres con alteración de la DMO (Grupos 2 y 3) fueron significativamente menores con respecto a aquellos con DMO normal (Grupo 1; p<0,05 y p<0,001, respectivamente); además, la circunferencia de cintura fue significativamente menor en el Grupo 3 con respecto al Grupo 2 (p<0,05). Esto refleja que a menor IMC y circunferencia abdominal hubo mayor pérdida de masa ósea. El resto de las variables estudiadas fueron similares en los 3 grupos; llama la atención que los indicadores de hipogonadismo, testosterona total y score de AMSS, no mostraron diferencias.
Variables demográficas y clínicas de los pacientes estudiados según resultados de densitometría ósea
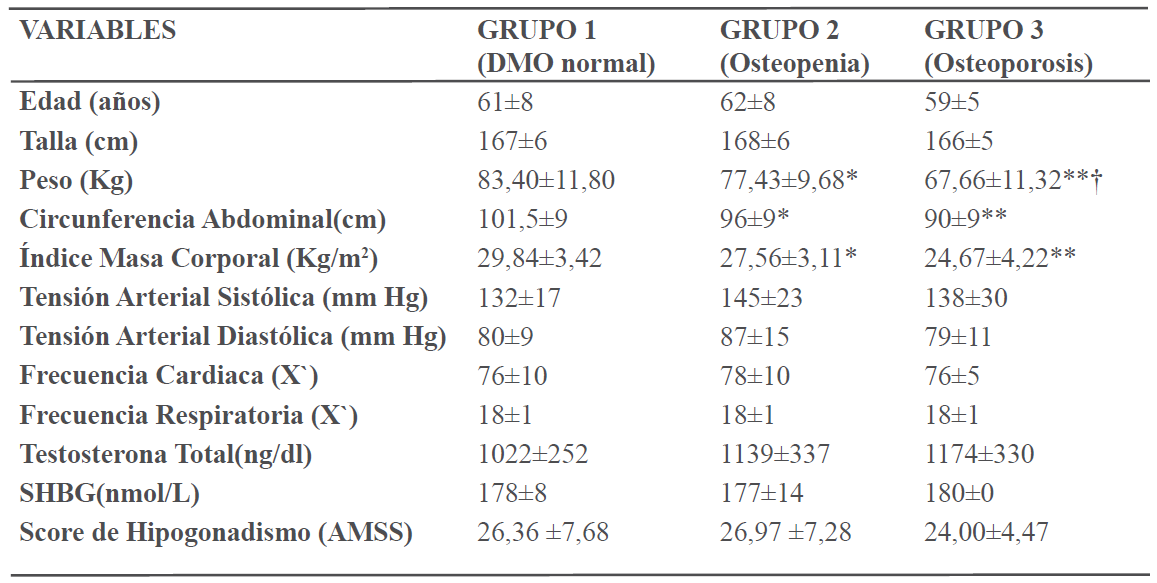
Datos en X±DE. ANOVA *p < 0,05 **p < 0,001 vs Grupo 1. † p <0,05 vs Grupo 2; AMSS: Aging Males Symptoms
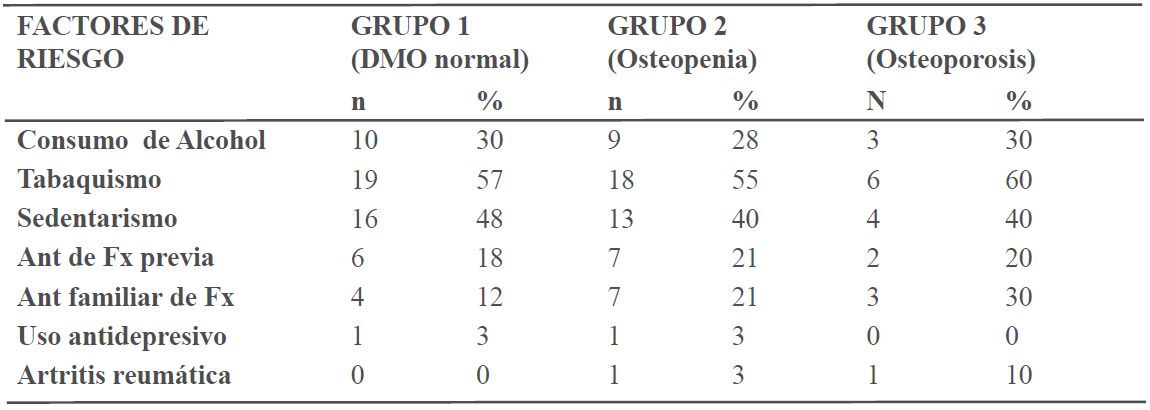
Entre los factores de riesgo estudiados, predominaron el tabaquismo, el sedentarismo y el consumo de alcohol. No se encontró una diferencia significativa entre los grupos de alteración de la DMO y la presencia de factores de riesgo para osteoporosis. No hubo casos de hipogonadismo ni de consumo de glucocorticoides (Ver tabla II).
Como era de esperar, en la tabla III se observa que la DMO está significativamente más baja en los grupos 2 y 3 en comparación con el grupo 1 (DMO normal), así como los valores de T-score de fémur y columna (p<0,001). Cuando se analizan los resultados del FRAX y el FRAX HIP, se observa que el mayor porcentaje de riesgo de fractura obtenido se encontraba en los grupos con osteopenia y osteoporosis, lo que demuestra una relación directa de ésta con la DMO (p<0,001).
Las patologías asociadas más frecuentes en los pacientes estudiados fueron: hipertensión arterial (42%), hiperplasia prostática benigna (16%), diabetes mellitus (10%), asma bronquial (8%), litiasis renal (2,6%), artritis reumatoide (2,6%) y cáncer de vejiga (1%). El 21% niega enfermedad asociada. No se observó correlación significativa entre el nivel de testosterona, el test de hipogonadismo y la densidad mineral ósea, sin embargo, fue evidente una correlación positiva entre la edad y el test de hipogonadismo (r = 0,515, p <0,001).
Factores de riesgo de osteoporosis en los pacientes estudiados según resultados de densitometría ósea
Valores de la densidad mineral ósea (DMO), T-score de fémur y columna lumbar y Herramienta FRAX en los pacientes estudiados según resultados de densitometría ósea.
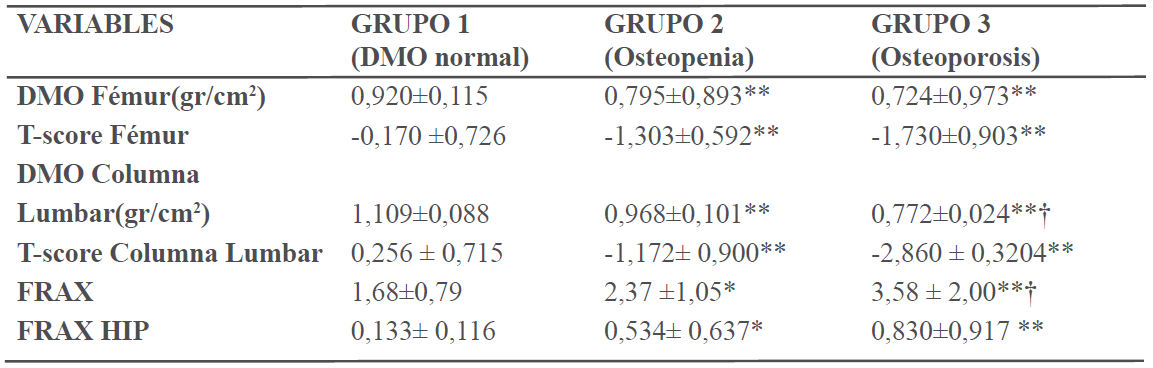
Datos en X±DE. ANOVA: * p< 0,05 ** < 0,001 vs Grupo 1; † p<0,001 vs Grupo 2
DISCUSIÓN
La prevalencia de la osteoporosis en hombres ha aumentado a nivel mundial en los últimos años. Khosla y cols7 utilizando los datos del NHANES III, observaron una prevalencia en hombres del 6% de osteoporosis y 47 % de osteopenia. Jaller y cols29 en un estudio realizado en Colombia, en una población de 401 hombres mayores de 20 años, reportaron osteoporosis en el 18,5%, osteopenia en el 34,4% y densitometría normal en el 52,9%; aproximadamente un tercio se clasificó con osteoporosis primaria (37,2%) y las dos terceras parte restantes tenían una causa secundaria bien conocida (62,8%). Así mismo, en sus resultados resaltan que las causas más frecuentes de osteoporosis fueron el consumo de esteroides en 21,7%, la artritis reumatoide 19,6% y el cáncer de próstata 6,5%, entre otras. Llama la atención que estos pacientes estudiados fueron extraídos de una consulta de enfermedades crónicas, lo que hace una incidencia mayor de osteoporosis secundaria en individuos más jóvenes. En nuestra serie, la frecuencia fue 13,3% de osteoporosis, con predominio de afectación lumbar (60% de los casos), y 42,3% de osteopenia, no asociada a una patología de base, la cual se asemeja más a los resultados del NHANES7, aunque con una incidencia mayor con respecto a osteoporosis.
La aplicación del instrumento FRAX corrobora que los pacientes con menor DMO tienen mayor riesgo de fractura, lo cual enfatiza su eficacia. Los resultados presentados por Briot y cols30 en Francia muestran una prevalencia de osteoporosis en hombres mayores de 50 años de 13% frente a 40% en mujeres, y riesgo de presentar una fractura osteoporótica de 15%; los resultados en hombres son similares a los nuestros, lo que nos asemeja más a la población francesa. Además de esto, ellos no encontraron factores de riesgo predominantes, y determinaron que la osteopenia fue la primera manifestación de la historia natural de la enfermedad que debe alertarnos a prevenir, diagnosticar y seguir el curso de la misma. Esta similitud con la población francesa, pudiera estar relacionada con los valores del IMC y la circunferencia de cintura de nuestros pacientes estudiados, los cuales se asemejan a los de los parisinos.
Datos obtenidos por Zhao y cols31 mostraron que existe una correlación inversa entre el tejido adiposo y la masa ósea. El valor más bajo de IMC y de cintura abdominal tiene más riesgo de osteoporosis, similar a nuestros hallazgos, donde los grupos afectados mostraron menores valores de peso, IMC y circunferencia de cintura. El peso corporal es considerado un predictor de masa ósea tanto en hombres como en mujeres. Estudios epidemiológicos han reportado que el IMC elevado se correlaciona positivamente con un aumento de la DMO y con reducción del riesgo de facturas. La explicación de esta relación se centra en que un mayor IMC induce una mayor carga mecánica sobre el hueso, con un incremento de la formación ósea, sumado a una beneficiosa mayor formación de estrógenos a nivel del tejido adiposo32,33. Según Maclaughlin y cols 34, un IMC menor o igual a 20 kg/m2 incrementa el riesgo de fractura, mientras que un IMC mayor o igual a 30 Kg/m2 reduce el riesgo de fractura de cadera.
Pereira y cols19 en Caracas, Venezuela, estudiaron a 49 hombres entre ambulatorios y hospitalizados en el Hospital del Oeste, donde evidenciaron 42,9% de osteopenia, 24,4% osteoporosis y 32,7% con densitometría normal. Es importante señalar que todos los pacientes tenían factores de riesgo para osteoporosis, entre los cuales destacaban la desnutrición, el uso de glucocorticoides, la hepatopatía alcohólica, el uso de hormonas tiroideas, entre otras. Al confrontar estos resultados con el obtenido en nuestra población, tomada de la población general, se considera que la diferencia radica en que ellos tenían un gran número de factores de riesgo para osteoporosis secundaria, lo que explica la incidencia mayor de la misma.
Al evaluar los factores de riesgo, se encontró que el hábito tabáquico, el sedentarismo y el consumo de alcohol fueron los predominantes en todos los grupos; es importante señalar que los pacientes con alguna alteración tenían al menos un factor de riesgo para osteopenia y osteoporosis. Según Haney y cols1, aproximadamente entre 30 y 60% de los hombres presentan osteoporosis secundaria, y entre las causas principales de esta destacan el consumo excesivo de alcohol, la terapia con glucocorticoides y el hipogonadismo. En nuestra población, no se observaron factores determinantes causantes de osteoporosis secundaria, ya que estos tres factores mencionados estuvieron presentes en los tres grupos. Además, no se observó correlación entre los niveles de testosterona, el test de hipogonadismo y la densidad mineral ósea. La mayoría de los pacientes presentaron niveles de SHBG elevados con testosterona normal. Según Le Blanc y cols35, la SHBG se asocia a fractura de una manera independiente o combinada con esteroides sexuales.
En el estudio de Jaller y cols29, fumar fue el factor de riesgo predominante para osteoporosis, en un 28,2%. En el estudio European Vertebral Osteoporosis Study (EVOS)17 con 15.570 hombres y mujeres se encontró una relación significativa entre los factores de riesgo y la presencia de fracturas vertebrales. Shepherd y cols36, al evaluar el NHANES III y compararlo con The Male Osteoporosis Risk Estimation Score (MORES)37, reportaron que el IMC bajo (menor de 22 kg/m2), el hábito tabáquico y el sedentarismo son factores de riesgo independiente para osteoporosis, y la presencia de uno o más factores predispone a la misma. En nuestro estudio no se midieron valores de vitamina D, ni hormonas tiroideas que pudieran ser estudiados como factores determinantes de osteoporosis.
Similar a otros estudios, las patologías asociadas más frecuentes en los pacientes estudiados fueron hipertensión arterial 42%, diabetes mellitus 10%, hiperplasia prostática benigna 16%, asma bronquial 8%, litiasis renal 2,6%, cáncer de vejiga 1%, y el 21% niega enfermedad asociada. Barret y cols38 en el estudio MrOs en 5.995 sujetos mayores de 65 años encontraron que 43,4% de ellos tenía antecedente de hipertensión arterial y 10,8 % diabetes mellitus. Sin embargo, en nuestro estudio no se encontró asociación entre estas patologías y la presencia de DMO baja.
De acuerdo a nuestros hallazgos, se concluye que en el grupo de hombres mayores de 50 años estudiados, provenientes de la población general, la frecuencia de osteoporosis fue de 13,3%, osteopenia de 42,7% y masa ósea adecuada o normal de 44%, con predominio de osteoporosis lumbar. No hubo asociación con factores de riesgo clásicos de osteoporosis, excepto por la menor adiposidad entre aquellos hombres afectados con osteopenia y osteoporosis. En la población estudiada no se observaron causas de osteoporosis secundaria.
Es importante que este estudio abra las puertas para el desarrollo de investigaciones futuras que consideren los factores riesgo y así llegue a entenderse un poco más la etiología de un gran problema de salud pública como es la osteoporosis en hombres.
REFERENCIAS BIBLIOGRÁFICAS
1. Haney E.,Bliziotes M. Male osteoporosis: new insights in an understudied disease. Curr Opin Rheumatol 2008;20:423-428.
2. Khosla S, Amin S and Orwoll E. Osteoporosis in men. Endocrin Rev 2008; 29,4: 441-464.
3. Vanderschueren D, Laurent MR, Claessens F, Gielen E, Lagerquist MK, Vandenput L, Börjesson AE, Ohlsson C. Sex steroid actions in male bone. Endocr Rev 2014; 35:906-960.
4. Gennari L, Bilezikian JP. Osteoporosis in men. Endocrinol Metab Clin North Am 2007, 36:399-419.
5. Cheung A. Osteoporosis: the connection to urologic health. Can Urol Assoc J 2014;8:S156-158.
6. Khan AA, Bachrach L, Brown JP, Hanley DA, Josse RG, Kendler DL, Leib ES, Lentle BC, Leslie WD, Lewiecki EM, Miller PD, Nicholson RL, O'Brien C, Olszynski WP, Theriault MY . Standards and guidelines for performing central dual-energy x-ray absorptiometry in premenopausal women, men, and children. J Clin Densitom 2004;7:51-64.
7. Khosla S, Lawrence RB, Atkinson EJ, Oberg LA, McDaniel LJ, Holets M, Peterson JM, Melton LJ. Effects of sex and age on bone microstructure at the ultradistal radius: a population- based noninvasive in vivo assessment. J Bone Miner Res 2006;21:124-131.
8. Olszynski WP, Shawn DK, Adachi JO. Osteoporosis in men: epidemiology, diagnosis, prevention, and treatment. Clin Ther 2004;26:15-28.
9. Jackson SA, Tenenhouse A, Robertson L. Vertebral fracture definition from population- based data: preliminary results from the Canadian Multicenter Osteoporosis Study (CAMOS). Osteoporos Int 2000;11:680-687.
10. Kanis JA, Oden A, Johansson H, Borgström F, Ström O, McCloskey E. FRAX and its applications to clinical practice. Bone 2009;44:734-743.
11. Riera-Espinoza G, Lopez D, Kanis JA. Life time risk of hip fracture and incidence rates in Carabobo, Venezuela. Osteoporos Int 2008;19 (Suppl. 2):S356.
12. Fink HA, Ewing SK, Eusrud KE, Barret-Connor E, Taylor BC, Cauley JA, Orwoll ES. Association of testosterone and estradiol deficiency with osteoporosis and rapid bone loss in older men. J Clin Endocrinol Metab 2006;91:3908-3915.
13. Ebeling P. Osteoporosis in men N Engl J Med 2008;358:1474-1482.
14. Moro-Álvarez MJ, Blázquez J.A. Osteoporosis en el varón. Rev Clin Esp 2010;210:317-370.
15. Szulc P, Munoz F, Marchand F, Delmas PD. Semiquantitative evaluation of prevalent vertebral deformities in men and their relationship with osteoporosis: the MINOS study. Osteoporos Int 2001;12:302-310.
16. Roy DK, O'Neill TW, Finn JD, Lunt M, Silman AJ, Felsenberg D, Armbrecht G, Banzer D, Benevolenskaya LI, Bhalla A, Bruges Armas J, Cannata JB, Cooper C, Dequeker J, Diaz MN, Eastell R, Yershova OB, Felsch B, Gowin W, Havelka S, Hoszowski K, Ismail AA, Jajic I, Janott I, Johnell O, Kanis JA, Kragl G, Lopez Vaz A, Lorenc R, Lyritis G, Masaryk P, Matthis C, Miazgowski T, Gennari C, Pols HA, Poor G, Raspe HH, Reid DM, Reisinger W, Scheidt-Nave C, Stepan JJ, Todd CJ, Weber K, Woolf AD, Reeve J; European Prospective Osteoporosis Study (EPOS). Determinants of incident vertebral fracture in men and women: results from the European Prospective Osteoporosis Study (EPOS). Osteoporos Int 2003;14:19-26.
17. Armbrecht G, Felsenberg D, Ganswindt M, Lunt M, Kaptoge SK, Abendroth K, Aroso Dias A, Bhalla AK, CannataAndia J, Dequeker J, Eastell R, Hoszowski K, Lyritis G, Masaryk P, van Meurs J, Miazgowski T, Nuti R, Poór G, Redlund-Johnell I, Reid DM, Schatz H, Todd CJ, Woolf AD, Rivadeneira F, Javaid MK, Cooper C, Silman AJ, O'Neill TW, Reeve J. Degenerative inter-vertebral disc disease osteochondrosis intervertebralis in Europe: prevalence, geographic variation and radiological correlates in men and women aged 50 and over. Rheumatology 2017;56:1189-1199.
18. Willson T, Nelson S, Newbold J, Nelson RE, LaFleur J. The clinical epidemiology of male osteoporosis: a review of the recent literature. Clin Epidemiol 2015;7:65-76.
19. Pereira JM, Essenfeld E. Epidemiología de la osteoporosis en una población masculina. Rev Med Int 2010;26:124-132.
20. Rizzoli R, Branco J, Brandi ML, Boonen S, Bruyère O, Cacoub P, Cooper C, Diez-Pérez A, Duder J, Fielding RA, Harvey NC, Hiligsmann M, Kanis JA, Petermans J, Ringe JD, Tsouderos Y, Weinman J, Reginster JY. Management of osteoporosis of the oldest old. Osteoporos Int 2014;25:2507-2529.
21. Cosman F, Krege JH, Looker AC, Schousboe JT, Fan B, SarafraziIsfahani N, Shepherd JA, Krohn KD, Steiger P, Wilson KE, Genant HK. Spine fracture prevalence in a nationally representative sample of US women and men aged ≥40 years: results from the National Health and Nutrition Examination Survey (NHANES) 2013-2014. Osteoporos Int 2017;28:1857-1866.
22. Misiorowski W. Osteoporosis in men. Menopause Rev 2017;16:70-73.
23. Golds G, Houdek D, Arnason T. Male hypogonadism and osteoporosis: the effects, clinical, consequences, and treatment of testosterone deficiency in bone health. Int J Endocrinol 2017;2017: 4602129. doi: 10.1155/2017/4602129.
24. Tolba MF, El-Serafi AT, Omar HA. Caffeic acid phenethyl ester protects against glucocorticoid- induced osteoporosis in vivo: impact on oxidative stress and RANKL/OPG signals. Toxicol Appl Pharmacol 2017;324:26-35.
25. Luo Z, Liu Y, Liu Y, Chen H, Shi S, Liu Y. Cellular and molecular mechanisms of alcohol-induced osteopenia. Cell Mol Life Sci 2017;74:4443-4453.
26. Kelly JJ, Moses M. Osteoporosis in men: the role of testosterone and other sex-related factors. Curr Opin Endocrinol Diabetes 2005;12:452-458.
27. Jurguin C. Quetelet's scientific work. science. 1924;60:351-352.
28. Wang C, Nieschlag E, Swerdloff R, Behre HM, Hellstrom WJ, Gooren LJ, Kaufman JM, Legros JJ, Lunenfeld B, Morales A, Morley JE, Schulman C, Thompson IM, Weidner W, Wu FC; International Society of Andrology; International Society for the Study of Aging Male; European Association of Urology; European Academy of Andrology; American Society of Andrology. Investigation, treatment, and monitoring of late-onset hypogonadism in males: ISA, ISSAM, EAU, EAA, and ASA recommendations. Eur Urol 2009;55:121-130.
29. Jaller R, Navarro E, Varga RF. Osteoporosis y factores de riesgo en una población masculina latinoamericana. Rev Colom Reumatol 2007;14: 99-105.
30. Briot K, Cortet B, Trémolliéres F, Sutter B, Thomas T, Roux C, Audran M, Comité Scientifique du GRIO. Male osteoporosis: diagnosis and fracture risk evaluation. Joint Bone Spine 2009;76:129-133.
31. Zhao LJ, Jiang H, Papasian CJ, Maulik D, Drees B, Hamilton J, Deng HW. Correlation of obesity and osteoporosis: effect of fat mass on the determination of osteoporosis. J Bone Miner Res 2008;23:17-29
32. De Laet C, Kanis JA, Odén A, Johanson H, Johnell O, Delmas P, Eisman JA, Kroger H, Fujiwara S, Garnero P, McCloskey EV, Mellstrom D, Melton LJ 3rd, Meunier PJ, Pols HA, Reeve J, Silman A, Tenenhouse A. Body mass index as a predictor of fracture risk: a meta-analysis. Osteoporos Int 2005;16:1330-1338.
33. Gonnelli S, Caffarelli C, Nuti R. Obesity and fracture risk. Clin Cases Miner Bone Metab 2014;11:9-14.
34. MacLaughlin EJ. Improving osteoporosis screening, risk assessment, diagnosis, and treatment initiation: role of the health-system pharmacist in closing the gap. Am J Health Syst Pharm 2010;67:S4-S8.
35. LeBlanc ES1, Nielson CM, Marshall LM, Lapidus JA, Barrett-Connor E, Ensrud KE, Hoffman AR, Laughlin G, Ohlsson C, Orwoll ES; Osteoporotic Fractures in Men Study Group. The effects of serum testosterone, estradiol and sex hormone binding globulin levels on fracture risk in older men. J Clin Endocrinol Metab 2009;94:3337-3346
36. Shepherd A, Cass A, Carlson C, Ray L. Development and internal validation of the male osteoporosis Risk Estimation score. Ann Fam Med 2007;5: 540-546
37. Cass A, Shepherd A, Asirot R, Mahajan M, Nizami M. Comparison of the Male Osteoporosis Risk Estimation Score (MORES) with FRAX in identifying men at risk for osteoporosis. Ann Fam Med 2016;14:365-369.
38. Barret-Connor E, Nielson CM, Orwoll E, Bauer D, Cauley JA, for the Osteoporotic Fractures in Men (MrOS) Study Group. Epidemiology of rib fractures in older men: Osteoporotic Fractures in Men (MrOS) prospective cohort study. BMJ 2010;340:c1069
