Resumen: Sobre la historia, el corazón ha sido considerado órgano vital por su función de bomba sanguínea impelente y aspirante, permitiendo la fisiológica perfusión a todos los rincones del cuerpo humano. Sin embargo, tras este rol de bomba se encuentra una función poco discutida, esto es, el rol endócrino-metabólico del corazón, en calidad de órgano sintetizador de hormonas y, por su función de bomba, distribuidor de hormonas ajenas a él. Comprender la incidencia de los péptidos sintetizados en el corazón ofrece una nueva perspectiva sobre la relevancia del corazón en la homeostasis y como la enfermedad cardiovascular puede alterar el metabolismo. El presente trabajo tiene por objeto revisar la más vigente información sobre el rol de los péptidos natriuréticos producidos en el corazón y su función endocrino-metabólica. Estos son los péptidos natriuréticos auricular, cerebral y tipo C. Se concluye que la concepción del corazón como un órgano de regulación endocrino-metabólico, cuyas hormonas son elementales para la homeostasis del organismo, es fundamental para la medicina de este siglo y para los avances venideros, en materia de nuevas estrategias terapéuticas que permitan mejorar la calidad de vida de los pacientes.
Palabras clave:CorazónCorazón,metabolismometabolismo,péptido natriurético auricularpéptido natriurético auricular,péptido natriurético encefálicopéptido natriurético encefálico,péptido natriurético tipo-cpéptido natriurético tipo-c.
Abstract: Regarding history, the heart has been considered a vital organ due to its role as an impeller and aspirating blood pump, allowing physiological perfusion to all corners of the human body.However, behind this role as a pump there is a function little discussed, that is, the endocrine-metabolic role of the heart, as a hormone-synthesizing organ and, due to its function as a pump, a distributor of hormones not related to it. Understanding the incidence of synthesized peptides in the heart offers a new perspective on the relevance of the heart in homeostasis and how cardiovascular disease can alter metabolism. The present work aims to review the most current information on the role of natriuretic peptides produced in the heart and their endocrine-metabolic function. These are the atrial, brain and type C natriuretic peptides. It is concluded that the conception of the heart as an endocrine-metabolic regulating organ, whose hormones are elementary for the homeostasis of the organism, is fundamental for the medicine of this century and for the upcoming advances, in terms of new therapeutic strategies that manage to improve the quality of life of patients.
Keywords: Heart, metabolism, natriuretic peptide, atrial, natriuretic peptide, brain, natriuretic peptide, c-type.
Revisión
CORAZÓN COMO ÓRGANO ENDOCRINO-METABÓLICO|
HEART AS AN ENDOCRINE-METABOLIC ORGAN
Sociedad Venezolana de Endocrinología y Metabolismo

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 3.0 Internacional.
Recepción: 15 Septiembre 2020
Aprobación: 15 Enero 2021
El corazón es un órgano de vital importancia, su función principal es bombear sangre hacia todo el cuerpo conduciendo nutrientes hacia todos los tejidos1. Está ubicado en la caja torácica, en el espacio denominado mediastino medio. Guarda una estrecha relación con los pulmones en sus bordes, con el esternón en su cara anterior y en la parte posterior con el esófago2. Su base se encuentra dirigida hacia arriba, a la derecha y ligeramente hacia atrás, de esta nacen los grandes vasos sanguíneos, su ápex reposa sobre el diafragma3. Su configuración interna está dada por cuatro cámaras, dos superiores denominadas, los atrios o aurículas, y dos inferiores, los ventrículos4. Yace envuelto por una capa fibro- serosa denominada pericardio, misma que facilita un medio de fijación y protección al evitar el estiramiento excesivo. Su pared está estructurada por tres capas, el epicardio, la más externa y en relación con el pericardio; el miocardio, que contiene células llamadas miocardiocitos, que le permiten función contráctil; y el endocardio, la capa interna, formada por tejido conjuntivo y por donde discurre el sistema de conducción.5 Su tejido se caracteriza por presentar una capa de músculo estriado cardíaco y un esqueleto fibroso que forma los orificios valvulares6.
La velocidad en que late el corazón por minuto está regulada por el centro cardiovascular del bulbo raquídeo, enviando señales químicas a través de los nervios simpáticos y parasimpáticos. Además, existe un control humoral mediado por hormonas vasoconstrictoras: adrenalina, noradrenalina, angiotensina, vasopresina, serotonina; y hormonas vasodilatadoras: bradicinina, histamina, prostaglandinas.7 Para efectuar su función de bomba de manera eficaz y eficiente, se relaciona con otros órganos y sistemas, riñón, sistema nervioso central y sistema endócrino8. No obstante, el corazón cumple otra función propia además de mantener el flujo constante de sangre, se trata del control sobre distintos procesos metabólicos a través de la secreción de péptidos natriuréticos (PNs).
En 1981, el bioquímico Alfredo de Bold descubrió la presencia de una hormona que permitía regular la presión arterial por medio de diuresis y natriuresis en ensayos con ratas knockout (KO) a través de la inyección de extractos de músculo auricular. En años posteriores se logró aislar un polipéptido sintetizado a partir de células cardíacas al cual se denominó péptido natriurético (PN)9.
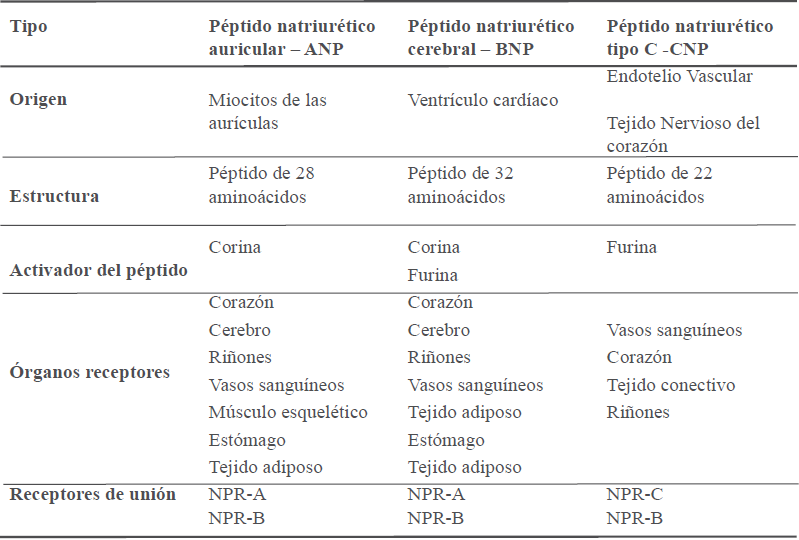
Luego de su descubrimiento se identificaron diferentes tipos de esta hormona, las cuales se clasifican en: Péptido natriurético atrial o auricular (ANP), Péptido natriurético cerebral (BNP) y Péptido natriurético tipo C (CNP). En la tabla 1 se resumen algunas características de los PNs.
ANP está formado por una cadena larga de 28 aminoácidos que forma a su vez un anillo de 17 aminoácidos unidos por una ligadura de disulfuro. Es sintetizado, almacenado y secretado por los miocardiocitos auriculares, se libera como prohormona (pro-ANP) para después pasar a su forma activa ANP10,11. Los granulocitos de miocitos auriculares cumplen el papel de almacenar este péptido, pero puede situarse en otros órganos en menor proporción. La síntesis de este péptido se da a partir de un gen precursor de 151 aminoácidos (pre-proANP), el cual se degrada formando la proANP, péptido de 126 aminoácidos que se almacena como gránulos en los cardiomiocitos auriculares12. Tras un estímulo, esta prohormona se libera y se sitúa en la periferia de las células cardíacas. Mediante una prohormona convertasa, corina, este compuesto se divide en un ANP 1-98 N-terminal y el ANP de 28 aminoácidos en su forma activa. La vida media a partir de la secreción de ANP es de 2-5 minutos, mientras que el N-terminal pro-péptido natriurético auricular (NT-ANP) puede seguir circulando en los vasos sanguíneos durante 60 minutos13,14. La secreción del pro ANP está regulada por el estiramiento de los miocitos atriales en situaciones de aumento de tensión de pared auricular que refleja el aumento de volumen y cargas de presión15.
Hormonas secretadas por el corazón – tipos de péptidos natriuréticos
La denominación BNP hace alusión a que su descubrimiento se dio en cerebros porcinos y posterior a ello se lo aisló en los ventrículos de los humanos. Dicha hormona presenta una estructura de 32 aminoácidos con una similitud en el anillo que se encuentra en el ANP. Es sintetizado por los miocardiocitos ventriculares y en menor proporción por los auriculares. Para dar origen a esta hormona se forma un precursor pre-proBNP, para luego pasar a proBNP16,17. Este compuesto se divide en presencia de una serina proteasa, corina, o por una endoproteasa, furina, las cuales producen el BNP de 32 aminoácidos, que es la forma activa de este péptido y una cadena peptídica N-terminal pro-péptido natriurético cerebral (NT-proBNP) de 76 aminoácidos. Una vez secretados, estos dos compuestos se mantienen en la circulación sanguínea de 20 a 90 minutos. El BNP difiere en su almacenamiento en relación al ANP, puesto que se sintetiza de forma exclusiva por necesidad, estimulado por el aumento de presión de los miocitos ventriculares18–20.
Por último, el CNP difiere de su origen con los anteriores péptidos, ya que no es sintetizado directamente por el corazón sino en el tejido nervioso del mismo y en mayor proporción por el endotelio vascular21. Se produce a partir de la prohormona proCNP, la cual termina su forma circundante con una estructura de 22 aminoácidos y el anillo característico de todos los PNs22. Se sintetiza a partir del gen NPPC el cual forma un precursor pre-proCNP de 126 aminoácidos y posterior a ello a proCNP de 103 aminoácidos, para ser finalmente secretado como CNP-53 unido a la serina endoproteasa intracelular furina23. La presencia de furina permite que este compuesto se divida en CNP-53 y CNP-22. Estos dos compuestos tienen funciones similares, pero se diferencian por el lugar donde predominan, el CNP-53 se encuentra en mayor proporción en el corazón, endotelio y cerebro; en tanto el CNP-22 se halla en el líquido cefalorraquídeo y el plasma24.
De manera general, los PNs se sintetizan, almacenan y liberan de forma fisiológica, sin embargo existen ciertos condicionantes que aumentan su expresión, el más importante, el estrés de las paredes cardíacas inducido por hipertrofia o sobrecarga de volumen26.
Los PNs presentan receptores en los diferentes órganos en los que actúan, clasificándose en tres: NPR-A y NPR-B que son receptores de ANP y BNP principalmente y de CNP en menor proporción, que forman parte de la familia del guanilil ciclasas particuladas, y NPR-C que es receptor de CNP26. Los receptores NPR-A y NPR-B se distribuyen en el cuerpo en órganos como el corazón, cerebro, riñones, vasos sanguíneos, músculo esquelético, estómago y tejido adiposo. Además de ser similares en cuanto a su locación, también presentan una estructura semejante. Contienen tres dominios, un segmento de 450 aminoácidos donde se fijan los PNs, un segmento transmembrana de 570 aminoácidos (dominio de homología de quinasa), y un dominio de guanilil ciclasa donde se sintetiza el cGMP, que es un segundo mensajero de los PNs27,28. El proceso de recepción de PNs está dado por tres pasos: 1) El PN está en su forma basal, se reprime la actividad del guanilil ciclasa a través de dominio de homología de quinasa, 2) El PN se une al receptor, tomando su forma activa, logrando que los dominios de guanilil ciclasa se unan, 3) Existe una desfosforilación de los sitios de unión de hormonas, permitiendo que el receptor se inactive y repita el proceso de activación y recepción de hormonas29.
El NPR-C presenta un solo dominio de 440 aminoácidos y una cola de 37 aminoácidos, se encuentra en las glándulas endocrinas, pulmones, riñones y en mayor proporción, en las células endoteliales30. La unión del receptor con un PN permite que exista una serie de reacciones que elimina los péptidos de la sangre. Esto le otorga la función de control y depuración de los PNs22,31. Si existe alguna disfunción de este receptor se reflejaría en la alteración de PNs en el plasma sanguíneo. En los órganos en que se encuentra este receptor se ha descubierto que su estructura está formada por 37 aminoácidos, contiene dos enlaces disulfuros y se encuentra glicosilado; al ser una cadena más corta que la de otros receptores no presenta actividad catalítica, pero sí de señalización29. Existe otro mecanismo de degradación de PNs mediado por la neprilisina, actualmente la degradación de esta metaloproteinasa integral de membrana tipo 2 es una diana farmacológica importante para el tratamiento de insuficiencia cardíaca con fracción de eyección reducida (IC-FEr)20,25,32.
Los PNs desempeñan un rol fisiológico importante, intervienen en distintos procesos celulares que regulan la homeostasis del organismo humano33. Los efectos cardinales son diuresis, natriuresis y vasodilatación, sin embargo, es importante reconocer que sus mecanismos de acción no se encuentran limitados a estos, puesto que, en realidad ejercen efectos en el propio corazón, vasculatura, a nivel renal, poseen estrecha relación con el metabolismo de los lípidos, el tejido adiposo y el estrés oxidativo, es decir, constituyen un grupo de hormonas cuyas funciones son autocrinas y paracrinas34–36. Las principales funciones de los PNs se ilustran en la figura 1.
Los NPR se expresan en los miocitos y fibroblastos cardíacos, lo cual demuestra una evidente relación de los PNs con suprincipalórganode síntesis. Quien ejerce las funciones más importantes es el ANP, las mismas consisten en efectos antihipertróficos y antifibróticos37,38. Se ha demostrado en estudios con ratones KO que el bloqueo de la codificación genética del ANP se relaciona con el desarrollo de hipertrofia cardíaca e hipertensión en respuesta a hipoxia crónica y dietas altas en sal39,40. Además, en el contexto de sobrecarga de volumen, se encontraron resultados similares independientes del consumo de sal, relacionados con el desarrollo de hipertrofia cardíaca y disrupción genética del ANP41,42.
El mecanismo por el cual el ANP ejerce un efecto antihipertrófico es la inhibición del receptor de potencial transitorio canónico 6 (TRPC-6), proceso mediado por la proteína quinasa G (PKG). TRPC- 6 es el encargado de inducir hipertrofia cardíaca a través de la activación del factor nuclear de las células T activadas (NFAT), calcineurina y la activación de proteínas como MKP-1, p38MAPK y ERK43,44.
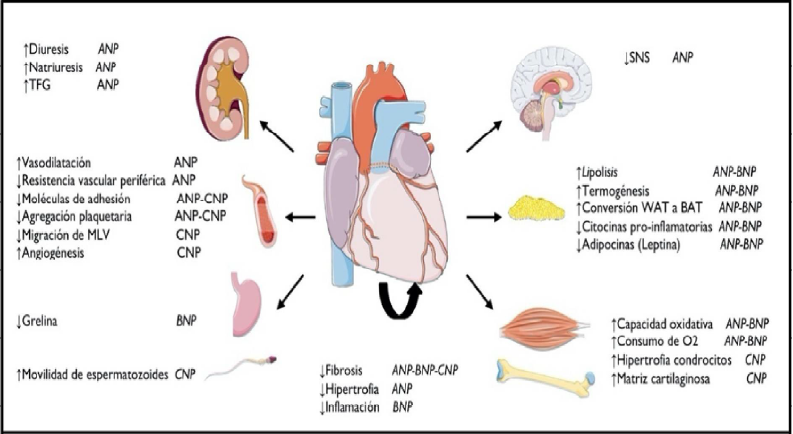
Figura 1
Funciones de PNs: Corazón, riñón, vasos sanguíneos, sistema digestivo, sistema neurológico, tejido adiposo, músculo y tejido conectivo. Se detallan las funciones con sus principales PNs relacionados. PNS Péptidos natriuréticos, ANP Péptido natriurético auricular, BNP Péptido natriurético cerebral, CNP Péptido natriurético C, TFG Tasa de filtrado glomerular, MLV Músculo liso. Imágenes obtenidas a partir de: © 2020 LES LABORATOIRES SERVIER, todos los derechos reservados. URL: https://smart.servier.com/. Licencia de Creative Commons Reconocimiento 4.0 Internacional. No se realizó modificación alguna sobre las imágenes.
BNP y CNP ejercen funciones en el corazón, aunque en menor medida comparado con ANP. Dentro de las características más llamativas, está la inhibición de la fibrosis, el efecto antihipertrófico es menor comparado con ANP 37. Los mecanismos propuestos para explicar su papel antifibrótico son, la inhibición del factor de crecimiento transformador beta (TGF-B) por parte del BNP y la reducción de síntesis de colágeno por parte del CNP, este último, aumenta su producción ante estímulos pro-fibróticos45. BNP tiene la capacidad de modular la reacción inflamatoria en el contexto de lesión cardíaca, disminuyendo monocitos, linfocitos B y células NK en sangre periférica, además regula la quimiotaxis de monocitos y producción de moléculas inflamatorias por los macrófagos en el tejido cardíaco46.
Adicionalmente, en el marco del ejercicio clínico, se emplea ANP y BNP/Pro-BNP como los biomarcadores mejor establecidos para diagnóstico y pronóstico de insuficiencia cardíaca (IC), donde el incremento de los niveles plasmáticos de estos PNs indicaría la presencia de IC incluso con fracción de eyección conservada, mientras un resultado negativo descartaría la patología. A pesar de esto, no existen límites estandarizados respecto a las concentraciones plasmáticas47,48.
ANP y CNP son los principales PNs que actúan a este nivel, sin embargo, es fundamental tener en cuenta que ambos son sintetizados en el corazón y el endotelio vascular49. Es decir, sus efectos podrían estar mediados por ambos. La evidencia disponible se basa en estudios in vitro y estudios ex vitro en ratones KO50. ANP contribuye a la activación de PKG a través de su unión con NPR-A y NPR-B, proceso mediado por cGMP, estimulando al complejo Ca2/calmodulina dependiente de la enzima óxido nítrico sintasa, así, el resultado es mayor producción de óxido nítrico (NO), promoviendo la relajación de las células del músculo liso vascular, lo que disminuye la presión arterial sistémica a través de vasodilatación46,51. Un efecto indirecto que tiene relación con la función vascular es la acción inhibitoria ejercida por los PNs sobre el SRAA, disminuyendo la resistencia vascular46. Estudios in vitro en células endoteliales de venas umbilicales humanas demuestran que la variante genética de ANP, C2238, está relacionada con disfunción endotelial dependiente de estrés oxidativo52–55.
ANP Y CNP demostraron una reducción en la expresión de moléculas de adhesión como MCP-1 y P-selectina, importantes en el proceso aterosclerótico al estimular la infiltración de leucocitos a través de las células endoteliales en el contexto de una lesión y estimular la adhesión y agregación plaquetaria56,57. La migración de células del músculo liso vascular desde la capa media hasta la capa íntima del endotelio, contribuye a la formación de placas de ateroma. ANP, BNP y CNP inhiben esta migración, siendo el CNP quien ejerce un efecto mayor en comparación con los demás PNs58. Además, CNP cumple un rol importante en la angiogénesis y remodelación vascular luego de eventos isquémicos, mediante la activación de NPR-C, el cual se encuentra acoplado a proteína G inhibidora (Gi) a quinasas reguladas por señal extracelular 1/2 (ERK1/2) y a la proteína quinasa B (Akt) para promover la proliferación y migración endotelial59. Sangaralingham y col. demostraron en un estudio epidemiológico de 12 años de seguimiento, que las concentraciones de CNP elevado en el plasma, estaban en relación con mayor incidencia de eventos cardiovasculares mortales y no mortales60.
Todos los PNs brindan protección cardiorrenal, sin embargo, es el CNP quien tiene la menor capacidad para producir efectos renales y ANP quien ejerce las funciones más importantes. Las principales acciones que ejercen los PNs son natriuresis y diuresis61,62. La reabsorción de Na a través del túbulo colector es dependiente del canal de sodio sensitivo a amilorida (ENaC), y a nivel de la rama ascendente gruesa del asa de Henle por el cotransportador Na-K-2Cl con la ayuda de adenosina trifosfatasa de sodio y potasio (Na-K-ATPasa), estos permiten la entrada pasiva de este ion desde la luz tubular hacia el torrente sanguíneo. ANP inhibe la función de ENaC y Na-K-ATPasa, provocando el efecto de natriuresis51,63,64. ANP interacciona con el SRAA, inhibiendo la secreción de renina y la producción de aldosterona, disminuyendo entre otros su efecto antidiurético65,66. Favorece a la diuresis al inhibir la secreción de vasopresina por la neurohipófisis inducida por angiotensina II67,68. La vasopresina actúa a nivel del túbulo distal y túbulos colectores, a través de su receptor V2, el cual también puede ser inhibido por ANP. Además, induce un aumento de la tasa de filtrado glomerular (TFG), al provocar vasodilatación de la arteriola aferente y vasoconstricción de la arteriola eferente. Puede interferir en la vasoconstricción de la arteriola aferente mediada por el sistema nervioso simpático a través de noradrenalina51,69.
Estudios sugieren que ANP aumenta la TFG a través de la relajación de las células mesangiales intraglomerulares en el espacio entre el endotelio capilar y los podocitos, aumentando el área de filtración70. Existen datos de pacientes con enfermedad renal crónica (ERC) que poseen bajos niveles de corina, crucial en la activación de ANP, es decir, en este grupo se favorece el desarrollo de hipertensión arterial, sin embargo los mecanismos no se encuentran totalmente dilucidados71,72
Los PNs actúan modulando la actividad del sistema nervioso autónomo, ANP disminuye la frecuencia cardíaca al inhibir el sistema simpático, provocando que predomine la función vagal27. La inhibición simpática a nivel renal provoca disminución de secreción de renina, mencionada con anterioridad, al igual que los efectos sobre la vasopresina67,73.
El metabolismo de los lípidos está regulado especialmente por dos lipasas, lipoproteína lipasa y lipasa sensible a hormonas. Éstas median los procesos de entrada, almacenamiento y salida de ácidos grasos libres (FFA) y glicerol a través de la hidrólisis de los triglicéridos74. La lipasa sensible a hormonas es especialmente importante ya que contribuye al proceso antes mencionado, y a partir de esto, el glicerol se transporta al hígado, y es utilizado para gluconeogénesis, mientras que los FFA se transportan por medio de albúmina sérica a los tejidos donde son catabolizados para obtener energía75,76. La estimulación de la lipólisis está regulada por estímulos adrenérgicos y por la insulina, quienes contribuyen a la conversión de la forma inactiva a la activa de la lipasa sensible a hormonas77.
El tejido adiposo se encuentra en estrecha relación con los PNs, en él se expresan NPR-A que une a ANP y BNP y NPR-C que promueve su eliminación78,79. Los PNs inducen síntesis de ácidos grasos libres y glicerol por estimulación de lipólisis en el tejido adiposo a través de la activación de la lipasa sensible a hormonas, acción mediada por el complejo PNA/cGMP/PKG80–82. Birkenfeld y col., demostraron que la infusión de ANP en pacientes jóvenes estaba relacionada con mayores concentraciones plasmáticas de ácidos grasos libres y glicerol, mediante efectos independientes del sistema adrenérgico. El ejercicio aeróbico y de resistencia mejoran el proceso de lipólisis inducida por ANP en el tejido adiposo humano84,85.
Los depósitos de grasa que forman el tejido adiposo se dividen según su coloración y tienen características individuales, estos son: tejido adiposo marrón (BAT), tejido adiposo blanco (WAT) y tejido adiposo beige o brite (bAT)86. WAT está relacionado con el almacenamiento y movilización de sustratos energéticos, además expresa una gran variedad de hormonas como leptina, adiponectina, angiotensina, visfatina, glucocorticoides, esteroides sexuales e incluso moduladores inflamatorios como interleucina 6 (IL-6), además de intervenir en el proceso de expresión de ácidos grasos libres mediado por lipasa sensible a hormonas87,88. Por el contrario, BAT posee abundantes mitocondrias las cuales cuentan con proteína desacopladora 1 (UCP1), que desacopla la fosforilación oxidativa de síntesis de ATP, sustituyéndolo por la generación de calor, la activación de peroxisome proliferator- activated receptor γ co-activator 1 α (PGC1a) estimula la génesis mitocondrial y la producción de factor de crecimiento endotelial vascular (VEGFB) quien propicia la entrada de ácidos grasos libres para la producción de calor, es decir, contribuyen al proceso de termogénesis; la activación del desacoplamiento mitocondrial y de la termogénesis en el BAT, depende de la acción conjunta del sistema adrenérgico y de las hormonas tiroideas89–91.
Los PNs fomentan la conversión de tejido adiposo WAT en BAT, además fomentan la expresión de genes termogénicos que codifican PGC1a y UCP1, proceso mediado por el complejo PNA/cGMP/ PKG/p38 MAPK92–95. Estos datos demuestran la influencia de los PNs en el metabolismo al aumentar el gasto energético a través de la regulación de la lipólisis aumentando la disponibilidad de FFA y contribuyendo al proceso de termogénesis favoreciendo la biogénesis mitocondrial.
Los PNs desempeñan un papel importante en el músculo esquelético al aumentar la biogénesis mitocondrial y mejorar la capacidad oxidativa96-97. Engeli y col. demostraron que el entrenamiento físico regula positivamente la expresión de genes que codifican RPN-A en el músculo esquelético, además de la asociación positiva, luego de 8 semanas de entrenamiento aeróbico, entre los niveles de este receptor, su señalización y genes codificadores de proteínas que intervienen en el procesode fosforilación oxidativa, además de genes que codifican peroxisome proliferator-activated receptor γ co-activator 1 α (PGC1a). Existieron cambios en las concentraciones plasmáticas de ANP y BNP luego del entrenamiento físico, lo que sugiere un vínculo fisiológico entre la señalización de estos PNs por su receptor con la capacidad de regulación oxidativa y consumo de oxígeno en el músculo esquelético98.
ANP inhibe la secreción de adipocinas por adipocitos, citocinas proinflamatorias y quimiocinas por macrófagos en el tejido adiposo, muchas de estas relacionadas con resistencia insulínica en el contexto de obesidad, como leptina, IL-6, TNF-α inhibidor tisular de metaloproteinasa (TIMP) -1, RBP-4, así como quimiocinas (MCP- 1, MIP-1β, MCP-2 y GRO-α)99,100. BNP ejerce efectos inhibiendo la ghrelina, hormona reguladora del apetito101. CNP se encuentra relacionado con funciones como estimulación de la proliferación e hipertrofia de condrocitos, producción de matriz cartilaginosa, modulación de la motilidad de los espermatozoides, desarrollo de células germinales testiculares102,103.
En condiciones patológicas, como hipertensión arterial, existe hiperactivación de SRAA y del sistema nervioso simpático (SNS) con mayor retención de sodio y agua; en la insuficiencia cardíaca además de estas 2 características mencionadas previamente hay sobrecarga de volumen y estrés cardíaco inducido por el estiramiento de las cámaras, lo que provoca un aumento de la secreción de PNs, en particular de ANP, proceso que no sucede en la hipertensión arterial puesto que estudios no han demostrado un papel compensatorio de los PNs en respuesta a un aumento de la PA, sin embargo, una falla de este sistema de péptidos se encuentra relacionado con la patogénesis de la enfermedad13,104–106.
La hiperactivación del SRAA y SNS en estadios iníciales de la insuficiencia cardíaca, proporciona un mecanismo compensatorio para aumentar el gasto cardíaco y vasoconstricción periférica con el fin de mantener la homeostasis cardiovascular; con el tiempo, la activación prolongada de estos sistemas se vuelve perjudicial y contribuyen a la progresión de la enfermedad, a partir de aquí es crucial la acción de mecanismos reguladores, entre ellos el aumento de la secreción de PNs, sobre todo ANP y BNP quienes ofrecen efectos protectores induciendo diuresis, natriuresis, vasodilatación, protegiendo al paciente de la sobrecarga de volumen. No obstante, durante la evolución de la enfermedad, estos PNs pierden gradualmente su efecto natriurético, lo que sugiere la aparición de resistencia renal a estos. Existen varias hipótesis que explican este mecanismo, entre ellas un aumento local en la degradación de NP o una disminución en la concentración renal de NPR-A13,27.
Actualmente la terapia con sacubitril/valsartán ha innovado el tratamiento de la insuficiencia cardíaca, al combinar un antagonista del receptor de la angiotensina II con un inhibidor de la neprilisina, molécula relacionada con la degradación de los PNs, teniendo efectos reductores en la PA y aumento de la diuresis y natriuresis107–111; cuyos efectos metabólicos en este contexto son igual de destacables. En un análisis post-hoc del ensayo PARADIGM, los pacientes con insuficiencia cardíaca y diabetes con HbA1c ≥ 6,5% que fueron asignados al azar a la terapia con sacubitril/valsartán tuvieron un mejor control glucémico que los sujetos que recibieron enalapril112. Durante el seguimiento monitoreando las concentraciones de HbA1c y el nuevo uso de insulina o hipoglucemiantes orales, los resultados fueron significativamente más bajos en el grupo sacubitril/valsartán en comparación con el grupo de control. En una cohorte de sujetos con hipertensión y obesidad, ocho semanas posteriores al inicio de tratamiento con sacubitril/valsartán aumentó la sensibilidad a la insulina y lipólisis en el tejido adiposo subcutáneo abdominal13,27,108. Estos datos sugieren la importancia del papel del sistema cardiovascular, y específicamente de los PNs en el contexto de la enfermedad cardiovascular sobre el metabolismo.
Más allá de su función como bomba aspirante e impelente, la concepción del corazón como un órgano de regulación endocrino-metabólico, cuyas hormonas son elementales para la homeostasis del organismo, es fundamental para la medicina de este siglo y para los avances venideros.
La comprensión de los diferentes péptidos natriuréticos y su utilidad clínica, así como de los distintos grados de disfunción cardíaca y su impacto en distintos ejes metabólicos/hormonales, son muy importantes y no debe infravalorizarse, para de esta forma dar un enfoque integral a los pacientes con enfermedades cardiometabólicas. Resulta conveniente acotar que el descubrimiento y estudio de los péptidos natriuréticos auriculares no solo ha sido beneficioso para el diagnóstico y pronóstico de la insuficiencia cardíaca, también contribuye en el desarrollo de nuevas estrategias terapéuticas que permitan mejorar la calidad de vida de los pacientes.
CONFLICTO DE INTERESES: Los autores declaran no tener conflictos de intereses de ninguna índole que impidan o comprometan la publicación del presente artículo.
Hormonas secretadas por el corazón – tipos de péptidos natriuréticos


Figura 1
Funciones de PNs: Corazón, riñón, vasos sanguíneos, sistema digestivo, sistema neurológico, tejido adiposo, músculo y tejido conectivo. Se detallan las funciones con sus principales PNs relacionados. PNS Péptidos natriuréticos, ANP Péptido natriurético auricular, BNP Péptido natriurético cerebral, CNP Péptido natriurético C, TFG Tasa de filtrado glomerular, MLV Músculo liso. Imágenes obtenidas a partir de: © 2020 LES LABORATOIRES SERVIER, todos los derechos reservados. URL: https://smart.servier.com/. Licencia de Creative Commons Reconocimiento 4.0 Internacional. No se realizó modificación alguna sobre las imágenes.
