Artículos Originales

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 15 Agosto 2016
Revisado: 20 Octubre 2016
Aprobación: 12 Diciembre 2016
Resumen: El carcinoma colorrectal representa la patología oncológica de mayor frecuencia dentro del tracto gastrointestinal. Es la segunda causa de muerte por patología oncológica a nivel mundial. La mutación de los genes KRAS y NRAS se reporta en algunas series de casos hasta en un 50 % de los pacientes con carcinoma colorrectal metastásico; sin embargo, hasta la fecha no ha sido demostrada el valor pronóstico de este hallazgo. OBJETIVO: Determinar la frecuencia de la mutación de los genes KRAS y NRAS en pacientes con cáncer de colon metastásico o en recaída y sus probables implicaciones en la supervivencia. MÉTODO: Estudio retrospectivo de cohorte analítico, unicéntrico. RESULTADOS: La frecuencia de la mutación en nuestro estudio fue de 13,15 % para el gen KRAS y de 2,6 % para el gen NRAS. Se realiza análisis por método de Kaplan Meier sin obtener diferencias estadísticamente significativas en términos de supervivencia global entre pacientes wild type y pacientes mutados. CONCLUSIONES: En nuestra experiencia, la frecuencia de la mutación de los genes KRAS y NRAS en este grupo de pacientes, es menor a lo señalado en la literatura en poblaciones europeas y norteamericanas. No pudimos demostrar relación entre la mutación de los genes estudiados con la supervivencia global.
Palabras clave: Carcinoma, colorrectal, KRAS, NRAS, supervivencia global, metastásico.
Abstract: The colorectal cancer represents the most frequent oncologic disease in the gastrointestinal tract neoplasm. It was the second cause of death from cancer in the worldwide. The mutation of KRAS and NRAS genes is reported in more of 50 % of patients with metastatic colorectal cancer in some series; however, it has not be demonstrated the prognosis value of this feature. OBJECTIVE: To determine the frequency of the mutation of KRAS and NRAS genes in the patients with metastatic or relapsing colorectal cancer and the probably implications of this issue in the overall survival. METHOD: A retrospective trial of analytic cohort was made for us. RESULTS: The frequency of the mutations in our experience is 13.15 % for the KRAS gene and 2.6 % for the NRAS gene. We realized analysis with the Kaplan Meier method for the overall survival and wasn’t statically significates between the wild type patients versus the mutated ones. CONCLUSIONS: In our experience, the frequency of the KRAS and the NRAS gene mutation in these patients, is less than the one reported in the bibliography for European and the American populations. We could not demonstrate any relationship between overall survival and the mutational status of the genes in study.
Keywords: Colorectal carcinoma, KRAS, NRAS, overall survival, metastatic.
INTRODUCCIÓN
De acuerdo con los datos estadísticos de T he American Cancer Society (1), el cáncer colorrectal (CCR) representa el cáncer más frecuente dentro de las neoplasias del tracto digestivo. Es además, el tercer cáncer más frecuente y afecta tanto a hombres como a mujeres, con un riesgo de por vida de desarrollar la enfermedad, de 1/21 (4,7 %) y 1/27 (4,4 %) respectivamente. De igual manera, la mortalidad a causa de este cáncer, se ubica en la segunda causa más frecuente, cuando los datos se analizan globalmente. Datos similares en cuanto a incidencia se reportan en la estadística Europea (2); no obstante cabe acotar que la mortalidad en hombres es mayor que en mujeres, reportándose de 11 a 32/100 000 muertes anuales en la población masculina y de 7 a 16/100 000 muertes anuales en la población femenina.
Se estima que para el 2016, se diagnosticarán 95 270 nuevos casos de cáncer de colon y 39 220 nuevos casos de cáncer de recto. La mortalidad esperada es de 49 190 muertes (1). En Venezuela, son pocos los datos estadísticos, no obstante, de acuerdo al último reporte del Ministerio del Poder Popular para la Salud, la patología neoplásica de colon y recto ocupa el quinto lugar en frecuencia de muerte por cáncer (3). Estos datos concuerdan claramente con una disminución de la incidencia, derivada de los programas de pesquisa, cambios en hábitos dietéticos, implementación de ejercicio en el día a día, así como en la disminución de hábitos carcinogénicos como el tabaquismo.
Así como la incidencia, la mortalidad también ha experimentado un importante descenso desde 1980 y 1990 (4), esto relacionado al empleo de combinación de regímenes de quimioterapia basados en fluoruracilo, oxaliplatino e irinotecán. Más recientemente se ha experimentado una duplicación en cuanto a la supervivencia de los pacientes con CCR en relación a la identificación de características moleculares en el desarrollo de la enfermedad, que se dibujan en la actualidad como factores predictivos de respuesta clínica a tratamiento dirigido.
Ras es una familia de oncogenes que incluye KRAS, NRAS y HRAS. En el CCR las mutaciones se localizan sobre todo en el exón 2 (codones 12,13) de KRAS (en torno al 40 % de los pacientes) y menos frecuentemente, y de forma excluyente, en los exones 3 (codones 59,61) y 4 (codones 117,146) de KRAS. En cuanto a NRAS, las mutaciones se han determinado en los exones 2 y 3 y en menor medida 4; además en estrecha relación con 10 % de los pacientes que tienen KRAS Exón 2 no mutado(5,6).
El valor de las mutaciones de KRAS y NRAS, como factor pronóstico o predictivo, se ha analizado en los pacientes con CCR tanto en la situación adyuvante como en la enfermedad avanzada. La incidencia de mutaciones de los genes KRAS y NRAS en el CCR se sitúa cercana al 50 %. Estudios recientes no indican valor pronóstico de mutaciones de KRAS-NRAS en los estadios II y III de CCR; mientras que en la enfermedad metastásica es controversial. Por otra parte, el valor de las mutaciones de KRAS-NRAS, como factor predictivo de respuesta a la quimioterapia en el tratamiento adyuvante, es muy limitado, caso contrario a lo que ocurre en enfermedad metastásica.
Si bien la mayoría de las características del CCR que se conocen actualmente, surgen de estudios realizados en poblaciones de Europa y de EE.UU, un número muy pequeño de estudios han reportado la frecuencia de mutaciones en pacientes con CCR en América Latina. El estudio de Ciardello y cols.(7); en pacientes con diagnóstico de CCR, que incluyó países de Centro y Suramérica como Argentina, Brasil, México y Venezuela, reportándose una frecuencia de mutaciones en el gen KRAS de 36 %, similar a la frecuencia reportada en Europa (40 %), pero superior a la de Asia (22 %). Particularmente, Venezuela se perfila con una alta tasa de gen KRAS salvaje (77 %) (7).
A pesar de la relevancia del estudio molecular del CCR, tanto como factor pronóstico y predictivo de respuesta a tratamiento, no existe información publicada en nuestro medio, que permita la caracterización de la población venezolana a gran escala. De tal manera, se desconoce no sólo la frecuencia, sino también el tipo de mutaciones presentes en nuestra población, lo que no permite establecer patrones de comportamiento de la enfermedad y en este sentido su prevención. Por tal motivo, es interés de los autores determinar la frecuencia de las mutaciones del KRAS-NRAS en pacientes con diagnóstico de CCR metastásico o en recaída, así como las implicaciones del estatus mutacional en la supervivencia global de estos pacientes.
ANTECEDENTES
La familia de los genes RAS (HRAS, NRAS y KRAS) es uno de los grupos de oncogenes más frecuentemente alterados en las neoplasias humanas como: pulmón 30 %, colon 40 %, páncreas 80 %, tiroides 55 %, entre los más frecuentes.
En una observación retrospectiva realizada por Karapetis y cols. (8) se observó que de 394 pacientes estudiados, el 42 % portaban mutaciones del gen KRAS, específicamente a nivel del exón 2. Asimismo, la efectividad de la adición de cetuximab estaba íntimamente ligada a la mutación del KRAS (P=0,01 y P<0,001 para la interacción de la mutación con la sobrevida global y con la sobrevida libre de progresión específicamente). Concluyeron así, que la evaluación del estado mutaciones del gen KRAS es necesario en pacientes con CCR, para asegurar un tratamiento adecuado, identificando aquellos pacientes no respondedores al tratamiento anti-EGFR.
De tal manera, y de acuerdo a data internacional, en la actualidad se afirma que aproximadamente el 30 %-50 % de los tumores colorrectales cuentan con al menos un exón del gen KRAS mutado; esto indica que hasta un 50 % de los pacientes con CCR podría responder a la terapia con anticuerpos anti-receptor del factor de crecimiento epidérmico (EGFR). Sin embargo, el 40 %-60 % de los pacientes con KRAS salvaje (Wild Type) (WT), no responden a tal terapia, y en ese contexto existe la sospecha de que se encuentra involucrada la mutación del gen BRAF, que suele estar presente en un 5 %-10 % de estos tumores y que conlleva por tanto, a alteración de la respuesta a terapia blanco(9).
En el mismo orden de ideas, observaciones hechas por dos metanálisis(10, 11) concluyen que la adición de anticuerpos monoclonales anti EGFR en pacientes con KRAS WT mejoró de manera significativa la tasa de respuesta objetiva, así como una mejoría estadísticamente significativa en la sobrevida libre de progresión y en la sobrevida global, tanto en pacientes de primera línea, como en segunda y tercera línea, sobre todo en aquellos pacientes que recibieron tratamiento con esquemas infusionales de 5-Fluouracilo. Sin embargo, en cuanto al valor pronóstico de KRAS, pese a que existen algunos estudios que han demostrado que algunos tipos específicos de mutación de KRAS tienen relación con la sobrevida, como la mutación G12V, la que se asociaría a un pronóstico más adverso de la enfermedad en relación a otros tipos de mutaciones(12), no se ha consensuado que los pacientes portadores de mutaciones activantes en el gen KRAS presenten una sobrevida global (SG)y sobrevida libre de enfermedad (SLE) mayor o menor respecto a aquellos pacientes que no portan dichas mutaciones (13).
En Venezuela, según el estudio de Estrada y cols. (14); realizado en la ciudad de Maracaibo, se encontraron mutaciones en los codones 12 y 13 del oncogén KRAS en el 23,33 % de los pacientes. De estos 28,57 % en el codón 12, en el codón 13 se encontró un 57,14 % y 14,29 % para ambos codones.
MÉTODO
Estudio retrospectivo de cohorte analítico. Se analizaron todas las historias de los pacientes con ADC de colon metastásico o en recaída del Departamento de Historias Médicas, durante los años 2009 - 2015. De un total de 239 pacientes en el espacio de tiempo descrito, se identificaron 38 pacientes a los que se les realizó determinación del estatus mutacional KRAS y NRAS, todas las cuáles fueron incluidas en el estudio.
La evaluación molecular de los genes KRAS y NRAS se realizó a través del siguiente método: evaluamos los exones 2 (codones 12 y 13) y 3 (codón 61) para el gen KRAS y el exón 2 (codones 12 y 13), exón 3 (codones 59 y 61) y exón 4 (codones 117 y 146) del gen NRAS. Todos los exones requeridos para cada prueba genética son amplificados por PCR con cebadores de secuencia específica y posteriormente secuenciados por electroforesis capilar con el kit: BigDye 3.1 (Applied Biosystems). Equipo: ABI9700 Thermocycler (Applied Biosystems) en el Genetic Analyzer Sequencer ABI310 de Applied Biosystems® . El software de análisis utilizado es: Sequencing Analysis 5.2 y SeqScape v2.5.
Se revisaron 239 historias con las características previamente señaladas; obteniéndose un total de 38 pacientes para incluir en el estudio. Se registraron datos demográficos, histológicos y moleculares de dichos pacientes.
Se realizó un formato de recolección de datos para el análisis de cada historia clínica. todos los datos fueron registrados en el programa Excel de Microsoft Office 2014®. Se presentaron los datos en Figuras. Se realizaron cálculos de media y desviaciones estándar. Los datos fueron representados en valores absolutos y/o valores relativos según cada caso. La SG se calculó a través del método de Kaplan Meier. Para el análisis de significancia estadística se empleó el método de χ2, para un intervalo de confianza de 95 % y 1 grado de libertad, con un α = 3,84.
RESULTADOS
Se incluyeron en el estudio 38 pacientes con ADC de colon metastásico o en recaída, con evaluación molecular los genes KRAS y NRAS, durante los años 2009- 2015.
La edad media de los pacientes en el estudio fue de 54,6 años de edad; siendo de 54,9 años para el sexo femenino y 54,38 para el sexo masculino. La distribución por sexo con un total de 20 mujeres y 18 hombres.
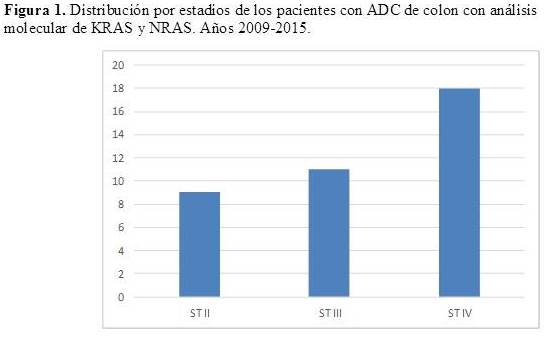
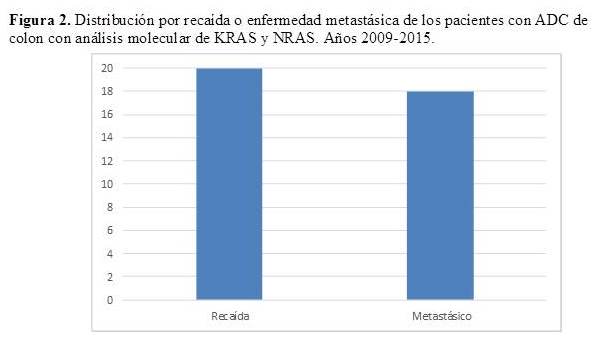
La Figura 1 y 2 representan la distribución de pacientes con análisis molecular de KRAS y NRAS según estadificación inicial y según recaída o enfermedad metastásica. En cuanto a la estadificación inicial, 9 pacientes fueron estadio II, 11 estadios III y 18 pacientes estadio IV. Por su parte, hubo un total de 20 pacientes en recaída y 18 pacientes metastásicos al momento del diagnóstico (estadio IV).
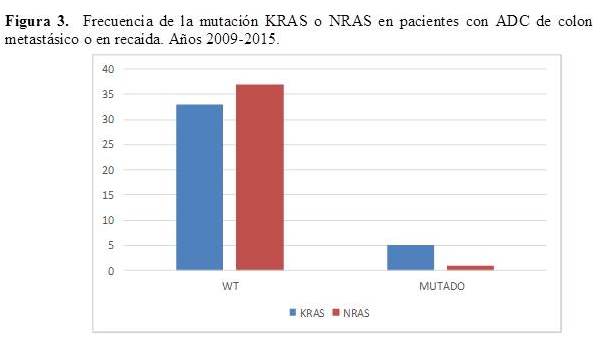
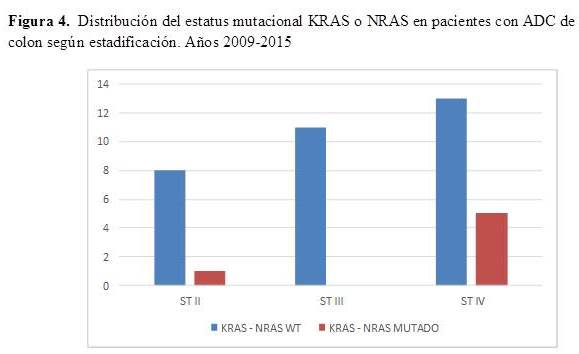
Se registraron 5 pacientes con mutación del gen KRAS, todas presentaron dicha mutación en el codón 12 del exón 2. Sólo se registró 1 paciente con mutación en el codón 117 del exón 4 del gen NRAS (Figura 3). La presencia de mutaciones de los genes KRAS o NRAS fue más frecuente en pacientes con estadío IV, con un total de 5 pacientes mutados; mientras que, sólo 1 paciente con estadío II fue detectado con mutación del gen KRAS (Figura 4).
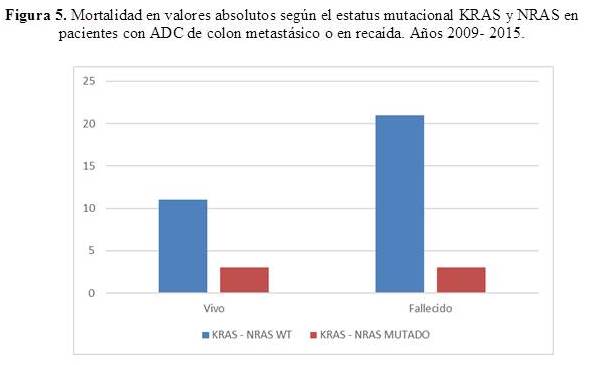
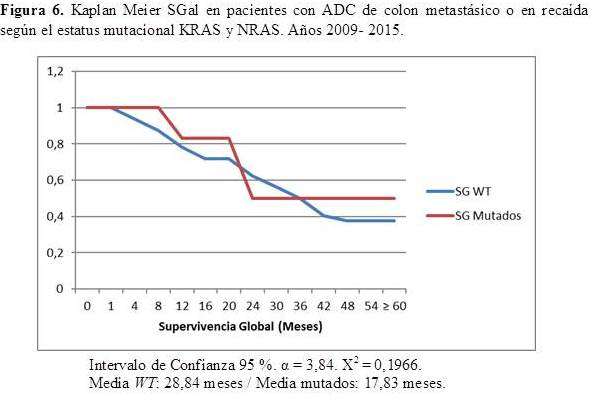
En cuanto a la mortalidad y su relación con el estatus mutacional de los genes KRAS y NRAS, está representado en la Figura 5. Se registran 11 pacientes vivos y 21 fallecidos con KRAS o NRAS WT; mientras que, 3 pacientes con mutaciones detectadas están vivos y 3 fallecidos. Asimismo, se relacionó la SG según el estatus mutacional para los genes en estudio. Se realiza una figura de Kaplan Meier donde ambas curvas se superponen. Las medias de SG distintas para el grupo WT (28,84 meses) y el grupo de pacientes con mutaciones detectadas (17,83 meses); sin embargo, esta diferencia no fue estadísticamente significativa, con un valor de Χ2 = 0,1966 para un IC de 9 5% y un α = 3,84.
DISCUSIÓN
En nuestra experiencia, los datos obtenidos en cuanto a la frecuencia de mutaciones KRAS / NRAS no se comparan con la bibliografía revisada. En nuestro estudio, de un total de 38 pacientes incluidos, 32 pacientes resultaron WT y se registraron 5 mutaciones KRAS (todas las mutaciones en el codón 12 del exón 2); lo cual representa en valores relativos un 84,21 % de pacientes WT; con 13,15 % de mutación en el gen KRAS y sólo 2,6 % de mutaciones del gen NRAS.
La bibliografía revisada, señala frecuencia de mutaciones que del 40 % (8), 50 % (9) para la familia RAS. Por otro lado, estudios realizados en Venezuela, señalan una frecuencia de la mutación en 23,33 % (14); este hecho es comparable con lo obtenido en nuestros estudios, aun cuando nuestra experiencia señala un índice menor de mutaciones de la familia RAS. Hasta la fecha no encontramos reporte de frecuencia de la mutación para el gen NRAS en nuestra población, señalando que en nuestra experiencia, la mutación de dicho gen tiene una frecuencia baja, de apenas 2,6 %.
Por otro lado, se trató de vincular la relación entre los pacientes con estatus mutacional WT y los pacientes con mutaciones en los genes KRAS o NRAS y la SG, en fin de caracterizar dicha mutación con pronóstico en este grupo de pacientes. En nuestra experiencia, la presencia de la mutación no tiene valor pronóstico en este grupo de pacientes, analizado a través del método de Kaplan Meier se obtiene curvas de comportamiento similar, con un valor de χ2 de 0,1966, sin significancia estadística. Esto a pesar de la diferencia en los valores de SG media para ambos grupos, donde fue de 28,84 meses para los WT vs. 17,83 meses para los mutados; sin embargo, se requieren estudios con mayor población y mayor tiempo de seguimiento para determinar el valor pronóstico de la mutación de los genes KRAS o NRAS. La bibliografía consultada revela datos similares, donde a pesar de haber un valor predictivo para tratamiento en cuanto al estatus mutacional de los genes mencionados, no existen datos concluyentes para su valor como factor pronóstico (10, 11, 13).
En nuestra experiencia, pareciera que la frecuencia de las mutaciones de los genes KRAS y NRAS en nuestra población es menor a lo reportado en la literatura de poblaciones Europeas y Norteamericanas; sin embargo, se requieren estudios con mayor cantidad de población y de preferencia multicéntrico para concluir este hallazgo. Hasta la fecha no se ha demostrado que la presencia de mutaciones en los genes KRAS y NRAS tenga valor pronóstico en estos pacientes.
Referencias
1. 2016 Cancer Statistics. The American Cancer Society´s. Disponible en: URL: http://www.cancer.org/research/cancerfactsstatistics/cancerfactsfigures2016/
2. Bosetti C, Levi F, Rosato V, Bertuccio P, Lucchini F, Negri E, et al. Recent trends in colorectal cancer mortality in Europe. Int J Cancer. 2011;129(1):180-191.
3. Anuario de epidemiología y estadística MPPS. 2006, Venezuela. Disponible en: URL: http://www.mpps.gob.ve.
4. Chu KC, Tarone RE, Chow WH, Hankey BF, Ries LA. Temporal patterns in colorectal cancer incidence, survival and mortality from 1950 through 1990. J Natl Cancer Inst. 1994;86(13):997-1006.
5. Roth AD, Tejpar S, Delorenzi M, Yan P, Fiocca R, Klingbiel D, et al. Prognostic role of KRAS and BRAF in stage II and III resected colon cancer: Results of the translational study on the PETACC-3, EORTC 40993, SAKK 60-00 trial. J Clin Oncol. 2010;28(3):466-474.
6. Ogino S, Meyerhardt JA, Irahara N, Niedzwiecki D, Hollis D, Saltz LB, et al. KRAS mutation in stage III colon cancer and clinical outcome following intergroup trial CALGB 89803. Clin Cancer Res. 2009;15(23): 7322-7329.
7. Ciardiello F1, Tejpar S, Normanno N, Mercadante D, Teague T, Wohlschlegel B, et al. Uptake of KRAS mutation testing in patients with metastatic colorectal cancer in Europe, Latin America and Asia. Target Oncol. 2011;6(3):133-145.
8. Karapetis CS, Khambata-Ford S, Jonker DJ, O'Callaghan CJ, Tu D, Tebbutt NC, et al. K-ras mutations and benefit from cetuximab in advanced colorectal cancer. N Engl J Med. 2008;359(17):1757-1765.
9. Neumann J, Zeindl-Eberhart E, Kirchner T, Jung A. Frequency and type of KRAS mutations in routine diagnostic analysis of metastatic colorectal cancer. Pathol Res Pract. 2009;205(12):858-862.
10. Vale CL, Tierney JF, Fisher D, Adams RA, Kaplan R, Maughan TS, et al. Does anti-EGFR therapy improve outcome in advanced colorectal cancer? A systematic review and meta-analysis. Cancer Treat Rev. 2012;38(6):618-625.
11. Petrelli F, Borgonovo K, Cabiddu M, Ghilardi M, Barni S. Cetuximab and panitumumab in KRAS wild-type colorectal cancer: A meta-analysis. Int J Colorectal Dis. 201126(7):823-833.
12. Winder T, Mundlein A, Rhomberg S, Dirschmid K, Hartmann BL, Knauer M, et al. Different types of K-Ras mutations are conversely associated with overall survival in patients with colorectal cancer. Oncol Rep. 2009;21(5):1283-1287.
13. Roth AD, Tejpar S, Delorenzi M, Yan P, Fiocca R, Klingbiel D, et al. Prognostic role of KRAS and BRAF in stage II and III resected colon cancer: Results of the translational study on the PETACC-3, EORTC 40993, SAKK 60-00 trial. J Clin Oncol. 2010;28(3):466-474.
14.Estrada P, Rojas-Atencio A, Zabala W, Borjas L, Soca L, Urdaneta K. Frecuencia y asociación clínico-patológico de las mutaciones del oncogen K-ras en pacientes venezolanos con cáncer colorrectal. Invest Clín. 2009;50(1):55-63.
Notas de autor
barbara_martinez_alfonzo@hotmail.com
