Artículos Originales
RADIOTERAPIA HIPOFRACCIONADA EN TRATAMIENTO PRESERVADOR DEL CÁNCER DE MAMA ESTADIO PRECOZ EXPERIENCIA DE 6 AÑOS
RADIOTERAPIA HIPOFRACCIONADA EN TRATAMIENTO PRESERVADOR DEL CÁNCER DE MAMA ESTADIO PRECOZ EXPERIENCIA DE 6 AÑOS
Revista Venezolana de Oncología, vol. 29, núm. 1, pp. 22-31, 2017
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 01 Septiembre 2016
Revisado: 23 Septiembre 2016
Aprobación: 15 Diciembre 2016
Resumen: OBJETIVO: Presentar resultados actualizados de nuestra experiencia de 6 años en tratamiento preservador del cáncer de mama precoz con radioterapia hipofraccionada. MÉTODO: Se realizó una revisión retrospectiva de 499 pacientes con carcinoma precoz de mama, tratada con cirugía preservadora y radioterapia hipofraccionada en el período 2009-2015. Técnica utilizada fue RTC3D, dosis a la glándula mamaria fue 42,56 Gy en 16 fracciones, seguida de 3 dosis adicionales dirigidas al lecho tumoral completando 50,54 Gy. RESULTADOS: La mayoría de las pacientes fueron estadio I: 75 %. Tipo histológico más común fue carcinoma ductal infiltrante (67,7 %). Sobrevida global a los 5 años fue 95,6 %, sobrevida causa específica 96,4 % y la sobrevida libre de enfermedad 94 %. Se obtuvo control locorregional en 99,6 % de las pacientes. La toxicidad aguda más frecuente fue radiodermatitis grado 1 observada en 56 % de los casos. La toxicidad crónica incluyó complicaciones cutáneas grado 1 y 2 en 21,7 % y 0,6 % respectivamente y 61,7 % de las pacientes no desarrolló ninguna complicación. CONCLUSIONES: El tratamiento radiante hipofraccionado en pacientes con diagnóstico de cáncer de mama precoz pos tratamiento preservador ha mostrado ser efectivo y con resultados comparables a los esquemas de fraccionamiento convencional. Los resultados favorables obtenidos en 6 años, en cuanto a sobrevida global, sobrevida libre de enfermedad, control locorregional y morbilidad aguda y tardía, son comparables con los reportados a nivel internacional, por lo que justificamos el uso de este esquema.
Palabras clave: Cáncer, mama, tratamiento, preservador, radioterapia, hipofraccionada.
Abstract: OBJECTIVE: The objective of this work is to report our 6 years experience in the preservation treatment of the early stage breast cancer with radiotherapy hypofractionated. METHOD: A retrospective review study of 499 patients was conducted with the early breast carcinoma treated with conservative surgery and radiotherapy hypofractionated in the period between 2009 and 2015. The technique used was the 3DCRT; the dose was 42.56 Gy in the mammary gland in 16 fractions, followed by 3 additional doses targeted to the tumor bed completing the dose of 50.54 Gy. RESULTS: Most patients were stage I: 75 %. The most common histological type was the invasive ductal carcinoma (67.7 %). Overall survival at 5 years was 95.6 % the cause specific survival was 96.4 % and the disease free survival 94 %. Locoregional control was observed in 99.6 % of 411 patients with adequate follow-up. The most common acute toxicity was observed in grade 1 radio-dermatitis 56 %. The chronic skin complications toxicity included grade 1 and 2 in 21.7 % and 0.6 % respectively and 61.7 % of patients did not develop any complications. CONCLUSIONS: The preserver treatment of breast cancer in early stage, with hypofractionated radiation therapy has demonstrated effectiveness comparable to the conventional fractionation schemes results. The favorable results obtained in 5 years, the overall survival, the locoregional control and early and late morbidity are comparable with those reported internationally so we justify the use of this scheme.
Keywords: Cancer, breast, treatment, preserver, radiotherapy, hypofractionated.
INTRODUCCIÓN
En la actualidad, la cirugía preservadora de mama seguida de radioterapia es la modalidad terapéutica estándar para los estadios precoces de carcinoma de mama. Diversos estudios clínicos (1,2,3,4,5) han demostrado que la radioterapia (RT) es fundamental en el tratamiento del cáncer de mama, evitando la extirpación total de la glándula mamaria, con resultados satisfactorios en cuanto a control local y sobrevida; logrando el 5 % de aumento absoluto en la sobrevida causa especifica de cáncer de mama en 15 años . En el esquema convencional de radioterapia se administra una dosis total de 45 Gy a 50 Gy a toda la glándula mamaria, con fracciones diarias de 1,8 Gy -2 Gy, administrados en un período de 5 a 6 semanas, con o sin dosis adicional (boost) al lecho tumoral de 10 Gy-16 Gy. En las últimas dos décadas el esquema de radioterapia hipofraccionada se ha evaluado de manera extensiva y se ha comparado con las técnicas convencionales. El empleo de hipofraccionamiento en cáncer de mama, en la década de 1960-1970, produjo un aumento de las complicaciones tardías de la radioterapia, porque a menudo no se redujo la dosis total de radiaciones de manera adecuada cuando se desarrollaron estos regímenes de tratamiento; posteriormente aparecieron varios ensayos clínicos que han demostrado la utilidad de la radioterapia hipofraccionada en esta neoplasia, en los cuales se realizó un ajuste de la dosis total logrando el equivalente biológico de la dosis al fraccionamiento convencional (6). En el hipofraccionamiento se aumenta la dosis diaria por fracción con una disminución de la dosis total de radiación, lo que conlleva a abreviar el tiempo total de tratamiento a 3 semanas.
Cuatro importantes estudios clínicos aleatorios se han llevado a cabo en el Reino Unido y Canadá, los cuales demuestran que los protocolos de hipofraccionamiento producen resultados comparables en cuanto a control tumoral, sobrevida libre de enfermedad, sobrevida global, efectos cosméticos y toxicidad, al comparar con el fraccionamiento convencional(7,8,9,10).
Motivados por la evidencia existente, en el año 2009 iniciamos el uso de radioterapia hipofraccionada para las pacientes con carcinoma de mama precoz tratadas con cirugía preservadora. En el presente estudio daremos a conocer los resultados actualizados en cuanto a nuestra experiencia en los últimos 6 años, de las pacientes tratadas con regímenes de hipofraccionamiento en la Unidad de Radioterapia Oncológica del Instituto Médico La Floresta y en el Servicio de Radioterapia Dr. Enrique Gutiérrez del Centro Médico Docente La Trinidad.
MÉTODO
Se realizó una revisión de las historias clínicas de las pacientes con cáncer de mama estadio precoz, ganglios negativos, tratadas con cirugía preservadora y radioterapia hipofraccionada, en la Unidad de Radioterapia Oncológica GURVE del Instituto Médico La Floresta y en el Servicio de Radioterapia Dr. Enrique Gutiérrez del Centro Médico Docente La Trinidad (CMDLT) en el período comprendido entre los años 2009- 2015. Se revisaron 519 historias clínicas, 20 pacientes fueron excluidas por tener enfermedad localmente avanzada. Las pacientes fueron tratadas en acelerador lineal (AL) de energía dual empleando fotones de distintas energías para irradiar toda la glándula mamaria y electrones y/o fotones, para el “boost” o dosis adicional al lecho tumoral.
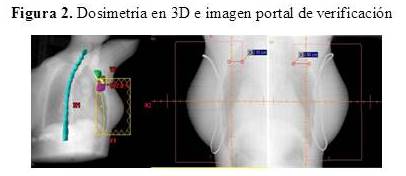
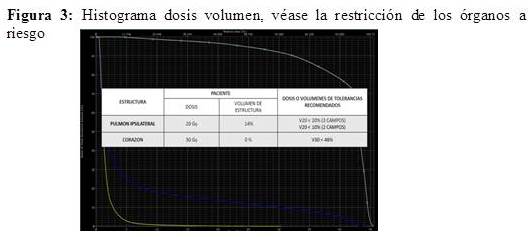
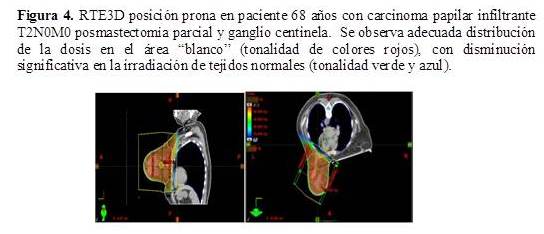
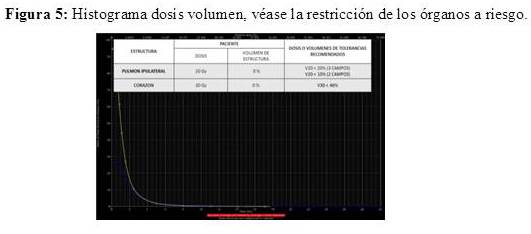
Todas las pacientes recibieron radioterapia posoperatoria utilizando técnica conformada con planificación 3D (RTC3D). Se utilizó para esta planificación una tomografía computarizada de tórax, por medio de un tomógrafo helicoidal de 64 cortes; se delimitaron los volúmenes “blanco” (mama afecta y lecho) y los órganos a riesgo (pulmones y corazón) en cada una de las pacientes. Para la planificación del tratamiento se define el volumen tumoral clínico (CTV) que incluye toda la glándula mamaria, la cual se delimita mediante marcadores fiduciarios (alambres metálicos radiopacos). El volumen de planificación (PTV) incluye el CTV, más un margen que usualmente es de 2 cm en sentido cráneo caudal. Se emplean campos tangenciales opuestos para el tratamiento de la mama, los cuales se conforman a través del colimador multiláminas, para excluir el área cardíaca y disminuir al máximo la irradiación del tejido pulmonar (Figura 1 y 2). Se realizó dosimetría en 3D, para determinar la dosis en la glándula mamaria, empleando cuando fue necesario filtros en cuña, para lograr una mayor homogeneidad en la distribución de la dosis. Por medio de histogramas dosis-volumen se evalúa la dosimetría, a nivel de la mama y la dosis en órganos a riesgo (Figura 3). 461 pacientes fueron colocadas en posición supina utilizando un soporte de mama en plano inclinado y 33 pacientes en posición prona, en un soporte en el cual queda suspendida la mama a tratar (Figura 4 y 5).

El esquema de tratamiento utilizado, fue similar al del estudio de Canadá (7), con la variante de emplear dosis adicional (boost) al lecho tumoral. Se administró una dosis de 42,6 Gy en 16 fracciones de 2,66 Gy a toda la glándula mamaria, seguida de 3 fracciones adicionales al lecho tumoral (boost) para un total de 50,54 Gy, para el boost se utilizó un haz de electrones o campos tangenciales reducidos con fotones de 6 MEV, dependiendo de la profundidad del lecho tumoral.
Para el seguimiento, usamos los datos de la historia clínica de radioterapia, o se contactaron a los médicos referidores, de no existir información se contactó a las pacientes por vía telefónica. La mediana de seguimiento fue de 29 meses, con un rango de 0 a 83,7 meses.
Se realizó el análisis de los datos demográficos, clínicos y de la terapéutica administrada, presentando los resultados de sobrevida, control local, complicaciones agudas y tardías del tratamiento. El análisis de la sobrevida fue hecho por el método Kaplan-Meier (11).
RESULTADOS
Se analizaron un total de 499 pacientes con carcinoma de mama estadio precoz tratadas con radioterapia hipofraccionada posterior a cirugía preservadora, entre el período 2009-2015. La edad promedio fue de 59,7 años, con un rango de 29 a 90 años. La evaluación inicial de las pacientes incluyó, perfil de laboratorio, ultrasonido mamario, mamografía, biopsia, anatomía patológica, TC de tórax.
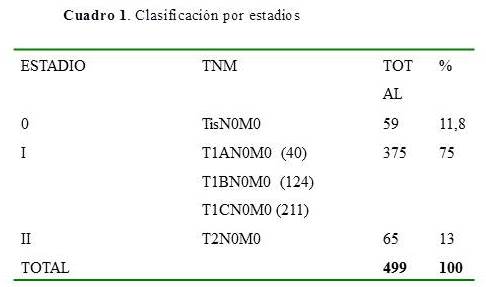
Para la clasificación por estadios seguimos el sistema de la AJCC (American Joint Committee on Cáncer) (12), la mayoría de las pacientes fueron clasificadas como estadio I: 75 %, estadio II: 13 % y carcinoma in situ: 11,8 %
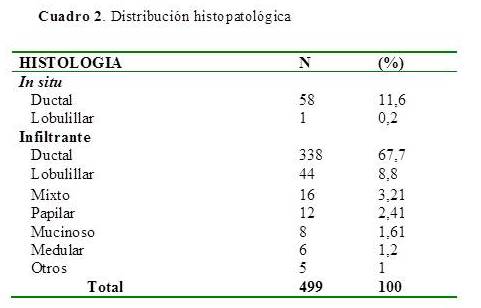
Los grupos histopatológicos fueron registrados en base a los informes de anatomía patológica, provenientes de los servicios de patología. No se realizó de rutina revisión del material de la biopsia. El subtipo histológico más común fue el carcinoma ductal infiltrante en 338 pacientes (67,7 %), seguido de ductal in situ en 58 pacientes (11,6 %), lobulillar infiltrante en 44 (8,8 %) y otros.
El tiempo de seguimiento fue de 29 meses, con un intervalo de 0 a 83,7 meses.
En el seguimiento de nuestras pacientes se encontró que de las 499 pacientes en estudio, hasta la fecha 411 (82,5 %) se encuentran vivas sin enfermedad (VSE), 6 (1 %) fallecieron a causa de la enfermedad (MCE), 7 (1,4 %) se encuentran vivas con enfermedad hasta su último control y 3(0,6 %) fallecieron sin enfermedad y por otras causas (MSE); 72 (14,5 %) se encuentran perdidas de control (se consideró pérdida de control aquella paciente, cuyo seguimiento es menor a seis meses sin haber muerto).
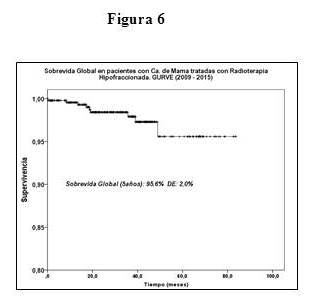
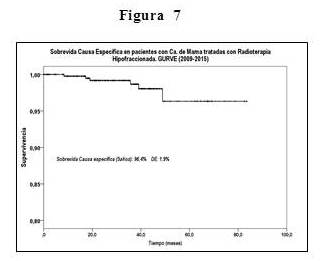
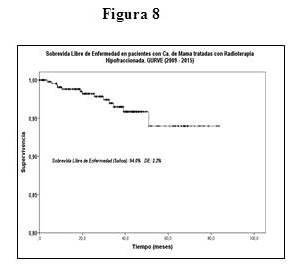
Con respecto a la sobrevida global (SG), a los 5 años fue 95,6 %, la sobrevida causa específica (SCE) 96,4 %, y la sobrevida libre de enfermedad 94 % (Figura 6, 7 y 8). En cuanto al control locorregional, obtuvimos 99,6 %, 2 pacientes presentaron recidivas locales, en 7 pacientes hubo progresión a distancia; el tratamiento de rescate consistió en quimioterapia.
COMPLICACIONES
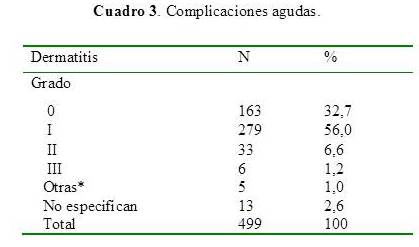
La toxicidad aguda y tardía fue evaluada según los criterios del grupo de radioterapia oncológica (RTOG) (13). Las complicaciones agudas más frecuentes se observaron a nivel de piel, radiodermatitis grado 1 en 279 (56 %) pacientes, dermatitis grado 2 en 33 pacientes (6,6 %) y grado 3 en 6 pacientes (1,2 %) que lo asociamos a mamas muy péndulas. 163 (32,7 %) de las pacientes no presentó complicaciones. En 1 % observamos hipersensibilidad del área tratada (Cuadro 3).
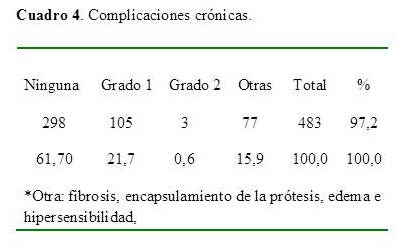
En cuanto a las complicaciones tardías, en 298 pacientes (61,7 %) no se presentaron complicaciones en piel, no se reportó reacciones cutánea grado 3, grado 2 en 3 (0,6 %), grado 1 en 105 pacientes (21,7 %) y aumento de la sensibilidad, fibrosis leve y edema en área tratada se vio en 15,9 %, en 1 (0,2 %) paciente se encapsuló la prótesis.
DISCUSIÓN
Se ha demostrado que los tejidos sanos y malignos tienen 2 tipos de respuesta a la radioterapia, que son la reacción aguda y la tardía, lo cual se revela en la radiosensibilidad. Estos conceptos han sido definidos en el modelo lineal cuadrático (relación α/β) que nos permite predecir las diferentes respuestas de los tejidos. El tejido mamario tiene una relación α/β baja, lo que hace que él sea más sensible al tamaño de la fracción. Estos modelos biológicos apoyan el concepto de hipofraccionamiento, donde con un incremento leve de la fracción diaria con una disminución de la dosis total es equivalente al fraccionamiento estándar con respecto al control local y la morbilidad tardía a la radiación (14,15).
El grupo de Oncología Clínica de Ontario (OCOG) condujo un trabajo de hipofraccionamiento, con 1 234 pacientes con cáncer de mama, ganglios negativos y márgenes libres, tratadas con cirugía preservadora(7,16). Estos investigadores compararon el régimen hipofraccionado de 42,5 Gy en 16 fracciones en 22 días (2,66 Gy) vs., el estándar de 50 Gy en 25 fracciones en 35 días (2 Gy/día), observando que con un seguimiento de 5-8 años, la incidencia de recurrencia local fue de 3,2 % para el grupo estándar y de 2,8 % para el grupo hipofraccionado. En cuanto a los resultados cosméticos, los resultados fueron buenos en un 77 % de los pacientes del grupo estándar y 77 % en el tratado con hipofraccionamiento. La toxicidad en piel grado II o III, fue infrecuente, de 3 % en ambos grupos. Igualmente, la fibrosis del tejido celular subcutáneo fue de 5 % y 7 % respectivamente.
En los estudios del Reino Unido, START A y START B se realizó una comparación del régimen estándar de radioterapia vs., el hipofraccionado, ambos estudios fueron llevados en paralelo, evaluando el control locorregional del tumor, efectos sobre los tejidos normales, calidad de vida e impacto económico. En estos ensayos clínicos se permitió el uso de quimioterapia y/u hormonoterapia. En el START A se midió la sensibilidad de los tejidos normales y malignos al tamaño de la fracción comparando 2 esquemas de hipofraccionamiento con la finalidad de determinar cuál esquema equivale al convencional; 39 Gy en fracciones de 3 Gy y 41,66 Gy en fracciones de 3,2 Gy vs., 50 Gy en fracciones de 2,0 Gy (9,10)
El START A (9) incluyó 2 236 pacientes con cáncer de mama invasivo, pT13PN0-1M0, mayores de 18 años que necesitaron radioterapia pos-cirugía preservador o mastectomía. El seguimiento medio fue de 5,1 años y máximo de 8 años, encontrándose el 84,1 % de las pacientes vivas sin recaída y 4,2 % de las pacientes con recaída locorregional, no observándose diferencia estadísticamente significativa entre los 3 grupos. Las recaídas a distancia, la sobrevida libre de enfermedad y la sobrevida global fueron similares en los distintos esquemas de fraccionamiento.
El START B (10) incluyó 2 215 mujeres asignadas a 2 esquemas diferentes: 40 Gy en 15 fracciones a 2,67 Gy/día en 3 semanas vs. 50 Gy en 25 fracciones a 2,6 Gy en 5 semanas con el objetivo de medir recurrencia locorregional, efectos sobre tejidos normales y calidad de vida. Con un seguimiento medio de 6 años, el riesgo de recurrencia locorregional a los 5 años fue de 2,9 %, sin diferencia entre los 2 grupos. Los cambios en la apariencia de la mama y endurecimiento fueron significativamente menores (P:02) en el grupo hipofraccionado comparado con el fraccionamiento convencional de 50 Gy.
En ambos estudios del Reino Unido el seguimiento es muy corto para determinar el potencial daño cardíaco, la prioridad es proteger el corazón a la exposición de la radiación, lo cual ahora es posible con las nuevas tecnologías. La proporción de pacientes con resultados cosméticos excelentes o buenos es similar en ambos grupos; concluyendo que 40 Gy en 15 fracciones en 3 semanas ofrece un control locorregional y cosmético bueno, equivalente al estándar de 50 Gy en 25 fracciones en 5 semanas.
Whelan y cols. (16) condujeron un estudio con 1 234 pacientes con cáncer de mama invasivo, axila negativa sometidas a cirugía preservadora, asignadas en formas aleatoria a 50 Gy en 25 fracciones en 35 días (grupo control) o 42,5 Gy en 16 fracciones en 22 días (grupo hipofraccionado). Se excluyeron pacientes con carcinoma in situ, márgenes comprometidos, tumores mayores de 5 cm y mamas voluminosas. La recurrencia local a los 10 años fue de 6,7 % en el grupo control y 5,2 % en el grupo hipofraccionado. El hipofraccionamiento parece ser menos efectivo en tumores de alto grado, con una recurrencia local a los 10 años de 4,7 % en grupo control contra 15,6 % en grupo hipofraccionado. La sobrevida a los 10 años fue de 84,4 % en el grupo control vs. 84,6 % en el grupo hipofraccionado. No hubo diferencias en cuanto a los resultados cosméticos en los 2 grupos. A los 10 años, 71,3 % de las mujeres del grupo control obtuvieron un resultado cosmético de excelente a bueno, en comparación con 69,8 % en el grupo hipofraccionado. Con un seguimiento de 12 años, el riesgo de recurrencia local es bajo en ambos grupos; sin embargo, en el subgrupo de pacientes de alto riesgo (alto grado nuclear) el régimen hipofraccionado parece ser menos efectivo.
La radioterapia se ha asociado con un aumento en el riesgo de muerte por enfermedad coronaria, observado posterior a los 10 años de tratamiento. En este trabajo no hubo diferencia en cuanto a sobrevida global en ambos grupos con un seguimiento de 12 años, y tampoco en la incidencia de enfermedad cardiaca, 1,5 % con fraccionamiento estándar vs. 1,9 % con radioterapia hipofraccionada(16).
Williamson y cols., del Princess Margaret Hospital han extrapolado la experiencia del tratamiento hipofraccionado en carcinoma invasivo al carcinoma ductal in situ . Estos autores evaluaron 366 pacientes con diagnóstico CDIS o carcinoma microinvasivo (≤ 1 mm de invasión) tratadas con cirugía preservadora con o sin muestreo ganglionar. El 39 % de las pacientes recibieron 50 Gy en 25 fracciones y 61 % recibieron esquemas hipofraccionados: 42,2 Gy en 16 fracciones o 40 Gy en 16 fracciones más dosis de refuerzo al lecho tumoral (12,5 Gy). Las recurrencias locales han sido similares a los 4 años, 6 % para el esquema control vs. 7 % para los grupos hipofraccionados. En los tumores de alto grado nuclear se observó un aumento del riesgo de recurrencias, 11 %, comparado con un 4 % para las lesiones grado II y ninguna para los grados I (P 0,029). La presencia de comedonecrosis, se asoció con un riesgo de recurrencias locales del 8 % a los 4 años, vs. 2 % en ausencia de este factor. Estos autores concluyen que no hay diferencia entre los esquemas hipofraccionados y convencionales, en pacientes con CDIS, con una baja tasa de recurrencia local (17).
Las mamas voluminosas generalmente se asocian con una dosis no homogénea lo que influye para una mayor ocurrencia de reacciones agudas (18). Sin embargo, con la modificación en el tratamiento en posición prona, se puede lograr mayor homogeneidad de la dosis y con ello disminuir los efectos secundarios en piel durante el tratamiento radiante.
Stuti y cols. (19) compararon la radioterapia convencional durante 6 semanas vs. hipofraccionamiento durante 3 semanas, en 83 mujeres con carcinoma de mama en estadios 0 a IIIA con factores de riesgo (ganglios positivos, jóvenes y receptores negativos), con seguimiento medio de 40 meses, dosis total 36,63 Gy a toda la mama en 11 fracciones, seguido de boost a lecho quirúrgico por 4 fracciones adicionales de 3,33 Gy; se obtuvieron resultados de sobrevida libre de recurrencia a tres años 95,9 % y resultado cosmético excelente en 94 % de las pacientes evaluables.
Bhavana y cols. (20) del departamento de radioterapia oncológica de la Universidad de Pittsburgh, identificaron 5 112 pacientes tratadas con radioterapia hipofraccionada desde el año 2009 al 2014, en quienes se cumplieron los criterios de inclusión, demostrando que el uso del hipofraccionamiento se incrementó de manera significativa desde el año 2009 (8,3 %) al año 2014 (81,4 %) y este hecho fue más notorio en centros que brindan educación académica que en otros centros de radioterapia. Encontrando que la experiencia clínica es un mecanismo eficaz para la normalización de los patrones de la práctica clínica y la promoción del cambio consistente con las guías basadas en la evidencia actual para el uso de la radioterapia hipofraccionada en mujeres con diagnóstico de cáncer de mama estadio precoz.
Nuestros resultados indican, que las complicaciones y los efectos cosméticos, observados en las 499 pacientes tratadas con hipofraccionamiento, son comparables a los regímenes de fraccionamiento convencional. El tratamiento preservador del cáncer de mama en estadio precoz constituye el estándar actual terapéutico de esta afección neoplásica logrando altas cifras de sobrevida global (95,6 %), sobrevida causa específica (96,4 %) y control local (99,6 %).
La radioterapia con esquemas de hipofraccionamiento en períodos de 3 a 4 semanas, en el tratamiento preservador del cáncer de mama, produce resultados comparables a los esquemas de fraccionamiento convencional de 50 Gy en 25 fracciones. En 4 estudios aleatorios se ha demostrado la efectividad de estos regímenes de fraccionamiento, más convenientes para las pacientes, para los servicios de radioterapia, y la integración con otras modalidades terapéuticas.
Los resultados obtenidos en esta serie de 499 pacientes tratados con cirugía preservadora y radioterapia hipofraccionada, tienen una sobrevida global de 95,6 %, sobrevida causa especifica de 96,4 %, sobrevida libre de enfermedad de 94 % y control locorregional de 99,6 % a los 5 años, parecen estar de acuerdo con los reportados en otras revisiones. Los resultados del presente estudio, nos animan a continuar el empleo de estos esquemas de radioterapia en la práctica clínica. Según estudios recientes (19) las técnicas actuales de radioterapia con hipofraccionamiento usando esquemas reducidos (3 semanas) en aquellas pacientes con factores de riesgo (ganglios positivos, pacientes jóvenes y receptores negativos), parecen ser efectivos, ofreciendo baja toxicidad con excelentes resultados cosméticos y logrando resultados de sobrevida libre de progresión y control local; estos puntos serán objeto de estudio para futuras investigaciones.
Referencias
1. Clarke M, Collins R, Darby S, Davies C, Elphinstone P, Evans V, et al. Effects of radiation therapy and of differences in the extent of surgery for early breast cancer on local recurrence and 15- years’ survival: An overview of the other randomized trials. Lancet. 2005;366(9503):2087-2106.
2. Fisher B, Anderson S, Bryant J, Margolese RG, Deutsch M, Fisher ER, et al. Twenty year follow up of a randomized trial comparing total mastectomy, lumpectomy and lumpectomy plus radiation for the treatment of invasive breast cancer. N Engl J Med. 2002;347(16):1233-1241.
3. Veronesi U, Luini A, Del Vecchio M, Greco M, Galimberti V, Merson M, et al. Radiotherapy after breast preserving surgery in women with localized cancer of the breast. N Engl J Med. 1993;328(22):1587-1591.
4. Clark RM, Whelan T, Leuvine M, Roberts R, Willan A, McCulloch P, et al. Randomized clinical trial of breast irradiation following lumpectomy and axillary dissection for node negative breast cancer: An update. J Nat Cancer Inst. 1996;85:1659-1664.
5. Haffty BG, Sucre CV, Vera A. Cáncer de mama. En: Urdaneta N, Vera A, Peschel RE, Wilson LW, editores. Radioterapia oncológica enfoque multidisciplinario. Caracas: Editorial Disinlimed; 2009.p.671-729.
6. Yarnold J, Bentzen SM, Coles C, Haviland J. Hypofractionated whole breast radiotherapy for women with early breast cancer myths and realities. Int J Radiat Oncol Biol Phys. 2011;79(1):1-9.
7. Whelan TJ, Pignol JP, Levine MN, Julian JA, MacKenzie R, Parpia S, et al. Long-term results of hypofractionated radiation therapy for breast cancer. N Engl J Med. 2010;362(6)513-520.
8. Haviland JS, Owen JR, Dewar JA, Agrawal RK, Barrett J, Barrett-Lee PJ, et al. The U.K. Standardization of breast radiotherapy (START) trials of radiotherapy hypo-fractionation for treatment of early breast cancer: 10 year follow-up results of two randomized controlled trials. Lancet Oncol. 2013;14(11):1086-1094.
9. START Trialists' Group, Bentzen SM, Agrawal RK, Aird EG, Barrett JM, Barrett-Lee PJ, et al. The UK standardization of breast radiotherapy (START) trial A of radiotherapy hypo-fractionation for treatment of early breast cancer: A randomized trial. Lancet Oncol. 2008;9(4):331-341.
10. START Trialists' Group, Bentzen SM, Agrawal RK, Aird EG, Barrett JM, Barrett-Lee PJ, et al. The UK standardization of breast radiotherapy (START) trial B of radiotherapy hypofractionation for treatment of early breast cancer: A randomized trial. Lancet Oncol. 2008;371(9618):1098-1107.
11. Matthews DE, Farewell VT, editores. Using and understanding Medical Statistics. S Margen-AG, Suiza; 2007.p.54.
12. Edge SBB, Compton DR, Fritz CC, Greene AG, Trotti A, editores. AJCC Cancer Staging Manual 7a edición. Nueva York, NY: Springer; 2010.
13. Radiation Therapy Oncology Group (RTOG/EORTC). Acute and late radiation morbidity score criteria. Disponible en: URL: http://bit.ly/2eOpw7C
14. Sharon X, White J, Allen Li X. Is α/β for breast cancer really low? Disponible en: URL: http://bit.ly/2fxDNpg
15. Theberge V, Whelan T, Shaitelman SF, Vicini FA. Altered fractionation: Rationale and justification for whole and partial breast hypofractionated radiotherapy. Semin Radiat Oncol. 2011;21(1):55-65.
16. Whelan T, Kim DH, Sussman J. Clinical Experience using hypofractionated radiation schedules in breast cancer. Semin Radiat Oncol. 2008;18(4):257-264.
17. Williamson D, Dinniwell R, Fung S, Pintilie M, Done SJ, Fyles AW. Local control with conventional and hypofractionated adjuvant radiotherapy after breast-conserving surgery for ductal carcinoma in situ. Radiother Oncol. 2010;95(3):317-320.
18. Deantonio L, Gambaro G, Beldi D, Masini L, Tunesi S, Magnani C, et al. Hypofractionated radiotherapy after conservative surgery for breast cancer: Analysis of acute and late toxicity. Radiat Oncol. 2010;5:112.
19. Ahlawat S, Haffty BG, Goyal S, Kearney T, Kirstein L, Chen C, et al. Short-course hypofractionated radiation therapy with boost in women with stages 0 to IIIA breast cancer: A phase 2 trial. Int Radiat Oncol Biol Phys. 2016;94(1):118-125.
20. . Chapman BV, Rajagopalan MS, Heron DE, Flickinger JC, Beriwal S. Clinical pathways: A catalyst for the adoption of hypofractionation for early-stage breast cancer. Int J Radiat Oncol Biol Phys. 2015;93(4):854-861
Notas de autor
sandralopezvera@hotmail.com