
Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 31 Agosto 2017
Revisado: 23 Septiembre 2017
Aprobación: 20 Enero 2018
Resumen: OBJETIVO: Reportar la experiencia de nuestra institución en el tratamiento de los tumores desmoides con radioterapia. MÉTODO: Revisión retrospectiva de 23 pacientes tratados con radioterapia en el período 2000 a 2015. Los 74 % localizados en el tronco. 56 % eran recurrentes. En 22 se practicó cirugía. 82 % recibió radioterapia posoperatoria, 13 % radioterapia preoperatoria y 5 % radioterapia sola 69,5 %. En 82 % se empleó RTC3D. Dosis oscilaron de 4 600 - 6 000 cGy. La media de seguimiento 14,4 meses. RESULTADOS: De los 23 pacientes 14 vivos sin enfermedad, 5 vivos con enfermedad (3 con progresión 2 estables. Sobrevida libre de progresión a los 5 años 94,7 %, 10 años 70 %. No hubo toxicidad aguda severa. Complicaciones crónicas incluyeron fibrosis con limitación funcional y radionecrosis en 2 pacientes. CONCLUSIONES: La radioterapia es un tratamiento efectivo en los tumores desmoides como complemento a la cirugía con resección incompleta, en recidivas y tumores irresecables. Los resultados de sobrevida libre de progresión y control local se comparan con otras series.
Palabras clave: Tumores, desmoide, radioterapia, tratamiento, cirugía.
Abstract: OBJETIVE: Report our experience in the treatment of desmoids tumors with radiotherapy. METHOD: Retrospective review 23 patients treated with radiotherapy in the period 2000-2015. The anatomic locations trunk was 74 %, extremities 13 %, head and neck 8.6 % 4.3 % multifocal. 56 % were recurrences after surgery. 22 of 23 had surgery. Adjuvant radiotherapy was used in 82 % of patients, 13 % neoadjuvant radiotherapy and 5 % radiotherapy alone. 82 % of patients were treated with 3DCRT techniques. Dose varied from 4 600 - 6 000cGy. Median follow up was 14.4 months RESULTS: The majority of patients, 14 are alive without disease. 5 alive with disease (3 with progression and 2 stable), 4 were lost of follow up. Super life free progression was 94.7 %, 70 % at 5 years and 10 years respectively. CONCLUSION: Radiotherapy is an effective treatment in desmoids tumors as an adjuvant to surgery with incomplete resection, in recurrent tumors and unresectable lesions. The results local control and super life free progression compare with another series.
Keywords: Tumors, desmoids, radiotherapy, treatment, surgery.
INTRODUCCIÓN
Los tumores desmoides, también llamados fibromatosis agresiva son lesiones benignas que se originan del tejido conectivo y aparecen en la fascia muscular profunda, aponeurosis, tendones (1,2,3). Son de crecimiento lento, localmente agresivos con tendencia a invadir estructuras adyacentes y capaces de adquirir grandes tamaños (4) pero rara vez producen metástasis a distancia y des-diferenciación, con posibilidad de recurrencia incluso después de una resección completa, pudiendo ser multifocales, algunos casos raros regresan espontáneamente.
Los desmoides representan el 0,03 % de todas las neoplasias y menos del 3 % de todos los tumores de tejidos blandos, alcanzando una incidencia de 2 a 4 por millón de habitantes por año (4,5). Existe una leve predominancia en el sexo femenino con una relación de 1:1.5-2.5 (5,6) con un pico de incidencia entre la 3a y 4a década de la vida, pero pudiendo ocurrir tanto en la infancia como en la vejez (7,8,9,10).
La fibromatosis profunda se presenta en tres localizaciones:(4)
· Extra-abdominal. Más frecuente en cintura escapular y pelviana, pared costal y cuello.
· Abdominal (pared abdominal). Comúnmente diagnosticada en mujeres durante la gestación o en el posparto.
· Intra-abdominal. En pelvis o mesenterio. En ocasiones, las fibromatosis mesentéricas se asocian con la poliposis adenomatosa familiar, síndrome de Gardner.
La etiología de los tumores desmoides es desconocida, aunque se ha asociado su aparición en algunos casos con traumas o lechos quirúrgicos o con factores genéticos como en los casos de localización intra-abdominal asociados con el síndrome de poliposis adenomatosa familiar (6).
Recientemente se han estudiado los eventos moleculares que intervienen en la etiopatogenia de estos tumores. Se han encontrado una fuerte relación del gen APC y la Beta catenina componente de la vía de señalización Wnt en la patogénesis molecular de los tumores desmoides esporádicos y los asociados con el síndrome de Gardner (11). Estudios de biología molecular han comprobado que los desmoides constituyen una proliferación celular clonal y no un proceso reactivo policlonal, lo que confirma la naturaleza neoplásica de estas afecciones (12).
Otras mutaciones descritas en tumores desmoides esporádicos incluyen la trisomía 8 y 20 además mutaciones AKT1,BRAF y PT53 en desmoides esporádicos (13).
Poseen una fuerte semejanza con el fibrosarcoma bien diferenciado. Desde el punto de vista microscópico predominan las fibras de colágeno con baja celularidad, y células fusiformes dispuestas en fascículos en paralelo. Con actividad mitótica baja y las atipias son extremadamente raras. No se observa necrosis ni pleomorfismo significativo. En la periferia células gigantes multinucleadas, macrófagos y linfocitos abundantes; a diferencia de los fibrosarcomas malignos en los cuales éstas células son poco frecuentes. La inmuhistoquímica es positiva para vimentina, con positividad variable para actina de músculo liso (SMA), CD117(c-Kit) y desmina. Siendo negativo para CD34. La expresión del c-kit indica la posibilidad de usar agentes dirigidos como el imatinib (14).
Clínicamente se presentan como masas que causan dolor leve con una historia de crecimiento lento asociados íntimamente con estructuras adyacentes (15,16,17). En el diagnóstico por imágenes de estas afecciones es de gran utilidad la resonancia magnética nuclear (RM) y la Tomografía (TC) para determinar la extensión del tumor, relación con estructuras adyacentes, resecabilidad y la evolución clínica de estas lesiones (9,16). En el estudio histológico se prefiere la biopsia incisional en vez de la biopsia por punción (6).
El tratamiento de elección es la cirugía;(16) sin embargo, las recurrencias después del tratamiento quirúrgico están alrededor del 50 % cuando los márgenes de resección son positivos o inadecuados y 20 % con márgenes negativos (18). La radioterapia (RT) puede ser de gran utilidad en caso de resección incompleta del tumor, lesiones inoperables o en recidivas de la enfermedad después del tratamiento quirúrgico. Algunos autores han recomendado, observación en casos de resección inicial del tumor primario con márgenes positivos si la progresión de la enfermedad no acarrea morbilidad significativa; esta práctica sólo podía llevarse a cabo en contadas ocasiones y con un seguimiento muy cuidadoso del paciente (18,19.20,21).
El objetivo del presente trabajo es describir nuestra experiencia en el manejo de tumores desmoides tratados en la unidad de radioterapia oncológica del IMLF y servicio de radioterapia Dr. Enrique M Gutiérrez del CMDLT durante un período de 15 años.
MÉTODO
Se realizó una revisión retrospectiva de 23 pacientes con el diagnóstico histológico de tumor desmoide tratados con radioterapia en los dos centros antes mencionados durante el período 2000 a 2015. Los datos obtenidos de las historias clínicas fueron registrados en una hoja de cálculo en Microsoft Office Excel®. Además en casos necesarios se obtuvo el seguimiento contactando los pacientes y/o al médico referente por vía telefónica. Se obtuvo una estadística descriptiva de la población en cuanto a datos demográficos, presentación clínica, estudios diagnósticos, tratamiento, complicaciones, cifras de sobrevida y control local por el método actuarial Kaplan Meier (22).
Se analizan un total de 23 pacientes, 13 de ellos presentaban recidivas locales después de cirugía al momento de ser referidos para RT, y 10 como tumor primario. En cuanto al sexo la mayoría (17) fueron del sexo femenino. La edad de los pacientes varió entre 1 a 65 años con un promedio de 30,8 años. En relación a la localización anatómica, la mayoría de las lesiones estuvieron localizadas en el tronco 17 pacientes (Cuadro 1). El tiempo de evolución entre el primer síntoma al momento de la consulta inicial osciló de 1 mes a 3 años, en 12 pacientes fue de 6 meses a 3 años. El tamaño del tumor osciló entre 2,3 cm a 16 cm, con un promedio de 8 cm; 52 % de los casos median entre 5 cm a 10 cm.
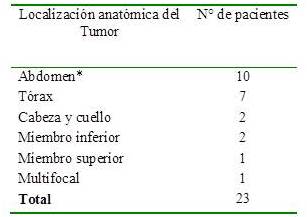
Cuadro 1
Localización del tumor.
* NOTA: Tres (3) de estos son intra-abdominal.
En 22 pacientes se realizó resección quirúrgica, y un paciente fue considerado irresecable. En 3 pacientes se aplicó RT preoperatoria, y en 19 RT después de la cirugía. Al analizar los márgenes de resección, en los tres pacientes sometido a RT pre operatoria, 1 de ellos presentó márgenes microscópicos positivos (R1), otro márgenes negativos (R0) y en otro se desconoce el estado de los márgenes; en los 19 pacientes sometidos a RT posoperatoria 4 presentaban márgenes estrechos (ME<5mm), 4 R1, y 4 R2, y 4 R0 pero fueron referidos a RT por presentar recidivas locales las cuales fueron resecadas.
La RT se aplicó en 23 pacientes, en 19 se empleó RT posoperatoria, en 3 RT preoperatoria y 1 paciente se trató con RT como tratamiento único. El tratamiento radiante fue administrado mediante diferentes técnicas, con un acelerador lineal (AL) de 4 MV inicialmente en los primeros años del estudio, y luego un AL de energía dual empleando fotones de 6 MV y 18 MV, en algunos casos se empleó haz de electrones sólo o haz mixto de fotones y electrones. La técnica más utilizada fue RT conformada con planificación 3D (RTC3D) en 16 pacientes, en 3 pacientes se utilizó RT de intensidad modulada y terapia modulada con arcos volumétricos. La dosis administrada osciló de 5 000 a 6 000 cGy con fracciones de 180 o 200 cGy, a excepción de un paciente con un desmoide intra-abdominal que recibió 4 600cGy. La dosis más elevada de 6 000cGy por lo general fue aplicada en pacientes con enfermedad macroscópica o con recidivas (Figura 1). En 2 pacientes se utilizó braquiterapia (BT), uno de ellos lactante de 7 meses tratada con resección parcial, seguida de BT con técnica de carga diferida remota alta tasa de dosis 2 000 cGy en fracciones de 200 cGy, seguida de RT externa con electrones 4 000 cGy con fracciones de 200 cGy, la otra paciente con lesión en pared abdominal presentó recidiva después de cirugía y RT externa, sometida a nueva resección quirúrgica y braquiterapia intersticial 300 cGy en 12 fracciones BID alcanzando 3 600 cGy.
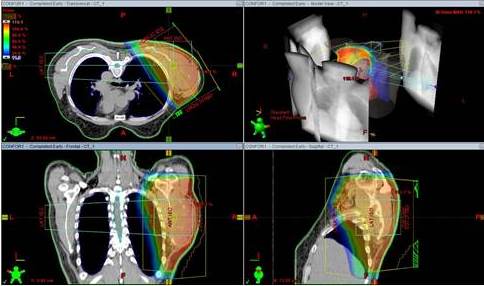
Figura 1
Paciente masculino de 61 año con tumor desmoide en región escapular y axilar izquierda. Irresecable Recibe RTC3D dosis 6 000cGy con fracciones de 200 cGy. La distribución porcentual de la dosis en los planos axial, coronal y sagital está representada por diferentes tonalidades de colores cuyos valores pueden observarse en la columna de la izquierda.
El seguimiento de la población se realizó por medio de consultas de control, contacto a través de llamadas telefónicas al paciente o solicitando información a los médicos referentes. Para la fecha se encuentran perdidos de control cuatro (4) pacientes (17,4 %). El tiempo de seguimiento osciló entre 1,8 a 504 meses con una mediana de 104,6 meses. Con un promedio de 145,4 meses.
RESULTADOS
Al analizar los 23 pacientes tratados con radioterapia se encuentran 14 pacientes vivos sin enfermedad (VSE); 5 pacientes vivos con enfermedad (VCE); 4 pacientes perdidos del seguimiento y ninguno ha fallecido (Cuadro 2). La sobrevida libre de progresión (SLP) a los 5 años fue 94,7 % y a los 10 años es de 70,0 %. La media de tiempo de sobrevida para esta población es de (360,2 ± 51,9) meses con un intervalo de confianza (IC): 95 % (258,4; 461,9) meses (Cuadro 2).
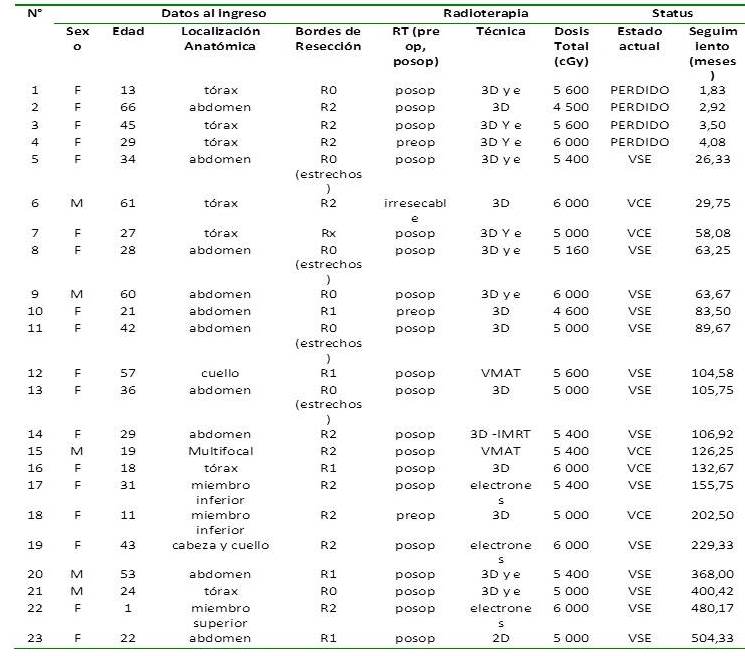
Cuadro 2
Seguimiento total de los 23 pacientes con tumores desmoides
*los R0 se trataron por ser tumor recurrente * Rx: se desconoce el estado del margen
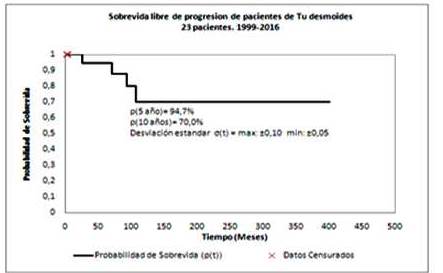
Figura 2.
Se observaron recidivas locales después de RT en 3 de 23 pacientes (13 %) 2 de ellos tenían lesiones localizados en el tórax (mama y región paravertebral) y 1 en pared abdominal. En 1 caso los márgenes de resección fueron negativos, en los otros 2 fueron positivos. Estos pacientes recibieron: 5 000 cGy (R0); 5 400cGy (R2) y 6 000cGy (R1). No se encontró una diferencia significativa en el control local para los pacientes que recibieron dosis < 5 400cGy VS >5 400cGy.
Todas las recurrencias estuvieron dentro del campo de tratamiento. Actualmente a 2 les plantean realizar cirugías de rescate mientras el otro se encuentra recibiendo tratamiento con imatinib.
La complicación aguda más frecuente fue radiodermatitis grado II, la cual no ameritó la interrupción del tratamiento radiante, la dermatitis grado I ocurrió en 39 % y la dermatitis grado II ocurrió en 43 %. Además se observaron complicaciones gastrointestinales grado I en 3 pacientes y grado en 2 en 1 paciente.
En cuanto a las complicaciones tardías se observó fibrosis grado I en 47 % y la radiodermatitis grado I en 60,8 %. En 1 paciente con lesión en la pared torácica se presentó dehiscencia de la herida operatoria e infección local, actualmente se encuentra en espera de evaluación por cirujano. La paciente en edad pediátrica con lesión del antebrazo tratada con resección parcial más BT y RT externa con electrones presenta fibrosis y limitación funcional parcial del antebrazo, otra paciente con lesión en la pared abdominal recidivante después de cirugía y RT externa presentó radionecrosis de la pared abdominal después de cirugía de rescate y BT, ameritando cirugía reconstructiva, ambas pacientes se encuentra actualmente sin enfermedad (Cuadro 3).
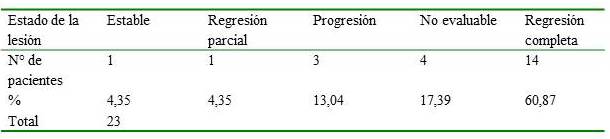
Cuadro 3
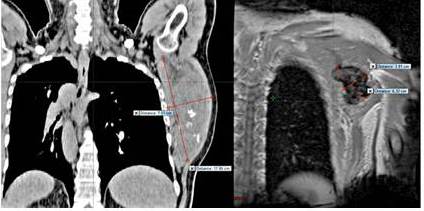
Figura 3
Paciente masculino de 61 años con tumor desmoide en región axilar y escapular izquierda. Imagen de TC en vista coronal antes de la radioterapia (A) y RM vista coronal 1 año después de tratamiento (B).
DISCUSIÓN
El tratamiento de elección inicial en los tumores desmoides es la cirugía siempre que pueda lograrse la resección completa del tumor con márgenes negativos, sin embargo, esta modalidad terapéutica está limitada por los límites anatómicas y la naturaleza infiltrativa de estas lesiones. Por lo tanto el objetivo fundamental del tratamiento quirúrgico debe ser la extirpación completa preservando la funcionalidad, cosmesis y reduciendo al mínimo la morbilidad
Existen ciertos aspectos que falta dilucidar acerca de este tumor, como es el caso del impacto de los márgenes positivos de resección en cuanto al control local y riesgo de recurrencia (23). No obstante una cirugía con márgenes microscópicos positivos (R1) es aceptable si la obtención de márgenes de resección adecuados podría ocasionar morbilidad excesiva. En un estudio de 426 pacientes con tumores desmoides, de ellos 370 se trataron con cirugía inicialmente en 252 se pudieron evaluar los márgenes quirúrgicos, se observó que no hay diferencia en los resultados en la sobrevida libre de progresión (SLP) a los 5 años, entre los pacientes con márgenes de resección adecuados (R0) 63 % vs., márgenes de resección microscópicos positivos (R1) 61 %, pero en los R2 la SLP fue sólo 22 % (24). Por lo tanto en ciertos casos seleccionados en lesiones asintomáticas sin morbilidad potencial podría considerarse la observación de cerca, con seguimiento estricto y tratamiento precoz al detectar la progresión de la enfermedad. Asimismo, también se debe tomar en cuenta la localización del tumor porque se ha reportado un mayor riesgo de recurrencia en los tumores de la pared abdominal comparados con los desmoides localizados en las extremidades (25,26).
La RT es una modalidad de tratamiento efectiva con pocos efectos locales y es de elección para tumores no resecables. Las indicaciones son: tumor primario no resecable, tumor recurrente y tumor resecado con márgenes positivos (27). En un meta análisis reciente, que incluyó 22 estudios retrospectivos con 780 pacientes de tumores desmoides se encontró que las tasas de control local global en los pacientes tratados con cirugía sola fueron 61 % vs. 75 % con cirugía + RT y 78 % con RT exclusiva aún después de dividir los casos en grupos de márgenes libres, positivos y en tumores primarios o recurrentes, se observó que el control local fue superior con RT o cirugía + RT (28).
En cuanto a las dosis de RT recomendadas oscilan entre 5 000 a 6 000 en fracciones de 180 a 200 cGy. En donde en casos de enfermedad microscópica la dosis debería ser alrededor de 5 000cGy y en caso de enfermedad macroscópica o de sospecha se debe alcanzar 5 600cGy con campos amplios con margen de 5 cm de acuerdo a la situación clínica (29,30,31,32). La respuesta después de la RT es lenta, presentando regresión continua incluso después de los 3 años (33).
En el Cuadro 4 se presenta 6 series de pacientes con tumores desmoides tratados con y sin cirugía para un total de 283 casos, el control local osciló entre 71 % a 81 % y la tasa de recidiva de 45 % a 8,5 %. En la presente serie de 23 pacientes, 22 fueron tratados con RT + cirugía y 1 RT únicamente. Las dosis utilizadas oscilaron de 4 600 a 6 000cGy, aunque el número de pacientes es reducido no se observó una relación clara entre las dosis <5 400cGy y >5 400cGy la tasa de recurrencia fue del 13 %. La SLP fue de 94,7 % a los 5 años y 70 % a los 10 años. Se observaron recurrencias locales en 3 pacientes. Ningún paciente hasta la fecha ha fallecido por la enfermedad
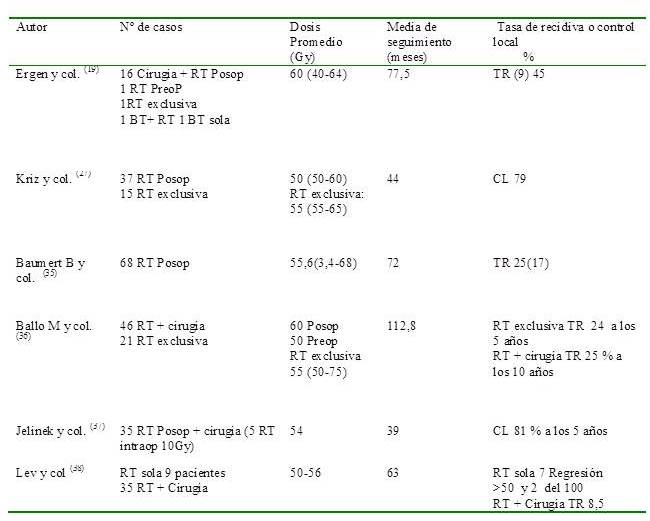
Cuadro 4
Resultados de tratamiento con RT.
TR: tasa de recidiva CL: control local
En nuestro país hasta la fecha se han publicado pocos trabajos sobre tumores desmoides. Liuzzi y col., (39) publican en 2014 2 casos de lesiones de cabeza y cuello. Dugarte y col., (40) reportaron otro caso en pie izquierdo, y Gómez y col., (41) presentaron otro paciente con tumor desmoide localizado en la pared abdominal.
La terapia sistémica que se usa en estos casos son los AINES que incluyen el sulindac o celecoxib, hormonas como el tamoxifeno o toremifeno, agentes biológicos como el interferón alfa, imatinib o sorafenib y drogas citotóxicas como la doxorrubicina, metrotexate, vinorelbina y vinblastina obteniendo resultados favorables siendo una opción para tumores avanzados, irresecables o que recurren después de cirugía más RT (42,43).
Las complicaciones agudas de la RT por lo general son limitadas principalmente dermatitis usualmente moderada grado II. Las complicaciones crónicas incluyen fibrosis 9 % a 23 % de los casos, disminución del rango de motilidad 6 %, parestesias, fracturas, edema 2 % a 3 %. En raras ocasiones se han reportado tumores inducidos por radiación 0,7 % de los casos sobretodo sarcomas (27,28). En la presente serie de 23 pacientes no se presentaron complicaciones agudas severas; las complicaciones crónicas incluyeron en un paciente dehiscencia de la herida operatoria e infección local, y en otra paciente pediátrica con lesión del antebrazo tratada con resección parcial + BT y RT externa con electrones fibrosis y limitación funcional parcial del antebrazo, y otra paciente con lesión en la pared abdominal sometida a re-irradiación con BT después de cirugía de rescate por recidiva pos cirugía y RT externa presentó radio necrosis de la pared abdominal ameritando cirugía reconstructiva
Referencias
1. Enzinger FM, Shiraki M. Muscle aponeurotic fibromatosis of the shoulder girdle (extra-abdominal desmoids). Analysis of 30 cases followed up for 10 or more years. Cancer. 1967;20:1131-1140.
2. Goy BW, Lee SP, Eilber F, Dorey F, Eckardt J, Fu YS, et al. The role of adjuvant radiotherapy in the treatment of resectable desmoid tumors. Int J Radiat Oncol Biol Phys. 1997;39:659-665.
3. Karakousis Cp, Mayordomo J. Zografos GC, Driscoll DL. Desmoid tumors of the trunk and extremity. Cancer.1993;72:1637-1641.
4. Enzinger FM, Weiss SW. Soft tissue tumors. St. Louis: Mosby-Year Book Inc; 1995.
5. Reitamo JJ, Häyry P, Nykyri E, Saxén E. The desmoid tumor. I. Incidence, sex-, age- and anatomical distribution in the Finnish population. Am J Clin Pathol. 1982;77:665-673.
6. Reitamo JJ, Scheinin TM, Hayry P. The desmoid syndrome. New aspects in the cause, pathogenesis and treatment of the desmoid tumor. Am J Surg. 1986;12:230-237.
7. Faulkner LB, Hajdu SI, Kher U, La Quaglia M, Exelby PR, Heller G, et al. Pediatric desmoid tumor: Retrospective analysis of 63 cases. J Clin Oncol. 1995;13:2813-2818.
8. Hoffmann W, Weidmann B, Schmidberger H, Niederle N, Seeber S, Bamberg M. The clinical picture and therapy of aggressive fibromatosis (desmoids). Strahlenther Onkol. 1993;169:235-241.
9. Urdaneta N, Ruan L. Radioterapia en el tratamiento de las enfermedades benignas. En: Urdaneta N, Vera A, Peschel RE, Wilson LD (editores) Radioterapia oncológica enfoque multidisciplinario. 2a edición. Caracas: Disinlimed; 2009.p.789.
10. Kirschner MJ, Sauer R. The role of radiotherapy in the treatment of desmoid tumors. Strahlenther Onkol.1993;169:77-82.
11. Escobar C, Munker R, Thomas JO, Li BD, Burton GV. Update on desmoid tumors. Ann Oncol. 2012; 23:562-569.
12. Lucas DR, Shroyer KR, McCarthy PJ, Markham NE, Fujita M, Enomoto TE. Desmoid tumor is a clonal cellular proliferation: PCR amplification of HUMARA for analysis of patterns of X-chromosome inactivation. Am J Surg Pathol. 1997;21:306-311.
13. Ravi V, Patel S, Raut CH, DeLaney T. Desmoid tumors: Epidemiology, risk factors, molecular pathogenesis, clinical presentation, diagnosis, and local therapy.URL: Disponible en: http://www.uptodate.com/contents/desmoid-tumors-epidemiology-risk-factors-molecular-pathogenesis-clinical-presentation-diagnosis-and-local therapy?source=search_result&search=desmoid+tumor&selectedTitle=1~34
14. Micke O, Eich H, Bruns T. Aggressive fibromatosis/desmoid tumors. En: Seegenschmiedt M, Makoski H, Trott K, Brady LW, editores. Radiotherapy for non-malignant disordes. Berlin: Springer;2008.
15. Church JM. Mucosal ischemia caused by desmoid tumors in patients with familial adenomatous polyposis: Report of four cases. Dis Colon Rectum. 1998;41:661-663.
16. Sagar PM, Möslein G, Dozois RR. Management of desmoid tumors in patients after ileal pouch-anal anastomosis for familial adenomatous polyposis. Dis Colon Rectum. 1998;41:1350-1355.
17. Penna C, Tiret E, Parc R, Sfairi A, Kartheuser A, Hannoun L, et al. Operation and abdominal desmoid tumors in familial adenomatous polyposis. Surg Gynecol Obstet. 1993;177:263-268.
18. Melis M, Zager JS, Sondak VK. Multimodality of desmoid tumors: How important is a negative surgical margin ?. J Surg Oncol. 2008;98:594-602
19. Ergen S, Tiken E, Öksüz D, Dinçbaş F, Dervişoğlu, Mandel N. The role of radiotherapy in the treatment of primary or recurrent desmoid tumors and long-term results. Balkan Med J. 2016;33(3): 316-321.
20. Spear MA, Jennings LC, Mankin HJ, Gebhardt MC Springfield DS, Gebhardt MC, et al. Individualizing management of aggressive fibromatoses. Int J Radiat Oncol Biol Phys. 1998;40:637-645.
21. Arvanitis ML, Jagelman DG, Fazio VW, Lavery IC, McGannon E. Mortality in patients with familial adenomatous polyposis. Dis Colon Rectum. 1990;33:639-642.
22. Matthews DE, Farewell VT. Using and understanding medical statistics. 4a edición. Suiza: Karger AG;2007.
23. Melis M, Zager JS, Sondak VK. Multimodality management of desmoid tumors: How important is a negative surgical margin? J Surg Oncol. 2008;98:594-602.
24. Salas S, Dufresne A, Bui B, Blay JY, Terrier P, Ranchere-Vince D, et al. Prognostic factors influencing progression-free survival determined from a series of sporadic desmoid tumors: A wait-and-see policy according to tumor presentation. J Clin Oncol. 2011;29:3553-3558.
25. Gronchi A, Casali P, Mariani L, Lo Vullo S, Colecchia M, Lozza L, et al. Quality of surgery and outcome in extra-abdominal aggressive fibromatosis: A series of patients surgically treated at a single institution. J Clin Oncol. 2003;21:1390-1397.
26. Crago AM, Denton Bm Salas S, , Dufresne A, Mezhir JJ, Hameed M, et al. A prognostic normogram for prediction or recurrence in desmoid fibromatosis. Ann Surg. 2013;258:347-353
27. Kriz J, Eich Hans, Haverkamp U, Seegenschmiedt MH, Heide J, Bruns F, et al. Radiotherapy is effective for desmoid tumors (Aggressive fibromatosis)-long-term results of a German Multicenter Study. Oncol Res Treat 2014;37:255-260.
28. Nuyttens JJ, Rust PF, Thomas CR Jr, Turrisi AT 3rd. Surgery versus radiation therapy for patients with aggressive fibromatosis or desmoid tumors: A comparative review of 22 articles. Cancer. 2000;88(7):1517-23.
29. Leibel SA, Wara WM, Hill DR, Bovill EG Jr, de Lorimier AA, Beckstead JH, et al. Desmoid tumors local control and patterns of relapse following radiation therapy. Int J Radiat Oncol Biol Phys. 1983;9:1167-1171.
30. Park HC, Pyo HR, Shin K, Suh CO. Radiation treatment for aggressive fibromatosis: Findings from observed patterns of local failure. Oncology. 2003;64:346-352
31. Acker JC, Bossen EH, Halperin EC. The management of desmoid tumors. Int J Radiat Oncol Biol Phys. 1993;26:851-858.
32. Ballo MT, Zagars GK, Pollack A. Radiation therapy in the management of desmoid tumors. Int J Radiat Oncol Biol Phys. 1998;42:1007-1014.
33. Santti K, Beule A, Tuomikoski L, Rönty M, Jääskeläinen AS, Saarilahti K, et al. Radiotherapy in desmoid tumors : Treatment response, local control, and analysis of local failures. Strahlenther Onkol. 2017;193(4):269-275.
34. Keus R, Nout R, Blay J, de Jong JM, Hennig I, Saran F, et al. Results of a phase II pilot study of moderate dose radiotherapy for inoperable desmoid-type fibromatosis-an EORTC STBSG and ROG study (EORTC 62991-22998). Ann Oncol. 2013;24:2672-2676.
35. Baumert B, Sphar M, Hochstetter A, Beauvois S, Landmann C, Fridrich K, et al. The impact of radiotherapy in the treatment of desmoid tumours. An international survey of 110 patients. A study of the Rare Cancer Network. Radiat Oncol. 2007;2:12.
36. Ballo M, Zagars G, Pollack A, Pisters PW, Pollack RA. Desmoid tumor: Prognostic factors and outcome after surgery, radiation therapy, or combined surgery and radiation therapy. J Clin Oncol. 1999; 7(1):158-167.
37. Jelinek J, Stelzer K, Conrad E, Bruckner J, Kliot M, Koh W, Laramore GE. The efficacy of radiotherapy as postoperative treatment for desmoid tumors. Int J Radiat Oncol Biol Phys. 2001;50(1):121-125.
38. Lev D, Kotilingam D, Wei C, Ballo MT, Zagars GK, Pisters PW, et al. Optimizing treatment of desmoid tumors. J Clin Oncol. 2007;25(13):1785-1791.
39. Liuzzi J, Garriga E, Dacunha M, Tirado E, Siso S, Brito E. Fibromatosis agresiva extra abdominal de cabeza y cuello. Rev Venez Oncol. 2014; 26(3):217-222.
40. Dugarte A, Morante V, Kouris E, Giansante E, Peña G, Merati O, et al. Tumor desmoide en dorso de pie izquierdo reporte de un caso. Dermatol Venez. 2009;47(1,2):38-42.
41. Gómez M, González H, Castellano L, García G, Navas M. Tumor desmoide reporte de un caso. Rev Venez Oncol. 2008;20(1):38-41.
42. De Camargo V, Keohan ML, D’Adamo D, Antonescu CR, Brennan MF, Singer S, et al. Clinical outcomes of systemic therapy for patients with deep fibromatosis (desmoid tumor). Cancer. 2010;116:2258-2265.
43. Janinis J, Patriki M, Vini L, Aravantinos G, Whelan JS. The pharmacological treatment of aggressive fibromatosis: A systematic review. Ann Oncol. 2003;14:181-190.
Notas de autor
Correspondencia: Dr. Carlos Hernández. Av. Intercomunal el Hatillo. Unidad Santa Inés, sótano 2. CMDLT. Tel: 04241330504. E-mail: carlosluismed@gmail.com
