Factores predictivos de la biopsia de ganglio centinela en cáncer de mama. Experiencia Venezolana.
Factores predictivos de la biopsia de ganglio centinela en cáncer de mama. Experiencia Venezolana.
Revista Venezolana de Oncología, vol. 30, núm. 1, pp. 16-23, 2018
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 16 Septiembre 2017
Revisado: 27 Octubre 2017
Aprobación: 22 Diciembre 2017
Resumen: El estado ganglionar axilar es el factor pronóstico más importante en el manejo del cáncer de mama. Actualmente la biopsia de ganglio centinela ha reemplazado el vaciamiento ganglionar axilar en pacientes con cáncer de mama. El tamaño tumoral y otras características histológicas-moleculares del tumor pueden predecir el resultado de biopsia. OBJETIVO: Evaluar la relación entre las características clínico-patológicas del cáncer de mama y resultado de la biopsia de ganglio centinela en las pacientes con cáncer de mama de la consulta de Patología Mamaria del Servicio de Ginecología del Hospital Universitario de Caracas sometidas a tratamiento quirúrgico con indicación de esta biopsia, desde enero 2010 a diciembre de 201. MÉTODO: Estudio retrospectivo, descriptivo, observacional y de corte transversal. RESULTADOS: De 252 pacientes con diagnóstico de cáncer de mama, solo 41 % tuvieron indicación de realización de biopsia de ganglio centinela con edad promedio de 54,8 años. De ellas, el 76 % fue negativo y solo 21 % de los casos resultó positivo. Un caso fue reportado diferido y otro no fue posible identificarlo. Se demostró según prueba de hipótesis que el tamaño tumoral, el tipo y grado histológico, el subtipo molecular se relacionó con el resultado con un nivel de confianza de 95 %. Fue estadísticamente significativo la relación tamaño tumoral y grado histológico con el resultado. CONCLUSIONES: el tamaño tumoral, la histología, el grado histológico y más recientemente, el subtipo molecular, predicen el resultado de la biopsia del ganglio centinela.
Palabras clave: Cáncer, mama, biopsia, ganglio centinela, factor predictivo.
Abstract: The axillary node status is the most important prognostic factor in the management of the breast cancer. Currently the sentinel node biopsy has replaced the axillary lymph node dissection in the breast cancer patients. Tumor size and other histological molecular characteristics of the tumor can predict the outcome of the sentinel node biopsy. OBJECTIVE: To evaluate the relationship between the clinical and the pathological features of the breast cancer and the sentinel node biopsy outcome in the patients with breast cancer at the Breast Pathology Clinic of the Gynecology Department of the University Hospital of Caracas, submitted to surgical treatment with indication of sentinel node biopsy, from January 2010 to December 2015. METHOD: Retrospective, descriptive, observational and cross sectional study. RESULTS: In 252 patients diagnosed with breast cancer, only the 41 % had an indication of the sentinel node biopsy with an average age of 54.8 years old. The result was negative in 76 % and only 21 % of the cases were positive. One case was reported deferred and another could not be identified. We hypothesized that the tumor size, the type and the histological grade, the molecular subtype was related to the result with a confidence level of 95 %. The tumor size and the histological grade were statistically significant with the result. CONCLUSIONS: The tumor size, histology and histologic grade and more recently, the molecular subtype of the tumor, predict the outcome of the sentinel node biopsy.
Keywords: Cancer, breast, sentinel node, biopsy, predictive factor.
INTRODUCCIÓN
El compromiso ganglionar axilar es el factor pronóstico más importante en el manejo del cáncer de mama; su estatus marcará la pauta en el tratamiento. Hasta hace poco la disección ganglionar era el procedimiento estándar para conocer el compromiso de los ganglios linfáticos, por lo tanto era un procedimiento de rutina, no exento de complicaciones, que llevó a la necesidad del desarrollo de procedimientos menos invasivos como lo es la biopsia del ganglio centinela (BGC) con aportes importantes en la estadificación del cáncer de mama (1).
En 2003 Veronesi y col., publican por primera vez resultados sobre BGC, demostrando que no hubo recidivas en pacientes con BGC negativa a quienes se les omitió la disección ganglionar axilar; además tuvieron supervivencia a corto plazo similar al ser comparados con pacientes con ganglios negativos sometidos a disección axilar. De tal manera, que sus resultados fueron de gran aporte para la estadificación ganglionar axilar del cáncer de mama (2). En base a esto, en 2005 la Sociedad Americana de Oncología Clínica (ASCO) publicó por primera vez directrices de práctica clínica basadas en la evidencia sobre el uso de la BGC para pacientes con cáncer de mama en estadio temprano (3).
Basado en el análisis de distintas investigaciones y revisiones sistemáticas, recientemente han sido publicadas recomendaciones en relación al resultado BGC, pudiéndose omitir así la disección ganglionar axilar en mujeres con BGC negativo y en aquellas mujeres con uno o dos ganglios centinela metastásicos que serán sometidas a una cirugía conservadora de la mama con radioterapia completa a la misma. Mientras que en mujeres con metástasis en BGC, que se someterán a mastectomía, se les debe ofrecer disección ganglionar. Pacientes con tumores T3-T4, en caso de carcinoma inflamatorio y en embarazadas, no deberían someterse a BGC (4).
Cada día más surge la necesidad de entender la biología de la metástasis. La identificación de los complejos fenotipos moleculares del tumor y características clínicas, así como factores propios de cada paciente, son datos importantes a tener en consideración como posibles factores pronósticos subyacentes implicados en el desarrollo de la enfermedad metastásica. El objetivo debe ir más allá de la identificación de cada uno de ellos como predictivos del resultado de la BGC, debe abarcar el desarrollo de distintos enfoques específicos para prevenir y tratar las metástasis (5), de tal manera, que la edad, el tamaño del tumor, el tipo y grado histológico, el compromiso ganglionar, la presencia de invasión linfovascular y más recientemente, el comportamiento biológico o tipo molecular del tumor dado por la expresión de receptores de estrógenos (RE), receptores de progesterona (RP) y receptor de factor de crecimiento epidérmico humano (HER2), son los factores pronósticos más conocidos para cáncer de mama (6). De acuerdo con la inmunohistoquímica, los tumores de mama se clasifican desde el punto de vista molecular en: luminal A (RE+ y/o RP+, Ki67↓ y HER2+), luminal B (RE+ y/o RP+, Ki67↑) y estos a su vez según la expresión del HER2 serán luminal B HER2- o luminal B HER2+; los otros dos grupos corresponde al HER2 positivo (RE- , RP- y HER2+) y los triple negativo (RE- , RP- y HER2-) (7,8). De estos, el estado ganglionar es el factor pronóstico más importante.
El objetivo de esta investigación consiste en conocer si las características clínico-patológicas del cáncer de mama predicen de forma independiente la
Objetivos
Objetivo general
Evaluar la relación entre las características clínico-patológicas del cáncer de mama y el resultado de la BGC.
Criterios de inclusión
1. Todas las pacientes con diagnóstico histológico de carcinoma de mama in situ e infiltrante T1 y T2, sin metástasis; estadificados según el sistema de estadificación del American Joint Committee on Cancer (AJCC), a cuya biopsia por trucut se le realizó prueba de inmunohistoquímica, y fueron sometidas a mastectomía total o parcial oncológica más BGC con azul patente, con 99Tc y/o con técnica combinada.
Criterios de exclusión
1. Pacientes sin confirmación histológica para cáncer de mama.
2. Pacientes con contraindicación de BGC.
3. Pacientes con metástasis.
4. Pacientes con tumores T3.
MÉTODO
Se trata de un estudio retrospectivo, observacional y de corte transversal. La población está constituida por todas las pacientes que acudieron la consulta de Patología Mamaria del Servicio de Ginecología del Hospital Universitario de Caracas con diagnóstico de cáncer de mama (252 pacientes), desde enero 2010 a diciembre de 2015.
La muestra estuvo constituida por todas aquellas pacientes de la consulta de Patología Mamaria del Servicio de Ginecología del Hospital Universitario de Caracas con diagnóstico de cáncer de mama, que fueron sometidas a mastectomía o tratamiento preservador de la mama y que cumplieron con los criterios de realización de BGC (105 pacientes), desde enero 2010 a diciembre de 2015.
RESULTADOS
BGC y su relación con las características clínico-patológicas del tumor
Del total de 252 pacientes con diagnóstico de cáncer de mama, solo 41 % (n=105) tuvieron indicación de realización de BGC con una edad promedio de 54,8 años, resultando 76 % (n=80) negativo y apenas 21 % (n=22) positivo. En dos casos no fue posible obtener resultado intraoperatorio de la BGC, reportándose por anatomía patológica como diferida y otro no identificado por parte del equipo quirúrgico cada uno el 1 %, ambas pacientes con diagnóstico histológico de carcinoma ductal infiltrante.
· BGC negativo
Al comparar los resultados de la BGC negativo con el tamaño del tumor, se encontró que el tamaño T= 2 (2 a ≤ 5cm) fue el más común, presentándose en 51 % (n=40) de las paciente, seguido del tamaño tumoral T1 (1 a <2 cm) en 27 % (n=21) de las pacientes el pTO el 21 % y pTX 1 %.
Por otro lado, 69 % (n=54) de este grupo de pacientes (BGC-) fueron diagnosticadas con el tipo histológico ductal infiltrante. El otro tipo histológico frecuente fue el ductal in situ, diagnosticado en 19 % (n=14) de los casos. Los otros tipos histológicos fueron diagnosticados en menos del 5 %. (Figura 1)
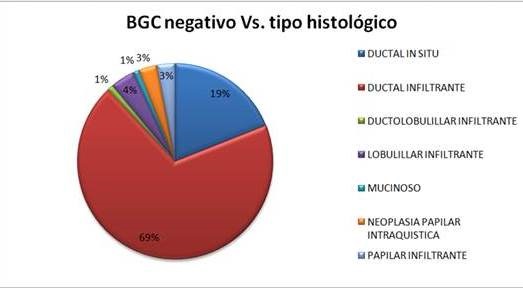
Figura 1.
Resultado negativo de la biopsia de ganglio centinela y su relación con el tipo histológico del tumor.
El 63 % (n=45) de las pacientes con resultado negativo para la BGC eran tumores con grado histológico 2, seguido por el grado 3 con 28 % (n=20) (Figura 2).
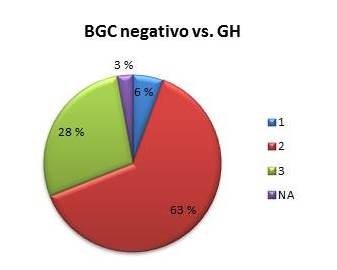
Figura 2.
Resultado negativo de la biopsia de ganglio centinela y su relación con el grado histológico
El tipo molecular donde se registró la mayor cantidad de pacientes, fue el luminal A con 37 % (n=19), seguido por 23 % (n=12) del tipo luminal B (HER2 NEG). (Figura 3)

Figura 3
Resultado de negativo de la biopsia de ganglio centinela y su relación con el tipo molecular del tumor.
· BGC Positivo
En cuanto al tamaño del tumor, donde se reportaron más casos de pacientes con resultado en la BGC positivo fueron los tipos T= 1 (1 a ≤ 2 cm) y T= 2 (2 a ≤ 5 cm), ambos tamaños con 9 pacientes, es decir 82 % de estas 22 pacientes. (Figura 4)
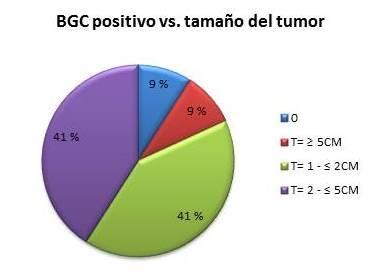
Figura 4
Resultado positivo de la biopsia de ganglio centinela y su relación con el tamaño tumoral.
Al relacionar el tipo histológico de cáncer de mama con este grupo de pacientes, se encontró que el 76 % (n=16) de las pacientes tenían tipo histológico ductal infiltrante, 14 % lobulillar infiltrante, 5 % in situ, y 5 % neoplasia papilar intraquística.
El grado histológico más frecuente fue 2, diagnosticado en el 91 % (n=20) de las pacientes en 9 % grado 3.
Finalmente, el tipo molecular más común entre las pacientes con resultado positivo en la BGC fue luminal B HER2 NEG, diagnosticado en 42 % (n=7) de las pacientes, seguido de luminal B HER2 POS diagnosticado en 35 % (n=6) de los casos. (Figura 5)
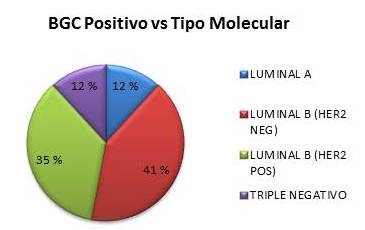
Figura 5.
Resultado de positivo de la biopsia de ganglio centinela y su relación con el tipo molecular del tumor.
Con la finalidad de determinar si existe una relación entre los resultados de la BGC y el tamaño del tumor, el tipo histológico, el grado nuclear y el tipo molecular, se realizaron pruebas de hipótesis de tipo Chi-Cuadrado, mediante tablas de contingencia.
Con la finalidad de determinar si existe una relación entre los resultados de la BGC y el tamaño del tumor, el tipo histológico, el grado nuclear y el tipo molecular, se realizaron pruebas de hipótesis de tipo Chi-Cuadrado, mediante tablas de contingencia.
Una tabla de contingencia cuenta las observaciones por múltiples variables. Las filas y columnas de las tablas corresponden a estas variables observadas. Estas tablas la mayoría de las veces, son utilizadas en la búsqueda de un patrón que indique la relación, (o la falta de ella), entre las variables estudiadas.
Las pruebas de hipótesis se realizaron a un nivel de confianza del 95 %, es decir que se aceptaran o rechazaran las hipótesis nulas (supuesto que queremos se corroborara en la investigación) con un 95 % de confianza o certeza. Cada hipótesis nula tiene asociada una hipótesis llamada: hipótesis alternativa.
Cada prueba tiene asociada una probabilidad conocida como P-valor con la cual se puede determinar si se acepta o se rechaza la hipótesis nula. Ahora bien, en general con un nivel de confianza del 95 % se tiene que:
· Si el P-valor es mayor que 0,05 se acepta la hipótesis nula.
· Si el P-valor es menor que 0,05 se rechaza la hipótesis nula (se acepta la hipótesis alternativa).
Hipótesis planteadas
1. Hipótesis para la prueba asociada estudiar la posible relación entre los resultados de la BGC y el tamaño final:
· H0 (hipótesis nula): El tamaño del tumor es independiente del resultado de la BGC.
· HA (hipótesis alternativa): El tamaño del tumor depende del resultado de la BGC.
El resultado para esta prueba fue el siguiente: el P-valor asociado a esta prueba es P= 0 Como el valor de P= 0 es menor que 0,05 rechazamos la hipótesis nula, es decir, aceptamos la hipótesis alternativa que nos dice que el tamaño del tumor tiene relación con los resultados de la BGC.
2. Hipótesis para la prueba asociada: estudiar la posible relación entre los resultados de la BGC y el tipo histológico:
· H0 (hipótesis nula): el resultado del tipo histológico es independiente del resultado de la BGC.
· HA (hipótesis alternativa): el resultado del tipo histológico está relacionado con el resultado de la BGC.
El resultado para esta prueba fue el siguiente: el P-valor asociado a esta prueba es P= 0. Como el P-valor P= 0 es menor que 0,05 rechazamos la hipótesis nula, es decir, aceptamos la hipótesis alternativa que nos dice que el tipo histológico tiene relación con los resultados de la BGC.
3. Hipótesis para la prueba asociada: estudiar la posible relación entre los resultados de la BGC y el grado nuclear:
· H0 (hipótesis nula): el grado histológico es independiente del resultado de la BGC.
· HA (hipótesis alternativa): el grado histológico depende del resultado de la BGC.
El resultado para esta prueba fue el siguiente: el P-valor asociado a esta prueba es P= 0 Como el valor de P= 0 es menor que 0,05 rechazamos la hipótesis nula, es decir, aceptamos la hipótesis alternativa que nos dice que el grado nuclear está vinculado con el resultado de la BGC.
4. Hipótesis para la prueba asociada: estudiar la posible relación entre los resultados de la BGC y el tipo molecular:
· H0 (hipótesis nula): el tipo molecular es independiente del resultado de la BGC.
· HA (hipótesis alternativa): el tipo molecular depende del resultado de la BGC.
El resultado para esta prueba fue el siguiente: el P-valor asociado a esta prueba es P =0, como el valor de P= 0 es menor que 0;05 rechazamos la hipótesis nula, es decir, aceptamos la hipótesis alternativa que nos dice que el tipo molecular está vinculado con el resultado de la BGC.
Por otro lado, se estudió la significancia estadística con la posible relación entre los resultados de la BGC y el tamaño tumoral; el resultado para esta prueba fue estadísticamente significativo (P= 0,0000000427); interpretándose que el tamaño del tumor tiene relación con los resultados de la biopsia. De igual manera se determinó la posible relación entre los resultados de la BGC y el diagnóstico histopatológico; no obteniéndose significancia estadística (P= 0,9973579), concluyéndose que el tipo histológico no está vinculado con el resultado de la BGC. Al estudiar la posible relación entre los resultados de la BGC y el grado histológico; se obtuvo el valor de P= 3,8 x 10-15. Como el valor de P= 3,8 x1 0-15 es menor que 0,05 rechazamos la hipótesis nula planteada inicialmente, es decir, aceptamos la hipótesis alternativa que nos dice que el grado histológico está vinculado con el resultado de la BGC.
DISCUSIÓN
El diámetro máximo del componente invasivo del tumor primario se ha correlacionado con la afectación de los ganglios linfáticos axilares, sin embargo, para algunos investigadores es una relación poco confiable; tumores de tamaño <10 mm y <20 mm, en el 15 % y el 25 % de los casos, respectivamente, han resultado con ganglios linfáticos axilares positivos (9,10). Asimismo, la correlación entre el grado tumoral y la afectación de los ganglios linfáticos axilares está bien reconocida (11). El sistema modificado de Bloom y Richardson incluye una medida de proliferación celular, pleomorfismo y diferenciación tisular (12). De estos tres parámetros importantes, la magnitud de la mitosis de las células tumorales o el índice Ki67 (que se correlaciona con la fracción de fase S y el índice mitótico) es un indicador pronóstico independiente y se correlaciona con la metástasis de los ganglios linfáticos (13). El tipo de tumor histológico también se ha correlacionado con la afectación de los ganglios linfáticos axilares con tipos de tumor favorables, incluyendo tubulares, mucinosos, medulares y carcinomas cribriformes (14, 15). En relación al subtipo molecular y la afectación los ganglios linfáticos, los resultados son inconsistentes (16).
Al relacionar el grupo de BGC negativo con el tamaño del tumor, se encontró que en 51 % de los casos predominó el tamaño T= 2 y en el 69 % fueron tipo histológico ductal infiltrante. En cuanto al grado histológico, el más común fue 2, el cual fue diagnosticado en el 63 % (n=45) de las pacientes. El tipo molecular donde se registró la mayor cantidad de pacientes, con un 37 % (n=19) fue luminal A. Estos resultados fueron comparados con los estudios de Peinado y col., en Granada en 2011, y Ángel y col., en Colombia cuyos resultados se corresponden con nuestra muestra obteniendo tamaño tumoral < 5 cm, subtipo molecular luminal A, tipo histológico ductal infiltrante; el grado histológico 2 (17,18). Asimismo, Helio y col., demostraron en su investigación que fueron tumores grado histológico 2 y subtipo molecular luminal A los que se asociaron con mayor frecuencia a la negatividad del ganglio centinela (19).
En cuanto al grupo de BGC positivo al relacionarlo con el tamaño del tumor, este resultado fue más frecuente en los tumores T= 1 - ≤ 2 cm y T= 2 - ≤ 5 cm, ambos tamaños con 9 pacientes, es decir 82 % de estas 22 pacientes. Asimismo, el 76 % (n=16) de las pacientes tenían tipo histológico ductal infiltrante con grado histológico 2, en el 91 % (n=20) de las pacientes; predominando en el subtipo molecular luminal B (HER2 NEG), en 42 % (n=7) de las pacientes. Ángel y col., obtuvieron resultados similares en su investigación, al igual que Zénola y col (18,20). Por otro lado, López T y col., no encontraron relación entre el subtipo molecular de cáncer de mama y el resultado de BGC en una población venezolana (21).
La BGC es un predictor del estado ganglionar axilar en pacientes con cáncer de mama, actualmente ha reemplazado la disección ganglionar axilar en la estadificación del cáncer de mama con ventajas sustentables en distintas investigaciones científicas. Son consistentes los resultados de numerosas investigaciones que reportan la manera en que el tamaño tumoral predice el resultado de la BGC, mientras que otras características histopatológicas como el tipo y grado histológico, presencia de invasión linfovascular y más recientemente el subtipo molecular para algunos autores son inconsistentes o podrían estar presente de forma complementaria al primer factor de riesgo, el tamaño tumoral. En nuestra investigación se pudo demostrar que en la población estudiada el tamaño tumoral, el tipo y grado histológico, y subtipo molecular se relacionaron con el estado ganglionar axilar a través de la prueba de hipótesis Chi-cuadrado, con un nivel de confianza de 95 %. Además, fue significativamente estadístico la relación tamaño tumoral y grado histológico con el resultado de BGC.
Referencias
1. Canavese G, Catturich A, Vecchio C, Tomei D, Gipponi M, Villa G, et al. Sentinel node biopsy compared with complete axillary dissection for staging early breast cancer with clinically negative lymph nodes: Results of randomized trial. Ann Oncol. 2009; 20:1001-1007.
2. Veronesi U, Paganelli G, Viale G, Luini A, Zurrida S, Galimberti V, et al. A randomized comparison of sentinel-node biopsy with routine axillary dissection in breast cancer. N Engl J Med. 2003;349:546-553.
3. [No author´s list]. ASCO Guideline Recommendations for sentinel lymph node biopsy in early-stage breast cancer: Guideline summary. J Oncol Pract. 2005;(4):134-136.
4. Lyman GH, Temin S, Edge SB, Newman LA, Turner RR, Weaver DL, et al. Sentinel lymph node biopsy for patients with early-stage breast cancer: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol. 2014;32:1365-1383.
5. Kimbung S, Loman N, Hedenfalk I. Clinical and molecular complexity of breast cancer metastases. Semin Cancer Biol. 2015;35:85-95
6. Early Breast Cancer Trialists' Collaborative Group. Polichemotherapy for early breast cancer: An overview of the randomized trials. Lancet. 1998;352:930-942.
7. Voduc KD, Cheang M, Tyldesley S, Gelmon K, Nielsen T, Kennecke H. Breast cancer subtypes and the risk of local and regional relapse. J Clinl Oncol. 2010;28(10):1684-1691.
8. Goldhirsch A, Wood WC, Coates AS, Gelber RD, Thurlimann B, Senn HJ, et al.. Strategies for subtypes dealing with the diversity of breast cancer: Highlights of the St. Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2011. Ann Oncol 2011: 22(8):1736-1747.
9. Carter CL, Allen C, Henson DE. Relation of tumor size, lymph node status, and survival in 24,740 breast cancer cases. Cancer 1989;63:181-187.
10. Ahlgren J, Stal O, Westman G, Arnesson LG. Prediction of axillary lymph node metastases in a screened breast cancer population. South-East Sweden Breast Cancer Group. Acta Oncol 1994;33:603-608.
11. Elston CW, Ellis IO. Pathological prognostic factors in breast cancer. I. The value of histological grade in breast cancer: Experience from a large study with long-term follow-up. Histopathology. 1991;19(5):403-410.
12. Van Diest PJ, van der WE, Baak JP. Prognostic value of proliferation in invasive breast cancer: A review. J Clin Pathol. 2004;57:675-681
13. Orucevic A, Reddy VB, Bloom KJ, Bitterman P, Magi-Galluzzi C, Oleske DM, et al. Predictors of lymph node metastasis in T1 breast carcinoma, stratified by patient age. Breast J. 2002;8(6):349-355.
14. Hasebe T, Sasaki S, Imoto S, Ochiai A. Proliferative activity of intratumoral fibroblasts is closely correlated with lymph node and distant organ metastases of invasive ductal carcinoma of the breast. Am J Pathol. 2000;156:1701-1710.
15. Viale G, Zurrida S, Maiorano E, Mazzarol G, Pruneri G, Paganelli G, et al. Predicting the status of axillary sentinel lymph nodes in 4 351 patients with invasive breast carcinoma treated in a single institution. Cancer. 2005;103(3):492-500.
16. Chua B, Ung O, Taylor R, Boyages J. Frequency and predictors of axillary lymph node metastases in invasive breast cancer. ANZ J Surg. 2001;71:723-728.
17. Peinado, M. Validación de la técnica de detección intraoperatoria y biopsia selectiva del ganglio centinela en pacientes con cáncer de mama operable tratadas con quimioterapia neoadyuvante. Granada, España: Editorial de la Universidad de Granada;2011.
18. Angel G, Salas P, Borrero M, Madrid J, Herazo F, Ossa C, et al. Ganglio centinela en cáncer temprano de mama. Experiencia Instituto de Cancerología Clínica Las Américas Medellín Colombia 2004-2012. Instituto de Cancerología Medellín. Disponible en: URL: http://www.idclasamericas.co/Documentos/Investigacion/Reconocimientos/Ganglio_Centinela.pdf
19. de Oliveira Filho HR, Dória MT, Piato JR, Soares Junior JM, Filassi JR, Baracat EC, et al. Criteria for prediction of metastatic axillary lymph nodes in early-stage breast cancer. Rev Bras Ginecol Obstet. 2015; 37(7):308-313.
20. Zénzola V, Bolívar E, Betancourt L, Salas J, Jiménez R, Guerra M, et al. Factores clínico-patológicos en cáncer de mama relación con metástasis en ganglios no centinelas axilares cuando el centinela es positivo. Rev Venez Oncol. 2011;23(3):134-144.
21. López M, Pesci Feltri A, García IF, Guida V, Fernándes A, Blanch R. Relación entre el tipo molecular de cáncer de mama y el resultado de la biopsia de ganglio centinela. Rev Venez Oncol. 2017;29(1):32-37.
Notas de autor
Correspondencia: Dr. Marcos López T. Servicio de Ginecología, Hospital Universitario de Caracas. E-mail: marcolop82@gmail.com