PRECISIÓN DE LA BIOPSIA ENDOMETRIAL Y RESONANCIA MAGNÉTICA PARA PREDECIR CÁNCER ENDOMETRIAL DE ALTO RIESGO
PRECISIÓN DE LA BIOPSIA ENDOMETRIAL Y RESONANCIA MAGNÉTICA PARA PREDECIR CÁNCER ENDOMETRIAL DE ALTO RIESGO
Revista Venezolana de Oncología, vol. 30, núm. 4, pp. 228-235, 2018
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 20 Marzo 2018
Revisado: 14 Julio 2018
Aprobación: 12 Agosto 2018
Resumen: La estratificación de riesgo a través de evaluación preoperatoria en cáncer endometrial, ha sido un tema de debate. OBJETIVO: Evaluar rendimiento de la resonancia magnética e histología preoperatoria, en la predicción del riesgo de invasión ganglionar. MÉTODO: Se realizó revisión de historias clínicas de pacientes que presentaron cáncer de endometrio en el período 2002-2015, que recibieron tratamiento inicial quirúrgico convencional, con linfadenectomía. 43 pacientes cumplieron criterios de inclusión, el promedio de edad fue 58 años. RESULTADOS: El 50 % de las pacientes se encontraban en estadio IA. La efectividad de la resonancia magnética nuclear para la infiltración del miometrio presentó una sensibilidad de 13,2% y especificidad de 100 %. El grado de diferenciación presentó buena concordancia (0,724). La frecuencia más alta fue registrada en grupo de bajo riesgo 32 pacientes (74,4 %). El grupo de bajo riesgo presentó 6,2 % de ganglios positivos, mientras que grupo de alto riesgo tuvo 33,3 % de ganglios positivos. DISCUSIÓN: La biopsia preoperatoria permite predecir de manera precisa los tumores tipo 2 y predicción de tipos histológicos poco diferenciados es alta. La resonancia presenta una pobre correlación con los estadios FIGO mayores al IA. Al combinar los grupos de riesgo basándose en la resonancia más la biopsia, se observa alta especificidad y VPN, lo que permite identificar los pacientes con bajo riesgo.
Palabras clave: Cáncer, endometrio, resonancia magnética, biopsia endometrial.
Abstract: The risk of the stratification through the preoperative evaluation in the endometrial cancer has been a subject of debate. OBJECTIVE: The aim of this study was to evaluate the performance of the preoperative nuclear magnetic resonance and the histology in predicting the risk of lymph node invasion. METHOD: We review the medical records of the patients who had endometrial cancer in the period 2002-2015 was performed, which received conventional surgical of initial treatment with the addition of the lymphadenectomy. RESULTS: 43 patients met the inclusion criteria; the average age was 58 years old. The 50 % of patients were in stage IA disease. The effectiveness of the nuclear magnetic resonance for infiltration of the myometrium had a sensitivity of 13.2 % and a specificity of 100 %. The degree of differentiation showed good agreement (0.724). The highest rate was recorded in the low risk group with 32 patients (74.4 %). The low risk group showed 6.2 % of positive nodes, while the high risk group had 33.3 % of positive nodes. DISCUSION: The preoperative biopsy can accurately predict type 2 tumors and poorly differentiated histologic the resonance has a poor correlation with higher FIGO IA. By combining the risk groups based on biopsy and resonance, high specificity and NPV is observed, which helps identify the low risk patients.
Keywords: Endometrial cancer, magnetic resonance, endometrial biopsy.
INTRODUCCIÓN
El cáncer de endometrio es la malignidad ginecológica más frecuente en los países desarrollados y es la segunda más común en los países en desarrollo (1). La mayoría son diagnosticados en estadios tempranos, lo que resulta en altas tasas de supervivencia después del tratamiento quirúrgico. La terapia quirúrgica estándar para el cáncer de endometrio incluye la histerectomía y salpingooforectomía bilateral (2). La linfadenectomía pélvica y para-aórtica se recomienda para pacientes con riesgo de diseminación linfática; sin embargo, esto varía entre los médicos e instituciones (3).
La estratificación de riesgo a través de la evaluación preoperatoria e intra-operatoria en cáncer endometrial, ha sido un tema de debate entre los expertos desde hace muchas décadas. El concepto de grupos de riesgo se introdujo a partir del año 2000 (4,5) para estimar el riesgo de invasión ganglionar y, a más largo plazo, la recurrencia, de la enfermedad en estadio temprano. En el estudio realizado por Bendifallah y col., (4) analizaron la utilidad de diferentes grupos de estratificación de riesgo modelos y concluyeron que ninguno de los estos era ideal para la predicción de la recurrencia y de invasión a los ganglios linfáticos.
La evaluación preoperatoria recomendado por el Instituto Nacional del Cáncer Francés, incluye resonancia magnética y examen histológico de una muestra endometrial (6). Los tres grupos de riesgo: bajo, el estadio IA, grado 1 o 2, variante histológica de tipo 1; intermedio el estadio IA, grado 3 y estadio IB, de grado 1 o 2, histológico de tipo 1; alto riesgo, IB estadio, grado 3 y, por extensión, fase II ≥, histológico tipo 1, así como todos los tipo 2, tumores de cualquier etapa y los tumores de cualquier tipo o etapa con invasión linfovascular, según las directrices francesas (6).
El objetivo de este estudio fue evaluar el rendimiento de la resonancia magnética y la histología preoperatoria, en la predicción del riesgo de invasión ganglionar y la recurrencia.
MÉTODO
Se realizó revisión de las historias clínicas de pacientes que presentaron cáncer de endometrio en el período 2002-2015, que recibieron tratamiento inicial quirúrgico convencional, con linfadenectomía. Se realizó un estudio retrospectivo, descriptivo y comparativo, para evaluar la precisión de la biopsia preoperatoria junto a la resonancia magnética, para predecir enfermedad ganglionar según la estratificación de riesgo. La recolección de datos, se realizó en Cuadros computarizados, luego se procedió al análisis estadístico de los datos. El procesamiento de datos se elaboró mediante el programa SPSS Statistics v 22.0.0.
RESULTADOS
Se revisaron un total de 155 historias, en 56 casos se realizó resonancia magnética como estudio de diagnóstico, 14 de ellas no se les realizó cirugía, por lo tanto 43 pacientes cumplieron los criterios de inclusión, el promedio de edad fue 58 años, promedio de edad de menopausia 46,66 años, 38 pacientes de estas fueron posmenopáusicas. El IMC en promedio fue de 31,42 kg/m2.
LA Figura 1, muestra el porcentaje de pacientes según el estadio clínico al momento del diagnóstico, el 50 % de las pacientes se encontraban en estadio IA de la enfermedad.
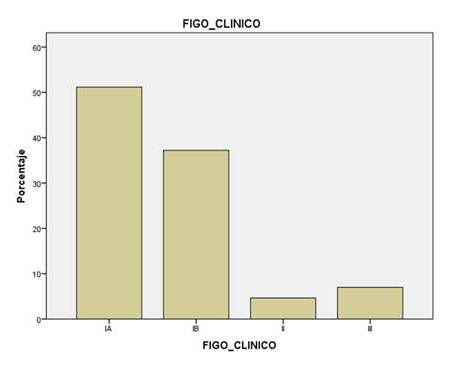
Figura 1
Porcentaje de pacientes según el estadio clínico al momento del diagnóstico.
En cuanto a la biopsia preoperatoria y su relación con la biopsia definitiva, se observa mediante el cálculo por el modelo de Kappa, mínima concordancia (0,222) (Cuadro 1). En relación al diagnóstico del tipo de cáncer endometrial se observó sensibilidad de 100 % para tipo 1 y tipo 2, en cuanto a la especificidad mostró un valor de 50 % en relación al tipo 1, sin embargo, el valor de especificidad para tipo 2 fue del 100 %. (Cuadro 2)
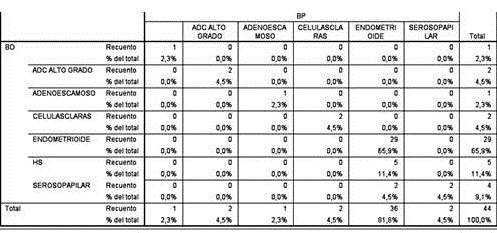
Cuadro 1.
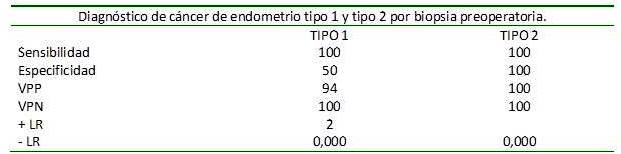
Cuadro 2
En el Cuadro 3 se observa la estimación del riesgo, evidenciándose la efectividad de la resonancia magnética nuclear para determinar la infiltración del miometrio, confirmado por la biopsia definitiva, que proporciona los datos de sensibilidad: 13,2 %, especificidad: 100 %.
El grado de diferenciación (Cuadro 4), presentó una buena concordancia 0,724 según el modelo de Kappa.

Cuadro 3.
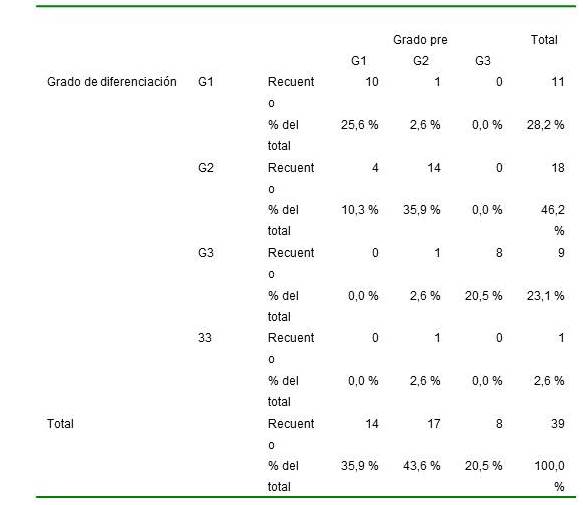
Cuadro 4.
La estratificación de las pacientes se realizó por grupos de riesgo (Cuadro 5), para enfermedad ganglionar según Instituto Nacional de Cáncer Francés, clasificándose en: bajo riesgo, riesgo intermedio y alto riesgo. La frecuencia más alta fue registrada en bajo riesgo con 32 pacientes (74,4 %).
De acuerdo a la positividad de ganglios y su relación con los grupos de riesgo (Cuadro 5), el grupo de bajo riesgo presentó 6,2 % de ganglios positivos, mientras que el grupo de alto riesgo tuvo 33,3 % de ganglios positivos. El riesgo intermedio 0 % de ganglios positivos.
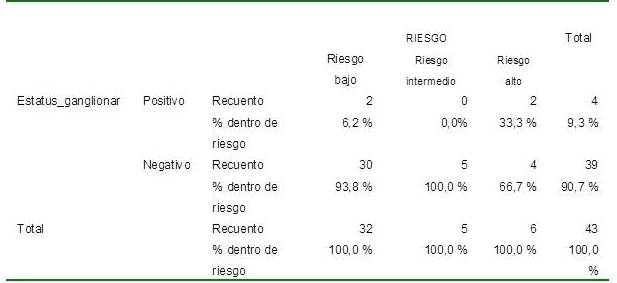
Cuadro 5.
La precisión del diagnóstico por biopsia preoperatoria para los grupos de riesgo intermedio y alto en relación a la detección de tumores tipo 2 y tumores con grado de diferenciación 3 tuvo sensibilidad 100 % para los tumores tipo 2 y 80 % para los G3, con especificidad de 100 % en ambos casos, en el caso de la resonancia la capacidad de predecir estadios tumorales superiores al IA, se observó una sensibilidad baja del 6 % con especificidad del 100 % con VPP del 100 % y VPN de 59 % (Cuadro 6).
Al combinar la resonancia con la histología preoperatoria, para la estratificación de riesgo, para predecir metástasis ganglionar, se obtuvo una sensibilidad de 50 % para grupo de alto riesgo y 50 % para grupo riesgo alto/intermedio. La especificidad fue mayor para predecir grupo alto riesgo (90 %) en comparación a grupos que incluyan riesgo alto e intermedio (especificidad: 77 %). El VPP para predecir grupo de alto riesgo fue de 33 %, y el VPN fue de 95 %, mientras que para el grupo de riesgo alto/intermedio fue de 18 % para el VPP y 94 % para VPN (Cuadro 6).
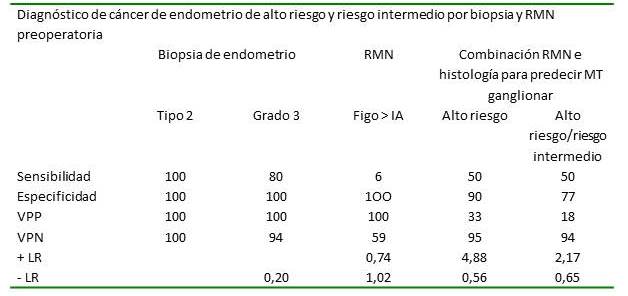
Cuadro 6
DISCUSIÓN
En los pacientes con cáncer de endometrio en estadios tempranos, con bajo riesgo de metástasis a ganglios linfáticos, el beneficio de la linfadenectomía se ha visto reducido (7,8,9). La identificación preoperatoria, emerge como una clave para el manejo quirúrgico adecuado de estas pacientes (10).
El tratamiento quirúrgico estándar es un histerectomía total extra-fascial más salpingooforectomía bilateral, mientras que la disección linfática pélvica y para aortica es recomendada como procedimiento para estadificar (11).
Dos estudios aleatorizados europeos, el ASTEC y el de Benedetti P y col., han sugerido, que no hay beneficio en la sobrevida con la linfadenectomía pélvica de rutina, en cáncer endometrial en estadio temprano con bajo riesgo de enfermedad ganglionar metastásica (7,8).
La identificación preoperatoria de los pacientes con bajo riesgo de enfermedad ganglionar, es un punto importante de escrutinio, y varios modelos han sido diseñados en base a parámetros quirúrgicos, así como la muestra endometrial, marcadores tumorales y datos obtenidos por estudios de imagen (10,12,13,14).
En general, estos estudios son evaluados desde el punto de vista de su utilidad clínica con puntos de corte de tasas de falsos negativos menores de 2 %, cuando al prevalencia de metástasis ganglionar es asumida como 10 % (10).
Los niveles de concordancia entre el grado preoperatorio y el grado posoperatorio, son bajos como ha sido reportado en estudios previos. Sin embargo, se han evidenciado altos niveles de valor predictivo positivo, en particular para el diagnóstico preoperatorio de grado de diferenciación 1 (aproximadamente 85 %), lo cual podría permitir estimar los especímenes posquirúrgicos de bajo riesgo, especialmente si se toma en cuenta con otros parámetros (15). Este trabajo demostró buena concordancia para los tres grados de diferenciación.
La recomendación del manejo quirúrgico omitiendo la linfadenectomía pélvica en los pacientes con tumores IA G1, se basa en la baja tasa de metástasis ganglionar, indicando la linfadenectomía pélvica en pacientes de riesgo intermedio de metástasis ganglionar, y limitando la linfadenectomía sistémica (pélvica y para-aortica) para tumores IB G3 o pacientes con histologías desfavorables (15). Los niveles de metástasis ganglionar observada para el grupo de bajo riesgo en este trabajo fueron del 6,2 %.
La mayoría de los investigadores coinciden, que la enfermedad confinada al útero, grado 1-2, subtipos endometroide sin invasión miometrial, permite clasificar los casos de bajo riesgo, mientras que el tamaño tumoral no se usa generalmente en la estratificación de riesgo. Existen estudios que evalúan la utilidad del tamaño tumoral en la estratificación de riesgo. El tamaño tumoral discrimina exitosamente entre pacientes de bajo riesgo y riesgo intermedio de enfermedad metastásica, en casos con tamaño tumoral menor de 2 cm (16,17).
Cuando hay enfermedad macroscópica extrauterina presente, con tamaño tumoral de 2 cm o menos, con FIGO grado 1 o 2, histología endometroide o mixta y/o hiperplasia atípica, el riesgo de enfermedad ganglionar positiva o recurrencia ganglionar es inferior al 1 % y la tasa de supervivencia libre de recurrencia a los 3 años es de 98,7 %, con sólo el 16 % y el 2 % de las pacientes con linfadenectomía y tratamiento adyuvante (braquiterapia y/o quimioterapia) respectivamente (18).
La combinación de biopsia preoperatoria con el diámetro tumoral, permite lograr una precisión considerablemente alta, para predecir diseminación linfática. Solo el 6 % de las pacientes presentan variación en el diagnóstico posoperatorio y en la estratificación de riesgo, cuando se usa biopsia preoperatoria y el tamaño tumoral de forma combinada (18).
El propósito de usar criterios patológicos pre e intra-operatorios en conjunto con variables clínicas y radiológicas, puede aumentar la precisión de la estatificación de riesgo en cáncer endometrial. La resonancia magnética ha sido usada en la evaluación preoperatoria de las pacientes con cáncer endometrial con sensibilidad cerca del 9 % para la detección de invasión miometrial (19,20). Se obtuvo para este trabajo sensibilidad de 13,2 % con especificidad de 100 %.
Estudios previos han concluido que la resonancia magnética nuclear, subestima el estadio de cáncer endometrial en 20 % de los casos, y que la muestra endometrial subestima el tipo y grado en 4 % y 9 % de los casos respectivamente. El grupo de riesgo para invasión ganglionar fue subestimado en 31,9 % de las pacientes, permitiendo que en un 30,7 % de las pacientes con cáncer endometrial, se realice una estadificación quirúrgica incompleta o sin realización de linfadenectomía (21).
Varios autores han estudiado la correlación entre la histología preoperatoria y el resultado final. Estos estudios reportan tasas de precisión entre 74 % y 92 %, con diferencias no significativas estadísticamente entre la técnica de toma de muestra (22). Sin embargo, en este trabajo no se observó concordancia entre la biopsia preoperatoria y el diagnóstico histológico final.
Al catalogar las características de riesgo para enfermedad ganglionar metastásica, la biopsia preoperatoria permite predecir de manera precisa los tumores tipo 2, del mismo modo la predicción de tipos histológicos poco diferenciados es alta. Mientras que la resonancia presenta una pobre correlación con los estadios FIGO mayores al IA, es decir infiltración miometrial mayor al 50 %. Al combinar los grupos de riesgo basándose en la resonancia más la biopsia preoperatoria, podemos observar alta especificidad y VPN, que permite identificar los pacientes con bajo riesgo de enfermedad ganglionar.
Este trabajo presenta limitaciones, basadas principalmente por el número significativo de pacientes excluidos por no contar con un registro médico adecuado. Este estudio permitió confirmar hallazgos previos, que sugieren que la muestra endometrial, no es lo suficientemente precisa para predecir el estado patológico final en cáncer endometrial. Del mismo modo la resonancia magnética presenta poca utilidad para precisar el grado de invasión miometrial.
Las pacientes con cáncer endometrial clasificadas como bajo riesgo determinado por la evaluación preoperatoria, pueden resultar útiles para planificar la cirugía; sin embargo, es importante tener en cuenta las tasas de subestimación. La biopsia preoperatoria más la resonancia permiten la detección de riesgo con alta especificidad, pero baja sensibilidad. La biopsia peri-operatoria pudiera afinar la decisión de realizar la linfadenectomía en conjunto con los parámetros preoperatorios. La técnica de ganglio centinela podría ser útil para limitar la morbilidad asociada a la linfadenectomía de rutina en pacientes con bajo riesgo, debido al bajo desempeño de la evaluación preoperatoria, bien sea por biopsia endometrial o estudios de imagen.
Referencias
1. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136(5):E359-386
2. Kilgore LC, Partridge EE, Alvarez RD, Austin JM, Shingleton HM, Noojin III F, et al. Adenocarcinoma of the endometrium: Survival comparisons of patients with and without pelvic node sampling. Gynecol Oncol. 1995;56(1):29-33.
3. Creasman WT, Mutch DE, Herzog TJ. ASTEC lymphadenectomy and radiation therapy studies: Are conclusions valid? Gynecol Oncol. 2010;116(3):293-294.
4. Bendifallah S, Canlorbe G, Collinet P, Arsene E, Huguet F, Coutant C, et al. Just how accurate are the major risk stratification systems for early-stage endometrial cancer? Br J Cancer. 2015;112(5):793-801.
5. Colombo N, Preti E, Landoni F, Carinelli S, Colombo A, Marini C, et al. Endometrial cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2011;22 (Suppl 6):vi35-39.
6. Cancer de l’endomètre, Institut National du cancer; 2010. Disponible en: URL: www.e-cancer.fr/content/download/95903/.../PLACEND10.pdf
7. Benedetti Panici P, Basile S, Maneschi F, Alberto Lissoni A, Signorelli M, Scambia G, et al. Systematic pelvic lymphadenectomy vs. no lymphadenectomy in early-stage endometrial carcinoma: Randomized clinical trial. J Natl Cancer Inst. 2008;100(23):1707-1716.
8. ASTEC Study Group, Kitchener H, Swart AM, Qian Q, Amos C, Parmar MK. Efficacy of systematic pelvic lymphadenectomy in endometrial cancer (MRC ASTEC trial): A randomized study. Lancet. 2009;373(9658):125-136.
9. Todo Y, Kato H, Kaneuchi M, Watari H, Takeda M, Sakuragi N. Survival effect of para-aortic lymphadenectomy in endometrial cancer (SEPAL study): A retrospective cohort analysis. Lancet. 20103; 75(9721):1165-1172.
10. Kang S, Lee JM, Lee JK, Kim JW, Cho CH, Kim SM, et al. How low is low enough? Evaluation of various risk-assessment models for lymph node metastasis in endometrial cancer: A Korean multicenter study. J Gynecol Oncol. 2012;23(4):251-256.
11. Benedet JL, Bender H, Jones 3rd H, Ngan HY, Pecorelli S. FIGO staging classifications and clinical practice guidelines in the management of gynecologic cancers. FIGO Committee on Gynecologic Oncology. Int J Gynaecol Obstet 2000;70(2):209-262.
12. Teixeira M, Ribeiro R, Kathleen M, Schmeler K, Herzog TJ. A preoperative and intraoperative scoring system to predict nodal metastasis in endometrial cancer. Int J Gynecol Obstet.2017;137:78-85.
13. Tuomi T, Pasanen A, Luomaranta A, Leminen A, B€utzow R, Loukovaara M. Risk-stratification of endometrial carcinomas revisited: A combined preoperative and intraoperative scoring system for a reliable prediction of an advanced disease. Gynecol Oncol. 2015;137(1):23-27.
14. Helpman L, Kupets R, Covens A, Saad RS, Khalifa MA, Ismiil N, et al. Assessment of endometrial sampling as a predictor of final surgical pathology in endometrial cancer. Br J Cancer. 2014 ;110(3):609-615.
15. Batista TP, Cavalcanti CL, Tejo AA, Bezerra AL. Accuracy of preoperative endometrial sampling diagnosis for predicting the final pathology grading in uterine endometrioid carcinoma, Eur J Surg Oncol. 2016;42(9):1367-1371.
16. Creasman WT, Morrow CP, Bundy BN, Homesley HD, Graham JE, Heller PB, et al. Surgical pathologic spread patterns of endometrial cancer. A Gynecologic Oncology Group study. Cancer. 1987;60(Suppl 8):S2035-2041.
17. Morrow CP, Bundy BN, Kurman RJ, Creasman WT, Heller P, Homesley HD, et al. Relationship between surgical-pathological risk factors and outcome in clinical stage I and II carcinoma of the endometrium: A Gynecologic Oncology Group study. Gynecol Oncol. 1991;40(1):55-65.
18. AlHilli MM, Podratz KC, Dowdy SC, Bakkum-Gamez JN, Weaver AL, McGree ME, et al. Preoperative biopsy and intraoperative tumor diameter predict lymph node dissemination in endometrial cancer. Gynecol Oncol. 2013;128:294-299.
19. Pakkal MV, Rudralingam V, McCluggage WG, Kelly BE. MR staging in carcinoma of the endometrium and carcinoma of the cervix. Ulster Med J. 2004;73(1):20-24.
20. Frei KA, Kinkel K, Bonel HM, Lu Y, Zaloudek C, Hricak H. Prediction of deep myometrial invasion in patients with endometrial cancer: Clinical utility of contrast-enhanced MR imaging a meta-analysis and Bayesian analysis. Radiology. 2000;216(2):444-449.
21. Body N, Lavoué V, De Kerdaniel O, Foucher F, Henno S, Cauchois A, et al. Are preoperative histology and MRI useful for classification of endometrial cancer risk? BMC Cancer. 2016;16:498.
22. Huang GS, Gebb JS, Einstein MH, Shahabi S, Novetsky AP, Goldberg GL. Accuracy of preoperative endometrial sampling for the detection of high-grade endometrial tumors. Am J Obstet Gynecol. 2007;196(3):243.
Notas de autor
tatianafandinor@gmail.com