
Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 28 Abril 2018
Revisado: 24 Junio 2018
Aprobación: 15 Julio 2018
Resumen: Se describe un caso clínico en una paciente posmastectomía parcial en la que se utiliza la técnica para la recuperación de tejido blando. Choukroum J, desarrolla la técnica del plasma rico en fibrina, el coágulo de PRF contiene un 97 % de plaquetas y más de un 50 % de leucocitos, dando lugar a una matriz fuerte de fibrina con una distribución tridimensional específica capaz de liberar factores de crecimiento y proteína implicadas en la curación de heridas durante más de 7 días promoviendo la diferenciación y proliferación celular. Los fundamentos de esta técnica son los efectos de las sustancias implicadas en el proceso de cicatrización y regeneración tisular, que conlleva la fibrina, leucocitos, citoquinas y los factores de crecimiento plaquetarios, multiplicando el efecto de coagulación y regeneración tisular en forma de un coagulo natural de fibrina que une los tejidos lesionados, permitiendo la proliferación y migración celular.
Palabras clave: Plasma, plaquetas, factores de crecimiento, cirugía, mastectomía.
Abstract: A clinical case is described of a post partial mastectomy in patient in whom the Choukroun technique is used for the recovery of soft tissue. Choukroun J, developed the technique of fibrin rich plasma, the clot of PRF contains 97 % of platelets and over 50 % leucocytes, allowing the formation of a strong fibrin matrix with a specific tridimensional distribution capable of releasing growth factors and the proteins implicated in the mending of wounds over a period of 7 days promoting the differentiation and the cellular proliferation. The foundation of this technique are the effects of the substances implicated in the process of cicatrization and the tissue regeneration, with the fibrin, the leukocytes the cytokines, and the platelet growth factors, multiplying the coagulation effects and tissue regeneration in the shape of a natural clot of fibrin that binds the injured tissue, allowing the proliferation and cellular migration.
Keywords: Plasma, platelets, grows factors, surgery, mastectomy.
INTRODUCCIÓN
La utilización de los factores de crecimiento plaquetario, tiene más de tres décadas de uso y aplicación en distintas ramas de la medicina bio-regenerativa y estética. Aldeoca A en 1995, explica la técnica para la obtención del plasma rico en plaquetas; en 1997 Whitman y col., presentaron el gel de plaquetas como una alternativa autóloga al adhesivo de fibrina en cirugía oral y maxilofacial, utilizándolo no solo como adhesivo tisular sino como procedimiento para la consolidación de injertos cortico esponjosos de los maxilares (1,2,3). Durante más de 10 años, existió un falta de unificación de criterios en los términos empleados para definir los concentrados de plaquetas. Dohan-Ehrenfest y col., realizaron una clasificación en el 2009 de los distintos derivados de plaquetas y los dividieron en 4 familias dependiendo de su contenido de leucocitos y su arquitectura de fibrina: plasma rico en plaquetas puro, plasma rico en plaquetas y leucocitos, fibrina rica en plaquetas pura, y fibrina rica en plaquetas y leucocitos (4). El plasma rico en plaquetas puro (P-PRP), y el plasma rico en plaquetas y leucocitos (L- PRP), son suspensiones de plaquetas líquidas, sin y con leucocitos, se usan como suspensiones inyectables. Después de su activación con trombina, cloruro de calcio u otros agentes se convierten en fibrina. Con una arquitectura sésil de la misma la fibrina rica en plaquetas pura (P-PRF), y la L-PRF son biomateriales de fibrina sólida sin y con leucocitos, puede ser natural (L-PRF), o artificial (P-PRF) con la adición a la sangre extraída de sustancias activadoras, lo que da lugar a una fibrina fuerte (5). Más tarde algunos autores observaron que el plasma rico en plaquetas aumentaba la concentración de plaquetas en los injertos, observando en el mismo al menos la presencia de tres factores de crecimiento plaquetarios y vieron que las células esponjosas tenían receptores para estos factores de crecimiento (2). No es hasta los años 90 que se empieza a emplear el plasma rico en plaquetas, como regenerador tisular en procesos de cirugía, por su alto contenido en plaquetas solubles, que son capaces de actuar en la regeneración tisular, diferenciación celular y quimio-taxis. Choukroum J, desarrolla la técnica del plasma rico en fibrina en el año 2001, primeramente en Francia, y lo bautiza como concentrado de plaquetas de 2a generación “plasma de segunda generación” (2). Para el uso específico de cirugía e implantología oral y maxilo-buco-facial. Esta técnica a diferencia del plasma rico en plaquetas no requiere anticoagulantes, ni aditivos, ni uso de trombina bovina para la obtención del concentrado plaquetario y no es más que sangre centrifugada sin ningún aditivo, lo cual hace al PRF un biomaterial autólogo, natural y sin riesgos colaterales (3).
CASO CLÍNICO
Se trata de paciente femenina de 17 años sin antecedentes personales ni familiares de importancia. Antecedentes ginecobstétricos: I gesta I para distócico simple a término en diciembre de 2017. Quien consulta el 07/3/2017 por fiebre, dolor y aumento de volumen de mama derecha de 20 días de evolución, la cual no había cedido con medicación casera ni medidas térmicas, (paños de agua caliente alternados con agua fría, lo que ocasionó quemadura en la zona), en vista de presentar dolor e inflamación progresiva es ingresada con el diagnóstico de sepsis de punto de vista de partida tejidos blandos y mastitis abscedada de mama derecha, a la Unidad de Cuidados intensivos (UCI) con los siguientes paraclínicos cuenta y fórmula blanca 42 550 x mm3 a expensas de segmentados 90 %, bilirrubina total 6,31 mm/dL bilirrubina directa 4,95 mm/dL bilirrubina indirecta 1,96 mm/dL, recibió antibiótico terapia en su estancia hospitalaria en UCI con ceftriaxona, vancomicina (EV), fluconazol. Se decide realizar mastectomía parcial con la finalidad de eliminar foco infeccioso y áreas necróticas, se toma biopsia producto del acto quirúrgico donde se ve comprometido 50 % del tejido mamario a nivel de ambos cuadrantes inferiores, el diagnóstico anatomopatológico: mastitis abscedada (Figura 1). Se realiza ecosonograma mamario de control el que reporta mastitis y adenopatía. Se le solicita interconsulta con cirugía plástica, y en vista de no contar con el especialista en el servicio, se valora con oncología y mastología previa biopsia mamaria (mastitis abscedada), y se sugiere la colocación de membranas de fibrina en reunión del servicio, conjuntamente con el servicio de hematología. Se procedió a realizar una primera aplicación de mallas de fibrina en el servicio antes de su egreso, donde se le tomó a la paciente una muestra de sangre de 20 cm3 obtenida por vacutainer para mayor facilidad en el llenado directo al vacío de los tubos, tubos estériles de PRF tapa roja (técnica del Dr. Joseph Choukroum). El protocolo de centrifugación fue de 1 300 revoluciones durante 8 min dichos tubos se distribuyeron en la centrífuga obteniendo en ellos dos estratos: los elementos formes o serie roja, y la segunda fracción PRF fibrina rica en plaquetas. Los tubos fueron puestos al reposo sin tapón en la gradilla durante 2 min, posteriormente se procedió a sacar la membrana de cada tubo con pinza estéril y limpiar los restos de contenido hemático sobre una gasa estéril, y se colocaron en la APRFBox, caja metálica especial para prensar membranas de fibrinas, durante 2 min, luego estas fueron colocadas expuestas en el tejido, y cubiertas con apósito seco y estéril. Fue citada nuevamente durante 5 veces consecutivas cada 7 días para la colocación de nuevas membranas, con la misma técnica y protocolo, cabe destacar que el área de necrosis hizo compromiso del complejo areola pezón el cual se desprendió, a medida que se fueron realizando las curas (Figura 2), observamos cómo se iba restituyendo la arquitectura del tejido mamario, y en cada sesión disminuíamos el número de membranas para su colocación.
Posterior a las seis sesiones realizadas de aplicación cada siete días de membranas de fibrinas APRF y seguimiento de la paciente, así como control ecográfico, pudimos corroborar y comprobar la completa regeneración del tejido mamario y arquitectura de la misma con recuperación de sensibilidad, tono de la piel sin cicatrices, ni efectos colaterales observados ni referidos por la paciente.
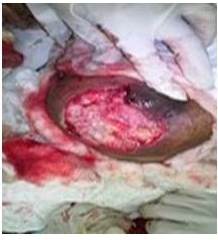
Figura 1
Mama derecha posmastectomía parcial
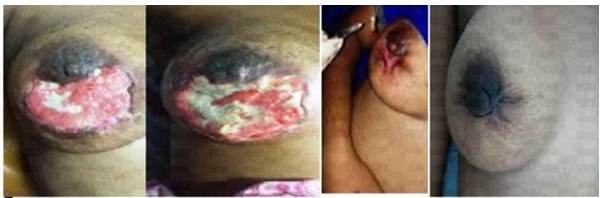
Figura 2
Evolución clínica de mama afectada durante tratamiento con mallas de fibrina
DISCUSIÓN
El coagulo de PRF contiene un 97 % de plaquetas y más de un 50 % de leucocitos, dando lugar a una matriz fuerte de fibrina con una distribución tridimensional específica capaz de liberar factores de crecimiento y proteínas implicadas en la curación de heridas durante más de 7 días promoviendo la diferenciación y proliferación celular (8,9).
Es de destacar que los tubos de extracción sanguínea tienen que estar adaptados según la norma de ISO 10993 para el uso clínico, porque los tubos estándar tienen partículas de sílice que pueden introducir citotoxicidad, mutagenicidad, irritación dérmica y hemolisis entre otros efectos indeseables, por lo que su uso se limita únicamente para pruebas in vitro, por otra parte la manipulación manual de las membranas puede añadir microorganismos y contaminantes ambientales indeseados previamente su aplicación, por lo que se recomienda la utilización de cajas quirúrgicas esterilizadas (7). El material necesario para preparar membranas de fibrina por la técnica adecuada, compone una centrífuga que tenga como parámetros regulables el tiempo y las revoluciones por min, un kit de extracción sanguínea, una caja quirúrgica, y un kit de regeneración tisular. Los fundamentos de esta técnica son los efectos de las sustancias implicadas en el proceso de cicatrización y regeneración tisular, que conlleva la fibrina, leucocitos, citoquinas y los factores de crecimiento plaquetarios, multiplicando el efecto de coagulación y regeneración tisular en forma de un coagulo natural de fibrina que une los tejidos lesionados, permitiendo la proliferación y migración celular (8). En el mecanismo de acción de cicatrización y regeneración tisular se lleva a cabo en varias etapas: una primera etapa donde se produce hemostasia para evitar las hemorragias, mediada por vasoconstricción y agregación plaquetaria. Una segunda fase las plaquetas contienen gránulos alfas, que son reservorios de proteínas activas, aproximadamente más de 30 factores de crecimiento plaquetarios, con liberación de los factores de crecimiento 5 veces más que el plasma rico en plaquetas, logrando angiogénesis capilar y proceso de regeneración (8,9).
Luego una tercera fase con la formación de fibrina que actúa como andamiaje para las células mesenquimales, vascularización del tejido facilitando la diferenciación para contribuir a la curación y cicatrización de heridas.
Posteriormente, se produce una fase inflamatoria esencial para el proceso de migración y activación de los leucocitos. Y se produce un proceso de re-plasma, plaquetas, factores de crecimiento, cirugía, mastectomía, con formación de nuevos vasos sanguíneos y síntesis de colágeno. Entre los factores de crecimiento plaquetario liberados está el factor de crecimiento vascular endotelial que es un promotor de la angiogénesis otro sería el factor de crecimiento insulínico tipo 1, el factor de crecimiento fibroblástico, cuyas funciones son la división, proliferación y angiogénesis entre otras (9).
Todos estos productos son liberados en el lugar de la herida en forma lenta y mantenida durante un tiempo prolongado de 7 días in vitro (3,4,5,7,9).
Se destaca que es una técnica sencilla, económica que se realiza rápidamente en menos de 20 min, que solo precisa una centrifugación (3,4). Es un material natural, biológico fisiológico que no precisa el empleo de aditivo y que además tiene propiedades moleculares favorables que permiten la liberación de factores de crecimiento. El éxito de la técnica depende absolutamente del tiempo transcurrido entre la extracción de sangre y su transferencia a la centrifugadora, para que la preparación sea clínicamente utilizable debe ser inmediata, antes que se inicie la cascada de coagulación. Todo ello permite la curación del lecho quirúrgico, riesgo de contaminación, disminuye el edema, dolor posoperatorio. Permite la obtención de varias membranas simultáneamente con propiedades elásticas y resistentes, lo que las hace fácilmente saturables (6,8); otra de las ventajas es que es inocuo, porque se toma de la propia sangre del paciente, elimina la posibilidad de trasmisión de enfermedades, así como de alergias o reacciones de rechazo (8,9).
Se ha comprobado y demostrado que después de la centrifugación el 97 % de las plaquetas y el 50 % de los leucocitos del volumen de sangre original se concentran en la fracción de fibrina del coagulo del PRF (8).
No existen reportados en la literatura que desaconsejen el uso de la técnica. Entre las técnicas anteriores el inconveniente era el tiempo de obtención de la membrana y su inserción del lecho quirúrgico porque la sangre una vez que entraba con el contacto del tubo comenzaba a coagularse produciendo una polimerización difusa de la fibrina que conduce a la obtención de un coagulo sin consistencia (9).
Actualmente la utilización de las cajas quirúrgicas puede retrasar hasta 3 a 4 h la inserción de las membranas, y se pueden obtener de 8 a 10 membranas simultáneas (8).
Entre las indicaciones tienen numerosas en el área de implantología oral y campo de la cirugía, recientemente se comenzó a utilizar en traumatología, dermatología, estética y ginecología cosmética (3).
Las membranas de PRF (membranas de fibrina ricas en factores de crecimiento plaquetarios autólogos ) diseñadas y obtenidas por este sistema de obtención de membranas por la técnica del Dr. Joseph Choukroum, es una técnica simple, económica, eficaz que permite la aceleración de la cicatrización, regeneración de los tejidos blandos y duros (óseos), y su principal ventaja es que es obtenido de la sangre del propio paciente, sin aditivos, que evitan las reacciones adversas, riego de infección y transmisión de enfermedades, logrando así la bio-regeneración del tejido con efecto de cicatrización adecuado devolviéndole calidad de vida a la paciente. Se sugiere seguir realizando más trabajos y publicaciones al respecto en otras áreas de la medicina desde el aspecto curativo y regenerativo.
Referencias
1. Tatum H. Maxillary and sinus implant reconstruction. Dent Clin North Am. 1986;30:207-209.
2. Dohan DM, Choukroun J, Diss A, Dohan SL, Dohan AJ, Mouhyi J, et al. Platelet-rich fibrin (PRF): A second generation platelet concentrate. Part 1 Technological concepts and evolution. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006;101(3):e37-44.
3. Preeja C, Aurun S. Platelet-rich fibrinits role in periodontal regenerative. The Saudi J Dent Res. 2014;5:117-122.
4. Dohan-Ehrenfest DM, Ranmusson L, Ablbrektsson T. Classification of platelet concentrates: Frompure platelet-rich plasma (p-PRP) to leucocyte-and platelet-rich fibrin (L-PRF). Trends Biothecnol. 2009;27:158-167.
5. Choukroum J, Adda F, Shoeffer C, Vervelle A an opportunity in perio-implantology. Implantodontie. 2000;42:55-62.
6. Kobayashi M, Kawser T, Horimisy M, Okuda K, Wolff L, Yoshie H. A proposed protocol for the standardized preparation of PRF membranes for clinical uses. Biologicals. 2012;40(5):323-329.
7. Dohan Ehrenfest DM, Pinto NR, Pereda A, Jiménez P, Corso MD, Kang BS, et al. The impact of the centrifugation protocols on the cells, growth factors and fibrin architecture of a leukocyte and platelet-rich fibrin (l-PRF) clot and membrane. Platelets. 2018;2:171-184.
8. Leigha R. Potential of platelet rich fibrin in regenerative periodontal therapy: Literature review. Can J Dent Hygiene. 2013;47(1):33-37.
9. Sunitha V, Munirathnam E. Platelet-rich fibrin: Evolution of a second-generation platelet concentrate. Indian J Dent Res. 2008;(1):42-46.
Notas de autor
florangelvera@gmail.com
