CÁNCER DE TIROIDES EN ESTADIOS AVANZADOS TRATADOS CON INHIBIDORES DE TIROSINA QUINASA (SORAFENIB)
CÁNCER DE TIROIDES EN ESTADIOS AVANZADOS TRATADOS CON INHIBIDORES DE TIROSINA QUINASA (SORAFENIB)
Revista Venezolana de Oncología, vol. 31, núm. 1, pp. 2-7, 2019
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 04 Abril 2018
Revisado: 20 Septiembre 2018
Aprobación: 19 Octubre 2018
Resumen: OBJETIVO: Este estudio pretende evaluar la sobrevida global en los pacientes con carcinoma diferenciado de tiroides localmente avanzado yodo refractario. MÉTODO: Son 8 casos tratados con inhibidores de tirosina quinasa (Sorafenib) en el período comprendido entre 2014-2017. Las variables estudiadas fueron: Epidemiológicas, laboratorios tiroideos, histología, tratamiento, supervivencia posterior al tratamiento. Se tomó como significativo una P<0,05. RESULTADOS: Edad media entre los pacientes fue 51 años ±22,1 años, el sexo prevaleciente fue femenino (75 %). El lugar de procedencia más incidente fue Estado Miranda (50 %). Los valores de laboratorio al momento del diagnóstico fueron tiroglobulina (290,2 ± 250,7), la TSH (11,3± 13,9) y la antitiroglobulina solo fue positiva en un paciente (87,5 %). La T predominante fue T3 (50 %), la N que prevaleció fue N1B (62 %) y M1 (62,5 %). El estadio predominante fue IVC (50 %). El grupo histológico predominante fue papilar (62,5 %). Se les realizó tiroidectomía total con vaciamiento bilateral al 75 % de los pacientes. Posteriormente recibieron 131I, para los cuales se obtuvieron una dosis media de 227,5 mCi con desviación de estándar: 188,1 mCi. La mayoría recibió radioterapia externa a región cervical (87,50 %). La sobrevida global 3 años posteriores al tratamiento fue 87,5 %. CONCLUSIONES. El control de la enfermedad a largo plazo en estos pacientes avanzados puede obtenerse con Sorafenib. En nuestro estudio evidenciamos que es un fármaco adecuado para controlar la enfermedad en pacientes con cáncer de tiroides yodo refractarios.
Palabras clave: Cáncer, tiroides, papilar, yodo, Sorafenib.
Abstract: OBJECTIVE: This study aimed evaluates overall survival in patients with locally advanced thyroid iodine refractory differentiated carcinoma. METHOD: 8 cases treated with inhibitors of tyrosine kinase (Sorafenib) in the period 2014-2017. The variables studied were: epidemiological, laboratory thyroid histology, treatment, post-treatment survival. P was taken as meaningful < 0. 05. RESULTS: Mean age among patients was 51 years ±22.1 year, prevailing sex female (75 %). Place of origin more incident was Miranda State (50 %). At the time of the diagnostic laboratory values were thyroglobulin (290.2 ± 250.7), TSH (3± 13.9 11) and the single antithyroglobulin was positive in one patient (87.5 %). The predominant T was T3 (50 %), the N that prevailed was N1B (62 %) and M1 (62.5 %). The predominant stadium was IVC (50 %). The predominant histological group was papillary (62.5 %). The predominant stadium was IVC (50 %). The predominant histological group was papillary (62.5 %). He was performed in total thyroidectomy with bilateral clearing to 75 % of patients. Subsequently received 131I, for which an average dose of 227.5 mCi with standard deviation were obtained: 188.1 mCi. Most received radiotherapy external cervical region (87.50 %). Global survival 3 years after treatment was 87.5 %. CONCLUSIONS: The control of disease in long run in these advanced patients can get with Sorafenib. In our study we showed that it is a suitable drug to control the disease in patients with cancer of thyroid iodine refractory.
Keywords: Cancer, thyroid, papillary, iodine, Sorafenib.
INTRODUCCIÓN
El cáncer de tiroides es la neoplasia endocrina más frecuente siendo el carcinoma papilar de tiroides (CPT) el subtipo histológico de mayor incidencia, que representa el 75 %- 80 % de los casos. Clásicamente se le ha considerado a este cáncer como de buen pronóstico teniendo en cuenta los datos que describen cánceres ocultos en autopsias en hasta un 20 % de pacientes fallecidos por otras causas. Está generalmente caracterizado por un curso lento y es potencialmente curable cuando se descubre en etapas tempranas (1,2).
Posee una baja aunque creciente incidencia, así como una baja letalidad. En 2008, la incidencia mundial de carcinoma de tiroides estimada fue 213 179 (una tasa global estandarizada por edad de 3,1 casos por cada 100 000 personas), asociada a una estimación de 35 383 muertes por carcinoma de tiroides (3).
La incidencia de cáncer de tiroides aumentó exponencialmente en todo el mundo a expensas de pequeños tumores de estirpe papilar. La causa de esta tendencia no está totalmente clara, pero podría reflejar los efectos combinados de una mayor detección debido al uso rutinario de la ecografía de la región cervical (y tiroidea), asociados a un mayor acceso a la salud y al nivel socioeconómico del paciente (4).
En Venezuela la incidencia del cáncer de tiroides para el 2012 fue del 1 % según cifras reportadas por el Ministerio del Poder Popular para la Salud (5).
La cirugía es la principal modalidad de tratamiento en pacientes con CDT, en la mayoría de los casos, tiroidectomía total. Tras la cirugía inicial, se administra yodo radioactivo (RIA) con el objetivo de conseguir la ablación total de cualquier resto de tejido tiroideo y el posible tumor residual microscópico (3).
La mayoría de personas tienen un buen pronóstico tras el tratamiento estándar, sin embargo, existe un pequeño grupo de pacientes en los que el cáncer progresa a pesar del tratamiento con RIA. La supervivencia a largo plazo de pacientes con CDT resistente a RIA es bastante pobre, con una supervivencia global a los 10 años de sólo el 10 %. Una vez el carcinoma no responde a RIA, la supervivencia global cae a una media de tres años (3).
En los pacientes con enfermedad avanzada o metástasis y resistentes a yodo, las opciones son muy limitadas, valorándose en este punto la inclusión de los pacientes en ensayos clínicos (4). La quimioterapia es una alternativa eficaz en un porcentaje limitado de pacientes (20 %-30 %) a expensas de una alta toxicidad. Se han ensayado distintos agentes en monoterapia como doxorrubicina, dacarbacina o 5-fluorouracilo. Otras alternativas son los análogos de somatostatina marcados con el radiofármaco 90Y (DOTATOC) o la administración de etilyodobencilguanidina (MIBG) para el cáncer medular (6).
La Asociación Americana de tiroides y la Asociación Latinoamericana de tiroides, entre otras sociedades en el mundo, actualmente brindan recomendaciones para indicar a los pacientes con CDT avanzado refractario al radioyodo el tratamiento con un inhibidor quinasa (7).
Los inhibidores de la tirosina quinasa, a diferencia de la quimioterapia, están obteniendo resultados esperanzadores. En junio de 2014, el Sorafenib fue autorizado por la EMA para el tratamiento de pacientes con CDT (papilar / folicular / de células de Hürthle) en progresión, localmente avanzado o metástasico, resistente al tratamiento con yodo radiactivo (3, 8).
Las tirosina quinasas (TC) son enzimas que catalizan la transferencia de fosfatos del adenosín trifosfato (ATP) a determinadas proteínas y desempeñan un papel central en la modulación de señales de crecimiento celular interviniendo en diversos procesos normales de regulación. Formas activas de estas enzimas pueden causar aumentos de la proliferación de células tumorales, generar efectos antiapoptóticos así como, promover la angiogénesis y el desarrollo de metástasis. Por tal motivo constituyen un blanco especial e importante de las terapias dirigidas en oncología (9).
Existen diferentes mecanismos por los cuales la alteración de la regulación de los receptores de TC interviene en la oncogénesis. El primero de ellos consiste en un re-arreglo cromosómico, que determina una activación constitutiva del receptor en ausencia de ligando. Otra forma de desregulación es la mutación de la cinasa (dominio catalítico) del receptor. Un tercer mecanismo consistiría en la expresión aumentada o aberrante del receptor, de su ligando o de ambos. Finalmente, la ausencia de factores que limiten la actividad tirosina quinasa (fosfatasas) sería otro de los mecanismos propuestos (10).
En un estudio fase III en pacientes yodo refractarios se evaluó la eficacia del Sorafenib evaluando dos brazos de tratamiento, donde se evidencia de que el Sorafenib mejoró la sobrevida libre de progresión en comparación con el grupo control (11-12).
MÉTODO
Se revisaron historias clínicas desde 2004 al 2017 con el diagnóstico histológico de CDT yodo refractario tratados con inhibidores de tirosina quinasas (Sorafenib) durante el período comprendido entre 2014 - 2017, los cuales provenían de la consulta de tiroides del servicio de Radioterapia y Medicina Nuclear del Hospital Universitario de Caracas, identificando 8 casos. Las variables estudiadas fueron: 1. Epidemiológicas (sexo, edad, y procedencia); 2. Laboratorios tiroideos (tiroglobulina, anticuerpo anti-tiroglobulina y TSH); 3. Histología (tipo); 4. Tratamiento (cirugía, radioterapia, quimioterapia y radioiodoablación (RIA); y 5. Supervivencia posterior al tratamiento, valorando a los pacientes libres o sin evidencia de enfermedad, con persistencia de enfermedad y recurrencia de la misma. Se realizó el test estadístico Chi-2 y curvas de sobrevida por el método de Kaplan Meier, tomando como significativo una P<0,05, usando el software estadístico SPSS ver22.
RESULTADOS
Se analizaron un total de 8 historias de pacientes con CDT yodo refractario, los cuales acudieron a la consulta de tiroides de nuestra institución durante los períodos comprendidos 2004 hasta el 2016, para un total de 14 años de estudio.
En cuanto a la distribución por edades, la edad media entre los pacientes fue de 51 años ±22,1 años, 87 % en adultos y 13 % edad escolar, el sexo que prevaleció fue el femenino con un 75 % 25 % masculino. De la población total el lugar de procedencia más incidente fue el Estado Miranda (50 %) (Figura 1).
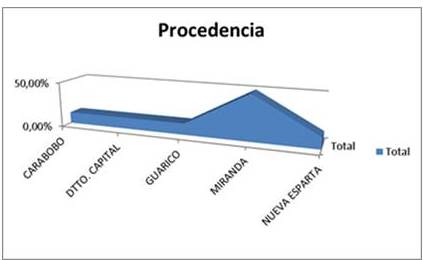
Figura 1
Distribución según procedencia
Para los valores de laboratorio al momento del diagnóstico fueron estudiadas la tiroglobulina (290,2 ± 250,7), la TSH (11,3± 13,9) y el anticuerpo anti-tiroglobulina la cual solo fue positiva en un paciente (87,5 % negativo 13 % positivo).
De acuerdo a la clasificación TNM se obtuvo que la T predominante fue T3 (50 %), la N que prevaleció fue N1B (62 %) y M1 (62,5 %). En resultados se obtuvo que el estadio predominante fue estadio IVC (50 %). (Figura 2). El grupo histológico predominante fue el papilar (62,5 %). Distribuyéndose en iguales proporciones entre sus variedades histológicas (Cuadro 1).
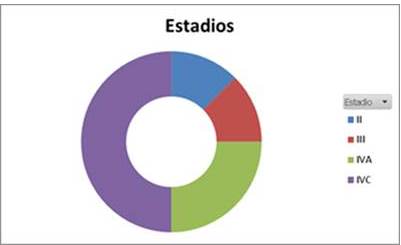
Figura 2
Distribución según el estadio

Cuadro 1
Distribución según histologías
Con respecto al tratamiento quirúrgico a la mayoría de los pacientes se les realizó tiroidectomía total con vaciamiento bilateral (75 %) (Figura 3).
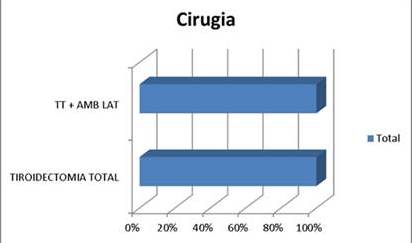
Figura 3
Distribución según el tipo de cirugía
Posterior al tratamiento quirúrgico se realizó tratamiento con 131I, para los cuales se obtuvieron una dosis media de 227,5 mCi con una desviación de estándar: 188,1 mCi. Asimismo, la mayoría recibió radioterapia externa a región cervical (87,50 %) (Figura 4).
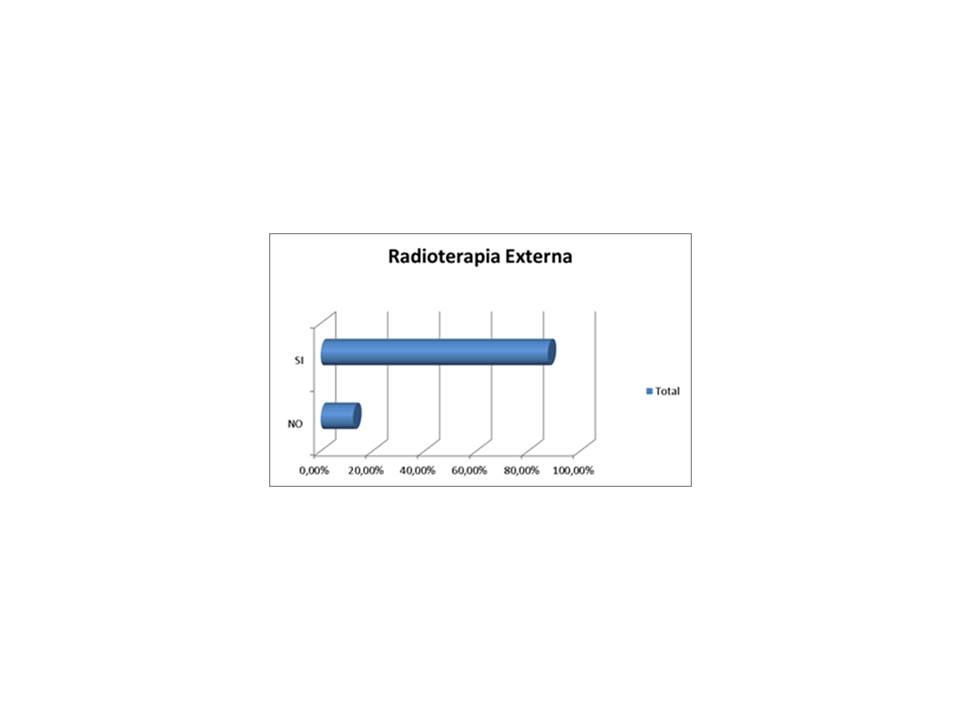
Figura 4.
Distribución según la aplicación de radioterapia externa
En lo que concierne a la sobrevida global los 3 años posteriores al tratamiento fue del 87,5 %, la cual dio diferencias estadísticas con respecto al sexo femenino (P: 0,03) y a la evidencia de abundante remanente posquirúrgico en el rastreo con 131I posterior a dosis ablativa (P: 0,05) (Figura 5).
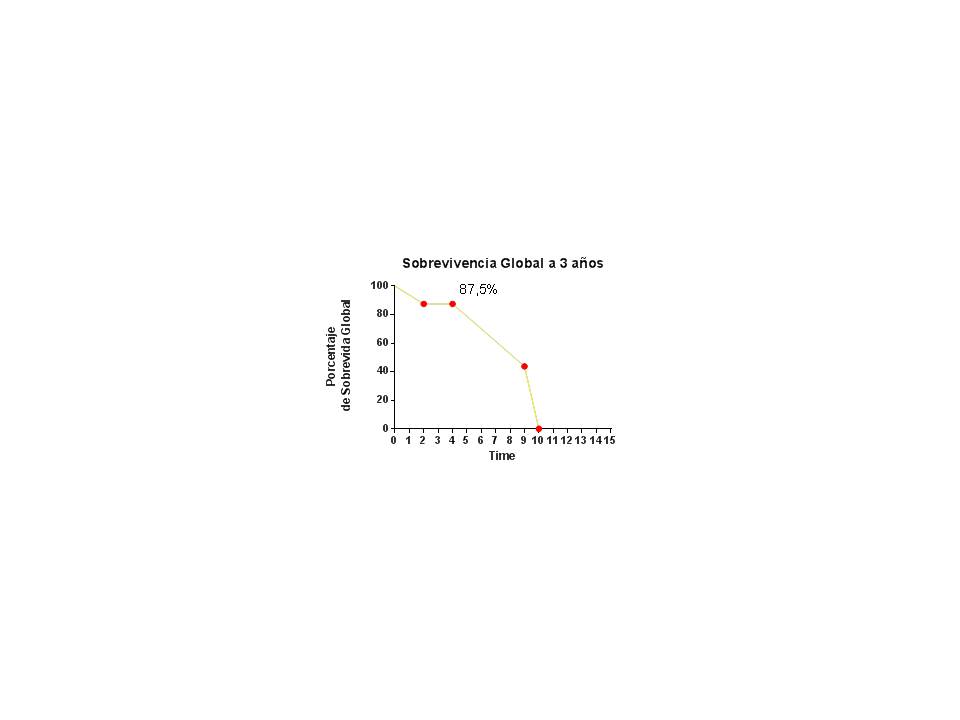
Figura 5.
Sobrevida Global de la enfermedad a los 3 años posterior al tratamiento
DISCUSIÓN
En los datos epidemiológicos reportados por nuestro estudio se observó una prevalencia en pacientes femeninos del 75 % con una edad media al momento del diagnóstico de 51 años, estos datos se asemejan a los obtenidos por Cabanillas y col., (13) los cuales reportaron que el 60 % de su población pertenecían al sexo femenino, sin embargo, la media de edad fue un poco mayor a la nuestra ubicándose en 61 años. Estos resultados contrastan con los reportados por Gupta-Abramson y col.,(14) los cuales reportaron una distribución igualitaria para ambos géneros con una relación 1:1, y una edad media de 63 años, en un rango de los 31 a los 89 años. Por su parte Dadu y col.,(15) reportaron una mayor prevalencia en el sexo masculino (53 %), y una edad media de 53 años, semejante a la de nuestro estudio.
En cuanto a lo que fue la distribución histopatológica Kloos y col.,(16) en su estudio evaluaron a 46 pacientes, de los cuales el 78 % presentó histología de tipo papilar al momento del diagnóstico; contrastando con los resultados obtenidos en nuestra serie donde la afectación por histología, preponderó el carcinoma papilar, el cual se ubicó con un 62,5 % en el primero lugar de predominancia.
Nuestro estudio reportó como estadio de la enfermedad al momento del diagnóstico predominante el estadio IVC, correspondiendo a un 50 % de la población estudiada, datos similares a los obtenidos por Dadu y col.,(15) los cuales ubicaron la mayoría de su muestra en el estadio IVC (30 %).
Diversas series reportan elevadas tasas de sobrevida global, Ahmed y col.,(17) la ubicó en el 100 % a los 2 años, Kloos y col.,(16) y Dadu y col.,(15) reportaron una sobrevida global media de 36 meses, estos últimos no encontraron asociación estadística entre lo que fue la sobrevida global, el sexo, hallazgos histológicos y estadio al momento del diagnóstico, lo que difiere de nuestro estudio donde si encontramos una asociación estadísticamente significativa entre lo que fue la sobrevida global y el sexo femenino (P: 0,03). La sobrevida global en nuestro estudio se ubicó en el 87,5 %.
Actualmente, no existe una guía estándar para el tratamiento de pacientes con cáncer diferenciado de tiroides avanzado refractario a la terapia ablativa (18). El desarrollo de inhibidores de la enzima quinasa es el primer avance importante en el tratamiento con cáncer de tiroides yodo refractario en más de 30 años. El control de la enfermedad a largo plazo en pacientes con CDT avanzado puede obtenerse con Sorafenib, un fármaco oral con un perfil de toxicidad bastante tolerado y ha demostrado su eficacia contra el DTC en numerosos ensayos clínicos, lo que resulta principalmente en la estabilización de la enfermedad (19). En nuestro estudio evidenciamos que el Sorafenib es un fármaco adecuado para controlar la enfermedad en pacientes con cáncer de tiroides yodo refractarios, tomando en cuenta que la quimioterapia actualmente no ha tenido buenos resultados para el control de la enfermedad. Asimismo, hay que tener presente que se necesitan aún más estudios para respaldar el papel de Sorafenib en el cáncer de tiroides.
REFERENCIAS
1. González H, Mosso L. Cáncer papilar de tiroides: visión actual. BOLETÍN DE LA ESCUELA DE MEDICINA. 2006;31(2):87-91.
2. González C, Yaniskowski M, Wyse E, Giovannini A, Lopez M, Wior M, et al. Cáncer de tiroides estudio descriptivo retrospectivo. Medicina (Buenos Aires). 2006;66(6):526-532.
3. Agencia de Evaluación de Tecnologías Sanitarias de Andalucía. Lenvatinib en carcinoma de tiroides diferenciado progresivo, localmente avanzado o metastático, refractario a yodo radioactivo. Eficacia y seguridad. 2015. Disponible en: URL: http://www.aetsa.org/download/publicaciones/antiguas/IS-Lenvatinib-Publicado.pdf
4. Pitoia F, Califano I, Vázquez A, Faure E, Gauna A, Orlandi A. Consenso intersocietario sobre tratamiento y seguimiento de pacientes con cáncer diferenciado de tiroides. 2014 [Internet]. 2014 [citado 20 de julio de 2018]. Disponible en: URL: http://www.scielo.org.ar/pdf/raem/v51n2/v51n2a05.pdf
5. Negrín L. Resumen del cáncer en Venezuela. 2012. Rev Venez Oncol. 2015;27(4):256-268.
6. García A, López P, Triviño E, Escobar F. Manejo terapéutico del carcinoma medular de tiroides metastásico: Papel de los nuevos inhibidores de la tirosincinasa. Endocrinol Nutr. 2013;60(3):152-153.
7. Pitoia F. Response to sorafenib treatment in advanced metastatic thyroid cancer. Arq Bras Endocrinol Metabol. 2014;58(1):37-41.
8. Schneider T, Abdulrahman R, Corssmit E, Morreau H, Smit J, Kapiteijn E. Long-term analysis of the efficacy and tolerability of sorafenib in advanced radio-iodine refractory differentiated thyroid carcinoma: Final results of a phase II trial. Eur J Endocrinol. 2012;167(5):643-650.
9. Bielski L, Orlandi A, Boquete H. Inhibidores de tirosina cinasa y disfunción tiroidea. Rev Argent Endocrinol Metab. 2016;53(3):96-105.
10. Krause D, Van Etten R. Tyrosine kinases as targets for cancer therapy. N Engl J Med. 2005;353(2):172-187.
11. Brose M, Nutting C, Jarzab B, Elisei R, Siena S, Bastholt L, et al. Sorafenib in radioactive iodine-refractory, locally advanced or metastatic differentiated thyroid cancer: A randomized, double-blind, phase 3 trial. Lancet. 2014;384(9940):319-328.
12. Thomas L, Lai S, Dong W, Feng L, Dadu R, Regone R, et al. Sorafenib in metastatic thyroid cancer: A systematic review. Oncologist. 2014;19:251-258.
13. Cabanillas M, Waguespack S, Bronstein Y, Williams M, Feng L, Hernandez M, et al. Treatment with tyrosine kinase inhibitors for patients with differentiated thyroid cancer: The M. D. Anderson experience. J Clin Endocrinol Metab. 2010;95(6):2588-2595.
14. Gupta-Abramson V, Troxel A, Nellore A, Puttaswamy K, Redlinger M, Ransone K, et al. Phase II trial of sorafenib in advanced thyroid cancer. J Clin Oncol. 2008;26:4714-4719.
15. Dadu R, Devine C, Hernandez M, Waguespack S, Busaidy N, Hu M, et al. Role of salvage targeted therapy in differentiated thyroid cancer patients who failed first-line sorafenib. J Clin Endocrinol Metab. 2014;99(6):2086-2094.
16. Kloos R, Ringel M, Knopp M, Hall N, King M, Stevens R, et al. Phase II trial of sorafenib in metastatic thyroid cancer. J Clin Oncol. 2009;27:1675-1684.
17. Ahmed M, Barbachano Y, Riddell A, Hickey J, Newbold K, Viros A, et al. Analysis of the efficacy and toxicity of sorafenib in thyroid cancer: A phase II study in a UK based population. Eur J Endocrinol. 2011;165(2):315-322.
18. Keefe S, Cohen M, Brose M. Targeting vascular endothelial growth factor receptor in thyroid cancer: The intracellular and extracellular implications. Clin Cancer Res. 2010;126:778-783.
19. Pitoia F, Jerkovich F. Selective use of sorafenib in the treatment of thyroid cancer. Drug Des Devel Ther. 2016;10:1119-1131.
Notas de autor
acalles@fmed.luz.edu.ve
Información adicional
Reconocimiento: Trabajo ganador Premio Dr. Gustavo Rojas Martínez 2018.