TRATAMIENTO CON RADIOTERAPIA QUIMIOTERAPIA NEOADYUVANTE VS. ADYUVANTE EN ADENOCARCINOMA DE RECTO. EXPERIENCIA DE 15 AÑOS
TRATAMIENTO CON RADIOTERAPIA QUIMIOTERAPIA NEOADYUVANTE VS. ADYUVANTE EN ADENOCARCINOMA DE RECTO. EXPERIENCIA DE 15 AÑOS
Revista Venezolana de Oncología, vol. 31, núm. 1, pp. 60-78, 2019
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 26 Septiembre 2018
Revisado: 14 Octubre 2018
Aprobación: 12 Noviembre 2018
Resumen: OBJETIVO: Experiencia 15 años tratamiento neoadyuvante vs., adyuvante ADC recto. MÉTODO: 223 pacientes ADC recto tratamiento RT QT período 2000-2015, divididos 3 grupos: 1. Tratamiento adyuvante (110), 2. Tratamiento neoadyuvante (93), 3. Tratamiento neoadyuvante no operados (20). RT administrada técnica conformada 3D todos los pacientes excepto 3 RT intensidad modulada, dosis 4 500-4 600 cGy fracciones diarias 180-200 cGy, a pelvis técnica 4 campos, reducción sitio lesión macroscópica (RT neoadyuvante) o área de anastomosis (RT adyuvante) 5 000-5 040 cGy. Esquemas QT más utilizados 5FU, 5FU-leucovorina, capecitabina sola o combinación oxaliplatino. RESULTADOS: Mayoría estadio III, mayor IIIB grupo neoadyuvante, 44 % vs. 30 % grupo adyuvante. Sobrevida global 5 años grupo RT-QT adyuvante 69,03 % vs. 81,24 % grupo RT-QT neoadyuvante, resultado no estadísticamente significativo (P=0,37) sobrevida libre enfermedad 5 años 80 % grupo RT-QT neoadyuvante vs. 56 % pacientes grupo RT-QT adyuvante, diferencia estadísticamente significativa (P=0,000392). 20 tratamiento neoadyuvante no cirugía, sobrevida global 5 años 50 %, resultados inferiores a tratamiento adyuvante y neoadyuvante. 59,2 % grupo neoadyuvante 86,4 % adyuvante se pudo preservar el esfínter. Toxicidad aguda más frecuente gastrointestinal, grado II-III, mayor grupo adyuvante (57 % vs. 45 %). Complicaciones crónicas GI, grado III, 2 pacientes grupo adyuvante 1 grupo neoadyuvante, grado IV. 2 grupo adyuvante 1 neoadyuvante. CONCLUSIONES: En 223 pacientes ADC recto, no se encontraron diferencias significativas SG tratamiento adyuvante vs., neoadyuvante pero SLE fue superior grupo tratamiento neoadyuvante. Toxicidad parece menor con tratamiento preoperatorio.
Palabras clave: Radioterapia, quimioterapia, neoadyuvante, adyuvante, adenocarcinoma, recto.
Abstract: OBJECTIVE: 15 years’ experience treatment ADC rectal with adjuvant RT-CT vs., neoadjuvant RT-CT. METHOD: 223 patients rectal ADC treated with RT-CT surgery, during 2000-2015. Divided 3 groups: 1. Adjuvant therapy (110). 2. Neoadjuvant therapy (93) 3. Neoadjuvant therapy without surgery (20). Three D conformal RT used all patients except 3 treated with intensity modulated RT, doses 4 500-4 600 with 180-200 cGy daily fractions pelvis 4 field technique, 5 000-5 040 cGy boost rectal tumor or the anastomosis. Chemotherapy more frequently was 5FU, 5FU-leucovorin, capecitabine alone or oxaliplatin. RESULTS: Majority stage III, IIIB was more frequent neoadjuvant group, 44 % vs., 30 % adjuvant group. 5 years overall survival was 69.03 % adjuvant RT-CT vs. 81.24 % with neoadjuvant RT-QT (P=0.37 disease free survival was higher neoadjuvant therapy, 80 % vs. 56 %, (P=0.000392). 20 treated neoadjuvant RT-CT no surgery, had 50 % OS 5 years, lower than adjuvant or neoadjuvant therapy. Grade II-III acute gastrointestinal toxicity was more common in patients with adjuvant therapy, 57 % vs. 45 % neoadjuvant therapy. One patient in each group grade IV, acute GI toxicity. Chronic grade III GI toxicity occurred, 2 with adjuvant therapy one neoadjuvant therapy, grade IV also 1 patient with preoperative RT-CT in 2 postoperative RT-CT. CONCLUSIONS: 223 rectal ADC, did not show significant difference in OS between adjuvant RT-CT and neoadjuvant RT-CT but DFS was higher with preoperative therapy. Toxicity seems lower in group treated with neoadjuvant therapy.
Keywords: Radiotherapy, chemotherapy, neoadjuvant, adjuvant, adenocarcinoma, rectal.
INTRODUCCIÓN
El cáncer de colon y recto es la tercera neoplasia maligna más común y la cuarta causa de muerte por cáncer a nivel mundial, con una incidencia estimada de 1 400 000 casos nuevos y 700 000 muertes en el año 2012 (1). En EE.UU, para el año 2018 ocupa el tercer lugar de morbilidad y mortalidad por cáncer, con 140 250 nuevos pacientes por año y una mortalidad de 50 630 casos, de estos la incidencia anual estimada de cáncer de recto fue de 43 030 pacientes (2).
En nuestro país las estadísticas más recientes corresponden al año 2012, para ese momento se reportaron 3 135 casos de cáncer colorrectal y 1 557 defunciones; comparado con cifras mundiales fue la cuarta causa de morbilidad y mortalidad por cáncer en ambos sexos (3).
La cirugía es el tratamiento curativo de elección en cáncer de recto, sus resultados son favorables en enfermedad precoz, con cifras de recaída local menores del 10 % en estadio I; sin embargo, en estadios II y III las recidivas locales en varios estudios oscilan entre 25 % y 50 % en pacientes con tumores T3-T4 o ganglios positivos, siendo las recidivas a distancia igualmente importantes (4).
En vista del pronóstico desfavorable en lesiones más avanzadas tratadas sólo con cirugía, desde hace más de 50 años se ha venido utilizando la radioterapia y posteriormente la quimioterapia como tratamientos neoadyuvantes o adyuvantes al tratamiento quirúrgico. Los trabajos iniciales en los años 1970 con radioterapia preoperatoria (5,6,7) y posteriormente los resultados de trabajos con radioterapia posoperatoria, dieron resultados variables que sirvieron de base para realización de nuevos estudios clínicos (8,9).
En los años 1980 y 1990 se publican estudios prospectivos aleatorios de tratamientos combinados de quimioterapia y radioterapia del GITSG (10), NCCTG (11) y NSABP (12) como tratamientos adyuvantes posteriores a la cirugía. En base a estos estudios el NIH en una conferencia de consenso en 1990, recomienda la quimioterapia (QT) y radioterapia (RT) posoperatoria a la pelvis como tratamiento estándar después de la resección quirúrgica en cáncer de recto estadios II y III (13). En 2004 se reportan los resultados de un estudio fundamental realizado en Alemania donde se demuestra la superioridad del tratamiento preoperatorio con RT-QT comparado con la terapéutica posoperatoria, en cuanto al control local y la toxicidad (14). Desde entonces ha cambiado el paradigma y se está regresando a la terapia neoadyuvante en cáncer de recto (15).
El objeto del presente trabajo es reportar nuestra experiencia de 15 años en el tratamiento neoadyuvante y adyuvante con RT-QT en adenocarcinoma de recto, por medio de un análisis retrospectivo.
MÉTODO
Se realizó una revisión retrospectiva de las historias clínicas de los pacientes con adenocarcinoma (ADC) de recto tratados en la Unidad de Radioterapia Oncológica GURVE del Instituto Médico La Floresta y del Servicio de Radioterapia Dr. Enrique M. Gutiérrez del Centro Médico Docente La Trinidad durante los años 2000-2015. Se presenta una estadística descriptiva de la población en estudio, evaluando las diferentes modalidades de tratamiento radiante y quimioterapia utilizadas. Se realizó un análisis de los aspectos clínicos, y los resultados de sobrevida global (SG), sobrevida libre de enfermedad (SLE), control local (CL) y toxicidades agudas y crónicas.
Los datos obtenidos de las 508 historias clínicas revisadas fueron registrados en una hoja de cálculo en Microsoft Office Excel®. Se excluyeron 285 pacientes del estudio en vista de no haber recibido tratamiento combinado de RT-QT, y en el grupo de tratamiento neoadyuvante aquellos individuos en los cuales no se registraron datos sobre la cirugía, los clasificados como estadios IV al momento del diagnóstico, otros con estadios precoz sin criterio para tratamiento radiante, pacientes pediátricos, con diagnóstico de carcinoma de canal anal y aquellos con recaída local (RL) locorregional (RLR); por último 12 pacientes de los 285, fueron tratados sólo con RT y en 10 de ellos se administró QT concurrente, este grupo tampoco fue incluido en el presente análisis.
En cuanto a la RT, la técnica más utilizada fue la conformada con planificación tridimensional (RTC 3D), sólo en 3 pacientes se empleó la técnica de intensidad modulada (RTIM). Se utilizaron 4 campos, dos laterales, uno anterior y otro posterior, que inicialmente incluían toda la pelvis, con fracciones diarias de 180-200 cGy hasta una dosis de 4 500-4 600 cGy, realizando posteriormente reducción al sitio de lesión macroscópica (RT neoadyuvante) o al área de anastomosis (RT adyuvante) hasta completar 5 000-5 040cGy (Cuadro 1 y Figura 1-4).
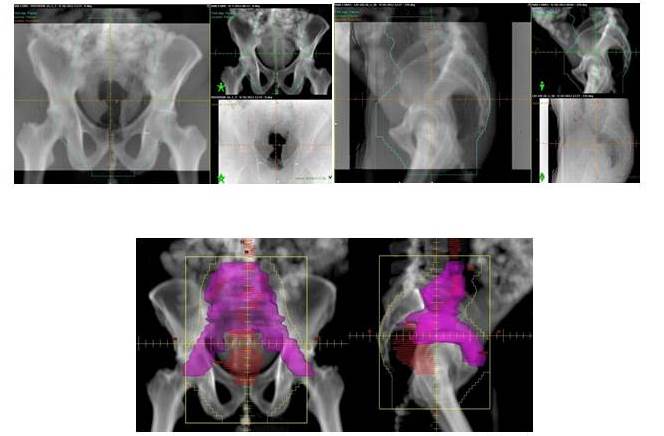
Figura 1 y 2
Diseño de los campos de tratamiento en el sistema de planificación Eclipse se pueden observar los límites de los campos anterior posterior y laterales establecidos por el colimador multiláminas. Igualmente se señalan los contornos de los ganglios linfáticos pélvicos y del tumor (GTV).
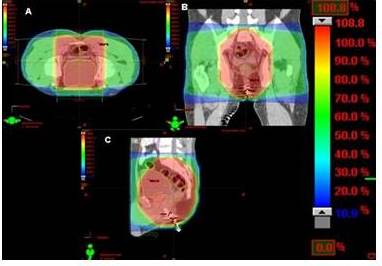
Figura 3.
Figuras 3 y 4. Distribución porcentual de la dosis indicada por las diferentes tonalidades de colores cuyos valores se pueden observar en la columna de la derecha e izquierda, en los planos axial, coronal y sagital. Las asas delgadas reciben una dosis significativamente menor. El paciente fue tratado en posición prona.
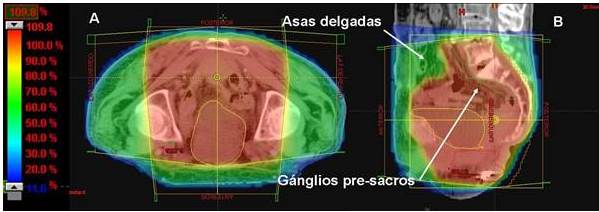
Figura 4
La QT fue administrada utilizando distintos esquemas de tratamiento de acuerdo al criterio de los oncólogos médicos referentes. En el grupo de tratamiento neoadyuvante los esquemas más utilizados fueron a base de 5FU o 5FU-Leucovorina (36 %), seguido de capecitabina sola o en combinación con oxaliplatino (20 %). Mientras que en el grupo de tratamiento adyuvante, el agente más utilizado fue la capecitabina sola o en combinación con oxaliplatino alrededor de 40 % de los casos, seguida de 5FU o 5FU-Leucovorina (12 %) y en el grupo no operado igualmente la capecitabina sola o en combinación con oxaliplatino. En 84 pacientes (37 %) no se pudo obtener información sobre el esquema de QT administrado (Cuadro 1).
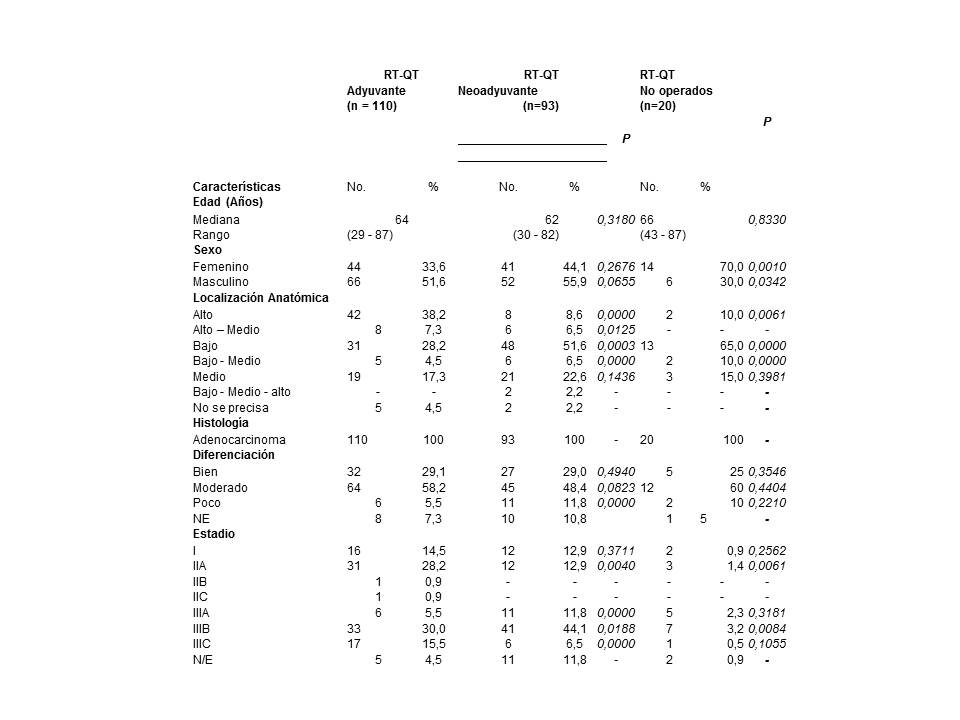
Cuadro 1
Características clínicas de los pacientes y modalidad de tratamiento
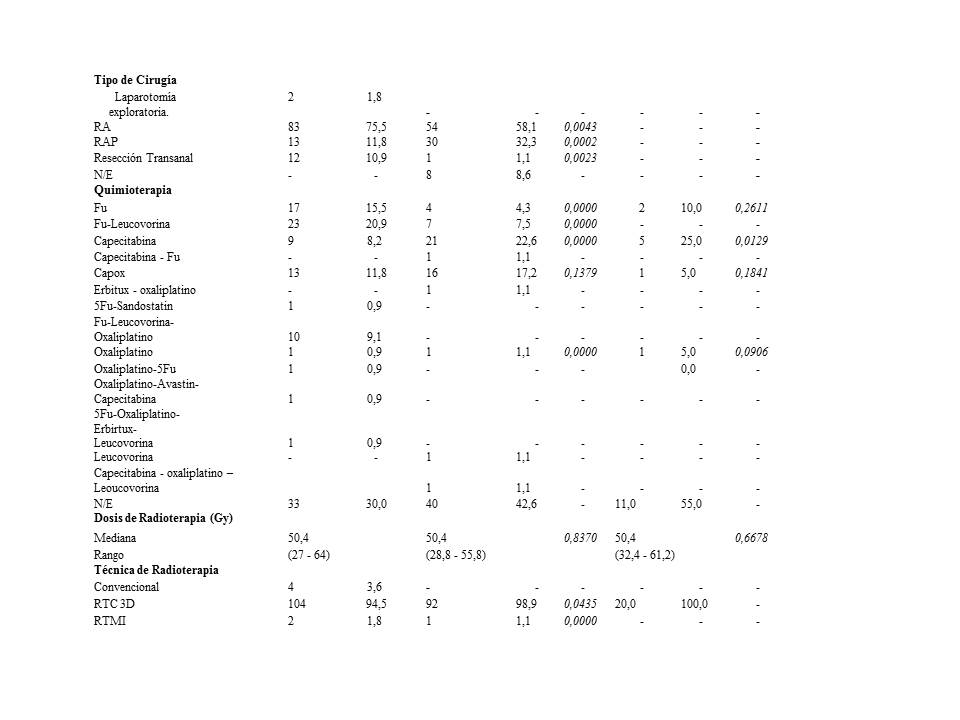
Cuadro 1 (continuación)
Características clínicas de los pacientes y modalidad de tratamiento
La SG de los pacientes incluidos en el grupo de tratamiento adyuvante y neoadyuvante se presenta en la Figura 5. Aunque parece haber una diferencia en favor del grupo neoadyuvante, sobrevida de 5 años 81 % vs. 69 % en el grupo adyuvante, esta diferencia no fue estadísticamente significativa (P=0,37). La SLE a los 5 años fue de 80 % para el grupo neoadyuvante vs. 56 % en los pacientes del grupo adyuvante, diferencia que fue estadísticamente significativa (P=0,000392) (Figura 6).
En el grupo de 20 pacientes que recibieron tratamiento neoadyuvante y no fueron sometidos a cirugía, la SG fue 50 % a los 5 años, resultados que al ser comparadas con las cifras de las cohortes de tratamiento adyuvante (69,0 3%) y neoadyuvante (81,2 %) son inferiores, lo que resalta la importancia del tratamiento quirúrgico en cáncer del recto (Figura 7 y 8).
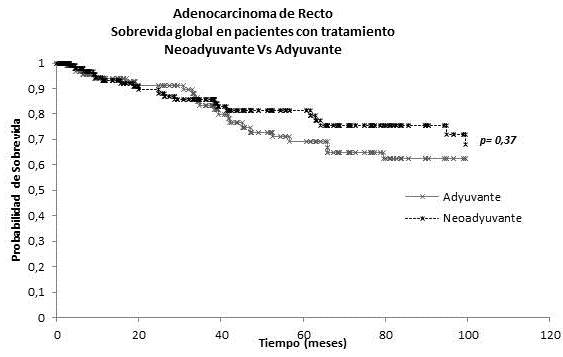
Figura 5.
Para caracterizar la población se utilizaron datos estadísticos como: media, mediana y desviación estándar. Para el análisis de sobrevida se utilizó el método estadístico de Kaplan Meier (16), a fin de obtener curvas de SG y SLE y el método empleado para comparación en la curvas fue el Long Rank Test. Para el seguimiento se utilizaron los datos de la historia clínica de RT o de Oncología Médica (ARSUVE); y con los pacientes incluidos en el estudio que no habían acudido a la consulta de RT, se realizó contacto directo con los médicos tratantes y médicos referentes, con los pacientes y/o familiares (vía telefónica y personalmente).

Figura 6
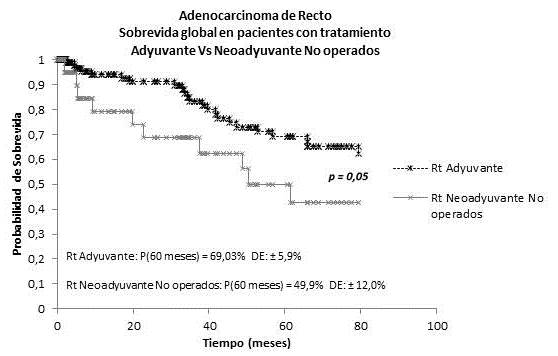
Figura 7.
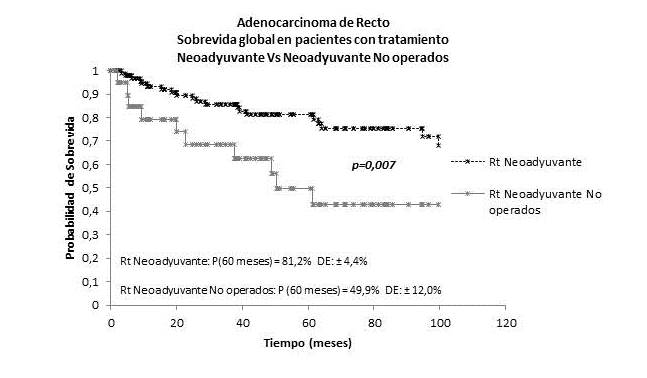
Figura 8.
El estado de los pacientes para el momento del análisis, se presenta en el Cuadro 2. Se puede observar que en el grupo de tratamiento adyuvante 54 pacientes (49,1 %) estaban vivos sin enfermedad (VSE), y 2 (1,8 %) murieron sin enfermedad (MSE), en aquellos sometidos a tratamiento neoadyuvante 57 (61,3 %) estaban VSE, y 6 (6,5 %) MSE y de los 20 pacientes sometidos a RT-QT neoadyuvante que no fueron operados, 6 (30 %) VSE, y 2 (10 %) MSE.
grupo de tratamiento adyuvante en 12 pacientes de 110 se practicó RTA, de ellos 6 están VSE y uno MSE, siendo la SG a los 50 meses de 68,6 % (Figura 9). Sólo 1 de los 93 pacientes del grupo neoadyuvante fue sometido a RTA y se encuentra VCE.
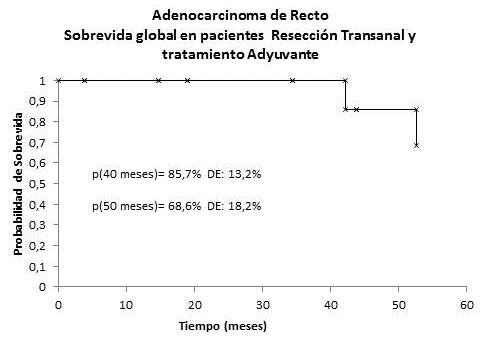
Figura 9.
Para la evaluación de la toxicidad se utilizó el sistema de clasificación del grupo de radioterapia oncológica (RTOG) y de la organización Europea para investigación y tratamiento del cáncer (EORTC) (18). En relación a las complicaciones agudas, las complicaciones gastrointestinales grado II-III fueron mayores en el grupo de pacientes que recibieron tratamiento adyuvante que en el neoadyuvante, 57 % vs. 45 % y sólo un paciente de cada grupo presentó toxicidad grado IV, una de ellas presentó fistula recto-vaginal y otro paciente pseudo-obstrucción intestinal. Las complicaciones hematológicas grado II-III fueron poco frecuentes solo se registraron en 10 % de los pacientes sometidos a tratamiento posoperatorio y en 5 % de los pacientes con tratamiento preoperatorio, en este grupo también se presentó toxicidad hematológica grado IV. Las complicaciones genitourinarias fueron poco frecuentes, no hubo complicaciones grado IV. La toxicidad en piel grado III fue sólo de 3 % en ambos grupos, no hubo toxicidad grado IV. No se registraron muertes relacionadas al tratamiento.
En cuanto a la toxicidad crónica gastrointestinal, en 2 pacientes del grupo adyuvante y en 1 del grupo neoadyuvante se presentó toxicidad grado III, con cuadro de obstrucción intestinal. Asimismo, en 2 pacientes del grupo de tratamiento adyuvante se presentó toxicidad grado IV, uno de ellos desarrolló una fistula recto-uretral con necrosis del recto inferior, este paciente recibió una dosis total de 6 070 cGy, después de RTA, y en el otro caso se presentó una fístula recto-vaginal; y en el grupo neoadyuvante se presentó un caso que desarrolló necrosis intestinal ameritando colostomía (Cuadro 4).
El estado de los pacientes para el momento del análisis, se presenta en el Cuadro 2. Se puede observar que en el grupo de tratamiento adyuvante 54 pacientes (49,1 %) estaban vivos sin enfermedad (VSE), y 2 (1,8 %) murieron sin enfermedad (MSE), en aquellos sometidos a tratamiento neoadyuvante 57 (61,3 %) estaban VSE, y 6 (6,5 %) MSE y de los 20 pacientes sometidos a RT-QT neoadyuvante que no fueron operados, 6 (30 %) VSE, y 2 (10 %) MSE.
En cuanto al CL de la enfermedad en el grupo neoadyuvante fue 72% vs. 52,7 % en el grupo adyuvante. Asimismo, en el 67,7 % de los pacientes sometidos a tratamiento preoperatorio no se observó recaída de la enfermedad a distancia vs., 47 % en el grupo de tratamiento posoperatorio. Es importante señalar que en alrededor del 40 % que fueron tratados con RT-QT adyuvante y en cerca del 20 % de los incluidos en el grupo con RT-QT neoadyuvante no se pudo conseguir información suficiente para evaluar el estado de la enfermedad. Por tanto no se pudo calcular cifras actuariales de recaída de la enfermedad. En cuanto a los 20 pacientes no sometidos a cirugía, en 8 (40 %) se presentó RL o persistencia de la enfermedad y en 20 % se evidenció metástasis a distancia (Cuadro 3)
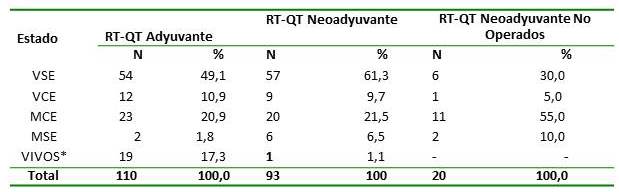
Cuadro 2
Estado de los pacientes de acuerdo al grupo de tratamiento
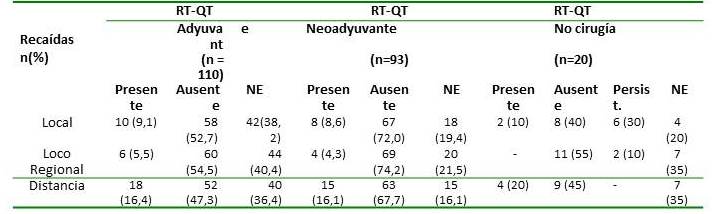
Cuadro 3.
Incidencia de recaídas local y a distancia en los tres grupos de tratamiento
NE: No se especifica Persist.: Persistencia
grupo de tratamiento adyuvante en 12 pacientes de 110 se practicó RTA, de ellos 6 están VSE y uno MSE, siendo la SG a los 50 meses de 68,6 % (Figura 9). Sólo 1 de los 93 pacientes del grupo neoadyuvante fue sometido a RTA y se encuentra VCE.
Para la evaluación de la toxicidad se utilizó el sistema de clasificación del grupo de radioterapia oncológica (RTOG) y de la organización Europea para investigación y tratamiento del cáncer (EORTC) (18). En relación a las complicaciones agudas, las complicaciones gastrointestinales grado II-III fueron mayores en el grupo de pacientes que recibieron tratamiento adyuvante que en el neoadyuvante, 57 % vs. 45 % y sólo un paciente de cada grupo presentó toxicidad grado IV, una de ellas presentó fistula recto-vaginal y otro paciente pseudo-obstrucción intestinal. Las complicaciones hematológicas grado II-III fueron poco frecuentes solo se registraron en 10 % de los pacientes sometidos a tratamiento posoperatorio y en 5 % de los pacientes con tratamiento preoperatorio, en este grupo también se presentó toxicidad hematológica grado IV. Las complicaciones genitourinarias fueron poco frecuentes, no hubo complicaciones grado IV. La toxicidad en piel grado III fue sólo de 3 % en ambos grupos, no hubo toxicidad grado IV. No se registraron muertes relacionadas al tratamiento.
En cuanto a la toxicidad crónica gastrointestinal, en 2 pacientes del grupo adyuvante y en 1 del grupo neoadyuvante se presentó toxicidad grado III, con cuadro de obstrucción intestinal. Asimismo, en 2 pacientes del grupo de tratamiento adyuvante se presentó toxicidad grado IV, uno de ellos desarrolló una fistula recto-uretral con necrosis del recto inferior, este paciente recibió una dosis total de 6 070 cGy, después de RTA, y en el otro caso se presentó una fístula recto-vaginal; y en el grupo neoadyuvante se presentó un caso que desarrolló necrosis intestinal ameritando colostomía (Cuadro 4).
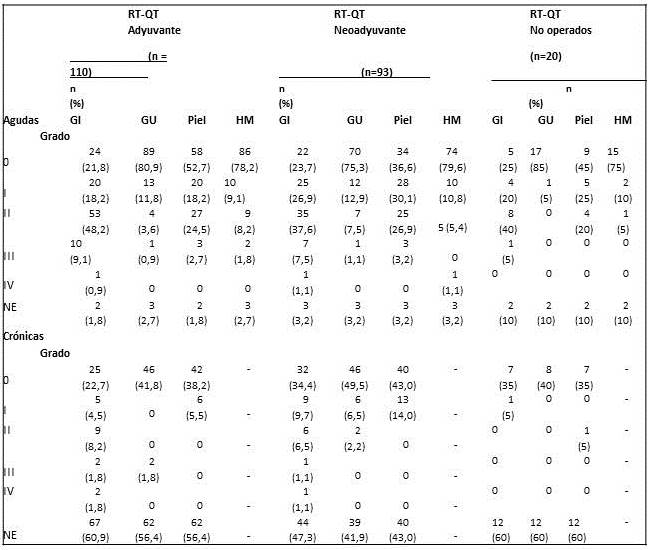
Cuadro 4
Toxicidad aguda y crónica relacionada al tratamiento
RT - QT: Radio - Quimioterapia RAP: Resección Abdominoperineal RTC 3D: Radioterapia conformada 3D N/E: No especificado RA: Resección Abdominal RTA :Resección Transanal RTIM: Radioterapia de Intensidad Modulada
DISCUSIÓN
La terapéutica del cáncer de recto está en evolución continua. No obstante, los adelantos en el área de diagnóstico de la enfermedad y en la aplicación de las modalidades de tratamiento: la cirugía arma fundamental, y de la RT y el tratamiento sistémico, aún no existe un tratamiento óptimo para esta afección.
En el presente trabajo se analizan los resultados retrospectivos en dos series de pacientes tratados con RT-QT neoadyuvante (93 pacientes) o RT-QT adyuvante (110 pacientes). Estos pacientes fueron referidos a nuestros centros de RT por diversos cirujanos y oncólogos médicos sin seguir un protocolo pre-establecido, por tanto la localización anatómica de la lesión rectal, y el estadio de la enfermedad no son del todo comparables. El tratamiento radiante en ambos grupos fue bastante similar, sin embargo, en la QT se utilizaron diversos esquemas de acuerdo al criterio de los oncólogos médicos.
Las bases del tratamiento adyuvante RT-QT se establecen con los estudios cooperativos realizados en los años 1980 y 1990. En el estudio del GTSG (10,19) pacientes con lesiones Dukes B y C fueron asignados aleatoriamente en 4 grupos cirugía sola, RT posoperatoria (4 000-4 800 cGy), QT posoperatoria (5FU+ MeCCNU), o combinación de RT-QT; solo en el grupo QT-RT hubo una diferencia significativa en la SLE y la SG en comparación con la cirugía, además en los dos grupos tratados con RT, se observó una disminución significativa en las RL, como sitio inicial de reactivación de la enfermedad. En el estudio Mayo/NCCTG (11) se incluyeron 204 pacientes con tumores con invasión profunda de la pared rectal o metástasis ganglionares, dividiéndolos en 3 grupos: cirugía sola, cirugía + RT (4 500-5 040cGy), o QT-RT, un ciclo de MeCCNU+5FU seguido de RT (4 500- 5 040 cGy) +5FU seguida de otro ciclo de MeCCNU+5FU; observándose mejoría en la SG y SLE y reducción significativa en la incidencia de RL y metástasis a distancia en los pacientes sometidos a QT-RT adyuvante. Posteriormente en dos estudios aleatorios con QT-RT adyuvante, se encontró que el MetilCCNU no produjo un efecto aditivo, cuando se combina con RT+5FU (20,21).
En el estudio de Noruega, en 136 pacientes con cáncer del recto (Dukes B y C) divididos aleatoriamente en 2 grupos: cirugía sola o RT posoperatoria (4 600 cGy) y 5FU en bolus administrado antes de las 6 fracciones de RT, se observó una reducción significativa en las RL, y mejoría en la sobrevida libre de recaída y en la SG (22).
El estudio del NSABP R01, incluyó 555 pacientes con cáncer del recto Dukes B o C resecado, los cuales se dividieron aleatoriamente en 3 grupos: observación, QT adyuvante sola (MetilCCNU, Vincristina y 5FU-MOF) y RT posoperatoria sola (4 600-4 700cGy). Se observó una mejoría en la SLE en el grupo tratado con QT comparado con cirugía sola o RT posoperatoria, y solo una mejoría marginal en la SG; no se observó reducción en las metástasis a distancia ni en las recidivas locales. En los pacientes tratados con RT se encontró una reducción en las RL, pero no hubo mejoría en la sobrevida comparada con cirugía sola (12).
En base en gran parte a estos ensayos clínicos, la conferencia de consenso del NIH en 1990, recomendó el uso de la QT y RT (4 500-5 500cGy) posoperatoria como tratamiento estándar, después de la resección quirúrgica en cáncer del recto estadios II y III. No se especificó el régimen de QT óptimo (13).
En las normas actuales del NCCN, se recomienda el tratamiento combinado de cirugía, RT a la pelvis y QT con regímenes a base de fluoropirimidinas, en el tratamiento de la mayoría de los pacientes con cáncer de recto estadio II y III (23). La capecitabina es equivalente al 5FU en el tratamiento combinado QT-RT perioperatorio (24). En cuanto al uso de otras drogas como el oxalipaltino, en conjunto con 5FU+RT o capecitabina+RT, el NCCN no recomienda actualmente su empleo en el tratamiento combinado RT-QT, debido al incremento en la toxicidad sin mejoría significativa en los resultados de sobrevida o recurrencias locales. Además del tratamiento combinado RT-QT, se recomienda la QT adyuvante en pacientes con cáncer del recto estadio II y III, con esquemas que contengan oxaliplatino, 5FU-leucovorina–oxaliplatino (FOLFOX) o capecitabina+oxaliplatino (CAPOX); otras opciones podrían incluir 5FU-leucovorina o capecitabina. La duración del tratamiento adyuvante (QT+RT seguido de QT adyuvante) no debe ser superior a 6 meses (23).
En cuanto a las técnicas de tratamiento radiante se recomienda el empleo de RT conformada con planificación 3D (RTC3D) con 3 a 4 campos con dosis de 4 500- 5 000cGy, en 25-28 fracciones a la pelvis. La radioterapia con intensidad modulada (RTIM) no se recomienda de rutina, sólo en caso de ensayos clínicos o en casos de re-irradiación y en ciertas localizaciones anatómicas (23,24).
El estudio del Intergrupo (GI INT 0144) (25) en el cual 1 917 pacientes con ADC del recto T3-4, N0, M0 o T1-4 N1-2,M0 después de resección quirúrgica fueron divididos aleatoriamente en 3 grupos: 1. 5FU en bolus por 2 ciclos de 5 días cada 28 días antes y después de la RT+5FU en infusión continua prolongada (ICP), 2. Grupo de ICP solamente, 5FU en ICP 42 días antes y 56 días después de la RT+5FU en ICP, 3) Grupo con 5FU en bolus+Leucovorina (LV) en 2 ciclos de 5 días antes y después de RT+5FU en bolus+LV (se administró levamisole en cada ciclo antes y después de RT). La toxicidad hematológica grado III-IV fue 49 % a 55 % en los grupos con 5 FU en bolus vs. 4 % en el grupo de 5FU en ICP, no encontrándose diferencias en la SG o SLE entre los 3 grupos a los 3 años. Las recidivas locales como primer sitio de recaída fueron 8 % en el grupo 1, 4,6 % en el grupo 2 y 7 % en el grupo 3.
El cambio hacia los esquemas de tratamiento neoadyuvante fue influenciado por el estudio fundamental realizado en Alemania (14), en el cual se incluyeron 823 pacientes T3-T4N+, los cuales fueron divididos aleatoriamente para recibir RT preoperatoria (5 040cGy con fracciones de 180 cGy/día) + 5FU en infusión continua (IC) seguida de cirugía con resección total del mesorecto (RTM) en 421 pacientes, vs., cirugía (RTM) seguida de RT posoperatoria (5 040 cGy con fracciones de 180 cGy/día + dosis adicional de 5 040 cGy) + 5FU (IC), en 402 pacientes. Aunque no se observó diferencia significativa en la SG a los 5 años, 76 % con RT+QT preoperatoria vs. 74 % con RT+QT posoperatoria, se encontró una diferencia significativa en las RL a los 5 años 6 % con tratamiento neoadyuvante vs. 13 % con tratamiento adyuvante (P=0,006). La toxicidad aguda fue mayor con RT+QT posoperatoria 40 % vs. 27 %, así como también la toxicidad crónica 14 % vs. 24 %. Además se logró preservación del esfínter en un mayor número de casos con tratamiento neoadyuvante, 39 % vs. 19 %. En una publicación más reciente se actualizaron los datos de este importante estudio; 799 pacientes elegibles, 404 en el grupo preoperatorio y 395 en el grupo posoperatorio. No se observó diferencia en la sobrevida a los 10 años 59,6 % en los pacientes tratados con RT+QT preoperatoria vs. 59,9 % con RT+QT posoperatoria. Se mantuvo la diferencia en las RL 7,1 % y 10,1 % en los grupos preoperatorio y posoperatorio, respectivamente (P=0,048), no habiendo diferencia en la incidencia de metástasis a distancia y en la sobrevida libre de enfermedad. Los autores plantean implementar tratamientos sistémicos más efectivos para mejorar los resultados de SG y reducir las metástasis a distancia (26).
El estudio de la NSABP R-03 comparó la RT-QT adyuvante vs., la RT-QT neoadyuvante en pacientes cT3-T4 N+. La QT consistió en 5FU y LV, y en la RT se administró una dosis de 4 500 cGy a la pelvis con reducción hasta 5 040 cGy. De un total de 254 pacientes, 123 fueron tratados con RT-QT preoperatoria y 131 con RT-QT posoperatoria. La SLE a los 5 años para el grupo de RT-QT preoperatoria fue de 64,7 % vs. 53,4 % del grupo de RT-QT posoperatoria (P=0,011) y la SG a los 5 años fue de 74,5 % en el grupo de RT-QT preoperatoria fue de 74,5 % vs. 65,6 % en el grupo de RT-QT posoperatoria (P=0,065). En el grupo de pacientes de RT-QT preoperatoria se alcanzó 15 % de respuestas patológicas completas y ninguno de ellos presentó recurrencias (27).
En un estudio coreano de 240 pacientes con cáncer de recto, T3 potencialmente resecable, cT4 o N+, se asignaron aleatoriamente en dos grupos: RT-QT preoperatoria y RT-QT posoperatoria. La RT-QT consistió en 5 000 cGy en 25 fracciones en concurrencia con capecitabina y RTM. Las características clínicas fueron similares en ambos grupos, excepto que en el grupo de QT-RT preoperatoria había mayor número de pacientes con lesiones de localización baja (<5 cm desde el margen anal) 60 % vs. 46 % en el grupo RT-QT posoperatoria (P=0,041). Las tasas de RL, SLE y SG a los 3 y 5 años fueron similares en ambos grupos, al igual que las toxicidades agudas y crónicas. Sin embargo, en pacientes con tumores de localización muy baja del grupo de RT-QT preoperatoria se obtuvo mayor tasa de preservación del esfínter comparado con el grupo de RT-
QT posoperatoria (68 % vs. 42 %, P= 0.008) (28).
Los resultados obtenidos en el presente trabajo revelan una SG a los 5 años en el grupo de RT-QT posoperatoria de 69,03 % vs. 81,24 % en el grupo de RT-QT preoperatoria, este resultado no fue estadísticamente significativo (P=0,37). La SLE a los 5 años fue de 80 % para el grupo de RT-QT preoperatorio vs. 56 % en los pacientes del grupo de RT-QT posoperatorio, esta diferencia si fue estadísticamente significativa (P=0,000392).
La mayoría de los pacientes pertenecientes al grupo de RT-QT preoperatoria presentaban lesiones rectales de localización baja, 56 (60 %) y 35 (37,7 %) tumores de recto alto o medio. La cirugía más comúnmente realizada fue la RA (58,1 %) y en un paciente se practicó RTA. En esta cohorte, en 55 pacientes (59,2 %) se pudo preservar el esfínter. Con respecto a las respuestas patológicas completas estas fueron reportadas en 12 pacientes (12,9 %). En relación al grupo de RT-QT posoperatoria fueron más frecuentes las lesiones del recto alto o medio, 69 pacientes (62,8 %) y de ellos 95 (86,4 %) acudieron a nuestros centros después de una RA o una RTA. Estos dos grupos no eran comparables en cuanto a la localización anatómica del tumor para poder evaluar la tasa de preservación del esfínter.
En relación a la toxicidad aguda en pacientes que reciben RT-QT adyuvante, en un análisis de 386 pacientes, 13 pacientes (4 %) desarrollaron enteritis aguda con síntomas como diarrea (68 %), con náuseas, vómitos y dolor abdominal en menor proporción. La enteritis crónica se diagnosticó en 18 pacientes (6 %) uno de ellos tuvo una lesión intestinal aguda. Se encontró proctitis crónica en 38 pacientes (12 %). La incidencia de las complicaciones intestinales se relacionó con la dosis, no observándose complicaciones con dosis media de 5 045 cGy, mientras que los pacientes que presentaron complicaciones recibieron una dosis promedio de 5 400 cGy (29). Kollmorgen y col., (30) en una serie de 100 pacientes tratados con RA encontraron que aquellos sometidos a QT-RT adyuvante al ser comparados con aquellos sometidos a cirugía solamente presentaron mayor frecuencia de evacuaciones en general, evacuaciones nocturnas, incontinencia fecal, urgencia para la evacuación y uso de pañales. En el estudio del Intergrupo (GI INT 0144) (25) aunque la toxicidad hematológica fue menor en los pacientes tratados con 5FU en ICP, se encontró que la toxicidad aguda intestinal con diarreas severas fue del 21 % en pacientes tratados con RT a la pelvis más 5FU en ICP vs. 13 % con 5FU en bolus y más frecuentes en pacientes tratados con RAP (31).
La RT-QT neoadyuvante, por lo general, no aumenta las complicaciones perioperatorias (14). Sin embargo, se conoce bien que la incontinencia fecal ocurre mayormente en pacientes que reciben RT-QT preoperatoria y luego RTM, sin embargo, no hubo efectos adversos en la función eréctil o urinaria (32). La disfunción sexual también es mayor en pacientes irradiados sin embargo, este efecto secundario se relaciona directamente con el tipo de cirugía, siendo más frecuente en aquellos pacientes sometidos a RAP (33). Otra de las complicaciones crónicas son las fracturas del sacro las cuales se presentaron en mayor proporción en el sexo femenino, en mujeres mayores de 60 años y en aquellos que padecían de osteoporosis (34).
Al comparar las complicaciones de la RT-QT preoperatoria vs., la RT-QT posoperatoria, Sauer y col., destacan que la toxicidad gastrointestinal grado III-IV fueron similares en ambos grupos, y la tasa de morbilidad posoperatoria no fue mayor en los pacientes sometidos a terapia neoadyuvante. Sin embargo, un pequeño pero significante grupo de pacientes de RT-QT neoadyuvante presentó menos estenosis en la anastomosis comparado con aquellos que recibieron RT-QT posoperatoria (2,7 % vs. 8,5 %) (14).
En la presente serie de 223 pacientes, las complicaciones agudas gastrointestinales grado II-III fueron mayores en el grupo de pacientes que recibieron tratamiento adyuvante que en el neoadyuvante, 57 % vs., 45 % y sólo un paciente de cada grupo presentó toxicidad grado IV, una de ellas presentó fistula recto-vaginal y otro paciente pseudo-obstrucción intestinal. Las complicaciones hematológicas y genitourinarias fueron poco frecuentes. No se presentaron muertes relacionadas al tratamiento. En cuanto a las complicaciones crónicas gastrointestinales, 2 pacientes del grupo adyuvante y en 1 del grupo neoadyuvante presentaron toxicidad grado III, con cuadro de obstrucción intestinal. Asimismo, en 2 pacientes del grupo de tratamiento adyuvante se presentó toxicidad grado IV, uno de ellos desarrolló una fistula recto-uretral con necrosis del recto inferior, este paciente recibió una dosis total de 6 070 cGy, después de RTA, y en el otro caso se presentó una fístula recto-vaginal; y en el grupo neoadyuvante se presentó un caso que desarrolló necrosis intestinal ameritando colostomía. Dada la naturaleza del presente estudio retrospectivo, es probable que exista un sub-registro en la incidencia de complicaciones, sobre todo en las crónicas, porque no se pudo hacer un estudio detallado de la toxicidad.
En nuestro país en el año 2009, Raúl Vera y col., realizaron un estudio retrospectivo de 50 pacientes con carcinoma de recto, de ellos 33 recibieron tratamiento posoperatorio y 17 preoperatorio. El 64 % recibió radioterapia a la pelvis, a dosis de 4 500- 5 540 cGy con fracciones de 180/día durante 5-6 semanas concurrente con 5FU en ICP y 36 % también recibió 5FU en bolus con bajas dosis de leucovorina. La mayoría de los pacientes eran estadio III. Las toxicidades grado III-IV más frecuentes en el grupo tratado con 5FU en IC concurrente con RT fueron diarrea y enteritis; en los tratados con 5FU en bolus y leucovorina concurrente con RT fueron diarrea, radiodermatitis y neutropenia. No hubo muertes asociadas al tratamiento. Al 60 % se les realizó RA. El porcentaje de recaídas locales fue 12 % y a distancia 24 %. Para el momento del análisis el 42 % de los pacientes se encontraban vivos sin enfermedad y la principal causa de falla del tratamiento fue la recaída a distancia (35).
Por otra parte, también se ha presentado la experiencia de otras instituciones con el uso de la RT-QT preoperatoria en cáncer de recto en nuestro país, habiéndose reportado respuestas patológicas completas del orden de 50 % después de tratamiento neoadyuvante (36).
En la actualidad el tratamiento estándar de pacientes con diagnóstico de carcinoma de recto localmente avanzado, consiste en RT-QT preoperatoria seguida de RTM y QT posoperatoria. Este enfoque, por lo general, aporta beneficios en cuanto a las tasas de control local, sin repercusión alguna en la SG y la sobrevida libre de enfermedad a distancia. En este sentido y con objeto de mejorar las posibilidades de curación de la enfermedad, se han intensificado los esquemas de QT preoperatoria previo al tratamiento concurrente RT- QT, lo que se ha denominado terapia neoadyuvante total (TNT) (37)
Un estudio español (38) incluyó 108 pacientes con cáncer de recto localmente avanzado divididos aleatoriamente en dos grupos: A. QT+RT preoperatoria (CAPOX+RT) seguida de cirugía y cuatro ciclos de CAPOX adyuvante y B. TNT iniciando con CAPOX (capecitabina, oxaliplatino) de inducción luego QT con CAPOX en concurrencia con RT seguido de cirugía, no observándose diferencias entre ambos grupos en cuanto a SG, Sobrevida libre de recaídas, respuestas patológicas completas y márgenes de resección negativos; pero con mayor toxicidad 3 y 4 en el grupo de QT posoperatoria que en el de QT de inducción. Recientemente en el año 2015 (39) con un seguimiento de 69,5 meses estos resultados se han mantenido, en cuanto a la toxicidad grado 3-4, 54 % con QT posoperatoria vs.19 % con QT de inducción (P= 0,0004).
La experiencia del Hospital Memorial Sloan Kettering Cancer Center(40) reunió 61 pacientes tratados con QT de inducción con 7 ciclos de FOLFOX: ácido folínico, fluorouracilo y oxaliplatino). En 4 se observó excelente respuesta a la QT y fueron directamente a cirugía (RTM), los 57 restantes recibieron QT-RT (dosis: 5 000 cGy), sólo 12 no fueron sometidos a cirugía por distintas causas. Del total de 61 pacientes, 22 (36 %) alcanzaron respuestas completas, 13 patológicas y 9 clínicas. De los 49 pacientes sometidos a cirugía todos fueron R0 (100 %), 23 (47 %) alcanzaron reducción del tumor >90 % y 13 (27 %) respuestas patológicas completas. En una publicación más reciente de esta misma institución se reportan 628 pacientes, divididos en dos grupos: 320 con QT+RT preoperatoria y posteriormente QT adyuvante y otro con 308 sometidos a, QT de inducción con FOLFOX o CAPOX seguida de QT+RT preoperatoria. La tasa de respuestas completas (RC) que incluyeron RC patológica y RC clínica a los 6 meses del tratamiento, fue del 21 % en el grupo QT adyuvante y de 36 % en TNT. La mediana de seguimiento fue de 40 meses en el grupo de QT adyuvante y de 23 meses en TNT. No hubo diferencias estadísticamente significativas en la SLE a distancia entre los dos grupos. Los autores concluyen que la TNT, facilita la administración del tratamiento sistémico planificado, y dada su alta tasa de RC puede ser de utilidad como parte de una estrategia de tratamiento no quirúrgico dirigida a la preservación de órganos (37).
En vista de la morbilidad de la cirugía radical (RAP) en los pacientes con carcinoma de recto bajo se está desarrollando una nueva estrategia terapéutica para omitir el tratamiento quirúrgico en casos que presentan respuestas completas al tratamiento combinado de QT y RT. En este sentido los primeros trabajos fueron realizados en Brasil (41), Habr-Gama y col., reportaron su experiencia más reciente en 183 pacientes tratados con QT a base de 5FU y RT 5 040- 5 400 cGy. De estos, 90 (49 %) desarrollaron respuesta clínica completa, y fueron sometidos a un protocolo de vigilancia activa, difiriendo la cirugía, observando recurrencias locales en 28 (31 %) y recidivas a distancia en 13 pacientes (14 %), con un tiempo de seguimiento medio de 60 meses. En 26 pacientes (93 %) se practicó cirugía de rescate con una sobrevida libre de recaída local a los 5 años de 69 % para todos los pacientes con recaídas locales y 94 % en aquellos sometidos a cirugía de rescate. La sobrevida cáncer específica a los 5 años fue de 91 % y la sobrevida libre de enfermedad 68 % para todos los pacientes con respuestas clínicas completas no tratados con cirugía inmediata (42).
Posteriormente se han realizado en EE.UU y en Europa, protocolos similares de vigilancia activa en otras instituciones que confirman la utilidad de esta estrategia terapéutica para preservación del órgano (43,44). Igualmente en nuestro país, Gil A y col., reportaron la primera experiencia venezolana en manejo no quirúrgico del cáncer de recto con repuesta clínica completa posterior a terapia neoadyuvante, en 11 pacientes con una mediana de seguimiento de 52 meses no se registró ninguna recaída locorregional ni a distancia, la supervivencia por causa específica fue de 100 % (45).
Igualmente en un meta-análisis reciente, se concluyó que no había diferencia en la SG y la SLE a los 5 años en pacientes con cáncer de recto localmente avanzado tratados con o sin manejo quirúrgico inicial después de respuesta clínica completa posterior a la RT-QT (45).
En la presente serie se analizaron 20 pacientes que recibieron tratamiento neoadyuvante y no fueron sometidos a cirugía, por diversas causas, comorbilidades, edad avanzada o algunos de ellos rehusaron el tratamiento quirúrgico. La SG fue 50 % a los 5 años, resultados inferiores a la sobrevida de los cohortes de tratamiento adyuvante (69,03 %) y neoadyuvante (81,2 %). Este grupo no puede ser comparado con los pacientes en los cuales se demuestra remisión completa después de tratamiento con RT-QT y son susceptibles a vigilancia activa.
REFERENCIAS
1. Arnold M, Sierra MS, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global patterns and trends in colorectal cancer incidence and mortality. Gut. 2017r;66(4):683-691.
2. Siegel RL, Miller KD, Jemal A. Cancer Statistics, 2018. Ca Cancer J Clin. 2018;68:7-30.
3. Capote L. Resumen de las estadísticas de cáncer en el año 2012. Disponible en: URL: http://www.oncologia.org.ve/site/userfiles/svo/Estad%C3%ADsticas%20de%20c% C3%A1ncer%20en%20el%202012.pdf.
4. Libutti SK, Willett CG, Saltz LB, Levine RA. Cancer of the rectum. En: Devita VT, Lawrence TS, Rosenberg SA, editores. Cancer Principles and practice of oncology. 10a edición. Filadelfia:Wolters Kluwer Health; 2015.
5. Dwight RW, Higgins GA, Roswit B, LeVeen HH, Keehn RJ. Preoperative radiation and surgery for cancer of the sigmoid colon and rectum. Am J Surg. 1972;123:93-103.
6. Kligerman MM, Urdaneta N, Knowlton A, Vidone R, Hartman PV, Vera R. Preoperative irradiation of recto sigmoid carcinoma including its regional lymph nodes. Am J Roentgenol Radium Ther Nucl Med. 1972;114(3):498-503.
7. Stearns MW Jr, Deddish MR, Quan SHQ, Leaming RH. Preoperative roentgen therapy for cancer of the rectum and recto-sigmoid. Surg Gynecol Obstet. 1974;138:584-586.
8. Mohiuddin M, Marks G, Kramer S, Pajak . Adjuvant radiation therapy for rectal cancer. Int J Radiat Oncol Biol Phys. 1984;10:977-980.
9. Tepper JE, Cohen AM, Wood WC, Orlow EL, Hedberg SE. Postoperative radiation therapy of rectal cancer. Int J Radiat Oncol Biol Phys. 1987;13:5-10.
10. Gastrointestinal Tumor Study Group. Prolongation of the disease-free interval in surgically treated rectal carcinoma. N Engl J Med. 1985;312:1465-1472.
11. Krook JE, Moertel CG, Gunderson LL, Wieand HS, Collins RT, Beart RW, et al. Effective surgical adjuvant therapy for high-risk rectal carcinoma. N Engl J Med. 1991; 324:709-715.
12. Fisher B, Wolmark N, Rockette H, Redmond C, Deutsch M, Wickerham DL, et al. Postoperative adjuvant chemotherapy or radiation therapy for rectal cancer: Results from NSABP protocol R-01. J Natl Cancer Inst. 1988;80:21-29.
13. [No author´s listed]. NIH consensus conference. Adjuvant therapy for patients with colon and rectal cancer. JAMA. 1990;264:1444-1450.
14. Sauer R, Becker H, Hohenberger W Rödel C, Wittekind C, Fietkau R, et al. Preoperative vs. postoperative chemo radiotherapy for rectal cancer. N Engl J Med. 2004;351:1731-1740.
15. Cercek A, Roxburgh CSD, Strombom P, Smith JJ, Temple LKF, Nash GM, et al. Adoption of total neoadjuvant therapy for locally advanced rectal cancer. JAMA Oncol. 2018;4(6):e180071.
16. Matthews DE, Farewel VT. Using and understanding medical statistics. 4a edición. Londres: Karger AG; 2007.
17. Amin, MB, Edge S, Greene F, Byrd DR, Brookland RK, Kay M, et al. Editores. AJCC Cancer Staging Manual. 8a edición. Washington: Springer; 2017.
18. Rockwell S, Collingridge DR. Principios de Radiobiología. En: Urdaneta N, Vera A, Peschel RW, Wilson LD. Radioterapia oncológica enfoque multidisciplinario. Caracas: Disinlimed; 2009.
19. Douglass HO Jr, Moertel CG, Mayer RJ, Thomas PR, Lindblad AS, Mittleman A, et al. Survival after postoperative combination treatment of rectal cancer. N Engl J Med. 1986;315(20):1294-1295.
20. [No author´s listed]. Radiation therapy and fluorouracil with or without semustine for the treatment of patients with surgical adjuvant adenocarcinoma of the rectum. Gastrointestinal Tumor Study Group. J Clin Oncol. 1992;10:549-557.
21. O’Connell M, Wieand H, Krook J, Martenson, J, Macdonald J, Rich T, et al. Lack of value for methyl CCNU (MeCCNU) as a component of effective rectal cancer surgical adjuvant therapy. Interim analysis of intergroup protocol 86-47-51. Prog Proc Am Soc Clin Oncol. 1991;abst134.
22. Tveit KM, Guldvog I, Hagen S, Trondsen E, Harbitz T, Nygaard K, et al. Randomized controlled trial of postoperative radiotherapy and short-term time-scheduled 5-fluorouracil against surgery alone in the treatment of Dukes B and C rectal cancer. Norwegian Adjuvant Rectal Cancer Project Group. Br J Surg. 1997;84(8):1130-1135.
23. NCCN Clinical practical guidelines in oncology. (NCCN Guidelines). Disponible en: URL: https://www.nccn.org/professionals/physician_gls/pdf/rectal.pdf.
24. Hofheinz RD, Wenz F, Post S, Matzdorff A, , Laechelt S, Hartmann JT, Müller L, et al. Chemo radiotherapy with capecitabine versus fluorouracil for locally advanced rectal cancer: A randomized, multicenter, non-inferiority, phase 3 trial. Lancet Oncol. 2012;13(6):579-588.
25. Smalley SR, Benedetti JK, Williamson S, Robertson JM, Estes NC, Maher T, et al. Phase III trial of fluorouracil-based chemotherapy regimens plus radiotherapy in postoperative adjuvant rectal cancer: GI INT 0144. J Clin Oncol. 2006;24(22):3542-3547.
26. Sauer R, Torsten L, Merkel S, Fietkau R, Hohenberger W, Hess C, et al. Preoperative versus postoperative chemo radiotherapy for locally advanced rectal cancer: Results of the German CAO/ARO/AIO-94 randomized phase III trial after a median follow-up of 11 years. J Clin Oncol. 2012;30:1926-1933.
27. Roh MS, Colangelo LH, O'Connell MJ, Yothers G, Deutsch M, Allegra CJ, et al. Preoperative multimodality therapy improves disease-free survival in patients with carcinoma of the rectum: NSABP R- 03. J Clin Oncol. 2009;27:5124-5130.
28. Park JH, Yoon SM, Yu CS, Kim JH, Kim TW, Kim JC. Randomized phase 3 trial comparing preoperative and postoperative chemo radiotherapy with capecitabine for locally advanced rectal cancer. Cancer. 2011;117:3703-3712.
29. Miller AR, Martenson JA, Nelson H, Schleck CD, Ilstrup DM, Gunderson LL, et al. The incidence and clinical consequences of treatment-related bowel injury. Int J Radiat Oncol Biol Phys. 1999;43:817-825.
30. Kollmorgen CF, Meagher AP, Wolff BG, Pemberton JH, Martenson JA, Illstrup DM. The long-term effect of adjuvant postoperative chemo radiotherapy for rectal carcinoma on bowel function. Ann Surg. 1994;220:676-682.
31. Miller RC, Sargent DJ, Martenson JA, Macdonald JS, Haller D, Mayer RJ, et al. Acute diarrhea during adjuvant therapy for rectal cancer: A detailed analysis from a randomized intergroup trial. Int J Radiat Oncol Biol Phys. 2002;54:409-413.
32. Loos M, Quentmeier P, Schuster T, Nitsche U, Gertler R, Keerl A, et al. Effect of preoperative radio (chemo) therapy on long-term functional outcome in rectal cancer patients: A systematic review and meta-analysis. Ann Surg Oncol. 2013;20:1816-1828.
33. Hendren SK, O'Connor BI, Liu M, Asano T, Cohen Z, Swallow CJ, et al. Prevalence of male and female sexual dysfunction is high following surgery for rectal cancer. Ann Surg. 2005;242(2):212-223.
34. Kim HJ, Boland PJ, Meredith DS, Lis E, Zhang Z, Shi W, et al. Fractures of the sacrum after chemo radiation for rectal carcinoma: Incidence, risk factors, and radiographic evaluation. Int J Radiat Oncol Biol Phys. 2012;84:694-699.
35. Vera GR, Sucre C, Arbona RE, Vivas L, Salazar H, Rosales T, et al. Tratamiento con radioterapia y quimioterapia en pacientes con carcinoma de recto 10 años de evaluación. Rev Venez Oncol. 2009;21(3):138-145.
36. Figueroa M, Briceño J, Puerta D, Del Valle W, Hurtado M, Sánchez N, et al. Radioterapia y quimioterapia preoperatoria en cáncer de recto. 2015. Rev Venez Oncol. 2015; 27(1):11-21.
37. Fernández-Marto C, Pericay C, Aparicio J, Salud A, Safont M, Massuti B, et al. Phase II, randomized study of concomitant chemo radiotherapy followed by surgery and adjuvant capecitabine plus oxaliplatin (Capox) compared with induction Capox followed by concomitant chemo radiotherapy and surgery in magnetic resonance imaging defined, locally advanced rectal cancer: Grupo Cancer de Recto 3 Study. J Clin Oncol. 2010;28:859-865.
38. Fernandez-Martos C, Garcia-Albeniz X, Pericay C, Maurel J, Aparicio J, Montagut C, et al. Chemo radiation, surgery and adjuvant chemotherapy versus induction chemotherapy followed by chemo radiation and surgery: Long-term results of the Spanish GCR-3 phase II randomized trial†. Ann Oncol. 2015;26(8):1722-1728.
39. Cercek A, Goodman KA, Hajj C, Weisberger E, Segal NH, Reidy-Lagunes DL, et al. Neoadjuvant chemotherapy first, followed by chemoradiation and then surgery, in the management of locally advanced rectal cancer. J Natl Compr Canc Netw. 2014;12(4):513-519.
40. Habr-Gama A, Perez RO, Nadalin W, Sabbaga J, Ribeiro U Jr, Silva e Sousa AH Jr, et al. Operative versus no operative treatment for stage 0 distal rectal cancer following chemo radiation therapy: Long- term results. Ann Surg. 2004 ;240(4):711-717.
41. Habr-Gama A, Gama-Rodrigues J, São Julião GP, Proscurshim I, Sabbagh C, Lynn PB, et al. Local recurrence after complete clinical response and watch and wait in rectal cancer after neoadjuvant chemo radiation: Impact of salvage therapy on local disease control. Int J Radiat Oncol Biol Phys. 2014;88:822-828.
42. Maas M, Beets-Tan RG, Lambregts DM, Lammering G, Nelemans PJ, Engelen SM, et al. Wait-and-see policy for clinical complete responders after chemo radiation for rectal cancer. J Clin Oncol. 2011;29(35):4633-4640.
43. Smith J, Ruby JA, Goodman KA, Saltz LB, Guillem JG, Weiser MR, et al. Non operative management of rectal cancer with complete clinical response after neoadjuvant therapy. Ann Surg. 2012;256(6):965-972.
44. Gil A, Delgado R, Russo L. Primera experiencia venezolana en manejo no quirúrgico del cáncer de recto con respuesta clínica completa posterior a terapia neoadyuvante. Rev Venez Oncol. 2017;29(1):65-75.
45. Fiorica F, Trovò M, Anania G, Marcello D, Di Benedetto F, Marzola M, et al. Is it possible a conservative approach after radio chemotherapy in locally advanced rectal cancer (LARC)? A systematic review of the literature and meta-analysis. J Gastrointest Canc. 2017; doi: 10.1007/s12029-017-0041-8.
Notas de autor
rreyes@radioterapia.com.ve
Información adicional
Reconocimiento: Trabajo ganador Premio Dr. Fernando Rodríguez Montalvo. 2018