RADIOTERAPIA EN EL TRATAMIENTO DEL QUISTE ANEURISMÁTICO ÓSEO. REPORTE DE 2 CASOS REVISIÓN DE LA LITERATURA.
RADIOTERAPIA EN EL TRATAMIENTO DEL QUISTE ANEURISMÁTICO ÓSEO. REPORTE DE 2 CASOS REVISIÓN DE LA LITERATURA.
Revista Venezolana de Oncología, vol. 31, núm. 3, 2019
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 12 Febrero 2019
Revisado: 18 Marzo 2019
Aprobación: 14 Mayo 2019
Resumen: OBJETIVO: Reportar nuestra experiencia en el uso de radioterapia en el tratamiento de dos pacientes con quistes óseos aneurismáticos y realizar una revisión de la bibliografía más reciente. MÉTODO: Se realizó una revisión retrospectiva de dos pacientes tratados con radioterapia. El primer paciente masculino de 15 años de edad con lesión en C2 irresecable tratado con RTC3D 2 000 cGy dosis total a 200 cGy/día, y la segunda paciente femenina de 18 años con lesión a nivel del sacro irresecable, tratada con radioterapia intensidad modulada con arcos volumétricos, dosis total 2 600 cGy a 200 cGy/día. Tiempo de seguimiento 10 y 4 años respectivamente. RESULTADOS: En ambos pacientes se logró el control local de la enfermedad sin complicaciones agudas y crónicas. Aunque la cirugía es el tratamiento de elección en esta afección, la revisión de la literatura demuestra la efectividad de la radioterapia en el quiste óseo como tratamiento único o adyuvante en aquellas lesiones irresecables, no susceptibles a la cirugía o recidivas con posibilidades de control local del 50 % al 100 % CONCLUSIONES: La radioterapia es un tratamiento efectivo y seguro en estos casos como complemento a la cirugía en casos de resección incompleta, recidivas o lesiones irresecables. Las dosis recomendadas oscilan entre 2 000 a 3 000 cGy con fracciones de 180 a 200cGy diarios y menores a 2 000cGy en edad pediátrica.
Palabras clave: Radioterapia, quiste, aneurismático, hueso, tratamiento.
Abstract: OBJECTIVE: Report our experience in the treatment of two patients with diagnostic of aneurysmal bone cysts treated with radiation therapy and we present a review of the most recent literature. METHOD: Retrospective review of two patients with aneurysmal bone cysts treated with radiation therapy. The first patient a fifteen years old male with unresectable lesion in C2, treated with 3DCRT, received 2 000 cGy in two weeks with 200 cGy daily fractions; second patient eighteen years old female unresectable lesion in the sacrum, treated with modulated intensity radiation and volumetric arc, with 2 600 cGy using 200 cGy daily fractions. Follow up time 10 and 4 years respectively. RESULTS: In both patients local control of the ABC was obtained without acute or chronic complications. Although surgery is the gold standard in the treatment of ABC, literature review confirms the effectiveness of radiation as a primary or adjuvant treatment, in the management of this disease, in unresectable lesions or not amenable to surgery or in recurrences, with local control rates 50 to 100 %. CONCLUSION: Radiotherapy is effective and safe in the treatment of ABC, in unresectable lesions or as adjuvant to surgery in cases of incomplete resection or in recurrences of the disease. Recommended doses oscillate between 2 000-3 000 cGy with 180 to 200 cGy daily fractions, and bellow 2 000 cGy in pediatrics patients.
Keywords: Radiotherapy, aneurismal, bone, cyst, treatment.
INTRODUCCIÓN
El quiste aneurismático óseo (QAO) es una lesión ósea benigna lítica compuesta por conductos llenos de sangre separados por tabiques fibrosos (1) fue descrito por primera vez en 1942 por Jaffe y Lichtenstein, llamándolos así por su analogía con los aneurismas de las arterias usando el término quístico para enfatizar su localización intra-ósea (2). Sin embargo, estas lesiones no son ni aneurismáticas, ni quísticas, puesto a que no son quistes verdaderos y carecen de pared endotelial, pero pueden ser expansivas produciendo cavidades dentro del hueso, y se encuentran revestidos por fibroblastos proliferativos, células gigantes y hueso trabecular (3).
Antes se creía que se formaban por el incremento de la presión venosa que causaba extravasación de células y contenido sanguíneo en una especie de quiste o espacio vacío dentro del hueso. La etiología y patogénesis de esta afección no está bien dilucidada, se ha considerado que no es una neoplasia verdadera, sin embargo, se compone de un proceso hemorrágico e hiperplásico (1). Pero recientemente se ha identificado una alteración en el genTRE17/USP6 (ubiquitina proteasa específica) que define al menos un grupo de QAO como una lesión neoplásica primaria (4). El QAO se puede presentar como una lesión primaria, o en otras ocasiones en un 29 %-57 % como secundaria acompañada como otras lesiones tales como: tumores de células gigantes o enfermedades propios del hueso como ontogénesis imperfecta, displasia fibrosa, condroblastoma, fibroma condromixoide, fibroma no osificante, condrosarcoma, fibromixoma, fibrosarcoma, histiocitoma fibroso, granuloma eosínofílico, osteoblastoma,osteosarcoma, entre otras (1).
Los QAO representan alrededor del 1 % al 1,5 % de todas las lesiones óseas, aparecen de forma más frecuente en las primeras dos décadas de la vida, y es ligeramente más común en el sexo femenino con una tasa de 1,2 a 1,31. Puede localizarse en cualquier parte ósea, con predilección por las metáfisis de los huesos largos en un 60 %- 80 % de todos los casos, sobre todo en los miembros inferiores (fémur y tibia) el 3 % - 30 % de los casos, se localiza en la columna vertebral siendo más común la región cervical y dorsal (1).
En el diagnóstico, la radiografía convencional sigue siendo de importancia, usualmente estas lesiones expansivas osteolíticas en los huesos largos muestran un contorno ovoide. La mayoría se localiza en la metáfisis y usualmente sin extensión a la epífisis. Por lo general, presentan tabiques que van disminuyendo de la periferia a la región central de la lesión, sin embargo, en las vértebras es raro ver los tabiques pero se observan trabéculas en 20 % a 25 % de los casos. Hoy en día la tomografía computarizada (TC) permite ver los tejidos blandos al igual que la resonancia magnética, sin embargo, la TC es mejor para observar la reacción tisular perióstica (1,5). El uso de los estudios angiográficos muestra la gran vascularización que se observa en la periferia de la lesión (1). El gammagrama óseo usualmente muestra incremento del radio trazador en la periferia de la lesión con disminución en la porción central de la misma, y aunque no es específico para distinguir este tipo de lesión, puede ser de ayuda para distinguirla de un tumor maligno (6).
Aunque no existe un sistema de clasificación por estadios comúnmente aceptado, el sistema propuesto por Enneking y la sociedad de tumores músculo esqueléticos, podría ser de utilidad: estadio I latente: permanece estático y regresa espontáneamente. Estadio II activo: de crecimiento progresivo sin destrucción cortical. Estadio III: localmente agresivo de crecimiento progresivo con destrucción cortical significativa (1,7).
En el tratamiento del QAO existen varias opciones terapéuticas con buenos resultados, sin embargo, no existen pautas establecidas en su abordaje debido a ser una patología poco frecuente. El tratamiento quirúrgico ha sido la modalidad de elección, el curetaje aunque usado frecuentemente se acompaña de una alta tasa de recurrencia, por lo tanto debe asociarse a un tratamiento adyuvante (1,8). La resección amplia si es posible de realizar produce una tasa control local mayor del 90 % (1). Otras modalidades empleadas han sido la escleroterapia, embolización arterial, inyecciones de agentes citotóxicos, criocirugía, bifosfonatos entre otras. Recientemente se ha empleado la terapia molecular dirigida con un inhibidor del RANKL, para contrarrestar la actividad osteoclástica del QAO, la cual podría ser un tratamiento novedoso de utilidad (1,8,9,10,11).
La radioterapia es un tratamiento de utilidad que puede emplearse en casos seleccionados no susceptibles a tratamiento quirúrgico como tratamiento único o adyuvante a la cirugía (1).
El objetivo del presente trabajo es presentar nuestra experiencia en el tratamiento de dos pacientes con QAO sometidos a radioterapia y hacer una revisión de la literatura.
CASO 1
Adolescente masculino de 15 años de edad, quien en enero de 2008 presentó dolor y dificultad para la lateralización del cuello. En la TC se observó lesión expansiva a nivel de C2 multilobulada y heterogénea con extensión hacia el arco lateral del pedículo y partes blandas paravertebrales de lado izquierdo. Evaluado por un cirujano de cabeza y cuello, se consideró una lesión irresecable. El diagnóstico radiológico fue compatible con QAO. Es referido a la unidad de Radioterapia Oncológica del Instituto Médico La Floresta, Estado Miranda.
Se realiza simulación con máscara termoplástica inmovilizadora. Se planifica tratamiento con técnica de radioterapia conformada 3D, utilizando campos laterales opuestos y fotones de 6 MV dirigidos a la lesión a nivel de la cervical 2 (C2). Recibió una dosis total de 2 000 cGy, en dos semanas, con 10 fracciones diarias. Desde el 28/04/08 al 09/05/08. La tolerancia fue satisfactoria (Figura 1). El paciente ha evolucionado favorablemente en el último control de febrero 2014, la lesión en C2 se había reducido. En el último control clínico de abril de 2015 estaba asintomático, sin alteraciones al examen físico (Figura 2). Fue contactado por vía telefónica en agosto de 2018 y no refiere síntomas.
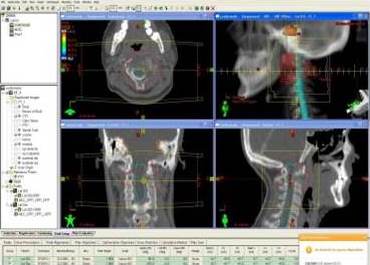
Figura 1
Imágenes del sistema planificación, se aprecia un corte en los 3 planos (axial, coronal y sagital) con la delimitación de la lesión macroscópica y las proyecciones de ambos campos laterales opuestos (derecho e izquierdo).
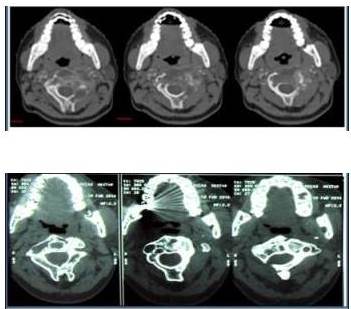
Figura 2.
Imágenes comparativas de tomografía donde se observa mejoría a nivelradiológicodada por la disminución del componente heterotópico de la lesión y formación del callo óseo.
2008 antes de la radioterapia y 2014 después de la radioterapia
CASO 2
Paciente femenina de 18 años de edad, con dolor urente en región lumbar bilateral de fuerte intensidad asociado a hipoestesias en ambos miembros inferiores de 4 años de evolución (desde el 2010). Se realiza RM de pelvis que muestra lesión en L5 y S1 que condiciona estrechez del canal medular. Se realiza biopsia la cual fue compatible con QAO. Fue evaluado por neurocirujanos que intentan resecar y embolizar en dos tiempos quirúrgicos los cuales no se pudieron realizar por sangrado durante el acto operatorio, referida al Centro Integral de Oncología Servicio de Radioterapia Raúl Vera en Clínica Guerra Méndez Estado Carabobo.
Se realiza simulación en posición prona con dispositivo de inmovilización tipo Belly-Board® que consiste en tablero con abertura central donde descansa el abdomen del paciente y condiciona un desplazamiento de las asas intestinales alejándolas del campo de irradiación. Se planifica radioterapia externa con técnica de arcos volumétricos modulados dirigidos a lesión en L5-S1 (Figura 3), con dos arcos con fotones de 6 MV a 200 cGy/día hasta 2 600 cGy en 13 aplicaciones desde el 21/5/14 al 6/6/14. Se evalúa la paciente en agosto de 2018 encontrándose sin síntomas ni alteraciones al examen físico, sin complicaciones, se realiza tomografía y resonancia con notable mejoría (Figura 4 y 5).
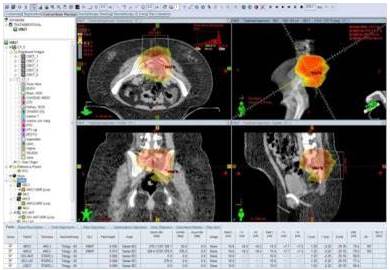
Figura 3
Imágenes del sistema planificación, se aprecian un corte en los 3 planos (axial, coronal y sagital) con la distribución del 100 % de la dosis en color rojo en el área de la lesión macroscópica.
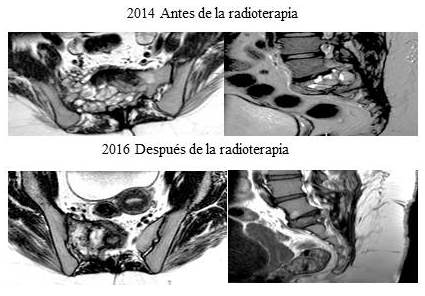
Figura 4
Cortes axiales y sagitales de resonancia en secuencia T1 que muestra el patrón típico en “panal de abeja” y luego se observa notable mejoría por disminución de la heterogeneidad y tamaño de la lesión.
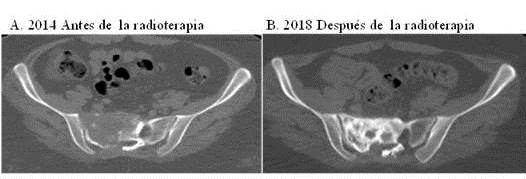
Figura 5
Imágenes comparativas de tomografía en corte axial donde se observa mejoría radiológica dada por la formación del callo óseo.
DISCUSIÓN
Aunque la radioterapia (RT) no es el tratamiento primario de elección en el QAO, es una modalidad de gran utilidad demostrada en pacientes en ciertas localizaciones óseas de la enfermedad dónde la resección amplia no es posible o conlleva una alta morbilidad. El mecanismo de acción de las radiaciones no está completamente dilucidado (12). La hipótesis más aceptada propone que la RT produce obliteración de los vasos de pequeño calibre y que la reducción de la irrigación sanguínea en el QAO conduce a una disminución del tamaño de la lesión y el efecto analgésico de la RT (12,13).
En cuanto a la técnica de tratamiento, aún no se conoce la dosis óptima en el manejo de esta afección. Se han utilizado a través de los años, diferentes dosis de RT desde 500 a 6 000 cGy. Algunos autores han utilizado 4 000 cGy en 4 semanas 4 000 cGy (1,14), otros han encontrado que dosis más bajas, del orden de 2 000 cGy a 3 000 cGy en 2 a 3 semanas pueden ser igualmente efectivas (14,15) o 1 400-1 600 cGy en 7 a 8 fracciones y aún dosis de 500 cGy en 4 fracciones pueden traer respuesta completa y control del tumor(1,14,16,17).
Es imprescindible en la actualidad el uso de técnicas modernas de RT, equipos de mega-voltaje como los aceleradores lineales, con una mayor precisión en la administración del tratamiento disminuyendo al máximo las dosis en los tejidos normales para reducir la morbilidad. La dosis recomendada recientemente por autores de amplia experiencia en estas lesiones está entre 2 000 y 3 000 cGy (1,8,12,18,19,20). En pacientes en edad pediátrica es preferible, emplear dosis aún menores (por debajo de 2 000 cGy) para reducir las complicaciones a largo plazo; como problemas de crecimiento y osteosarcoma secundarios asociados al tratamiento radiante(19,20).
En cuanto a los resultados de la RT, varias series se ha comprobado su efectividad, con tasas de remisión completa que oscilan entre el 50 % al 100 %, cuando se utiliza como tratamiento único o asociado al curetaje o resección parcial (Cuadro 1). Si se comparan algunas series en la literatura se puede observar que los resultados de la RT son comparables a los de la cirugía (12,13,14,15,21,22,23,24,25,26,27).
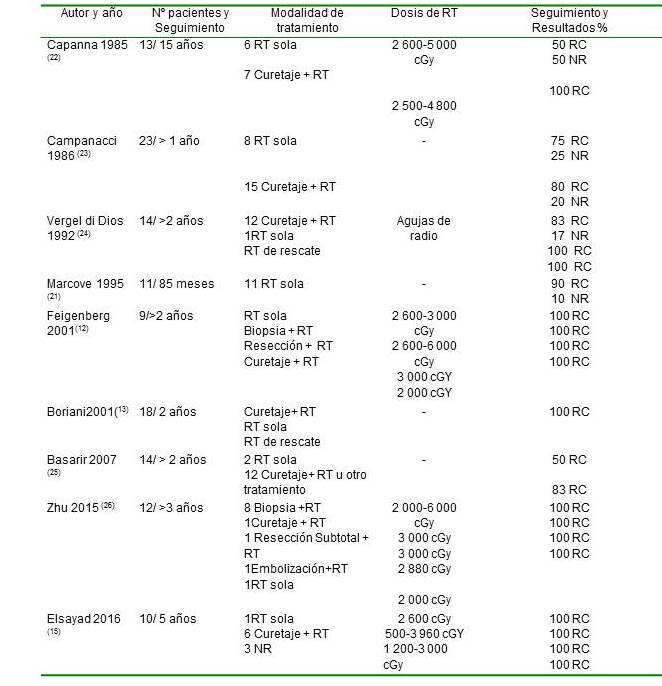
Cuadro 1.
Resultados QAO con radioterapia única y adyuvante
RC: Remisión Completa NR: No remisión
En los dos casos reportados en el presente trabajo es en un paciente con QAO en C2 se empleó una dosis de 2 000 cGy en 2 semanas a 200 cGy/día y en la otra paciente con lesión a nivel del sacro se utilizó 2 600 cGy igualmente con fracciones de 200 cGy/día. Se utilizó en ambos pacientes las técnicas modernas, RT conformada con planificación tridimensional (3D) y RT de intensidad modulada con arcos volumétricos (VMAT). En ambos pacientes la enfermedad está controlada con tiempo de seguimiento de 10 y 4 años, respectivamente, después de la administración de la RT. La mayoría de las recidivas en los pacientes con QAO ocurren dentro de los primeros 2 años (1). Por otra parte, hay reportes del uso de re-irradiación con resultados favorables en caso que no exista otra opción terapéutica (1).
Una de los posibles efectos adversos a largo plazo de la RT, ha sido la inducción de neoplasias secundarias en particular sarcomas inducidos por radiación, sin embargo, en la mayoría de estos pacientes habían sido tratados con altas dosis de RT y técnicas hoy en día arcaicas, utilizando campos de tratamiento no bien conformados con energía de ortovoltaje, con la cual se administraba altas dosis a los tejidos adyacentes, hueso y piel(13,19,20). Además existen reportes de transformación maligna en pacientes que no habían recibido RT (27). En la actualidad con las técnicas modernas de tratamiento y la reducción de la dosis de radiación, la aparición de este tipo de complicaciones se ha reducido significativamente (1,15,24). En los dos pacientes reportados en la presente serie con 10 y 4 años de seguimiento no hemos observado complicaciones a largo plazo.
REFERENCIAS
1. Heyd R, Seegenschmiedt M. Aneurysmal Bone Cyst. En: Brady LW, Heilmann HE, M. Molls M, Nieder C, editores. Radiotherapy for non-malignant disorders. Berlin. Springer. 2008.p. 441.
2. Jaffe HL, Lichtenstein L. Solitary unicameral bone cyst. Arch Surg. 1942;44(6):1004-1025.
3. Fletcher CDM, Unni KK, Mertens F. En: World Health Organization classification of tumours. Pathology and genetics of tumours of soft tissue and bone. Lyon: IARC Press; 2002.
4. Ye Y, Pringle LM, Lau AW, Riquelme DN, Wang H, Jiang T, et al. TRE17/USP6 oncogene translocated in aneurysmal bone cyst induces matrix metallo proteinase production via activation of NF-kappaB. Oncogene. 2010;29(25):3619-3629. doi:10.1038/onc.2010.116.
5. Mahnken AH, Nolte-Ernsting CC, Wildberger JE, Heussen N, Adam G, Wirtz DC, et al. Aneurysmal bone cyst: Value of MR imaging and conventional radiography. Eur Radiol. 2003;13(5):1118-1124.
6. Hudson TM. Scintigraphy of aneurysmal bone cysts. AJR Am J Roentgenol. 1984;142(4):761-765. doi: 10.2214/ajr.142.4.761
7. Enneking WF. A system of staging musculoskeletal neoplasms. Clin Orthop Relat Res. 1986;(204):9-24.
8. Kransdorf MJ, Sweet DE. Aneurysmal bone cyst: Concept controversy, clinical presentation and imaging. AJR Am J Roentgenol. 1995;164:573-580
9. Bonakdarpour A, Levy WM, Aegerter E. Primary and secondary aneurysmal bone cyst: A radiological study of 75 cases. Radiology. 1978;126(1):75-83.
10. Martinez V, Sissons HA. Aneurysmal bone cyst. A review of 123 cases including primary lesions and those secondary to other bone pathology. Cancer. 1988;61(11):2291-2304.
11. Kieser DC, Mazas S, Cawley DT, Fujishiro T, Tavolaro C, Boissiere L, et al. Bisphosphonate therapy for spinal aneurysmal bone cysts. Eur Spine J. 2018;27(4):851-858. doi: 10.1007/s00586-018-5470-y.
12. Feigenberg SJ, Marcus RB Jr, Zlotecki RA, Scarborough MT, Berrey BH, Enneking WF. Megavoltaje radiotherapy for aneurysmal bone cyst. Int J Radiat Oncol Biol Phys. 2001;49:1243-1247.
13. Boriani S. De Iure F, Campanacci L, Gasbarrini A, Bandiera S, Biagini R, et al. Aneurysmal bone cyst of the mobile spine. Report of 41 cases. Spine (Phila Pa 1976). 2001;26(1):27-35.
14. Urdaneta N, Ruan L. Radioterapia en el tratamiento de las enfermedades benignas. En: Urdaneta N, Vera A, Pesschel RE, Wilson L, editores. Radioterapia Oncológica Enfoque Multidisciplinario. 2a edición. Caracas: Disinlimed;2009.
15. Elsayad K, Kriz J, Seegenschmiedt H, Imhoff D, Heyd R, Eich HT, Micke O. Radiotherapy for aneurismal bone cysts: A rare indication. Strahlenther Onkol. 2017;193(4):332-340. doi: 10.1007/s00066-016-1085-6.
16. Marks RD, Scruggs HJ, Wallace KM, Fenn JO. Megavoltage therapy in patients with aneurysmal bone cysts. Radiology. 1976;118(2):421-424.
17. Nobler MP, Higinbotham NL, Phillips RF. The cure of aneurysmal bone cyst. Irradiation superior to surgery in an analysis of thirty three cases. Radiology. 1968;90: 1185-1192.
18. Jereb B. Smith J. Giant aneurysmal bone cyst of the innominate bone treated with irradiation. Br J Radiol. 1980;53:489-491.
19. Shah V, Shingal NC, Udawat JP. Response of aneurysmal bone cyst to low doses of cobalt-60 gamma radiation with prolonged treatment. Br J Radiol. 1978;51:608-612.
20. Maeda M, Tateishi H, Takaiwa H, Kinoshita G, Hatano N, Nakano K. High energy low dose radiation therapy for aneurysmal bone cyst. Report of a case. Clin Orthop. 1989;243:200-203.
21. Marcove R, Sheth DS, Takemoto S, Healey JH. The treatment of aneurysmal bone cyst. Clin Orthop Relat Res. 1995;(311):157-163.
22. Capanna R, Albisinni U, Picci P, Calderoni P, Campanacci M, Springfield DS. Aneurysmal bone cyst of the spine. J Bone Joint Surg Am. 1985;67(4):527-531.
23. Campanacci M, Capanna R, Picci P. Unicameral and aneurysmal bone cyst. Clin Orthop Relat Res. 1986;(204):25-36.
24. Vergel De Dios AM, Bond JR. Shives TC, McLeod RA, Unni KK. Aneurysmal bone cyst. A clinicopathologic study of 238 cases. Cancer. 1992;69(12):2921-2931.
25. Başarir K, Pişkin A, Güçlü B, Yildiz Y, Sağlik Y. Aneurysmal bone cyst recurrence in children: A review of 56 patients. J Pediatr Orthop. 200727(8):938-943.
26. Zhu S, Hitchcock KE, Mendenhall WM. Radiation therapy for aneurysmal bone cysts. Am J Clin Oncol. 2017;40(6):621-624. doi: 10.1097/COC.0000000000000208.
27. Kyriakos M. Hardy D. Malignant transformation of aneurysmal bone cyst, with an analysis of the literature. Cancer. 1991;68(8):1770-1780.
Notas de autor
rreyes@radioterapia.com.ve