Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 16 Septiembre 2019
Aprobación: 12 Noviembre 2019
El CDT es la neoplasia endocrina más común y su presentación más frecuente es como un nódulo tiroideo.
El manejo del carcinoma diferenciado del tiroides (CDT) requiere de un equipo multidisciplinario de diversas especialidades médico quirúrgicas e imagenológicas, así como de la participación activa de los patólogos, médicos especialistas en medicina nuclear, radioterapeutas oncólogos y más recientemente de los oncólogos médicos, porque el abordaje del paciente con la visión del grupo de trabajo permite ofrecerle las mejores alternativas terapéuticas, haciendo énfasis en el no sobretratar al paciente de bajo riesgo y si tratar adecuadamente al paciente que realmente lo requiera.
EVALUACIÓN PREOPERATORIA
1. Laboratorio
2. Evaluación de cuerdas vocales
3. Imágenes
4. Marcadores moleculares
5. Otros estudios
El estudio de elección para la evaluación de los nódulos tiroideos es el ultrasonido tiroideo (US). Se debe utilizar un transductor lineal de alta resolución (>10 MHz) para poder discriminar las microcalcificaciones sospechosas de malignidad. El informe ecográfico debe incluir las características de la glándula (medidas, volumen, ecotextura y presencia de nódulos). Es importante ubicar la localización de los nódulos tiroideos (tercio superior, medio e inferior y anterior o posterior). La descripción de los nódulos tiroideos debe seguir el léxico de la ACR TI-RADS © 2017 (V2) (1) a. Composición, b. Ecogenicidad, c. Forma, d. Márgenes y e. Focos ecogénicos. Se obtiene un puntaje y los nódulos se clasifican en:
1. Benigno (TR 1)
2. No sospechoso (TR 2)
3. Levemente sospechoso (TR 3)
4. Moderadamente (TR 4A o 4B)
5. Altamente sospechoso (TR 5)
Se debe incluir una evaluación ecográfica de los ganglios cervicales y se deben caracterizar sus hallazgos en caso de apariencia sospechosa: a. Forma b. Tamaño c. Presencia o no de microcalcificaciones y d. Si es posible vascularidad al Doppler color (Power)(2). En caso de detectar adenomegalias de carácter sospechoso debe realizarse estudio citológico y de ser posible, determinación de Tg en líquido de lavado de la aguja.
BIOPSIA POR PUNCIÓN ASPIRACIÓN CON AGUJA FINA (PAAF)
La biopsia por punción aspiración por aguja fina (PAAF) se debe realizar en base al tamaño del nódulo y a su categorización TI-RADS © (TR de 3 a 5), al igual que su seguimiento y se deben seguir las recomendaciones ACR TI-RADS © 2017 (V2) (Cuadro 1).
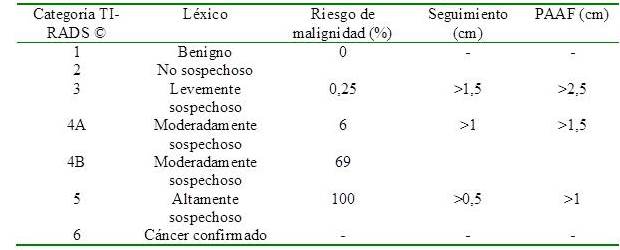
Cuadro 1
Clasificación, puntuación y léxico TI-RADS © 2017 V2
Se recomienda la utilización de agujas 22-23G y aspiración con inyectadora de 10 cm3 y bajo guía ecográfica. Se evalúa la vascularidad del nódulo a punzar. Si muestra mucha vascularidad al Doppler se realiza punción sin aspiración (por capilaridad). Se recomienda aspirar todo el contenido líquido y reservarlo para estudio citológico de centrifugado y apartarlo de la toma del componente sólido (3).

Cuadro 2.
Porcentaje de sensibilidad, especificidad, valor predictivo positivo (VPP), razón de falsos positivos (RFP) y razón de falsos negativos (RFN) de las PAAF
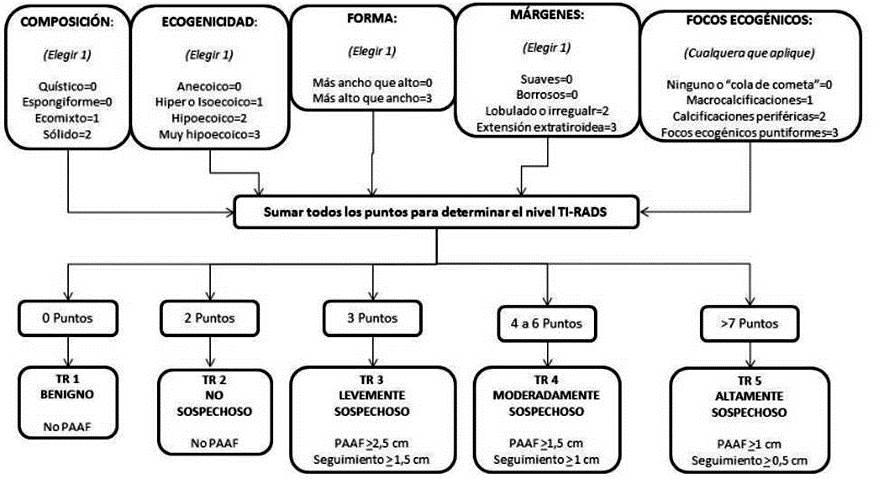
Figura 1.
Escala de puntuación en base a los hallazgos ecográficos (TI-RADS © 2017 V2)
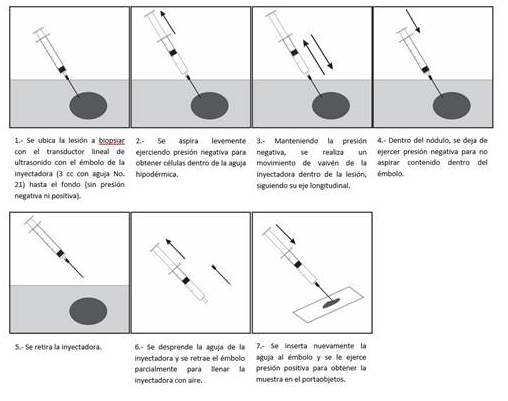
Figura 2.
Procedimiento para realizar la PAAF.
Figura 3
Colocación del transductor en forma paralela y perpendicular (Foto. Sztajnworc D, Lilue R)
LABORATORIO
- Tiroglobulina (Tg): es inespecífica, porque un nivel elevado puede encontrarse en diversas patologías, por tanto, su determinación no está validada en el preoperatorio (4,5, 6).
- Anticuerpos anti-tiroglobulina (AcTg): su presencia, nos alertará sobre posible limitación de la Tg como marcador tumoral, en el seguimiento posquirúrgico (6).
EVALUACIÓN DE CUERDAS VOCALES
Debe realizarse estudio laringoscópico porque en muchos casos es asintomática.
OTROS ESTUDIOS IMAGENOLÓGICOS
El uso de otros estudios de imagen como la tomografía computada (TC) o la resonancia magnética (RM) (7,8) no aportan mayor información que el US. Su utilidad se limita en casos puntuales, como: a. Crecimiento de la tiroides hacia el mediastino (bocio sumergido) b. Fijación con estructuras adyacentes c. Tumor localmente avanzado (mejor evaluable con RM) d. Metástasis pulmonares (mejor evaluables con TC). Se recomiendan para estudios de extensión locorregional y ganglionar, aunque los ganglios cervicales se evalúan en forma satisfactoria con el US diagnóstico en manos competentes. Sin embargo, se pueden observar hallazgos incidentales en estudios tomográficos y de RM de lesiones nodulares en la glándula tiroides que pueden sugerir lesiones neoplásicas malignas. Se recomienda el uso de contrastes endovenosos en los estudios tomográficos y de RM para extensión tumoral (locorregional y ganglionar). La TC con contraste yodado hidrosoluble, el cual tiene vida media corta, aclarándose de la circulación al mes de administrado, no interfiriendo con el uso de RAI si el paciente tiene indicación de esta terapia a posteriori (9). Se pueden realizar estudios de RM con saturación grasa y/o difusión para detectar ganglios de características malignas (8) (Cuadros 3 y 4).
MARCADORES MOLECULARES
El riesgo de malignidad es aproximadamente 30 % en nódulos con citología indeterminada (categoría III y IV de Bethesda) Los marcadores moleculares son de utilidad para definir la naturaleza de estos nódulos, evitando la realización de cirugía en un porcentaje significativo de casos (9,10,11,12).
TRATAMIENTO
ABORDAJE QUIRÚRGICO LOCAL
Las herramientas en el tratamiento para el CDT son: la cirugía que es el pilar fundamental, el tratamiento con hormona tiroidea para suprimir el TSH y yodo radiactivo 131I (13).
La extensión de la resección quirúrgica adecuada en pacientes con el carcinoma tiroideo temprano ha sido tema de controversia.
OBJETIVOS DE LA CIRUGÍA EN EL CDT
El objetivo principal de la cirugía es eliminar el tumor primario macroscópico de la tiroides. El logro de márgenes adecuados es menos complicado cuando el tumor no supera los límites de la cápsula tiroidea. Sin embargo, esto es más difícil en áreas donde la cápsula tiroidea pierde continuidad como en el ligamento de Berry, las glándulas paratiroides y la fascia traqueal.
La cirugía debe permitir la estadificación precisa y la estratificación del riesgo de la enfermedad (14,15). Otro objetivo es la reducción del tejido tiroideo normal remanente en la lobectomía y en la tiroidectomía total. Los sitios donde accidentalmente se deja tejido tiroideo remanente son el lóbulo piramidal, el polo superior de la glándula tiroides y el ligamento de Berry. Esto es particularmente beneficioso en la tiroidectomía total, porque puede disminuir las posibilidades de recomendación de yodo radiactivo después de la cirugía y para obtener una prueba de Tg indetectable. También, cuando se realiza una lobectomía y posteriormente se indica completar la tiroidectomía total, evita tener que revisar el lado ya operado con sus posibles complicaciones.
Para evitar complicaciones, debe ser identificado el nervio laríngeo recurrente, realizar la ligadura de las ramas terminales de la arteria tiroidea inferior con la visualización y la preservación de las glándulas paratiroides. Para identificar y preservar la rama externa del nervio laríngeo superior se recomienda una disección cuidadosa del pedículo superior, utilizando el plano avascular entre el polo superior y el músculo cricotiroideo (16,17).
El espécimen resecado debe examinarse y cualquiera de las glándulas paratiroides extraídas inadvertidamente debe ser reimplantada en el músculo esternocleidomastoideo (preferentemente) o en los músculos pre-tiroideos.
Para minimizar el riesgo de lesiones accidentales del nervio laríngeo recurrente se ha recomendado el monitoreo neuronal intra-operatorio continuo, en especial para re-intervenciones (18).
ALTERNATIVAS DE TRATAMIENTO
Las alternativas de tratamiento local aceptados del CDT incluyen tiroidectomía total, lobectomía y la istmectomía (para tumores pequeños en la línea media, en casos muy seleccionados con criterios de buen pronóstico). La indicación de una cirugía más conservadora está condicionada a los factores de riesgo y la extensión de la enfermedad.
Las ventajas de la tiroidectomía total serían que la resección de todo el tejido tiroideo asegura la extirpación de una posible enfermedad multifocal oculta en el lóbulo contralateral, facilita la aplicación de yodo radiactivo adyuvante, mejorando en el posoperatorio la detección y tratamiento de enfermedad residual o metastásica y optimiza el uso de Tg sérica como un marcador para detectar enfermedad residual y/o recurrente.
La ventaja de la lobectomía es la reducción de la tasa de complicaciones quirúrgicas y puede evitar la necesidad de terapia de reemplazo con levotiroxina de por vida, así como el uso de yodo radiactivo (18)
En el consenso de 2004 (19) se consideró la tiroidectomía total como el tratamiento primario de elección para el carcinoma diferenciado de tiroides > 1 cm independientemente de otros factores de riesgo. Los estudios disponibles mostraban una mejoría en la sobrevida y una menor tasa de recurrencia (20,21,22,23), sin embargo, datos recientes han demostrado que seleccionando los pacientes según determinados factores de riesgo, en aquellos de bajo riesgo, los resultados clínicos son muy similares después de lobectomía o tiroidectomía total (24,25,26,27,28). Además, actualmente se selecciona a los pacientes que deben recibir tratamiento con yodo radiactivo, por lo que su uso ya no es rutinario (29,30).
La lobectomía puede obviar la necesidad de tratamiento de por vida con hormona tiroidea exógena y evita complicaciones como el hipoparatiroidismo y la parálisis vocal bilateral, que son de difícil manejo (31,32).
CRITERIOS PARA LA TOMA DE DECISIONES CUANDO SE TIENE UN DIAGNÓSTICO PREOPERATORIO O INTRA-OPERATORIO DE CDT
El uso de PAAF en la práctica clínica actual ha resultado en una elevada tasa de diagnóstico de carcinoma de tiroides (usualmente papilar) previo a la intervención, que puede alcanzar un valor predictivo positivo del 97 % -99 % (15).
Con respecto a la PAAF y el corte congelado, es un tema que depende de muchas variables como la calidad de la muestra (experiencia del médico que toma la muestra), experiencia del patólogo, comunicación, confianza y relaciones del equipo de trabajo, por lo cual el consenso recomienda que si el resultado de la PAAF proviene de un citotecnólogo que forma parte del equipo de trabajo o es de un patólogo reconocido y hay congruencia con la clínica del paciente y los hallazgos ultrasonográficos, se puede omitir el corte congelado, de no tener estos requisitos o de haber alguna duda, se debe realizar la biopsia por congelación.
Ante un diagnóstico de malignidad, la cirugía recomendada es una tiroidectomía total o una lobectomía, según los criterios expuestos en el (Cuadro 4) (18, 19, 33, 34).

Cuadro 4.
Criterios para realizar una lobectomía o una tiroidectomía total en CDT
CRITERIOS PARA LA TOMA DE DECISIONES CUANDO SE TIENE UN DIAGNÓSTICO POSOPERATORIO DE CDT
Generalmente esto ocurre cuando se realiza una lobectomía debido a que no se tenía un diagnóstico de CDT previamente a la intervención, y por los hallazgos encontrados por el patólogo al estudiar la pieza y ofrecer un resultado definitivo. Existen factores de riesgo para realizar una re-intervención y completar la tiroidectomía. Con frecuencia se trata de carcinoma folicular y carcinoma de células de Hürthle, porque estas variantes generalmente no se pueden diagnosticar por PAAF de rutina o por corte congelado (biopsia peroperatoria) (16).
Se debe completar la tiroidectomía en los siguientes casos (19)
• Tumor> 4 cm de diámetro.
• Márgenes positivos.
• Extensión extra-tiroidea.
• Enfermedad multifocal macroscópica.
• Metástasis ganglionares.
• Enfermedad contralateral confirmada.
• Invasión vascular.
• Histología desfavorable
MANEJO DEL CUELLO
La evaluación del cuello en CDT debe estar basada en el examen físico, US cervical y PAAF eco guiada, otros estudios como la TC y/o RM con contraste debe considerarse en enfermedad voluminosa (17,33.34,35).
DEFINICIONES
Disección terapéutica: es definida como aquella realizada en enfermedad nodal clínicamente evidente, pre o trans operatorio, usando el examen físico, métodos de imagen, o por patología (incluye PAAF, y/o biopsia intra-operatoria).
Disección profiláctica o electiva: es aquella que se realiza en el contexto de ausencia de enfermedad ganglionar demostrada por clínica o por imágenes.
Definición de los compartimientos del cuello
Compartimiento central: incluye ganglios pre laríngeos, delfiano, pre-traqueales y para-traqueales afectados, los límites de la disección son desde el hueso hioides hasta la arteria innominada y lateralmente la carótida primitiva (niveles VI y VII)
Disección lateral: incluye niveles IIa, III, IV y Vb.
Indicaciones para la disección central
Disección central electiva: el consenso recomienda la disección central total o unilateral dependiendo de la extensión y ubicación de la enfermedad en T3 o T4, extensión extra capsular, cuello lateral positivo (N1b), multicentricidad. Puede considerarse la disección central electiva en aquellos pacientes con cirugía tiroidea incompleta y factores de riesgo desfavorables, considerar la disección central homolateral.
Disección central terapéutica: N1 central clínicamente aparente, preoperatorio documentado por imágenes y/o estudio citológico, en caso de ser posible, o trans-operatorio clínicamente sospechoso con confirmación histológica por biopsia intra-operatoria (35).
Indicaciones para la disección lateral
Disección lateral electiva: no está recomendada.
Disección lateral terapéutica: N1b aparente clínicamente preoperatorio y/o documentado por imágenes con comprobación cito-histológica. Involucra niveles IIa, III, IV y Vb (36,37,38).
ESTUDIO ANATOMOPATOLÓGICO
De los métodos disponibles en la actualidad, la PAAF es considerada el método de elección para el abordaje inicial. Este procedimiento debe ser realizado y analizado por personal experimentado en esta patología (3).
CDT
Definición. Clasificación.
Son aquellos que conservan características funcionales y morfológicas parecidas a las células foliculares normales de la glándula tiroides (17).
Los carcinomas que se derivan de las células foliculares se clasifican en:
• Carcinoma papilar (PTC). (Supervivencia global mayor del 90 %- 95 % a 10 años).
• Carcinoma folicular (FTC). (Supervivencia global mayor a 90 %-95 % a 10 años).
• Carcinoma pobremente diferenciado. (50 % supervivencia global a 10 años).
• Carcinoma anaplásico. (10 % de supervivencia global a los 10 años) frecuentemente representa una progresión de un PTC o FTC.
Los dos primeros son los carcinomas diferenciados.
Es importante acotar que las reglas de estadificación no se aplican a los carcinomas que se originan en quistes del conducto tirogloso u otros sitios ectópicos (ovario). Deben diferenciarse también del carcinoma medular, que se origina de las células para-foliculares.
Las variedades o subtipos de carcinoma papilar son: clásica, microcarcinoma papilar, folicular no encapsulada, macro-folicular, oncocítica u oxifílica, células claras, esclerosante difusa, células altas, células columnares, sólida, cribiforme morular, con estroma tipo fasciitis nodular, de células en tachuela.
Las variantes del carcinoma folicular son: oncocítica (células de Hürthle) y células claras (39).
EVALUACIÓN DEL NÓDULO TIROIDEO
La PAAF es el procedimiento de elección en la evaluación de nódulos tiroideos.
Se reporta utilizando los grupos diagnósticos del Sistema Bethesda (38) para las muestras de citopatología tiroidea. Las categorías, el riesgo estimado de malignidad, media % actual de malignidad en nódulos extirpados (rango), son las siguientes:

Cuadro 5.
Categorías de riesgo
La sensibilidad y especificidad de la PAAF puede llegar a ser superior al 90 %, si la muestra es adecuada; en caso de una muestra inadecuada, se sugiere repetir la punción (17).
Una PAAF adecuada requiere 6 o más grupos de células foliculares bien preservadas, con 10 a 20 células por grupo, en dos extendidos citológicos diferentes. La PAAF con menor cantidad de células foliculares, y con escaso coloide deben considerarse como muestras no diagnósticas. Una muestra de PAAF que presenta abundante coloide y pocas células epiteliales, es muy probable que sea benigna. Muestras hipo-celulares con criterios citológicos de malignidad, deben interpretarse como sospechosas. La PAAF debe ser realizada por un médico especialista con amplia experiencia en la aspiración de nódulos tiroideos. Se sugiere emplear agujas de calibre 22- 23G, con un mínimo de cuatro punciones en diferentes áreas del nódulo para reducir el error de muestreo. Los extendidos citológicos mínimo 4 y máximo 6, se dejan secar, inmediatamente se fijan en alcohol isopropílico y se colorean con tinciones varias (hematoxilina-eosina, Papanicolaou, Diff- Quik).
Se emplea la coloración con hematoxilina y eosina de rutina debido a su disponibilidad en todos los servicios de anatomía patológica; sin embargo, cualquier tinción utilizada requiere un adecuado conocimiento de los criterios citológicos establecidos para las distintas lesiones tiroideas. El material remanente en la aguja debe lavarse repetidamente en un tubo de ensayo con formol, para posterior estudio histológico.
Es fundamental que el médico tratante proporcione información clínica pertinente para una adecuada interpretación de los extendidos y correlación clínico-patológica.
La posibilidad de pedir una segunda opinión acerca de la PAAF, debe ser considerada, sobre todo cuando exista disparidad ante el aspecto clínico y el resultado de la PAAF.
CORTE CONGELADO
• Pacientes con citología positiva para cáncer de tiroides es recomendable confirmar el diagnóstico mediante corte congelado.
• Cuando no hay diagnóstico preoperatorio, está indicado el corte congelado.
• La consulta intra-operatoria en patología tiroidea está indicada en casos diagnosticados por PAAF como carcinoma papilar o con hallazgos citológicos sugestivos de carcinoma papilar, más no concluyentes de malignidad. En casos de neoplasia folicular o de células de Hürthle, la consulta intra-operatoria no está indicada, debido a que el diagnóstico de malignidad en estas lesiones depende de la demostración de invasión a la cápsula y vascular en cortes histológicos definitivos. La realización de citología intra-operatoria conjuntamente con el corte congelado aumenta la sensibilidad y especificidad de la consulta intra-operatoria.
INFORME ANATOMOPATOLÓGICO.
Aspectos importantes.
El informe anatomopatológico debe incluir los siguientes parámetros:
a. Diagnóstico histológico y variante del carcinoma
b. Localización del tumor
c. Multicentricidad
d. Tamaño tumoral
e. Presencia o no de cápsula
f. Presencia de un componente poco diferenciado (áreas sólidas o características citológicas de alto grado expresado en porcentaje)
g. Invasión capsular o vascular (número de vasos con émbolos neoplásicos)
h. Extensión extra-tiroidea
i. Bordes quirúrgicos
j. Patología asociada
k. Presencia de glándulas paratiroides (número)
l. Ganglios linfáticos (número, tamaño, presencia o no de metástasis, la metástasis de mayor tamaño y extensión extra-capsular, tipo y variedad histológica de la metástasis, igual o diferente al primario) (17)
m. Opcional: necrosis, mitosis, características histológicas adicionales
n. Hallazgos histoquímicos e inmunohistoquímicos
o. Microcalcificaciones (cuerpos de Psammoma) en el tumor primario y en los ganglios linfáticos.
• La presencia de invasión capsular incompleta y la ausencia de invasión vascular en una lesión folicular con atipias citológicas francas, debe designarse como neoplasia folicular de comportamiento indeterminado.
• Histopatológicamente, el carcinoma papilar es un tumor maligno bien diferenciado originado de las células foliculares tiroideas, que muestra rasgos microscópicos nucleares característicos. Aunque un crecimiento papilar es observado frecuentemente, éste no es indispensable para el diagnóstico.
• Recientes avances consideran a los tumores encapsulados con invasión vascular microscópica solamente, como mínimamente invasivos, mientras aquellos tumores angioinvasivos se colocan en una categoría diferente.
• La extensión extra-tiroidea debe ser documentada histológicamente.
• El carcinoma papilar variante folicular encapsulada actualmente se denomina: neoplasia folicular no invasiva con características nucleares tipo papilar (NIFTP). Existen criterios histológicos mayores, menores y excluyentes bien definidos para su diagnóstico. Debe ser tratada conservadoramente y no ser considerada como un cáncer, por lo tanto no debe ser estadificada como tal; solo debe ser informado o reportado el tamaño, localización y bordes quirúrgicos de la lesión.
• La inmunohistoquímica tiene utilidad básicamente para definir el origen de neoplasias pobremente diferenciadas.
• La determinación de las alteraciones moleculares aunque tiene cierta utilidad pronostica en algunos casos de este tipo de carcinoma, en nuestro medio actualmente no se justifica su utilización debido a la relación costo-beneficio.
• Un adecuado diagnóstico de la patología tumoral maligna de la glándula tiroides requiere no solo del conocimiento de sus características cito-histológicas y su amplio espectro de diagnósticos diferenciales, sino un sólido apoyo clínico-radiológico, para así lograr una correlación clínico-patológica idónea (38,39,40).
• Es indispensable informar los pertinentes negativos pues el médico tratante debe tener la certeza de los parámetros evaluados en el espécimen quirúrgico.
EVALUACIÓN POSOPERATORIA
MANEJO INMEDIATO
1. Cuando iniciar el tratamiento con levotiroxina
El endocrinólogo tratante debe decidirlo de acuerdo a cada caso en particular.
Se indicará en el posoperatorio inmediato en las siguientes situaciones:
• Pacientes con tumores menores de 1 cm, sin adenopatías en quienes se considere que no requieren tratamiento con iodo radiactivo.
• Pacientes en los cuales se utilizará estimulación con TSH recombinante (rhTSH)
• Pacientes de riesgo no definido en los cuales se requiere esperar el resultado anatomopatológico.
• Cuando se requiera esperar, por no existir disponibilidad de radio-iodo.
En aquellos casos en los cuales la aplicación del iodo se realice bajo el régimen de deprivación hormonal, se debe programar la suspensión del tratamiento coordinadamente con el médico nuclear, de acuerdo a la disponibilidad del radiofármaco. Existen varios protocolos publicados, unos con suspensión de T4 por 4 semanas o suspensión de T4 por 4 semanas, y sustitución por T3 durante las primeras dos semanas (40). Este último difícil de realizar en el país por la falta de disponibilidad comercial de T3. Se ha demostrado que el nivel de TSH óptimo previo al tratamiento ablativo debe ser > 30 mUI/mL (41,42) y éste puede lograrse en un paciente con tiroidectomía total en un lapso menor, pero debe ser confirmado por laboratorio antes de la aplicación del iodo. Se ha demostrado que la demora en la aplicación de la dosis ablativa no implica mayor riesgo para el paciente (41).
2. Categorización del riesgo
El Sistema TNM del American Join Comittee on Cancer/International Union Against Cancer (AJCC/UICC) ha sido recientemente actualizado. Es un buen predictor de riesgo de mortalidad, pero su sensibilidad para determinar recurrencia es baja. Su última edición (8ª), se resume en los Cuadros 6A y B (41).

Cuadro 6 A
Sistema TNM (8ª edición)
Definición del tumor primario
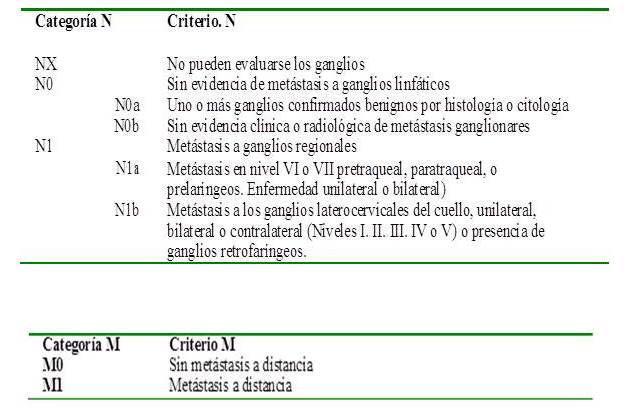
cont cuadro 6A
Definición de linfonódulos regionales (N) Definición de Mt a distancia
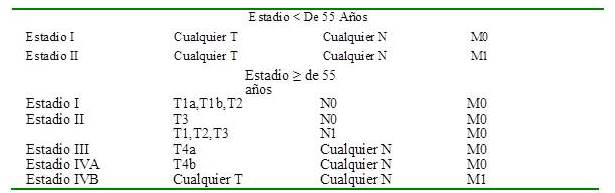
Cuadro 6 B
Estadificación de riesgo de mortalidad
Los cambios principales en relación a la 7ª edición incluyen un incremento en la edad de corte (55 años en vez de 45 años) (42,43), una reducción en la importancia de la enfermedad extra-tiroidea microscópica y la presencia de metástasis ganglionares, como factores predictivos de riesgo para mortalidad.
La Asociación Norteamericana de tiroides (ATA) publicó en 2015 sus nuevas guías, estableciendo una clasificación de riesgo de recurrencia basados en información clínica, el estudio anatomopatológico de la lesión, presencia de tejido iodocaptante extra-tiroideo y el nivel de Tg posoperatorio (44,45,46,47,48,49,50,51). Requiere del aporte de varias especialidades, siendo imprescindible la formación de un equipo multidisciplinario. Es un concepto dinámico, de manera que, a través del tiempo se debe establecer la re-categorización de riesgo, según la respuesta al tratamiento, permitiendo un seguimiento más exhaustivo solo en aquellos con mayor riesgo. La clasificación incluye tres grupos: riesgo bajo, intermedio y alto.
Bajo riesgo
• Ca papilar sin invasión de estructuras vecinas
• Histología no agresiva
• Ausencia de invasión vascular
• N0 0 ≤ 5 micrometástasis
• Ca papilar variedad folicular intratiroideo, encapsulado
• Ca folicular bien diferenciado
• Microcarcinoma papilar uni o multifocal
• Incluyendo aquello con mutación BRAFV600E
Riesgo intermedio
• Ca papilar con invasión microscópica a tejidos blandos peritiroideos
• Histología agresiva
• Detección de Mt iodo-captantes en cuello pos-ablación
• Invasión vascular
• N1 detectada clínicamente o ≤ 5 N1con ganglios < 3 cm en su diámetro mayor
• Microcarcinoma papilar multicéntrico con extensión extratiroidea y mutación BRAFV600E
Riesgo alto
• Invasión macroscópica a tejidos blandos peritiroideos
• Resección incompleta de la lesión
• N1 con al menos 1 linfonódulo metastásico > 3 cm
• Mt a distancia
• Tg posoperatoria elevada
• Ca folicular con extensa invasión linfática (más de 4 vasos)
3. Cuándo medir Tg posoperatoria
Su determinación previa al tratamiento ablativo no es factor predictivo de riesgo, pero puede servirnos como valor basal y punto de comparación con las evaluaciones subsiguientes. Debe realizarse a las 4 semanas pos-cirugía y en todos los pacientes que reciban una dosis ablativa de 131I tras la suspensión hormonal o después de estimular con rhTSH, conjuntamente con la determinación de AcTg.
4. ¿Qué dosis de levotiroxina administrar y cuál es el nivel óptimo de TSH?
Existe evidencia de que solamente pacientes de alto riesgo se benefician de la terapia supresiva por tanto, el nivel de TSH debe fijarse en base al riesgo.
La ATA recomienda en el manejo inicial posoperatorio el siguiente esquema:
Riesgo alto: TSH < 0,1 mUI/L
Riesgo intermedio: TSH entre 0,1- 0,5 mUI/L
Riesgo bajo:
• Pacientes con terapia ablativa y Tg no detectable: deben mantenerse en el rango de referencia bajo. TSH entre (0,5- 2 mU/L)
• Pacientes con terapia ablativa y Tg detectable: debe mantenerse discretamente suprimida normal (TSH 0,1-0,5 mU/L).
• Pacientes con lobectomía: debe mantenerse en el rango normal bajo (TSH 0,5-2 mU/L). No se requiere tratamiento con levotiroxina, si el nivel de TSH posoperatorio se mantiene en este rango.
LOCALMENTE AVANZADOS, RECIDIVAS
Manejo quirúrgico de la enfermedad ganglionar recurrente
Aunque en enfermedad de bajo volumen la sobrevida global no está bien establecida, se recomienda la cirugía (44,45), disección lateral como primera opción terapéutica en la recurrencia lateral cuando los ganglios son de 10 mm con confirmación por PAAF y la disección total en el compartimiento central en ganglios centrales mayores o iguales de 8 mm, confirmados por PAAF, otras alternativas terapéuticas como la ablación con etanol, uso de radiofrecuencia, radioterapia estereotáxica, terapias target, son alternativas en aquellos casos donde el riesgo quirúrgico supera el beneficio.
Es importante definir el volumen y localización de la recaída regional con estudios de imagen como US de alta resolución, TC con contraste, FDG/PET-CT o RAI-SPECT/CT y documentarlo con PAAF.
En caso de re-intervención todo paciente debe ir a NFL con la finalidad de evaluar la movilidad de ambas cuerdas vocales. Se recomienda preservar la paratiroides o reimplantarla en el esternocleidomastoideo ipsilateral marcándolo con clips.
En caso de involucrar el cricoides o la tráquea a veces es posible hacer un afeitado y no una resección segmentaria. Las indicaciones para una resección mayor pueden ser determinadas con una TC, laringoscopia, broncoscopia o esofagoscopia antes de la cirugía, si hay compromiso mayor de 180 grados del cricoides especialmente hacia el lado posterior o compromiso de la movilidad de ambas cuerdas vocales, el paciente es candidato para una laringectomía total (45).
Manejo quirúrgico del CDT localmente avanzado
Sólo con una evaluación preoperatoria adecuada, un alto índice de sospecha de invasión y la experiencia quirúrgica para la resección completa con baja morbilidad, los pacientes con cáncer de tiroides bien diferenciado localmente avanzado, probablemente obtengan la mejor oportunidad de supervivencia y bajo riesgo de recurrencia.
Invasión de los músculos pre-tiroideos
Cuando están invadidos, la resección de los músculos pretiroideos se puede realizar fácilmente sin necesidad de reconstrucción y tiene una consecuencia mínima para el paciente (44).
Invasión del nervio laríngeo recurrente
Se ha recomendado la laringoscopia preoperatoria en todos los pacientes sometidos a cirugía tiroidea cuando la voz es anormal, si hay antecedentes de cirugía en la que el nervio vago o nervio laríngeo recurrente estaban en riesgo, o si hay sospecha preoperatoria de malignidad con extensión extra-tiroidea. Se indica la resección del nervio laríngeo recurrente si está infiltrado por tumor y si existe parálisis vocal ipsilateral. Se puede intentar su preservación por afeitado si el nervio está englobado por el tumor y la función de las cuerdas vocales es normal antes de la operación y particularmente si la cuerda vocal contralateral presenta parálisis o paresia (para evitar una parálisis vocal bilateral), siempre que se elimine toda la enfermedad macroscópica. En estos casos se debe considerar la terapia adyuvante con yodo radiactivo y/o radioterapia externa (44,45).
Invasión aero-digestiva
Cuando sea técnicamente factible, se recomienda la cirugía para la enfermedad invasiva aero-digestiva en combinación con yodo radiactivo y / o radioterapia externa. El resultado terapéutico está relacionado con la resección completa de toda la enfermedad macroscópica con la preservación de la función, con técnicas que van desde el “afeitado” del tumor de la laringe, tráquea o el esófago, por una invasión superficial, a técnicas más agresivas cuando la laringe, tráquea o el esófago están invadidos más profundamente (por ejemplo, invasión intra-luminal directa), que incluyen la resección traqueal o laringofaringoesofagectomía. La toma de decisiones quirúrgicas puede ser compleja y debe equilibrar la preservación de órgano y función con una cirugía resectiva pero que represente un posible intento de curación, y en otras circunstancias, que ofrezca una significativa paliación en pacientes con asfixia inminente o una hemoptisis significativa (44,45).
Criterios de irresecabilidad
En general, la clasificación TNM de la AJCC incluye como T4b aquellos tumores que reflejan dificultad para poder ser resecados. Incluye 3 criterios que son: invasión e inclusión vascular, invasión del espacio pre-vertebral e invasión de estructuras mediastínicas. Sin embargo, la biología del CDT, permite márgenes quirúrgicos más estrechos que en casos bien evaluados y seleccionados, son aún factibles de resecar.
El CDT rara vez se complica con una invasión vascular importante y afortunadamente, algunos de estos tumores siguen siendo resecables. El inesperado descubrimiento intra-operatorio de afectación vascular masiva puede augurar una potencial catástrofe quirúrgica. Cuando se sospecha afectación vascular, debe ampliarse la evaluación por imágenes habitualmente indicada para determinar la resecabilidad y la extensión de la cirugía. Se debe considerar un US de cuello con especial atención dirigida a los grandes vasos, una TC con evaluación angiográfica cervical y torácica, una angiografía convencional para confirmar la permeabilidad del polígono de Willis. Se puede considerar la RM porque es efectiva para predecir la invasión de la laringe, el esófago y las estructuras mediastínicas. Si se contempla la resección carotidea, también sería prudente la consulta con cirugía cardiovascular (46,47,48,49,50,51).
La presencia de afectación de la fascia pre-vertebral es definida clínicamente por la fijación del tumor a la musculatura pre-vertebral. En muchos casos, tratar de extirpar el tumor de los músculos longus colli / capitis presenta dificultades y a menudo deja enfermedad residual. La invasión mediastínica puede verse en raras ocasiones en pacientes con cáncer de tiroides. Se presenta con infiltración de grasa mediastinal y la invasión vascular de sus vasos supra-aórticos y / o el arco aórtico de forma circunferencial, así como también puede incluir infiltración traqueal y esofágica. Un intento de resección debería incluir la participación de un cirujano torácico (45,46,47,48,49).
TERAPIA CON RADIOYODO
Objetivos del radioyodo (RAI)
Luego de la tiroidectomía total, el 131I puede utilizarse
A. Ablativo (eliminar remanentes tiroideos normales)
B. Adyuvante (eliminar micrometástasis sospechadas, aunque no confirmadas)
C. Terapéutico (tratar enfermedad persistente conocida).
En la mayoría de los casos, el objetivo de la ablación con RAI consiste en destruir el tejido tiroideo normal residual luego de la tiroidectomía total y generalmente en la mayoría de los casos, solo se necesita una dosis. Incluso las metástasis pequeñas no detectadas por US o RX de tórax, concentran el 131I selectivamente en una alta proporción (32,33).
La eficacia del RAI depende de factores que incluyen la biología tumoral y la dosis de radiación al tumor.
La ablación permite aumentar la especificidad de la Tg como marcador tumoral (y en casos seleccionados, también de los rastreos corporales con 131I), facilitando por lo tanto el seguimiento y la detección temprana de enfermedad persistente o recurrente (33).
Preparación para la terapia con yodo radiactivo
Recomendaciones nutricionales
Dieta con bajo contenido en yodo
Aunque en este aspecto hay bastante controversia, la mayoría de los centros que realizan rutinariamente ablación prescriben una dieta con bajo contenido de yoduro para aumentar la acumulación de RAI en los restos tiroideos. Sin embargo, nunca se ha demostrado de manera convincente la eficacia de una dieta baja en yoduro, en la ablación del remanente tiroideo. La restricción y la duración de la restricción del consumo de yodo en la dieta varía en las diferentes guías, la ATA recomienda <50 mcg/día por 1-2 semanas (50.51,52).
Suspensión hormonal (TSH mayor a 30 mUi/ml) vs., TSH recombinante humana (Thyrogen®)
Ambos métodos recomendados por las diferentes guías (33, 34, 53).
Suspensión del reemplazo de hormonas tiroideas
En pacientes adultos de 4 a 6 semanas antes de recibir el RAI. Los niños alcanzarán este nivel de TSH en 14 días de retirada la levotiroxina (34,54).
Detener la ingesta de hormonas tiroideas hará que la TSH aumente a un nivel de 30 mUI/mL o superior.
El paciente quedará significativamente hipotiroideo y experimentará síntomas y signos de hipotiroidismo tales como fatiga, intolerancia al frío, ganancia de peso, retención de líquido, piel seca, estreñimiento, cambios en piel, uñas frágiles, cabello fino, irregularidades menstruales, problemas psiquiátricos, depresión, cambios de humor, etc.
La otra alternativa a la suspensión de la hormona tiroidea es el uso de TSH recombinante (rhTSH). Se utilizan 2 dosis de 0,9 mg, intramuscular, con intervalo de 24 h, dos días previos a la administración de RAI.
Existe evidencia para su uso en pacientes de bajo, intermedio y alto riesgo de recurrencia, incluso no hay diferencias en la supervivencia a 5 años en pacientes con CDT metastásico tratados con RAI, estimulados con suspensión del tratamiento con levotiroxina o rhTSH, con escasos efectos adversos como: cefalea 7,3 %, náuseas 10,5 %, astenia 3,4 %, vómitos 2, %, escalofríos 1 %, fiebre 1 % y debilidad 1,5 % (54,55,56,57).
Descartar embarazo
Se debe confirmar que las pacientes femeninas en edad reproductiva, no estén embarazadas, por lo tanto, deben consignar una prueba de embarazo negativa (33).
Pacientes que fueron sometidos a contraste yodado
Anteriormente, el uso de contrastes yodados durante la realización de estudios radiológicos como TC impedía la administración del RAI debido a interferencia del yodo contenido en el contraste, con el yodo radiactivo, sin embargo, evidencia reciente demuestra que los contrastes actuales son hidrosolubles y con un lapso de espera de 1 mes es suficiente, porque no disminuyen la captación de RAI (9).
Complicaciones del tratamiento
En general el RAI es seguro y bien tolerado, pero no está exento de efectos secundarios. Los efectos secundarios agudos más comunes incluyen disfunción de las glándulas salivales, que ocurre en 16 %-54 % de los pacientes, lo que lleva a sialoadenitis, epífora y disgeusia (58).
También se puede observar la pérdida transitoria del olfato y la disfunción gonadal temporal, con oligospermia en un 20 %-73 % de los pacientes masculinos y amenorrea en 20 %-27 % de las pacientes femeninas.
Los efectos tardíos crónicos incluyen xerostomía, disminución del gusto y disfunción de la glándula lagrimal que lleva a la sequedad de ojos (reportada en el 11 % de los pacientes). Además, en pacientes que reciben altas dosis de RAI (100-200 mCi) e incluso algunos que reciben dosis repetidas, la mayoría (60 %) presentan efectos a más largo plazo (más de 1 año) como la pérdida de sabor u olor. Anemia aplásica y mielosupresión, aunque raro, también se han descrito (59).
En el largo plazo, el riesgo más preocupante del RAI es la mayor probabilidad de desarrollar segundas neoplasias malignas primarias, debido a los efectos de la radiactividad por la concentración del yodo en otros tejidos del cuerpo. Rubino y col. (58) estimaron que para 100 mCi de RAI, la tasa de segundas neoplasias atribuibles a esta terapia serían 53 tumores malignos sólidos y 3 leucemias entre 10 000 pacientes seguidos durante 10 años.
Otro efecto tardío del RAI, es el desarrollo de fibrosis pulmonar, que ocurre en aquellos pacientes con CDT que tienen metástasis pulmonares. El riesgo de fibrosis pulmonar se correlaciona con la intensidad de la captación del 131I y varía inversamente con la edad del paciente, ocurriendo en el 10 % de los niños, pero solo en el 1 % de los adultos (60,61).
Se ha demostrado que el riesgo de fibrosis pulmonar depende de la dosis de RAI retenida en las metástasis pulmonares.
RCT diagnóstico antes de la administración de la dosis ablativa
La realización rutinaria de RCT diagnóstico previamente a la administración de la dosis ablativa no se recomienda. No obstante, en los casos en que la magnitud del remanente no sea clara, ya sea por dudas en cuanto a la extensión de la cirugía o en pacientes de alto riesgo o sospecha de metástasis a distancia, se podría considerar la realización de un RCT con una dosis baja de RAI (1 a 3 mCi), para evitar aturdimiento de la célula tiroidea (32).
RCT pos-dosis ablativa
Luego de aproximadamente 5-7 días posteriores a la administración de una dosis ablativa de RAI, se debe efectuar siempre un RCT. Esta conducta se justifica porque entre un 10 % y 26 % de los pacientes pueden presentar focos adicionales de enfermedad que modifican la estadificación inicial (33).
Por otro lado, el empleo de un equipo híbrido producto de la unión de una gammacámara SPECT (tomografía computarizada por emisión de fotón único o monofotónica) con un tomógrafo computarizado (SPECT/CT), tiene ventajas importantes, porque permite localizar anatómicamente los focos captantes, ayuda a incrementar la validez diagnóstica, lo cual podría llevar a cambios en la estrategia terapéutica hasta en un 40 % de los casos (62).
Papel del RAI en pacientes con CDT de bajo riesgo
La recurrencia de la enfermedad estructural en pacientes de bajo riesgo es menos del 2,1 % (33). Esto se ha demostrado en 3 estudios retrospectivos durante un período de seguimiento de 5-10 años (31,62,63,64,65).
El primer estudio prospectivo de Janovsky y col. (62) demostraron que los pacientes que no se sometieron a la ablación con RAI resultaron en remisión completa y con niveles de Tg que se volvieron indetectables en el transcurso del tiempo. No hay evidencia que sugiera que la ablación pos-quirúrgica mejore la tasa de recurrencia en pacientes de bajo riesgo. El riesgo general de enfermedad persistente será menor al 3 % cuando la Tg sérica sea indetectable, por toda esta evidencia no se recomienda el uso de RAI en pacientes de bajo riesgo para recurrencia.
Papel del RAI en pacientes de riesgo intermedio
Existen diferentes estudios retrospectivos donde se ha estimado que el riesgo de recurrencia en este grupo de pacientes es del 8 %, lo cual representa un porcentaje significativo y por lo tanto justifica la administración de la terapia con intención ablativa (66).
Diferentes autores han comparado la efectividad de la terapia con RAI en función de la actividad administrada, en un rango que varía entre 30 y 100 mCi. Castagna y col.,(63) compararon pacientes tratados con dosis bajas (30 o 50 mCi) o dosis altas (100 mCi) demostrando que no existen diferencias significativas en cuanto al porcentaje de remisión y presencia de recidivas de la enfermedad en ambos grupos durante el seguimiento.
La tendencia mundial se enfoca en obtener resultados óptimos con bajas dosis de RAI que nos permiten reducir los efectos adversos que pueden asociarse al uso de dosis altas (63,64,65,66,67). En promedio se usan 50 mCi en forma rutinaria.
Papel del RAI en paciente de alto riesgo
Se recomienda de forma rutinaria el uso de RAI después de la tiroidectomía total para los pacientes con riesgo alto por ATA, debido a que el riesgo de recurrencia (RR) cuando hay factores como la extensión extra-capsular nodal o la extensión extra-tiroidea, es alto. Cuando la extensión extra-capsular nodal es < de 3 ganglios comprometidos, el RR es del 2 %, pero con más de 3 adenopatías, el RR es del 38 %, igualmente el RR en pacientes con extensión extra-tiroidea, cuando es mínima es del 3 %-9 % y cuando es macroscópica, a estructuras adyacentes es del 23 %-40 % (32,53).
Es importante destacar que el RR en carcinoma folicular es del 30 % cuando existe una extensa invasión vascular (mayor a 4 focos) (33).
La dosis recomendada con intención ablativa en este grupo de pacientes está entre 100 a 150 mCi (33).
Las metástasis pueden ser descubiertas en el momento del diagnóstico o pueden ser identificadas durante el seguimiento. Si se encuentran después de la terapia inicial, algunos pacientes pueden lograr posteriormente una reducción de la carga tumoral con los tratamientos adicionales, que pueden ofrecer un beneficio en la supervivencia o de forma paliativa (68).
En los pacientes con enfermedad a distancia la dosis recomendada es de 100 mCi con intervalos 6 a 12 meses con un máximo de 6 dosis (66,67,68,69,70).
En los casos en que las metástasis tengan capacidad para concentrar RAI, este es el tratamiento de elección como primera línea. El pulmón es el sitio más frecuente de diseminación a distancia del CDT. En caso de lesiones únicas, se recomienda la resección. No obstante, la mayoría de los pacientes presentan lesiones múltiples. En las metástasis micro-nodulares el RAI es el tratamiento de elección (66). Este debe repetirse cada 6-12 meses, mientras se evidencie respuesta objetiva y en ausencia de toxicidad actínica. Dosis acumuladas por encima de 600 mCi no han demostrado mayor eficacia (68). Si bien el RAI es potencialmente curativo en 30 % de los casos, su utilidad se observa principalmente en pacientes jóvenes, con tumores bien diferenciados y enfermedad micro-nodular pulmonar. Independientemente de la capacidad de concentrar RAI, la curación es improbable en macro-metástasis pulmonares o metástasis óseas (68,71).
El tratamiento con RAI no debe repetirse en ausencia de beneficio objetivable independientemente de la intensidad de captación.
La dosis utilizada puede ser empírica o calculada por dosimetría. Las metástasis óseas ocurren en el 10 % de los pacientes con CDT, siendo más frecuentes en pacientes de edad avanzada. La utilidad del RAI es limitada en estos pacientes, observándose remisión de enfermedad en 0 %-7 %. Las metástasis cerebrales ocurren en menos del 1 % de los CDT, en los casos que presenten avidez por RAI, puede considerarse su uso (72).
Uso de PET/CT
El 18FDG PET/CT es una herramienta diagnóstica útil en pacientes con Tg elevada, cuando existe sospecha de enfermedad estructural y que no muestran captación de RAI en el rastreo corporal diagnóstico (sospecha de desdiferenciación) (73,74).
Asimismo, el 18FDG PET/CT es un indicador pronóstico de agresividad tumoral y de sobrevida (74).
PAPEL DE LA RADIOTERAPIA EXTERNA
1. Enfermedad residual macroscópica
2. Márgenes positivos (> 3 mm)
3. T4 N1 posquirúrgico (N extenso)
4. Adyuvante en caso de enfermedad macroscópica residual en pacientes de alto riesgo (disminución de la recaída locorregional)
5. Posoperatorio en mayores de 50 años con extensión extra-tiroidea macroscópica
6. Tumor o restos tumorales irresecables
7. Enfermedad local o ganglionar con extensión a tejidos blandos (no respuesta a RAI)
8. En combinación con RAI en T4 y N extenso
9. Pacientes de alto riesgo, con cirugías adecuadas, con enfermedad residual, que no recibirá RAI: controversial
10. Enfermedad ganglionar mayor de 2 cm- 3 cm o invasión extra-capsular nodal controversial (77)
11. Pacientes de alto riesgo, con enfermedad residual microscópica, en tumores con invasión a estructuras adyacentes
12. Enfermedad recurrente no controlable con cirugía ni RAI
13. Histologías de alto riesgo: carcinoma de células de Hürthle o de células altas (78,79)
14. Con fines paliativos:
a. Grandes masas tumorales o ganglionares irresecables
b. Hemorragia
c. Estridor
d. SVCS
e. Disfagia
f. Compresión medular
g. Compresión radicular
h. Metástasis óseas: en combinación de cirugía cuando sea posible y con tratamiento con 131I si hay captación en las metástasis, (como tratamiento resolutivo o como control del dolor)(80,81)
i. Metástasis en SNC: está indicada la Rt si no son operables ni ávidas de yodo (72)
TÉCNICAS DE TRATAMIENTO
• Rt 2D
• Rt 3D
• IMRT
• Rapid Arc
En el tratamiento de la radioterapia externa se deberá colocar al paciente en posición decúbito supino y con colocación de mascara termoplástica a fin de garantizar la inmovilización del paciente TC de planificación con cortes cada 2 mm -3 mm, uso de contraste EV.
El volumen blanco clínico (CTV) en pacientes de bajo riesgo, incluye lecho tiroideo, ganglios no afectados cervicales bilaterales (niveles II-IV,VI ± retro-faríngeos) y el mediastino superior. El CTV de alto riesgo incluye el lecho tumoral primario, los ganglios centrales y los niveles ganglionares afectados. La dosis para el CTV de bajo riesgo 54 Gy y para el CTV de alto riesgo 60 Gy para el volumen tumoral inicial, y 66-70 Gy para enfermedad microscópica y macroscópica (79,80,81,82,83).
Volumen blanco clínico (CTV) y dosis de radioterapia externa en el cáncer de tiroides bien diferenciado
Grupos CTV Dosis
Bajo riesgo Ganglios no afectados 54 Gy
Cervicales bilaterales Mediastino superior
Alto riesgo Lecho tumoral primario 60 Gy en vol tumoral inicial Ganglios centrales 66-70 Gy en enfermedad Ganglios centrales residuales
Ganglios afectados
En la enfermedad residual microscópica se debería administrar una dosis total de 50-60 Gy al cuello, FSC y mediastino superior, en 25-30 fracciones, 5 por semana. Boost de 5-10 Gy a la enfermedad residual macroscópica y plastrones adenopáticos.
ÓRGANOS A RIESGO
Esófago 50-60 Gy
Glándulas salivares 26-32 Gy
Médula espinal 45 Gy
Plexo braquial 60 Gy
Pulmón 20 Gy
COMPLICACIONES DEL TRATAMIENTO
• Agudas: esofagitis, faringitis, mucositis, xerostomía, linfedema, epidermitis, laringitis
• Tardías: fibrosis cutánea, estenosis traqueal, estenosis esofágica (82).
SEGUIMIENTO
1. TERAPIA HORMONAL DURANTE EL SEGUIMIENTO
Durante los dos primeros años:
Pacientes sin evidencia de enfermedad
Alto riesgo TSH < 0,1 mUI/L por 3-5 años.
Pacientes con persistencia de enfermedad (bioquímica o estructural) TSH < 0,1 mUI/L
Riego intermedio TSH < 0,1 mUI/L por 3-5 años.
Riesgo bajo TSH 0,3 a 2,0 mUI/L (32)
2. SEGUIMIENTO A LARGO PLAZO
¿Cómo y cuándo evaluar después de aplicado el tratamiento?
EL nivel de Tg sérica y la ecografía de cuello, son las herramientas fundamentales para definir curación, enfermedad bioquímica (Tg elevada) o estructural (enfermedad visible en estudios de imágenes ECO, TC o RM) (40).
Parámetros indicativos de inactividad de la enfermedad
• Ausencia de manifestaciones clínicas.
• Tg < 0,1 mUI/L bajo terapia hormonal, en ausencia de AcTg.
• Ecografía de cuello sin lesiones sospechosas a nivel de lecho tiroideo o en cadenas ganglionares.
• Ausencia de estimulación de Tg posterior a la administración de rhTSH o TSH endógena.
Qué evaluación hacer de acuerdo al riesgo
• Bajo riesgo sin tratamiento ablativo
Determinación de Tg y AcTg, ecografía de cuello. Los hallazgos negativos sugieren remisión y continuarán con controles anuales.
Tg >1 ng/mL mantener determinaciones periódicas de Tg, AcTg y observar comportamiento de los mismos.
• Bajo riesgo más tratamiento ablativo
En pacientes de bajo riesgo con ablación, se debe medir Tg y AcTg bajo terapia hormonal asociado a ecografía cervical en intervalos de 6-12 meses (33).
Dentro de los primeros 2 años se recomienda solicitar Tg estimulada (rhTSH o suspensión hormonal) en pacientes con respuesta incompleta (32,53). El RCT diagnóstico no adiciona datos de relevancia en este grupo de pacientes.
• Riesgo intermedio
17 % 40 % de los pacientes de este grupo presentarán evidencia de enfermedad estructural en el seguimiento a largo plazo. En este grupo se sugiere solicitar Tg bajo terapia hormonal cada 6 meses luego del tratamiento inicial. Si estos valores fueran indetectables, está indicada la medición de Tg estimulada dentro de los primeros 12-24 meses de seguimiento. La realización de un RCT diagnóstico asociado a la medición de Tg estimulada en pacientes de riesgo intermedio, es recomendada.
• Riesgo alto
El seguimiento de pacientes de alto riesgo debe hacerse de manera estricta dentro de los primeros 6 meses de tratamiento dada la elevada posibilidad de persistencia de enfermedad estructural. Las recurrencias se presentan en alrededor del 45 % al 85 % de este grupo de pacientes. En la mayoría de los casos las lesiones son locales.
Cuando los niveles de Tg bajo terapia hormonal supresiva son indetectables, se recomienda efectuar un primer control de ecografía y Tg estimulada a los 6 meses. Si la Tg es detectable bajo terapia inhibitoria y se desconoce la localización de la enfermedad, se recomienda la búsqueda de recurrencia estructural mediante estudios de diagnóstico por imágenes (TC con contraste y/o RM). Igualmente, el RCT se recomienda en este grupo.
Aspectos de importancia en relación a la determinación de Tg
El método más utilizado en el presente para su determinación es el inmunorradiométrico. Estudios comparativos han demostrado variación significativa del valor obtenido con diversos ensayos comerciales, por lo que se recomienda utilizar el mismo método en el seguimiento del paciente. La ATA (33), sugiere la calibración del ensayo con el estándar internacional CRM457.
El radioinmunoensayo es poco utilizado en la actualidad. La mayoría de los ensayos tienen una sensibilidad funcional de 1 ng/mL, sin embargo, han sido desarrollados ensayos ultrasensibles con una sensibilidad funcional de 0,2 ng/mL. La utilización de ensayos ultrasensibles en el futuro reduciría la necesidad de realizar Tg estimulada en el seguimiento de paciente de mayor riesgo, porque en estudios publicados se demostró que un valor < 0,2 ng/mL en la mayoría de los casos coincide con valores de Tg estimulada menor a 2 ng/mL, bajo terapia hormonal (4,6).
AbTg
Deben ser determinados conjuntamente con la Tg porque su presencia en el suero, interfiere con el ensayo, dando valores inferiores al valor real cuando se utilizan ensayos inmunorradiométrico, mientras que se produce una sobrestimación con métodos de radioinmunoensayo.
El título de anticuerpos puede variar en el tiempo, por tanto, deben determinarse cada vez que se requiere evaluar Tg. Su elevación durante el seguimiento del paciente, es sugestivo de recurrencia (6).
En la actualidad, en Venezuela, los métodos utilizados por un mismo laboratorio pueden variar dependiendo de la disponibilidad en el mercado; el médico tratante está en la obligación de obtener la información correspondiente, para la correcta interpretación de los resultados.
CDT IODO REFRACTARIOS
El CDT tiene una baja mortalidad y representa el 0,3 % de todas las muertes por cáncer. Sin embargo, el 10 % de estos pacientes tienen un pobre pronóstico con una enfermedad local avanzada o enfermedad metastásica difusa que puede severamente afectar la calidad de vida (84).
El pronóstico en pacientes con CDT es usualmente favorable aun cuando las metástasis ávidas de 131I estén presentes. Por esta razón el RAI es considerado el gold standard en el tratamiento de enfermedad metastásica.
Los pacientes con enfermedad metastásica al momento del diagnóstico representan el 5 % de todos los CDT, de los cuales el 25 % puede ser definitivamente curado con 131I, 45 % tienen metástasis que al inicio son ávidas de 131I pero nunca alcanzan la cura definitiva y 30 % tienen metástasis a distancia incapaz de captar 131I desde el primer tratamiento (84). Estos dos últimos grupos representan aquellos casos definidos como refractarios al 131I y que junto a los carcinomas pobremente diferenciados que son el 5 % de todos los casos de carcinoma de tiroides, representan un desafío clínico real para su tratamiento. Afortunadamente estos tumores son de crecimiento lento en la mayoría de los casos (85).
No hay indicación para posteriores tratamientos con 131I cuando el paciente es clasificado como refractario aunque el tumor lo capte.
Cuando el tumor pierde la capacidad de concentrar 131I, después que previamente lo captaba que generalmente ocurre en pacientes con grandes y múltiples metástasis, es debido a la erradicación de las células diferenciadas por el tratamiento con 131I y no a las pobremente diferenciadas que no captan 131I y progresaran.
Cuando la enfermedad progresa a pesar de que exista una significativa captación de 131I en los meses siguientes al tratamiento, está claro que no habrá respuesta tumoral a subsiguientes tratamientos con 131I, aún con actividades altas, y en estos pacientes no hay indicación a proseguir con otro curso de tratamiento (33, 85).
La radiorefractariedad incluye pacientes que han recibido más de 600 mCi de dosis acumulativa de 131I debido a que estos pacientes no se benefician de tratamientos adicionales (85).
Los pacientes con CDT metastásico refractarios al 131I, frecuentemente tienen un curso clínico indolente sin síntomas aparentes o impacto adverso por muchos años.
En ausencia de tratamientos tolerables con significante probabilidad de inducir remisión completa o mejoría en la SG, el tratamiento debería ser limitado a intervenciones que previenen morbilidad o paliación de síntomas.
Así, una vez que la enfermedad metastásica refractaria ha sido definida, la atención debería ser dirigida a:
- Determinar la extensión de la enfermedad metastásica por estudios de imagen como TC, FDG-PET/CT o RM
- Evaluar el grado de síntomas actuales o potenciales de la enfermedad
- Comprender las comorbilidades que pueden influenciar la escogencia de terapias para la enfermedad metastásica
- Determinar la tasa de progresión de lesiones radiológicamente evidentes (32,33,34,35,36,37,38,39,40,41,42,43,44).
El tratamiento de las metástasis en CDT es multidisciplinario, especialmente en metástasis óseas, incluyendo ablación y/o cementoplastia, asociado a tratamiento sistémico, a fin de mejorar la calidad de vida, disminuir el dolor y evitar en el tiempo los eventos esqueléticos.
Muchos progresos han sido realizados en los últimos años en el tratamiento CDT avanzado con la aprobación de varios inhibidores de kinasa. Desafortunadamente estas drogas no son curativas y los pacientes eventualmente desarrollan resistencia. Además, muchos pacientes con enfermedad metastásica o recurrente tienen un curso indolente. Por eso estas drogas son reservadas para pacientes con enfermedad progresiva o aquellos con enfermedad que estén afectando estructuras vitales o causando síntomas substanciales (86).
Los tratamientos localizados pueden ser considerados para pacientes con enfermedad lentamente progresiva y de este modo retardar la necesidad del tratamiento sistémico. Por ejemplo la radioterapia externa o el embolismo en el caso de Mt óseas o hepáticas, en aquellos pacientes que puedan causarle morbilidad (82,86).
En pacientes con enfermedad locorregional, la cirugía debería ser considerada en el entorno apropiado y la metastasectomía puede ser considerada para enfermedad metastásica de bajo volumen si esto retardaría o prevendría morbilidad (87).
En los últimos años considerables investigaciones dedicadas al CDT han sido realizadas. La expresión del factor de crecimiento vascular esta aumentada en carcinoma de tiroides y su expresión se relaciona con la patogénesis del carcinoma tiroideo, esto ha llevado a investigadores a evaluar el uso de drogas que bloqueen estas vías en pacientes con enfermedad avanzada (52). Estudios clínicos con resultados exitosos han llevado a la aprobación de 2 inhibidores de la enzima tirosin kinasa por la US Food and Drug Administration y European Medicines Agency, el Sorafenib y el Lenvatinib. Estas drogas son inhibidores multikinasa con propiedades antiangiogénicos. No se deben usar en pacientes con enfermedad estable, lentamente progresiva o que tengan morbilidades específicas que exacerben las toxicidades de estos fármacos.
Se debe instruir al paciente acerca de los riesgos y beneficios del tratamiento, además del mantenimiento de la supresión de la TSH con el uso de la levotiroxina.
Las complicaciones inherentes al tratamiento afectan negativamente la calidad de vida, por lo que se disminuye la dosis en 2/3 de los casos, y suspensión del mismo en el 20 %. Son susceptibles a complicaciones mayores como trombosis, hemorragias, IC, endocrinopatías, hepatotoxicidad, fistulas y perforación GI y riesgo de muerte del 1,5 %-2 %.
SORAFENIB
El Sorafenib fue aprobado para el CDT en 2013 en base a los resultados favorables de un ensayo clínico multicéntrico fase 3, aleatorizado, doble ciego, placebo controlado (DECISION) (85) donde se incluyeron 457 pacientes con estadio avanzado o metastásico de CDT (papilar, folicular, de células Hürthle y poco diferenciado) en progresión, refractario a RAI que no habían recibido quimioterapia, inhibidores de tirosina kinasa, anticuerpos monoclonales anti VEGF, fueron asignados a recibir 400 mg de Sorafenib dos veces al día continuo o placebo. El 96 % de los pacientes tenían enfermedad metastásica. El estudio evidenció un aumento en la sobrevida libre de progresión con una reducción del riesgo de progresión de la enfermedad o fallecimiento del 41 %. La mediana de sobrevida libre de progresión fue de 10,8 meses para Sorafenib vs., 5,8 meses para placebo.
LENVATINIB
El ensayo con Lenvatinib (SELECT), un estudio multicéntrico fase 3 aumentó significativamente la supervivencia libre de progresión (SLP), en comparación con el placebo (86). Lenvatinib (24 mg diarios) muestra una mediana de SLP de 18,3 meses, frente a los 3,6 meses del placebo. Además, el estudio destaca la respuesta rápida obtenida con Lenvatinib, con una mediana de tiempo transcurrido hasta producirse la primera respuesta objetiva de dos meses y una tasa de respuesta objetiva del 64,8 %, frente al 1,5 % observado con placebo. La droga fue aprobada en 2015. En un subgrupo de análisis de este estudio, una mejoría significante en la sobrevida general, fue observada en pacientes mayores de 65 años comparados con pacientes menores de 65 años.
En una comparación indirecta entre Lenvatinib y Sorafenib, el primero logró una sobrevida libre de progresión mayor (86).
Ningún ITK tiene efecto citotóxico, las células no se destruyen solo se mantienen en estado quiescente, por tal motivo no se observan respuestas completas. La respuesta se debe a isquemia tumoral, por lo que el tratamiento se mantiene por tiempo indefinido hasta la progresión o efectos tóxicos intolerables.
OTROS INHIBIDORES DE LA ENZIMA TIROSIN KINASA
El rol de otros inhibidores de tirosina kinasa (pazopanib, vandetanib, axitinib) en CDT no está bien definido. Se está evaluando la eficacia de estos fármacos en relación a alteraciones de las vías de señalización intracelular. Vemurafenib ha sido estudiado en carcinoma papilar de tiroides con BRAF mutado con buenos resultados.
Toxicidad de inhibidores de tirosina kinasa
La vigilancia y la intervención oportuna en las toxicidades pueden afectar la calidad de vida o ser fatales, por lo que se debe hacer una selección adecuada de los pacientes y monitorizarlos para detectar los efectos tóxicos.
Estos inhibidores de tirosina kinasa están también asociados con efectos adversos como hipertensión, exantema, síndrome mano-pie, diarrea, fatiga, pérdida de peso, estomatitis, cardiotoxicidad (disminución de la FE y aumento del intervalo QT), hepatotoxicidad, alteraciones endocrinas (aumenta los niveles del TSH, por lo que debe medirse antes del tratamiento).
QUIMIOTERAPIA
La quimioterapia ha sido poco evaluada, y muchas veces en forma inadecuada al incluir en los estudios a pacientes con todas las histologías. No hay evidencias que otras drogas o la combinación de ellas produzca más beneficio que la doxorrubicina como monodroga, siendo el beneficio de esta discutible y marginal.
Pacientes con progresión de la enfermedad con respuesta inicial a IQ, sin efectos adversos prohibitivos, van a segunda línea de IQ, en el marco de ensayos clínicos terapéuticos.
TRATAMIENTO DE LAS METÁSTASIS CEREBRALES
• Resección quirúrgica.
• Radioterapia estereotáxica, preferible a Rt a todo encéfalo.
Las Mt cerebrales se ven más en pacientes mayores, con enfermedad avanzada, y tienen mal pronóstico.
TRATAMIENTO DE LAS METÁSTASIS ÓSEAS
• Bifosfonatos (pamindronato 90 mg, ácido zolendrónico 4 mg, ibandronato 150 mg mensual)
• Denosumab (anticuerpo monoclonal inhibidor de RANK-ligando, dosis: 120 mg subcutáneo cada 4 semanas)
Se usa en pacientes con Mt óseas difusas o sintomáticas de CDT refractario al yodo, como único tratamiento o con otras terapia sistémicas. Su eficacia se basa en la experiencia en el uso en otros tumores sólidos con metástasis óseas.
Debe tener niveles de calcio y función renal adecuados, y realizarse evaluación odontológica por la probabilidad de necrosis de maxilar (87).
CDT CONSIDERACIONES PEDIÁTRICAS
Los carcinomas de la glándula tiroides son neoplasias poco frecuentes en las primeras décadas de la vida, con una prevalencia del 4 % de todas las neoplasias malignas en niños y adolescentes y un incremento de nuevos casos del 1,8 % en menores de 20 años reportado en los EE.UU. Su incidencia viene aumentando sobre todo en el grupo de pacientes con edades comprendidas entre los 15 y 19 años hasta un 5 % según datos del departamento de vigilancia epidemiológica del Instituto Nacional del Cáncer de los EE.UU para el año 2015. La incidencia de malignidad de los nódulos tiroideos diagnosticados en este grupo etario es del 20 % al 26 % (90,91).
En la población general, la incidencia de CDT varía de 0,2 a 5 casos por millón de personas/año, con lo que se convierte en la neoplasia endocrina más frecuente. Entre las variedades del CDT, el carcinoma papilar (CP) es la forma que más se presenta en la edad pediátrica (90 %), esporádicamente se observa el carcinoma folicular (CF) y menos a menudo los carcinomas medular y anaplásico (92).
A diferencia de los adultos, el CDT tiene una presentación más agresiva en los niños, es frecuentemente multifocal, bilateral y con metástasis en ganglios linfáticos regionales. Las metástasis a pulmón ocurren sobre el 25 % de los casos. A pesar de esta presentación clínica, las tasas de supervivencia de estos tumores son elevadas, cercanas al 95 % a los 15 años de seguimiento. (93).
Antes de la pubertad, la incidencia del CDT es similar en ambos sexos. Durante la pubertad se incrementa en hasta 10 veces su incidencia y es en una relación 5:1 más frecuente en el sexo femenino (91).
Dado las diferencias existentes en relación con la forma de presentación, las bases moleculares y la evolución del CDT en la edad pediátrica, la American Thyroid Association (ATA) Task Force on Pediatric Thyroid Cancer publicó las guías para el tratamiento de los nódulos tiroideos y el cáncer diferenciado de tiroides en los niños, basadas en opiniones de panel de expertos y datos probatorios científicos hasta la fecha de su publicación. La edad pediátrica se considera en dicho documento a todo paciente menor de 18 años (92).
Los niños con CDT en forma ideal deben ser tratados por equipos multidisciplinarios con experiencia, para asegurar una terapia óptima que ayude a disminuir la posibilidad de que la opción terapéutica escogida sea, demasiado agresiva o inadecuada (91,94).
A pesar de que los nódulos tiroideos son más frecuentes en los adultos, en la población pediátrica hay mayor riesgo de que sean malignos y es por esto que la conducta ante los mismos varía de acuerdo a la edad de presentación, siendo distinta a la recomendada en la adultez. Se han asociado diversos factores de riesgo al desarrollo de nódulos tiroideos en los niños y estos incluyen la deficiencia de iodo, historia de exposición a radiaciones, antecedentes de enfermedad tiroidea y algunos síndromes genéticos (91).
Recomendaciones para la evaluación preoperatoria en cáncer de tiroides diferenciado en niños y adolescentes
a. Ecosonografía detallada de todas las regiones del cuello, realizada por un médico con experiencia.
b. TC o RM de cuello: se deben considerar cuando se sospeche invasión del tracto aerodigestivo.
c. RX o TC del tórax: pacientes con enfermedad considerable en los ganglios linfáticos cervicales.
d. Estudios moleculares: considerar en las citologías indeterminadas dada la alta probabilidad de malignidad en estas categorías, siendo útiles para definir la conducta terapéutica. A diferencia del adulto, en la edad pediátrica las mutaciones BRAF son muy raras, siendo más comunes la presencia de genes re-acomodadores RET/PTC (95).
Las mutaciones puntuales del BRAF y del RAS se relacionan con una manifiesta diferenciación en la estabilidad genómica por descenso de expresión del co-transportador sodio/iodo. En contraste los RET reacomodadores, más comunes en carcinoma papilar de tiroides en niños, no llevan a inestabilidad genómica. Estas diferencias moleculares podrían explicar la mejor respuesta al tratamiento con radioiodo (RAI) en niños con carcinoma papilar, la baja mortalidad y la rara progresión de los tumores poco diferenciados (94,96).
De la Ecografía y PAAF
a. En niños, el tamaño del nódulo no predice la malignidad por los cambios en el volumen de la tiroides asociado al crecimiento. Por tanto, las características ecográficas y el contexto clínico (crecimiento rápido del nódulo) podrían ser utilizados para identificar los nódulos a ser punzados en este grupo etario.
b. Una diferencia importante del CPT en niños es que pudiera presentarse como infiltración difusa de la glándula; cuando la misma está asociada a adenopatías cervicales palpables y/o micro calcificaciones debe sospecharse el diagnóstico de carcinoma y hacer PAAF.
c. El riesgo de malignidad para las categorías indeterminadas es mayor en los niños respecto a los adultos. En la categoría 3, 28 % vs., 5 % a 15 %. En la categoría 4, 58 % vs., 15 % a 30 %. Este riesgo elevado de probabilidad de malignidad en los niños justifica que se recomiende la intervención quirúrgica para categorías indeterminadas de PAAF en la edad pediátrica (95).
CIRUGÍA EN NIÑOS
Basado en el hecho de que los niños y adolescentes muestran una elevada incidencia de enfermedad bilateral y multifocal con mayor riesgo de recurrencias se recomienda la tiroidectomía total en la mayoría de los pacientes en este grupo etario; además, para optimizar el seguimiento con Tg y el RCT. Alternativamente, en los casos de un tumor unilateral, confinado a la tiroides y de pequeño tamaño se podría considerar tiroidectomía cercana a la total. Estas consideraciones deben ser analizadas en el contexto general del paciente (88,89,90,91).
La disección terapéutica de los ganglios del compartimiento central del cuello está indicada si hay evidencia pre o intraoperatoria de metástasis central, lateral y/o evidencia clínica de invasión extra tiroidea.
La disección profiláctica del compartimiento central del cuello puede ser considerada de acuerdo al tamaño del tumor, a su focalización y a la experiencia del cirujano; no así en el caso de los compartimientos laterales donde la disección profiláctica no es usualmente recomendada (97,100). El riesgo de complicaciones quirúrgicas es mayor en los pacientes pediátricos que en los adultos, más aún en los menores de 10 años, en presencia de extensión extra-tiroidea, disección ganglionar y cirugías repetidas. Las más frecuentes son el hipoparatiroidismo transitorio o permanente, por lo que se recomienda en el posoperatorio inmediato realizar mediciones seriadas de calcio, fósforo, PTH (un valor de PTH intacta menor de 10 a 15 pg/mL está correlacionada con elevado riesgo de desarrollar hipocalcemia clínicamente significativa) (98) y el autotransplante de tejido paratiroideo; respectivamente. Otras complicaciones son lesión del nervio laríngeo recurrente y del nervio espinal accesorio.
Recomendaciones para la evaluación posoperatoria en cáncer de tiroides diferenciado en niños y adolescentes
a. Clasificación y asignación del riesgo
Pese a los datos probatorios limitados para el entorno pediátrico, el Sistema TNM del American Join Comittee on Cancer/International Union against Cancer (AJCC/UICC) es recomendado por la ATA Task Force para definir el riesgo de enfermedad cervical persistente en niños y determinar cuáles pacientes podrían estudiarse para descarte de metástasis a distancia y definir aquellos que se beneficiarían de terapia adicional. Usando este sistema se puede clasificar a los pacientes en 3 grupos de riesgo:
- Bajo riesgo: enfermedad confinada a la tiroides, N0 o NX, o pacientes con N1a diagnosticada de manera fortuita (metástasis microscópica en un número pequeño de ganglios centrales del cuello). Si bien estos pacientes tienen el riesgo más bajo de metástasis a distancia, aún tienen riesgo de enfermedad cervical residual; en particular, si la cirugía inicial no incluyó una disección central del cuello.
- Riesgo intermedio: enfermedad extensa N1a o enfermedad N1b mínima. Si bien estos pacientes tienen un riesgo bajo de metástasis a distancia, tienen un aumento del riesgo de una resección incompleta de ganglios linfáticos y de enfermedad cervical persistente.
- Alto riesgo: enfermedad regional extensa (N1b) o enfermedad localmente invasora (T4), con metástasis a distancia o sin esta. Los pacientes de este grupo tienen el riesgo más alto de resección incompleta, enfermedad persistente y metástasis a distancia.
En los últimos años se han producido cambios sustanciales en el enfoque de la estratificación de riesgo del CPT propuesta por las guías ATA 2015, con miras a ser reemplazado por la llamada estratificación dinámica de riesgo (“Dynamic Risk Stratification”, DRS por sus siglas en inglés) donde se evalúa la respuesta al tratamiento aplicado mediante los estudios de imágenes, los niveles de Tg (estimulada o suprimida) y el nivel de los AbTg para asignar las siguientes categorías: excelente respuesta, respuesta bioquímicamente incompleta, respuesta estructuralmente incompleta o respuesta indeterminada (Cuadro 7) con el fin de mejorar la predicción y el riesgo de enfermedad recurrente e individualizar el manejo y el seguimiento del paciente (100,101.102,103).
Varios estudios retrospectivos muestran una alta proporción de pacientes inicialmente clasificados como riesgo intermedio o alto que lograron completar remisión (101, 104, 105).
Esta estratificación se ha propuesto para ser utilizada durante los 2 primeros años de tratamiento con seguimiento en cualquier momento. Se considera que el riesgo de recurrencia para CPT en un paciente en particular varía de acuerdo a la respuesta obtenida a la terapéutica (101,104).
Falta validar este nuevo enfoque de estratificación de riesgo en estudios prospectivos, con mayor número de pacientes y tiempo de seguimiento más prolongados.
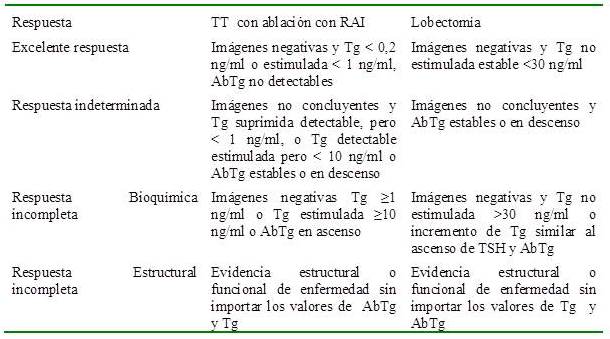
Cuadro 7.
Definición de estratificación dinámica de riesgo basada en la respuesta inicial al tratamiento
*Tg:tiroglobulina,* AbTg: Anticuerpos antitiroglobulina, *RAI :Iodo radiactivo *TT: tiroidectomía total *TSH: hormona estimuladora del tiroides.
Determinación de Tg y AbTg solo en los pacientes a los que se haya realizado tiroidectomía total
Los niveles de Tg sérica sirven como un marcador sensible de enfermedad recurrente o residual. En conjunto con el US y otros estudios de imágenes la Tg es esencial en el manejo de CPT pediátrico tanto en la clasificación inicial de riesgo en el posoperatorio, como en la posterior re-estratificación y seguimiento a largo plazo (91).
Es importante que ambas determinaciones sean realizadas de manera simultánea, en el mismo laboratorio y que este sea confiable, haciendo especial énfasis en el control de calidad. Asimismo, es necesario determinar el nivel de corte de acuerdo al método de laboratorio utilizado.
El valor de Tg pos-estimulación de TSH en ausencia de AbTg debe ser menor a 2 ng/mL; con resultados entre 2 a 10 ng/mL en ausencia de otra evidencia de enfermedad activa puede ser indicativo de un paciente libre de enfermedad, sobre todo si los niveles son estables o decrecientes en el tiempo. Al contrario, una elevación en el valor de la Tg es sugestivo del reinicio clínico de la enfermedad y en el caso de un valor de Tg (TSHe) mayor de 10 ng/mL se necesitan de otras evaluaciones para localizar la enfermedad y decidir si se indica cirugía adicional, terapia con RAI o considerar una conducta expectante (91).
Hay estudios que sugieren que los niveles de Tg en niños pueden ser mayores que en adultos con similar extensión de la enfermedad (95).
Debido a que los AbTg responden a cambios en los niveles de Tg circulante, los mismos representan indirectamente cambios en la masa del tejido tiroideo por lo tanto son útiles como marcador tumoral del CPT. Similar a lo que ocurre con la Tg, la tendencia en las concentraciones de AbTg es más relevante para detección de enfermedad que una sola medición.
Hay que tomar en cuenta que la presencia de AbTg puede interferir con los valores obtenidos de Tg pudiendo ser falsos negativos y/o falsos positivos.
Iniciar tratamiento supresivo con levotiroxina sódica para evitar hipotiroidismo posterior
La estadificación inicial se deberá realizar dentro de las 4-6 semanas posteriores a la cirugía con el propósito de evaluar si hay indicios de enfermedad locorregional persistente e identificar a los pacientes con más probabilidades de beneficiarse de la terapia adicional con 131I (RAI)
USO DE RAI EN NIÑOS Y ADOLESCENTES
En la mayoría de los casos, la evaluación, tratamiento y seguimiento de los niños con neoplasia tiroidea se ha realizado basado en las guías de tratamiento para los adultos. Hasta ahora, este enfoque dio como resultado una elevada tasa de curación, pero requirió que todos los niños fueran sometidos a una terapia que incluía tiroidectomía total seguida de ablación con RAI. Desafortunadamente, estudios recientes, con seguimiento que abarcan varias décadas, revelan un aumento en la mortalidad por todas las causas para los sobrevivientes de CDT infantil, siendo en la mayoría de los casos debido a segundos tumores malignos en niños tratados con radiación (95, 97, 98,99,100).
En la preparación de los pacientes pediátricos para el uso del RAI se debe asegurar un valor de TSH de 30 o más mUI/mL. La mayoría lo alcanza con suspensión del tratamiento con levotiroxina por 2 semanas; para tal fin también se puede indicar rhTSH. Aunque los datos son escasos en niños, se cree que se pueda usar la misma dosis que para adultos (0,9 mg por 2 dosis cada 24 h) sobretodo en los casos donde el hipotiroidismo endógeno debiera ser evitado o cuando sea imposible que la TSH aumente con la omisión de levotiroxina (95).
Determinación de la actividad de RAI terapéutico
El uso de RAI en el posoperatorio es un tema controversial, especialmente en los pacientes de bajo riesgo, no sólo porque hay menos niños con CDT de bajo riesgo, sino porque los mismos presentan un elevado riesgo de recurrencia en comparación con los adultos (100).
A pesar de la evidencia de que el tratamiento con RAI puede mejorar la supervivencia libre de enfermedad en adultos jóvenes y posiblemente en adolescentes (97). Rivkees y col. (104) evaluaron una serie de factores en niños y adolescentes con CDT promoviendo la ablación en este grupo, lamentablemente todos los estudios al respecto son de carácter retrospectivo y muestran datos contradictorios sobre la ablación del remanente en pacientes pediátricos de bajo riesgo. A pesar de esto, las recomendaciones actuales sugieren que para el paciente pediátrico de bajo riesgo, el RAI puede ser omitido y debe realizársele seguimiento de la enfermedad con niveles Tg y US de cuello.
La gran mayoría de los pacientes pediátricos tendrán compromiso ganglionar (94, 105) Por lo que, el uso del RAI se ve favorecido en este escenario.
Debido a las diferencias en el peso corporal, en el clearence del iodo en los niños comparado con los adultos, los efectos de éste pueden ser amplificados en este grupo etario debido además a que la actividad del iodo radiactivo es distribuida en distancias más cortas, es captado por órganos más pequeños y se acumula en células en crecimiento, se recomienda que el cálculo de la dosificación sea hecha por expertos en niños.
La administración terapéutica de RAI se basa comúnmente en dosificación empírica o dosimetría corporal total. No existen actividades estandarizadas de RAI para niños y adolescentes, no hay datos que comparen la eficacia, seguridad o los resultados a largo plazo de la administración de RAI en niños que usen estos diferentes enfoques (95).
Las actividades de RAI para tratar la enfermedad residual deben basarse en el peso corporal (1,0-1,5 mCi /kg; 37-56 MBq /kg) (95).
La dosis más alta que sea segura (nivel AHASA) que se ha determinado para el tratamiento de recurrencia o metástasis a distancia por CDT, está determinada en actividades de hasta 2,5 a 5 mCi / kg (200 MBq / kg), demostrando ser el límite seguro más bajo (106,107).
Los niños con metástasis pulmonares iodocaptantes visualizadas con RCT, son buenos candidatos para la terapia con RAI (96). Leboulleux y col. (106) detallan su enfoque terapéutico con RAI, en niños con metástasis pulmonares de CDT. La dosis administrada fue de 1 mCi (37 mBq) / kg). El tratamiento se repitió cada 6 meses hasta que el paciente se consideró curado. Entre 4 a 6 tratamientos lograron curación en el 80 % de los niños. Para pacientes con enfermedad pulmonar, el riesgo de fibrosis pulmonar se redujo mediante el uso de 1 mCi/ kg o menos y más de 6 meses de intervalo inter-tratamiento (100).
La administración de varios tratamientos con RAI pueden dar como resultado la remisión de la enfermedad o enfermedad metastásica estable, provocando baja mortalidad específica (95).
La frecuencia óptima de tratamientos con RAI no ha sido determinada. Se sugieren intervalos más largos entre los tratamientos con RAI en el niño que no demuestra enfermedad progresiva (95). Si la respuesta clínica, estructural y bioquímica de la Tg sugiere enfermedad persistente o progresión después de la terapia con RAI, se recomienda una evaluación adicional con un RCT con dosis bajas (2 a 3 mCi) y un nivel de Tg estimulada y luego se debe repetir el tratamiento, siempre que hayan transcurrido 12 meses desde la actividad previa de RAI. En todos los casos, los tratamientos repetidos con RAI deben considerarse solo si se sabe o se presume que el paciente tiene una enfermedad yodo ávida y no ha recibido actividades acumuladas altas del mismo. Si el paciente persiste con enfermedad o esta progresa a pesar de las altas dosis recibidas, es poco probable que la terapia adicional con RAI sea útil (97).
SEGUIMIENTO
Los niveles de riesgo pediátrico establecidos por la ATA ayudan a determinar el alcance de las pruebas en el seguimiento
a. En caso de bajo riesgo
• Medición de Tg con inhibición de la TSH; cada 3 a 6 meses durante 2 años y luego anual
• No es necesaria la realización de RCT diagnóstico con 131I
• Medición de TSH: se debe procurar mantener concentraciones de 0,5 a 1,0 mUI/L
• Ecografía de cuello: a los 6 meses de la cirugía y luego, cada año durante 5 años.
b. En caso de riesgo intermedio
• Medición de Tg con estimulación de la TSH. Las concentraciones de Tg (durante la terapia de reemplazo hormonal) se miden cada 3 a 6 meses durante 3 años y, luego, cada año
• RCT diagnóstico con 131I para estratificación y determinación de estatus de la enfermedad
• Medición de TSH: se debe procurar mantener concentraciones de 0,1 a 0,5 mUI/L.
• Ecografía de cuello: para los pacientes sin indicios de enfermedad, la vigilancia debe realizarse a los 6 meses de la cirugía y, luego, cada 6 a 12 meses durante 5 años (después, con menor frecuencia); se debe considerar la evaluación de la Tg con estimulación de la TSH y el RCT con 131I al cabo de 1 o 2 años.
c. En caso de alto riesgo
• Evaluación de la Tg con estimulación de la TSH. Las concentraciones de Tg (durante la terapia de reemplazo hormonal) se miden cada 3 a 6 meses durante 3 años y luego, cada año
• RCT con 131I para estratificación y determinación de estatus de la enfermedad.
• Medición de TSH: se debe procurar obtener concentraciones menores o iguales de 0,1 mUI/L
• Ecografía de cuello: para los pacientes sin indicios de enfermedad, la vigilancia debe incluir una ecografía a los 6 meses de la cirugía y luego, cada 6 a 12 meses durante 5 años (después, con menor frecuencia).
En niños y adolescentes el tratamiento supresivo con levotiroxina a largo plazo ha sido poco estudiado; sin embargo, los riesgos potenciales descritos incluyen aceleración del crecimiento, avance de la maduración ósea, pubertad temprana, masa ósea reducida, pobre rendimiento académico y taquiarritmia.
Debido a la importancia del tratamiento supresivo con T4 para el control de la enfermedad, es necesario insistir en su cumplimiento porque es conocida la poca adherencia a los tratamientos crónicos en este grupo etario, sobre todo en los adolescentes (91).
En los pacientes tratados con 131I
Se debe considerar la evaluación de la Tg con estimulación de la TSH y posiblemente, un RCT diagnóstico al cabo de 1 o 2 años en los. Para los pacientes con AbTg, se debe sopesar demorar la estadificación posoperatoria para dar tiempo a la depuración de anticuerpos, excepto para pacientes con enfermedad T4 o M1.
Opciones de tratamiento en evaluación clínica del carcinoma de tiroides papilar y folicular recidivante
En general, los niños con CDT tienen una supervivencia excelente; sin embargo, la recidiva es frecuente (35 % - 45 %) y se observa más a menudo en niños menores de 10 años y aquellos con ganglios linfáticos cervicales palpables en el momento del diagnóstico. Es posible prever que incluso en los pacientes con un tumor diseminado a los pulmones no disminuirá la esperanza de vida después de un tratamiento adecuado (94).
Cabe notar que, entre 35 % y 45 % de los cánceres de tiroides en los niños y adolescentes expresan el transportador unidireccional de sodio-yodo (una glicoproteína cotransportadora unida a la membrana) que es esencial para la captación de yodo y la síntesis de la hormona tiroidea. Los pacientes con tumores que expresan el transportador unidireccional de sodio-yodo tienen un riesgo más bajo de recidiva y habitualmente, responden al tratamiento con yodo radiactivo (100).
En los pocos casos donde no hay captación del RAI con una enfermedad que continúa progresando podría ser dado una supresión continua con levotiroxina y tratamientos alternativos aunque estos no han sido estudiados ampliamente en niños (94).
REFERENCIAS
1. Tessler FN, Middleton WD, Grant EG, Hoang JK, Berland LL, Teefey SA, et al. ACR thyroid imaging, reporting, and data system (TI-RADS): White paper of the ACR TI-RADS Committee. J Am Coll Radiol. 2017;14:587-595.
2. Russ G, Royer B, Bigorgne C, Rouxel A, Bienvenu-Perrard M, Leenhardt L. Prospective evaluation of thyroid imaging reporting and data system on 4 550 nodules with and without elastography. Eur J Endocrinol. 2013;168(5):649-655.
3. Kim MJ, Kim EK, Park SI, Kim BM, Kwak JY, Kim SJ, et al. Us-guided fine-needle aspiration of thyroid nodules: Indications, techniques, results. Radiographics. 2008;28:1869-1886.
4. Spencer CA, Bergoglio LM, Kazarosyan M, Fatemi S, LoPresti JS. Clinical impact of thyroglobulin (Tg) and Tg autoantibody method differences on the management of patients with differentiated thyroid carcinomas. J Clin Endocrinol Metab. 2005;90:5566-5575.
5. Suh I, Vriens MR, Guerrero MA, Griffin A, Shen WT, Duh QY, et al. Serum thyroglobulin is a poor diagnostic biomarker of malignancy in follicular and Hurtle-cell neoplasms of the thyroid. Am J Surg. 2010;200:41-46.
6. Sushima Y, Miyauchi A, Ito Y, Kudo T, Masuoka H, Yabuta T, et al. Prognostic significance of changes in serum thyroglobulin antibody levels of pre- and post-total thyroidectomy in thyroglobulin antibody-positive papillary thyroid carcinoma patients. Endocrine J. 2013;60(7):871-876.
7. Bin Saeedan M, Aljohani IM, Khushaim AO, Bukhari SQ, Elnaas ST. Thyroid computed tomography imaging: Pictorial review of variable pathologies. Insights Imaging. 2016;7:601-617.
8. Hoang JK, Branstetter BF 4th, Gafton AR, Lee WK, Glastonbury CM. Imaging of thyroid carcinoma with CT and MRI: Approaches to common scenarios. Cancer Imaging. 2013;13(1):128-139.
9. Padovani RP, Kasamatsu TS, Nakabashi CC, Camacho CP, Andreoni DM, Malouf EZ, et al. One month is sufficient for urinary iodine to return to its baseline value after the use of water of soluble iodinated contrast agent in post-thyroidectomy patients requiring radioiodine therapy. Thyroid. 2012;22(9):926-930.
10. Beaudenon-Huibregtse S, Alexander EK, Guttler RB, Hershman JM, Babu V, Blevins TC, Moore P, et al. Centralized molecular testing for oncogenic gene mutations complements the local cytopathology diagnosis of thyroid nodules. Thyroid. 2014;24(10):1479-1487.
11. Labourier E, Shifrin A, Busseniers AE, Lupo MA, Manganelli ML, Andruss B, et al. Molecular testing for miRNA, mRNA, and DNA on fine-needle aspiration improves the preoperative diagnosis of thyroid nodules with indeterminate cytology. J Clin Endocrinol Metab. 2015;100(7):2743-2750.
12. Nguyen QT, Lee EJ, Huang MG, Park YI, Khullar A, Plodkowski RA. Diagnosis and treatment of patients with thyroid cancer. Am Health Drug Benefits. 2015;8(1):30-40.
13. Hay ID, Thompson GB, Grant CS, Bergstralh EJ, Dvorak CE, Gorman CA, et al. Papillary thyroid carcinoma managed at the Mayo Clinic during six decades (1940-1999): Temporal trends in initial therapy and long-term outcome in 2 444 consecutively treated patients. World J Surg. 2002; 26:879-885.
14. Brierley JD, Panzarella T, Tsang RW, Gospodarowicz MK, O'Sullivan B. A comparison of different staging systems predictability of patient outcome. Thyroid carcinoma as an example. Cancer. 1997;79:2414-2423.
15. Bliss RD, Gauger PG, Delbridge LW. Surgeon's approach to the thyroid gland: Surgical anatomy and the importance of technique. World J Surg. 2000;24(8):891-897.
16. Nasef HO, Nixon IJ, Wreesmann VB. Optimization of the risk-benefit ratio of differentiated thyroid cancer treatment. Eur J Surg Oncol. 2018;44(3):276-285.
17. Asimakopoulos P, Nixon IJ. Surgical management of primary thyroid tumours. Eur J Surg Oncol. 2018;44(3):321-326.
18. Kovatch KJ, Hoban CW, Shuman AG. Thyroid cancer surgery guidelines in an era of de-escalation. Eur J Surg Oncol. 2018;44(3):297-306.
19. García Colina J, Pérez A, Mata JF, Lugo J, García F, Altimari R, et al. Reunión de Consenso en cáncer diferenciado del tiroides. Rev Venez Oncol 2005;17(4):229-240.
20. Bilimoria KY, Bentrem DJ, Ko CY, Stewart AK, Winchester DP, Talamonti MS, et al. Extent of surgery affects survival for papillary thyroid cancer. Ann Surg. 2007;246:375-381.
21. Grant CS, Hay ID, Gough IR, Bergstralh EJ, Goellner JR, McConahey WM, et al. Local recurrence in papillary thyroid carcinoma: Is extent of surgical resection important? Surgery. 1988; 104:954-962.
22. Hay ID, Grant CS, Bergstralh EJ, Thompson GB, van Heerden JA, Goellner JR. Unilateral total lobectomy: Is it sufficient surgical treatment for patients with AMES low-risk papillary thyroid carcinoma? Surgery. 1998;124:958-964.
23. Mazzaferri EL, Kloos RT. Clinical review 128: Current approaches to primary therapy for papillary and follicular thyroid cancer. J Clin Endocrinol Metab. 2001;86:1447-1463.
24. Matsuzu K, Sugino K, Masudo K, Nagahama M, Kitagawa W, Shibuya H, et al. Thyroid lobectomy for papillary thyroid cancer: Long-term follow-up study of 1 088 cases. World J Surg. 2014;38:68-79.
25. Adam MA, Pura J, Gu L, Dinan MA, Tyler DS, Reed SD, et al. Extent of surgery for papillary thyroid cancer is not associated with survival: An analysis of 61,775 patients. Ann Surg. 2014;260:601-605.
26. Nixon IJ, Ganly I, Patel SG, Palmer FL, Whitcher MM, Tuttle RM, et al. Thyroid lobectomy for treatment of well differentiated intra-thyroid malignancy. Surgery. 2012;151:571-579.
27. Vaisman F, Shaha A, Fish S, Michael TR. Initial therapy with either thyroid lobectomy or total thyroidectomy without radioactive iodine remnant ablation is associated with very low rates of structural disease recurrence in properly selected patients with differentiated thyroid cancer. Clin Endocrinol (Oxf). 2011;75:112-119.
28. Barney BM, Hitchcock YJ, Sharma P, Shrieve DC, Tward JD. Overall and cause-specific survival for patients undergoing lobectomy, near-total, or total thyroidectomy for differentiated thyroid cancer. Head Neck. 2011;33:645-649.
29. Mendelsohn AH, Elashoff DA, Abemayor E, St John MA. Surgery for papillary thyroid carcinoma: Is lobectomy enough? Arch Otolaryngol Head Neck Surg. 2010;136:1055-1061.
30. Haigh PI, Urbach DR, Rotstein LE. Extent of thyroidectomy is not a major determinant of survival in lower high-risk papillary thyroid cancer. Ann Surg Oncol. 2005;12:81-89.
31. Marti JL, Morris LGT, Ho AS. Selective use of radioactive iodine (RAI) in thyroid cancer: No longer "one size fits all". Eur J Surg Oncol. 2018;44(3):348-356.
32. Haugen BR, Alexander EK, Bible KC, Doherty GM, Mandel SJ, Nikiforov YE, et al. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid. 2016;26(1):1-133.
33. Asimakopoulos P, Nixon IJ. Surgical management of primary thyroid tumours. Eu J Surg Oncol. 2018;44 321-326.
34. Goepfert RP, Clayman GL. Management of the central compartment in differentiated thyroid carcinoma. Eu J Surg Oncol. 2018;44:327-331.
35. Schoppy DW, Holsinger FC. Management of the neck in thyroid cancer. Otolaryngol Clin North Am. 2014;47:545-556.
36. Cracchiolo RJ, Wong RJ. Management of the lateral neck in well differentiated thyroid cancer. Eur J Surg Oncol. 2018;44:332-337.
37. Vanzat A, Mercalli F, Rosai J. The "sprinkling" sign in the follicular variant of papillary thyroid carcinoma: A clue to the recognition of this entity. Arch Pathol Lab Med. 2013;137:1707-1709.
38. Cibas ES, Ali SZ. NCI thyroid FNA State of the Science Conference. The Bethesda System for reporting thyroid cytopathology. Am J Clin Pathol. 2009;132(5):658-665.
39. Lee J, Yun MJ, Nam KH, Chung WY, Soh EY, Park CS. Quality of life and effectiveness comparisons of thyroxine withdrawal, triiodothyronine withdrawal, and recombinant thyroid- stimulating hormone administration for low-dose radioiodine remnant ablation of differentiated thyroid carcinoma. Thyroid. 2010;20:173-179.
40. Edmonds CJ, Hayes S, Kermode JC, Thompson BD. Measurement of serum TSH and thyroid hormones in the management of treatment of thyroid carcinoma with radioiodine. Br J Radiol. 1977;50:799-807.
41. Tuttle RM, Haugen B, Perrier ND. The updated AJCC/TNM staging system for differentiated and anaplastic thyroid cancer (8th edition): What changed and why? Thyroid. 2017;27(6):751-756.
42. Conzo G, Docimo G, Pasquali D, Mauriello C, Gambardella C, Esposito D, et al. Predictive value of nodal metastases on local recurrence in the management of differentiated thyroid cancer. Retrospective clinical study. BMC Surg. 2013;13(Suppl 2): S53.
43. Randolph G, Duh QY, Heller KS, LiVolsi VA, Mandel SJ, Steward DL, et al. The prognostic significance of nodal metastases from papillary thyroid carcinoma can be stratified. Based on the size and number of metastatic lymph nodes as well as the presence of extra nodal extension. Thyroid. 2012;22(11):1144-1152.
44. Shindo ML, Caruana S, Kandil E, McCaffrey JC, Orloff L, Porterfield JR, et al. Management of invasive well-differentiated thyroid cancer an American Head and Neck Society consensus statement. Head Neck. 2014;36:1379-1390.
45. Kebebew E, Clark OH. Locally advanced differentiated thyroid cancer. Surg Oncol. 2003;12:91-99.
46. Avenia N, Ragusa M, Monacelli M, Calzolari F, Daddi N, Di CL, et al. Locally advanced thyroid cancer: Therapeutic options. Chir Ital. 2004; 56:501- 508.
47. Janjua N, Wreesmann VB. Aggressive differentiated thyroid cancer. Eur J Surg Oncol. 2018;44(3):367-377.
48. Lee YS, Chung WY, Chang HS, Park CS. Treatment of locally advanced thyroid cancer invading the great vessels using a Y‐shaped graft bypass. Interact Cardiovasc Thorac Surg. 2010;10:1039-1041.
49. Yousem DM, Gad K, Tufano RP. Resectability issues with head and neck cancer. AJNR Am J Neuroradiol. 2006;27(10):2024-2036.
50. Pluijmen MJ, Eustatia-Rutten C, Goslings BM, Stokkel MP, Arias AM, Diamant M, et al. Effects of low-iodide diet on postsurgical radioiodine ablation therapy in patients with differentiated thyroid carcinoma. Clin Endocrinol (Oxf). 2003;58(4):428-435.
51. American Thyroid Association (ATA) Guidelines Taskforce on Thyroid Nodules and Differentiated Thyroid Cancer, Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009;19:1167-1214.
52. Perros P, Boelaer, K, Colley S, Evans C, Evans RM, Gerrard BG, et al. Guidelines for the management of thyroid cancer. Clinical Endocrinology (Oxford). 2014;81(Suppl 1):S1-122.
53. Hugo J, Robenshtok E, Grewal R, Larson S, Tuttle RM. Recombinant human stimulating hormone- assisted radioiodine remnant ablation in thyroid cancer patients at intermedia to high risk of recurrence. Thyroid. 2012;(22)10:1007-1015.
54. Pak K, Cheon GJ, Kang KW, Kim SJ, Kim IJ, Kim EE, et al. The effectiveness of recombinant human thyroid-stimulating hormone versus thyroid hormone withdrawal prior to radioiodine remnant ablation in thyroid cancer: A meta-Analysis of randomized controlled trials. J Korean Med Sci. 2014;29(6):811-817.
55. Haugen BR, Pacini F, Reiners C, Schlumberger M, Ladenson PW, Sherman SI, et al. A comparison of recombinant human thyrotropin and thyroid hormone withdrawal for the detection of thyroid remnant or cancer. J Endocrinol Metab. 1999;84(11):3877-3885.
56. Clement SC, Peeters RP, Ronckers CM, Links TP, van den Heuvel-Eibrink MM, Nieveen van Dijkum EJ, et al. Intermediate and long term adverse effects of radioiodine therapy for differentiated thyroid carcinoma a systematic review. Cancer Treat Rev. 2015;41(10):925-934.
57. Alexander C, Bader JB, Schaefer A, Finke C, Kirsch CM. Intermediate and long-term side effects of high-dose radioiodine therapy for thyroid carcinoma. J Nucl Med. 1998;39(9):1551-1554.
58. Rubino C, de Vathaire F, Dottorini ME, Hall P, Schvartz C, Couette JE, et al. Second primary malignancies in thyroid cancer patients. Br J Cancer. 2003;89(9):1638-1644.
59. Van Nostrand D, Neutz J. Atkins F. Side-effects of rational dose iodine-131 therapy for metastatic well-differentiated thyroid carcinoma. J Nucl Med. 1986;27:1519-1527.
60. Avram A. Radioiodine scintigraphy with SPECT/CT: An important diagnostic tool for thyroid cancer staging and risk stratification. J Nucl Med. 2012;53:754-764.
61. Durante C, Montesano T, Attard M, Torlontano M, Monzani F, Costante G, et al. Long term surveillance of papillary thyroid cancer patients who do not undergo postoperative radioiodine remnant ablation: Is there a role for serum thyroglobulin measurement? J Clin Endocrinol Metabol. 2012;97(8):2748-2753.
62. Janovsky CCPS, Maciel RMB, Camacho CP, Padovani RP, Nakabashi CC, Yang JH, et al. A prospective study showing an excellent response of patients with low-risk differentiated thyroid cancer who did not undergo radioiodine remnant ablation after total thyroidectomy. Eur Thyroid J. 2016;5:44-49.
63. Castagna MG, Cevenini G, Theodoropoulou A, Maino F, Memmo S, Claudia C, et al. Post-surgical thyroid ablation with low or high radioiodine activities results in similar outcomes in intermediate risk differentiated thyroid cancer patients. Eur J Endocrinol. 2013;169:23-29.
64. Abelleira E, Bueno F, Smulever A, Pitoia F. Riesgo dinámico en pacientes con cáncer diferenciado de tiroides no ablacionados. Revista de Endocrinología y Metabolismo. 2017;54(2):69-75.
65. Schlumberger M, Challeton C, De Vathaire F, Travagli JP, Gardet P, Lumbroso JD, et al. Radioactive iodine treatment and external radiotherapy for lung and bone metastases from thyroid carcinoma. J Nucl Med. 1996,37:598-605.
66. Durante C, Montesan T, Torlontano M, Attard M, Monzani F, Tumino S, et al. PTC study group papillary thyroid cancer: Time course of recurrences during post-surgery surveillance. J Clin Endocrinol Metab. 2013;98:636-642.
67. Martins Filho R, Ward LS, Amorim BJ, Santos AO, Lima MC, Ramos CD, et al. Cumulative doses of radioiodine in the treatment of differentiated thyroid carcinoma: Knowing when to stop. Arq Bras Endocrinol Metab. 2010:54:807-812.
68. Califano I, Löwenstein A, Deutsch S, Abalovich M, Cabezón C, Pitoia F. Impacto de las metástasis óseas en 47 pacientes con cáncer diferenciado de tiroides. Rev Arg Endocrinol Metab. 2014;2:52-58.
69. McWilliams RR, Giannini C, Hay ID, Atkinson JL, Stafford SL, Buckner JC. Management of brain metastases from thyroid carcinoma: A study of 16 pathologically confirmed cases over 25 years. Cancer. 2003;98:356-362.
70. Hall NC, Kloospet RT. PET Imaging in differentiated thyroid cancer: Where does it fit and how do we use it? Arq Bras Endocrinol Metab. 2007;51(5):793-805.
71. Marcus C, Whitworth PW, Surasi DS, Pai SI, Subramaniam RM. PET/CT in the management of thyroid cancers. AJR Am J Roentgenol. 2014;202:1316-1329.
72. Chow SM, Law Sc, Mendelnhall WM, Au SK, Chan PT, Leung TW, et al. Papillary thyroid carcinoma: Prognostic factors and the role of radioiodine and external radiotherapy. Int J Radiat Oncol Bio Phys. 2002;52(3):784-795.
73. Wu XL, Hu, Li QH, Guo JR, Sun D, Yan JH, et al. Value of postoperative radiotherapy for thyroid cancer. Head Neck Surg. 1987;10(2):107-112.
74. Ito Y, Hirokawa M, Jikuzono T, Higashiyama T, Takamura Y, Miya A, et al. Extra nodal tumor extension to adjacent organs predicts a worse cause-specific survival in patients with papillary thyroid carcinoma. World J Surg. 2007;31(6):1194-1201.
75. Brierley JD, Tsang RW. External beam radiation therapy for thyroid cancer. Endocrinol Metab Clin North Am. 2008;37(2):497-509.
76. Haigh PI, Ituarte PH, Wu HS, Treseler PA, Posner MD, Quivey JM, et al. Completely resected anaplastic thyroid carcinoma combined with adjuvant chemotherapy and irradiation is associated with prolonged survival. Cancer. 2001;91(12):2335-2342.
77. Zettinig G, Fueger BJ, Passler C, Kaserer K, Pirich C, Dudczak R, et al. Long-term follow-up of patients with bone metastases from differentiated thyroid carcinoma-surgery or conventional therapy? Clin Endocrinol (Oxford). 2002;56:377-382
78. Marcocci C, Pacini F, Elisei R, Schipani E, Ceccarelli C, Miccoli P, et al. Clinical and biological behavior of bone metastases from differentiated thyroid carcinoma. Surgery. 1989;106:960-966.
79. Ford D, Giridharan S, McConkey C, Hartley A, Brammer C, Watkinson JC, et al. External beam radiotherapy in the management of differentiated thyroid cancer. Clin Oncol (R Coll Radiol). 2003;15:337-341.
80. Mazzarotto R, Cesaro MG, Lora O, Rubello D, Casara D, Sotti G. The role of external beam radiotherapy in the management of differentiated thyroid cancer. Biomed Pharmacother. 2000;54:345-349.
81. Matrone A, Valerio L, Pieruzzi L, Giani C, Cappagli V, Lorusso L, et al. Protein kinase inhibitors for the treatment of advanced and progressive radio-refractory thyroid tumors: From the clinical trials to the real life. Best Pract Res Clin Endocrinol Metab. 2017;31:319-334.
82. Durante C, Haddy N, Baudin E, Leboulleux S, Hartl D, Travagli JP, et al. Long term outcome of 444 patients with distant metastases from papillary and follicular thyroid carcinoma: Benefits and limits of radioiodine therapy. J Clin Endocrinol Metab. 2006;91(8):2892-2899.
83. Kwong N, Marqusee E, Gordon MS, Larsen PR, Garber JR, Kim MI, et al. Long term treatment-free survival in select patients papillary thyroid cancer. Endocr Connect. 2014;3(4):207-214.
84. Cabanillas ME, McFadden D, Durante C. Thyroid cancer. Lancet 2016;388:2783-2795.
85. Brose MS, Nuttin CM, Jarzab, Elisei R, Siena S, Bastholt L,et al. Sorafenib in radioactive iodine-refractory, locally advanced or metastatic differentiated thyroid cancer: A randomized, double blinded phase III trial. Lancet. 2014;384:319-328.
86. Shiumberg M, Tahara M, Wirth LJ, Robinson B, Brose MS, Elisei R, et al. Lenvatinib versus placebo in radioiodine-refractory thyroid cancer. N England J Med. 2015;372:621-630.
87. Gutiérrez J. Osteonecrosis of the jaw associated to bisphosphonates treatment in osteoporosis patients: A review. Rev Fac Odontol Univ Antioq. 2013;24(2):307-320.
88. Golpanian S, Perez EA, Tashiro J, Lew JI, Sola JE, Hogan AR, et al. Pediatric papillary thyroid carcinoma: Outcomes and survival predictors in 2504 surgical patients. Pediatr Surg Int. 2016;32(3):201-208.
89. Dermody S, Walls A, Harley EH Jr. Pediatric thyroid cancer: An update from the SEER database 2007-2012. Int J Pediatr Otorhinolaryngol. 2016;89:121-126.
90. Cotterill SJ, Pearce MS, Parker L. Thyroid cancer in children and young adults in the North of England. Is increasing incidence related to the Chernobyl accident? Eur J Cancer. 2001;37(8):1020-1026.
91. Kaplan MM, Garnick MB, Gelber R, Li FP, Cassady JR, Sallan SE, et al. Risk factors for thyroid abnormalities after neck irradiation for childhood cancer. Am J Med. 1983;74(2) 272-280.
92. Francis GL, Waguespack SG, Bauer AJ, Angelos P, Benvenga S, Cerutti JM, et al. Management guidelines for children with thyroid nodules and differentiated thyroid cancer. The American Thyroid Association Guidelines Task Force on Pediatric Thyroid Cancer. Thyroid. 2015;25(7):716-759.
93. Nikita ME, Jiang W, Cheng SM, Hantash FM, McPhaul MJ, Newbury RO, et al. Mutational analysis in pediatric thyroid cancer and correlations with age, ethnicity, and clinical presentation. Thyroid. 2016;26(2):227-234.
94. Machac J. Thyroid cancer in pediatrics. Endocrinol Metab Clin North Am. 2016;45(2):359-404.
95. Grigsby PW, Gal-or A, Michalski JM, Doherty GM. Childhood and adolescent thyroid carcinoma. Cancer. 2002;95:724-729.
96. Jarzab B, Handkiewicz Junak D, Wloch J, Kalemba B, Roskosz J, Kukulska A, et al. Multivariate analysis of prognostic factors for differentiated thyroid carcinoma in children. Eur J Nucl Med. 2000;27:833-841.
97. Welch Dinauer CA, Tuttle RM, Robie DK, McClellan DR, Svec RL, Adair C, et al. Clinical features associated with metastasis and recurrence of differentiated thyroid cancer in children, adolescents and young adults. Clin Endocrinol (Oxf). 1998;49:619-628.
98. Krajewska J, Chmielik E, Jarząb B. Dynamic risk stratification in the follow-up of thyroid cancer: What is still to be discovered in 2017. Endocr Relat Cancer. 2017;24:387-402.
99. Van der Wardt RA, Persoon AC, Klein Hesselink EN, Links TP. Long-term follow-up for differentiated thyroid carcinoma patients: A reconsideration. Thyroid. 2017;27(3):475-476
100. Kim K, Kim WW, Choi JB, Kim MJ, Lee CR, Lee J, et al. Usefulnes of dynamic risk stratification in pediatric patients with differentiated thyroid carcinoma. Ann Surg Treat Res. 2018;95(4):222-229.
101. Zanella AB, Scheffel RS, Nava CF, Golbert L, Laurini de Souza Meyer E, Punales M, et al. Dynamic risk stratification in the follow-up of children and adolescents with differentiated thyroid cancer. Thyroid. 2018;28(10):1285-1292.
102. Parisi MT, Eslamy H, Mankoff D. Management of differentiated thyroid cancer in children: Focus on the American Thyroid Association Pediatric Guidelines. Semin Nucl Med. 2016 ;46(2):147-164.
103. Mazzaferi EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med, 1994;97:418-428.
104. Rivkees SA, Mazzaferri EL, Verberg FA, Reiners C, Luster M, Breuer CK, et al. The treatment of differentiated thyroid cancer in children: Emphasis on surgical approach and radioactive iodine therapy. Endocr Rev. 2011;32:798-826.
105. Jarzab B, Handkiewicz-Junak D, Wloch J. Juvenile differentiated thyroid carcinoma and the role of radioiodine in its treatment: A qualitative review. Endocr Relat Cancer. 2005;12:773-803.
106. Leboulleux S, Baudin E, Hartl DW, Travagli JP, Schlumberger M. Follicular-cell derived thyroid cancer in children. Eur J Cancer. 2004;40:1655-1659.
107. Biko J, Reiners C, Kreissl MC, Verburg FA, Demidchik Y, Drozd V. Favourable course of disease after incomplete remission on 131I therapy in children with pulmonary metastases of papillary thyroid carcinoma: 10 years follow-up. Eur J Nucl Med Mol Imaging. 2011; 38:651-655.
Notas de autor
svoncologia@gmail.com
Información adicional
AGRADECIMIENTO: A las Sociedades Venezolanas de Oncología, Endocrinología y Medicina Nuclear, a todos los participantes, a la empresa Meditron, al grupo Gurve, laboratorio Farma, G&P Suministros Médicos representante de la marca Pajunk, a la Clínica el Ávila por haber prestado sus espacios a través del Dr. Ignacio Taronna y al Sr. Granados encargado del Auditorio de la mencionada clínica.