
Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 10 Mayo 2020
Revisado: 16 Junio 2020
Aprobación: 19 Julio 2020
Resumen: El tumor carcinoide gástrico es un subtipo infrecuente de las neoplasias neuroendocrinas, su incidencia máxima se presenta en la sexta década de vida. Este pólipo supone 3 de cada 1 000 neoplasias gástricas. Los tumores carcinoides gástricos se dividen en 3 tipos principalmente. Tipo 1 y 2 (Caracterizados por hipertrofia de las células enterocromafines, tumores múltiples, no esporádicos, hipergastremia) y el tipo 3 (gastrina normal, tumor solitario, esporádico). Alguna literatura señala un cuarto tipo misceláneo. CASO CLÍNICO: Se presenta caso clínico de una mujer de 49 años edad que acude al servicio médico por cuadro de dispepsia de larga evolución, fue diagnosticada con un carcinoide tipo II, el diagnóstico se realizó mediante endoscopias digestiva alta y biopsia de la mucosa acompañada de estudio inmunohistoquímico. Se decidió realizar una gastrectomía subtotal, la resolución fue completa. La vigilancia oncológica no presenta datos de recurrencia. DISCUSIÓN: Los tumores carcinoides gástrico son los hallazgos más inusuales de los carcinoides gastrointestinal. La paciente presentó neoplasia carcinoide gástrico tipo 2 con morfología atípica; pólipo único característico de la lesión gástrico polipoidea tipo 3 y la prueba de gastrina indicó hipergastrinemia. El tratamiento utilizado con más frecuencia para remover tumor neuroendocrino tipo 2 es resección endoscópica, sin embargo, a la paciente se le realizó cirugía gástrica antral. CONCLUSIÓN: El tipo 1 y 2 normalmente son tratados con resección endoscópica y el tipo 3 con cirugía, la elección del tratamiento está estrechamente relacionada al criterio clínico.
Palabras clave: Neoplasia, tumor carcinoide, tumor neuroendocrino, cirugía.
Abstract: The gastric carcinoid tumor is an infrequent subtype of neuroendocrine neoplasms, its maximum incidence occurs in the sixth decade of the life. This polyp accounts for 3 out of every 1 000 gastric malignancies. The gastric carcinoid tumors are divided into 3 main types. Type 1 and 2 are (Characterized by enterocromafines cell hypertrophy, multiple, non-sporadic tumors, hipergastremia) and the type 3 (normal gastrin, solitary, sporadic tumor). Some literature indicates a fourth miscellaneous type. CLINICAL CASE: We present a clinical case of a 49 year old woman who comes to the medical service for long term dyspepsia, she was diagnosed with a type II carcinoid, and the diagnosis was made by the upper digestive endoscopy and biopsy of the mucosa accompanied by the immunohistochemically study. It was decided to perform a subtotal gastrectomy, the resolution was complete. The oncological surveillance does not present recurrence data. DISCUSION: The gastric carcinoid tumors are the most unusual findings of the gastrointestinal carcinoids. The patient presented type 2 gastric carcinoid neoplasm with atypical morphology; a unique polyp characteristic of the type 3 polypoid gastric lesion and the gastrin test indicated hypergastrinemia. The most frequently used treatment to remove type 2 neuroendocrine tumor is endoscopic resection, however, the patient underwent antral gastric surgery. CONCLUSION:The main types 1 and 2 are normally treated with the endoscopic resection and the type 3 with surgery, the choice of treatment is closely related to clinical criteria.
Keywords: Neoplasm, carcinoid tumor, neuroendocrine tumor, surgery.
INTRODUCCIÓN
Los tumores carcinoides se originan en las células similares a las enterocromafines (ECL), células neuroendocrinas difusas, ubicadas en el tubo gastrointestinal. Son neoplasias infrecuentes, su incidencia máxima se presenta en la sexta década de vida. Las principales manifestaciones clínicas son a causa del efecto mecánico del tumor o actividad endocrina, aunque pueden ser asintomáticos (1,2,3).
Tradicionalmente comprendían 2 %-3 % de los tumores neuroendocrinos en el tubo gastrointestinal, sin embargo, estudios realizados recientemente consideran que la incidencia ha aumentado de un 11 %-41 % gracias a la detección por diagnóstico endoscópico (4,5).
Los tumores carcinoides gástricos se clasifican generalmente en tres tipos, en algunos casos se llega a considerar un cuarto tipo (6,7,8).
Tipo I: Los carcinoides gástricos tipo I son aquellos asociados a gastritis crónica atrófica autoinmune y anemia perniciosa, representan un 70 %-80 % de los tumores gastrointestinales. Son tumores múltiples y se acompañan de hipergastrinemia y pH gástrico elevado, y tienen un mejor pronóstico (7,9,10).
Tipo II: Este tipo de tumores se asocian a los gastrinomas y al síndrome Zollinger-Ellison secundario, su prevalencia es de un 5 %-10 %. Su malignidad es intermedia y exhiben hipertrofia en las ECL, hipergastrinemia y pH gástrico elevado, son tumores neuroendocrinos múltiples. Los pólipos suelen medir menos de 1 cm, se localizan en el fondo, cuerpo y a veces antro gástrico (8,10).
Tipo III: Los tumores carcinoides gástricos tipo III, son neoplasias esporádicas y solitarias, normalmente surgen en el cuerpo o antro gástrico, se desarrollan con niveles de gastrina normales y no se asociación a hipertrofia de las ECL. Son tumores biológicamente agresivos con alta tasa de metástasis > 50 %(8,9). Se presentan con mayor frecuencia en hombres, y su tamaño usualmente es mayor a 10 mm. No se relaciona con infección por H Pylori ni cambios en el pH gástrico. La neoplasia suele relacionarse con mutaciones y sobreexpresión en el gen p53, sin embargo, su patogenia no está bien definida (10,11).
Tipo IV: Se considera un tumor misceláneo, caracterizado por múltiples y pequeñas lesiones y representa menos del 1 % (4,11). La detección de tumores carcinoides gástricos, ha incrementado gracias al uso de vídeo endoscopia digestiva alta (VEDA) marcadores tisulares y a un diagnóstico histológico más preciso. La disección submucosa endoscópica actualmente es considerada una técnica factible, por su capacidad para resecar lesiones de gran tamaño (12,13,14).
CASO CLÍNICO
Se presenta el caso de paciente femenina de 49 años de edad, procedente de Santa Bárbara, Honduras. Sin antecedentes personales patológicos, en enero de 2018 acude al servicio médico por cuadro de dispepsia de 5 meses de evolución, epigastralgia urente de predominio matutino, severidad moderada, que se exacerba con la ingesta de alimentos y se atenúa con inhibidores de bomba de protones (lansoprazol 30 mg/d). Negativa para; náuseas, vómitos, cefalea, mareo, diarrea, pérdida de peso, hiporexia.
Al examen físico sin apariencia de enfermedad, biotipo asténico, sin alteración en examen físico segmentario. Datos de laboratorio: Hb: 11,2 g/dL Hct: 35,9 % Wbc: 2 900/L Plt: 351 000, VCM: 90,0 ft, HCM: 30,0 p/g.
El 30 de enero de 2018, se le realizó una endoscopia digestiva alta por indicación de dispepsia persistente, en la que se observaron anomalías en la mucosa esofágica con aspecto eritematoso en la parte distal del esófago (esofagitis distal grado A), no se visualizaron úlceras. La mucosa gástrica se localizó eritematosa en toda la extensión, con presencia de erosiones elevadas en el antro y cuerpo de los cuales se tomó muestra para prueba de ureasa y estudios histológicos, el diagnóstico de relevancia fue pangastritis eritemato-erosiva moderada antral. No se encontraron lesiones sub-cardiales ni otras alteraciones relevantes. La prueba de ureasa fue negativa para H Pylori.
El reporte anatomopatológico describe mucosa con áreas de erosión epitelial y zonas con arreglo neoplásico que exhibe un patrón organoide con cierta hipercromasia y disposición tubular y acinar. La inmunohistoquímica reporta cromogranina A positivo, un fuerte indicador de tumores neuroendocrinos. TAC de tórax y abdomen, no informa hallazgos de interés.
En 13 de marzo del mismo año, se realizó una segunda endoscopia digestiva alta y valores de gastrina por sospecha de carcinoide gástrico: Los hallazgos endoscópicos mostraron que, en el fondo y cuerpo gástrico, las paredes estaban distensibles, con pliegues conservados y mucosa distal con parches pálidos aislados más notable en antro donde además se observa ligero eritema y 2 zonas longitudinales de engrosamiento hacia la curvatura menor de las cuales se tomó biopsia. En la porción distal hacia la cara posterior se localiza un pólipo tipo olla, redondeado, de 1 mm x 1 mm diámetro, bordes regulares y bien definido, ligeramente congestivo. La prueba de gastrina con resultados 333 H, superior al rango normal que es menor o igual a 100 pg∕mL, evidenció hipergastrinemia.
El 26 de marzo de 2018 se decidió realizar una gastrectomía subtotal distal, la pieza operatoria pesa 1 000 g, la biopsia posterior a gastrectomía demostró que el tumor neuroendocrino es de infiltrado A en la mucosa muscaris mucosae, con lecho quirúrgico libre, sin afección en los ganglios linfáticos. La cirugía se consideró resolutiva en su totalidad. Actualmente la paciente está en vigilancia oncológica, se le toman niveles de gastrina, realiza TAC de abdomen una vez al año. La cita de seguimiento más reciente del caso fue en enero de 2020, la paciente no presentó datos de recurrencia.
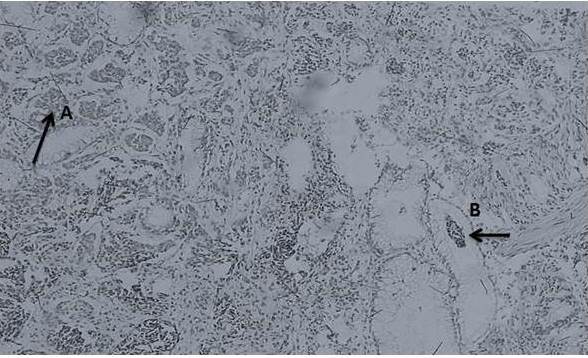
Figura 1
Mucosa gástrica antral con proliferación neoplásica en células enterocromafines (ECL) A. B. Zonas de arreglo neoplásico, hipercromáticos con disposición tubular acina y nichos celulares que cohesionan entre sí, núcleos redondeados con cromatina granular.
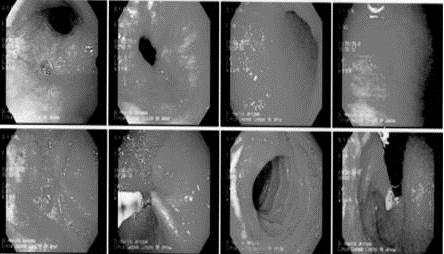
Figura 2.
Endoscopia digestiva alta por indicación de dispepsia, se observa esofagitis tipo A, pangastritis eritemato-erosiva moderada de predominio antral. Premedicación Dormicum (5mg, 5ml), Propofol 1 % 10 mg.
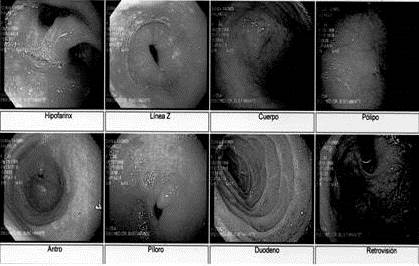
Figura 3
Endoscopia digestiva alta por indicación de sospecha de carcinoide por biopsia y cromatogranina realizada previamente. En la región antral se observó un pólipo gastico congestivo, redondeado, con bordes definidos, con 1 mm x 1 mm de diámetro.
DISCUSIÓN
El tubo digestivo es una estructura anatómica de alta actividad endocrina; con aumentada secreción y excreción hormonal. El tracto gastrointestinal cuenta con el mayor número y variedad de células endocrinas en comparación a otros órganos secretores de hormonas (4). Las células endocrinas que componen el tejido digestivo se caracterizan por sintetizar sustancias hormonalmente activas a través de la descarboxilación de precursores aminas; sistema celular APUD (por sus siglas en inglés: Amine Precursor Uptake and Decarboxilation)(15). El estómago cuenta con tipos de células especializadas en la actividad neurosecretora: 1. Las células G secretoras de gastrina, 2. ECL principales secretoras de histamina, 3. células D encargadas de la liberación de somatostatina y en menor proporción otros tipos celulares (4). Los tumores carcinoides son entidades raras, sin embargo, son los tumores neuroendocrinos más frecuentes en el tracto gastrointestinal y provienen de alteración en las células ECL. La mayoría de estas neoplasias gastrointestinales se encuentran en el intestino delgado 45 %, generalmente en el íleon, en el recto 20 %, apéndice 16 %, colon 1 1% y el menos común como este caso es el gástrico 7 % (16,17,18). Macroscópicamente los carcinoides son lesiones polipoides que protruyen hacia la luz, pueden ser intra-murales o submucosas, son tumores firmes y pueden tener coloración amarilla o parda (3).
Los tumores carcinoides gástricos genéticamente pueden clasificarse como esporádicos, o no esporádicos dentro de la última categoría se encuentran las neoplasias neuroendocrinas múltiples (MEN) tipo 1 y tipo 2 que se asocian a síndromes autosómico dominante, alteración en el cromosoma locus 11q13 predispone a MEN-1. El resultado de una mutación en el proto-oncogén RET se asocia a MEN-2. Los tipos 3 son neoplasias esporádicas, su patogenia no está definida completamente. El riesgo de sufrir un tumor carcinoide gástrico incrementa en mujeres diabéticas y antecedentes familiares de cáncer (16,17). Las neoplasias neuroendocrinas gástricas suelen ser de gran tamaño e infiltrados, regularmente se detectan en estadios avanzados debido a la ausencia de síntomas, por lo tanto, no son diagnosticados hasta que presentan signos de obstrucción (1). En contraste, en el caso presentado la paciente no es diabética, sin patologías personales relevantes, ni antecedentes familiares de cáncer gástrico u otra neoplasia. Para llegar al diagnóstico del tumor neuroendocrino se requiere conjuntamente la clínica y estudios complementarios, como endoscopia digestiva alta, estudios de imagen como la TAC para descartar focos metastásicos. Además, se debe ordenar un panel de hormonas con marcadores específicos que incluyen insulina, gastrina, VIP, serotonina (16,18). A la paciente se le realizó la prueba de gastrina, a causa de la presentación clínica y la accesibilidad del marcador hormonal. Las pruebas de insulina, VIP y serotonina además, de no estar disponibles, se utilizan frecuentemente para tumores neuroendocrinos en otras localizaciones.
El diagnóstico diferencial fue adenocarcinoma gástrico, pero se descartó por el resultado histopatológico de la biopsia.
Se confirmó la presencia de un tumor carcinoide por la cromatogranina A positiva. La neoplasia gástrica observada por endoscopia mostró un pólipo único con bordes definidos, la morfología tumoral que orientó a un tumor carcinoide tipo 3, sin embargo, por las zonas de eritema en los márgenes y el tamaño no fue posible categorizar el tipo tumoral. Cuando se solicitó la prueba de gastrina quedó en evidencia la hipergastrinemia, una característica del tumor tipo 1 y 2. Mediante estudios patológicos e histológicos del parénquima tumoral, se confirmó que la neoplasia carcinoide gástrica era de tipo 2. Un hallazgo inusual, la literatura cataloga este tumor carcinoide tipo 2 como neoplasia tumoral múltiple.
El tratamiento depende del tipo tumoral, para los tipos 1 y 2 se utiliza con frecuencia la resección endoscópica. Para el tipo 3 se necesitan tratamientos más invasivos como la gastrectomía total o subtotal, siendo la ultima el gold standard en tratamiento quirúrgico (5,7,9). La supervivencia del paciente dependerá de diversos factores como ser: tamaño del tumor, grado de invasión vascular, índice Ki67 (8). La decisión terapéutica para la resolución de tumor carcinoide gástrico tipo 2 descrita en el caso fue una gastrectomía subtotal, decisión que fue tomada en base a experiencia clínica y revisión de la literatura que muestra evidencia que la cirugía tiene mejor pronóstico.
Los tumores carcinoides gástrico son los hallazgos más inusuales de los carcinoides neuroendocrinos en el sistema gastrointestinal, sin embargo, su incidencia ha incrementado en los últimos años. Debido a su ambigua sintomatología, recursos como estudios de imagen, histoquímicos y la endoscopia son necesarios para el diagnóstico preciso. El tipo 1 y 2 normalmente son tratados con resección endoscópica y el tipo 3 con cirugía, no obstante, el médico evalúa cual es la mejor opción terapéutica para el paciente atendiendo el tamaño, forma y otras alteraciones que acompañen al tumor o tumores.
REFERENCIAS
1. Astudillo A. Clasificación y caracterización biológico de los tumores neuroendocrinos del tracto gastrointestinal. Oncología (Barc.). 2004;27(4):51-56.
2. Bordi C, D’Adda T, Azzoni C, Canavese G,Brandi ML. Gastrointestinal endocrine tumors: Recent developments. Endocr Pathol. 1998;9:99-115.
3. Kumar V, Abbas AK, Fausto N. En: Robbins SL, Cotran RS. Patología estructural y funcional. Barcelona: Elsevier;2015.
4. Angeles-Angeles A. Tumores endocrinos del estómago. Análisis de 13 casos. Gac Méd Méx. 2005;141(3):207-213.
5. Córdoba Soriano JG, Galo Díaz A, Gutiérrez MV, López Neyra I. Síndrome anémico. Carcinoide gástrico tipo 1 (Papel de la ultrasonografía endoscópica en el diagnóstico y tratamiento). Rev Clín Med Fam. 2010;3(3):217-219.
6. Akhter R, Khuroo M, Dar Z, Qayoom N, Bhat N. Neuroendocrine carcinoma of stomach: A case report. IJBC. 2015;7(4):195-197.
7. Roncon Dias A, Camargo Azevedo B, Valente Alban LB, Yagi OK, Kodama Pertille Ramos MF, Jacob CE, et al. Gastric neuroendocrine tumor: Review and update. Arq Bras Cir Dig. 2017;30(2):150-154.
8. Jiménez-Contreras S, Romero-Vázquez J. Síndrome carcinoide y tumores neuroendocrinos gástricos. Disponible en: URL: https://www.sapd.es/revista/2009/32/4.
9. Crovari EF, Marambio GA, Maturana OR, Jarufe CN, Funke HR, Boza WC. Gastrectomía laparoscópica en carcinoide gástrico. Rev. Chil. Cir. 2013;65(5):396-401.
10. Sundaresan S, Kang J, Merchant L. Pathophysiology of gastric NETs: Role of gastrin and menin. Curr Gastroenterol Rep.2017;19(7):32.
11. Binstock AJ, Johnson CD, Stephens DH, Lloyd RV, Fletcher JG. Carcinoid tumors of the stomach: A clinical and radiographic study. AJR Am J Roentgenol. 2001;176(1):947-951.
12. Mondragón-Sánchez A, Mondragón-Sánchez R, Bernal RM, Baquera-Heredia J, Gómez-Gómez E. Carcinoma neuroendocrino gástrico. Rev Gastroenterol Mex. 2003;68(2):129-132.
13. Shimoyama S, Fujishiro M, Takazawa Y. Successful type-oriented endoscopic resection for gastric carcinoid tumors: A case report. World J Gastrointest Endosc. 2010;2(12):408-412.
14. Donoso DA, Sharp PA, Gellona VJ, Parra BA, Pimentel MF, Escalona PA, et al. Disección sub-mucosa endoscópica en cáncer gástrico incipiente. Rev. Chil. Cir. 2013;65(2):180-186.
15. Angeles-Angeles A. Neoplasias endocrinas del estómago. Revista de Investigación Clínica. 2005;57(1):76-81.
16.Varas Lorenzo MJ. Tumores neuroendocrinos: Fascinación e infrecuencia. Rev. esp. enferm. dig. 2009;101(3):195-202.
17. Hassan MM, Phan A, Li D, Dagohoy C, Leary C, Yao J. Risk factors associated with neuroendocrine tumors: A U.S.-based case-control study. Int J Cancer. 2008;123(4):867-873.
18. Medina AS, Motola Kuba M, González Híjar A, Herrera Bello H, González Chon O. Carcinoide gástrico. Rev Invest Med Sur Mex. 2010;7(3):141-143.
Notas de autor
claryliss1@gmail.com
