LINFOMA CUTÁNEO DE CÉLULAS T (MICOSIS FUNGOIDE) RADIOTERAPIA CUTÁNEA TOTAL CON ELECTRONES. EXPERIENCIA DE 20 AÑOS.
LINFOMA CUTÁNEO DE CÉLULAS T (MICOSIS FUNGOIDE) RADIOTERAPIA CUTÁNEA TOTAL CON ELECTRONES. EXPERIENCIA DE 20 AÑOS.
Revista Venezolana de Oncología, vol. 33, núm. 2, 2021
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 15 Julio 2020
Revisado: 14 Agosto 2020
Aprobación: 08 Noviembre 2020
Resumen: OBJETIVO: Reportar nuestra experiencia de 20 años en tratamiento con irradiación cutánea total con electrones pacientes con linfoma cutáneo de células T. MÉTODO: 53 pacientes durante 2000-2020; 47/irradiación cutánea total técnica ángulo fijo dual, con electrones 4 MEV, dosis total 36 Gy/9 semanas, 6/radioterapia superficial localizada. 19 tratamiento radiante inicial, 28 referidos después de recaída posterior a otras terapéuticas. RESULTADOS: Estadio IB (50 %) IIB (26,5 %). 60,4 % estadios precoces (IA y IIA) 39,6 % estadios avanzados (IIB, IIIA y IIIB). Mediana seguimiento 45,2 meses, promedio 67,3 meses, rango 0,47-236,5. Respuesta completa 57,4 % parcial 42,5 %, respuesta global 100 % después de irradiación con electrones. Radioterapia superficial: 5 respuestas completa 1 parcial. 47 tratados con electrones, supervivencia global 5 años 74,4 % 24,7 %, 10 años libre de progresión 69,4 % 21,5 %, respectivamente. No diferencia significativa en la global entre grupo de irradiación con electrones como tratamiento inicial y quienes recibieron otros tratamientos, diferencia estadísticamente significativa limítrofe en supervivencia libre de progresión 36 % vs. 19 % (P=0,05). 6 pacientes con radioterapia total superficial, 2 estadio IA y IB, respectivamente. Complicaciones agudas cutáneas grado I 58,5 % grado II 33,9 %, grado III 5,6 %. Conjuntivitis 28 %. Toxicidad cutánea crónica: alopecia, xerosis, telangiectasias. 2 pacientes/carcinomas basocelulares CONCLUSIONES: Irradiación total con electrones es tratamiento tópico efectivo, en estadios precoces puede ser curativo, estadios avanzados importante en manejo de enfermedad cutánea conjunto con otras terapéuticas tópicas o sistémicas.
Palabras clave: Radioterapia, linfomas cutáneos, micosis fungoides, irradiación cutánea total.
Abstract: OBJECTIVE: To report our 20-year experience in treatment with total skin irradiation with electrons patients with skin cell lymphoma T. METHOD: 53 patients during 2000-2020; 47/total skin irradiation dual fixed angle technique, with electrons 4 MEV, total dose 36 Gy in 9 weeks, 6 localized superficial radiation therapy. 19 initial radiant treatments, 28 referrals relapse after other therapeutics. RESULTS: IB stage (50 %) IIB (26.5 %). 60.4 % early stages (IA and IIA) 39.6 % advanced stage (IIB, IIIA and IIIB). Median follow-up 45.2 months, the average 67.3 months, range 0.47-236.5. The complete response was 57.4 % partial in 42.5 %, overall response 100 % after the irradiation with electrons. Surface radiation therapy: 5 complete response 1 partial. 47 treated with electrons, overall survival 5 years 74.4 % 24.7 %, 10 years progression free 69.4 % 21.5 %, respectively. No significant difference in overall radiation group with electrons as initial treatment and those receiving other treatments, statistically significant difference limiting progression-free survival 36 % vs. 19% (P=0.05). 6 patients with total surface radiation therapy, 2 stage IA and IB, respectively. Acute skin complications grade I 58.5 % grade II 33.9 %, grade III 5.6 %. Conjunctivitis in 28 %. The chronic skin toxicity: alopecia, xerosis, telangiectasias. 2 patients with basocelular carcinomas. CONCLUSIONS: Total irradiation with electrons is effective topical treatment, in early stages can be curative, advanced stages important in managing joint skin disease with other topical or systemic therapeutics.
Keywords: Radiotherapy, cutaneous lymphoma, mycosis fungoid, total skin electron beam therapy.
INTRODUCCIÓN
Los linfomas cutáneos ocupan el tercer lugar en frecuencia dentro de los linfomas no Hodgkin extra-nodales, después de los del tracto gastrointestinal y los linfomas de cabeza y cuello, siendo alrededor de 80 % de los casos, linfomas de células T. La Micosis Fungoide (MF) y sus variantes representan la forma más común de linfomas cutáneos de células T (LCCT), alrededor del 50 % de esta variedad de linfomas primarios de la piel. La enfermedad fue descrita inicialmente por Albert en Francia en 1806. Se considera que la célula neoplásica de la enfermedad se deriva de las células T de memoria CD4+ con tropismo cutáneo. En su etiopatogenia se han considerado una serie de factores como: exposición a productos químicos y pesticidas, factores genéticos, ocupacionales y virales, pero los datos epidemiológicos no sustentan estas hipótesis como causas potenciales de la MF (1,2,3,4).
La tasa de incidencia ajustada por edad para los EE.UU fue 0,55 por 100 000 persona-años para la MF y de 0,01 para el síndrome de Sézary, predomina en el sexo masculino, con una relación M-H de 1,57 y es más frecuente en los afroamericanos, representando alrededor de 4 % de todos los linfomas no Hodgkin (4,5).
En nuestro país de acuerdo con el registro central de cáncer del programa de oncología del MPPS, durante el período 2005 - 2014, se recopiló un total de 2 691 casos de linfomas no Hodgkin (LNH) (2,8 % de todos los casos de cáncer). De ellos los linfomas cutáneos sumaron un total de 82 casos, de los cuales 31 fueron clasificados como MF y 51 como linfomas cutáneos primarios. Las MF representaron el 1,7 % de los casos de LNH. Probablemente hay un sub-registro, porque del total de estos linfomas, el 37,6 % corresponde a LNH SAI (sin otra especificación) (6).
Aunque esta entidad es considerada como de curso clínico indolente, su historia natural es compleja, y de difícil manejo terapéutico, especialmente en las etapas de enfermedad avanzada cutánea. A nivel de la piel, las lesiones pueden ir desde una erupción macular eritematosa con descamación en la fase pre-micótica, y luego máculas, placas, tumores, eritema confluente o eritrodermia, que ocasionan una morbilidad significativa, especialmente cuando afectan una gran superficie cutánea. En estadios más avanzados también puede aparecer afectación ganglionar, visceral y de la sangre periférica la cual es la variante leucémica de la enfermedad, acompañada de eritrodermia (Síndrome de Sézary). (1,4).
En el manejo de la MF se han empleado una gran variedad de modalidades de tratamiento, tópicas y sistémicas, pudiendo obtenerse respuestas favorables, sin embargo, con frecuencia la enfermedad tiende a recurrir y progresar con el paso del tiempo. El problema más complejo es el manejo de la afectación cutánea.
La MF se caracteriza por una alta radio-sensibilidad. La radioterapia (RT) fue utilizada por primera vez en 1902 por Scholtz en Alemania (7), es una de las modalidades de tratamiento tópico, más efectiva, y puede utilizarse con campos localizados, RT superficial limitada (RTSL), en pacientes con estadio IA con lesiones únicas o con dos o tres lesiones contiguas; o en la mayoría de los casos con irradiación cutánea total con electrones (ICTE) en etapas más avanzadas de la enfermedad (1).
El objetivo del presente trabajo es presentar nuestra experiencia de 20 años en el tratamiento con ICTE en pacientes con LCCT (MF) por medio de un análisis de los datos clínicos y los resultados terapéuticos. Además, se hará una revisión de la literatura más relevante sobre este tópico. Es importante resaltar que este trabajo es el primer reporte presentado en Venezuela, en relación al uso de esta técnica de RT en esta afección.
MÉTODO
Se realizó una revisión de las historias clínicas de los pacientes con LCCT (MF) tratados con RT, irradiación cutánea total con electrones (ICTE) durante el período 2000-2020, en la unidad de Radioterapia Oncológica GURVE del Instituto Médico La Floresta y en el Servicio de Radioterapia Dr. Enrique M. Gutiérrez del Centro Médico Docente La Trinidad.
Se presenta una estadística descriptiva de la población en estudio, análisis de los aspectos clínicos, descripción y evaluación de la técnica de tratamiento, tasas de respuesta, duración de la misma, supervivencia actuarial y complicaciones del tratamiento radiante.
Los datos obtenidos de las 96 historias clínicas revisadas fueron registrados en una hoja de cálculo en Microsoft Office Excel. Se excluyeron 43 pacientes por no haber recibido tratamiento radiante o no finalizar el mismo. En el presente trabajo se reportan los resultados de 53 pacientes tratados con RT, 47 fueron tratados con ICTE y 6 con RTSL. De los pacientes tratados con ICTE, 19 recibieron tratamiento radiante como modalidad inicial y 28 fueron referidos después de recaída posterior a tratamiento tópico con otros agentes como: mostaza nitrogenada (MN) y Psoralen y luz ultravioleta A (PUVA) o después de terapias sistémicas con bexaroteno, interferón o quimioterapia con agente único como metotrexato o ciclofosfamida o con varias drogas. En 2 pacientes se administró un segundo curso de ICTE después de recaída a la RT cutánea total con electrones. En relación a los 6 pacientes sometidos a RTSL en 2 se administró tratamiento tópico previo con MN y PUVA, respectivamente. Ningún paciente recibió otro tratamiento concomitante durante la RT. Posteriormente al tratamiento radiante en 24 pacientes se administró otra modalidad terapéutica por recaída o persistencia de la enfermedad con tratamiento tópico con MN en 2 y PUVA en 1 paciente, en el resto se empleó tratamiento sistémico con metotrexato, bexaroteno o quimioterapia múltiple.
Para caracterizar a la población se utilizaron datos como: media, mediana y desviación estándar. Para el análisis de supervivencia se utilizó el método de Kaplan Meier, a fin de obtener curvas de supervivencia global actuarial (SG) y supervivencia libre de progresión (SLP), el método para comparación de las curvas fue el long rank test (8). Para el seguimiento se utilizaron los datos de la historia clínica de RT; y con los pacientes que no habían acudido a la consulta de RT, se realizó contacto directo con los médicos referentes y otros médicos tratantes, con los pacientes y/o familiares, por vía telefónica o personalmente.
En relación a la ICTE, hemos utilizado la técnica de ángulo fijo dual, empleando dos haces de electrones en forma secuencial a lo largo del plano vertical del paciente, como ha sido descrito previamente (1,9). La energía del haz de electrones es de 4 MEV. Se utilizan 6 campos de tratamiento para tratar toda la superficie cutánea, el tratamiento es administrado diariamente 4 días por semana, 1 Gy por día hasta una dosis total de 36 Gy, en 9 semanas. El tratamiento semanal se divide en 2 ciclos, el primer día se tratan los campos anteriores, oblicuo posterior izquierdo y oblicuo posterior derecho, y en el segundo día del ciclo los campos posteriores, oblicuo anterior izquierdo y oblicuo anterior derecho. De esta manera los pacientes reciben 2 Gy a toda la piel en cada ciclo, hasta alcanzar la dosis total de 36 Gy. La planta de los pies, el periné, y las áreas de pliegues pronunciados en tórax y abdomen reciben dosis suplementarias de 20 Gy (1 Gy por día), y el cuero cabelludo 6 Gy (2 Gy por día), respectivamente (Figura 1).

Figura 1
Técnica de ICTE. Se pueden observar 4 de las 6 posiciones utilizadas para la irradiación corporal total.

Figura 2.
Posición del equipo para irradiación del ángulo superior utilizando la técnica de ángulo fijo dual.
RESULTADOS
Las características de la población de 53 pacientes, la edad promedio fue de 53,7 años con un rango de 27 - 87 años. En la distribución por sexo fue prácticamente similar, 27 pacientes (50,9 %) pertenecían al sexo masculino y 26 (49,1 %) al femenino. En relación a la presentación clínica las lesiones más frecuentemente observadas fueron las placas (50,9 %), seguido de tumores (24,5 %), la eritrodermia se presentó solo en 12 % de los pacientes.
El diagnóstico histopatológico se hizo en base al reporte de anatomía patológica enviado por el médico referente, no se realizó de rutina revisión del material de biopsia. De los 53 pacientes en 9 (17 %) se reportó enfermedad foliculotrópica y en 29 (54,7 %) se realizó estudio de inmunohistoquímica.
Los pacientes fueron evaluados desde el punto de vista clínico con un examen físico detallado para determinar la extensión de la enfermedad cutánea y presencia de adenomegalias palpables.
Se realizó tomografía computarizada en 41 pacientes (77,4 %) como estudio de extensión al momento del diagnóstico. En 45 de los 53 pacientes se realizó estudio de sangre periférica para determinación de células de Sézary, en 8 (17,7 %) de ellos resultaron positivas y en 37 (82,2 %) negativas. En 2 individuos se practicó examen de líquido cefalorraquídeo el cual fue negativo. En 11 (20,7 %) biopsia de médula ósea que fue reportada como negativa.
Se dividieron los pacientes siguiendo la clasificación por estadios TNMB, de la MF y el SS revisada por la ISCL/EORTC (10). Aproximadamente 50 % fueron clasificados como estadio IB y 26,5 % IIB (Cuadro 1).
Además, de acuerdo al pronóstico se dividieron los pacientes en dos grupos: estadios precoces IA y IIA 32 pacientes (60,4 %) y estadios avanzados IIB, IIIA y IIIB, 21 pacientes (39,6 %). En cada una de estas dos últimas categorías se trató de clasificar los casos en relación a los factores de riesgo establecidos por el índice pronóstico internacional de los linfomas cutáneos (CLIPi), para la MF y el síndrome de Sézary (SS) (Cuadro 2).
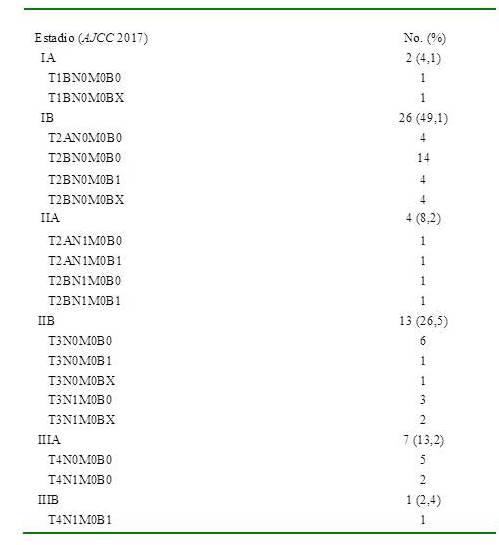
Cuadro 1.
Clasificación por estadios

Cuadro 2
Índice pronóstico internacional de los linfomas cutáneos
En relación a la RT, de los 47 pacientes tratados con ICTE con la técnica anteriormente descrita, en 9 de ellos se administró una dosis adicional a las lesiones voluminosas tumorales. En 2 pacientes se utilizó un segundo curso de ICTE después de recaída a la RT cutánea total con electrones con un intervalo de 32 y 41 meses respectivamente, entre ambos tratamientos.
De los 47 pacientes sometidos a ICTE, 19 recibieron tratamiento radiante como modalidad inicial y 28 fueron referidos después de recaída posterior a tratamiento tópico con otros agentes como: mostaza nitrogenada (MN) y PUVA o después de terapias sistémicas con bexaroteno, interferón o quimioterapia con agente único como metotrexato o ciclofosfamida o con varias drogas. En los 6 pacientes sometidos a RTSL en 2 se administró tratamiento tópico previo con MN y PUVA, respectivamente. Ningún paciente recibió otro tratamiento concomitante durante la RT. Posteriormente al tratamiento radiante en 24 pacientes se administró otra modalidad terapéutica por recaída o persistencia de la enfermedad con tratamiento tópico con MN en 2 y PUVA en 1 paciente, en el resto se empleó tratamiento sistémico con metotrexato, bexaroteno o quimioterapia múltiple.
La mediana de seguimiento fue de 45,2 meses, promedio 67,3 meses, con un rango de 0,47-236,5 meses. Del total de 53 pacientes, 18 (33,9 %) están perdidos de control, a pesar de intentar contactarlos por vía telefónica o a través de los médicos referentes.
La respuesta clínica a la RT se determinó en base al examen físico practicado al finalizar el tratamiento y en los controles sucesivos. (Figura 3, 4, 5 y 5a). En los pacientes sometidos a ICTE se observó respuesta completa (RC) en 27 individuos (57,4 %) y respuesta parcial (RP) en 20 (42, 5%), para una respuesta global (RG) del 100 %. Aquellos sometidos a RTSL 5 obtuvieron RC y 1 RP.
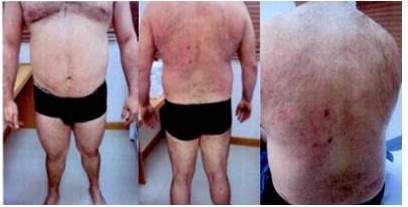
Figura 3.
ICTE
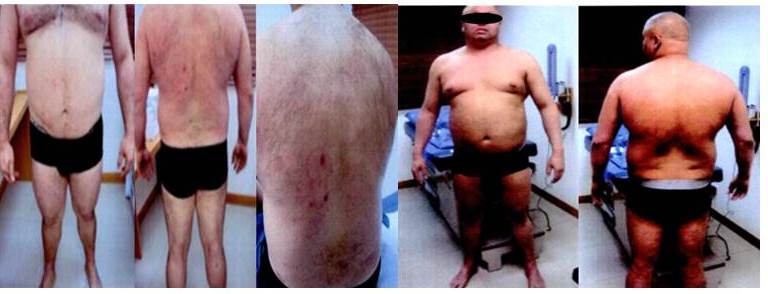
Figura 4.
Después de la RT
Figura 3 y 4. Paciente masculino de 39 años con LCCT (MF) T2bN0M0B0 (IB). Lesiones en tórax, abdomen y extremidades. No recibió tratamiento previo. ICTE dosis 36 Gy en 9 semanas. Presentó RC pero 1 año más tarde recaída en piel, se trata con interferón por 1 año. Actualmente sin evidencia de enfermedad 8 años después del tratamiento.
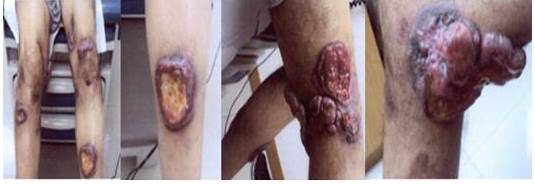
Figura 5.
Imágenes antes de la RTSL
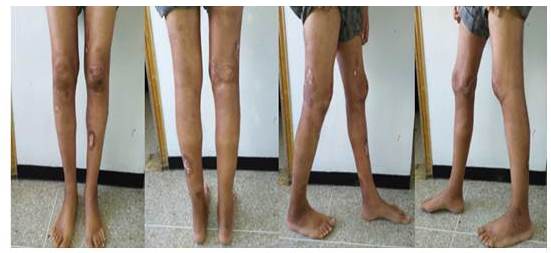
Figura 6
Imágenes actuales 2 años después de la RT
Figura 5 y 6
Al analizar la supervivencia de acuerdo a la extensión de la enfermedad, se encontró que en el grupo de pacientes con estadios precoces (estadios IA-IIA) 19 de 32 (59,37 %) se encuentran vivos sin enfermedad (VSE) 13 de ellos con seguimientos superiores a 60 meses y sólo 4 (12,5 %) han muerto por la enfermedad. Por el contrario, en los estadios avanzados solo 4 de 21 (19 %) pacientes se encuentran VSE y 7 de 21 (33,3 %) fallecieron por la enfermedad (Cuadro 3).
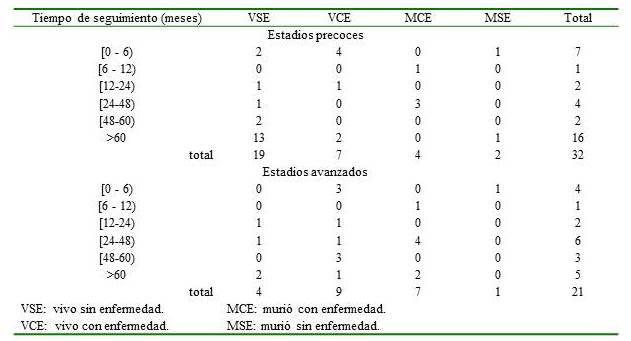
Cuadro 3.
Seguimiento
La SG y la SLP se representan en la (Figura 6), para la totalidad de los casos (53 pacientes) la SG fue de 76,5 % a los 5 años y 72,2 % a los 10 años y la SLP fue 27,6 % y 24,9 %, respectivamente. Al dividir los pacientes de acuerdo a la extensión de la enfermedad se observó que en aquellos con estadios precoces la SG fue de 82,7 % a los 5 y 10 años y 66,6 % y 49,9 %, respectivamente en los estadios avanzados. (P=0,04) (Figura 7).
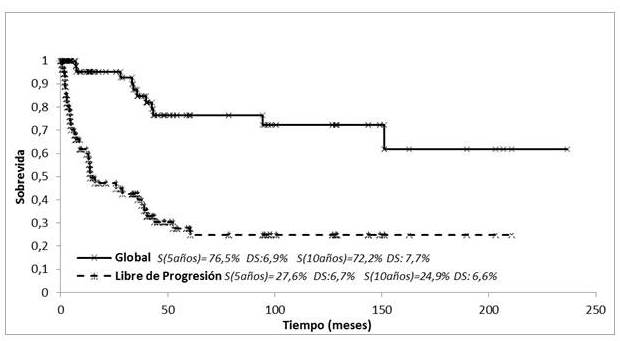
Figura 6
SG y LP. MF tratados con RT.
n=53
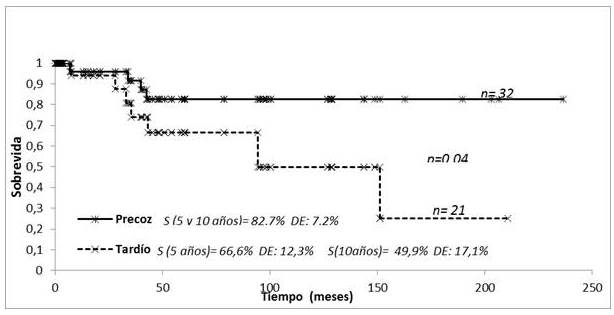
Figura 7
SG MF clasificados por estadio tratados con RT.
Al clasificar los pacientes en los 3 grupos de riesgo de acuerdo al índice pronóstico internacional (CLIPi) se observó que en los estadios tempranos la SG fue de 100 % a los 5 y 10 años en el grupo de riesgo bajo, 89,9 % en riesgo intermedio y 45,7 % en aquellos de riesgo alto (P=0,027) (Figura 8). En los estadios avanzados sólo se pudieron establecer 2 grupos de riesgo, siendo la SG a los 5 años 68,4 % y 45,6 % a los 10 años para el riesgo bajo, en el grupo de riesgo intermedio sólo se incluyeron 2 pacientes (Figura 9).
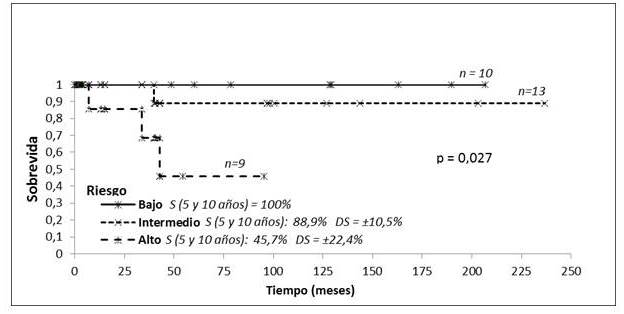
Figura 8
SG MF estadio precoz clasificada por grupos de riesgo tratados con RT.
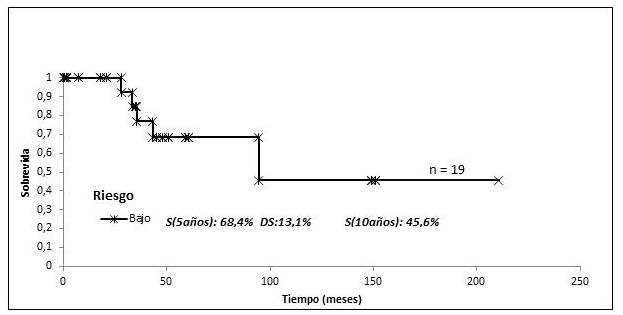
Figura 9
SG MF estadio tardío clasificada por grupos de riesgo tratados con RT.
En cuanto a la SLP en relación a los grupos de riesgo antes mencionados, en los estadios precoces en riesgo bajo fue de 38 % a los 5 y 10 años, 52,1 % en riesgo intermedio, y de 18,4 % a los 3 años en aquellos de riesgo alto (P=0,06) (Figura 10). En los estadios avanzados solo fue posible determinar la curva de SLP para los 19 pacientes del grupo de riesgo bajo la cual fue de 5,9 % a los 5 y 10 años. Solo 2 pacientes pertenecían al grupo de riesgo intermedio y ambos murieron con enfermedad a los 7,4 y 151 meses, respectivamente y no se identificaron pacientes en el grupo de riesgo alto (Figura 11).
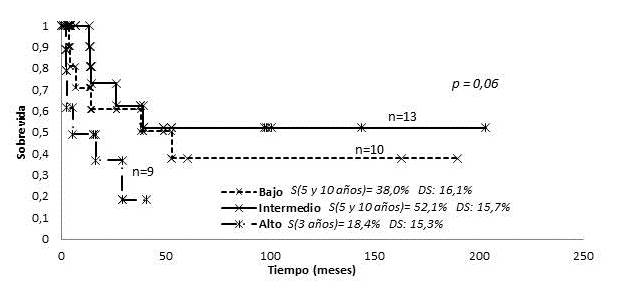
Figura 10.
MF estadio precoz clasificada por grupos de riesgo tratados con RT.
La RTSL fue utilizada en 6 pacientes, 2 de ellos estadio IA y IB, respectivamente y los 4 restantes estadio IIB. Los dos pacientes con estadios precoces obtuvieron RC de la enfermedad después de la RT, uno de ellos, estadio IA está vivo sin enfermedad a los 8 años después del tratamiento y el otro murió sin evidencia de enfermedad por enfermedad cardiovascular. De los 4 pacientes con estadios avanzados 3 se encuentran vivos sin enfermedad, 2 de ellos con seguimientos mayores de 10 años y 15 años respectivamente, 2 de estos pacientes recibieron metotrexato posterior a la RTSL; el otro paciente estaba vivo con evidencia de enfermedad pero perdido de control.
Al analizar los 47 pacientes tratados con ICTE, se encontró que la SG a los 5 años fue de 74,4 % y 24, 7 % a los 10 años, siendo la SLP de 69,4 % y de 21,5 % a los 5 y 10 años, respectivamente (Figura 12). Al dividir los pacientes de acuerdo al estadio se encontró que la SG en los 30 pacientes con estadios precoces fue de 81,9 % a los 5 y 10 años vs. 60,9 % a los 5 años y 30,4 % a los 10 años en los 17 restantes con estadios avanzados (P=0,016); siendo la SLP 35 % vs. 6,8 % a los 5 y 10 años respectivamente (P=0,011).
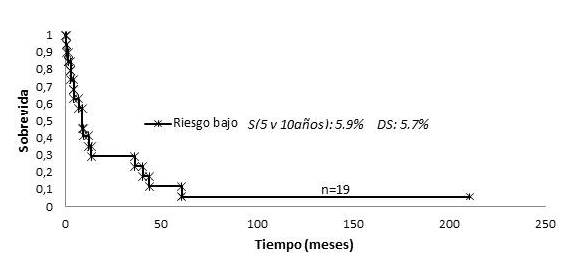
Figura 11
SG y LP MF tratados con técnica de ICTE.
En relación a las complicaciones agudas las más frecuentes fueron a nivel cutáneo siendo grado I el 58,5 % y grado II 33,9 % sólo se observó toxicidad aguda grado III en el 5,6 % de los pacientes. Se presentó conjuntivitis en el 28 % de los pacientes. Las complicaciones crónicas más frecuentemente observada fue atrofia de la piel, alopecia, xerosis y en algunos pacientes telangiectasias, de acuerdo a los datos registrados en las historias fueron clasificadas como grado I en el 64 % de los pacientes
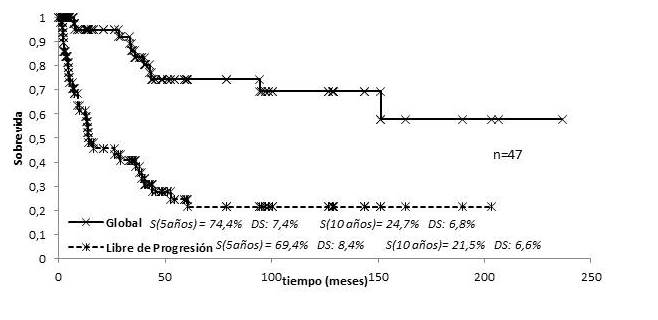
Figura 12
SG y LP MF tratados con técnica de ICTE.
Si se comparan los 19 pacientes sometidos a ICTE como tratamiento inicial con aquellos que recibieron irradiación cutánea total después de haber sido sometidos a otra modalidad terapéutica se observó que la SG a los 5 años fue de 85,1 % y 67,7 %, respectivamente, diferencia no significativa (P=0,25), sin embargo, la SLP a los 5 años fue de 36 % y 19 % diferencia estadísticamente significativa (P= 0,05).
En relación a las complicaciones agudas las más frecuentes fueron a nivel cutáneo siendo grado I el 58,5 % y grado II 33,9 % sólo se observó toxicidad aguda grado III en el 5,6 % de los pacientes. Se presentó conjuntivitis en el 28 % de los pacientes. Las complicaciones crónicas más frecuentemente observada fue atrofia de la piel, alopecia, xerosis y en algunos pacientes telangiectasias, de acuerdo a los datos registrados en las historias fueron clasificadas como grado I en el 64 % de los pacientes.

Cuadro 4
Complicaciones agudas y crónicas.
En 2 pacientes se observaron segundos primarios, en ambos carcinomas basocelulares, uno en párpado inferior derecho y otro en labio inferior, los cuales aparecieron a los 14 y 6 años respectivamente, después de la RT. Estos tumores fueron tratados con cirugía y RT en el tumor del párpado inferior y cirugía en el del labio inferior y ambas lesiones están controladas.
DISCUSIÓN
El LCCT (MF) es una enfermedad poco frecuente; en vista de su evolución clínica peculiar y la complejidad de su terapéutica es fundamental contar con un equipo médico multidisciplinario en el cual deben participar patólogos, dermatólogos, oncólogos médicos y radioterapeutas oncólogos. El ideal es referir los pacientes a centros especializados, donde se haya acumulado experiencia suficiente en el manejo de esta enfermedad.
El diagnóstico inicial de esta patología puede ser difícil especialmente en estadio precoz (1). Se ha propuesto un algoritmo para el diagnóstico y estadificación de la MF en etapa precoz, basado en criterios clínicos, histopatológicos, moleculares e inmuno-patológicos, y se recomienda su aplicación para todos los pacientes incluidos en estudios clínicos y bases de datos (4,11).
La clasificación por estadios seguida en la actualidad se basa en la evaluación de la piel (T), ganglios linfáticos (N), afectación visceral (M) y de la sangre (B) (10) (Cuadro 5 y 6).
Asimismo, a través de un consenso internacional, se han establecido una serie de parámetros clínicos y criterios en la evaluación clínica inicial y para determinar la respuesta al tratamiento en los pacientes con MF y SS, con fin de unificar criterios para la realización de estudios de investigación (12). De manera general, la enfermedad puede dividirse de acuerdo al pronóstico en dos grupos: estadios precoces IA al IIA y estadios avanzados IIB al IV.
En la presente serie la SG de los 53 pacientes fue de 76,5 % a los 5 años y 72,2 % a los 10 años y la SLP fue 27,6 % y 24,9 %, respectivamente; y al dividirlos de acuerdo a la extensión de la enfermedad se observó que la SG en aquellos con estadios precoces fue de 82,7 % a los 5 y 10 años y de 66,6 % a los 5 años y 49,9 % a los 10 años en los estadios avanzados. (P=0,04). Asimismo, se observó una diferencia significativa en la SLP entre los estadios precoces y avanzados 31,5 % vs. 12 % (P=0,012).

Cuadro 5.
Clasificación de a MF y el SS revisada por La ISCL/EORTC. Estadios TNMB (10)
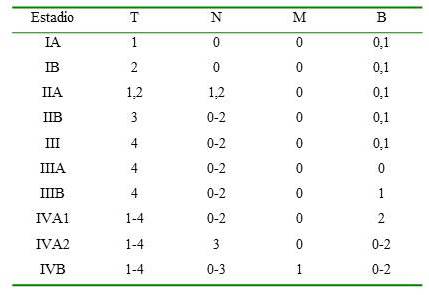
Cuadro 6.
Clasificación por estadios de la MF y el SS revisada por La ISCL/EORTC (10)
Por otra parte se ha encontrado, que algunas características histopatológicas, acarrean un pronóstico más desfavorable. La transformación de la MF a células grandes, y la variedad de MF foliculotrópica. El curso clínico en estos pacientes es usualmente más agresivo, y en algunos casos con cifras de supervivencia más bajas (4).
Se ha descrito un índice pronóstico internacional de los linfomas cutáneos (CLIPi), para la MF y el SS, basado en una data de 1 502 pacientes, tanto en casos de enfermedad en etapa precoz (IA- IIA), como para estadios avanzados (IIB-IVB). Los factores adversos para el pronóstico en enfermedad precoz fueron: sexo masculino, edad >60 años, presencia de placas, enfermedad foliculotrópica, y estadio N1, Nx; y en enfermedad avanzada: sexo masculino, edad >60 años, estadios B1/B2, N2/N3 y afectación visceral. En base a estas variables se definieron 3 grupos distintos para la enfermedad precoz y tardía: bajo riesgo (0-1 factor), riesgo intermedio (2 factores), alto riesgo (3-5 factores), encontrándose una diferencia significativa entre los grupos de riesgo y SG y SLP. En enfermedad precoz las SG a los 10 años fue de 90,3 %, 76,2 % y 48,9 % en los grupos de riesgo bajo, intermedio y alto respectivamente. Las cifras correspondientes para enfermedad avanzada fueron de 53,2 %, 19,8 % y 15 % (13).
En el presente trabajo, se trató de clasificar a los 53 pacientes, de acuerdo al CLIPi, observándose una correlación estadísticamente significativa de la SG a los 5 y 10 años en los estadios tempranos con los 3 grupos de riesgo, siendo en el grupo de riesgo bajo 100 %, 89,9 % en riesgo intermedio y 45,7 % en aquellos de riesgo alto (P=0,027). Sin embargo, los estadios avanzados sólo se pudieron clasificar en 2 grupos de riesgo, siendo la SG a los 5 años 68,4 % y 45,6 % a los 10 años para el riesgo bajo y de 35,4 % a los 5 y 10 años para los de riesgo intermedio (P=0,70). En la SLP no se observó una correlación significativa en los estadios precoces, en los tres grupos de riesgo señalados, es posible que la ausencia de correlación con el pronóstico de la enfermedad de acuerdo al CLIPi entre los grupos de riesgo bajo e intermedio se deba a la falta de uniformidad en la realización de estudios de extensión como la tomografía y al hecho de no haberse realizado de rutina una revisión de la patología (Figura 5). En los estadios avanzados solo se pudo determinar la SLP en los 19 pacientes del grupo de riesgo bajo la cual fue de 5,9 % a los 5 y 10 años. Solo 2 pacientes pertenecían al grupo de riesgo intermedio y no se identificaron pacientes en el grupo de riesgo alto (Figura 6).
Las alternativas de tratamiento pueden dividirse en medidas tópicas o sistémicas. Entre las terapias tópicas se incluyen: esteroides, luz ultravioleta B, PUVA, drogas de aplicación tópica como: MN y carmustine, imiquimod tópico, retinoides tópicos, RTSL, RT a cuerpo entero con haz de electrones, y combinación de estas modalidades. Las diversas alternativas de tratamiento sistémico incluyen: interferón, fotoféresis extracorpórea o foto-quimioterapia extracorpórea (ECP o FQE), administración por vía oral o parenteral de 8-metoxipsoralen, seguido de leucoféresis y exposición de los glóbulos blancos obtenidos en la féresis a luz ultravioleta A, estas células son luego re-infundidas al paciente, retinoides, quimioterapia con agente único como metotrexato a dosis bajas, doxorubicina liposomal pegilada, gemcitabina, fludarabina y otros, quimioterapia combinada con esquemas como CHOP, CVP, CAVE, anticuerpos monoclonales como: alemtuzumab, brentuximab vedotina y mogamulizumab entre otros, inhibidores de la histona desacetilasa (HDAC) como romidepsina y vorinostat, y finalmente en pacientes seleccionados con enfermedad refractaria se debe considerar el trasplante alogénico de células hematopoyéticas con intención curativa (1,14,15).
El objetivo primario en los pacientes con enfermedad precoz limitada a la piel, es obtener la curación de la enfermedad con terapias dirigidas a la piel. Si no es posible la curación en estos pacientes, se puede recurrir a diversas terapias tópicas secuenciales y de tratamiento sistémico por progresión de la enfermedad dérmica, transformación a alto grado, o diseminación (1).
RTSL
En pacientes con estadio IA precoz, con una lesión cutánea única o con dos o tres lesiones cercanas, las cuales puedan ser abarcadas con un campo de irradiación o por campos contiguos, se puede emplear la RTSL, con fines curativos. La serie de la Universidad de Yale (16), incluyó 21 pacientes con estas características, tratados con fotones de 100-280 Kv o con electrones de 4-12 MEV, con una dosis media de 20 Gy (17 de 21 pacientes recibieron ≥ 20 Gy). Ningún paciente había recibido irradiación previa, 6 recibieron tratamiento adyuvante, 5 con PUVA y 1 con esteroides. El tiempo de seguimiento medio fue 36 meses, siendo la tasa de remisión completa clínica de 97 %, con una SLE a los 5 y 10 años de 75 % y 64 % respectivamente, con control local de 75 % a los 10 años. En 13 de los 21 pacientes que presentaron una lesión única de MF se obtuvo una SLE local y a distancia de 91 % a los 10 años, datos que indican una tasa probable de curación superior al 80 % con irradiación superficial local. Resultados similares han sido descritos por otros autores, en la Universidad de Allegheny, en 18 pacientes con lesiones únicas de MF tratadas con campos localizados con electrones y dosis en la mayoría de los casos de 30 Gy con fracciones diarias de 1,8 -2 Gy. Se observó respuesta completa del 100 % y solo dos recidivas en sitios distantes a la lesión inicial, los cuales fueron tratados con MN tópica con control de la enfermedad. La SGL de recaída y la SG a los 10 años fueron 86,2 % y 100 % respectivamente (17).
En la presente serie se empleó la RTSL en 6 pacientes con dosis media de 33 Gy con un rango de 20-46 Gy, en un paciente con extensas lesiones ubicadas en miembros inferiores se emplearon fotones 6 MV y dosis adicional con electrones. En 2 se administró tratamiento tópico previo con MN y PUVA, respectivamente. Solo 2 de estos pacientes eran estadios precoces IA - IB, respectivamente, en ambos se obtuvo RC de la enfermedad, uno de ellos, estadio IA está vivo sin enfermedad a los 8 años después del tratamiento y el otro murió sin evidencia de enfermedad por patología cardiovascular. No se observó toxicidad cutánea severa en estos pacientes.
En las recomendaciones del grupo internacional de linfomas y RT oncológica, para el tratamiento con RTSL se afirma que el rango razonable de dosis oscila de 24 Gy a 30 Gy (18).
En estos pacientes con estadio IA “mínimo” los cuales representan alrededor del 5 % de todos los estadios IA, la RTSL en comparación con otras terapias dirigidas a la piel, tiene una toxicidad aguda menor y crónica limitada, y no acarrea riesgo significativo de desarrollo de neoplasias secundarias cutáneas. Asimismo, provee una alta posibilidad de curación, permitiendo en el futuro, la utilización de otras modalidades terapéuticas si es necesario, incluyendo la ICTE (1).
Por otra parte, la RT paliativa, es de gran utilidad, y puede emplearse en las recidivas cutáneas, afectación visceral y adenopatías sintomáticas. La irradiación local puede producir alivio de diversos síntomas y puede ser administrada después de recurrencias posterior a ICTE.
Por lo general se emplean dosis de 20 a 30 Gy en 2 a 3 semanas. En las lesiones cutáneas limitadas sobre todo en fase de tumor, puede ser más conveniente emplear esquemas de hipofraccionamiento, dosis de 8 Gy en dos fracciones o 7-8 Gy en una sola fracción, con respuestas completas mayores del 90 % (1,19, 20).
ICTE
El tratamiento de pacientes con ICTE utilizando Acelerador Lineal se inicia en 1958 en la Universidad de Stanford, perfeccionándose las técnicas en la década de los años 70, las cuales fueron adaptadas por otras instituciones incluyendo la Universidad de Mc Master en Hamilton, y la Universidad de Yale entre otras (1, 21).
En nuestro país hacia finales de la década de los ochenta se tratan los primeros pacientes en el Hospital Domingo Luciani a cargo de uno de los autores. Luego en el año 2000 con el asesoramiento de la Universidad de Yale y después de realizar un estudio de dosimetría (9) se comienza a implementar esta técnica inicialmente en la Unidad de Radioterapia Oncológica GURVE del Instituto Médico La Floresta y luego en el Servicio de Radioterapia Dr. Enrique M. Gutiérrez del Centro Medico Docente La Trinidad, en colaboración con el Servicio de Dermatología del Hospital Universitario de Caracas, UCV, especialmente con una de las autoras.
Los resultados de las series combinadas de Stanford y Hamilton fueron presentados en 1995; incluyeron un total de 561 pacientes tratados con ICTE solamente, realizando un estudio comprensivo sobre el tema, y además incluyendo el análisis de 730 pacientes adicionales tratados en otros centros (19). Las tasas de RC en piel en estadios IA a IIA oscilaron de 96 %-63 % y en IIB-IVB de 53 %-8 %. Al estudiar la relación entre la dosis
<25 Gy, 2) 25 a <35 Gy 3) 35Gy y el estadio se encontró que la RC fue mayor en el grupo T1 84 %-96 % sin una relación clara con la dosis administrada, mientras que en los grupos T2 a T4 se observó una mejoría en la RC con dosis de 35 Gy. A los 20 años la SLR, en estadio IA en la serie de Stanford fue 46 % y en Hamilton a los 15 años fue 33 %. Muchos de estos pacientes podrían estar curados. Por el contrario en estadios IB a III la SLR fue de 10 % a 25 %. La proporción de muertes por MF aumenta en relación con el estadio, de cifras de 20 % en estadio IA a 100 % en estadio IVB (21).
En base a este reporte y de otros estudios como los de la Universidad de Yale, se estableció para aquel momento la definición de la técnica “moderna” de ICTE, la cual consiste en la administración de 35 a 36 Gy, en 9 semanas, 4 fracciones semanales de 1Gy, con electrones de 4 MEV o de mayor energía (1).
En Inglaterra se han usado esquemas de fraccionamiento diferentes, 30 Gy en 20 fracciones, siguiendo la técnica de Stanford, con algunas modificaciones. En un total de 41 pacientes, estos autores reportaron una respuesta global de 91 % con tasa de RC de 51 % (59 % en estadio IB y 47 % en IIB). La supervivencia media global fue 35 meses para toda la serie, siendo >56 meses en estadio IB, 25 meses en IIB, 46 meses en estadio III y 23,5 meses en el IV. Se observaron recaídas de la enfermedad en 76 % de los casos, con un seguimiento medio de 18 meses, siendo el tiempo medio para la aparición de recaídas de 12 meses (22).
Algunos autores franceses en Dijon, reportaron su experiencia con ICTE, utilizando una camilla de tratamiento móvil, administrando una dosis de 30 Gy en 4 semanas, con fracciones diarias de 2 Gy, 4 días por semana. Esta serie incluyó 57 pacientes con enfermedad T1 y T2. La tasa de respuesta global (RG) fue de 94,7 %, observando RC en 87,5 % de los casos T1 y 84,8 % en T2. La SLR para todo el grupo fue 50 % a los 5 años, siendo la SG a los 5,10 y 15 años de 90 %, 65 % y 42 % respectivamente. En 31 pacientes (54,4 %) se observaron recidivas cutáneas (23).
En los últimos años ha habido un renovado interés en el uso de dosis bajas de ICTE, en comparación con el esquema estándar de 30-36 Gy. El grupo de Stanford revisó los datos de 101 pacientes clasificados como T2, T3 y T4, tratados entre 1958 y 1995, con un curso inicial de ICTE empleando dosis de 5 - < 30 Gy. La RG fue 90 % en casos tratados con 5<10 Gy, en comparación con RG de 98 % y 97 % en aquellos tratados con 10<20 Gy o 20 < 30 Gy, respectivamente. No se observó una diferencia significativa en la supervivencia media libre de progresión en pacientes T2 y T3 cuando fueron estratificados por grupo de dosis, y la SLP fue comparable a la obtenida con el esquema estándar (24).
Se ha ensayado igualmente con esquemas de ICTE a bajas dosis, como una modalidad de reducir la carga tumoral en MF. Hoppe y col. (25) presentaron recientemente un análisis en conjunto de 3 ensayos clínicos fase II, que incluyeron 33 pacientes estadios IB (22), IIA (2), IIB (7) y IIIA (2), tratados con ICTE, y dosis de 12 Gy en 3 semanas con 1 Gy por fracción. La tasa de RG fue 88 %, siendo la tasa de RC 27 %. La duración media del beneficio clínico fue de 70,7 semanas. La toxicidad fue baja y menor a la observada con el régimen convencional de 36 Gy, sin embargo, la tasa de RC después de 12 Gy es inferior a la obtenida con los esquemas estándar de dosis 27 % vs. 75 %. Este esquema de ICTE no debe administrarse con intento curativo, pero puede emplearse en conjunto con otras modalidades terapéuticas. Además, dada su menor toxicidad, hay mayor posibilidad de repetir el curso de ICTE, con menor morbilidad, en caso de recidivas cutáneas.
El grupo de linfomas del Reino Unido (RU) igualmente ha presentado los resultados de un esquema de ICTE con dosis de 12 Gy en 2 semanas y 8 fracciones, siguiendo la técnica de Stanford. En este estudio realizado en tres instituciones se incluyeron 103 pacientes, estadio IB (54), IIB (33), III (12) y estadio IV (4); el tiempo de seguimiento medio es corto de 20,6 meses. Se observó una tasa de RC de 18 % y de respuesta parcial 69 %. La duración media de la respuesta fue 11,8 meses; siendo la supervivencia media libre de progresión para todos los pacientes de 13,2 meses, mayor para el estadio IB 26,5 meses, que en el IIB 11,3 meses y en el estadio III 10,2 meses. La SG de 2 años fue de 94 % en estadio IB, 51 % en IIB, 74 % en III y 0 % en estadio IV. La toxicidad como era de esperar fue menor que con el régimen estándar de 30 Gy en 20 fracciones utilizado en el RU, pero el porcentaje de RC es inferior al reportado con los esquemas convencionales 18 % vs. 51 % (26).
En las recomendaciones del grupo internacional de linfomas y RT oncológica, para el tratamiento con ICTE se tiende a favorecer el empleo de dosis bajas en el rango de 10-12 Gy, argumentando que la duración del tratamiento es menor con menos efectos secundarios, aunque estos esquemas producen un porcentaje de RC inferiores al esquema convencional de 36 Gy (18). En las pautas del NCCN se consideran como dosis adecuadas para ICTE, 12-36 Gy, con fraccionamiento de 4 Gy semanal (15).
En la presente serie de 47 pacientes tratados con ICTE con dosis de 36 Gy, se observó RC en 27 (57,4 %) y RP en 20 (42, 5 %), con una RG del 100 %. La SG a los 5 años fue de 74,4 % y 24,7 % a los 10 años, siendo la SLP de 69,4 % y de 21,5 % a los 5 y 10 años, respectivamente. Si se comparan los pacientes sometidos a ICTE como tratamiento inicial con aquellos que recibieron irradiación cutánea total después de haber sido sometidos a otra modalidad terapéutica no se observó una diferencia estadísticamente significativa en la SG, sin embargo la SLP fue mejor en el grupo sometido a ICTE inicialmente (P=0,05).
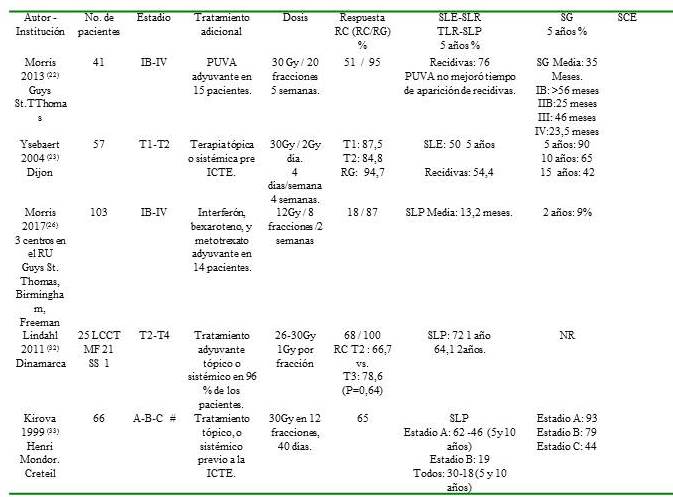
Los resultados de los estudios antes mencionados, otras series y del presente trabajo se muestran en el Cuadro 7
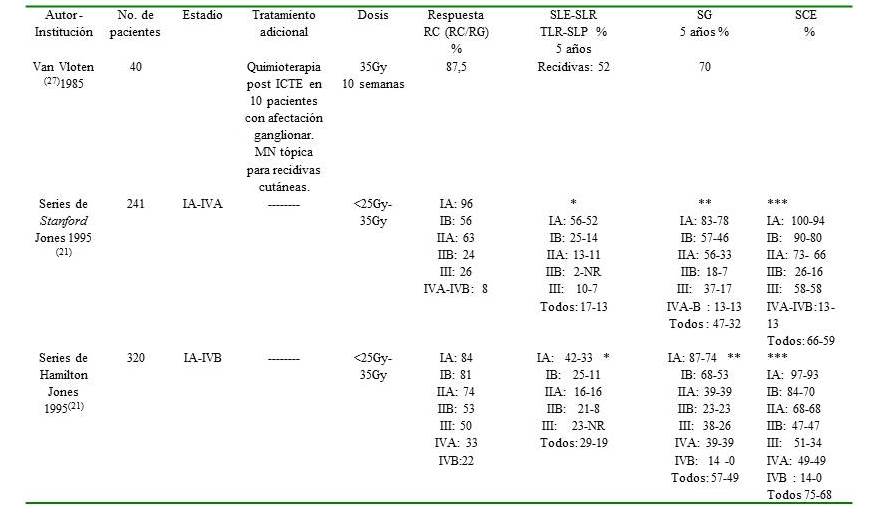
Cuadro 7.
Resultados del tratamiento con ICTE.
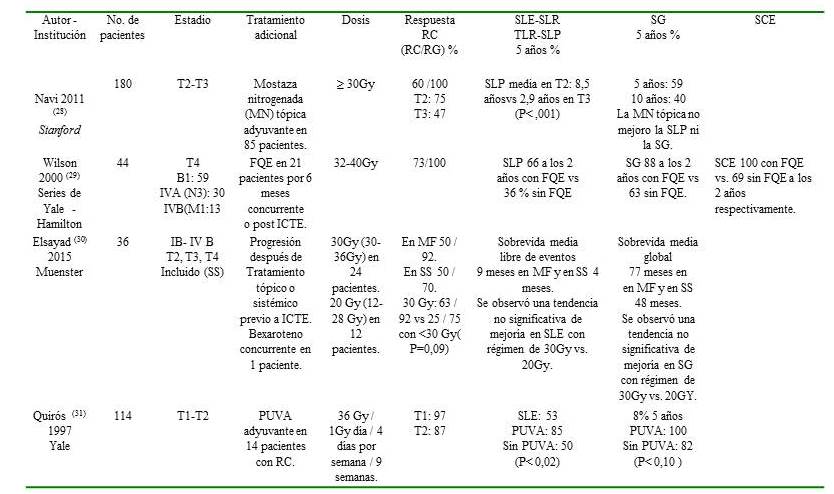
Cuadro 7.
Resultados del tratamiento con ICTE. (Continuación)
Cuadro 7
Resultados del tratamiento con ICTE. (Continuación)
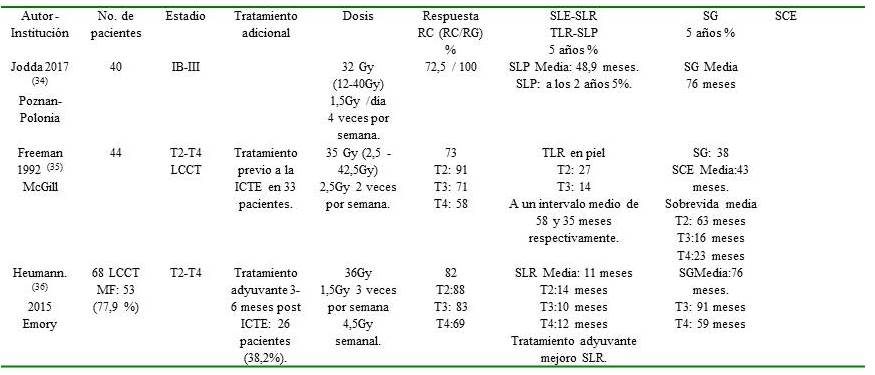
Cuadro 7.
Resultados del tratamiento con ICTE. (Continuación)

Cuadro 7.
Resultados del tratamiento con ICTE. (Continuación)
RC: Respuesta completa. RG: Respuesta global. SLE: Supervivencia libre de recaída. TLR: Tasa libre de recaída. SG: Supervivencia global. SCE: Supervivencia causa específica. SLP: Supervivencia libre de progresión. NR: No reportada. *Supervivencia libre de recaída a los 5 y 10 años **Supervivencia global a los 10 y 15 años *** Supervivencia causa específica a los 10 y 15 años # Estadios - A: Lesiones superficiales que abarcan <50 % de la superficie corporal. B: Lesiones superficiales que abarcan > 50 % de la superficie corporal. C: Tumores en piel, afectación ganglionar o visceral.
Tratamiento repetido con ICTE
Aunque por medio de la ICTE se pueden obtener altas tasas de remisión completa, muchos pacientes van a desarrollar enfermedad recurrente. En estos individuos si no ocurre respuesta a otras modalidades terapéuticas, y preferiblemente en aquellos que hayan presentado un intervalo libre de enfermedad significativo, se puede administrar un nuevo curso de RT con electrones a toda la piel.
Becker y col. (38) reportaron 15 pacientes tratados con dos cursos de ICTE, la dosis promedio del primer curso fue 32,6 Gy y 23,4 Gy en el segundo, con un intervalo promedio de 41,3 meses entre ambos. Después del primer esquema se observó RC en 73 % de los casos, con una duración media de la respuesta de 11,6 meses. El segundo curso produjo RC en 40 % y RP en 60 % de los casos. Asimismo, Wilson y col. (39) en la Universidad de Yale, presentaron una serie de 14 pacientes, que recibieron al menos dos cursos de ICTE, y en 5 de ellos se administró un tercer curso de radiación. La dosis media en cada curso respectivo fue de 36 Gy, 18 Gy y 12 Gy. Se observó una tasa de remisión completa de 86 % después del segundo curso con un intervalo libre de enfermedad de 11,5 meses, y RC en 3 de 5 pacientes (60 %) con el tercer curso. Las secuelas dermatológicas fueron similares (en ambas series), xerosis, depilación, cambios de pigmentación, anhidrosis, descamación, el tratamiento repetido fue relativamente bien tolerado (38,39).
Como parte del tratamiento de las recidiva cutáneas en la serie de Dijon (23) se empleó re-irradiación en 18 de los 31 pacientes que presentaron recaídas en la piel, después de ICTE, dosis de 18-24 Gy (en 6 RT segmentaria con electrones y en 12 ICTE), el resto fueron tratados con esteroides tópicos, PUVA, quimioterapia tópica o sistémica, o interferón. Después de un segundo curso de ICTE la tasa de libre de recaída a los 5 años fue de 70 % vs. 39 % en los pacientes tratados con otras modalidades. La toxicidad observada en los casos sometidos a un segundo curso de irradiación incluyó xerosis, telangiectasias aisladas y cambios distróficos en la uñas de manos y pies
En 2 pacientes se utilizó un segundo curso de ICTE después de recaída a la RT cutánea total con electrones con un intervalo de 32 y 41 meses respectivamente, entre ambos tratamientos, empleando una dosis de 20 Gy, uno de estos pacientes de sexo femenino que tenía antecedentes de trasplante renal después del segundo curso de ICTE recibió posteriormente RTSL a las lesiones tumorales sintomáticas. En ambos pacientes se observó respuesta clínica completa después de la re-irradiación, uno de ellos falleció con enfermedad 42 meses posteriores al tratamiento y la otra está viva con enfermedad con un seguimiento de 45 meses.
Tratamiento adyuvante a la ICTE
En vista de la historia natural de la MF, especialmente en los estadios avanzados, caracterizada por la aparición de recidivas después de lograr la RC con ICTE y otras modalidades terapéuticas empleadas, se han venido utilizando a través de los años varias estrategias, como tratamiento adyuvante o de mantenimiento(40,41). En las series de Stanford, en un análisis retrospectivo de 55 pacientes T2 y 27 T3, se encontró que la mostaza nitrogenada (NH2) tópica adyuvante luego de ICTE, prolongó el intervalo libre de recaída en el grupo T2, sin diferencia en la supervivencia (42). Sin embargo, en un trabajo más reciente de esta misma institución, en 180 pacientes T2 o T3 tratados con ICTE, no se encontró mejoría en la tasa libre de recaída, supervivencia libre de progresión o SG con el empleo de NH2 adyuvante tópica (28).
En Yale se empleó tratamiento adyuvante con PUVA después de ICTE en una serie de pacientes T1 y T2, con una cifra de SLE a los 5 años de 85 % comparado con 50 % (P <0,02) en aquellos que no recibieron tratamiento adyuvante (31). El tratamiento adyuvante con una de estas 2 modalidades debe ser considerado en los pacientes con enfermedad limitada a la piel después de finalizar la ICTE; sin embargo, se necesitan datos de estudios aleatorios para confirmar estos resultados.
A diferencia de otros tipos de linfomas, la quimioterapia en la MF no ha tenido un papel muy relevante, y debe considerarse como un tratamiento paliativo, hasta ahora no ha demostrado producir un aumento en la supervivencia(1,43). En el estudio aleatorio de Kaye y col. (44), se comparó la combinación de CAVE, asociado a ICTE hasta una dosis de 30 Gy, vs. tratamiento tópico secuencial que incluyó ICTE en el momento de progresión, siendo la tasa de remisión completa superior en el grupo de tratamiento combinado, pero la toxicidad igualmente mayor, no observándose una diferencia significativa entre los dos grupos en cuanto a la SLE o a la SG a los 75 meses. En Yale, Braverman (45) reportó los resultados iniciales obtenidos con la combinación de doxorrubicina y ciclofosfamida posterior al tratamiento con ICTE, observando un beneficio en la SLE después de 3 años, pero este resultado favorable no se mantuvo con seguimiento ulterior (46).
La foto-quimioterapia extracorpórea (FQE) ha sido utilizada en pacientes en combinación con otras medidas terapéuticas y en forma adyuvante en casos de MF avanzada. En Yale (46), en pacientes con enfermedad T3 y T4 en remisión completa después de ICTE se aplicó FQE, encontrando una mejoría que no alcanzó validez estadística (P<0,06) en la supervivencia al comparar estos pacientes con aquellos tratados con ICTE sola o en combinación con otras modalidades, sin embargo, el número de casos fue pequeño y el seguimiento limitado. Datos más recientes publicados por Wilson y col., revelan una mejoría significativa en la SLE y en la SCE a los 2 años, con el uso de FQE más ICTE, en pacientes con eritrodermia T4 (29).
Se ha utilizado también el eterinato en conjunto como tratamiento concurrente y adyuvante a la ICTE con una dosis de 35 Gy, no encontrándose mejoría significativa en la supervivencia libre de recaída, comparada con ICTE sola (47).
Wagner y col., (48) reportaron una serie de 30 pacientes tratados con ICTE (36 Gy en 18 fracciones) y con interferón alfa-2b de manera concurrente y luego adyuvante por un año, no observando mejoría en la SG ni en la SLP a los 5 años, al compararlos con 11 pacientes tratados con ICTE solamente.
En el Hospital MD Anderson, se ensayó un protocolo de tratamiento agresivo, que incluyó interferón alfa e isotretinoina oral seguida de ICTE (36 Gy) y luego mantenimiento con MN tópica e interferón alfa en 95 pacientes; de ellos 50 eran estadios IA y IIA y 45 estadios IIB-IVB. En los estadios avanzados se administró también quimioterapia con múltiples agentes, 6 ciclos antes de la ICTE. La tasa de respuesta global fue 85 % y de RC 60 %, siendo la SLE media de 62 meses en los estadios precoces y 6 meses en estadios avanzados, con SLE actuarial a los 5 años de 50 % y 27 % respectivamente. La SG a los 5 años fue 94 % en estadios IA y IIA y 35 % en estadios IIB-IVB. En este estudio no aleatorio, los autores concluyen que el esquema de tratamiento fue bien tolerado y podría producir una tasa de respuesta y SLE superior a la ICTE sola, sin haber una mejoría en la SF (49).
A pesar de no haber una evidencia sólida, sobre la utilidad del tratamiento adyuvante después de la ICTE, en las pautas del NCCN (15), en estadios IB, IIA se sugiere emplear luego de ICTE tratamiento con bexaroteno o interferón para mantener o prolongar la respuesta a la RT. En estadios IIB con lesiones tumorales localizadas sugieren tratamientos dirigidos a la piel, o tratamiento sistémico a base de retinoides, interferón, inhibidores de la HDAC, FQE, metotrexato, o anticuerpos monoclonales, con o sin RT localizada para las lesiones tumorales. Otra alternativa especialmente en pacientes con tumores generalizados, es la ICTE, seguida de tratamiento adyuvante con agentes biológicos como interferón o bexaroteno para prolongar la duración de la respuesta.
Pacientes con estadios III sin afectación sanguínea (B0), deben ser manejados inicialmente con terapias dirigidas a la piel; la ICTE es otra alternativa a considerar, pero en estos casos ha habido reportes de mayor toxicidad en pacientes con eritrodermia y piel muy atrófica los cuales pueden desarrollar descamación severa aun con dosis bajas de 4 Gy, sin embargo, aquellos individuos con piel muy engrosada pueden tolerar la ICTE convencional, se recomienda de todas formas emplear esquemas de dosis más bajas y con fracciones menores. Algunos autores recomiendan tratamiento sistémico con metotrexato o retinoides, y esteroides tópicos o sistémicos para mejorar los síntomas cutáneos, y emplear antibióticos por el mayor riesgo de infecciones secundarias que presentan estos pacientes. En estadio III con afectación sanguínea (B1), y en estadio IV el tratamiento sistémico es la primera opción con los agentes señalados, con o sin terapia dirigida a la piel de acuerdo a la evolución clínica; la ICTE en estos casos también se ha utilizado y puede ser muy efectiva como tratamiento paliativo, siendo preferible emplear los esquemas de bajas dosis(4,15). Finalmente en pacientes seleccionados con estadios IIB-IV enfermedad progresiva o refractaria al tratamiento, candidatos para trasplante alogénico, se ha empleado la ICTE (36 Gy) como terapia cito- reductora antes del trasplante (50).
En la presente serie de 47 pacientes tratados con ICTE, no se utilizó tratamiento adyuvante de rutina, sólo se emplearon otras modalidades terapéuticas al momento de recaída o persistencia de la enfermedad.
Toxicidad
Los efectos secundarios de la RTSL son muy limitados, en vista del tamaño de los campos utilizados y las dosis bajas de RT empleadas. Por lo general solo se observa eritema y alopecia, en el área tratada.
En cambio en la ICTE, empleando dosis convencionales, de 30 a 36 Gy, la toxicidad aguda es significativa, en un análisis detallado de las series de la Universidad de Yale se observó: eritema y descamación en 76 % de los casos, vesículas 52 %, hiper-pigmentación 50 %, y dolor cutáneo 48 %; además existe un mayor riesgo de infección cutánea en 32 % de los pacientes tratados. Sin embargo, la mayoría de las toxicidades encontradas (89 %) son grado 1 o 2, no se encontraron toxicidades grado 4 o 5 (51). Entre otras complicaciones agudas posibles están la xerosis, hipo-hidrosis, edema de miembros inferiores, y perdida de las uñas. Las secuelas cutáneas crónicas pueden incluir telangiectasias con atrofia, xerosis, alopecia e hipo-hidrosis. Por otra parte se han descrito casos de neoplasias malignas secundarias en pacientes tratados con ICTE (52), pero muchos de estos individuos habían sido tratados también con MN tópica y PUVA, factores que pueden contribuir al riesgo de aparición de esta complicación (53). El empleo subsecuente de RT con fotones o electrones después del tratamiento con ICTE, no parece incrementar el riesgo desarrollo de neoplasias malignas secundarias cutáneas (52). Debido a la penetración limitada de los electrones, no se debe observar toxicidad hematológica o gastrointestinal.
En la presente serie la mayoría de complicaciones agudas cutáneas fueron grado I en 58,5 % y grado II 33,9 %, sólo grado III en el 5,6 % de los pacientes. Se presentó conjuntivitis en el 28 % de los pacientes. La toxicidad cutánea crónica coincide con la descrita en otras series y la mayoría de las complicaciones fueron grado I, sin embargo, es posible que exista un sub-registro dado que algunos de estos pacientes no han sido controlados directamente en la consulta del servicio de RT. Al analizar los 8 pacientes con eritrodermia (T4) y los 2 sometidos a re-irradiación con ICTE no se observó un incremento significativo en las complicaciones comparadas con el resto de la población general. En cuanto a la aparición de segundos primarios, 2 pacientes presentaron un carcinoma basocelular de la piel del parpado inferior y labio inferior respectivamente, 14 y 6 años después de la ICTE, en estos individuos no se administró otro tratamiento tópico o sistémico.
REFERENCIAS
1. Wilson LD, Jones GW, Kacinski BM. Linfoma Cutáneo de Células T. En: Urdaneta N, Vera A, Peschel RE, Wilson LD, editores. Radioterapia Oncológica Enfoque Multidisciplinario. Disinlimed:Caracas; 2009.p.1099.
2. Papac R, Roberts KB, Prosnitz LR, Urdaneta N. En: Urdaneta N, Vera A, Peschel RE, Wilson LD, editores. Radioterapia Oncológica Enfoque Multidisciplinario Linfomas No Hodgkin. Disinlimed:Caracas; 2009.p.1031.
3. Alibert JLM. Tableau du Pian Fongoïde. Description des Maladies de la Peau, Observées a Hospital Saint-Louis et Exposition des meilleurs Méthodes Suivies pour leur Traitement. Barrois L′Aine & Fils, Paris. 1806;413-446.
4. Hoppe RT, Kim YH, Horwitz S. Mycosis Fungoides : Clinical manifestations, pathologic features, and diagnosis of mycosis fungoid. Treatment of early stage (IA to IIA) mycosis fungoid. Treatment of advanced stage (IIB to IV) mycosis fungoid. Disponible en URL: https://www.uptodate.com/contents/search.
5. Imam MH, Shenoy PJ, Flowers CR, Phillips A, Lechowicz MJ. Incidence and survival patterns of cutaneous T-cell lymphomas in the United States. Leuk Lymphoma. 2013;54:752-759.
6. Capote L. Estadísticas de cáncer en Venezuela. Disponible en: URL: www.mpps.gob.ve.
7. Scholtz W. Ueber den Einfluss der Rontgenstrahlen auf die Haut in gesunden und krankem Zustande. Archiv fur Dermatologie und Syphillis. 1902;59:421-449.
8. Matthews DE, Farewel VT. Using and understanding medical statistics. 4. edición. Londres: Karger AG;2007.
9. Reggio F, Dávila J. Optimización de la técnica de irradiación cutánea total con electrones. 2004. Disponible en :URL: https://www.researchgate.net/publication/237320328_OPTIMIZACION_DE_LA_TECNICA_DE_IRRADIACION_CUTANEA_TOTAL_CON_ELECTRONES
10. Olsen E, Vonderheid E, Pimpinelli N, Willemze R, Kim Y, Knobleret R, et al. Revisions to the staging and classification of mycosis fungoides and Sezary syndrome: A proposal of the International Society for Cutaneous Lymphomas (ISCL) and the cutaneous lymphoma task force of the European Organization of Research and Treatment of Cancer (EORTC). Blood. 2007;110:1713-1722.
11. Pimpinelli N, Olsen EA, Santucci M, Vonderheid E, C Haeffner AC, Stevens S, et al. Defining early mycosis fungoid. J Am Acad Dermatol. 2005;53:1053-1063.
12. Olsen EA, Whittaker S, Kim YH, Duvic M, Prince HM, Lessinet SR, et al. Clinical end points and response criteria in mycosis fungoid and Sézary syndrome: A consensus statement of the International Society for Cutaneous Lymphomas, the United States Cutaneous Lymphoma Consortium, and the Cutaneous Lymphoma Task Force of the European Organization for Research and Treatment of Cancer. J Clin Oncol. 2011;29(18):2598-2607.
13. Benton EC, Crichton S, Talpur R, Agar NS, Fields PA, Wedgeworth E, et al. A cutaneous lymphoma international prognostic index (CLIPi) for mycosis fungoides and Sezary syndrome. Eur J Cancer. 2013;49:2859-2868.
14. Tarabadkar ES, Shinohara MM. Skin directed therapy in cutaneous T-Cell lymphoma. Front Oncol. 2019;9:260. doi:10.3389/fonc.2019.00260
15. Horwitz S, Ansell S, Ai WZ. Primary cutaneous lymphoma: Mycosis fungoides/Sézary Syndrome. Disponible en: URL: https://www.nccn.org/professionals/physician_gls/default_nojava.aspx
16. Wilson LD, Kacinski BM, Jones GW. Local superficial radiotherapy in the management of minimal stage IA cutaneous T-cell lymphoma (Mycosis Fungoides). Int J Radiat Oncol Biol Phys. 1998;40:109-115.
17. Micaily B, Miyamoto C, Kantor G, Lessin S, Rook A, Brady L, et al. Radiotherapy for unilesional mycosis fungoides. Int J Radiat Oncol Biol Phys. 1998;42:361-364.
18. Specht L, Dabaja B, Illidge T, Wilson LD, T Hoppe RT, International Lymphoma Radiation Oncology Group. Modern radiation therapy for primary cutaneous lymphomas: Field and dose guidelines from the International Lymphoma Radiation Oncology Group. Int J Radiat Oncol Biol Phys. 2015;92:32-39.
19. Neelis KJ, Schimmel EC, Vermeer MH, Senff NJ, Willemze R, Noordijk EM. Low-dose palliative radiotherapy for cutaneous B- and T-cell lymphomas. Int J Radiat Oncol Biol Phys. 2009;74:154-158.
20. Thomas TO, Agrawal P, Guitart J, Rosen ST, Rademaker AW, Querfeld, C, et al. Outcome of patients treated with a single-fraction dose of palliative radiation for cutaneous T-cell lymphoma. Int J Radiat Oncol Biol Phys. 2013;85:747-753.
21. Jones GW, Hoppe RT, Glatstein E. Electron beam treatment for cutaneous T-cell lymphoma. Hematol Oncol Clin North Am. 1995;9:1057-1076.
22. Morris SL, McGovern M, Bayne S, Wain M, Child F, Whittaker S. Results of a 5-week schedule of modern total skin electron beam radiation therapy. Int J Radiat Oncol Biol Phys. 2013;86:936-951.
23. Ysebaert L, Truc G, Dalac S, Lambert D, Petrella T, Barillot I, et al. Ultimate results of radiation therapy for T1-T2 mycosis fungoides (including re-irradiation). Int J Radiat Oncol Biol Phys. 2004;58:1128-1134.
24. Harrison C, Young J, Navi D, Riaz N, Lingala B, Kim, Y, et al. Revisiting low-dose total skin electron beam therapy in mycosis fungoides. Int J Radiat Oncol Biol Phys. 2011;81:e651-657.
25. Hoppe RT, Harrison C, Tavallaee M, Bashey S, Sundram U, SLi S, et al. Low-dose total skin electron beam therapy as an effective modality to reduce disease burden in patients with mycosis fungoid: Results of a pooled analysis from 3 phase-II clinical trials. J Am Acad Dermatol. 2015;72:286-292.
26. Morris S, Scarisbrick J, Frew J, Irwin C, Grieve R, Humber C, et al. The results of low-dose total skin electron beam radiation therapy (TSEB) in patients with Mycosis Fungoides from the UK Cutaneous Lymphoma Group. Int J Radiat Oncol Biol Phys. 2017;99(3):627-633.
27. Van Vloten WA, de Vroome H, Noordijk EM. Total skin electron beam irradiation for cutaneous T-cell lymphoma (mycosis fungoides). Br J Dermatol. 1985;112:697-702.
28. Navi D, Riaz N, Levin YS, Sullivan NC, Kim YH, T Hoppe RT. The Stanford University experience with conventional-dose, total skin electron-beam therapy in the treatment of generalized patch or plaque (T2) and tumor (T3) mycosis fungoides. Arch Dermatol. 2011;147:561-567.
29. Wilson LD, Jones GW, Kim D, Rosenthal D, Christensen JR, Edelson RL, et al. Experience with total skin electron irradiation in combination with extracorporeal photopheresis in the management of patients with erythrodermic (T4) mycosis fungoides. J Am Acad Dermatol. 2000;43(1 Pt 1):54-60.
30. Elsayad K, Kriz J, Moustakis C, Scobioala S, Reinartz G, Haverkamp U, et al. Total skin electron beam for primary cutaneous T-cell lymphoma. Int J Radiat Oncol Biol Phys. 2015;93:1077-1086.
31. Quirós PA, Jones GW, Kacinski BM, Braverman IM, Heald PW, Edelson RL, et al. Total skin electron beam therapy followed by adjuvant psoralen/ultraviolet-A light in the management of patients with T1 and T2 cutaneous T-cell lymphoma (mycosis fungoides). Int J Radiat Oncol Biol Phys. 1997;38:1027-1035.
32. Lindahl LM, Kamstrup MR, Petersen PM, Wirén J, Fenger-Grøn M, Gniadecki R, et al. Total skin electron beam therapy for cutaneous T-cell lymphoma: A nationwide cohort study from Denmark. Acta Oncol. 2011;50:1199-1205.
33. Kirova YM, Piedbois Y, Haddad E, Levy E, Calitchi E, Marinello G, et al. Radiotherapy in the management of mycosis fungoides: Indications, results, prognosis. Twenty year experience. Radiother Oncol. 1999;51:147-151.
34. Jodda A, Pawlaczyk M, Fundowicz M, Piotrowskiet T. EP-1399. Rotary dual total skin electron beam therapy as palliative treatment for mycosis fungoid. Radiother Oncol. 2017;123:S748.
35. Freeman CR, Suissa S, Shenouda G, Vuong T, Souhami L, Pla M, et al. Clinical experience with a single field rotational total skin electron irradiation technique for cutaneous T cell lymphoma. Radiother Oncol. 1992;24:155-162.
36. Heumann TR, Esiashvili N, Parker S, Switchenko JM, Dhabbaan A, Goodman M, et al. Total skin electron therapy for cutaneous T cell lymphoma using a modern dual field rotational technique. Int J Radiat Oncol Biol Phys. 2015;92:183-191.
37. Georgakopoulos I, Papadavid E, Platoni K, Dilvoi M, Patatoukas G, Kypraiou E, et al. Clinical application of total skin electron beam (TSEB) therapy for the management of T cell cutaneous lymphomas. The evolving role of low dose (12 Gy) treatment schedule. Clin Transl Radiat Oncol. 2018;15:26-30.
38. Becker M, Hoppe RT, Knox SJ. Multiple courses of high-dose total skin electron beam therapy in the management of mycosis fungoides. Int J Radiat Oncol Biol Phys. 1995;32:1445-1449.
39. Wilson LD, Quiros PA, Kolenik SA, Heald P, Braverman I, Edelson R, et al. Additional courses of total skin electron beam therapy in the treatment of patients with recurrent cutaneous T-cell lymphoma. J Am Acad Dermatol. 1996;35:69-73.
40. Trautinger F, Eder J, Assaf C, Bagot M, Cozzio A, Dummer R, et al. European Organization for Research and Treatment of Cancer consensus recommendations for the treatment of mycosis fungoides/Sézary syndrome - Update 2017. Eur J Cancer. 2017;77:57-74.
41. Dummer R, Assaf C, Bagot M, Gniadecki R, Hauschild A, Knobler R, et al. Maintenance therapy in cutaneous T-cell lymphoma: Who, when, what? Eur J Cancer. 2007;43:2321-2329.
42. Chinn DM, Chow S, Kim YH, Hoppe RT. Total skin electron beam therapy with or without adjuvant topical nitrogen mustard or nitrogen mustard alone as initial treatment of T2 and T3 mycosis fungoides. Int J Radiat Oncol Biol Phys. 1999;43:951-958.
43. Rosen ST, Foss FM. Chemotherapy for mycosis fungoid and the Sezary syndrome. Hematol Oncol Clin North Am. 1995;9:1109-1116.
44. Kaye FJ, Bunn PA Jr, Steinberg SM, Stocker JL, Ihde DC, Fischmannet AB, et al. A randomized trial comparing combination electron-beam radiation and chemotherapy with topical therapy in the initial treatment of mycosis fungoides. N Engl J Med. 1989;321:1784-1790.
45. Braverman IM, Yager NB, Chen M, Cadman EC, Hait WN, Maynard T. Combined total body electron beam irradiation and chemotherapy for mycosis fungoides. J Am Acad Dermatol. 1987;161(1 Pt 1):45-60.
46. Wilson LD, Licata AL, Braverman IM, Edelson RL, Heald PW, Feldman AM, et al. Systemic chemotherapy and extracorporeal photochemotherapy for T3 and T4 cutaneous T-cell lymphoma patients who have achieved a complete response to total skin electron beam therapy. Int J Radiat Oncol Biol Phys. 1995;32:987-995.
47. Jones G, McLean J, Rosenthal D, Roberts J, Sauder DN. Combined treatment with oral etretinate and electron beam therapy in patients with cutaneous T-cell lymphoma (mycosis fungoides and Sézary syndrome). J Am Acad Dermatol. 1992;26:960-967.
48. Wagner AE, Wada D, Bowen G, Gaffney DK. Mycosis fungoides: The addition of concurrent and adjuvant interferon to total skin electron beam therapy. Br J Dermatol. 2013;169:715-718.
49. Duvic M, Apisarnthanarax N, Cohen DS, Smith TL, Ha CS, Kurzrock R. Analysis of long-term outcomes of combined modality therapy for cutaneous T-cell lymphoma. J Am Acad Dermatol. 2003;49:35-49.
50. Duvic M, Donato M, Dabaja B, Richmond H, Singh L, Wei W, et al. Total skin electron beam and non-myeloablative allogeneic hematopoietic stem-cell transplantation in advanced mycosis fungoides and Sezary syndrome. J Clin Oncol. 2010;28:2365-2372.
51. Lloyd S, Chen Z, Foss FM, Girardi M, Wilson LD. Acute toxicity and risk of infection during total skin electron beam therapy for mycosis fungoides. J Am Acad Dermatol. 2013;69:537-543.
52. Licata AG, Wilson LD, Braverman IM, Feldman AM, Kacinski BM. Malignant melanoma and other second cutaneous malignancies in cutaneous T-cell lymphoma. Arch Dermatol. 1995;131:432-435.
53. Stern RS, Nichols KT, Vakeva LH. Malignant melanoma in patients treated for psoriasis with methoxsalen (psoralen) and ultraviolet a radiation (PUVA). The PUVA Follow-Up Study. N Eng J Med. 1997;336(15):1041-1045.
Notas de autor
rreyes@radioterapia.com.ve
Información adicional
Trabajo ganador Premio: “Dr. Alejandro Calvo Lairet” 2020