ESTUDIO HISTOLÓGICO E INMUNOHISTOQUÍMICO DE TUMORES MEDIASTINALES
ESTUDIO HISTOLÓGICO E INMUNOHISTOQUÍMICO DE TUMORES MEDIASTINALES
Revista Venezolana de Oncología, vol. 33, núm. 4, pp. 240-265, 2021
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 05 Mayo 2021
Revisado: 13 Julio 2021
Aprobación: 26 Agosto 2021
Resumen: OBJETIVO: Evaluar aspectos histológicos e inmunohistoquímicos de tumores del mediastino recibidos en la Sección de Patología Respiratoria del Instituto Anatomopatológico Dr. José Antonio O’Daly, durante 2006-2014. MÉTODO: Estudio descriptivo, retrospectivo. RESULTADOS: 164 casos se seleccionaron 137 casos para el estudio. Rango de edad osciló entre 2 y 80 años. Del total de casos 80 pacientes (58,4 %) eran de sexo masculino y 57 (41,6 %) femenino. Histológicamente 40 casos (29,2 %) correspondieron a tumores epiteliales malignos, 37 (26,3 %) tumores linfoides, 24 (17,5 %) lesiones epiteliales benignas, 13 (10,2 %) fueron no clasificables, 12 (8,8 %) tumores mesenquimáticos y 11 (8,0 %) tumores germinales. 55 de estos (40,1%) se encontraban en el mediastino anterior, 6 (4,4 %) en mediastino medio, 7 casos (5,1 %) en mediastino posterior y los 69 casos restantes (50,4 %) sin especificar localización. En mediastino anterior, los más frecuentes fueron de estirpe linfoide (29,1 %), seguido de epiteliales malignos (21,8 %); en el mediastino medio, el 83,3 % correspondió a tumores epiteliales malignos y en mediastino posterior, los más frecuentes eran de origen mesenquimáticos (57,1 %). CONCLUSIÓN: Los tumores de mediastino son patologías poco frecuentes, se presentan a cualquier edad. Por lo tanto, debemos tenerlas presentes dentro de nuestros diagnósticos diferenciales. El pronóstico de este tipo de patología depende del tipo histológico del tumor, de su extensión anatómica y de la posibilidad de resecarlo completamente. El estudio histopatológico continua siendo indispensable para el diagnóstico.
Palabras clave: Mediastino, tumores de mediastino, biopsias, mediastino anterior, mediastino medio, mediastino posterior.
Abstract: OBJECTIVE: Histological and immunohistochemically evaluate aspects of mediastinal tumors received in the Section of Pathological Institute of Respiratory Diseases Dr. Jose Antonio O'Daly, during 2006-2014. METHOD: Descriptive, retrospective study. RESULTS: 164 biopsies referred to as mediastinal tumors 137 were selected for the study. Age ranged from 2 to 80 years. 80 patients (58.4 %) were male 57 (41.6 %) female. Histologically, 40 cases (29.2 %) corresponded to malignant epithelial tumors, 37 (26.3 %) lymphoid tumors, 24 (17.5 %) benign epithelial lesions, 13 (10.2 %) were unclassifiable, 12 (8.8 %) mesenchymal tumors and 11 cases (8.0 %) germ tumors. 55 (40.1 %) were in the anterior mediastinum, 6 (4.4 %) in the middle mediastinum, 7 cases (5.1 %) in the posterior mediastinum, and the remaining 69 cases (50.4 %) ) without specifying location. In anterior mediastinum, the most frequent were lymphoid (29.1 %), followed by malignant epithelial tumors (21.8 %); of those in the middle mediastinum, 83.3 % corresponded to malignant epithelial tumors and in the posterior mediastinum; the most frequent were mesenchymal origin (57.1 %). CONCLUSION: Mediastinal tumors are rare diseases, which can occur at any age. To reach them, we know them and have them present in our differential diagnosis. The prognosis for this type of pathology depends on the histological type of tumor, its anatomical extent and the possibility of completely drying it, so histopathology is essential and is still considered the gold standard for diagnosis.
Keywords: Mediastinum, mediastinal tumors, biopsy, anterior mediastinum, posterior mediastinum, middle mediastinum.
INTRODUCCIÓN
El mediastino es un espacio anatómico en el que asientan múltiples afecciones tanto neoplásicas como no neoplásicas (1). Existe una gran diversidad de estructuras anatómicas que discurren por el mediastino y cada una de ellas puede dar lugar a distintos tipos de tumores en función de los tejidos que las componen (2).
El mediastino está dividido en compartimientos anterior, medio y posterior. Una vez que los tumores tienen una localización anatómica preferencial, conocer la división del mediastino tiene importancia clínica y terapéutica (3).
Sus límites son hacia adelante la cara posterior del esternón conjuntamente con los cartílagos costales y hacia atrás la cara anterior de las vértebras torácicas. El límite inferior está conformado por el diafragma y el superior está en continuidad con el cuello y está representado por un plano transversal que pasa por la incisura yugular y por el disco intervertebral que separa la séptima vértebra cervical con la primera torácica (3).
El conocimiento de esta división tiene importancia porque los tumores y lesiones inflamatorias, congénitas o degenerativas tienden a localizarse en uno u otro compartimento, según el tejido que las origina; sin embargo, un tumor puede nacer en un compartimento mediastinal o hasta en otra región anatómica, pero por efecto de su crecimiento, relaciones anatómicas, peso y ley de la gravedad, puede alojarse en un sitio diferente al que le dio origen (4).
Las neoplasias mediastinales son tumores poco comunes que pueden aparecer a cualquier edad, pero son más comunes entre la tercera y la quinta década de la vida. Aproximadamente 40 % de las masas son asintomáticas y se descubren incidentalmente en una radiografía de tórax de rutina. El restante 60 % de los casos tienen síntomas relacionados con la compresión o la invasión directa de las estructuras que rodean el mediastino, o a síndromes para-neoplásicos (5).
El diagnóstico de estos tumores puede sospecharse por la clínica y la radiología, pero ninguna exploración ni manifestación clínica son características, y pueden simular diversas enfermedades. Siempre debe realizarse diagnóstico diferencial con otras patologías, sobre todo porque hay lesiones de aspecto benigno que pueden enmascarar lesiones neoplásicas malignas. La confirmación diagnóstica definitiva es anatomopatológica (1). Por lo tanto el diagnóstico histológico es esencial para un tratamiento adecuado. Anteriormente la mayoría de los pacientes debían ser sometidos a procedimientos quirúrgicos para establecer el diagnóstico de neoplasia mediastinal, sin embargo, los avances en métodos diagnósticos menos invasivos, técnicas inmunohistoquímicas y microscopía electrónica han mejorado la habilidad para diferenciar los tipos celulares en las neoplasias mediastinales. La biopsia percutánea guiada por TAC es ahora el estándar en la evaluación inicial de la mayoría de las masas mediastinales (3).
En Venezuela, existen pocas estadísticas acerca del tema, los informes sobre las características y cambios en los patrones de los tumores mediastinales, por tanto, la finalidad de este trabajo es determinar la frecuencia y las características histopatológicas correspondientes a los tumores del mediastino evaluados en la Sección de Patología Respiratoria del Instituto Anatomopatológico “Dr. José Antonio O’Daly” de la Universidad Central de Venezuela durante el período enero de 2006 y diciembre de 2013.
MÉTODO
Este estudio fue aprobado por la Comisión de Ética de la institución en el momento de la recolección y análisis de datos. Es un estudio de tipo descriptivo, retrospectivo.
La población estuvo constituida por todas las biopsias realizadas en el Instituto Anatomopatológico “Dr. José Antonio O’Daly” de la Universidad Central de Venezuela (IAP-UCV), durante el período comprendido entre enero de 2006 y diciembre de 2014. Las muestras estarán conformadas por casos de la población con diagnóstico clínico de tumores del mediastino que cumplen con los criterios de inclusión y exclusión.
Se incluyeron todos aquellos casos con el diagnóstico definitivo de tumor de mediastino de biopsias recibidas en el IAP-UCV con el diagnóstico definitivo de tumor de mediastino se excluyeron aquellos casos cuyas láminas o bloques no se encontraran en la sección o en el archivo general del IAP-UCV.
Se efectuó una reevaluación histológica de todos los casos de tumores de mediastino recibidos en la Sección de Patología Respiratoria del IAP-UCV desde enero de 2006 hasta diciembre de 2014. Se revisaron las boletas de solicitud de los casos recibidos en IAP-UCV. Se anotaron para cada caso las variables demográficas, cuantitativas y cualitativas establecidas en la investigación. Se revisó el material histológico y se realizó la descripción histopatológica de las láminas de H-E y de las reacciones de inmunohistoquímica correspondiente a cada uno de los casos.
ANÁLISIS ESTADÍSTICO
Para el análisis de variables cualitativas se utilizó la distribución simple de frecuencias expresadas en porcentajes y las cuantitativas por media aritmética y desviación estándar, la asociación entre variables cualitativas se realizó con el método de Chi cuadrado con un nivel de significancia estadística del 5 % (P < 0,05). La significancia estadística de las diferencias entre las variables cuantitativas se determinó con la prueba de Fisher, con un nivel de confianza de 95 % (P significativa < 0,05). Se realizó análisis univariado y multivariado, cuando fue necesario, para determinar la asociación entre diferentes variables (Prueba estadística de Chi cuadrado con corrección de Yates) con un nivel de significancia de 95 % (P significativa < 0,05). Todos los datos fueron tabulados bajo Excel 2007® para Windows Vista®, y los análisis estadísticos se realizaron con los programas SPSS 10.0®
REGISTRO DE DATOS
La recolección de datos se llevó a cabo mediante el uso de un formulario, que contuvo las variables epidemiológicas e histopatológicas
RESULTADOS
De los casos recibidos en las secciones de Patología Respiratoria y Hematopatología del Instituto Anatomopatológico “Dr. José A. O´Daly”, fueron 10 374 biopsias en total, de las cuales 164 estaban referidas clínicamente como tumor de mediastino, en el período comprendido entre enero de 2006-diciembre de 2014, siendo los años 2006, 2008 y 2010 los que tenían mayor número de casos.
El análisis de los resultados se realizó a 137 casos que cumplían con los criterios de inclusión establecidos en este estudio (55 casos de la sección de Hematopatología y 82 de la sección de Patología Respiratoria). La edad de los pacientes estuvo disponible en 135 de los 137 casos. La edad media fue de 38 ± 19 años, el rango osciló entre los 2 y los 80 años. Si bien los tumores mediastinales se pueden presentar a cualquier edad, el mayor porcentaje de casos estudiados se observó en el grupo etario de 20-29 años y 40-49 años, predominando el género masculino (Figura 1).
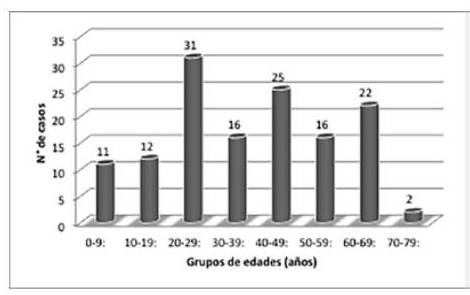
Figura 1
Número e casos
Del total de casos 80 pacientes (58,4 %) eran de sexo masculino y 57 (41,6 %) de sexo femenino.
La distribución según la localización fue de 55 casos (40,1 %) en el mediastino anterior, 6 casos (4,4 %) en el mediastino medio, 7 casos (5,1 %) en el mediastino posterior y los 69 casos restantes (50,4 %) sin especificar localización, constituyeron el mayor número de casos
En relación al tipo de tumor y la localización, se observó que en los tumores localizados en el mediastino anterior, fueron más frecuentes los de estirpe linfoide (29,1 %), seguido de los epiteliales malignos (21,8 %); de los tumores localizados en mediastino medio, el 83,3 % correspondió a tumores epiteliales malignos; de los tumores en mediastino posterior, los más frecuentes fueron de origen mesenquimático (57,1 %) (Cuadro 1)
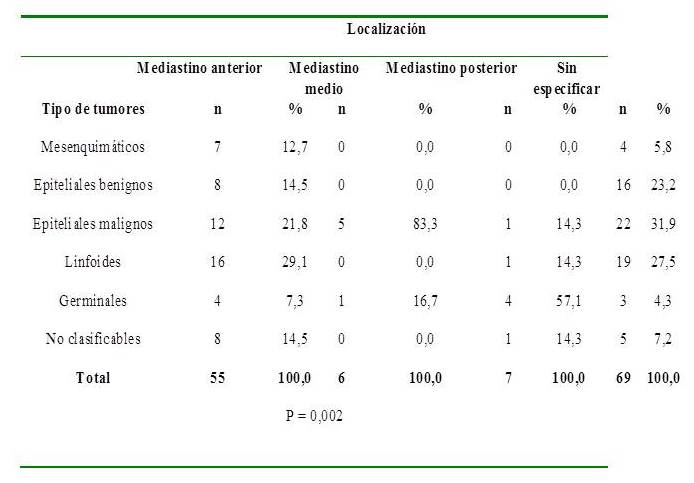
Cuadro 1.
Distribución del tipo de tumor según localización
Con respecto a las características histológicas, de los 137 casos estudiados de tumores mediastinales, 40 casos (29,2 %) correspondieron a tumores epiteliales malignos, 37 casos (26,3 %) tumores linfoides, 24 casos (17,5 %) lesiones epiteliales benignos, 13 casos (10,2 %) fueron no clasificables, 12 casos (8,8 %) tumores mesenquimáticos y 11 casos (8,0 %) tumores germinales.
LESIONES EPITELIALES BENIGNAS
Se evaluaron un total de 24 casos con lesiones epiteliales benignas, 6 correspondieron a hiperplasia tímica, 6 quistes (tímicos, broncogénico, branquial y gastro-entérico), 3 tejidos tímicos en involución, 2 adenitis reactivas, 2 histoplasmosis mediastinal, 2 hiperplasia nodular tiroidea y 1 criptococoma, 1 adenoma paratiroideo y 1 pleuritis fibrino-hemorrágica, de los cuales 13 fueron del sexo femenino y 11 del sexo masculino, con edades comprendidas entre 2 y 68 años, con una edad promedio de 34 años. Ocho de los tumores estaban localizados en el mediastino anterior y el resto (16 casos) sin especificar la localización clínicamente.
Microscópicamente las lesiones epiteliales benignas más frecuentes correspondieron a hiperplasia tímica la cual histológicamente muestra un aspecto similar al tejido tímico normal, con arquitectura lobulada, con una clara distinción entre corteza y médula en cada lóbulo. La corteza está constituida por células epiteliales dispersas y numerosos linfocitos agrupados cercanamente y la médula por el contrario exhibiendo un gran número de células epiteliales y menos linfocitos, resaltando en esta última la presencia de corpúsculos de Hassal, los cuales se caracterizan por la presencia de células epiteliales en un patrón concéntrico de queratinización (Figura 2).
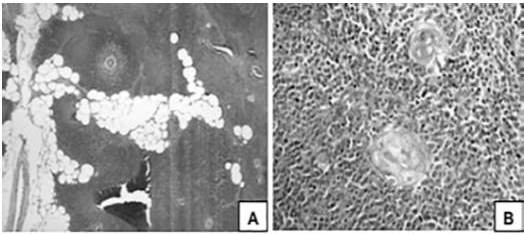
Figura 2.
Apariencia microscópica; caso de hiperplasia tímica
Hiperplasia tímica. A. Folículos linfoides aumentados en número y tamaño, confluentes con centro greminal. (H-E 100X) B. Corpúsculos de Hassal constituidos por células epiteliales en un patrón concéntrico de queratinización (H-E 400X
Con igual frecuencia se observaron cavidades quísticas, entre ellos, un quiste broncogénico, un quiste branquial, un quiste gastro-entérico y tres quistes tímicos (Figura 3).
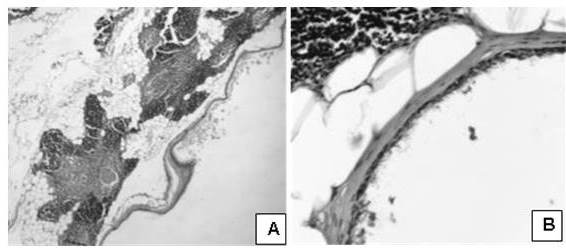
Figura 3.
Apariencia microscópica; caso de quiste tímico.
Quiste tímico. A. Cavidad quística de pared delgada rodeada por parénquima tímico. (H-E 100X) B. Pared del quiste con revestimiento de células ciliadas. (H-E 400X).
TUMORES EPITELIALES MALIGNOS
La mayoría de los casos en nuestra serie, correspondieron a tumores epiteliales en general, de los cuales 40 casos fueron diagnosticados como tumores epiteliales malignos, (21 casos correspondieron a carcinomas: 10 carcinomas neuroendocrinos, 4 carcinomas escamosos, 4 carcinomas poco diferenciados (Figura 4), 1 carcinoma papilar de tiroides (Figura 5) y un carcinoma folicular oxifílico (Figura 6), 12 se trataban de timomas, (5 timomas (AB) (Figura 7), 4 timomas tipo A (Figura 8), 2 timomas tipo B y 1 timoma combinado B2- B3), y 7 eran adenocarcinoma (Figura 9), de los cuales 14 fueron del sexo femenino y 26 del sexo masculino, con edades comprendidas entre 12 y 77 años, con una edad promedio de 52 años. En cuanto a la localización, veintidós casos venían sin especificar el compartimento mediastinal en el que se situaban, 12 de los tumores estaban localizados en el mediastino anterior, 5 en el mediastino medio y 1 se encontraba en el mediastino posterior.
Los tumores más frecuentes fueron carcinomas neuroendocrinos, predominantemente el de células pequeñas (Figura 10); microscópicamente están constituidos por células pequeñas que se disponen en patrón sólido, en nidos, trabéculas, o formando pseudorosetas, los núcleos tienden al moldeamiento, sin nucléolo, con frecuentes fenómenos de rotura e impregnación cromatínica de vasos (fenómeno de azzopardi), las figuras de mitosis son numerosas (promediando más de 60 mitosis por 2 mm2 ) y la invasión vascular y linfática es muy común. Entre estos se observó un caso de carcinoma de células pequeñas variedad de células intermedias (Figura 11).
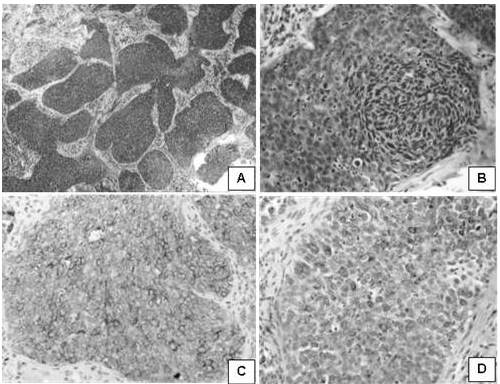
Figura 4.
Apariencia microscópica; caso de carcinoma poco diferenciado.
Carcinoma poco diferenciado. A. Masas de células tumorales separadas por septos fibrosos de tejido conectivo (H-E 100 X).B. Las células exhiben una alta relación núcleo-citoplasma, escaso citoplasma eosinófilo, núcleos vesiculosos y otros hipercromáticos con anisocariosis y mitosis atípicas (H-E 400 X). C. Inmunoreactividad para CKAE1/AE3 (IHQ 400 X). D. Inmunoreactividad para CK34BE12 (IHQ 400 X).
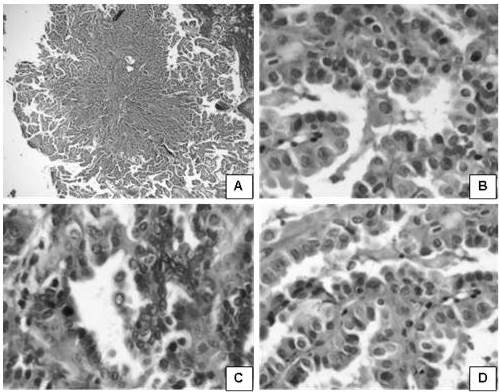
Figura 5.
Apariencia microscópica; caso de carcinoma papilar de tiroides.
Carcinoma papilar de tiroides. A. Arquitectura papilar (H-E 100X). B. Pseudo-inclusión nuclear (flecha hacia arriba. (H-E 400 X). C. Núcleo de apariencia ópticamente vacío “ojos de anita la huérfana” (H-E 400 X). D. Hendidura nuclear (H-E 400 X).
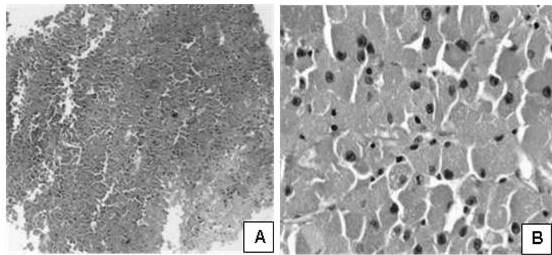
Figura 6
Apariencia microscópica; caso de carcinoma folicular oxifílico.
Carcinoma folicular oxifílico metastásico.A. Tumor hipercelular con patrón arquitectural sólido (H-E. 100 X). B. Las células tumorales son pleomórficas, muestran abundante citoplasma eosínofílico, granular (H-E. 400 X).
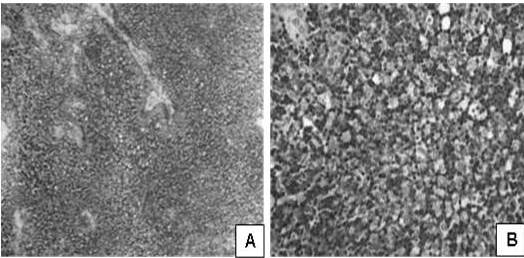
Figura 7
Apariencia microscópica; caso de timoma mixto.
Timoma mixto (AB). A. Tumor hipercelular sólido con células densamente empaquetadas (H-E. 100 X). B. componente de timoma tipo B rico en linfocitos (H-E. 400 X).
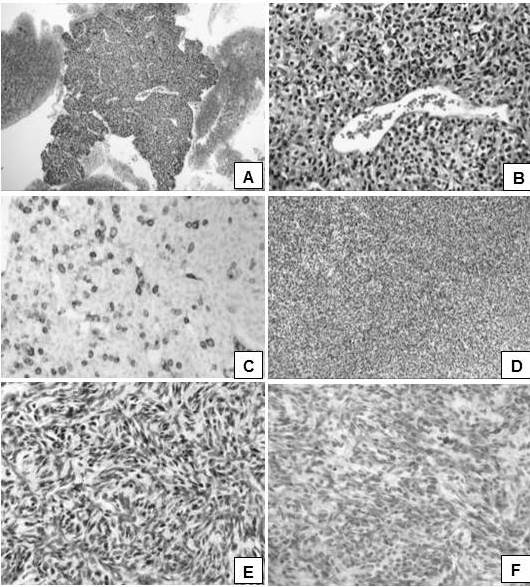
Figura 8.
Apariencia microscópica; caso de timoma A.
Timoma A. Tumor hipercelular sólido sin ningún patrón en particular (H-E. 100 X). B. Esta compuesto por células epiteliales ovales blandas (H-E 400X). C. El CD45 pone de manifiesto algunos linfocitos presentes en la lesión (H-E 400X). D y E. Timoma A compuesto por células fuso celulares (H-E 100X y 400 X respectivamente). F. Inmunoreactividad de las células tumorales para CKAE1/AE3 (IHQ 400X).
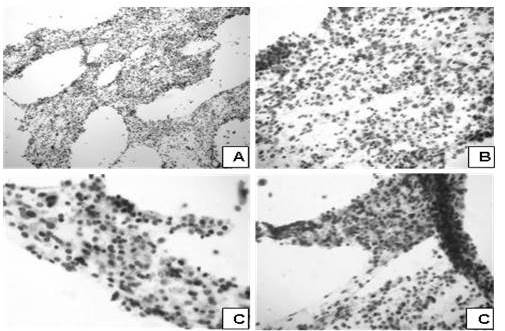
Figura 9.
Apariencia microscópica (citológica); caso de adenocarcinoma metastásico.
Adenocarcinoma metastásico. A. Extendido citológico hipercelular. (H-E. 100 X). B. Las células tumorales muestran anisonucleosis, con un tamaño nuclear mayor de al menos 2 a 3 veces el de un linfocito. (H-E. 200 X). C. Núcleos vesiculosos con nucléolos visibles rodeados de citoplasma abundante rosado y granular (H-E. 400 X). D. Trasfondo inflamatorio. (H-E. 400 X).
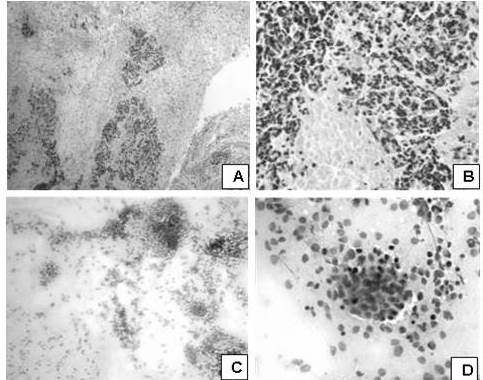
Figura 10
Carcinoma de células pequeñas con áreas de necrosis
Carcinoma de células pequeñas con áreas de necrosis. A. Neoplasia maligna de estirpe epitelial caracterizada por células dispuestas en placas con patrón infiltrativo y desmoplasia estromal. (H-E. 100 X).B. Células tumorales pequeñas con artificios de atrición y áreas de necrosis. (H-E. 400 X).C. células neoplásicas malignas de origen neuroendocrino, individuales y en placas cohesivas con escaso citoplasma (H-E. 100 X). D. Núcleos pequeños e intermedios con cromatina en sal y pimienta. (H-E. 400 X).
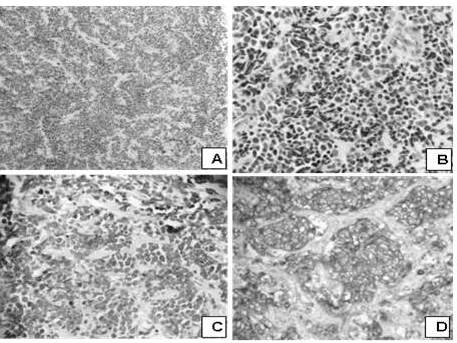
Figura 11
Apariencia microscópica; caso de carcinoma de células pequeñas variedad de células intermedias metastásico
Carcinoma de células pequeñas variedad de células intermedias metastásico. A. Patrón arquitectural en cordones, nido o trabéculas, con disposición organoide y rico estroma fibrovascular intermedio (H-E. 400 X).B. Células con marcada anisocariosis, núcleos vesiculosos con cromatina granular y nucléolos prominentes. Alto índice mitótico (H-E. 400 X).C. Inmunoreactividad de células tumorales para CKAE1/AE3 (IHQ. 100 X). D. Inmunoreactividad de células tumorales para cromogranina (H-E. 100 X).
LINFOMAS DE HODGKIN
De los 17 casos de linfoma de Hodgkin, se diagnosticaron 10 del tipo nodular esclerosante (Figura 12), 3 de tipo celularidad mixta (Figura 13), 3 sin especificar la variedad histológica y 1 linfoma de Hodgkin primario mediastinal. En lo que respecta al género, 13 resultaron de sexo femenino y 8 del sexo masculino. El rango de edad de los pacientes osciló entre los 4 y 64 años, con una edad promedio de 29 años. La localización en el mediastino anterior se observó en 8 casos, ninguno en el mediastino medio y 1 en el mediastino posterior. En los 8 casos restantes este dato fue omitido en la boleta de referencia.
Microscópicamente el tipo de linfoma de Hodgkin más frecuente fue el linfoma de Hodgkin clásico nodular esclerosante cuya histopatología se caracteriza por la presencia de amplias bandas de colágeno separando el tejido linfoide en nódulos bien definidos, citológicamente caracterizado por acúmulos de células de tipo histiocitario con características de células de Reed Stemberg de la variedad lagunar, célula característica de la esclerosis nodular, con núcleo plegado, multilobulado con retracción del citoplasma, rodeada de un espacio claro, mezclado en algunos sitios con linfocitos pequeños, eosinófilos y escasas células plasmáticas.
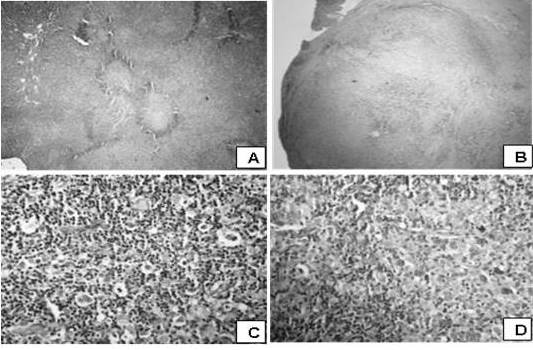
Figura 12.
Apariencia microscópica; caso de linfoma de Hodgkin nodular esclerosante grado I
Linfoma de Hodgkin nodular esclerosante grado I. A. Patrón arquitectural nodular con presencia de gruesas bandas de colágeno intercaladas. (H-E. 100 X). B. Cápsula gruesa y extensas áreas esclerosas. (H-E. 100 X). C. Células de Reed Stemberg con halo claro dispersas. (H-E. 400 X). D. Células de Hodgkin dispersas. (H-E. 400 X).
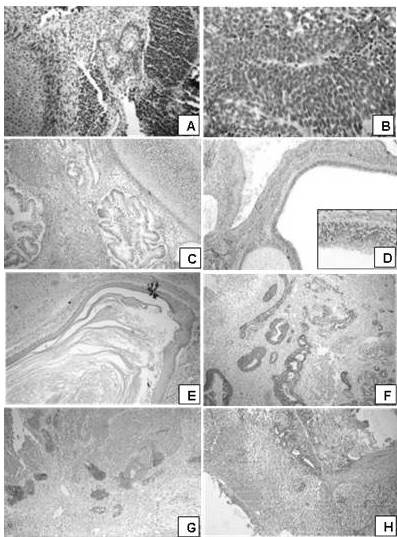
Figura 13
Apariencia microscópica; caso de linfoma de Hodgkin celularidad mixta.
Linfoma de Hodgkin celularidad mixta. A. Patrón difuso o vagamente nodular (H- E. 100 X). B. Background inflamatorio denso sin esclerosis (H-E. 200 X). C. Células de Reed Stemberg con halo claro, dispersas (H-E. 400 X). D. Célula mononuclear (de Hodgkin) con abundante citoplasma, núcleo ovoide con nucléolo evidente (H-E. 400 X).
LINFOMAS NO HODGKIN
El total de casos de linfoma no Hodgkin fue de 20 tumores en total (11 casos reportados como linfoma difuso de células grandes inmunofenotipo B (Figura 14),
seguido de 5 casos diagnosticados como linfoma linfoblástico inmunofenotipo T, 2 casos de leucemia linfoblástica aguda/linfoma linfoblástico inmunofenotipo “B”, 1 caso de leucemia linfoblástica aguda / linfoma linfoblástico inmunofenotipo “T” y 1 caso diagnosticado de forma general como linfoma no Hodgkin, debido a que los estudios de inmunohistoquímica no fueron concluyentes en vista de que el material disponible era muy escaso. Del total de casos evaluados (veinte) con linfomas no Hodgkin, 11 correspondieron al sexo femenino y 9 al sexo masculino, la edad promedio fue de 35,95 años con un rango de edad comprendido entre 2 a 60 años. Ocho de los tumores estaban localizados en el mediastino anterior y el resto (18 casos) sin especificar la localización en la boleta de consulta.
El linfoma difuso de células grandes, fue el linfoma no Hodgkin más frecuente observado en este grupo de tumores. Microscópicamente se caracteriza por una proliferación difusa de células linfoides grandes con una arquitectura parcial o totalmente borrada, las células tumorales alcanzan el tamaño de 5 linfocitos normales.
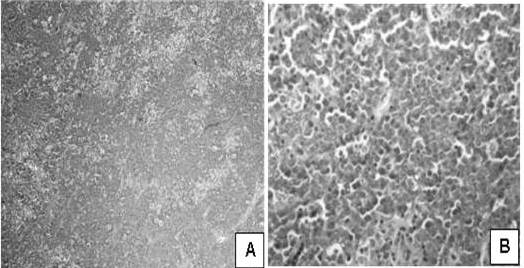
Figura 14
Apariencia microscópica; caso de difuso de células grandes B.
Linfoma difuso de células grandes B. A. Proliferación difusa de células linfoides (H- E. 100 X). B. Células linfoides grandes, con núcleos del tamaño de al menos 5 veces el de un linfocito (H-E. 400 X).
TUMORES GERMINALES
Se revisaron 11 casos en total, observándose heterogeneidad en los diversos tumores encontrados de la siguiente manera: 3 teratocarcinoma, 2 seminomas metastásicos, 1 teratoma trifásico: teratoma solido inmaduro de alto grado (Figura 15), 1 germinoma, 1 teratoma quístico maduro, 1 tumor germinal mixto con componente seminomatoso y de coriocarcinoma, 1 tumor mixto germinal con componentes de teratoma maduro y carcinoma embrionario, y 1 disgerminoma. En cuanto al género, la totalidad de los casos (once) eran del sexo masculino. El dato de la edad estuvo disponible en 10 de los 11 casos, con un rango entre los 15 y 38 años, y una edad promedio de 21,63 años. La mayoría de los casos estaban localizados en el mediastino anterior y los 4 casos restantes sin especificar la ubicación.
El tumor más frecuente en este grupo fue el teratocarcinoma, microscópicamente en su composición estructural presenta elementos de teratoma y carcinoma embrionario. El componente de teratoma muestra áreas quísticas cuyas paredes están compuestas de epitelio escamoso estratificado con glándulas sebáceas subyacentes, tallos de pelos y otras estructuras de los anejos cutáneos, además de áreas de cartílago hialino. Por su parte, el componente de carcinoma embrionario cuya celularidad es característica, con elementos de aspecto epitelioide, citoplasma abundante basófilo y núcleo vesiculoso de cromatina pulverulenta con atipia marcada, mostrando superposición nuclear, áreas de necrosis tumoral y mitosis frecuentes.
Uno de los tumores mostró tejido mesenquimático inmaduro, cartílago inmaduro (50 %) carcinoma embrionario (20 %) tumor de seno endodérmico (30 %) y presencia de neuro-epitelio.
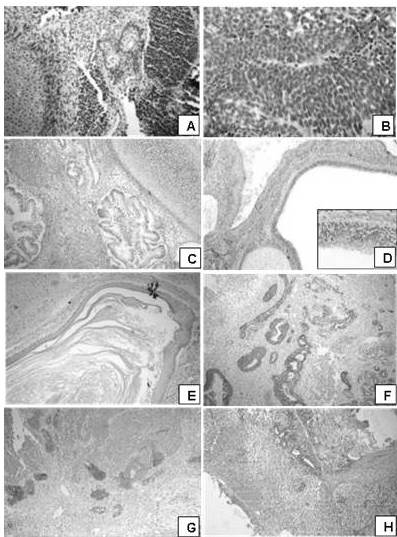
Figura 15.
Apariencia microscópica; caso de teratoma sólido inmaduro de alto grado. A.
Teratoma sólido inmaduro de alto grado. A. Mesénquima primitivo mezclado con cartílago inmaduro adyacente a área sólida conformada por células redondas hipercromáticas. (H-E 100X). B. Neuroepitelio primitivo formando rosetas (H-E 400X).C. Áreas de teratoma maduro de aspecto quístico y cartílago hialino (H-E 100X-400X). D. El revestimiento de estos quistes es de tipo respiratorio (H-E 100X-400X). E. Áreas de teratoma maduro de aspecto quístico revestidos por epitelio escamoso con presencia de queratina laminar en la luz (H-E 100X). F. Inmunoreactividad intensa de las células epiteliales para CKAE1/AE3 (IHQ 100X). G. Inmunoreactividad intensa del neuroepitelio para alfa-fetoproteína (PLAP) (IHQ 400X). H. Inmunoreactividad aislada de las células tumorales para PLAP (IHQ 100X).
TUMORES MESENQUIMÁTICOS
Se evaluados 12 casos correspondientes a tumores mesenquimáticos: 2 tumor maligno de la vaina del nervio periférico (Figura 16), 2 tumor fibroso solitario, 1 neurofibroma (Figura 17), 1 neuroblastoma (Figura 18) ,1 rabdomiosarcoma embrionario, 1 lipoma (Figura 19), 1 liposarcoma pleomórfico, 1 paraganglioma con atipias (Figura 20) y 1 sarcoma sinovial y 1 tumor cartilaginoso con cambios mixoides sugestivo de condrosarcoma de bajo grado. La distribución del género en este grupo de casos fue similar para ambos sexos, 6 del sexo femenino y 6 del sexo masculino, con edades comprendidas entre 6 y 71 años, y una edad promedio de 38,41 años. La localización más frecuente fue en el mediastino posterior con 5 casos (uno de ellos situado tanto en mediastino posterior como mediastino medio), seguido del mediastino anterior con 4 casos y en los 3 casos restantes éste dato no fue referido.
Los tumores mesenquimáticos más frecuentes fueron el tumor maligno de la vaina del nervio periférico y el tumor fibroso solitario. Histológicamente el tumor maligno de la vaina del nervio periférico mostró neoplasia maligna mesenquimal, compuesta por células fusiformes con núcleos aumentados de tamaño irregulares, con cromatina vesiculosa, nucléolos prominentes y ocasionales figuras mitóticas atípicas (7 en 10 campos de alto aumento), rodeadas por citoplasma eosinófilo tenue; éstas células se disponían en forma fasicular formando empalizadas sobre un estroma colagenizado, en el que se reconocían además, espacios pseudovasculares. Por su parte el tumor fibroso solitario se caracteriza por ser una neoplasia fusocelular, que alterna áreas de mayor densidad celular y áreas de escasa densidad celular con abundantes vasos sanguíneos.
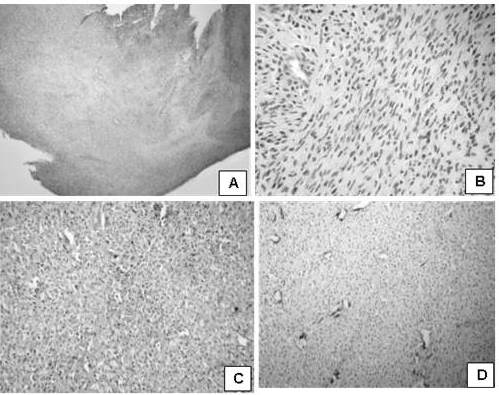
Figura 16.
Apariencia microscópica; caso de tumor maligno de la vaina del nervio periférico
Tumor maligno de la vaina del nervio periférico. A. Infiltración difusa del nervio por neoplasia con marcada hipercelularidad (H-E. 100 X). B. Células con núcleos en forma de huso con extremos cónicos, pleomorfismo nuclear y la actividad mitótica (H-E. 400 X). C. Inmunomarcaje citoplasmático y nuclear débil en las células tumorales (IHQ 200 X). D. Inmunomarcaje normal con Actina músculo liso (AML) en las paredes de los vasos sanguíneos. (IHQ 100 X).
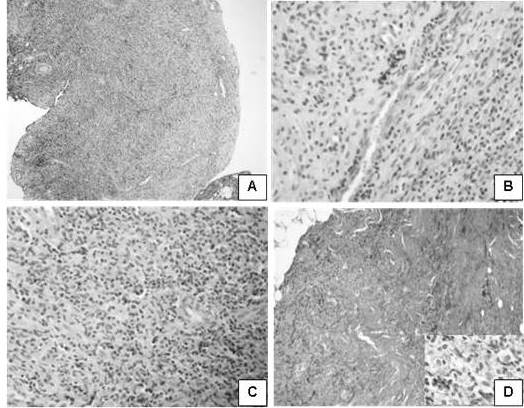
Figura 17.
Apariencia microscópica, neurofibroma
Neurofibroma. A. Tumor no encapsulado con patrón del infiltración difusa. (H- E. 100 X). B. Células con núcleos fusiformes y serpenteantes. (H-E. 100 X). Presencia de ocasionales mastocitos. (H-E. 400 X). C. La lesión es sólida e hipercelular con moderados vasos sanguíneos. En áreas de la lesión las células son menos alargadas y monomórficas (H & E. 400 X). D. Con la coloración de tricrómico de Gomori se pone en manifiesto la abundante matriz colágena en la que están inmersas las células (TMG 100X-400X)
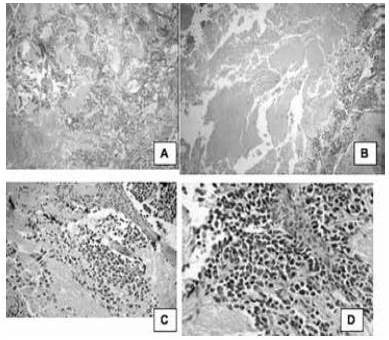
Figura 18
Apariencia microscópica; caso de neuroblastoma con extensas áreas de necrosis.
Neuroblastoma con extensas áreas de necrosis. A. Infiltración difusa por células pequeñas redondas azules. (H-E. 100 X). B. Extensas áreas de necrosis. (H-E. 100 X). C. Fondo fibrilar. (H-E. 400 X). D. Células pequeñas a medianas, con la cromatina en sal y pimienta, forma alargada y pequeña cantidad indiscernible de citoplasma (H-E. 400 X).
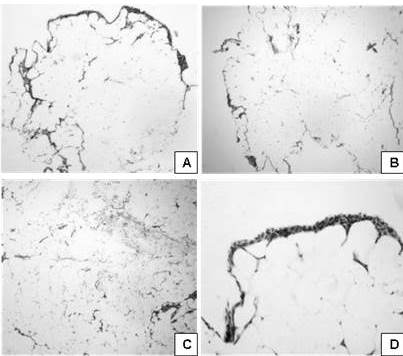
Figura 19.
Apariencia microscópica; caso de lipoma.
Lipoma. A. Lesión benigna mesenquimática de estirpe adiposa. (H-E. 100 X). B. Condensación conjuntiva periférica a modo de pseudo-cápsula. (H-E. 100 X). C. Arreglo en patrón lobulado, con septos conjuntivo-vasculares delicados. (H-E. 100 X). D. Células grasas adultas, de citoplasma ópticamente vacío y núcleos confinados a la periferia, células mesoteliales reactivas en la superficie. (H-E. 400 X)
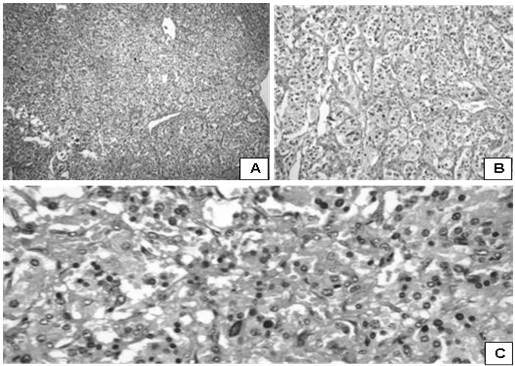
Figura 20.
Apariencia microscópica; caso de paraganglioma con atipias.
Paraganglioma con atipias. A. Células tumorales dispuestas en patrón trabecular y en nidos, dentro de una red vascular prominente. (H-E. 100 X). B. Patrón característico de crecimiento organoide, (llamado patrón Zellballen), en el que las células tumorales individuales son poligonales y están dispuestas en diversos nidos celulares. (H-E. 200 X). C. Células con atipias marcadas. (H-E. 400 X).
TUMORES NO CLASIFICABLES
Por último, aquellos tumores cuyo diagnóstico no fue concluyente incluso realizando el estudio inmunohistoquímico (13 casos), ocupan esta categoría, los más frecuentes fueron tumores malignos de células redondas con 7 casos, seguido de 3 casos diagnosticados como tumor maligno poco diferenciado, en 2 casos el material era inadecuado para diagnóstico y 1 caso en el cual no se observaron atipias. El género predominante fuel el sexo masculino con un total de 10 casos y los 3 casos restantes correspondieron al sexo femenino, con un rango de edad comprendido entre 7 y 64 años. La mayoría de los tumores estaban localizados en el mediastino anterior, 1 se encontraba en el mediastino posterior y casos no tenían este dato reportado.
Microscópicamente son tumores de células redondas que no mostraron una clara diferenciación, a cuatro de ellos se les realizó el estudio de inmunohistoquímica sin obtener un diagnóstico concluyente debido a diversos factores como muestra insuficiente, extensa necrosis o artificios de fijación.
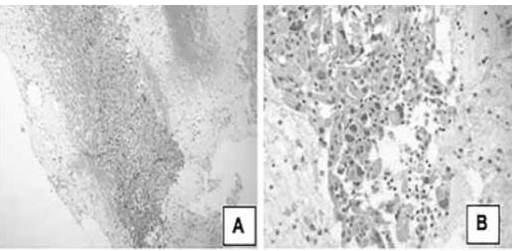
Figura 21
Apariencia microscópica; caso de tumor maligno poco diferenciado con áreas de necrosis.
Tumor maligno poco diferenciado con áreas de necrosis. A. Infiltración difusa por células tumorales con áreas de necrosis. (H-E. 100 X). B Las células exhiben abundante citoplasma, multi-nucleación, anisonucleosis y se acompaña de infiltrado inflamatorio mixto. (H-E. 400 X).
ESTUDIO DE INMUNOHISTOQUÍMICA
Mediante la técnica del polímero dextrano conjugado al anticuerpo secundario y marcado con peroxidasa, utilizando controles positivos adecuados y métodos de recuperación antigénica, se investigaron distintos anticuerpos en 65 de los 137 casos para investigar y/o confirmar la histogénesis de cada tumor. Cabe destacar que no existe ningún estudio inmunohistoquímico que sea 100 % específico, por lo que se requiere realizar varias inmuno-reacciones y el resultado debe ser interpretado por el patólogo con mucha precaución, tomando en cuenta el cuadro clínico y el estudio morfológico para establecer un acertado diagnóstico.
Se realizó el estudio inmunohistoquímico a 1 de 24 lesiones epiteliales benignas. Se trataba de un tumor constituido por dos tipos de células, unas con citoplasma claro y otras con citoplasma finamente granular dispuestas formando nidos, separados por finos septos de tejido fibro-conectivo vascularizado (patrón organoide) y túbulos con un material eosínofílico denso en la luz. No se observaron mitosis y presentaba extensas áreas de necrosis. En este caso la CKAE1/AE3 mostró fuerte positividad en las células neoplásicas al igual que la cromogranina y la enolasa neuronal específica, confirmando así el diagnóstico de adenoma paratiroideo. Se realizaron otros marcadores como sinaptofisina, tiroglobulina, parathormona los cuales fueron negativos.
De los 40 tumores epiteliales malignos, se estudió el inmunofenotipo de 21 casos. Los timomas en general resultaron positivos a la CKAE1/AE3, adicionalmente, los timomas mixtos mostraron un inmunomarcaje positivo a anticuerpos tales como CD5, CD99, CD3 y CD45RO que pone en evidencia el componente de linfocitos T maduros e inmaduros. Por otra parte, los carcinomas neuroendocrinos mostraron inmunomarcaje al menos a uno de los siguientes anticuerpos: cromogranina, enolasa neuronal específica y sinaptofisina, además de la CKAE1/AE3, CK7 y CEA. Los carcinomas epidermoide resultaron fuertemente positivos a la CK34BE12, los adenocarcinomas mostraban positividad de igual forma a la CKAE1/AE3, CK7 y por último, los carcinomas poco diferenciados fueron positivos a anticuerpos como CK34BE12, CK7 y en uno de ellos a la enolasa neuronal específica.
En el grupo de los linfomas, se realizó el estudio de inmunohistoquímica a 29 casos en total, 13/17 linfomas de Hodgkin y 16/20 linfomas no Hodgkin. Para los linfomas de Hodgkin el inmunomarcaje más frecuente era CD15 y CD30 positivo, CD20 y CD45Ro negativo o normal. Por su parte, los linfomas no Hodgkin mostraban positividad a algunos anticuerpos como el CD20, CD79A, Ki67, y particularmente los linfomas difusos de células grandes B exhibieron adicionalmente positividad al CD45 (ALC: antígeno leucocitario común) y CD45RO. La leucemia linfocítica/linfoma linfoblástico mostraron inmunomarcaje positivo al CD3, CD79a y CD34.
En cuanto a los tumores germinales, se evaluaron 5 de 11 tumores distintos con inmunohistoquímica. Las células tumorales en un caso de germinoma mostraron positividad intensa citoplasmática para fosfatasa alcalina placentaria (PLAP), también se observó focalmente CKAE1/AE3 positividad moderada citoplasmática, gonadotropina coriónica humana (HCG) positividad citoplasmática difusa de moderada intensidad y enolasa neuronal específica con positividad difusa débil en las células neoplásicas. Otro de los tumores evaluados fue un teratoma trifásico (teratoma sólido inmaduro de alto grado) en el cual se observó inmunomarcaje positivo para CKAE1/AE3 en células epiteliales, también positividad en el neuro-epitelio a la proteína ácido glial fibrilar y positividad aislada en células epiteliales para alfafetoproteína. Otros marcadores como: PLAP, CD30 y HCG fueron negativos. Un caso de seminoma metastásico mostró positividad para PLAP, siendo negativos otros marcadores como alfafetoproteína, lactógeno placentario, cromogranina, HCG y CD45 (ALC) los cuales fueron negativos. También fue estudiado un tumor germinal mixto con componente seminomatoso y componente de coriocarcinoma, en este caso se realizó HCG mostrando un inmunomarcaje positivo en el 60 % de las células tumorales, PLAP que mostró un inmunomarcaje positivo en el 40 % de las células tumorales y adicionalmente ALC y alfafetoproteína que resultaron negativos. Por último, tenemos un caso de disgerminoma al cual se le realizó CK AE1/AE3 resultando focalmente positivo y CD117 también positivo. Otros de los marcadores realizados fueron CD20, CD3, CD30 y HCG con resultados negativos y PLAP no evaluable.
El inmunofenotipo en los tumores mesenquimáticos se evaluó en 6 de 12 tumores en total. Dos de ellos diagnosticados como tumor maligno de la vaina del nervio periférico con inmunomarcaje positivo para S-100 y PGP 3,5. Por supuesto anticuerpos para CKAE1/AE3, CD20, CD79a, EMA y CD3 fueron negativos. También se evaluaron dos casos diagnosticados como tumor fibroso solitario en los cuales los principales marcadores inmunohistoquímicos realizados fueron CD34, CD79a, CD99 y vimentina positivo, además se realizó S-100 y CKAE1/AE3 resultando negativo. También se investigó el inmunofenotipo de un caso diagnosticado como liposarcoma pleomórfico en el cual los anticuerpos evaluados fueron: CD79a, S-100 Y PGP 3,5 positivo, siendo negativos la actina músculo liso (AML) y CKAE1/AE3. Por último, se realizó el estudio inmunohistoquímico a un caso diagnosticado como sarcoma sinovial, siendo CKAE1/AE3, además se realizaron otros marcadores tales como CD20, CD34, S-100, cromogranina, enolasa neuronal específica, sinaptofisina, PGP 3,5, negativos y CD45RO con marcaje normal.
Los tumores que no pudieron ser clasificados en alguno de los grupos de tumores previamente descritos se les realizaron los siguientes marcadores CKAE1/AE3, CK7, CK20, CK34BE12, CD5, CD30, CD34, ALC, CD45RO, CD68, vimentina, AML, cromogranina, sinaptofisina, PGP 3,5, TTF1, obteniendo resultados negativos. Sólo se observó positividad (en distintos casos) al CD20 y S-100, por lo cual no se llegó a una conclusión diagnóstica.
En la relación de los tumores de mediastino con la edad, el género y la localización se observó que las lesiones epiteliales benignas son más frecuentes en la cuarta década de la vida, predominando en el sexo femenino y se localizan con más frecuencia en el mediastino anterior. Por su parte, los tumores epiteliales malignos fueron más frecuentes en la sexta década de la vida, en pacientes masculinos e igualmente se localizan en el mediastino anterior. Los linfomas de Hodgkin fueron más frecuentes en la primera y segunda década por igual, el sexo más frecuente fue el femenino y se localizan también en el mediastino anterior. Los linfomas no Hodgkin también fueron más frecuentes en la segunda década de la vida, el sexo igualmente fue el femenino y se localizan en el mediastino anterior. Los tumores germinales se observaron con más frecuencia en la segunda década, en pacientes masculinos y la localización más frecuente en el mediastino posterior. Los tumores mesenquimales fueron más frecuentes en la tercera década de la vida, en ambos sexos por igual y la localización más frecuente fue al igual que la mayoría en el mediastino anterior. Por último los tumores no clasificables también se observaron con mayor frecuencia en la segunda década de la vida, en el sexo masculino y en el mediastino anterior (Cuadro 2).
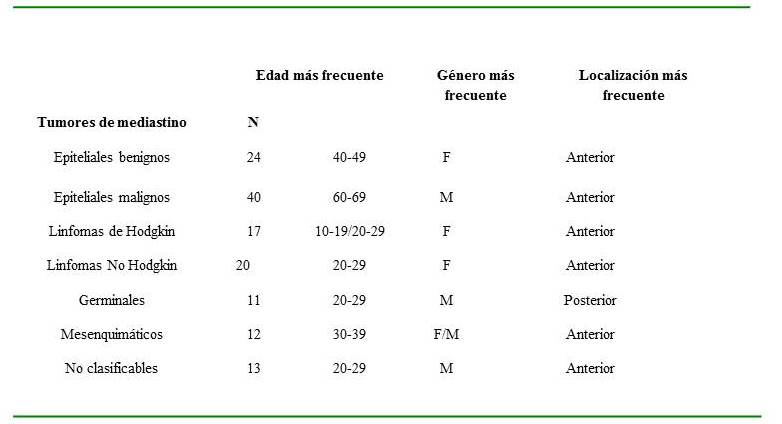
Cuadro 2
Relación entre los tumores de mediastino y la edad, el género y la localización.
DISCUSIÓN
Los tumores de mediastino son relativamente poco comunes y a pesar de esto constituyen entidades de gran importancia debido a que se encuentran adyacentes a estructuras vitales. En Venezuela hay muy pocos estudios actuales acerca de este tema, por lo que resulta interesante conocer la frecuencia con que se presentaron estos casos en un centro de referencia nacional, la naturaleza histológica de cada tumor, algunos datos epidemiológicos como la edad y el sexo de la población en estudio y la localización más frecuente.
Se revisaron biopsias correspondientes al período enero de 2006 y diciembre de 2014, de las secciones de Patología Respiratoria y Hematopatología del Instituto Anatomopatológico “Dr. José A. O´Daly”. De un total de 10 374 biopsias evaluadas en dicho período, se seleccionaron 137 casos (1,3 %), referidos clínicamente como tumor de mediastino.
La edad media de los pacientes fue de 38 ± 19 años y el rango de edad osciló entre los 2 y los 80 años, coincidiendo con el grupo etario del estudio de Asgary y col.(5)quienes evaluaron 109 pacientes en el período comprendido entre marzo de 2006 y marzo de 2012, en el cual reportaron una edad media de 35,84 ± 1,71años (rango de 7 a 79 años), estos resultados son similares con lo reportado por Rodríguez y col.(7)quienes en su revisión la edad promedio fue de 41 años, siendo el rango etario de 19 a 82 años. Por su parte, Thomas y col. (8) estudiaron una población de 38 pacientes con masas mediastínicas en un período de 5 años en la cual el 76,3 % de los pacientes estaban en la 3a y 4a décadas de la vida y la edad promedio fue de 33,7 ± 10 años(6,7, 8).
En nuestra serie, 58,4 % de los pacientes eran de sexo masculino y 41,6 % correspondieron al sexo femenino, de forma similar, Asgary y col.(3,5,6) reportaron en su trabajo que el sexo masculino fue el predominante con un 56,4 % (57 pacientes) seguido del sexo femenino con un 43,6 % (44 pacientes), lo que se asemeja a lo reportado en la literatura, según Rodríguez y col. (7) quienes reportan una serie de 27 pacientes con tumores mediastinales y observan el mismo hallazgo, el sexo masculino con un 70 % (19 pacientes) fue el género más frecuente aunque con datos superiores y el 30 % restante del sexo femenino (8 casos) (6, 7).
En cuanto a la localización, en este estudio el 40,1 % (55 casos) estaban ubicados en el mediastino anterior, 6 casos (4,4 %) en el mediastino medio, 7 casos (5,1 %) en el mediastino posterior, desafortunadamente los 69 casos restantes (50,4 %) venían sin especificar localización, similar a el reciente trabajo de Asgari y col.(5) en el cual el 78,2 % (79 casos) de los tumores mediastinales se encontraban en el mediastino anterior y la ubicación más baja se encontraban en el mediastino medio con un 5 % resultando estadísticamente significativo en ambos estudios con valores de (P<0,001) y (P = 0,002). Además, se asemeja al estudio de Hesami (7), en el cual la localización más común de tumores del mediastino en orden de frecuencia decreciente fue el mediastino anterior (66,9 %), mediastino medio (21,4 %) y el mediastino posterior. Con respecto al análisis de Rodríguez y col. (3) la ubicación topográfica más frecuente de los tumores de mediastino corresponde en un 63 % (17 casos) al mediastino anterior, distribuyéndose equitativamente los demás tumores en el mediastino medio y posterior con 18,5 % cada uno. En el estudio realizado por Thomas y col. (8), observaron de igual manera que la localización más frecuente eran los tumores del mediastino anterosuperior en 29 pacientes (76,3 %), mientras que el 18,4 % y el 2,6 % se encontraban en el mediastino posterior y mediastino medio respectivamente.(6, 7,9).
Con respecto al tipo de tumor más frecuente en éste estudio fue el linfoma no Hodgkin difuso de células grandes inmunofenotipo B, con un 7,2 %, a la par del linfoma de Hodgkin variedad nodular esclerosante con igual frecuencia (7,2 %), Asgary y col. (5) reportan que en su estudio el tumor mediastinal más frecuente fué el linfoma no Hodgkin (30,7 %), seguido de timomas ( 13,8 %) y el linfoma de Hodgkin (12,9 %), difiriendo un poco con el estudio de Hesami y col. (7), quienes describen en su estudio que los tumores más comunes del mediastino fueron: timoma (25,8 %) linfoma (15,7 %), tuberculosis (15,7 %), quiste mesenquimático, carcinoma de células escamosas de pulmón ( 9 %), tumor neurogénico (7,6 %), tumores de células germinales (5,6 %) y otros tumores (11,2 %). Rodríguez y col.(3) en contraste, informan que el tipo histológico más frecuente fueron el tumor de células germinales y los linfomas (tomados en conjunto) con un 22 %, seguidos en tercer lugar los timomas. Sin embargo, Thomas y col. (8)en su revisión encontraron que las masas tiroideas aportaron el 44,7 % de los tumores, mientras que los linfomas y los tumores neurogénicos fueron 26,3 % y 18,4 % (6-9).
ESTUDIO DE INMUNOHISTOQUÍMICA
Las citoqueratinas de bajo peso molecular, incluyendo CK8, CK18 y CK19, reconocidos por los anticuerpos CAM 5.2 o 35BH11, y un cóctel de queratinas (pankeratinas), reconocida por el anticuerpo AE1/AE3, son marcadores de cribado útiles para el reconocimiento de la diferenciación epitelial. Debido a que los carcinomas pobremente diferenciados son conocidos por ser heterogéneos en su expresión de antígenos reconocidos por los marcadores epiteliales, cuando se obtiene un resultado negativo con un solo anticuerpo y el diagnóstico de carcinoma todavía se sospecha, es prudente utilizar anticuerpos adicionales en un panel de respaldo. En un estudio de 98 carcinomas pobremente diferenciados se probó la efectividad de CAM 5.2 y antígeno de membrana epitelial (EMA) cada una detecto la diferenciación epitelial del 71 % de los casos, mientras que combinadas CAM 5.2 y EMA demostró la naturaleza epitelial del 99 % (10.11).
Weissferdt y col. (9,12) realizaron un estudio inmunohistoquímico en el diagnóstico de las neoplasias del timo, comprobando la fiel naturaleza epitelial de estas lesiones, las células neoplásicas de timoma muestran la tinción positiva para una gama de queratinas, por ejemplo pancitokeratina (AE1 / AE3), citoqueratina de bajo peso molecular (CAM5.2), citoqueratinas de alto peso molecular (34BE12), y CK5 / 6, tal y como lo observamos en nuestra investigación. En los últimos años una serie de nuevos marcadores han sido exitosamente aplicados a los timomas incluyendo Pax8, p63, Foxn1, y CD205. Pax8 y p63 mostrando reactividad nuclear difusa y fuerte en hasta el 100 % de los casos, mientras que la tinción positiva para Foxn1 y CD205 se encontró en el 89 % de los timomas de células fusiformes (OMS tipo A) y hasta el 100 % de los timomas OMS de tipo AB y B1. Al contrario del carcinoma tímico, la expresión de c-kit y CD5 sólo se observa en una minoría de los timomas El componente linfocitario de los timomas muestra un fenotipo de células T inmaduras y estos timocitos pueden ser demostrados con antígeno común de linfocitos, CD3, CD1a, desoxinucleotidiltransferasa terminal (TdT) y CD99. Sin embargo, hay que señalar que un pequeño número de linfocitos B CD20-positivo se puede encontrar en los timomas, ya sea como células individuales o dispersas u organizadas en centros germinales (11). Mediante inmunohistoquímica, los tumores carcinoides presentan un patrón de tinción positiva para citoqueratina AE/AE3 y CAM 5.2 y para marcadores neuroendocrinos tales como CD56 (NCAM), sinaptofisina, cromogranina y enolasa neuronal específica (NSE), similar a los resultados observados en nuestro estudio. El NCAM puede ser negativo en los tumores carcinoides típicos y asume intensidad de la tinción típicamente en tumores de mayor grado. El factor de transcripción tiroideo 1 (TTF1) es típicamente negativo (12).
El diagnóstico del linfoma de Hodgkin clásico se basa en la identificación morfológica de la célula de R-S (o sus variantes), el entorno inflamatorio celular, y en el inmunofenotipo de estas células. Por inmunohistoquímica la definición diagnóstica del linfoma de Hodgkin clásico es que las células de R-S sean positivas al CD30, al CD15 y negativas para el CD45 y el EMA, y en ocasiones positivas a marcadores B. Los linfocitos que rodean a estas células son linfocitos T (la mayoría son CD4). Lo más característico en el diagnóstico inmunohistoquímico del linfoma de Hodgkin clásico es la expresión del CD30 y CD15. Estos dos anticuerpos no son específicos de la célula de R-S; sin embargo, su expresión es positiva en un alto porcentaje de casos (98 % el CD30 y 84 % el CD15). Von Wasie-lewski, y col. (12) informaron que el inmunofenotipo puede tener correlación pronostica pues los pacientes con CD15 negativo tienen un curso clínico malo, comparado con los casos con expresión de CD15. Shamsuddin y col. (13) informaron que el total de casos de linfoma de Hodgkin en su estudio eran inmunorreactivos al CD30. En nuestro estudio 11 de 13 casos en total fueron inmunorreactivas al CD30 y 9 casos fueron inmunorreactivos al CD15. En nuestro estudio 9 de 12 casos de linfoma de Hodgkin fueron positivos para CD15 y 11 de 12 casos fueron también fueron positivos para CD30 (13).
Por otra parte, en lo que respecta al estudio inmunohistoquímico de los linfomas no Hodgkin, Bustamante y col. (11) reportaron que los dos subtipos histológicos de linfoma no Hodgkin primarios del mediastino más frecuentes son el linfoma B difuso de células grandes y el linfoma T linfoblástico. En el primer caso, las células neoplásicas expresan marcadores de inmunohistoquímica específicos para el linaje de células B, tales como CD19, CD20, CD22 y CD79a, también se ha detectado hasta en un 69 %-80 % reactividad para CD30, 20 %-25 % para CD10 y 45 % a 100 % para BCL6, con reactividad variable en los diferentes estudios para CD15 y MUM1. Afirman que los marcadores CD15 y CD21
También, Layla y col. (14) utilizaron un panel disponible comercialmente de anticuerpos en un estudio de 50 casos de LLA y concluyeron que la mayoría de marcadores sensibles y específicos de linaje eran MPO, TDT, CD10, CD79a (por linaje B) y CD3 (para ALL T).
Gao y col. (15) describen los hallazgos inmunohistoquímicos en su informe acerca de 48 casos de tumores de células germinales malignos extra-gonadales. En su estudio, el inmunomarcaje de PLAP (citoplasmático y de membrana) se detectó en 25 de 31 (80,6 %) germinomas / seminomas, y 3 de 3 (100 %) en el componente de germinoma / seminoma en tumores de células germinales mixtos malignos. El CD117 fue detectado en 29 de 31 (93,5 %) germinomas / seminomas, y 3 de 3 (100 %) en el componente de germinomas / seminomas en tumores de células germinales malignos mixtos. Además, el OCT3 / 4 se expresó en todos germinomas / seminomas (31/31), carcinoma embrionario (1/1), en los componentes de germinoma / seminoma (4/4) y carcinoma embrionario (1/1) de los tumores de células germinales mixtos, mientras que el tumor del saco vitelino, teratoma y coriocarcinoma fueron consistentemente negativos. Además, 4 pacientes con tumor del saco vitelino y un paciente con coriocarcinoma tenía una expresión positiva de PLAP, CD117 y OCT3 / 4.
La ß-HCG, CK AE1/AE3 y EMA se observaron en coriocarcinoma (1/1), y la alfafetoproteína, CK AE1/AE3, EMA y PLAP (focal) fueron vistos en tumor del saco vitelino (4/4). El inmunomarcaje de CD3, CK AE1/AE 3 y EMA fue positivo en carcinoma embrionario y en el componente de carcinoma embrionario de tumores de células germinales mixtos.
En nuestro estudio, se observó 3 casos de germinoma/seminoma con inmunomarcaje positivo para PLAP, positividad focal para CKAE1/AE3 en todos los casos, también positividad para vimentina, enolasa neuronal específica (inmunomarcaje débil y difuso) y positividad para HCG (difusa citoplasmática), demostrando así la utilidad que tiene el PLAP principalmente en el diagnóstico de este tipo de tumores, el resto de los anticuerpos utilizados (lactógeno placentario, alfafetoproteína, cromogranina, antígeno leucocitario común y HCG) fueron negativos.
En el caso de teratoma trifásico (teratoma sólido inmaduro de alto grado) se observó positividad en el inmunomarcaje para CKAE1/AE3, PAGF y alfafetoproteína. La HCG, PLAP y CD30 fueron negativos, similar a lo reportado en la literatura.
El único tumor germinal mixto con componente seminomatoso y de coriocarcinoma en este estudio fue positivo para PLAP en el 40 % de las células tumorales y positivas para HCG en el 60 % de las células tumorales. El ALC y alfafetoproteína resultaron negativos, similares a los resultados reportados por Gao y col (15).
Respecto a los marcadores inmunohistoquímicos de los tumores mesenquimáticos, Ortega y col. (16) utilizaron anticuerpos tales como MDM2 y S-100 en ocho casos de liposarcoma. El MDM2 mostró positividad nuclear dispersa en 5 / 5 casos de liposarcoma bien diferenciado y fue negativa en los tres casos de liposarcoma mixoide. Los tres casos de liposarcomas de bajo grado mostraron positividad nuclear dispersa para MDM2 y tinción negativa para la proteína S-100. Sólo uno de los casos de liposarcoma bien diferenciado mostró positividad focal de las células tumorales para la proteína S-100. Los tres casos de liposarcoma mixoide mostraron dispersos positividad para la proteína S-100 en las células tumorales. Ambos casos de lipoleiomiosarcoma mostraron una fuerte positividad del componente de músculo liso con actina músculo liso (AML) y desmina (16). En nuestro estudio tuvimos un solo caso de liposarcoma pleomórfico el cual tuvo un inmunomarcaje positivo para PGP 9,5 y S100. Otros marcadores como CKAE1/AE3, AML y CD34 fueron negativos.
Suster y col.(17) informaron acerca de su estudio de 4 rabdomiosarcoma en el mediastino anterior, que los estudios inmunohistoquímicos mostraron una tinción positiva de las células tumorales con anticuerpos como la actina, desmina, vimentina y con positividad focal para la mioglobina en tres casos, además de tinción positiva focal con la proteína S-100 en un caso. El resto de anticuerpos como queratinas de bajo y alto peso molecular, antígeno carcinoembrionario, alfafetoproteína, gonadotropina coriónica humana, la fosfatasa alcalina placentaria, antígeno leucocitario común, y enolasa neuronal específica fueron negativos (17).
En los casos estudiados en la presente revisión, se realizó el estudio inmunohistoquímico a dos casos diagnosticados como tumor fibroso solitario, observándose franca positividad a los marcadores CD34 y vimentina, Bcl2 focal en uno de los casos, AML negativa en ambos casos, similar a lo reportado por Gutiérrez y col.(18) quienes reportaron en su estudio 16 casos de tumor fibroso solitario observando vimentina positiva en todos los casos, el CD34 fue positivo en 15/16 casos y en uno focal en el citoplasma y la membrana celular; la proteína S100 fue positiva en nueve casos y focal en solo dos; el Bcl-2 resultó positivo en el citoplasma en 11 casos, la antiactina músculo liso fue negativa en todos los casos, destacando que el tumor fibroso solitario no tiene ningún marcador específico, por lo que el diagnóstico se basa en cortes de rutina, identificando los múltiples patrones histológicos donde todas las células son positivas a vimentina y CD34+, que también marcan otras lesiones benignas y malignas como dermatofibroma, dermatofibrosarcoma y hemangiopericitoma. El Bcl-2, gen anti-apoptótico que marca muchas lesiones, y el CD99 resultan positivos en 80 % de estos casos cuando se utilizan juntos, y son de gran ayuda aunados a la negatividad o positividad focal de proteína S100 como marcador neurogénico y a la antiactina músculo-específica (AAME), que permite descartar lesiones de origen neurogénico y muscular. En el tumor fibroso solitario siempre son negativas las tinciones para citoqueratinas de alto y bajo peso molecular (18).
Singh y col. informaron acerca de un caso de tumor maligno de la vaina del nervio periférico, en el estudio de inmunohistoquímica las células tumorales mostraron positividad a vimentina, CD34 y positividad focal para S-100, lo cual coincide con los resultados observados en nuestro estudio en el cual se observó el mismo inmunomarcaje en 2 casos, confirmando así el diagnóstico de tumor maligno de la vaina del nervio periférico (19).
Por último, en lo que respecta al sarcoma sinovial, Henninger y col., reportaron un caso en el cual inmuno-histoquímicamente las células tumorales fueron positivas para CAM 5.2, citoqueratina 7 (CK), bcl-2 y vimentina, y negativo para S100, CD34, CD99, desmina y SMA. Con estos hallazgos (especialmente queratina positiva y el Bcl-2) que era posible excluir a dos entidades que pueden parecerse más estrechamente sarcoma monofásico sinovial en esta ubicación: El tumor fibroso solitario (CD34 positivo) y el tumor de vaina nerviosa periférica (focalmente S-100 positivo). En nuestra serie, se observó el inmunomarcaje para CKAE1/AE3 positiva y CD20 CD34, S100, cromogranina, enolasa neuronal específica negativo y PGP 9,5 negativos (20).
Además, Salah y col., también reportaron un estudio de 40 casos de este tipo de tumores y de igual forma observaron la expresión de marcadores epiteliales en el componente similar al glandular (glandular like) y lo más importante en el componente de células fusiformes, lo cual apoya el diagnóstico. También reportan que el antígeno de membrana epitelial (EMA) es el marcador más comúnmente positivo entre todos los marcadores epiteliales. Las pan-citoqueratinas y citoqueratinas 7 y 19 también pueden ser positivos en el componente de tipo epitelial, así como el componente de células fusiformes. Además, la positividad para bcl-2 se puede ver en algunos casos (21).
En conclusión los tumores mediastinales son muy poco frecuentes representando el 1,3 % de los tumores recibidos en un período de 8 años en las secciones de Patología Respiratoria y Hematopatología del Instituto anatomopatológico “Dr. José A O’daly”. La segunda década de la vida fue la más afectada por tumores mediastinales, seguida de la cuarta década. La edad media fue de 38 ± 19 años. Los tumores mediastinales son más frecuentes en el sexo masculino. (58,4 % del total de casos observados), se localizan con más frecuencia en el mediastino anterior (40,1 %), seguido del mediastino posterior (5,1 %). Los tumores de mediastino más frecuentes son de estirpe epitelial (46,7 %: benignos 17,5 % y malignos 29,2 %) y los tipos de tumores más frecuentemente observados fueron el linfoma no Hodgkin difuso de células grandes inmunofenotipo B, con un 7,2 %, al igual que el linfoma de Hodgkin variedad nodular esclerosante (7,2 %) y el carcinoma neuroendocrino (7,2 %) del total de 137 casos evaluados. Los marcadores de inmunohistoquímica más utilizados en el diagnóstico de tumores epiteliales son CKAE1/AE3, CK7, CK34BE12 y CEA. Para los linfomas de Hodgkin el inmunomarcaje más frecuente era CD15 y CD30 positivo. Por su parte, los linfomas no Hodgkin mostraron positividad a algunos anticuerpos como el CD20, CD79A, y particularmente los linfomas difusos de células grandes B exhibieron positividad al CD45 (ALC: antígeno leucocitario común) y CD45RO. En el caso de los tumores germinales los anticuerpos más usados fueron la fosfatasa alcalina placentaria (PLAP), la BHCG, alfafetoproteína, el CD117, la CKAE1/AE3 y el antígeno de membrana epitelial (EMA). Por su parte los marcadores más utilizados para el diagnóstico de tumores mesenquimáticos fueron actina de músculo liso (AML), vimentina, y S100.
Nuestra recomendación para la realización de estudios posteriores es invitar e insistir a los médicos tratantes a llenar todos los datos que se solicitan en la boleta de anatomía patológica, porque tanto la ubicación del tumor como los datos demográficos son de gran interés para los patólogos que nos orientan al diagnóstico y es de gran utilidad al momento de realizar trabajos como este.
REFERENCIAS
1. Ríos A, Torres J, Roca MJ, Galindo P, Parrilla P. Tratamiento quirúrgico de los quistes mediastínicos no neoplásicos. Cir Esp. 2002;72(4):216-221. https://doi.org/10.1016/S0009-739X(02)72044-7
2. Lopez JL. Enfermedades del mediastino. Medicine. 2010;10(68):4667-4672.
3. Rodriguez C, Arce C, Amarilla L, Andreo T, Araujo D, Arzamendia L, et al. Características clínicas y patológicas de los tumores de mediastino en un hospital universitario. Cir. Parag. 2013;37(2):22-25.
4. Ibarra C, García J, Fernández M. Guía diagnóstico-terapéutica: tumores y masas del mediastino. Rev Inst Nal Enf Resp Mex. 2001;14(3):172-177.
5. Asgary M, Aghajanzadeh M, Hemmati H, Jafari M. Epidemiology of mediastinal tumors during six years (2006-2012) in Rasht City. Emergencias. 2014;2:88-94.
6. Thomas MO, Ogunleye EO. Mediastinal masses: Pathophysiological issues and management challenges in a developing world. Surgical Science. 2011;2(4):212-214.
7. Hesami SMA., Izadi B. Assessment of different types of mediastinal tumors removed by surgery at Taleghani Hospital, Kermanshah, (2002-2005). Journal of Kermanshah University of Medical Sciences (Behbood). 2007 [Cited 2020 march11];11(3 (34)):296-303. Disponible en: URL: https://www.sid.ir/en/journal/viewpaper.aspx?Id=114159
8. Bahrami A, Truong L, Ro J. Undifferentiated tumor: True identity by immunohistochemistry. Arch Pathol Lab Med. 2008;132(3):326-348.
9. Weissferdt A, Moran C. Immunohistochemistry in the diagnosis of thymic epithelial neoplasms. Appl Immunohistochem Mol Morphol. 2014;22(1):479-487.
10. Brcic L, Heidinger M, Popper H. Neuroendokrine neoplasien des mediastinums. Pathologe. 2016;37(1):434-440. https://doi.org/10.1007/s00292-016-0198-0
11. Bustamante S, Viveros J, Camargo D, Piedrahita A, Polo J, Carrillo J. Linfoma primario del mediastino (tímico): Presentación de un caso. Rev. Colomb. Radiol. 2016; 27(2):4464-4468.
12. Von Wasielewski R, Mengel M, Fisher R, Hansmann L, Hubner K, Franklin J, et al. Classical Hodgkin's disease. Clinical impact of the inmunophenotype. Am J Pathol. 1997;151(4):1123-1130.
13. Shamsuddin F, Khadilkar U, Debarshi S, Sreedharan S. Mediastinal lymphomas a clinic-pathologic study. Indian J Pathol Oncol. 2015;2(3):131-140.
14 Gwaiz LA, Bassioni W. Immunophenotyping of acute lymphoblastic leukemia using immunohistochemistry in bone marrow biopsy specimens. Histol Histopathol. 2008;23(10):1223-1228.
15. Gao Y, Jiang J, Liu, Q. Extra gonadal malignant germ cell tumors: A clinic-pathological and immunohistochemically analysis of 48 cases at a single Chinese Institution. Int J Clin Exp Pathol. 2015;8(5):5650-5657.
16. Ortega P, Suster D, Falconieri G, Zambrano E, Moran C, Morrison C, et al. Liposarcomas of the posterior mediastinum: Clinic-pathologic study of 18 cases. Mod Pathol. 2015;28(5):721-731.
17. Suster S, Moran C, Koss M. Rhabdomyosarcomas of the anterior mediastinum: Report of four cases unassociated with germ cell, teratomatous, or thymic carcinomatous components. Hum Pathol. 1994;25(4):349-356.
18. Gutiérrez M, Hernández A, Cruz H, González Y, Cicero R. Tumor fibroso solitario. Estudio clínico-patológico de 16 casos. Cir Cir. 2011;79(5):417-423
19. Singh S, Ralli M, Hasija S, Verma R. Intrathoracic malignant peripheral nerve sheath tumor: Histopathological and immunohistochemically features. Iran J Pathol. 2015;10(1):74-78.
20. Henninger B, Freund M, Zelger B, Putzer D, Bonatti H, Müller L, et al. Primary mediastinal synovial sarcoma: A case report and review of the literature. Cases Journal. 2009;2:6948. https://doi.org/10.4076/1757-1626-2-6948
21. Salah S, Salem A. Primary synovial sarcomas of the mediastinum: A systematic review and pooled analysis of the published literature. ISRN Oncol. 2014;412527. http://doi.org/10.1155/2014/412527.
Notas de autor
sanchitarut@gmail.com