CARCINOMA CON DIFERENCIACIÓN ECRINA/APOCRINA VULVO PERINEAL. CASO CLÍNICO Y REVISIÓN DE LA LITERATURA
CARCINOMA CON DIFERENCIACIÓN ECRINA/APOCRINA VULVO PERINEAL. CASO CLÍNICO Y REVISIÓN DE LA LITERATURA
Revista Venezolana de Oncología, vol. 34, núm. 1, pp. 18-24, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 29 Agosto 2021
Revisado: 12 Septiembre 2021
Aprobación: 11 Noviembre 2021
Resumen: Las lesiones apocrinas de la piel son raras y se encuentran principalmente en los pliegues corporales, como la axila, la ingle y pliegue anogenital. Los adenocarcinomas ecrinos/apocrinos son tumores epiteliales malignos muy raros de los anexos cutáneos, que se originan generalmente en las glándulas sudoríparas, sin embargo, están descritas en la vulva y región anogenital. Algunos autores los clasifican en carcinoma de las glándulas sudoríparas, enfermedad de Paget extra-mamaria y adenocarcinomas breast-like. Presentamos una paciente de 48 años con un carcinoma con diferenciación ecrina/apocrina de la región vulvoperineal, el procedimiento quirúrgico, tratamiento adyuvante y una breve revisión de la literatura.
Palabras clave: Carcinoma, neoplasias de glándulas sudoríparas, adenocarcinomas, enfermedad de Paget extra-mamaria, vulva, inmunohistoquímica.
Abstract: The apocrine skin lesions are rare and are found mainly in body folds, such as the armpit, the groin, and the anogenital fold. The eccrine/apocrine adenocarcinomas are very rare malignant epithelial tumors of the skin attachments, which generally originate in the sweat glands; however they are described in the vulva and the anogenital region. Some authors classify them as the sweat gland carcinoma, or extra-mammary Paget's disease, and also breast-like adenocarcinomas. We present a woman 48 year old patient with eccrine/apocrine differentiating carcinoma of the vulvoperineal region, the surgical procedure, the adjuvant treatment, and a brief review of the literature.
Keywords: Carcinoma, sweat gland neoplasms, adenocarcinomas, extra-mammary Paget disease, vulva, immunohistochemistry.
INTRODUCCIÓN
Los adenocarcinomas ecrinos/apocrinos son tumores epiteliales malignos muy raros de los anexos cutáneos, que se originan generalmente en las glándulas sudoríparas, sin embargo, están descritos en la vulva. Aunque en esta localización, su histogénesis no está muy clara, algunos autores los clasifican en carcinoma de las glándulas sudoríparas, enfermedad de Paget extra-mamaria y adenocarcinomas (ADC) breast-like de la vulva. Tienen potencial de metástasis regionales y a distancia, asociadas con mal pronóstico. El tratamiento consiste en cirugía, una vulvectomía parcial con o sin linfadenectomía inguino-femoral y radioterapia adyuvante.
CASO CLÍNICO
Paciente femenina de 48 años, quien consultó en febrero de 2019 a médico especialista por lesión en región vulvoperineal derecha, de seis meses de evolución. Realizan ultrasonido que reporta imagen de aspecto multiquístico. Le fue realizada PAF obteniéndose contenido líquido cuyo estudio citológico reporta contenido de quiste con escasos linfocitos sin atipias. Continúa con crecimiento lento por lo que solicitan tomografía computada, en la cual reportan tumor multilobulado sólido con componente quístico tabicado, de 95 mm x 78 mm x 60 mm, que ocupa el subcutáneo del periné y se extiende hacia el labio mayor derecho de la vulva y en profundidad ocupa la fosa isquiorrectal derecha. En febrero 2020, le fue realizada resección parcial, cuyo estudio histopatológico fue reportado como: carcinoma de células claras. Una segunda opinión anatomopatológica con inmunohistoquímica fue reportada como: adenocarcinoma con rasgos apocrinos.
Examen físico (12/05/2020): cicatriz oblicua entre el periné y el muslo derecho, con lesión subyacente de consistencia dura, entre el periné y el 1/3 posterior del labio mayor derecho de la vulva, de aproximadamente 8 cm, fijo a planos profundos. Pared vaginal y rectal con compresión extrínseca. Se palpa adenopatía de aproximadamente 10 mm en la región inguinal derecha sin criterios clínicos de sospecha.
ESTUDIOS DE IMÁGENES
Ultrasonido: lesión ocupante de espacio ecomixta, con áreas quísticas en región vulvoperineal. Adenopatía ovalada de 10 mm, sin signos ecográficos de sospecha.
Una nueva tomografía (marzo 2020) muestra dos lesiones densas de 3,5 cm irregulares dominantes, una en el subcutáneo entre periné y el glúteo derecho y la otra en plano profundo de la fosa isquiorrectal que compromete el labio mayor derecho de la vulva, unidas por área densa heterogénea con cambios posquirúrgicos que en conjunto mide 9,6 cm x 7,8 cm, sin compromiso óseo. Se realiza RMN para precisar compromiso de tejidos blandos y descartar infiltración ano rectal. Se observa, además, la adenopatía inguinal derecha, sin criterios de sospecha.
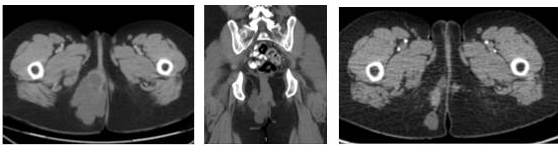
Figura 1.
RMN: izquierda corte axial y centro corte sagital previas a resección parcial. Derecha: axial previa a cirugia definitiva
PROCEDIMIENTO QUIRÚRGICO
El 26/02/2020, se realizó: 1. Inyección perivulvar derecha y peritumoral de 2 cm3 de azul patente. 2. Abordaje inguinal derecho, exéresis del ganglio palpable (no centinela) cuya biopsia por congelación fue negativa para metástasis y de dos ganglios centinelas, reportados como positivos para metástasis. 3. Disección inguino-femoral superficial y profunda. 4. Vulvectomía parcial derecha extendida al periné con resección tumoral en bloque incluyendo la cicatriz previa. Márgenes macroscópicos 1 cm. 5. Reconstrucción con colgajo miocutáneo de gracilis.
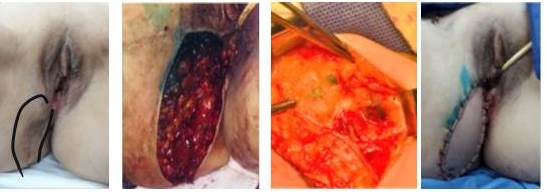
Figura 2.
De izquierda a derecha: lesión y márgenes de resección, defecto, ganglio centinela y reconstrucción
Resultados de patología: carcinoma con diferenciación ecrina/apocrina que sugieren origen anexial de 6,3 cm x 5,1 cm x 2,7 cm. Presencia de invasión vasculolinfática. Ausencia de infiltración perineural. Márgenes libres, oscilan entre 3 mm y 8 mm. Disección inguino-femoral: ganglio centinela (2): positivos para metástasis. Resto (7): negativos.
IHQ: citoqueratinas AE1/AE3, 7 y 34BE12 positivas, RE +30 %.
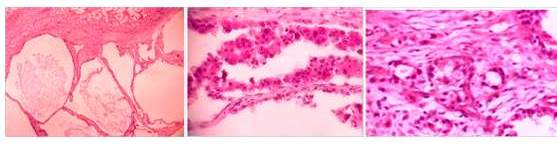
Figura 3.
De izquierda a derecha: microquistes revestidos de epitelio columnar. Quistes con proyecciones papilares, nucleos hipercromáticos de tamaño y forma variables y células apicales con secreción por decapitación. Glándulas irregulares infiltrando el estroma denso, con núcleos vesiculosos y nucleolos prominentes.
Recibió radioterapia adyuvante con acelerador lineal, equipo 3D, una dosis total de 5 400 cGy, en sesiones de 180 cGy, guiada por IGRT, entre el 25/8 y 8/10/2020.
DISCUSIÓN
La mayoría de los ADC de la vulva se originan principalmente de las glándulas de Bartolino. Menos frecuentes son los que derivan de las glándulas sudoríparas. Son neoplasias infrecuentes sin un esquema de clasificación uniforme o única acerca de su origen(1,2,3). Estas neoplasias han sido consideradas como carcinomas de glándulas sudoríparas ubicadas en otros sitios de la piel y/o relacionadas a un origen en glándulas mamarias supernumerarias si presentan características histológicas similares al cáncer de mama, basando esta última teoría en las "líneas de leche" que se presentan durante el desarrollo embrionario; sin embargo, ésta teoría fue debatida por Van der Putte y col. (1) al mencionar que dichas líneas sólo se extienden hasta la región inguinal durante el desarrollo embrionario, no encontrándose tejido mamario en la región anogenital.
En relación a esto último, es importante resaltar que la enfermedad extra-mamaria de Paget (EMPD) en la vulva, ha tenido una larga historia de controversias acerca de su derivación, con ecrinos, apocrinos y glándulas mamarias supernumerarias o relacionados con células germinales pluripotenciales como posibles orígenes (4,5); la presencia de glándulas mammary-like anogenital (MLG) revelan una histología específica diferente de ecrinas, apocrinas y glándulas mamarias, y al mismo tiempo presentan características similares con cada una de ellas (6). Inicialmente fueron llamadas glándulas sudoríparas ano-genitales por su apariencia a glándulas ecrinas, pero, debido a que características microscópicas de la glándula mamaria son más obvias, dicho término es ahora preferido. Los ADC de glándulas sudoríparas de la vulva son considerados tumores raros(6,7,8) que frecuentemente revelan un componente Pagetoide quedando pendiente aún por resolver si derivan de glándulas ecrinas o apocrinas o de sus células precursoras intra-epidérmicas. Los resultados de estudios morfológicos e histoquímicos han sido contradictorios y no han mostrado analogía en estudios similares de glándulas sudoríparas en otros sitios. Los test inmunohistoquímicos de EMPD no han mostrado una característica para diferenciar entre una derivación glandular apocrina o ecrina (9,10).
Van der Putte y col., señalan en algunas de sus investigaciones (11,12) que MLG además de presentar remanentes de glándulas mamarias, presentan también asociación con distintos elementos ecrinos y apocrinos, siendo sugerido el término glándulas sudoríparas ano-genitales con características distintas a las glándulas sudoríparas de otros sitios de la piel. La literatura actual (13), señala el adenocarcinoma de vulva dentro de tres categorías, ADC de glándulas sudoríparas nativas de la vulva, carcinoma primario de vulva mammary-like, y enfermedad de Paget extra-mamaria.
El caso que aquí nos ocupa, se trata de una variante de adenocarcinoma apocrino vulvar, también determinadas como neoplasias raras (14) que pueden presentarse in situ y confinadas a las glándulas sudoríparas nativas vulvar o invasivo; la enfermedad de Paget extra-mamaria está con frecuencia presente en conjunto con este tipo de neoplasias, sin embargo, dicha asociación no fue encontrada en el análisis histológico de la pieza operatoria ni en las metástasis ganglionares reportadas en nuestro caso. Actualmente los hechos para clasificar un ADC vulvar como un tipo mammary-like, incluye la presencia de glándulas mammary-like normales en la vecindad del tumor, la presencia de zonas de transición con cambios variables malignos entre ambos, la presencia de morfología típica de la mama y la expresión inmunohistoquímica de receptores de estrógenos y progesterona positivos (15).
El síntoma más frecuente del cáncer vulvar es el prurito (55 %), seguido por la aparición de un tumor en los genitales externos, así como la presencia de ulceraciones. Síntomas tardíos como las secreciones sero-hemáticas o el dolor asociado a infección o extensión a tejidos vecinos se relacionan con una enfermedad infiltrante o en estado avanzado y, en caso de afectación del meato uretral, se producen también síntomas urinarios. Es preciso realizar una adecuada inspección vulvar y exploración de pliegues vulvares, vagina, uretra, ano y cérvix, así como una palpación de las regiones inguinales para obtener un diagnóstico adecuado. El diagnóstico de este tipo de neoplasia, está basado principalmente en el examen e inspección de las estructuras vulvares así como la realización de vulvoscopia, en ocasiones, con aplicación de ácido acético. La biopsia obtenida mediante punción aspiración con aguja fina puede ofrecer buenos rendimientos diagnósticos; sin embargo, el método definitivo de diagnóstico es la biopsia de la lesión, para lo cual es preciso que la muestra incluya tejido celular subcutáneo. Histopatológicamente, hay una mezcla de patrones, incluidos los patrones papilar, trabecular y sólido. Las células tumorales son a menudos poligonales y con citoplasma eosínofílico (16,17,18). La inmunohistoquímica puede representar una herramienta útil a la hora de caracterizar el tumor y realizar un diagnóstico diferencial (19,20). Las glándulas sudoríparas ecrinas expresan positividad para queratina de bajo peso molecular (LMWK), antígeno de membrana epitelial (EMA) y antígeno carcinoembrionario (CEA), así como la proteína S100 en la capa basal. Tumores con diferenciación ecrina a menudo también expresan tinción inmunohistoquímica positiva para receptores de estrógeno y progesterona, lo que puede tener aplicación en el manejo hormonal (7). En el caso de nuestra paciente hubo expresión de receptores de estrógenos en 30 %. Los estudios han demostrado una fuerte correlación de la expresión del receptor de andrógenos en carcinoma apocrino cutáneo, aumentando el potencial de terapia anti-androgénica (18).
En el manejo diagnóstico y terapéutico del cáncer de vulva, en general, no hay demasiados estudios que describan la utilidad de la PET/TC, aunque, como ya reflejaron en su estudio Peiró y col. (16), se trata de una prueba muy útil tanto para la detección de lesiones primarias como para la discriminación en la afectación ganglionar y juega un papel importante por la aportación que supone en la planificación quirúrgica. En nuestra paciente este estudio no se realizó, dados lo inusual del caso y la necesidad de completar el tratamiento quirúrgico con la mayor celeridad posible. La base principal del tratamiento del carcinoma invasivo de vulva es la cirugía mediante técnica de vulvectomía simple/radical con linfadenectomía inguino-femoral uni o bilateral y radioterapia posoperatoria (en los casos de más de una metástasis ganglionar); no se practica, por norma general, una linfadenectomía pélvica adicional. La identificación y biopsia del ganglio centinela está considerado hoy en día como un procedimiento estándar en el carcinoma de la vulva en etapas tempranas, esto es, tumores unifocales de hasta 4 cm con infiltración en el estroma mayor de 1 mm y ganglios clínicamente negativos (T1-2 N0). En estas pacientes el compromiso ganglionar oscila entre 25 % y 35 % en las linfadenectomías electivas, resultando en la mayoría en un sobre-tratamiento (15,16). El porcentaje de detección con colorante vital es de 68 % a 75 % y combinando el colorante con radio-coloide es de 87 % a 100 % (16). Aunque no está descrito en la literatura la indicación de la biopsia de ganglio centinela en los carcinomas ecrinos/apocrinos, por ser una patología muy rara, ofrecimos el procedimiento con el fin de evitar una linfadenectomía innecesaria y su consecuente morbilidad. En nuestro caso, el ganglio centinela fue reportado como positivo y el resto de los ganglios en la disección resultaron negativos. Nuestra paciente presentó como complicación un hematoma en la región inguino-femoral con dehiscencia limitada de la herida. En el 2002 Covens A y col., publicaron una revisión bibliográfica en la que comparaban la radiación primaria frente a cirugía primaria en el tratamiento del cáncer precoz de vulva. En este estudio, llegaron a la conclusión de que la radioterapia, comparada con la cirugía, presenta menor morbilidad, pero, por otro lado, un mayor número de recurrencias inguinales (17). El papel de la quimioterapia en el tratamiento del cáncer vulvar diseminado o recidivante es limitado.
Los factores pronósticos más importantes de esta enfermedad son el estadio clínico y la afectación ganglionar, con una tasa de supervivencia general del 90 % en las pacientes con enfermedad resecable sin afectación ganglionar; sin embargo, en pacientes con compromiso ganglionar, esta tasa disminuye hasta el 50 %-60 % aproximadamente. La frecuencia global de recidivas se sitúa entre el 10 % y el 40 %, donde más de 2/3 se producen en los 2 primeros años. Como conclusión: los adenocarcinomas de vulva representan el 3 %-5 % de los cánceres de vulva y pueden originarse en la glándula de Bartolino, glándulas sebáceas, sudoríparas, apocrinas, en los focos endometriósicos, en mamas aberrantes o pueden ser secundarios a adenocarcinomas de otra localización (12). El perfil de las glándulas mamarias ano-genitales, que también puede revelar algunas características ecrinas o apocrinas, hace que estas glándulas sean la fuente más probable de una serie de lesiones que se producen en la región anogenital y que comprenden las glándulas lactantes, los fibroadenomas, la mayoría de casos de la enfermedad de Paget extra-mamaria, el adenocarcinoma invasivo. El origen de estas neoplasias está en las glándulas sudoríparas apocrinas o las glándulas ano-genitales del tipo «mammary-like», aunque esta afirmación se encuentra aún en discusión. Pueden dar lugar a diferentes tipos histológicos de tumores, y se aplican para su diagnóstico y tratamiento las mismas técnicas que en los casos de carcinomas primarios de la vulva, mientras que otros grupos de investigación proponen, incluso, la opción de aplicar la misma línea de tratamiento que en los cánceres de mama en casos de carcinomas del tipo «mammary-like».
El tratamiento consiste en la cirugía con márgenes quirúrgicos oncológicos con o sin radioterapia adyuvante. El compromiso ganglionar constituye un factor pronóstico relevante. La inmunohistoquímica constituye una herramienta diagnóstica en casos con diagnóstico patológico dudoso.
REFERENCIAS
1. Van der Putte SCJ, Van Gorp LHM. Adenocarcinoma of the mammary-like glands of the vulva: A concept unifying sweat glands carcinoma of the vulva, carcinoma supernumerary mammary glands and extramammary Paget’s disease. J Cutan Pathol. 1994;157-163.
2. Michael H, Roth LM. En: Wilkineon EJ, editor. Congenital and adacquiried cyst, benign and malignant skin adnexal tumors and Paget’s disease of the vulva. Nueva York: Churchill Livingstone;1987.p.25.
3. Ridley CM. The vulva. Edinburgh: Churchill Livingstone;1988.
4. Novak E, Stevenson RR. Sweat gland tumors of the vulva, bening (hidroadenoma) and malignant (adenocarcinoma). Am J Obstet Gynecol. 1945;50:641-659.
5. Weilburg RD, Miller GV, Von Pohle KG. Paget’s disease of the vulva associated with adenocarcinoma developing in a hidradenoma papilliferum. Am J Obstet Gynecol. 1967;98: (2):294-295.
6. Kazakov D, Spagnolo D, Kacerovska D, Michal M. Lesions of anogenital mammary-like glands: An update. Adv Anat Pathol. 2011;18(1):1-28.
7. Obaidat N, Alsaad K, Ghazarian D. Skin adnexal neoplasms-part 2: An approach to tumours of cutaneous sweat glands. J Clin Pathol. 2007;60:145-159.
8. Webb JB, Beswick BS. Ecrine hidroadenocarcinomas of the vulva with Paget’s disease. Case report with a review of the literature. Br J Obstet Gynecol. 1983;90(1):90-95.
9. Rich PM, Okagak T, Clark B, Prem KA. Adenocarcinoma of the sweat gland of the vulva. Cancer. 1981:47:1352-1357.
10. Pelosi G, Martingnoni G, Bonetti F. Intraductal carcinoma of mammary-type apocrine epithelium arising within a papillary hidradenoma of the vulva. Arch Pathol Lab Med. 1991;115:1249-1254.
11. Van der Putte SCJ. Anogenital sweat glands. Histology and pathology of a gland that may mimic mammary glands. Am J Dermatopathol. 1991;13:557-567.
12. Van der Putte SCJ. Ultraestructure of the human anogenital sweat gland. Anat Rec. 1993;235(4):583-590.
13. Alsaad KO, Obaidat N, Dube V, Chapman W, Ghazarian D. Vulvar apocrine adenocarcinoma: A case with nodal metastasis and intranodal mucinous differentiation. Pathol Res Pract. 2009;205(2):131-135.
14. Molero J, Hernández-Aguado JJ, Lailla JM. En: Bajo A JM,Lailla VJ, Xercavins Montosa J, editores. Carcinoma de la vulva. Fundamentos de Ginecología SEGO. Madrid: Médica Panamericana Inc; 2009.p.347-363.
15. Amalinei C, Giusca SE, Caruntu ID. Fibroadenomas of anogenital mammary-like glands: From embryogenesis anomaly to apocrine origin. Pol J Pathol. 2015;66:219-223.
16. Peiró V, Chiva L, González A, Bratos R, Alonso S, Márquez R, et al. Utilidad de la PET/TC en el manejo del cáncer de vulva. Rev Esp Med Nucl Imagen Mol. 2014;33:87-92.
17. Covens A, Vella E, Kennedy B, Reade C, Jimenez W, Le T. Sentinel lymph node biopsy in vulvar cancer: Systematic review, meta-analysis and guideline recommendations. Gynecol Oncol. 2015;137:351-361.
18. Baker G, Selim A, Hoang M. Vulvar adnexal lesions: A 32-year single-institution review from Massachusetts General Hospital. Arch Pathol Lab Med. 2013;137:1237-1246.
19. Collarino A, Fuoco V, Garganese G, Pereira L, Arias-Bouda, Perotti G, et al. Lymphoscintigraphy and sentinel lymph node biopsy in vulvar carcinoma: Update from a European expert panel. Eur J Nucl Med Mol Imaging. 2020;47:1261-1274.
20. Hyde SE, Ansink AC, Burger MP, Schilthuis MS, van der Velden J. The impact of performance status on survival in patients of 80 years and older with vulvar cancer. Gynecol Oncol. 2002;84:388-393.
Notas de autor
jfmata55@gmail.com.