CARCINOMA DUCTAL IN SITU CON MICROINVASIÓN ¿NECESARIO BIOPSIA DEL GANGLIO CENTINELA?
CARCINOMA DUCTAL IN SITU CON MICROINVASIÓN ¿NECESARIO BIOPSIA DEL GANGLIO CENTINELA?
Revista Venezolana de Oncología, vol. 34, núm. 2, pp. 58-66, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 30 Julio 2021
Aprobación: 16 Enero 2022
Resumen: OBJETIVO: Determinar necesidad de investigar estado axilar en pacientes con diagnóstico de carcinoma ductal in situ con microinvasión. MÉTODO: Análisis de 43 pacientes diagnosticadas, mediante biopsia percutánea con aguja de corte y vacío, intentando en la mayoría de casos de acuerdo al tamaño de la lesión, eliminación de la imagen. Se practicó biopsia de ganglio centinela con técnica dual con Tc99m y azul patente. Se estudiaron variables que pudieran contribuir a identificación de ganglios metastásicos. RESULTADOS: 42/43 pacientes con uno o más ganglios centinelas, edad mediana 60 años (rango: 30-82). 26,2 % tamaño tumoral ≤20 mm, diagnosticadas con aguja de corte y vacío, se logró eliminar imagen en su totalidad. En 2 no hubo lesión residual en pieza operatoria. Mediana de seguimiento 7,8 años (rango: 1-19 años). Ganglio centinela positivo en 1 (2,4 %). 2(4,8 %) recaídas, una local en mama ipsilateral 163,5 meses de seguimiento, otra regional en axila ipsilateral 20,2 meses de seguimiento. La supervivencia global 95,1 % a 5 años. Supervivencia libre de enfermedad 97,6 % 5 años. CONCLUSIÓN: Carcinoma ductal in situ con microinvasión es poco frecuente. La estandarización de su manejo es controversial, en lo que se refiere a la práctica de biopsia de ganglio centinela. Tamaño de la lesión, tipo de instrumento con que se practica la biopsia percutánea y posibilidad de eliminar la imagen que motivó la biopsia, son factores a considerar al momento de decidir llevar a cabo biopsia de ganglio centinela.
Palabras clave: Mama, cáncer, carcinoma ductal in situ, biopsia de ganglio centinela.
Abstract: OBJECTIVE: To determine the need to investigate axillary status in patients diagnosed with ductal carcinoma in situ with microinvasión. METHOD: Analysis of 43 patients diagnosed by percutaneous biopsy with cutting and vacuum needle, attempting in most cases according to size of the lesion, to remove the image. The sentinel node biopsy was performed with dual technique with Tc 99m and patent blue. The variables that could contribute to the identification of metastatic ganglion were studied. RESULTS: In 42/43 patients with one or more sentinel nodes, median age 60 years (range: 30-82). 26.2 % tumor size ≤20 mm, diagnosed with cutting needle and vacuum, was able to eliminate image in its entirety. In 2 there was no residual lesion in the operative piece. The median follow up was 7.8 years (range: 1-19 years). Sentinel ganglion positive in 1 (2.4 %). 2 (4.8 %) relapses, a local in ipsilateral breast 163.5 months of follow-up, another regional in ipsilateral armpit 20.2 months. The overall survival was 95.1 % at 5 years. The disease free survival was 97.6 % in 5 years. CONCLUSION: The ductal carcinoma in situ with micro-invasion is rare. The standardization of its management is controversial, in terms of the practice of sentinel node biopsy. Size of the lesion, type of instrument with which the percutaneous biopsy is performed and possibility of eliminating the image that motivated the biopsy, are factors to consider when deciding to carry out sentinel node biopsy.
Keywords: Breast, cancer, ductal carcinoma in situ, sentinel lymph node biopsy.
INTRODUCCIÓN
El carcinoma ductal in situ con microinvasión (CDIS mic), se presenta como una infiltración incipiente de la membrana basal, es una entidad poco frecuente (1,2,3), con un comportamiento cuyo pronóstico se ubica entre un CDIS puro y al cáncer de mama invasor T1a. Publicaciones reportan cifras de CDIS mic que no superan el 3,4 % (4,5,6). Debido a su baja incidencia, frecuentemente el CDIS mic es motivo de discusión y controversia, tanto en su diagnóstico como en la estrategia terapéutica.
Asunto particularmente polémico lo constituye la necesidad de conocer el estado axilar en las pacientes portadoras de CDIS así como de CDIS mic. De hecho, en el caso de CDIS, hemos propuesto estrategias para su manejo (7). La biopsia del ganglio centinela (BGC) es un procedimiento de escasa posibilidad de complicaciones, sin embargo, se han publicado estudios identificando eventos como anafilaxia (8), edema del brazo (9) y parestesias (10), por lo que, al considerar la BGC, debemos evaluar los riesgos frente al beneficio que se obtendría en relación a la posibilidad de encontrar ganglios linfáticos metastásicos. En este sentido, investigaciones registran porcentajes de afectación metastásica ganglionar que varían entre 0 % y 20 % (4, 11,12). En una serie de estudios realizados por investigadores del H. Lee Moffitt Cancer Center and Research Institute desde el año 2001 hasta el presente, se señalan cifras de presencia de ganglios metastásicos en CDIS mic que fluctúan entre 6,9 % y 20 % (4).
Numerosas investigaciones han identificado algunos factores o parámetros que dado su asociación con el sub-diagnóstico se pueden considerar para indicar BGC ante el diagnóstico de CDIS (7,13.14.15). El objetivo del presente trabajo es mostrar nuestra experiencia en la realización de la BGC en pacientes con CDIS mic.
MÉTODO
La investigación se llevó a cabo mediante un análisis retrospectivo de 43 pacientes con diagnóstico de CDIS mic diagnosticadas en el Centro Clínico de Estereotaxia CECLINES en quienes se llevó a cabo BGC (Figura 1). Adoptamos como definición de CDIS mic el propuesto en la octava edición del manual de estadiaje de la AJCC que lo define como aquel foco que presenta infiltración igual o menor a 1 mm(16,17).
En la mayoría de los casos, los diagnósticos se establecieron mediante biopsia mamaria percutánea asistida por estereotaxia o ultrasonido con aguja de corte y vacío. En algunos casos, se usó aguja de corte. El diagnóstico en la pieza operatoria, se hizo mediante cortes histológicos teñidos con el método de hematoxilina y eosina. De acuerdo a la extensión y tamaño de la lesión, durante el procedimiento de biopsia percutánea con aguja de corte y vacío, procuramos eliminar la imagen en su totalidad. Para ello, se tomó la mayor cantidad de muestras posible (18). La técnica empleada para la BGC fue la dual con Tc99m + azul patente. En algunos casos se utilizó solo azul patente. El estudio del GC se llevó a cabo previo al acto quirúrgico. Cada ganglio se seccionó en tantas partes como lo permitió el tamaño ganglionar. Se procesó el tejido ganglionar en su totalidad. Una vez incluido en bloque de parafina, se realizaron cortes histológicos de 3 μ -4 μ por niveles y se colorearon con hematoxilina y eosina. El tamaño de la imagen en la mama se determinó mediante medida en mamografía correspondiendo la mayoría a lesiones no palpables (LNP). Cuando la imagen se identificó por ultrasonido, se utilizó el mismo método para la determinación del tamaño. Para establecer el tamaño de la lesión en la pieza quirúrgica, se recurrió a la radiología del espécimen y observación de la misma por parte del imagenólogo y patólogo. Se constató la presencia de la lesión y su extensión. El tamaño real se estableció correlacionando los hallazgos histopatológicos con las imágenes.
En el análisis estadístico, las variables categóricas se presentaron en frecuencias absolutas y porcentajes, las cuantitativas en medidas de tendencia central y de dispersión, incluyendo la mediana y el rango intercuartílico. Se utilizó la curva de Kaplan Meier para la descripción de la supervivencia global y supervivencia libre de enfermedad. La supervivencia global fue el tiempo de vida transcurrido desde la intervención quirúrgica hasta la muerte por cualquier causa. La supervivencia libre de enfermedad fue el tiempo de vida transcurrido entre la intervención quirúrgica hasta el evento recaída. Para el análisis estadístico de los datos se utilizó el paquete SPSS versión 22.
RESULTADOS
La data de nuestra Institución muestra que desde 1996 hasta 2018 se diagnosticaron 3 434 carcinomas de mama. El CDIS puro se registró en el 14,5 % (497/3 434), el CDIS mic en 2,7 % (91/3 434) y el CDIS con signos indirectos de microinvasión en 0,6 % (20/3 434) (Figura 1). De las 91 pacientes con CDIS mic, se seleccionaron 43 (47,3 %, 43/91) pacientes quienes se trataron en nuestro centro y a las que se les practicó BGC. En 97,7 % (42/43) se identificó uno o más ganglios centinelas. De este modo, el grupo de estudio estuvo conformado por 42 casos de CDIS mic con uno o más ganglios centinelas, con edad mediana de 60 años (rango: 30-82) (Cuadro 1).
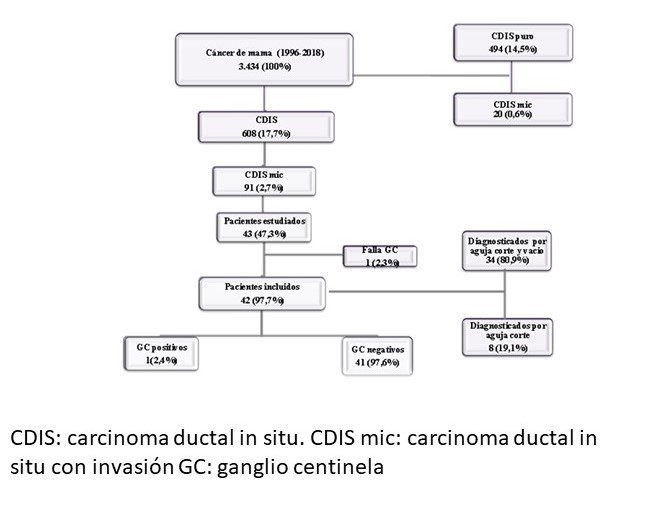
Figura 1.
Inclusión de las pacientes en el estudio

Cuadro 1
. Características clínicas y tumorales
En la mayoría de las pacientes, el diagnóstico histológico se hizo en material obtenido mediante biopsia mamaria percutánea asistida por estereotaxia o ultrasonido con aguja de corte y vacío calibre 8G, 9G y 11G (80,9 %, 34/42), para el resto de los diagnósticos se utilizó aguja de corte calibre 14G (19,1 %, 8/42) (Cuadro 1). En 26,2 % (11/42) pacientes con tamaños tumorales ≤ 20 mm, diagnosticadas por medio de aguja de corte y vacio, se logró eliminar la totalidad de la imagen. El reporte definitivo de la pieza operatoria de anatomía patológica, no localizó cáncer residual en 2 (4,8 %, 2/42) de estas pacientes.
Las LNP fueron registradas en el 71,4 % (30/42) de los casos, siendo la mayoría de ellas microcalcificaciones en el estudio mamográfico (73,3 %, 22/30). El tamaño tumoral promedio estimado a partir de la imagen fue de 36,2 mm (rango: 3-80), con una sobrestimación promedio de 2,6 mm con respecto a la pieza operatoria (33,6 mm, rango: 0-80).
En la evaluación de los receptores hormonales (Cuadro 1), la distribución fue como sigue: 42,8 % (18/42) de las pacientes presentó RE y RP positivos; 38,1 % (16/42) RE y RP negativos, 14,3 % (6/42) RE positivo y RP negativo y 4,8 % (2/42) RE negativo y RP positivo. Por su parte, la sobreexpresión del HER2, fue positiva (+3) en 16,7 % (7/42) de los casos, negativa en 47,6 % (20/42), no concluyente en 14,3 % (6/42) y desconocido en 21,4 % (9/42). El 21,4 % (9/42) de las pacientes presentó un índice de proliferación celular bajo (Ki-67 < 14 %). Se identificó un 16,7 % (7/42) de pacientes con RE, RP y Her 2-neu, negativos.
En relación con el tratamiento adyuvante, 50 % (21/42) de las pacientes recibió radioterapia y el 52,4 % cuyos RE fueron positivos, recibieron hormonoterapia (22/48) (Cuadro 1).
Se observó un promedio de 2 ganglios centinelas por paciente (rango: 1-9). El análisis definitivo del GC mostró un resultado positivo en 1 paciente (2,4 %, 1/42) (Cuadro 1). Dicha paciente de 68 años de edad, con un tamaño de la lesión en la pieza operatoria de 60 mm, con receptores hormonales positivos, Her 2-neu positivo (+3) y Ki-67 bajo (<14 %). Posteriormente, recibió radioterapia y hormonoterapia adyuvantes (Cuadro 2).

Cuadro 2.
Características de paciente con ganglio centinela positivo
Se registraron dos recaídas (4,8 %, 2/42) (Cuadro 3). Una de ellas, local ubicada en mama ipsilateral, registrada a los 163,5 meses de la cirugía inicial. Corresponde a una paciente de 50 años que se había tratado con cirugía preservadora, con un tamaño tumoral de 10 mm, receptores hormonales negativos, HER2 negativo y Ki67 no registrado. La recaída fue tratada quirúrgicamente, recibiendo radioterapia y tamoxifeno como terapias adyuvantes, el tamoxifeno debido a que los RE de la recaída fueron positivos. La paciente se encuentra sana a los 62,4 meses tras la cirugía de rescate (Cuadro 3).
La otra paciente de 49 años de edad, se presenta con una recaída regional en axila ipsilateral a los 20,2 meses de la cirugía y radioterapia. El informe de anatomía patológica de la lesión inicial, fue dede 60 mm, receptores hormonales positivos, HER2 desconocido y Ki67 bajo (<14 %). La recaída se trató con disección axilar y tamoxifeno como terapia adyuvante. Al presente, la paciente se encuentra sana después de 76,9 meses de la recaída (Cuadro 3).
Se registraron cinco muertes: dos en relación a la enfermedad (4,8 %, 2/42), otra falleció por cáncer primario de pulmón (2,4 %, 1/42) y las otras 2 (4,2 %,2/42) que en su último control (diciembre 2017), se encontraban sanas y libres de enfermedad, se desconoce la causa.
El tiempo mediano de seguimiento fue de 7,8 años (rango: 1-19 años).
La Figura 2 y 3 muestran las curvas de Kaplan Meier de supervivencia global y supervivencia libre de enfermedad. La supervivencia global fue de 95,1 % (ES: 3,4 %) a 5 años. Por su parte, la supervivencia libre de enfermedad fue de 97,6 % (ES: 2,4%) a 5 años.
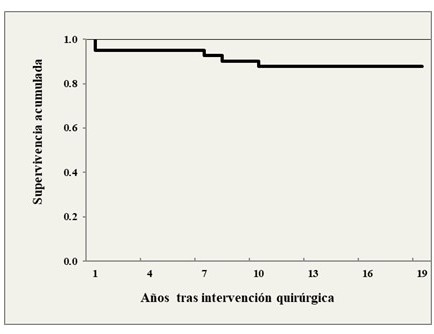
Figura 2.
Supervivencia global
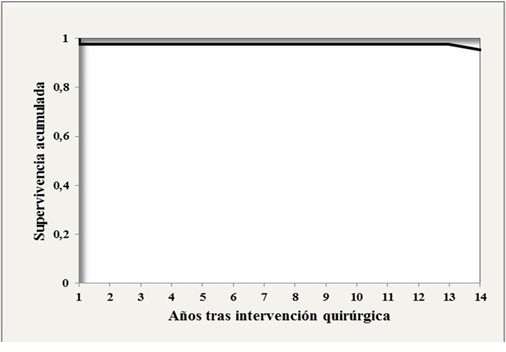
Figura 3.
Supervivencia libre de enfermedad
DISCUSIÓN
La data recopilada en nuestra institución en el período 1996-2018 registra un porcentaje de CDIS mic de 2,7 %, mostrando consistencia con hallazgos de otras investigaciones que la sitúan entre un 0,6 % y 3,4 % de todos los cánceres de la mama (4,5,6). Siendo el CDIS mic una patología infrecuente, las directrices para su adecuado tratamiento, incluyendo la necesidad de la BGC, es discutible. En relación con este aspecto, nuestro criterio para establecer el diagnóstico de CDIS mic, es riguroso en el sentido de lo estricto a la observación y categorización de la microinvasión. Insistimos en que, de acuerdo al tamaño de la lesión (microcalcificaciones en su mayoría), procuramos mediante el procedimiento de biopsia, llevada en la mayoría de los casos con sonda de corte y vacío, eliminar la totalidad de la imagen, en el entendido de que a menos imagen posterior a biopsia, la probabilidad de sub-diagnóstico será menor, disminuyendo la posibilidad de encontrarnos en la pieza operatoria con una lesión infiltrante, hecho éste que aumentaría la probabilidad de existir ganglios metastásicos, lo cual sería indicación de BGC. Es así como que en 11 de las pacientes cuyas imágenes fueron iguales o menores de 20 mm, y cuyas biopsias se llevaron a cabo mediante aguja de corte y vacío, logramos eliminar la totalidad de la imagen. De hecho, en 2 de esos casos no hubo lesión residual en la pieza operatoria.
Ahora bien, tanto el CDIS puro como el CDIS mic diagnosticados en biopsia percutánea, tienen posibilidad de sub-diagnóstico en la pieza operatoria, pudiendo pasar a una lesión invasiva (T1), que teniendo posibilidad de cursar con ganglios metastásicos, justifica la indicación de BGC (2,12). En el presente estudio el porcentaje de identificación de GC fue de 97,7 %. Resultado aceptable en la aplicación de la técnica de BGC (Figura 1). De los 42 pacientes en que se identificó el GC, 1 (2,4 %) paciente registró GC positivo. En este sentido, hallazgos de la literatura revelan variabilidad en los índices que muestran la posibilidad de que el CDIS mic curse con ganglios metastásicos, habiéndose descrito porcentajes que van desde 2,9 % hasta 10 % (2, 5, 19). La inclusión de pacientes con células tumorales aisladas en algunas de estas investigaciones podría explicar la dispersión de estos resultados. En esta línea, el H. Lee Moffitt Cancer Center and Research Institute reportó que el porcentaje de GC metastásicos en pacientes con CDIS mic, disminuyó de 20 % a 6,9 % al excluir el grupo de pacientes con células tumorales aisladas (4,5). Holm-Rasmussen y col., reportan 21,5 % de ganglios metastásicos en CDIS mic pero, al excluir las micrometástasis (7,7 %) y las células tumorales aisladas (9,9 %), el porcentaje de macrometástasis, fue 3,9 % (20).
Diversas investigaciones han identificado algunos factores o parámetros que dado su relación con el sub-diagnóstico se puede considerar para establecer la indicación de BGC ante el diagnóstico de CDIS, a saber, tamaño del tumor, subtipo sólido y CDIS de alto grado(13,14). Asimismo, Ko B y col., reportan que la presencia de invasión linfática y receptores de estrógenos positivos, son predictores independientes significativos de metástasis axilar en CDIS mic (15). El tamaño tumoral es uno de los factores particularmente asociado con la presencia de afectación ganglionar axilar. Ya en 1989, Carter y col., al estudiar 24 740 pacientes con cáncer de mama, identificaron que el tamaño tumoral era un factor pronóstico independiente de afectación ganglionar, observando una relación lineal entre el diámetro del tumor y el número de ganglios linfáticos positivos, concluyendo que la progresión de la enfermedad a sitios distantes no ocurría exclusivamente vía los ganglios linfáticos axilares, sino más bien que el estado de los ganglios linfáticos servía como un indicador de la capacidad del tumor para difundirse (21) . En investigación reciente, Yi y col., al valorar predictores de positividad de GC en pacientes con CDSI mic, hallaron que el único factor pronóstico independiente para la metastización al GC fue un tamaño tumoral > 50 mm (22). En este tenor, autores como Lillemoe y col., sugieren que en pacientes con cáncer de mama microinvasor, la indicación de BGC debe ser limitada a pacientes con tamaño tumoral ≥50 mm (23).
Como se indicó anteriormente, en el presente estudio se identificó sólo 1 caso de CDIS mic con GC positivo. En esta paciente el diagnóstico corresponde a un tumor de 60 mm, receptores hormonales positivos, HER2 positivo. Analizando este caso, observamos que la lesión era voluminosa (60 mm), lo que plantearía la posibilidad de la existencia de una infiltración mayor que no se evidenció en la biopsia percutánea ni en la pieza operatoria, hecho este que avala la opinión de Ya y col., en el sentido que debido a la posibilidad de subestimación diagnóstica, a lesiones mayores de 50 mm, se les debe practicar BGC. Por otro lado, el único caso de recidiva axilar se presenta igualmente, como una lesión de gran tamaño (40 mm) y además, si tomamos en cuenta que el tiempo transcurrido entre el acto quirúrgico y la recidiva axilar fue realmente corto (20,2 meses), podríamos concluir que existía un componente infiltrativo mayor que no fue identificado y que en el momento de la BGC, ya existía la metástasis axilar, correspondiendo esto, a un falso negativo de la BGC (24). No obstante, después de analizar estos aspectos controversiales, nuestros resultados muestran un bajo porcentaje de GC positivo, una supervivencia global de 95,1 % a 5 años y una supervivencia libre de enfermedad de 97,6 % a 5 años. Estos resultados nos permiten recomendar la individualización de los casos con diagnóstico de CDIS mic y, de acuerdo a algunas características, decidir sobre la necesidad de practicar BGC.
El bajo porcentaje de ganglio centinela positivo (2,4 %) registrado en nuestra experiencia, impide identificar factores predictores de axila positiva en pacientes con diagnóstico de CDIS mic y por ende, ser realmente precisos en cuanto a la necesidad o no de llevar a cabo la BGC en estos casos.
A pesar de esto y dado nuestros resultados concluimos que el tamaño de la lesión (<40 mm), el tipo de instrumento con que se practica la biopsia percutánea (con sistema de corte y vacío) y la posibilidad de eliminar la imagen que motivó la biopsia, son factores que debemos considerar para obviar la realización de la BGC en pacientes con diagnóstico de CDIS mic.
REFERENCIAS
1. Feinberg J, Wedtstone D, Greenstein D, Borgen P. Is CDIS overrated? Cancer Treat Res. 2018;173:53-72.
2. Sakr R, Barranger E, Antoine M, Prugnolle H, Daraï E, Uzan S. Ductal carcinoma in situ: Value of sentinel lymph node biopsy. J Surg Oncol. 2006;94(5):426-430.
3. Lagios M, Westdahl P, Margolin F, Rose M. Ductal carcinoma in situ: Relationship of extent of noninvasive disease to the frequency of occult invasion, multicentricity, lymph node metastases, and short-term treatment failures. Cancer. 1982;50:1309-1314.
4. Pimiento J, Lee MC, Esposito N, Kiluk J, Khakpour N, Bradford W, et al. Role of axillary staging in women diagnosed with ductal carcinoma in situ with microinvasion. J Oncol Pract. 2011;7:309-313.
5. Shatat L, Gloyeske N, Madan R, O´Neil M, Tawfik O, Fan F. Micro invasive breast carcinoma carries an excellent prognosis regardless of the tumor characteristics. Hum Pathol. 2013;44(12):2684-2689.
6. Matsen C, Hirsch A, Eaton A, Stempel M, Heerdt A, Van K, et al. Extent of microinvasion in ductal carcinoma in situ is not associated with sentinel lymph node metastases. Ann Surg Oncol. 2014;21(10):3330-3335.
7. Acosta-Marin V, Acosta-Freites V, Ramirez AK, Pérez-Fuentes J, Marín CE, Contreras A, et al. Utilidad del estudio del ganglio centinela en carcinoma ductal in situ diagnosticado mediante biopsia con sistema de corte por vacío. Rev Senol Mamar. 2017;30(1):15-20.
8. Krag DN, Anderson SJ, Julian TB, Brown AM, Harlow SP, Costantino JP, et al. Sentinel-lymph-node resection compared with conventional axillary-lymph-node dissection in clinically node-negative patients with breast cancer: Overall survival findings from the NSABP B-32 randomized phase 3 trial. Lancet Oncol. 2010;11:927-933.
9. McLaughlin SA, Wright MJ, Morris KT, Giron G, Sampson M, Brockway JP, et al. Prevalence of lymphedema in women with breast cancer 5 years after sentinel lymph node biopsy or axillary dissection: Objective measurements. J Clin Oncol. 2008;26:5213-5219.
10. Kelley, MC, Hansen N, McMasters KM. Lymphatic mapping and sentinel lymphadenectomy for breast cancer. Am J Surg. 2004;188:49-61.
11. Goyal A, Douglas-Jones A, Monypenny I, Sweetland H, Stevens G, Mansel RE. Is there a role of sentinel lymph node biopsy in ductal carcinoma in situ? Analysis of 587 cases. Breast Journal Res Treat. 2006;98(3):311-314.
12. Namm J, Mueller J, Kocherginsky M, Kulkarni S. The utility of sentinel lymph node biopsy in patients with ductal carcinoma in situ suspicious for micro-invasion on core biopsy. Ann Surg Oncol. 2015;22:59-65.
13. Tunon-de Lara C, Giard S, Butarelli M, Blanchot J, Classe JM, Baronm M, et al. Sentinel node procedure is warranted in ductal carcinoma in situ with high risk of occult invasive carcinoma and microinvasive carcinoma treated by mastectomy. Breast J. 2008; 14(2):135-140.
14. Acosta VF, Contreras A, Ravelo R, Marin CE, Perez J, Longobardi I, et al. Carcinoma ductal in situ de la mama. Primeros 100 Casos-Ceclines. Rev Venez Oncol. 2010;22(2):88-93.
15. Ko B, Lim W, Kim H, Yu J, Lee J, Kwan S, et al. Risk factors for axillary lymph node metastases in microinvasive. Breast cancer. Ann Surg Oncol 2012;19:212-216.
16. Boland G, Knox W, Bundred N. Molecular markers and therapeutic targets in ductal carcinoma in situ. Microsc Res Tech. 2002;59(1):3-11.
17. Silver S, Tavassoli F. Mammary ductal carcinoma in situ with microinvasion. Cancer.1998;82(12):2382-2390.
18. Acosta V, Contreras A, Ravelo R, Marín C, Pérez J, Longobardi I, et al. Carcinoma ductal in situ. Experiencia en Centro Clínico de Estereotaxia CECLINES. Rev Venez Oncol. 2006;18(1):2-8.
19. Sakr R, Antoine M, Barranger E, Dubernard G, Salem C, Daraï E, et al. Value of sentinel lymph node biopsy in breast ductal carcinoma in situ upstaged to invasive carcinoma. Breast J. 2008;14(1):55-60.
20. Holm-Rasmussen EV, Jensen MB, Balslev E, Kroman N, Tvedskov TF. Sentinel and non-sentinel lymph node metastases in patients with microinvasive breast cancer: A nationwide study. Breast Cancer Res Treat. 2019;!75(3):713-719.
21. Carter CL, Allen C, Henson DE. Relation of tumor size, lymph node status, and survival in 24740 breast cancer cases. Cancer. 1989;63:181-187.
22. Yi M, Krishnamurthy S, Kuerer HM, Meric-Bernstam F, Bedrosian I, Rosset M, et al. Role of primary tumor characteristics in predicting positive sentinel lymph nodes in patients with ductal carcinoma in situ or microinvasive breast cancer. Am J Surg. 2008; 196(1):81-87.
23. Lillemoe TJ, Tsai ML, Swenson KK, Susnik B, Krueger J, Harris K, et al. Clinic pathologic analysis of a large series of micro invasive breast cancers. Breast J. 2018;24(4):574-579
24. Seung Ah Lee, Hak Min Lee, HakWoo Lee, Ban Seok Yang , Jong Tae Park , Sung Gwe Ahn, et al. Risk factors for a false-negative result of sentinel node biopsy in patients with clinically node-negative breast cancer. Cancer Res Treat. 2018;50(3):625-633.
Notas de autor
dr.victoracostamarin@gmail.com
Información adicional
AGRADECIMIENTO: : Dra. Lucila Blanco de Cedres, responsable del análisis estadístico. Br. Ariana Ruiz recopilación de la información.