RECONSTRUCCIÓN DE PARED COSTAL EN CONDROSARCOMA CLÁSICO DE ARCOS COSTALES A PROPÓSITO DE UN CASO.
RECONSTRUCCIÓN DE PARED COSTAL EN CONDROSARCOMA CLÁSICO DE ARCOS COSTALES A PROPÓSITO DE UN CASO.
Revista Venezolana de Oncología, vol. 34, núm. 2, pp. 99-108, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 28 Agosto 2021
Aprobación: 17 Diciembre 2021
Resumen: OBJETIVO: Los tumores de pared costal son neoplasias poco frecuentes y de difícil tratamiento. Por su localización, los pacientes se presentan con una tumoración, dolor y dificultad respiratoria CASO CLÍNICO: Se trató de una paciente de 57 años con un tumor de pared costal. Fue intervenida en nuestro hospital en el año 2019. Se le realizó una resección en bloque, mastectomía total tipo Halsted no radical izquierda con pared costal anterior (4. 5. y 6. arcos costales) y reconstrucción con interposición de malla, alambre Kirschner y colgajo de dorsal ancho. La evolución posoperatoria fue satisfactoria. El resultado de la biopsia definitiva reporta condrosarcoma clásico grado II de Evans. CONCLUSION: Es importante que los pacientes con tumores de pared costal tengan una valoración preoperatoria para lograr resultados quirúrgicos y funcionales adecuados, con disminución de la morbilidad y mortalidad posoperatoria.
Palabras clave: Tumor, pared costal, condrosarcoma, cirugía, biopsia.
Abstract: OBJECTIVE: The primary tumors of the chest wall are uncommon and difficult to treat because of the location the patients present a mass, pain and respiratory shortness. CLINICAL CASE: A 57 year old woman presented in our institution with a chest wall mass. A whole tumor was excised in a block with 4th, 5th and 6th ribs, along with a left non radical Halsted mastectomy. The reconstruction of the defect was made with the interposition of the metallic wire and dorsal muscle flap. The postoperative evolution was satisfactory. The final diagnosis was chondrosarcoma Evan’s Grade II. The patient had an uneventful post operatory course CONCLUSION: The curative therapy of the chest wall chondrosarcomas is an adequate surgical resection. The proper evaluations of the patient are the keys for successful treatment and functional results, also lower mobility and mortality.
Keywords: Tumor, chest wall, chondrosarcoma, surgery, biopsy.
INTRODUCCIÓN
Los tumores malignos primarios de pared costal representan un grupo heterogéneo de neoplasias que se originan de partes blandas, huesos y cartílagos, de estos el condrosarcoma, es el más frecuente (1). Se trata de una neoplasia productora de cartílago que afecta principalmente los huesos largos (fémur proximal; húmero proximal, fémur distal y costillas) y huesos planos como la cadera. Las costillas, son el quinto o sexto lugar de localización, representando un 6 % de todos los condrosarcomas (2.3,4).
Los pacientes generalmente se presentan con dolor torácico asociado o no a tumor palpable, algunos con síntomas respiratorios por compresión cuando la lesión es grande o intra-torácica (5).
En estos pacientes es importante una planificación previa de la intervención que incluya el diagnóstico histológico preoperatorio para determinar los márgenes adecuados de resección, la extensión de la resección de la pared torácica y la forma de reconstrucción cuando genera grandes defectos (1,6,7,8).
Presentamos una paciente con un condrosarcoma del 5o arco costal anterior izquierdo, describimos la técnica quirúrgica utilizada para su resección y reconstrucción de la pared costal y realizamos una revisión de la literatura.
CASO CLÍNICO
Se trata de paciente femenina de 57 años de edad quien inició enfermedad actual hace 10 años caracterizada por dolor y discreto aumento de volumen en mama izquierda en cuadrantes inferiores. En diciembre de 2012 se le realizó una mastectomía parcial izquierda (MPI) por lesión nodular palpable en unión de cuadrantes inferiores de mama izquierda (UCI), cuya biopsia fue informada como “cambios fibro-quísticos”. Persiste con aumento de volumen lento y progresivo no doloroso, consulta a nuestro centro el 15 de marzo de 2019 por disnea y lesión retro-mamaria izquierda. Antecedentes de importancia: exéresis de nódulo de mama izquierda, cuya biopsia reportaron: quiste simple más condición fibroquística. Al examen físico la paciente se encontraba disneica, con murmullo vesicular abolido en 2/3 inferiores de campo pulmonar izquierdo, se observa un tumor en mama izquierda, consistencia pétrea, piel brillante, con red venosa colateral, no dolorosa a la palpación que ocupa la totalidad de la mama, sin adenopatías axilares y supraclaviculares. Resto del examen físico dentro de lo normal (Figura 1A).
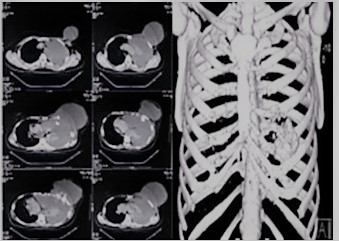
Figura 1 A.B.
TAC de tórax con contraste y reconstrucción 3D 2019: lesión voluminosa, de crecimiento expansivo, que rompe la cortical, se extiende a la mama izquierda, cavidad torácica y mediastino izquierdo
Entre los estudios de imágenes que se realiza, muestra una de RX tórax simple AP-L de 2019, donde se observa derrame pleural izquierdo con desplazamiento del cardiomediastino a la derecha (Figura 1B). Una RX de tórax PA de 2012 donde se evidencia cambios en la densidad ósea del 5o arco costal anterior izquierdo con pérdida de la cortical y TAC de tórax con contraste del mismo año en la cual se identifica un tumor de 4 cm x 5 cm en el 5o arco costal, de bordes definidos, de crecimiento expansivo con línea fina de cortical residual de la costilla sin signos de extensión a tejidos blandos, tórax o mama (Figura 2). En abril de 2019 realiza tomografía de tórax (Figura 3) con contraste y reconstrucción en 3D, donde se observa una lesión de 30 cm x 20 cm, que compromete 4o 5o y 6o arco costal anterior, expansiva, lítica, bordes mal definidos con destrucción de la cortical, desplazando pulmón izquierdo y mediastino sin infiltrarlos, compromete la totalidad de la mama izquierda, en relación íntima con el pericardio desplazándolo a línea media y derrame pleural izquierdo masivo.
El 28/05/19 se le realiza toma de biopsia con aguja gruesa, (B19-1276) cuyo resultado reporta: lesión condromixoide.
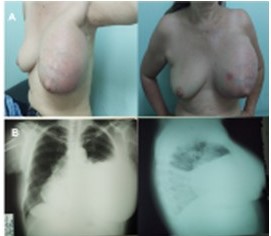
Figura 2
A: Vista frontal y lateral de mama izquierda con masa gigante de 30 cm x 20 cm, de consistencia indurada, con red venosa colateral. B: Radiología simple AP y lateral izquierdo donde se observa un velamiento extenso de los 2/3 inferiores del campo pulmonar izquierdo, con derrame pleural.
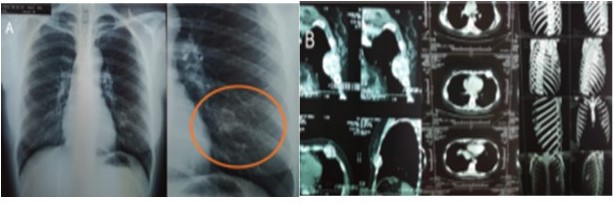
Figura 3.
RX de tórax AP y TAC de tórax contrastado y reconstrucción 3D 2012. A. Se evidencia cambios en la densidad y ruptura de la cortical del 5o arco costal anterior izquierdo. B. Presencia de masa expansiva, lítica de 4 cm x 5 cm en quinto arco costal anterior izquierdo.
TÉCNICA QUIRÚRGICA
Se realizó resección en bloque del tumor mediante mastectomía total izquierda, tipo Halsted no radical (Figura 4A), con resección del 4o, 5o y 6o arco costal anteriores (Figura 4B) (20 cm aproximadamente), realizándose disección del tumor intratorácico del pericardio y pulmón (Figura 4C), los cuales no presentaban signos de infiltración (Figura 5) y previa aspiración del derrame plural. Se reconstruye colocando una malla de Proceed® (malla dual con una cara parietal de polipropileno y una visceral de polidoxanona) (Figura 6), la estabilización de la pared torácica anterior mediante un entramado horizontal y vertical con alambre de Kirschner (modificación de la técnica de Leininger) (9,10,11) y cierre del defecto de partes blandas con colgajo miocutáneo del dorsal ancho (12) (Figura 7).
La paciente evolucionó satisfactoriamente, con hemitórax izquierdo hipo-expansible y murmullo vesicular audible en ambos campos pulmonares sin agregados (Figura 8), presenta sin embargo, en herida quirúrgica área de ¨tórax paradójico¨ sin compromiso ventilatorio.
La biopsia definitiva (B19-785) concluyó un condrosarcoma clásico grado II de Evans, con infiltración a la mama izquierda, tejido subcutáneo, alcanzando la dermis papilar. El margen de resección profunda y ósea esternal se encontraba infiltrado. No se observaron émbolos vasculares o linfáticos (Figura 9). Se refiere a radioterapia por presentar márgenes positivos.
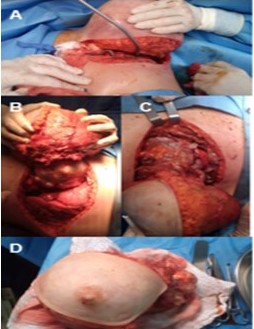
Figura 4
A: mastectomía tipo Halsted no radical. B: resección del tercer, cuarto y quinto arcos costales izquierdos. Se observa desplazamiento del pulmón. C: tumor desplazando el pericardio (Flecha). D: pieza definitiva.
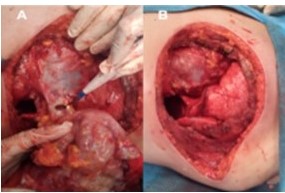
Figura 5
A. Disección del pericardio. B. Defecto en el pericardio.
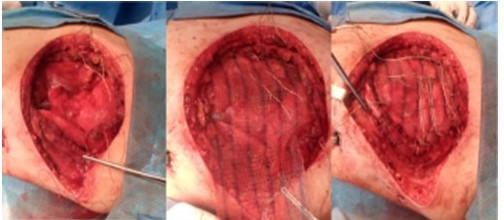
Figura 6
Estabilización de pared costal (4o, 5o y 6o arco costal anterior) mediante entramado horizontal y vertical con alambre de Kirchner, previa colocación de malla de Proceed®
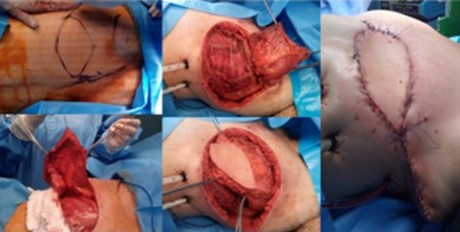
Figura 7.
Confección de colgajo del dorsal ancho para cubrir defecto definitivo
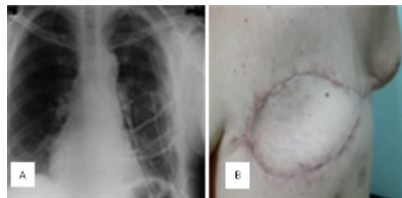
Figura 8
A: radiología pos quirúrgica. B: tórax hipo-expansible.
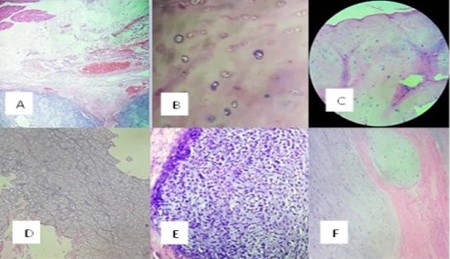
Figura 9.
A: borde de resección profundo con lóbulos de neoplasia condroide. B: áreas de lesión hipo celulares, con escaso pleomorfismo. C: incremento moderado de la celularidad. D: mayor hiper celularidad, con escaso pleomorfismo, sin figuras mitóticas. D: focos de células pleomórficas, de núcleos hipercrómicas con atipias marcadas. F: nidos de neoplasia bien diferenciada, infiltrando el tejido subcutáneo.
DISCUSIÓN
La integridad y la estabilidad de la pared torácica son los principales factores que aseguran la protección de los órganos intratorácicos y una función respiratoria adecuada. Las indicaciones para realizar resecciones de la pared torácica son tumores benignos, malignos y metastásicos (11). Los objetivos principales de este tipo de intervenciones son lograr una resección adecuada y el restablecimiento de la estabilidad de la pared torácica, con la finalidad de lograr un buen funcionamiento pulmonar y un resultado estético aceptable.
La cirugía siegue siendo la herramienta fundamental en el tratamiento de los tumores primarios malignos de la pared torácica, porque tienden a ser resistentes a la quimioterapia o la radioterapia. El propósito de la cirugía radical es la extirpación adecuada del tumor con un amplio margen libre de enfermedad.
El condrosarcoma primario de pared costal es un tumor poco frecuente (13). En ellos es primordial que las resecciones tengan un margen adecuado entre 2 cm (para los condrosarcomas bien diferenciados) y 4 cm a 6 cm para los condrosarcomas poco diferenciados, esto es la resección de 1 a 2 costillas por debajo y por arriba de la lesión, de esta manera se minimiza el riesgo de recurrencia local (6, 8).
El segundo objetivo de las resecciones amplias de la pared torácica, es planificar una serie de estrategias de reconstrucción que garanticen estabilidad y funcionalidad. Esta reconstrucción consta de dos partes, primero la estabilización del tórax óseo y segundo la cubierta del defecto. En realidad, varios materiales sintéticos, biológicos y metálicos están disponibles para reconstruir los defectos de la pared torácica, pero cada material protésico tiene sus propias ventajas y desventajas y ninguno ha demostrado ser claramente superior(14, 15). Para suministrar rigidez al tórax se utilizan halo injertos óseos, estos deben tener la rigidez óptima para la estabilidad y radio opacidad suficiente que permitan el seguimiento radiológico. Para cubrir el defecto se utiliza transferencia de músculos, la interposición de epiplón o material protésico (9).
Existen una gran variedad de mallas sintéticas que presentan las ventajas de una fácil manipulación y estabilidad (16). Todos ellos, más o menos, cumplen con las características del material protésico ideal según lo determinado por Le Roux y col. (17) a. Rigidez para abolir el movimiento paradójico. b. Inercia para permitir el crecimiento de tejido fibroso y disminuir la probabilidad de infección. c. Maleabilidad a la forma apropiada en el momento de la operación d. Radio lucidez para crear una referencia anatómica para hacer un mejor seguimiento e identificar una posible recaída neoplásica local. La mayoría de los parches son mallas sintéticas no absorbibles: parches de tejido blando de polipropileno, poliéster y politetrafluoroetileno (PTFE), generalmente doblados y suturados a costillas adyacentes y fascia para cubrir la superficie inmediata del defecto de la pared torácica.
Algunos autores informaron una tasa de infección entre 10 % y 25 % para las mallas sintéticas y la necesidad de eliminar la malla infectada para resolver el problema (16). En estos casos, se podría considerar una malla de Vicryl debido a su material inerte, no antigénico, bio-compatible y de absorción lenta o una malla biológica tan similar a la prótesis de pericardio bovino.
Recientemente se propusieron mallas de titanio (MDF Médica®) que presentan más resistencia que las mallas sintéticas, manteniendo la misma plasticidad y adaptabilidad en el defecto de la pared torácica. La malla de 5 mm de espesor podría obtener la rigidez adecuada en la pared torácica, evitando lesiones en los órganos endotorácicos, preservando el sistema por infección para la condición inerte de titanio y resultando bien tolerado por el paciente. Todas estas mallas a menudo resultan seguras y útiles para resolver el defecto de la pared torácica, pero para defectos anteriores, esternal o posterior inferior podría ser insuficiente, incluso si está bien suturado y estirado como un tambor, para proteger los órganos internos (16).
El metacrilato de metilo generalmente se intercala entre dos capas de la malla para fortalecer la rigidez de la reconstrucción. Podría prepararse en el campo quirúrgico, donde una primera capa de malla de polipropileno se fija directamente sobre la base del defecto de la costilla y el sustituto de metacrilato de metilo se agrega a la forma del defecto y se cubre con una segunda capa de la prótesis, endureciendo un reacción exotérmica y volverse rígido y formar un molde que se ajusta al defecto. Con esta técnica, sobre todo para defectos extensos de la pared torácica anterior y lateral, se evitan los movimientos paradójicos y las deformidades torácicas (16,18). Sin embargo, el material de metacrilato de metilo parece no ser permeable a los fluidos y, por lo tanto, se considera que aumenta el dolor y la rigidez excesiva de la pared torácica. Es posible una fractura del metacrilato y sobre todo aumenta el riesgo de infección (17).
El PTFE (GORE-TEX) es otro material muy adecuado y comúnmente utilizado para la reconstrucción de la pared torácica. Similar al metacrilato de metilo, el PTFE es hermético y provoca una reacción mínima de cuerpo extraño; sin embargo, es flexible, lo que le permite adaptarse a la pared torácica. Un taladro óseo o un clip de toalla afilado funcionan bien, creando agujeros en las costillas para la fijación. El PTFE se puede usar para estabilizar defectos grandes de la pared torácica y debe cubrirse completamente con tejido viable después de la implantación. Su uso está absolutamente contraindicado en campos infectados (19).
Las barras de titanio se introdujeron para apoyar la reconstrucción de la pared torácica después de la demolición por enfermedad neoplásica, como para reparar las fracturas de la caja torácica después de un traumatismo y dehiscencia esternal. El titanio es un material protésico ideal, que tiene una alta resistencia a la corrosión, un peso específico bajo, una notable resistencia a la tracción, es diamagnético, biológicamente inerte y altamente biocompatible con pocas complicaciones, entre as cuales la más descrita son las fracturas de dicho material que se presentan en del 0 %-11 % (11) a mayor desventaja es su alto costo.
Tanto los materiales bioprotésicos humanos, halo injertos y homoinjertos crio preservados, se utilizan con mayor frecuencia para restaurar la integridad estructural en defectos de la pared torácica grande. La principal ventaja es que pueden incorporarse al tejido nativo con revascularización y repoblación celular, lo que los hace más resistentes a las infecciones y útiles en campos contaminados (10). Este tipo de procedimiento requiere de la disponibilidad de un banco de tejido, el cual carece en nuestra institución.
Independientemente de la técnica utilizada para establecer la estabilidad esquelética, la cobertura total del tejido de la prótesis es obligatoria, utilizando sutura directa, injertos de piel, colgajos de avance local, colgajos miocutáneos pediculados o colgajos libres. La selección de la transferencia de tejido adecuada requiere la evaluación de las cicatrices quirúrgicas, la dimensión del defecto, la necesidad de material protésico o cobertura de vísceras, y si se requiere un volumen de tejido adicional para llenar un espacio vacío (20).
Entre los diversos músculos utilizados, el dorsal ancho se considera el caballo de batalla en la reconstrucción de la pared torácica antero lateral, porque este colgajo permite cubrir toda la pared torácica ipsilateral (19). El pectoral mayor se tiene en cuenta como el colgajo principal para la cobertura de defectos de la pared torácica esternal y anterosuperior, son colgajos pediculados (21).
El colgajo del recto abdominal, alimentado por sistemas epigástricos superiores o inferiores profundos, ofrece una versatilidad incomparable del diseño de la isla de la piel (pedículo de la piel orientado verticalmente (VRAM) - transversal (TRAM)), lo que ha permitido una amplia aplicación de este colgajo para la cobertura de defectos antero lateral o anterior (19).
Los colgajos musculares libres pueden estar indicados si el grupo muscular local ha sido resecado, previamente lesionado o irradiado (19). En la parte posterior (latissimus dorsi, parascapular), un colgajo fasciocutáneo o miocutáneo, en el muslo, el tensor de la fascia lata y el TRAM son algunos de los colgajos libres que generalmente se usan. El colgajo del omento mayor es otra gran opción para reparar defectos en la pared torácica anterior, en caso de que los colgajos pediculados o los colgajos libres mencionados anteriormente fallen o no sean adecuados.
En 1973 Leininger y col., describieron una técnica para estabilizar la pared costal (7). Esta fue modificada por el Guzmán F y col., Servicio de Cirugía de Tórax en el Hospital Universitario de Maracaibo, Estado Zulia, Venezuela en el año 2010 mediante la realización de un entramado horizontal y vertical con sutura de poliglactin 910 y malla de Marlex.
En nuestro caso se utilizaron alambres de Kirschner y malla dual (PROCEED®) con recubrimiento del defecto con colgajo de dorsal ancho que permitió una buena estabilidad de la pared torácica, un adecuado manejo ventilatorio posoperatorio y buenos resultados estéticos (Figura 10). La utilización de la malla PROCEED® por ser dual, es decir, que posee doble superficie, una visceral, lisa que es la que está en contacto con el parénquima pulmonar y otra corrugada, cara parietal. La finalidad del uso de este tipo de malla aparte de brindar una cobertura del defecto creado por la resección, es brindar una superficie que simule la pleura. Esta se fija en los bordes, más no en la zona central, es lo que determina que estos pacientes se comporten con un tórax inestable o paradójico, con complicaciones ventilatorias leves o moderadas.
La técnica de entramado con alambres de Kirschner, con previa interposición de malla, permitió una estabilidad de la pared torácica y este a su vez poder realizar resecciones amplias para adquirir márgenes óptimos, con buena evolución posoperatoria.
El defecto amplio de partes blandas posterior a la mastectomía total izquierda tipo Halsted no radical, realizada por necesidad en vista de la extensión y compromiso del tumor, se repara con colgajo miocutáneo del dorsal ancho. Este colgajo es ampliamente descrito en la literatura como un colgajo miocutáneo pediculado, cuya pastilla provee una buena cantidad de músculo y piel para cubrir grandes defectos. Nosotros decidimos implementar esta técnica que posee pocas probabilidades de necrosis tisulares, es relativamente rápida y se consigue un muy buen tejido vascularizado, dando en nuestro caso un buen resultado estético.
La complicación más importante de las resecciones amplias de la pared torácica es la inestabilidad de la pared torácica y generalmente los pacientes intervenidos necesitan ventilación mecánica posoperatoria, algunos incluso ameritan una intubación prolongada con el riesgo de neumonía nosocomial y neumonía asociada al ventilador.
La paciente permanece en la unidad de cuidados posoperatorios con ventilación mecánica durante 12 h, con parámetros ventilatorios y paraclínicos normales, estuvo 4 días posteriormente en hospitalización y egresa en buenas condiciones clínicas con área de tórax paradójico sin compromiso ventilatorio.
A los 3 meses del posoperatorio, la paciente presenta recaída local masiva con nódulos múltiples en pared torácica anterior, posterior y diafragmática, tejidos blandos de axila y región infraclavicular izquierda, en espera de iniciar radioterapia, no siendo posible planificarla y decidiéndose tratamiento sistémico paliativo.
Hay que tener una mirada al futuro y a pesar de los avances recientes en el diseño de barras protésicas de titanio para reparar muchas configuraciones de defectos de la pared torácica, las prótesis están lejos de ser ideales todavía una opción definitiva (21). Hubo buenos resultados con el uso de materiales bioabsorbibles (ácido poliglicolico, ácido poli-láctico, etc.) para la reparación de la pared torácica. Un nuevo desarrollo reciente podría ser una tomografía computarizada con imágenes tridimensionales (3D) reconstruidas, que podrían guiar la creación, a través de una tecnología de impresión 3D, resina, polímero, metal y prótesis de biomaterial degradable. Se puede usar una combinación de materiales, algunos biodegradables, otros para hacer rígida la estructura y una evolución que permita el crecimiento y la colonización por las propias células del paciente (21). Estas evoluciones tienden a tener una prótesis adaptada al hábito y la enfermedad del paciente.
El condrosarcoma clásico representa el 90 % de los tumores malignos primarios de todos los casos de pared costal. Se trató de un condrosarcoma de bajo grado con 10 años de evolución. Se planificó la resección quirúrgica evaluando diferentes técnicas y materiales (mallas sintéticas, epiplón, metacrilato, barras y placas de titanio), decidiéndose por la técnica de Leininger modificada, por disponibilidad de recursos y costos. El tratamiento de los pacientes con tumores de pared torácica debe ser personalizado o individualizado, teniendo en cuenta sus estados generales y expectativos de vida el cual debe ser llevado a cabo por un equipo multidisciplinario. Entre las diferentes técnicas que mencionan en la literatura, todas tienen ventajas así como desventajas, sin embargo, el objetivo principal que se busca lograr es la resección con márgenes adecuados y la estabilidad de la pared torácica, con la finalidad de cumplir siempre que se pueda con los tres objetivos fundamentales: margen oncológico, función ventilatoria adecuada y resultados estético aceptable.
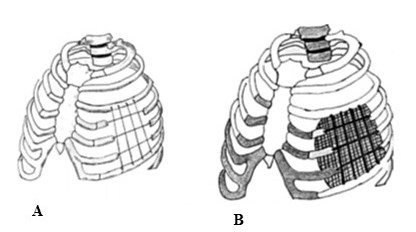
Figura 10.
A. Estabilización de la pared torácica con la técnica de Leininger. B. Estabilización de la pared torácica con la técnica de Leininger e interposición de malla
Referencias
1. Graeber GM, Snyder RJ, Fleming AW, Head HD, Lough FC, Parker JS, et al. Initial and long term results in the management of primary chest wall neoplasm. Ann Thorac Surg. 1982;34:664 -673.
2. Ochsner A, Lucas GL, McFarland GB. Tumours of the thoracic skeleton. Review of 134 cases. J Thorac Cardiovasc Surg.1966;52:311-321.
3. Walsh GL, Davis BM, Swisher SG, Vaporciyan AA, Smythe W, Willis-Merriman K, et al. A single institutional, multidisciplinary approach to primary sarcomas involving the chest wall requiring full thickness resections. J Thorac Cardiovasc Surg. 2001;121:48-60.
4. LeRoux BT, Shama DM. Resection of tumours of the chest wall. Curr Probl Surg. 1983;20:345-386.
5. Arnold PG, Pairolero PC. Chest-wall reconstruction: An account of 500 consecutive patients. Plast Reconstr Surg. 1996;98:804-810.
6. Banic A, Ris HB, Erni D, Striffeler H. Free latissimus dorsi flap for chest wall repair after complete resection of infected sternum. Ann Thorac Surg. 1995;60(4):1028-1032.
7. Leininger BJ, Barker WL, Langston HT. A simplified method of chest wall reconstruction. Ann Thorac Surg. 1972;13(3):258-260.
8. Martini N, Huvos AG, Burt ME, Heelan RT, Bains MS, McCormack PM, et al. Predictors of survival in malignant tumors of the sternum. J Thorac Cardiovasc Surg. 1996;111:96-105.
9. Rupprecht H, Spriewald BM, Hoffmann AR. Successful removal of a giant recurrent chondrosarcoma of the thoracic wall in a patient with hereditary multiple exostoses. Eur J Surg Oncol. 2001;27:216-217.
10. Ng CS. Recent and future developments in chest wall reconstruction. Semin Thorac Cardiovasc Surg. 2015;27(2):234-239.
11. Chapelier AR, Missana MC, Couturaud B, Fadel E, Fabre D, Mussot S, et al. Sternal resection and reconstruction for primary malignant tumors. Ann Thorac Surg. 2004;77:1001-1006.
12. Koto K, Sakabe T, Horie N, Ryu K, Murata H, Nakamura S, et al. Chondrosarcoma from the sternum: Reconstruction with titanium mesh and a transverse rectus abdominis myocutaneous flap after subtotal sternal excision. Med Sci Monit. 2012;18:CS77-81.
13. Athanassiadi K, Kalavrouziotis G, Rondogianni D, Loutsidis A, Hatzimichalis A, Belleniset I. Primary chest wall tumors: Early and long-term results of surgical treatment. Eur J Cardiothorac Surg. 2001;19:589-593.
14. Weyant MJ, Bains MS, Venkatraman E, J Downey RJ Park BJ, Flores RM, et al. Results of chest wall resection and reconstruction with and without rigid prosthesis. Ann Thorac Surg. 2006;81:279-285.
15. Deschamps C, Tirnaksiz BM, Darbandi R, Trastek VF, Allen MS, L Miller DL, et al. Early and long-term results of prosthetic chest wall reconstruction. J Thorac Cardiovasc Surg. 1999;117:588-591.
16. Thomas PA, Brouchet L. Prosthetic reconstruction of the chest wall. Thorac Surg Clin. 2010;20:551-558.
17. Butler CE, Langstein HN, Kronowitz SJ. Pelvic abdominal and chest wall reconstruction with AlloDerm in patients at increased risk for mesh-related complications. Plast Reconstr Surg. 2005;116:1263-1275.
18. McCormack P, Bains MS, Beattle EJ, Martini N. New trends in skeletal reconstruction after resection of chest wall tumors. Ann Thorac Surg. 1981;31:45-52.
19. Seder CW, Rocco G. Chest wall reconstruction after extended resection. J Thorac Dis. 2016;8 (Supl 11):S863-871.
20. Nahai F, Morales L, Jr, Bone DK, Bostwick J. Pectoralis major muscle turnover flaps for closure of the infected sternotomy wound with preservation of form and function. Plast Reconstr Surg. 1982;70:471-474.
21. Turna A, Kavakli K, Sapmaz E, Arslan A, Caylak H, Gokceet H, et al. Reconstruction with a patient-specific titanium implant after a wide anterior chest wall resection. Interact Cardiovasc Thorac Surg. 2014;18:234-236.
Notas de autor
jglf.88@gmail.com