INMUNOHISTOQUÍMICA PARA EVALUACIÓN DE LA SOBRE-EXPRESIÓN DE EGFR, PD-L1 Y REORDENAMIENTO ALK EN CARCINOMAS PULMONARES
INMUNOHISTOQUÍMICA PARA EVALUACIÓN DE LA SOBRE-EXPRESIÓN DE EGFR, PD-L1 Y REORDENAMIENTO ALK EN CARCINOMAS PULMONARES
Revista Venezolana de Oncología, vol. 34, núm. 2, pp. 109-121, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 30 Noviembre 2021
Aprobación: 18 Febrero 2022
Resumen: OBJETIVO: Evaluar el rendimiento diagnóstico de la inmunohistoquímica para determinar la sobreexpresión del EGFR, PD-L1 y reordenamiento ALK en los carcinomas de pulmón en biopsias del laboratorio de Anatomía Patológica del Centro Médico Docente la Trinidad en el período enero 2010- octubre 2020. MÉTODO: Estudio descriptivo, retrospectivo, observacional y experimental en el que se evaluaron todos los casos de carcinomas pulmonares recibidos en laboratorio de Anatomía Patológica del Centro Médico Docente la Trinidad realizando estudio de inmunohistoquímica con los anticuerpos EGFR, ALK y PD-L1 para su análisis histológico. RESULTADOS: La edad promedio fue 67,88 años (±12,171 DE, rango 50 a 99 años). El 48,28 % fueron de sexo masculino y 34,48 % de sexo femenino. El diagnóstico más común previo al estudio inmunohistoquímico fue carcinoma de células no pequeñas (23,08 %). Un total de 20,6 % de los casos mostraron inmunomarcaje positivo para EGFR. La positividad para ALK se observó en 24,13 % de los casos. La inmunoreactividad para PD-L1 se observó en 34,48 % de los casos. La expresión de EGFR está relacionada positivamente con la expresión de ALK y PD-L1. La expresión de ALK presentó asociación positiva con la expresión de EGFR. No se observó significancia estadística con la asociación tipo histológico y alguno de estos tres anticuerpos CONCLUSIÓN: El estudio de inmunohistoquímica es un método confiable para la determinación de mutaciones EGFR, ALK, y expresión PD-L1 importante como factores pronósticos y predictivos en pacientes con carcinomas pulmonares.
Palabras clave: Carcinomas, pulmonares, células no pequeñas, inmunohistoquímica, marcadores, mutaciones, EGFR, ALK, PD-L1.
Abstract: OBJECTIVE: To evaluate the diagnostic performance of the immunohistochemistry to determine the overexpression of the EGFR, PD-L1 and ALK rearrangement in the lung carcinomas in biopsies of the Pathological Anatomy laboratory of the Trinidad Medical Teaching Center in the period January 2010-october 2020. METHOD: A descriptive and retrospective, observational and experimental study will be carried out in which all cases of lung carcinomas received in the Pathological Anatomy laboratory of the Teaching Medical Center of Trinidad in the period January 2010-october 2020 was evaluated, conducting an immunohistochemistry study with the EGFR, ALK and PD-L1 antibodies for histological analysis. RESULTS: The mean age was 67.88 years old (± 12.171 SD, range 50 to 99 years). 48.28 % were male and 34.48 % female. The most common diagnosis prior to the immunohistochemically study was non-small cell carcinoma (23.08 %). A total of 20.6 % of the cases showed positive immuno-labeling for EGFR. ALK positivity was observed in 24.13 % of the cases. Immunoreactivity for PD-L1 was observed in 34.48 % of the cases. The EGFR expression is positively related to ALK and PD-L1 expression. The expression of ALK showed a positive association with the expression of EGFR. No statistical significance was observed with the histological type association and any of these three antibodies. CONCLUSION: The immunohistochemically study is a reliable method for the determination of EGFR, ALK mutations, and PD-L1 expression important as prognostic and predictive factors in patients with carcinomas pulmonary.
Keywords: Carcinomas, lung, non-small cell, immunohistochemistry, markers, mutations, EGFR, ALK, PD-L1.
INTRODUCCIÓN
El cáncer de pulmón figura entre los cinco tipos de neoplasias que ocasionan más números de muertes en el mundo, epidemiológicamente en Venezuela constituye la segunda causa de muerte por cáncer en hombres y la tercera causa en mujeres después del cáncer de próstata, cuello uterino y mama respectivamente según el boletín epidemiológico de la Organización Mundial de la Salud (OMS) del 2014, incidencia que se mantiene hasta la fecha según la Sociedad Anticancerosa de Venezuela para el año 2016 (1).
El adenocarcinoma (ADC) es el cáncer de pulmón más frecuente que corresponde al 40 %-50 % de los cánceres de pulmón mientras que el carcinoma de células escamosas (CCE) representa el 30 % de todos los cánceres de pulmón en hombres y 20 % en mujeres, por lo tanto es el segundo en frecuencia, ambos constituyen un grupo denominado carcinomas de células no pequeñas(2,3).
En general las células tumorales manifiestan aberraciones genéticas complejas que ocurren durante la carcinogénesis de etapas múltiples. La inestabilidad o selección genómica conduce a aberraciones que pueden agruparse en seis vías esenciales: 1. La adquisición de señales de crecimiento autosuficientes o autónomas; 2. Insensibilidad a las señales inhibidoras del crecimiento. 3. Resistencia a las señales de apoptosis. 4. Potencial de proliferación ilimitado. 5. Angiogénesis sostenida, invasión y metástasis (4,5).
Cada una de estas vías está regulada por otros conjuntos de sub-rutas que interactúan, lo que resulta en redundancia y complejidades adicionales. A pesar de esto, algunas aberraciones moleculares son más propensas que otras a influir en el comportamiento clínico de un cáncer, incluido el riesgo de metástasis. Dichas aberraciones, una vez identificadas, podrían servir como marcadores de pronóstico (6).
Estos marcadores pueden estar representados potencialmente por cambios en el número de copias de genes, expresión de ARN mensajero (ARNm) o niveles de expresión de proteínas. La inmunohistoquímica (IHQ) es un método práctico que permite localizar antígenos específicos en tejidos o células basadas en el reconocimiento antígeno-anticuerpo; busca explorar la especificidad proporcionada por la unión de un anticuerpo con su antígeno a nivel de microscopía óptica evaluando los cambios en la expresión de proteínas en histopatología, proporciona una evaluación semicuantitativa de la abundancia de proteínas y también define la localización celular de la expresión. Estas consideraciones han llevado al uso extensivo de IHQ para la valoración pronostica y predictiva en el cáncer (7).
Un factor pronóstico generalmente se define como un factor medido antes del tratamiento, que tiene un impacto en el resultado del paciente "independientemente" del tratamiento recibido o de la clase general de tratamiento, mientras que un factor predictivo es un factor que se espera que pueda identificar a los pacientes que se beneficiarán de un tratamiento específico (8).
El gen con las mutaciones más frecuentes en carcinomas de células no pequeñas es el EGFR (receptor del factor de crecimiento epidérmico), se sobre-expresa con frecuencia en el 40 %-80 % de los casos CPCNP, cumple una función importante en la supervivencia y proliferación de las células tumorales, es un receptor miembro de la familia tirosina quinasa (TK) que posee una acción esencial en el desarrollo y la progresión del carcinoma de células no pequeñas (4,5). Se ha informado que las vías de señalización de EGFR podrían influir en la angiogénesis, activación y regulación de la proliferación celular. Diversos estudios en la actualidad sugieren que el estado mutante del EGFR puede ser un factor predictivo para la respuesta a la quimioterapia citotóxica y el pronóstico de pacientes con carcinoma pulmonar de células no pequeñas (CPCNP) avanzado (9)
Por otra parte, el gen del receptor de la tirosina quinasa del linfoma anaplásico (EML4-ALK) se ha identificado como un potente controlador oncogénico en el CPCNP, en particular ADC. Define un subgrupo único de ADC pulmonar, que puede responder a los inhibidores de ALK (proteína de linfoma anaplásico) (10).
EGFR y ALK son importantes impulsores oncogénicos en el cáncer de pulmón de células no pequeñas (11) así como ROS1 y KRAS(12,13). Los avances en agentes terapéuticos específicos ya han aprobado el tratamiento de pacientes con mutación EGFR y translocación ALK (14). Los primeros estudios sugirieron que las mutaciones de EGFR y los reordenamientos de ALK son mutuamente excluyentes (15). Sin embargo, se han informado casos aislados con alteraciones concomitantes de EGFR y ALK (16,17).
Un conjunto de CPCNP presenta una alteración genética por la cual evade la detección y eliminación por parte del sistema inmune a través de la expresión del ligando de muerte programada 1 (PD-L1). PD-L1 luego se une a su receptor, la proteína de muerte celular programada 1 (PD-1) e inicia una cascada de señalización que conduce al agotamiento de los linfocitos, un estado de función deteriorada de respuesta inmune adaptativa. En este contexto se ha implementado el uso de terapias inmunomoduladoras sobretodo en pacientes con fracaso a terapéutica convencional con quimioterapia con resultados prometedores (18).
Se conoce en la actualidad que la determinación por PCR en tiempo real (PCR-RT) e hibridación fluorescente in situ (FISH) de EGFR, ALK y PD-L1 constituyen un factor pronóstico y predictivo en carcinomas pulmonares de células no pequeñas sin embargo, sería de interés comprobar la eficacia de su determinación por medio de estudio IHQ siendo este un método más sencillo y menos costoso. Por tal razón, se considera imperiosa la necesidad de utilizar la IHQ como método eficaz para determinar mutaciones genéticas relacionadas a sobreexpresión de EGRF ALK y PD-L1 en carcinomas pulmonares de células no pequeñas, con el fin de comprobar su sensibilidad y especificidad lo que permitiría conocer la proporción de cada una de estas aberraciones en nuestra población. En la actualidad no existen estudios enfocados a la determinación de marcadores pronósticos y predictivos a través del método de IHQ en carcinomas pulmonares en nuestro país. En vista de esto es necesaria la realización de marcadores inmunohistoquímicos que se sobre-expresen en términos de mutaciones asociadas a carcinomas pulmonares lo que permitiría también un mejor tratamiento para nuestros pacientes y daría paso a investigaciones futuras sobre los comportamientos de estos tumores.
MÉTODO
Este estudio fue aprobado por la Comisión de Ética de la institución en el momento de la recolección y análisis de datos.
Es un estudio de tipo transversal, descriptivo, observacional. La población estuvo constituida por todas aquellas biopsias obtenidas por punción, fibro-broncoscopia o especímenes de resección quirúrgica que fueron diagnosticadas como carcinomas pulmonares en el Laboratorio de Patología del Centro Médico Docente la Trinidad en el período comprendido entre enero 2010- octubre 2020.
La muestra consistió en todos los casos con el diagnóstico de carcinoma pulmonar en el estudio histopatológico que cumplieron con los criterios de inclusión: informe de solicitud de biopsia, láminas histológicas para revisión o el bloque de parafina respectivo en el período establecido.
Se excluyeron todos aquellos casos sin material en archivo (láminas histológicas y/o bloques de parafina) y casos con material escaso para evaluación.
Se llevó a cabo una revisión exhaustiva de los archivos de biopsias pulmonares, registrados durante el período de estudio en el Laboratorio de Patología; a través de los libros de registro y sistema automatizado de registro de pacientes del Centro Médico Docente la Trinidad, además de las boletas de las solicitudes de cada una de las biopsias con sus resúmenes clínicos a fin de obtener los datos epidemiológicos y clínicos de interés para el estudio. Seguidamente, se revisaron los preparados histológicos teñidos con Hematoxilina y Eosina (HE) de cada una de las biopsias pulmonares provenientes de los diferentes centros asistenciales y que se encuentran almacenadas en el archivo. Una vez obtenidos todos los casos se procedió a realizar estudio inmunohistoquímico con EGFR, ALK y PD-L1 para su posterior análisis histológico.
Para el estudio IHC se utilizaron los siguientes anticuerpos con el respectivo kit de IHQ: 1. ALK: anticuerpo monoclonal de ratón, clon ALK1 (1), marca Dako®, se considerará positivo el inmunomarcaje citoplasmático y nuclear. 2. EGFR: anticuerpo monoclonal de ratón, clon H11, Dako®, se considerará positivo el inmunomarcaje de membrana. 3. PD-L1: anticuerpo monoclonal de ratón, clon 405-9A11, marca Diagnostic BioSystems®, se considerará positivo el inmunomarcaje de membrana.
ANÁLISIS ESTADÍSTICO
Se calcularon la media y desviación estándar de las variables contínuas. En el caso de las variables nominales se calcularán su frecuencia y porcentaje. Se utilizó la correlación de Pearson en casos determinados para obtener el valor de P.
REGISTRO DE DATOS
La recolección de datos se llevó a cabo mediante el uso de un formulario, con las variables epidemiológicas e histopatológicas. Los datos de interés para la investigación se descargaron en una base de datos conforme las variables contempladas en el estudio bajo el programa de SSPS ®(Statistical Package for the Social Science) versión 25,0.
RESULTADOS
En el laboratorio de anatomía patológica del Centro Médico Docente La Trinidad se estudiaron 29 biopsias pulmonares con el diagnóstico de carcinoma pulmonar correspondientes a diez años de estudio entre el período comprendido entre enero de 2010 y octubre de 2020. De los casos evaluados (n═29) se obtuvo información en la edad en 18 casos (62,06 %) en los cuales la edad promedio fue 67,88 años (±12,171 DE, rango 50 a 99 años) (Cuadro 1).
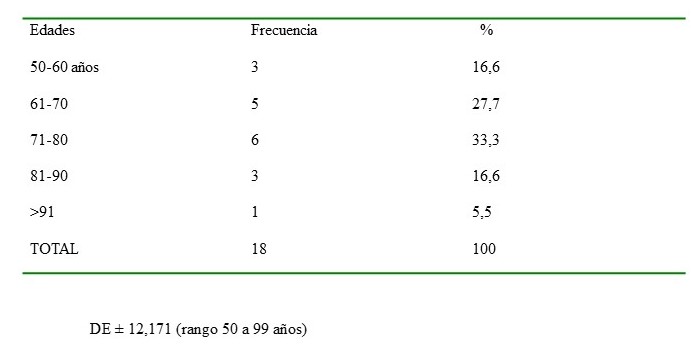
Cuadro 1.
Edades de los pacientes evaluados
En cuanto al sexo se obtuvo información de 24 casos (82,76 %) de los cuales 48,28 % fueron de sexo masculino y 34,48 % de sexo femenino.
En relación a los tipos histológicos de carcinoma el diagnóstico más común previo al estudio inmunohistoquímico fue carcinoma de células no pequeñas (23,08 %), seguido de CCE moderadamente diferenciado (15,38 %), y ADC poco diferenciado (11,54 %) Figura 1.
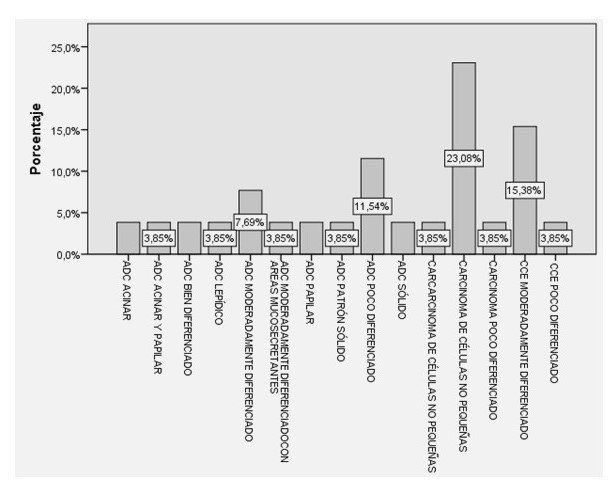
Figura 1
Tipos histológicos de carcinomas estudiados
Al determinar el inmunomarcaje con EGFR un total de 20,6 % de los casos mostraron inmunomarcaje positivo para EGFR, con casos que mostraron positividad focal 3,45 % y 17, 24 % mostraron positividad difusa, negativos 79,31 %.
Histológicamente el inmunomarcaje de EGFR mostró un patrón de tinción citoplasmático con la intensidad similar a los controles como es esperado (Figura 2).
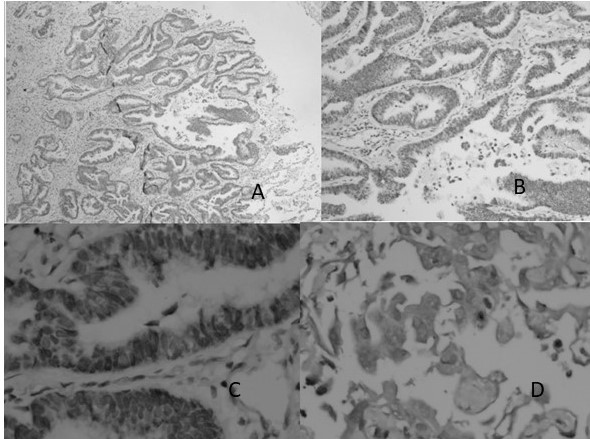
Figura 2
Caso de carcinoma positivo para EGFR: A.- 4.- ADC patrón predominantemente acinar positivo para EGFR; B.- 10X estructuras acinares revestidas por epitelio cilíndrico con expresión EGFR; C.- 40X; D.- ADC poco diferenciado positivo para EGFR.
La positividad para ALK se observó en 24,13 % de los casos, de este total 10,34 % expresaron positividad focal. En el material revisado la mayor parte de los casos positivos mostraron expresión citoplasmática fuerte y 3 casos observados mostraron inmunomarcaje focal de menor intensidad 10,34 pos focal, 13,70 % positivos y 75, 86 % negativos.
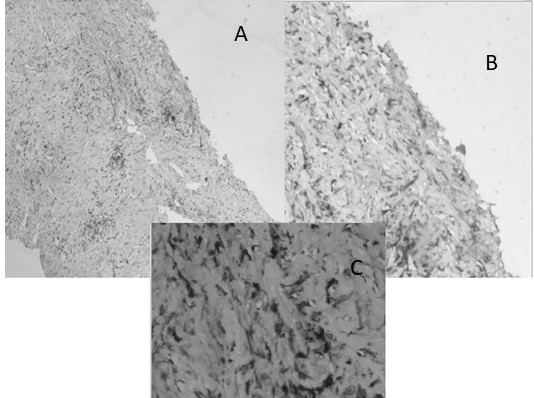
Figura 3
Caso de carcinoma de pulmón ALK positivo: A.- La lesión muestra poca diferenciación 4X IHQ; B y C: las células son fuertemente positivas para ALK IHQ 10X y 40X
Un mayor número de casos mostraron reactividad para PD-L1, siendo positivo en 34,48 % de los casos. Mostrando positividad fuerte difusa en 24,14 % y focal en 10,34 %, negativo 65,52 %
Los casos evaluados como positivos expresaron en su mayoría una tinción de fuerte 3+ a positiva moderada 2+. Se observó en algunos casos patrón de tinción de interfaz y patrones positivos focales aun considerándose positivo. Todos los casos positivos presentaron positividad en más del 1 % de las células tumorales (Figura 4).
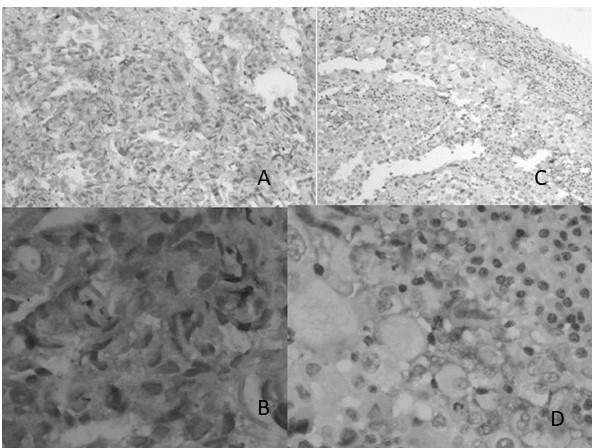
Figura 4.
Casos con expresión PD-L1: A y B Carcinoma poco diferenciado positivo para PD-L1 4X y 40X IHQ; C y D Carcinoma adenoescamoso con inmunomarcaje fuerte de membrana de interfaz tumor- células inmunes.
Al correlacionar la expresión de estos tres anticuerpos (ALK, EGFR, PD-L1), la expresión de EGFR está relacionada positivamente con la expresión de ALK y PD-L1 con valores significantemente estadísticos (menor a 0,05) (Cuadro 2)
Por otra parte la expresión de ALK presentó asociación positiva con la expresión de EGFR con valor de P menores a 0,05 y la expresión de PD-L1 tuvo asociación positiva con la expresión de EGFR sin embargo, no tuvo asociación con la expresión de ALK (Cuadro 2)
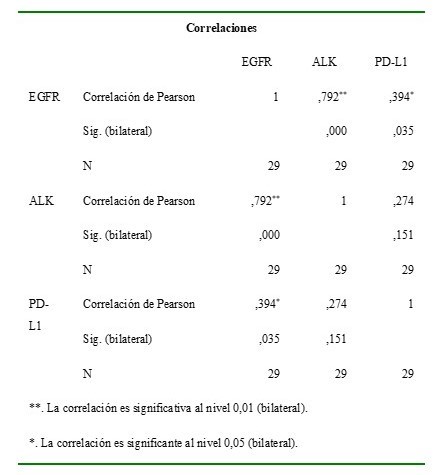
Cuadro 2.
Correlación de expresión de los tres anticuerpos
El inmunomarcaje para EGFR no mostró preferencia por algún tipo histológico (Cuadro 3), al igual que ALK (Cuadro 4). Sin embargo, el marcaje para PD-L1 presentó preferencia por ADC poco, ADC moderadamente diferenciado y CCE moderadamente diferenciado con 3 casos cada uno (Cuadro 5).
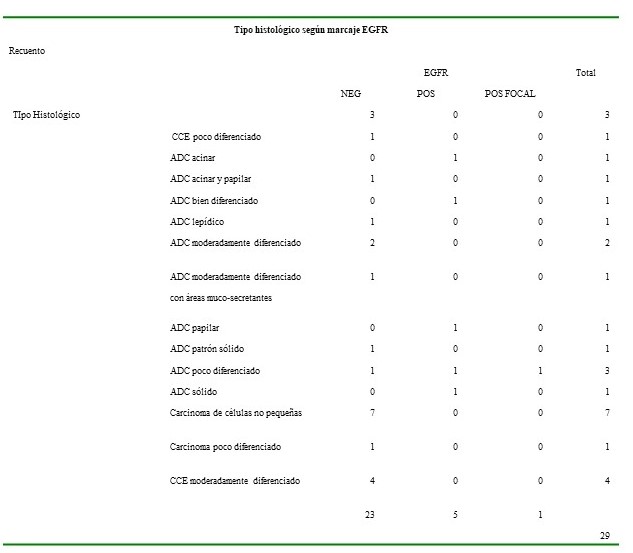
Cuadro 3
Relación tipo histológico- EGFR
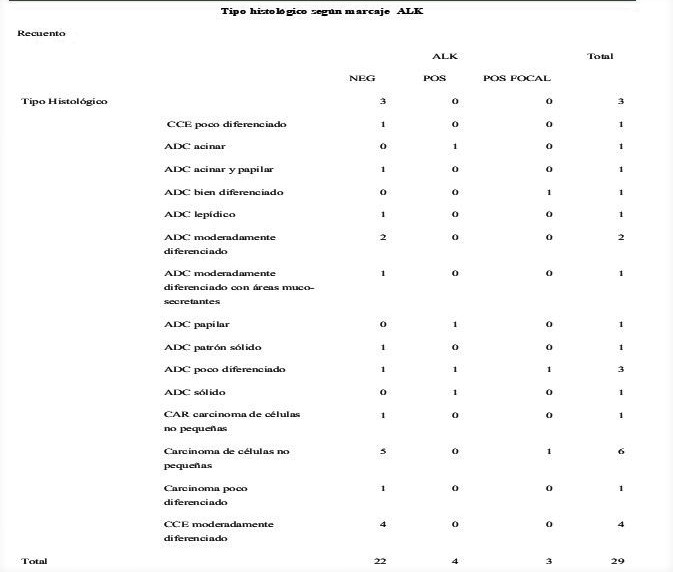
Cuadro 4.
Relación tipo histológico-ALK
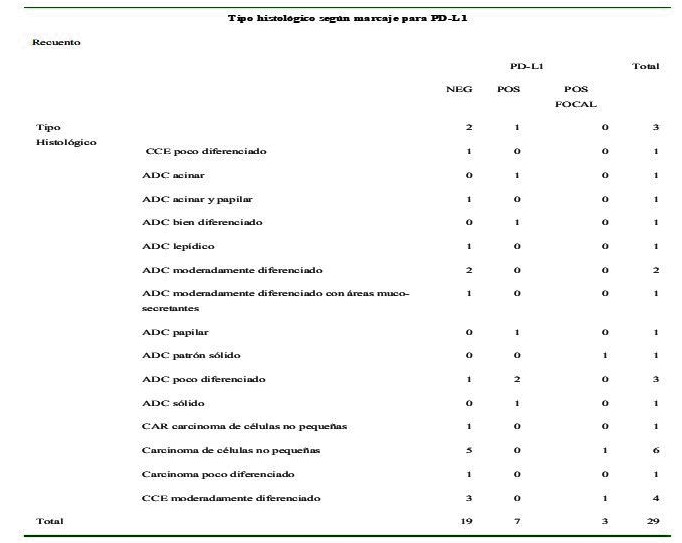
Cuadro 5.
Relación tipo histológico- PDL1
Siendo el tipo histológico diagnosticado con más frecuencia el CCNP se correlacionó el tipo histológico con la expresión de estos tres anticuerpos no se encontró relación significativa de estas cuatro variables (Cuadro 6).
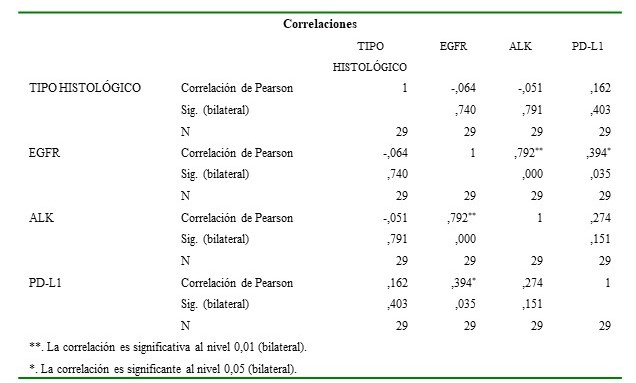
Cuadro 6.
Correlación EGFR, ALK, PD-L1 y tipo histológico
DISCUSIÓN
El cáncer de pulmón es la principal causa de muerte relacionada a cáncer en el mundo (1,2). Se estima que la tasa de supervivencia a los 5 años de pacientes con carcinomas de células no pequeñas es de 17,8 % (19). En el sexo masculino se ha reportado la sobrevida entre 6 % a 14 % y en el femenino entre 7 % a 18 % (20).
En Venezuela, el comportamiento de cáncer de pulmón ha venido presentando un crecimiento a través de los años, en el último boletín de la Sociedad Anticancerosa se observó un incremento en la mortalidad por cáncer de pulmón en pacientes masculinos en los últimos años apenas siendo superado en mortalidad por el cáncer de próstata, en base a lo anterior el cáncer de pulmón es un importante problema de salud pública en el que el rol del patólogo es importante para el diagnóstico adecuado, lo que trae consigo el tratamiento idóneo considerando las pautas establecidas por la OMS las cuales presentan un nuevo enfoque terapéutico y pronóstico (21).
En el presente estudio se estudiaron un total de 29 casos de carcinoma pulmonar de los cuales se evidenció que la edad promedio fue 67 años con un rango entre 50 y 99 años. Se tiene una percepción de que existe un incremento en la incidencia del carcinoma pulmonar así como modificaciones en cuanto a su epidemiología. Vercosa y col. (22) estudiaron un total de 27 pacientes con el diagnóstico de carcinoma broncogénico de los cuales el grupo etario más afectado fue de 40 a 49 años siendo el grupo etario afectado menor a nuestro estudio a pesar de ser una población latinoamericana; sin embargo, Tsao y col. (23) estudiaron una población más amplia constituida por 575 pacientes encontrando la edad promedio entre 55 y 64 años ; por otra parte Yoshizawa y col. (24) estudiaron 514 pacientes con diagnóstico de carcinoma pulmonar estadio I encontrando como edad promedio de 69 años (33-89 años) en ambos estudios la edad media afectada es similar a la encontrada en nuestra población, aunque Vercosa y col., tuvieron un número de casos similar (22).
En cuanto al sexo se obtuvo información de 24 casos (82,76 %) de los cuales 48,28 % fueron de sexo masculino y 34,48 % de sexo femenino lo que coincide con la teoría muchas veces planteada del cáncer de pulmón como una patología del sexo masculino. Machado y col. (19) realizaron un estudio en el Instituto Anatomopatológico de la UCV obteniendo de igual forma una presentación más frecuente en el sexo masculino con 83 casos (58,9 %) y 58 (41,1 %) del sexo femenino. Dhanasekar y col. (25) en su estudio de reclasificación de carcinomas pulmonares encontraron el género masculino más afectado frente al sexo femenino con 63 % y 37 % de los casos respectivamente notando que la cifra era 2:1 35; por otra parte este hallazgo difiere de Vercosa y col. (22) quienes encontraron el sexo femenino como más afectado con 17 pacientes (62,9 %) y 10 pacientes masculinos (37 %).
Previo al estudio inmunohistoquímico los tumores fueron planteados como es de esperarse en su mayoría como carcinoma de células no pequeñas (23,08 %) diagnóstico genérico previo a la diferenciación IHQ, seguido de CCE moderadamente diferenciado (15,38 %), y ADC poco diferenciado (11,54 %). Esto difiere en un estudio para reclasificación de Sánchez y col. (26) quienes obtuvieron como diagnóstico más común ADC (61,6 %), seguido del CCE (30,3 %), carcinoma neuroendocrino (5,4 %) y carcinoma sin especificar (1,5 %), difiere también de Shin y col. (27) estudiaron 230 casos con diagnóstico de carcinomas de pulmón siendo más frecuente el diagnóstico de ADC 63 %, seguido de CCE 37 % (11), aunque nuestro resultado es similar a Pradhan y col. (28) quienes realizaron un estudio clínico-patológico de 55 casos de carcinomas pulmonares reportando el CCE como el tipo más frecuente con 63,6 % de los casos.
La positividad para EGFR se observó en 20,6 %, el 3,45 % mostraron positividad focal y 17,24 % mostraron positividad difusa este hallazgo fue similar a Verdu (29) y col., quienes determinaron el estado mutacional EGFR mediante el estudio inmunohistoquímico obteniendo 22 % de los casos como positivos, en este estudio se hizo comparación con estudios moleculares obteniendo con uno de los anticuerpos utilizados (E746_A750) un valor predictivo positivo del 100 % con lo cual se puede reducir el uso de estudios moleculares considerándose la IHQ como una herramienta de cribado inicial. Sin embargo, fue distinto al estudio realizado por Hong kim y col. (30) y Hofman (31) y col., quienes obtuvieron en una muestra de 154 pacientes con CPCNP mutación EGFR en 62 pacientes (40,3 %) con un valor predictivo positivo de 94,5 % y 41 % de 151 casos concluyendo ambos estudios con que la IHQ es un medio específico para la identificación de mutaciones de EGFR. Aunque nuestro estudio no incluye comparaciones con cribado de biología molecular es un punto de partida para futuras comparaciones, tomando en cuenta que obtuvimos similar proporción de positividad EGFR a otros estudios Verdu y col. (29)
El reordenamiento ALK determinado por IHQ se observó en 24,13 % de los casos cifra similar a Hofman (31) y col., quienes obtuvieron 20 % de casos positivos en una población de 20 tumores sin embargo difiere de Zhou y col., (32) que obtuvieron apenas 8,4 % de casos positivos de 368 casos, este último estudio concluye que aquellos casos con marcaje débil deben considerarse como equívocos siendo necesario el complemento con FISH, por otra parte se plantea que cuando se obtiene un inmunomarcaje fuerte granular citoplasmático no es necesaria la confirmación por una segunda técnica. Aun en la actualidad el papel del FISH para determinar reordenamiento ALK como método estándar es discutido por motivos técnicos y patrones complejos por lo que este estudio plantea la posibilidad del uso de IHQ como un método económico que puede utilizarse como inicial o en casos de tinción fuerte como único método.
Se obtuvo expresión de PD-L1 en 34,48 % de los casos difiere de un estudio realizado O' Malley y col. ( 33) con 4 anticuerpos distintos evidenciando positividad de PD-L1 en 54 % y 69,6 % aunque en poblaciones más numerosas (530 y 733 casos), en los patrones de marcaje algo observado con frecuencia en este estudio fue el patrón de interfaz con células inmunes y tumorales positivas para este anticuerpo, este patrón de marcaje es dado a efecto de la interacción directa entre los antígenos de las células tumorales y la regulación positiva de la expresión de PD-L1 por las células inmunes adyacentes. De esta misma manera un hallazgo particular en nuestro estudio fue la presencia de dos casos de carcinomas adenoescamoso con positividad fuerte para este anticuerpo, según O' Malley y col. ( 33) los casos de carcinomas adenoescamoso son estadísticamente distintos a carcinomas poco diferenciados mostrando en su población una positividad de 43,9 % vs. 36 %, siendo este grupo de tumores uno de los que presentó mayor expresión de PD-L1 superándose por lesiones encontradas en otras localizaciones (timomas y linfomas). Hirsch y col. (34) revisaron 39 casos de CPCNP obteniendo el 50 % de los casos positivos, a pesar de que nuestro estudio mostró un porcentaje menor, en este estudio el porcentaje de expresión varía de acuerdo al anticuerpo utilizado, cabe destacar que no existen estudios comparativos con nuestro anticuerpo. En otro estudio de Tsao y col. (35) compararon rendimiento de tres distintos anticuerpos PD-L1 obteniendo positividad que varía del 14,3 % al 32,2 % en 982 pacientes cifras comparables a las obtenidas por nosotros, sin embargo, con otro clon PD-L1. En este estudio se concluye que la determinación PD-L1 puede ser de valor predictivo en paciente con CPCNP, excepto si se encuentran en estadio temprano de la enfermedad.
Se observó una correlación estadísticamente significativa entre la expresión IHQ para mutación de EGFR, reordenamiento ALK y expresión PD-L1 obteniendo tumores que albergan dos mutaciones impulsoras y sobreexpresión de PD-L1 tal como plantea Yoneshima y col., es necesario estudios para validar el beneficio de inmunoterapia en estos pacientes (36).
La co-expresión EGF y ALK presentó asociación positiva Azuma y col., sugirieron que la alta expresión de PD-L1 se asocia con la presencia de mutaciones de EGFR en CPCNP resecado quirúrgicamente y es un factor pronóstico negativo independiente para esta enfermedad (37).
Determinamos correlación entre la mutación EGFR y ALK a través de IHQ en donde se observó asociación positiva a pesar que estas mutaciones son consideradas como mutuamente excluyentes en un 15,4 % de los casos se puede observar esta asociación, esto tiene importancia terapéutica porque se ha observado que el uso de inhibidores ALK ha presentado eficacia en estos pacientes (38). Yang y col., revisaron 977 casos de CPCNP y obtuvieron esta asociación en 3.9 %. (39).
Existen estudios que reportan mayor expresión de PD-L1 en adenocarcinomas de patrón predominantemente acinar y sólido Miyazawa y col., y se considera que en general el tipo histológico más frecuentemente PD-L1 positivo es el adenocarcinoma (40). En nuestro caso la expresión PD-L1 estuvo asociada tanto a ADC como a CCE con la misma frecuencia.
En conclusión este estudio plantea el uso de inmunohistoquímica como una opción más accesible y sencilla para el cribado inicial de determinación para mutaciones EGFR, reordenamientos ALK, y sobreexpresión PD-L1 planteándose incluso como una opción para reemplazar los métodos de biología molecular en algunas circunstancias, ayudando a dar un mejor uso a esta técnica. Se obtuvieron estadísticas similares a otros estudios realizados con FISH para frecuencia de cada una de estas mutaciones. Morfológicamente el inmunomarcaje para PD-L1 es heterogéneo, por lo tanto es necesario que el patólogo conozca cada uno de estos patrones para el adecuado reporte. Se conoce que estas tres alteraciones pueden coexistir en un porcentaje de casos por lo que no se puede desestimar esta premisa.
Es necesario en todos los casos de carcinomas de pulmón de células no pequeñas sea realizado IHQ con EGFR, ALK y PD-L1, aunque la literatura considera imperativa un panel que además incluya ROS1, BRAF, KRAS, PIK3CA con el objetico pronóstico y terapéutico por lo cual recomendamos su realización. Se recomienda realizar estudios futuros para la comparación de estos clones frente al estudio de biología molecular.
La principal limitación de nuestra investigación fue la ausencia de bloques de parafina necesarios para realizar el estudio, esto se debe a que los bloques son extraídos por los pacientes para realizar biología molecular o que se trata de material de revisión. De 181 casos apenas tuvimos acceso a 29. Se tuvo limitación para obtener datos clínico-epidemiológicos de los pacientes por falta de boleta o ausencia de información clínica en la misma. Por tratarse de muestras en su mayoría transbronquiales el material al momento de realizar el estudio era escaso o se encontraba agotado por lo que se excluyeron dichos casos.
REFERENCIAS
1. Organización Mundial de la Salud. Perfiles oncológicos en los países 2014.Venezuela. [Consultado 6 de abril de 2017]. Disponible en: URL: http://www.who.int/cancer/country-profiles/es/.
2. Zugazagoitia J, Belen A, Nuñez J, Iglesias L, Ponce S. The new IASLC/ATS/ERS lung adenocarcinoma classification from a clinical perspective: Current concepts and future prospects. J Thorac Dis. 2014;6(5): 526-536.
3. Hanahan D, Weinberg R. The hallmarks of cancer. Cell. 2000;100(1):57-70.
4. Sieber O, Heinimann K, Tomlinson I. Genomic instability--The engine of tumorigenesis? Nat Rev Cancer. 2003;3(9):701-708.
5. Zhu Q, Shih W, Ling C, Tsao M. Immunohistochemical markers of prognosis in non‐small cell lung cancer: A review and proposal for a multiphase approach to marker evaluation. J Clin Pathol. 2006;59(8): 790-800.
6. Paesmans M. Prognostic and predictive factors for lung cancer. Breathe. 2012;9(12):112-121.
7. Grinberg M, Djureinovic D, Brunnstrom H, Hengstler G, Mattsson J, Edlund K, et al. Reaching the limits of prognostication in non-small cell lung cancer: An optimized biomarker panel fails to outperform clinical parameters. Mod Pathol. 2017;30(1) 964-977.
8. Nicolson R, Gee J, Harper M. EGFR and cancer prognosis. Eur J Cancer. 2001;37(Supl 4):S9-15.
9. Lonardo F, Dragnev K, Freemantle S, Ma Y, Memoli N, Sekula D, et al. Clin Cancer Res. 2002;8(1):54-60.
10. Fang S, Wang Z. EGFR mutations as a prognostic and predictive marker in non-small-cell lung cancer. Drug Des Devel Ther. 2014;26(8):1595-1611.
11. Bergethon K, Shaw A, Ou S, Katayama R, Lovly C, McDonald N, et al. ROS. rearrangements define a unique molecular class of lung cancers. J Clin Oncol. 2012; 30(8):863-870.
12. Santos E, Martin-Zanca D, Reddy E, Pierotti M, Della P, Barbacid M. Malignant activation of a K-ras oncogene in lung carcinoma but not in normal tissue of the same patient. Science. 1984;223(4637):661-664.
13. Lindeman N, Cagle P, Beasley M, Chitale D, Dacic S, Giaccone G, et al. Molecular testing guideline for selection of lung cancer patients for EGFR and ALK tyrosine kinase inhibitors: Guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. Arch Pathol Lab Med. 2013;137(6):828-860.
14. Gainor J, Varghese A, Ou S, Kabraji S, Awad M, Katayama R, et al. ALK rearrangements are mutually exclusive with mutations in EGFR or KRAS: An analysis of 1,683 patients with non-small cell lung cancer. Clin Cancer Res. 2013; 19(15):4273-4281.
15. Kono S, Flacco A, Tan A, Doebele R, Zhou Q, Crino L, et al. Optimizing the detection of lung cancer patients harboring anaplastic lymphoma kinase (ALK) gene rearrangements potentially suitable for ALK inhibitor treatment. Clin Cancer Res. 2010;16(22):5581-5590.
16. Yang J, Zhang X, Su J, Xu C, Zhou Q, Tian H, et al. Lung cancers with concomitant EGFR mutations and ALK rearrangements: diverse responses to EGFR-TKI and crizotinib in relation to diverse receptors phosphorylation. Cancer Res. 2014;20(5):1383-1392.
17. Herbst RS, Shin D. Monoclonal antibodies to target epidermal growth factor receptor-positive tumors: A new paradigm for cancer therapy. Cancer. 2002; 94(5):1593-1611.
18. Grigg C, Rizvi N. PD-L1 biomarker testing for non-small cell lung cancer: Truth or fiction? J Immunother Cancer. 2016;4:48.
19. Machado A. Carcinoma broncogénico: estudio histológico e inmunohistoquímico (período 2006-2010). [Trabajo de ascenso]. Caracas: Instituto Anatomopatológico "Dr. Jose A O` Daly", Universidad Central de Venezuela; 2010.
20. Tang E, Schreiner A, Bradley B. Advances in lung adenocarcinoma classification: A summary of the new international multidisciplinary classification system (IASLC/ATS/ERS). J Thorac Dis. 2014;(Supl 5):S489-550.
21. Sociedad Anticancerosa de Venezuela. Boletín de incidencia y mortalidad del cáncer basado en los datos del informe pronósticos de la mortalidad e incidencia de cáncer en Venezuela, año 2017. [Consultado 10 de octubre de 2020]. Disponible en: URL: https://www.cancervenezuela.org/descargas/boletin-incidencia-mortalidad-cancer-informe-pronosticos-mortalidad-venezuela-2017.pdf
22. Vercosa C, Gutierrez L. 11º Congreso ALAT: Incidencia y caracterización del cáncer. Disponible en: URL: https://www.archbronconeumol.org/index.php?p=revista&tipo=pdf-simple&pii=X0300289618627112.
23. Tsao M, Marguet S, Le Teuff G, Lantuejoul S, Sheperd F, Seymour L, et al. Subtype classification of lung adenocarcinoma predicts benefit from adjuvant chemotherapy in patients undergoing complete resection. J Clin Oncol. 2015;33(30):3439-3446.
24. Yoshizawa A, Motoi M, Riely G, Sima S, Gerald W, Kris MG, et al. Impact of proposed IASLC/ATS/ERS classification of lung adenocarcinoma: Prognostic subgroups and implications for further revision of staging based on analysis of 514 stage I cases. Mod Pathol. 2011;24(5):653-664.
25. Dhanasekar T, Duvooru P, Shankar S, Thanasekaran V. Clinic-pathological and immunohistochemical profile of non-small cell lung carcinoma in a tertiary care medical centre in South India. Lung India. 2014;31(1):23-28.
26. Sánchez R, Machado A. Carcinoma pulmonar estudio clínico-patológico. Rev Venez Oncol. 2021;33(1):11-32.
27. Shin B, Shin S, Chung M, Lee H, Koh W, Kim H, et al. Different histological subtypes of peripheral lung cancer based on emphysema distribution in patients with both airflow limitation and CT-determined emphysema. Lung Cancer. 2017;104(1):106-110.
28. Pradhan S, Shakya S, Shrestha S. Clinic-pathological study of lung carcinoma. J Pathol Nep. 2014;4 (8):623 -625.
29. Verdu M, Triasa I, Romanb R, Rodonb N, Pubil C,Calvo M, et al. EGFR mutations in lung cáncer. Rev Esp Patol. 2016;49 (4):226-233.
30. Hong Kim C, Hoon Kim S, Youngju Park S, Jinyoung Yoo, Kyoung Kim S, Hoon Kyo Kim Identification of EGFR Mutations by immunohistochemistry with EGFR mutation–specific antibodies in biopsy and resection specimens from pulmonary adenocarcinoma. Cancer Res Treat. 2015;47(4):653-660.
31. Hofman P, Ilie M, Hofman V, Roux S, Valent A, Berheim A, et al. Immunohistochemistry to identify EGFR mutations or ALK rearrangements in patients with lung adenocarcinoma. Ann Oncol. 2012;23(7):1738-1743.
32. Zhou J, Zhao j, Bo Wang K, Wang L, Chen X, Zheng J, et al. Accurate and economical detection of ALK positive lung adenocarcinoma with semiquantitative immunohistochemical screening. PLoS ONE. 2014;9(3):e92828
33. O’Malley1 D, Yang Y, Boisot S, Sudarsanam1, Wang J, Chizhevsket V, et al. Immunohistochemical detection of PD-L1 among diverse human neoplasms in a reference laboratory: Observations based upon 62,896 cases. Mod Pathol. 2019;2(9):929-942.
34. Hirsch FR, McElhinny A, Stanforth D, Ranger-Moore J, Jansson M, Kulangara K, et al. PD-L1 Immu-nohistochemistry assays for lung cancer: Results from Phase 1 of the“Blueprint PD-L1 IHC assay comparison project” J Thorac Oncol 2017;12:208-222.
35. Tsao M, Teuff L, Shepherd JP, Hainot P, Filipits M, Pirker R, et al. PD-L1 protein expression assessed by immunohistochemistry is neither prognostic nor predictive of benefit from adjuvant chemotherapy in resected non-small cell lung cancer. Ann Oncol. 2017;28(4): 882-889.
36. Yoneshima Y, Ijich Ki, Anai S, Keiichi O, Otsubo K, Iwama E, et al. PD-L1 expression in lung adenocarcinoma harboring EGFR mutations or ALK rearrangements. Lung Cancer. 2018;118(5):36-40.
37. Azuma K, Ota K, Kawahara A, Hattori S, Iwama E, Harada T, et al. Association of PD-L1 overexpression with activating EGFR mutations in surgically resected non-small-cell lung cancer. Ann Oncol. 2014;25(10):1935-1940.
38. Won J, Keam B, Koh J, Cho J, Jeon I, Kim D, et al. Concomitant ALK translocation and EGFR mutation in lung cancer: A comparison of direct sequencing and sensitive assays and the impact on responsiveness to tyrosine kinase inhibitor. Ann Oncol. 2015;26(2):348-354.
39. Yang J, Zhang X, Jian Su, Chong-Rui X, Zhou Q, Hong-Xia Tian, et al. Lung cancers with concomitant EGFR mutations and ALK rearrangements: Diverse responses to EGFR-TKI and Crizotinib in relation to diverse receptors phosphorylation. Clin Cancer Res. 2014;20(5):1383-1392
40. Miyazawa T, Marushima H, Saji H, Kojima K, Hoshikawa M, Takagi M, et al. PD-L1 Expression in non-small-cell lung cancer including various adenocarcinoma subtypes. Ann Thorac Cardiovasc Surg. 2019;25:1-9.
Notas de autor
sanchitarut@gmail.com