FISIOTERAPIA EN EL LINFEDEMA. EXPERIENCIA DE 13 AÑOS, REPORTE DE DOS CASOS
FISIOTERAPIA EN EL LINFEDEMA. EXPERIENCIA DE 13 AÑOS, REPORTE DE DOS CASOS
Revista Venezolana de Oncología, vol. 34, núm. 4, pp. 204-211, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 3.0 Internacional.
Recepción: 31 Marzo 2022
Aprobación: 30 Junio 2022
Resumen: El linfedema es un efecto adverso, latente del tratamiento del cáncer de mama. Es la complicación menos atendida, a menudo sin tratamiento y más discapacitante de esta entidad. Entre los factores de riesgo asociados con el desarrollo de linfedema, están la extensión de la disección ganglionar axilar, la radioterapia, las infecciones y la obesidad. OBJETIVO: Presentar la experiencia fisioterapéutica de 13 años, de dos pacientes, quienes presentaron linfedema posmastectomía. CASO CLÍNICO 1. Paciente femenina de 47 años de edad, con diagnóstico de carcinoma lobulillar infiltrante en mama derecha. Recibió quimioterapia neo- adyuvante, posteriormente se le realizó mastectomía radical derecha. Recibió radioterapia. Evaluada por fisioterapia, presentando linfedema de 10 cm en miembro superior derecho (mano y antebrazo) CASO CLINICO 2. Paciente femenina de 50 años de edad, con diagnóstico de adenocarcinoma ductal infiltrante grado IIB. Se le realizó mastectomía radical modificada + reconstrucción inmediata. Posteriormente recibió, quimioterapia, radioterapia y tratamiento hormonal. Evaluada por fisioterapia, presentando linfedema de 19 cm en miembro superior izquierdo (mano antebrazo y brazo.) CONCLUSIONES: Después de 13 años de tratamiento y seguimiento del linfedema, las pacientes mostraron una disminución del volumen de linfa a mediano y a largo plazo, mejorando la funcionalidad del brazo y su calidad de vida. Cimentado en dos pilares fundamentales: educación sanitaria y la aplicación del método triada terapéutica.
Palabras clave: Cáncer de mama, linfedema, factores de riesgo, prevención, tratamiento..
Abstract: The lymphedema is an adverse, latent effect of the breast cancer treatment. It is the least attended often untreated and most disabling complication of this entity. The risk factors associated with the development of lymphedema include axillary lymph node dissection, radiation therapy, infections, and the obesity. OBJECTIVE: To present the 13 year physiotherapeutic experience in two patients who presented with lymphedema postmastectomy. CLINICAL CASE 1. Patient 47 year old female was diagnosed with infiltrating lobular carcinoma of the right breast. The patient received neoadjuvant chemotherapy, and subsequently underwent radical right mastectomy. She received radiotherapy. Evaluated by physiotherapy, presenting lymphedema of 10 cm in the right upper limb (hand and forearm) CLINICAL CASE 2. 50 year old female patient, diagnosed with infiltrating ductal adenocarcinoma grade IIB. She underwent modified radical mastectomy + immediate reconstruction. Subsequently she received chemotherapy, radiotherapy and hormonal treatment. She was evaluated by physiotherapy, presenting lymphedema of 19 cm in left upper limb (hand, forearm and arm). CONCLUSIONS: After 13 years of treatment and follow up of the lymphedema, the patients showed a decrease in the volume of lymph in the medium and long term, improving the functionality of the arm and their quality of life. They results built on two fundamental pillars: The health education and the application of the therapeutic triad method.
Keywords: Breast cancer, lymphedema, risk factors, prevention, treatment.
INTRODUCCIÓN
La mayoría de los cánceres de mama son tumores epiteliales que se desarrollan a partir de las células que recubren los conductos o los lobulillos y se dividen en carcinomas in situ y cánceres invasores. - Carcinoma ductal in situ (CDIS) de la mama representa un grupo heterogéneo de lesiones confinadas en los ductus y lobulillos mamarios, sin atravesar la membrana basal (1) - Carcinoma lobulillar in situ (CLIS): hay 2 tipos: clásico y pleomorfos. El CLIS clásico no es maligno, pero aumenta el riesgo de desarrollar carcinoma invasor en cualquiera de las mamas. El CLIS pleomorfo se comporta más como CDIS, debe ser extirpado con márgenes negativos (2).
El linfedema es un efecto adverso latente del tratamiento del cáncer de mama, a menudo sin tratamiento, con consecuencias físicas, psicológicas y deterioro funcional más discapacitante de esta entidad. Es causado por la acumulación del flujo linfático debido a la obstrucción parcial de los vasos o ganglios linfáticos a nivel axilar. Entre los factores de riesgo están la extensión de la disección ganglionar axilar, a mayor número de ganglios extirpados mayor es la probabilidad de linfedema (3,4,5,6) seguido por la radioterapia (3,6,7,8).
También puede ser producido por infecciones, principalmente bacterias (9,10); la quimioterapia basada en taxanos (3), la obesidad (3,4, 8,10,11) y la edad (8,11). Otros factores, son las complicaciones en el posoperatorio inmediato (seromas (6,11), hematomas (6), necrosis cutánea, infecciones de la herida quirúrgica (6,11) y cicatrices constrictivas). Aunado a la falta de información sobre las medidas higiénicas del brazo, la detección tardía y la falta de tratamiento.)
La literatura reporta diferentes clasificaciones del linfedema basados en la clínica, la etiología, la topografía, la edad de inicio y otros aspectos. Este estudio tomó el estadiaje del linfedema de la International Society of Lymphology (ISL.) Estadio 0: condición subclínica o latente. No hay edema evidente, pero el transporte linfático esta alterado. Estadio 1. Hay acumulación de líquido proteináceo que desaparece con la elevación de la extremidad. Estadio 2. Temprano: la elevación del miembro por sı solo no reduce el linfedema y la depresión del edema con fóvea todavía es manifiesta. Estadio 2. Tardío: consistencia tisular duro-elástica. No deja fóvea, la fibrosis del tejido es cada vez más evidente. Estadio 3. Elefantiasis linfostática.
El tejido es duro (fibrosis) Aparecen cambios tróficos en la piel (engrosamiento, acantosis, depósitos de grasa, crecimiento verrugoso y papilomatosis) (12).
Según la severidad se distinguen tres grados. Grado 1: leve. La diferencia en la circunferencia es de 2 cm - 3 cm. Grado 2: moderado. La diferencia en la circunferencia es de 4 cm- 6 cm. Grado 3: grave. La diferencia en la circunferencia es mayor de 6 cm (13).
Este trabajo tiene como objetivo presentar la experiencia fisioterapéutica de dos casos clínicos con linfedema posmastectomía, durante 13 años de tratamiento y seguimiento.
CASO 1
Paciente femenina de 47 años de edad, con diagnóstico de carcinoma lobulillar infiltrante asociado a fibromatosis en mama derecha T2 N1 M0 estadio IIB. RE – RP – HER2 – KI67 baja, fenotipo triple negativo. Recibió quimioterapia neoadyuvante con el siguiente esquema taxotere, adriamicina ciclofosfamida. El día 06/08/07 cumplió tercer ciclo. En estudio de mamografía y eco mamario se evidencia que no hay disminución del tamaño de la lesión. Por lo que se indica cambio de esquema de tratamiento vinorelbina más gemcitabina. El 14/11/2007 cumplió tercer ciclo. En diciembre de 2007 se le realizó mastectomía radical derecha. Negativo para receptores de estrógenos y progesterona. Cerb2: negativo. Ki-67: actividad proliferativa baja. Recibe radioterapia externa en un acelerador lineal a pared costal y áreas de drenaje ganglionar con fraccionamiento de 150 cGy en 40 sesiones, dosis total 6 040 cGy desde el 29/01/2008 hasta el 13/03/2008.
Evaluada por fisioterapia en octubre de 2008, con un peso de 65 kg y talla: 1,67. Presentó linfedema de 10 cm en miembro superior derecho (MSD). Segmentos comprometidos mano: 5 cm y antebrazo: 5 cm (Cuadro1). Signo de fóvea positivo en mano, piel en buenas condiciones generales, aumento de la temperatura local (37,8°C) debilidad y limitación funcional en mano, con dificultad para realizar actividades de la vida diaria (AVD) de higiene y vestido. Dificultad en actividades que requieren la prensión y pinza. Tiempo de aparición del linfedema, diez meses después de la mastectomía. Entre los factores de riesgos presente están: 9 ganglios linfáticos resecados, 3 ganglios positivos, 40 sesiones de radioterapia externa.
En mayo de 2012, se le realizó ooforectomía bilateral + histerectomía (fibromatosis uterina.)
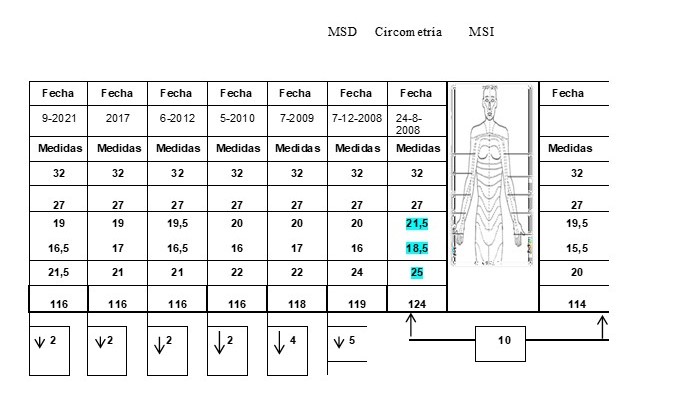
Cuadro 1
Caso 1. Circometría. Medición de los perímetros de MSD
CASO 2
Paciente femenina de 50 años de edad, con diagnóstico de adenocarcinoma ductal infiltrante T2N1MO estadio IIB, con infiltración lobulillar, componente ductal in situ focal, sin invasión vascular linfática o perineural RE+ RP+ HER2 (–) KI67 5 % fenotipo Luminal A.
En febrero 2006 se le realizó mastectomía radical modificada + reconstrucción inmediata con colgajo del músculo recto anterior del abdomen. El 27/03/2006 inicia tratamiento con quimioterapia a base de esquema adriamicina ciclofosfamida cada 21 días, por 4 ciclos. Seguido de radioterapia externa en acelerador lineal a pared costal y áreas de drenaje ganglionar 4 500 cGy y boost de 900 cGy con fraccionamiento de 150 cGy diario del 26/06 al 14/08/2006. Posteriormente docetaxel por 4 ciclos, último ciclo 07/11/2006. Continuó con tratamiento con bloqueo hormonal a base de tamoxifeno 20 mg al día por 5 años.
Evaluada por fisioterapia en agosto de 2008, con un peso de 60 kg y talla: 1,47. Presentó linfedema de 19 cm, en miembro superior izquierdo (MSI). Segmentos comprometidos mano: 1,5 cm; antebrazo: 9 cm y brazo: 8,5 cm (Cuadro 2). Signo de fóvea presente en mano y antebrazo. Edema de consistencia blando y piel en buenas condiciones generales al inicio, aumento de la temperatura local (38,1°C) en brazo y cavidad axilar, refiere sensación de pesadez, con limitación en hombro. Tiempo de aparición del linfedema, 24 meses después de la mastectomía. Inicia terapia física.
En mayo de 2009, presentó cuadro de erisipela en MSI, con aumento importante del edema linfático en miembro superior.
En junio de 2009 en estudio mamográfico se le diagnostica adenosis e hiperplasia ductal moderada en mama derecha. Debido a los antecedentes de cáncer en la familia y a petición de la paciente por su antecedente de enfermedad en mama izquierda, solicita tratamiento profiláctico, por lo que el 29/07/2009 se le realizó adenomastectomía subcutánea, con simetrización posterior en la mama derecha + reconstrucción con implante. Después de 3 meses ausente de tratamiento rehabilitador por antecedentes ya descritos, es reevaluada por fisioterapia el 30/08/2009 presentando linfedema de 25,5 cm en MSI, hombro doloroso e impotencia funcional que limita sus AVD. En marzo 2012 adquiere nueva infección por linfangitis. Entre los factores de riesgos presente están: 10 ganglios linfáticos resecados, 3 ganglios positivos, 30 sesiones de radioterapia externa, dos episodios de infecciones en el brazo y aumento del peso corporal.
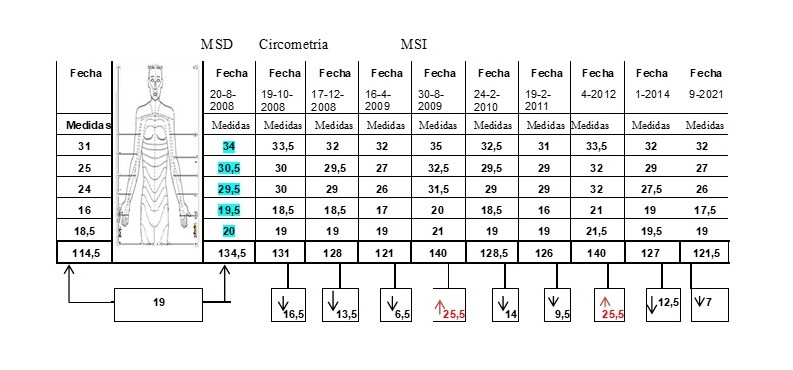
Cuadro 2
Caso 2. Circometría. Medición de los perímetros de MSI
DISCUSIÓN
Las dos pacientes, al ingresar a fisioterapia se les realizaron una evaluación física y funcional del miembro superior comprometido. La historia clínica detallada y la medición del volumen de la extremidad son fundamentales para el diagnóstico y seguimiento del linfedema. Se recogió medidas de peso y talla. La circometría fue el método usado para medir el linfedema. Se midió la circunferencia del brazo en cinco puntos anatómicos: iniciando por los metacarpianos (base del pulgar), 2 cm por arriba de la apófisis estiloides del cúbito, 2 cm por debajo y por arriba del olecranon y 16 cm por arriba de esta última eminencia ósea (14,15). La diferencia de la sumatoria de los dos brazos indica el volumen de linfedema. Se realizó la prueba clínica de fóvea a la presión digital, la palpación para la consistencia del edema, se inspeccionó el estado de la piel, se preguntó la dominancia manual, la ocupación y uso de sistema de compresión en el brazo.
Se evaluó las amplitudes del movimiento articular en hombro y las limitaciones funcionales del brazo a través de la realización de las AVD. Los resultados obtenidos se registraron en formatos previamente diseñados a partir del cual se elaboró un plan de tratamiento. También se estimaron los factores de riesgos, (seleccionados mediante reportes clínicos y un interrogatorio).
El tratamiento se desarrolló en dos fases: I. Educación sanitaria: inicialmente se les proporcionó a las pacientes toda la información a través de charlas educativas, personalizadas (mostrando los factores de riesgos presentes) y en grupo. También, por medio de material escrito acerca del linfedema, las manifestaciones clínicas, los cuidados e higiene para mantener sana la piel del brazo, los ejercicios indicados para la prevención y tratamiento del linfedema. II. Aplicación de un método de tratamiento denominado triada terapéutica (16) formado por (crioterapia (17), drenajes (18) y ejercicios).
El esquema de tratamiento se cumplió en el Centro de Rehabilitación Neuromuscular, en un lapso de tiempo de 13 años, de los cuales, de cuatro a cinco años recibieron terapia física, cumplidos de forma regular. Iniciando con una frecuencia de tres veces por semana y gradualmente de acuerdo a la evolución presentada, se distanciaron a una vez por semana. Posteriormente pasan a control, con seguimientos trimestrales y luego semestrales hasta octubre de 2021.
CASO 1. Presentó linfedema en mano y antebrazo, con mayor aumento del volumen de linfa en mano: 5 cm. Con base a las características físicas del edema, se clasificó en estadio 2, temprano, con severidad grado 3. Signo de fóvea positivo, edema blando al tacto, responde parcialmente al drenaje linfático postural (DLP), sin cambios en los tejidos blandos (piel y tejido celular subcutáneo TCS.)
Mostró buena respuesta a la terapia física con evolución satisfactoria. No se evidenció ninguna complicación durante el tratamiento ni durante el seguimiento (Figura 1). Mantuvo un peso corporal con muy pocas variaciones.
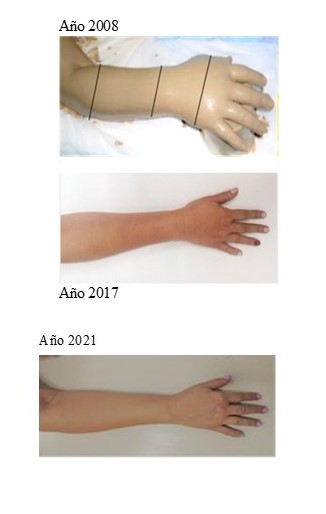
Figura 1
Linfedema en mano y antebrazo, MSD.
CASO 2
Presentó linfedema en mano, antebrazo y brazo, que aumentó a 25,5 cm en MSI después de dos episodios de infección en el brazo (erisipela y posteriormente linfangitis.) Con mayor volumen de linfa en antebrazo: 13 cm, seguido por el brazo: 9,5 cm y mano: 3 cm. Linfedema: estadio 2, tardío, con severidad grado 3. Deja fóvea a la presión fuerte, edema de consistencia duro-elástico al tacto, piel distendida, con cambios en el color (oscuro), no reduce con los cambios de postura (DLP), presentó aumento de peso y cambios en la morfología de MSI, impotencia funcional y consecuencias psicológicas importantes, que ameritó tratamiento físico y psicológico.
Respondió de forma lenta a la terapia física, pero mostrando mejoría clínica de los tejidos blandos con disminución del edema (Figura 2). Presentó aumento del peso corporal de 7 300 kg. El linfedema de MSI presentó más complicaciones que el de MSD.
Si bien, ambos edemas mostraron una clasificación de acuerdo al volumen en grado 3 (grave), no se evidenciaron otras manifestaciones clínicas en la piel y TCS, salvo las señaladas. No se observó cambios estructurales, probablemente por la intervención temprana a fisioterapia que evitó el daño en los tejidos blandos.
Las pacientes presentaron dominancia manual derecha, de profesión bioanalistas y no utilizaron ningún sistema de compresión en el brazo.
Actualmente se encuentran libres de enfermedad, con linfedema leve en sus brazos y activas laboralmente.
Podemos concluir en: aproximadamente entre 5 % al 30 % de la población con cáncer de mama padecerá linfedema (19). No hay estudios estadísticos que indiquen que el linfedema pueda prevenirse, debido a la complejidad en la patogenia y a las diferencias individuales. La historia natural del linfedema es una complicación del tratamiento del cáncer de mama y lleva implícitos riesgos inevitables como la disección ganglionar axilar y la radioterapia, no obstante, trabajando en la prevención de algunos factores se puede reducir el riesgo.
Entre los factores de riesgos modificables están: la movilización precoz del brazo en el posoperatorio inmediato, las medidas de higiene y autocuidado, el control de peso, la detección temprana (reconocimiento de los primeros síntomas) y el tratamiento oportuno, son factores modificables, en los que se pueden producir cambios significativos.
La prevención del linfedema en el paciente con cáncer de mama es una prevención secundaria; para lograrlo es determinante la educación a través de la enseñanza de nuevos hábitos de vida. El fisioterapeuta capacita al paciente en la prevención de las complicaciones derivadas de su propia enfermedad.
Después de 13 años de tratamiento y seguimiento del linfedema, las pacientes mostraron una disminución del linfedema a mediano y largo plazo, cimentados en dos pilares fundamentales; educación sanitaria y el método triada terapéutica.
Las participantes mejoraron la funcionalidad del miembro superior, medida por la correcta ejecución en las AVD, tales como (peinarse, abrocharse el brassier, cerrar el cierre, alcanzar objetos en alto, asir objetos con la mano, abrir y cerrar francos, escribir y realizar pinza fina).
Manifestaron mejor estado físico de salud, y mejor estado emocional, reflejados en bienestar y mejoras en su calidad de vida.
Las infecciones por erisipela y linfangitis aumentan la carga linfática en el miembro superior comprometido.
El linfedema en brazo limita la flexo elevación de hombro y en mano limita las funciones de prensión y pinza fina.
El diagnóstico precoz incrementa las perspectivas de recuperación, por lo tanto, la eficacia en el tratamiento estará en relación directa con la precocidad de instauración y tratamiento del mismo.
La limitación de este trabajo fue la falta de estudios complementarios (linfo-gammagrafía) para una mejor valoración, diagnóstico y manejo del linfedema.
Dada la complejidad del linfedema, su abordaje terapéutico también lo es, siendo un desafío para fisioterapeutas y médicos. Contamos con el tratamiento conservador que aplicado
desde estadios tempranos responde favorablemente y el tratamiento quirúrgico indicado para los pacientes con progresión de la enfermedad.
Recomendamos: la educación sanitaria es un programa de intervención terapéutica, debe iniciare una vez que el paciente es intervenido quirúrgicamente (Mastectomía.) Se recomiendan las movilizaciones tempranas en el brazo para evitar la retención de líquidos, la rigidez del hombro, la retracción de tejidos blandos y la atrofia muscular posquirúrgica. El ejercicio ha demostrado ser una herramienta eficaz en la prevención del linfedema (20). Todo paciente debe tener presente que el conocimiento y cumplimiento de las medidas de higiene y autocuidado del brazo, son fundamentales en la prevención.
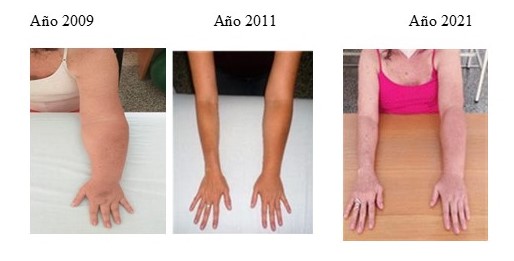
Figura 2
Linfedema en mano, antebrazo y brazo MSI
REFERENCIAS
1. Dominguez F, Blas J, de Castro G, editores. Guías clínicas de la asociación española de cirujanos. Cirugía de la mama 2. edición. Madrid: Arán Ediciones;2017.
2. Kosir MA. Cáncer de mama. Evaluación de los trastornos mamarios. 2020. Disponible en: URL:https://www.msdmanuals.com/es-ve/professional/ginecolog%C3%ADa-y-obstetricia/trastornos-mamarios/evaluaci%C3%B3n-de-los-trastornos-mamarios
3. Kilbreath SL, Refshauge KM, Beith JM, Ward LC, Ung OA, Dylke ES, et al. Risk factors for lymphoedema in women with breast cancer: A large prospective cohort. Breast. 2016;28:29-36.
4. Togawa K, Ma H, Sullivan-Halley J, Neuhouser ML, Imayama I, Baumgartner KB, et al. Risk factors for self-reported arm lymphedema among female breast cancer survivors: A prospective cohort study. Breast Cancer Res. 2014;16(4):414.
5. DiSipio T, Rye S, Newman B, Hayes S. Incidence of unilateral arm lymphoedema after breast cancer: A systematic review and meta-analysis. Lancet Oncol. 2013;14(6):500- 5 15.
6. Golshan M, Smith B. Prevention and management of arm lymphedema in the patient with breast cancer. J Support Oncol. 2006;4(8):381-386
7. Modi S, Stanton AW, Svensson WE, Peters AM, Mortimer PS, Levick JR. Human lymphatic pumping measured in healthy and lymphoedematous arms by lymphatic congestion lymphoscintigraphy. J Physiol. 2007;583(Pt 1):271-285.
8. Bentzen SM, Dische S. Morbidity related to axillary irradiation in the treatment of breast cancer. Acta Oncol. 2000;39(3):337-347.
9. Vaillant L, Gironet N. Complications infectieuses des lymphoedèmes [Infectious complications of lymphedema]. Rev Med Interne. 2002;23(Suppl 3):S403-407.
10. Ferguson CM, Swaroop MN, Horick N, Skolny MN, Miller CL, Jammallo LS, et al. Impact of ipsilateral blood draws, injections, blood pressure measurements, and air travel on the risk of lymphedema for patients treated for breast cancer. J Clin Oncol. 2016;34(7):691-698.
11. Bevilacqua JL, Kattan MW, Changhong Y, Koifman S, Mattos IE, Koifman RJ, et al. Nomograms for predicting the risk of arm lymphedema after axillary dissection in breast cancer. Ann Surg Oncol. 2012;19(8):2580-2589.
12. [No Auyhor’s List]. Executive Committee of the International Society of Lymphology. The diagnosis and treatment of peripheral lymphedema: 2020 Consensus Document of the International Society of Lymphology. Lymphology. 2020;53(1):3-19.
13. Arias-Cuadrado A, MJ, Álvarez Vázquez R, Mourelle M, Villarino- Díaz Jiménez C. Clínica, clasificación y estadiaje del linfedema. Rehabilitación (Madr). 2010;44(Supl 1): S29-34
14. Cuello-Villaverde E, Forner-Cordero I, Forner-Coredero A. Linfedema: métodos de medición y criterios diagnósticos. Rehabilitación (Madr). 2010;44 (Supl 1):S21-28.
15. Taylor R, Jayasinghe UW, Koelmeyer L, Ung O, Boyages J. Reliability and validity of arm volume measurements for assessment of lymphedema. Phys Ther. 2006;86(2):205-214.
16. Olmos Torres EP. Triada terapéutica para el tratamiento del linfedema posmastectomía. Rev Venez Oncol. 2018;30(2):137-147.
17. Olmos Torres EP. Crioterapia: dos modalidades terapéuticas para la rehabilitación del linfedema. Rev Venez Oncol. 2020:32(4):216-223.
18. Olmos Torres EP. Drenajes linfáticos para tratamiento del linfedema secundario a cáncer de mama. Fundamentación teórica y mecánica. Rev Venez Oncol. 2021;33(3):143-154, 2021
19. Szuba A, Shin WS, Strauss HW, Rockson S. The third circulation: Radionuclide lymphoscintigraphy in the evaluation of lymphedema. J Nucl Med. 2003;44(1):43-57.
20. Park JH, Lee WH, Chung HS. Incidence and risk factors of breast cancer lymphoedema. J Clin Nurs. 2008;17(11):1450-1459.
Notas de autor
patriciaolmos1@yahoo.es
Información adicional
Responsabilidades éticas: Se obtuvo el consentimiento informado de las dos participantes para la publicación de imágenes contenidas en este manuscrito, se resguarda su identidad.