¿ES EL SARS-COV-2 ONCOLÍTICO?
¿ES EL SARS-COV-2 ONCOLÍTICO?
Revista Venezolana de Oncología, vol. 34, núm. 4, pp. 217-221, 2022
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 3.0 Internacional.
Recepción: 30 Marzo 2022
Aprobación: 21 Junio 2022
Resumen: Es conocida la capacidad de algunos virus responsables de inducir al cáncer. Más recientemente también se ha estudiado el potencial oncolítico de algunos virus; su utilidad en la terapia contra el cáncer, ya sea induciendo la lisis celular al infectar las células tumorales y/o por potenciar mecanismos de inmunidad innata y adaptativa contra células cancerosas de manera específica. En esta línea, llama la atención como algunos pacientes oncológicos, incluso algunos refractarios a tratamiento, e infectados con coronavirus del Sars-Cov-2 y quienes desarrollan la enfermedad causada por el coronavirus 2019 se observa remisión del tumor. En la terapia contra el cáncer, se han ideado algunos medios para atacar al tumor e inducir apoptosis de las células enfermas, pudiendo aprovecharse la actividad de virus oncolíticos ya conocidos pero modificados con proteínas del coronavirus 2, tanto en la terapéutica directa como vacunas orientadas hacía pacientes oncológicos, abriendo así la posibilidad de obtener inmunidad contra la enfermedad por coronavirus 2019 y mantener o potenciar la actividad terapéutica oncológica, por lo cual surge la necesidad de investigar el potencial oncolítico del coronavirus 2.
Palabras clave: Cáncer, SARS-CoV-2, oncolítico, inmunidad, vacunas.
Abstract: The ability of some viruses responsible for inducing cancer known for us. More recently, the oncolytic potential of some viruses has mundial studied, its usefulness in the cancer therapy, either by inducing cell lysis by infecting tumor cells and or by enhancing mechanisms of innate and adaptive immunity against cancer cells in a specific way. In this line, it is striking how some cancer the patients, including some refractory to treatment, and infected with Sars-Cov-2 coronavirus and those who develop the disease caused by the coronavirus 2019 remission of the tumor is observed In the cancer therapy, some means have been devised to attack the tumor, and induces the apoptosis of the diseased cells; are being able to take advantage of the activity of oncolytic viruses already know but modified with coronavirus 2 proteins, both in direct therapy and vaccines aimed at cancer patients, this opening the possibility to obtain immunity against coronavirus disease 2019 and maintain or enhance the oncological therapeutic activity, which is why the need arises to investigate the oncolytic potential of the coronavirus 2.
Keywords: Cáncer, SARS-CoV-2, oncolytic, immunity, vaccines.
Existen algunos virus capaces de inducir la desprogramación de células y llevar al cáncer. Entre estos virus se describen aquellos cuyo material genético es ácido desoxirribonucleico (ADN) y ácido ribonucleico (ARN). En la actualidad se reconocen siete oncovirus humanos. Estos son: el virus de Epstein-Barr (EBV), el virus del papiloma humano (HPV), virus de hepatitis B y C (HBV y HCV), el virus linfotrópico de células T humanas-1 (HTLV-1), herpes virus humano-8 (HHV-8) y papiloma virus de células de Merkek (MCPyV) (1). El camino desde la infección viral hasta la tumorogénesis es lento e ineficiente; solo una minoría de las personas infectadas progresa a cáncer, por lo general años o incluso décadas después de la infección primaria (2).
En las últimas décadas, se ha estudiado el potencial oncolítico de los virus, y su utilidad en la terapia contra el cáncer, apoyado no sólo en su capacidad de inducir la lisis celular al infectar las células tumorales específicamente, sino además potenciando los mecanismos de inmunidad innata y adaptativa del paciente, contra dichas células, de manera más selectiva y eficiente (3). A raíz de esas hipótesis, se han establecido estudios con diversos virus con potencial oncolítico (distintos tipos de adenovirus, herpes virus simple tipo 1, entre otros) hasta ahora en su mayoría en modelos animales, sin embargo, hoy en día existen diversos estudios en fase III, con un perfil de seguridad aceptable (4).
Desde el comienzo de la pandemia en 2019, han sido mucho los estudios realizados en referencia al coronavirus causal del Síndrome Respiratorio Agudo tipo 2 (SARS-CoV-2), y hasta vacunas se han logrado desarrollar utilizando su material genético (5, 6). Dentro de estos estudios, en esta serie de evidencias se destaca la remisión de algunos cánceres ya descritos como casos reportados en la literatura lo que abre la puerta para continuar con investigaciones relacionadas (7).
La remisión temporal descrita por Pasin y col. (7), de un paciente varón con linfoma de células T/natural killer (NK) refractario durante la infección y desarrollo de la enfermedad causada por el coronavirus -19 (COVID-19) y que luego de superarla recae. Los lleva a pensar que el SARS-CoV-2 puede tener algún tipo de actividad oncolítica. Evidenciado por la mejora clínica y de laboratorio descritos. El agotamiento de linfocitos inducido por SARS-CoV-2 tiene un papel de diagnóstico fundamental y representa una herramienta pronostica válida. En pacientes recuperados de Covid-19 se ha documentado aumentos del recuento de linfocitos. En los pacientes Covid-19 se desarrolla una enorme tormenta de citoquinas, y la muerte se da por “síndrome hiperferritinémico”. Posiblemente el microambiente dado por la inflamación podría cambiar las funciones efectoras de las células NK, en Covid o formas inflamatorias secundarias del síndrome hiperferritinémico, se elevan interleukina 6 (IL-6) e interleukina 10 (IL10), como se ha observado en pacientes contaminados con SARS-CoV-2 y reducen la citotoxicidad de las células NK y aumenta la expresión del antígeno de diferenciación 94 (CD94 o NKG2A), lo que es muy importante para matar (eliminar) las células infectadas por el virus (8). Las células NK expresan la enzima convertidora de angiotensina 2 (ACE2), así que el virus puede infectarlas y es lo que llevaría a la disminución de la toxicidad por supresión de sus funciones (7,8).
Por otro lado, Challenor y col. (9) reportaron un interesante caso de remisión de linfoma de Hodgkin. Plantearon la hipótesis que la infección por SARS-Cov-2, es quien desencadenó la respuesta antitumoral y, que el mecanismo de acción podría deberse a una reactividad cruzada de células T específicas del patógeno con antígenos del tumor y la activación de células NK, llevado a cabo por las citoquinas inflamatorias que son secretadas en respuesta a la infección. Teniendo en cuenta los casos actuales de remisión de cáncer observada en pacientes infectados con SARSCoV-2, hay una necesidad urgente de investigar el desarrollo del oncolítico SARS-CoV-2 para dirigirse específicamente a células cancerígenas (10). En la lucha contra el cáncer se han ideado algunos medios para llegar al tumor y así lograr la remisión del mismo. La inducción de la apoptosis es una de las estrategias más prometedoras para el desarrollo de algún tipo de terapia (11).
Algunos tipos de cáncer de mama agresivos son producto de mutaciones en p53 y, muchos de ellos presentan mutaciones en los genes BRCA1 y BRCA2. El receptor ACE2 se expresa en estas células de cáncer de mama, este es el receptor usado por el SARS-CoV-2 a través de la proteína pico o espiga viral (S) y de la proteasa de serina transmembrana 2 (TMPRSS2) contribuye al cebado de la proteína S, mientras que la Dipeptidil Peptidasa IV(DPP-IV)se cree es un co-receptor para la entrada del SARS-CoV-2 y el principal receptor para la entrada del coronavirus del Síndrome Respiratorio de Oriente Medio (MERS-CoV) (12).
Los adenovirus oncolíticos (ONYX015) se han usado en terapia de tumores sólidos. Este virus tiene una deleción de 827 pb (región E1B) y una mutación puntual que genera un codón de parada (stop) que impide la expresión de forma truncada de la proteína E1B55K. Estas características lo hacen incapaz de bloquear las funciones de p53 y su degradación en células p53 (+). En células de tumor cuyo p53 no es funcional el ONYX-015 se replica selectivamente lo que da como resultado la eliminación selectiva de estas células de cáncer (13).
En células de cáncer de mama disminuye la expresión de ACE2 pero hay un aumento de la expresión de TMPRSS2 y DPP-IV. Aunque ONYX-015 ha demostrado ser eficaz en terapia contra el cáncer de mama, la entrada de este virus modificado depende de la expresión en la superficie de las células de Coxsackie y, receptor de adenovirus (CAR) por las células huésped. Esta lleva a la hipótesis que si ONYX-015 es restaurado incorporándole la proteína spike, con los genes que codifican la proteína S del SARS-CoV-2 y MERS-CoV se podría mejorar la entrada del ONYX-015 en esas células de cáncer de mama más agresivas y restaurar la remisión eficiente de células cancerosas (Figura 1) (12).
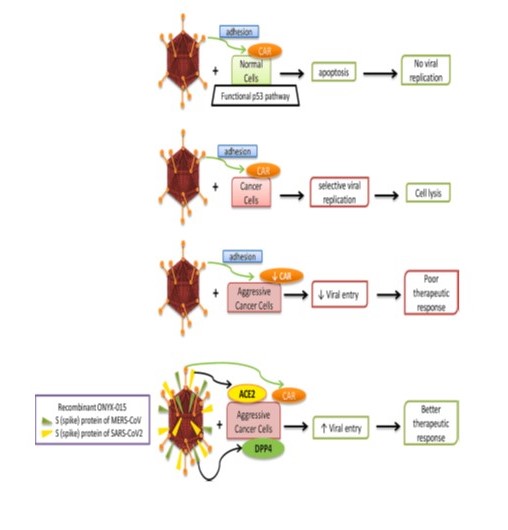
Figura 1
Efectos de ONYX-015 y virus reestructurado en varios tipos de células.
Esta figura muestra la respuesta terapéutica de ONYX-015 en pacientes normales, con cáncer y células agresivas de cáncer de mama. La reestructuración de ONYX-015 utilizando genes de proteína de pico de SARS-CoV-2 y MERS-CoV puede mejorar la respuesta terapéutica con la entrada viral facilitada
(12)Otro enfoque recientemente en estudio es el planteado por Sun y col.(14), quienes plantean el rol dual de una vacuna contra el SARS-CoV-2, orientada a pacientes oncológicos, utilizando un vector viral basado en herpes virus tipo 1 (otro de los virus con potencial oncolítico ya conocido). En un estudio llevado a cabo en 3 poblaciones distintas de ratones, cada una trasplantada con células tumorales distintas: melanoma, adenocarcinoma (ADC) de colon y ovario, los cuales fueron inoculados con una vacuna, basadas en el virus oncolítico modificado con la proteína spike del SARS-CoV-2, lograron producir una respuesta inmune satisfactoria creando anticuerpos anti-SARSCoV2, en ratones sin y con tumor, y además estos últimos mostraban una reducción de la actividad tumoral (producto de la acción del virus oncolítico usado como vector) lo cual abre la posibilidad de diseñar una vacuna específica para pacientes oncológicos, beneficiándolos con inmunidad contra COVID-19, y al mismo tiempo mantener su actividad terapéutica oncológica.
Concluimos en: la evidencia actual es escasa probablemente por el poco tiempo que ha tenido la comunidad científica para el estudio del SARS-CoV-2, sin embargo, respecto a su probable actividad oncolítica parece claro esgrimir que su potencial directo se relaciona con aquellas neoplasias de linaje linfoproliferativo (7,9), apoyado en la patogenia propia del virus y su impacto sobre el número y funcionalidad de la población linfocítica (8), mientras que los mecanismos de infección y estructuras virales abren la puerta, mediante ingeniería genética, para la utilización del genoma del SARS-CoV-2 como una herramienta para potenciar a otros virus oncolíticos y aumentar su efectividad ante otros tipos de cáncer no relacionados a estirpes linfoides (10,11,12,13), pudiendo incluso desarrollarse tecnologías, para potenciar dicha actividad oncolítica, dentro del marco de futuras vacunas dirigidas a la población oncológica como población especial (14)
No cabe duda de que el camino por descubrir respecto a las posibles propiedades oncolíticas del SARS-CoV-2 está aún en sus etapas iniciales, sin embargo, queda claro el potencial beneficio de explorar su actividad oncolítica intrínseca, así como la obtenida mediante ingeniería genética recombinante con otros virus oncolíticos más conocidos. Todo esto podría generar un beneficio a futuro en la lucha contra el cáncer, aun cuando, en el recuerdo, debamos mirar hacia a la pandemia vivida y sus consecuencias.
REFERENCIAS
1. Mui U, Haley C, Tyring S. Viral Oncology: Molecular Biology and Pathogenesis. Journal of Clinical Medicine [Internet]. 2017 [citado 23 febrero 2022];6(12):111. Disponible en: URL: https://www.mdpi.com/2077-0383/6/12/111
2. Liao J. Viruses and human cancer. Yale Journal of Biology and Medicine [Internet]. 2006 [citado 23 febrero 2022];79(3-4):115-22. Disponible en: URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1994798/pdf/yjbm_79_3-4_115.pdf
3. Cassady K, Haworth K, Jackson J, Markert J, Cripe T. To infection and beyond: The multi-pronged anti-cancer mechanisms of oncolytic viruses. Viruses [Internet]. 2016 [citado 23 febrero 2022];8(2):43. Disponible en: URL: https://doi.org/10.3390/v8020043.
4. Prado Hidalgo M, Llanos Méndez A. Seguridad y eficacia de los virus oncolíticos en el cáncer avanzado. Revisión sistemática informe de síntesis de tecnologías emergentes [Internet]. Sevilla: Agencia de Evaluación de Tecnologías Sanitarias de Andalucía; 2012 [citado 23 febrero2022]. Disponible en: URL: https://www.aetsa.org
5. Polack F, Thomas S, Kitchin N, Absalon J, Gurtman A, Lockhart S, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. New England Journal of Medicine [Internet]. 2020 [citado 24 febrero 2022];383(27):2603-2615. Disponible en: URL: https://www.nejm.org/doi/full/10.1056/NEJMoa2034577
6. Baden L, El Sahly H, Essink B, Kotloff K, Frey S, Novak R, et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 Vaccine. New England Journal of Medicine [Internet]. 2021 [citado 24 febrero 2022];384(5):403-416. Disponible en: URL: https://www.nejm.org/doi/full/10.1056/NEJMoa2035389
7. Pasin F, Mascalchi M, Calabrese A, Pizzarelli G, Bongiovanni I, Andreoli M, et al. Oncolytic effect of SARS-CoV2 in a patient with NK lymphoma: Spontaneous remission in NK/T-cell Lymphoma during Covid-19. Acta Biomed [Internet]. 2020 Sep. 7 [citado 2022 febrero 24];91(3):e2020047. Disponible en: URL: https://www.mattioli1885journals.com/index.php/actabiomedica/article/view/10141
8. Zheng M, Gao Y, Wang G, Song G, Liu S, Sun D, et al. Functional exhaustion of antiviral lymphocytes in COVID-19 patients. Cellular & Molecular Immunology [Internet]. 2020 [citado 23 febrero 2022];17(5):533-535. Disponible en: URL: https://pubmed.ncbi.nlm.nih.gov/32203188/
9. Challenor S, Tucker D. SARS‐CoV‐2‐induced remission of Hodgkin lymphoma. British Journal of Haematology [Internet]. 2021 [citado 23 febrero 2022];192(3):415-415. Disponible en: URL: https://pubmed.ncbi.nlm.nih.gov/33386647/
10. Donia A, Shahid R, Nawaz M, Yaqub T, Bokhari H. Can we develop oncolytic SARS-CoV-2 to specifically target cancer cells? Therapeutic Advances in Medical Oncology [Internet]. 2021 [citado 24 febrero 2022];13:17588359211061988. Disponible en: URL: https://pubmed.ncbi.nlm.nih.gov/34880954/
11. Singh PK, Doley J, Kumar GR, Sahoo AP, Tiwari AK. Oncolytic viruses & their specific targeting to tumour cells. Indian J Med Res. [Internet]. 2012 [citado 23 febrero 2022];136(4):571-584. Disponible en:URL: https://pubmed.ncbi.nlm.nih.gov/23168697/
12. Parmar H, Nayak A, Kataria S, Tripathi V, Jaiswal P, Gavel P, et al. Restructuring the ONYX-015 adenovirus by using spike protein genes from SARS-CoV-2 and MERS-CoV: Possible implications in breast cancer treatment. Medical Hypotheses [Internet]. 2022 [citado 24 febrero 2022];159:110750. Disponible en:URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8723760/
13. Kelly E, Russell S. History of oncolytic viruses: Genesis to genetic engineering. Molecular Therapy [Internet]. 2007 [citado 24 febrero 2022];15(4):651-659. Disponible en: URL: https://pubmed.ncbi.nlm.nih.gov/17299401/
14. Sun Y, Dong W, Tian L, Rao Y, Qin C, Jaramillo S, et al. Dual roles of a novel oncolytic viral vector-based SARS-CoV-2 vaccine: preventing COVID-19 and treating tumor progression. [Internet]. 2021 [citado 24 febrero 2022]; 447286. Disponible en: URL: https://pubmed.ncbi.nlm.nih.gov/34127971/
Notas de autor
saulvillasmil@gmail.com
Información adicional
DECLARACIÓN DE DIVULGACIÓN O CONFLICTO DE INTERESES: Todos los autores no tienen ningún conflicto de interés real o potencial, incluidas las relaciones financieras, personales o de otro tipo con otras personas u organizaciones del trabajo presentado que podría influir de manera inapropiada en su trabajo.