USO DEL TUMOR MUTATIONAL BURDEN COMO MARCADOR PREDICTIVO DE RESPUESTA AL TRATAMIENTO CON INMUNOTERAPIA.
USO DEL TUMOR MUTATIONAL BURDEN COMO MARCADOR PREDICTIVO DE RESPUESTA AL TRATAMIENTO CON INMUNOTERAPIA.
Revista Venezolana de Oncología, vol. 35, núm. 1, pp. 25-33, 2023
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 14 Octubre 2022
Aprobación: 09 Diciembre 2022
Resumen: El tumor mutational Burden se utiliza como marcador predictivo de respuesta al tratamiento con inmunoterapia. Este con valores superiores a 10 Mut/Mb se vincula con mayores tasas de respuesta al tratamiento con inhibidores del punto de control inmunológico. OBJETIVO: Evaluar la tasa objetiva de respuesta al tratamiento con inmunoterapia en pacientes con un tumor mutational Burden alto. MÉTODO: Estudio retrospectivo, descriptivo de cohorte analítico, unicéntrico. Se incluyeron en el estudio 80 pacientes, a los cuales se le realizó un estudio de secuenciación genética para determinar valores del tumor Burden. Se incluyeron pacientes que recibieron tratamiento con inmunoterapia sola o combinada. RESULTADOS: La frecuencia de este tumor mutational Burden es elevado en nuestro estudio fue de13,75 %. Se registra mayor frecuencia de un tumor mutational Burden alto en pacientes con cáncer de pulmón. 9 pacientes con mutación de los genes BRCA 1-2, coexistiendo con un tumor mutational Burden alto, 33,3 %. Se registran tasas de respuesta objetiva a tratamiento con inmunoterapia en pacientes con tumor mutational Burden elevado 71,42 % y con bajo 35,71 %, diferencia en tasas de respuesta, con un IC de 95 %; arrojó una P=0,122; se corresponde con una diferencia estadísticamente no significativa. CONCLUSIONES: En este estudio se observan mayores tasas de respuesta a tratamiento con inmunoterapia en pacientes con un tumor mutational Burden alto. Estudios con mayor muestra y mayor tiempo de seguimiento son requeridos, para darle mayor poder estadístico al estudio.
Palabras clave: Inmunoterapia, tumor Mutational Burden, tasas de respuesta, tumores sólidos.
Abstract: The tumor mutational Burden is used as predictive marker of response to treatment with immunotherapy. A tumor mutational Burden with values greater than 10 Mut/Mb is associated with higher response rates to treatment with immunological checkpoint inhibitors. OBJECTIVE: Evaluated the objective response rate to immunotherapy treatment in patients with high tumor mutational Burden. METHOD: A retrospective, descriptive. analytical cohort unicentric study was performed. 80 patients were included in the study, to whom a genetic sequencing study was carried out to determine tumor mutational burden values. We included patients who received treatment with immunotherapy alone or in combination. RESULTS: The frequency of a high tumor mutational Burden in our study was 13.75 %. A greater frequency of high tumor mutational Burden was reported in patients with lung cancer. There are 9 patients with mutation of the BRCA 1-2 genes, 3 of which coexisted with a high tumor mutational Burden (33.3 %). Responsive objective tasa to treatment with immunotherapy was 71.42 % in patients with high tumor muttions Burden and 35.71 % in patients with a low tumor mutational Burden, The differences in response rates, with a 95 % CI; yielded a P=0.122 which corresponds to a non-statistically significant difference. CONCLUSIONS: In this study, higher response rates to immunotherapy treatment were observed in patients with a high tumor mutational Burden. Studies with larger samples and longer follow-up time are required to give greater statistical power to these findings.
Keywords: Immunotherapy, tumor mutational Burden, response rate, solid tumor.
INTRODUCCIÓN
El tratamiento con inhibidores de punto de control inmunológicos en patologías oncológicas, viene en aumento desde su primera aprobación en el año 2010 cuando el uso de ipilimumab en pacientes con melanoma metastásico combinado con dacarbazina, vs., dacarbazina como monoterapia, demostró beneficios en términos de intervalo libre de progresión (ILP) y supervivencia global (SG); siendo este anticuerpo monoclonal anti CTLA4 el primer inhibidor de punto de control inmunológico aprobado por la FDA (Food & Drugs Administrarion) (1). Posteriormente, los anticuerpos monoclonales anti PD1 y anti PDL1 (nivolumab, pembrolizumab, atezolizumab y durvalumab) fueron aprobados en múltiples patologías oncológicas y hematoncológicas, siendo el principal punto de referencia para su uso la expresión de PDL1 en las células tumorales (2,3,4,5). Existen varios marcadores predictivos de respuesta: la expresión de PDL-1 en el tejido tumoral (6,7.8.9), la presencia de infiltrado inflamatorio linfocitario (9), la presencia de inestabilidad micro-satelital (10,11)y la presencia de TMB alto (Tumor Mutational Burden) (12).
El TMB, está definido como el número total de mutaciones somáticas por área de codificación del genoma del tumor, siendo esto una medida de todas las mutaciones codificantes somáticas no sinónimas en el exoma tumoral (13,14). Un TMB alto, se asocia con mayor inmunogenicidad, pues se interpreta que habrá mayor tasa de mutaciones somáticas; por lo tanto, mayor posibilidad de presentar antígenos que puedan originar una respuesta inmunológica (15,16); basado en esto, podría haber mayor respuesta oncológica con el uso de los inhibidores de punto de control inmunológico (12,17). El estudio Key-Note 0158, demostró que los pacientes con un TMB alto tienen mayor poder predictivo de respuesta que la expresión PDL1 (12). Otros estudios han demostrado la correlación entre TMB elevado y el beneficio clínico de anticuerpo anti CTLA4, anti PD1 y anti PDL1, hecho el cual es incluso apoyado por un meta-análisis (18,19). En el año 2020, se publicó en la revista Lancet de Oncología el estudio Key-Note 158, probablemente es el estudio que tiene mayor evidencia hasta la fecha, del beneficio del tratamiento con inhibidores de punto de control inmunológico asociado a TMB alto (12).
En Venezuela hasta la fecha, no hay estudios publicados sobre la incidencia de un TMB alto en pacientes con tumores sólidos, por las limitaciones de realizar estudios de secuenciación genética y del exoma completo del tumor. En este trabajo, se espera documentar el TMB en neoplasias sólidas y su posible asociación con la respuesta oncológica al tratamiento con inhibidores de punto de control.
ANTECEDENTES
El TMB es definido como el número de mutaciones somáticas por área codificante del genoma del tumor, es una medida de todas las mutaciones no sinónimas codificadas en el exoma tumoral(13,14). Se interpreta que a mayor TMB, hay mayor número de mutaciones somáticas endosinónimas y, por ende, mayor posibilidad de expresar antígenos que puedan desencadenar una respuesta inmunológica; por lo tanto, podría asociarse con respuesta a los inhibidores del punto de control inmunológico. El TMB alto, está asociado con mejores supervivencias y mayores tasas de respuesta en pacientes que reciben tratamiento con inhibidores del punto de control inmunológico (20). El estudio Check-Mate 227, es un estudio retrospectivo que señala como punto de corte ≥ 10 mut/Mb para establecer un TMB alto (21), siendo este valor el actual punto de referencia.
Las primeras evidencias de la asociación de TMB alto con respuesta oncológica y el uso de inhibidores de punto de control, se determinó en pacientes que tenían el TMB con más de 200 mutaciones por exoma y cuya conclusión determinó que había beneficio clínico y también en términos de SG (22). Otros trabajos determinaron que el uso de ipilimumab combinado con nivolumab en pacientes con carcinoma de pulmón de células no pequeñas y con un TMB mayor a 10, se asociaba con beneficio clínico (17,18,23,24). Por otro lado, en pacientes con melanoma, el TMB alto se asoció con respuesta a ipilimumab (25).
En el estudio Key-Note 158, con un universo de 1 073 pacientes, en el cual fueron evaluados 805 pacientes con tumores sólidos metastásicos, clasificados como incurables. Del total de pacientes, 105 tenían TMB alto. Se utilizó un número de 10 o más mutaciones por Mb para definir un TMB alto. El tratamiento fue pembrolizumab a la dosis de 200 mg cada 21 días. Las conclusiones arrojaron que después de 37,1 meses de seguimiento se detectó 29 % de respuesta objetiva vs. 6 % en el grupo de TMB normal. La conclusión del trabajo, fue que los pacientes con TMB alto obtuvieron una respuesta tumoral robusta a tratamiento con pembrolizumab como monodroga y se estableció en este momento el TMB, como un biomarcador predictivo de respuesta al tratamiento con pembrolizumab (12).
Otros hallazgos moleculares se asocian con TMB alto. Hay evidencia suficiente que sugiere que, la presencia de una inestabilidad micro-satelital elevada (MSIh), está asociada con un TMB alto (26). Por otro lado, la evidencia señala que las mutaciones de los genes BRCA 1/2, están asociadas con un aumento 2 a 3 veces mayor de la carga de neoantígenos, por lo que existe una asociación entre esta mutación y TMB alto (27).
MÉTODO
Tipo de estudio.
Estudio retrospectivo, transversal, de corte analítico.
Población y muestra.
Se analizaron todos los pacientes con un tumor sólido metastásico, clasificado como incurable, que acudieron al Servicio de Oncología (ARSUVE S.C) del Instituto Médico La Floresta y el Centro Médico Docente La Trinidad entre los años 2020 y 2022.
Se realizaron estudios de secuenciación genética de tejido tumoral, a través de lo cual se pudo evaluar el TMB. Se define un punto de corte ≥ 10 mut/Mb para un TMB alto. Se emplearon las plataformas de secuenciación genética de OncoDEEPTM, Oncotype MAPTM y el Paradigm Cancer Diagnostic PCDx (ParadigmTM).
Procedimiento
Se revisaron 110 historias clínicas con sus respectivos estudios mutacionales y que cumplieran con las características previamente señaladas; incluyéndose un total de 80 pacientes en el estudio. Se registraron datos demográficos, histológicos y moleculares de los pacientes mencionados. Se incluyeron parámetros de respuesta a tratamiento oncológico, según criterios RECIST v1.1; estableciéndose para ello las variables: respuesta completa (RC), respuesta parcial (RP), enfermedad estable (EE) y enfermedad progresiva (EP) (28). Los parámetros de RC, RP, y EE se consideran pacientes con respuesta oncológica, mientras que EP se considera fallo al tratamiento. Se consideraron a los pacientes que recibieron tratamiento con inmunoterapia: atezolizumab, nivolumab, pembrolizumab e ipilimumab. Se permitió tratamiento como monoterapia y combinados según las indicaciones aprobadas para cada tipo de tumor.
Tratamiento Estadístico Adecuado
Se incluyeron en un formato de recolección de datos los datos de cada historia clínica para su posterior análisis. Los datos de los pacientes fueron organizados y registrados utilizando el programa Excel de Microsoft Office 365. Se presentaron los datos en Figuras de barras. Se realizaron cálculos de media y se estableció la moda según cada caso. Los resultados fueron representados en valores absolutos y/o valores relativos según cada caso. Se elaboró un cuadro de 2 x 2 entre las variables TMB y respuesta al tratamiento con inmunoterapia. Se calcularon valores predictivos positivos y negativos de respuesta a tratamiento según el nivel del TMB. Se utiliza la prueba de X2 para establecer significancia estadística entre las variables mencionadas.
RESULTADOS
Se incluyeron un total de 80 pacientes, con diagnóstico de un tumor sólido y que se les realizó un estudio de secuenciación genética del tejido tumoral. La media para la edad fue de 64,17 años y la frecuencia por sexo fue de 40 pacientes del sexo masculino (50 %) y 40 del sexo femenino (50 %). El tumor más frecuente fue pulmón, con 26 pacientes (32,5 %), seguido de mama (10 %) y próstata (8,75 %) con 8 y 7 pacientes respectivamente. Los tumores de vías biliares, estómago, melanoma, vejiga, riñón, GIST, glándulas salivales y cabeza y cuello, se agruparon como otros. Hubo 5 pacientes (6,25 %) a los cuales no se les realizó la determinación de TMB. El resto de la distribución según tipo de tumor, se encuentra en la Figura 1.
La presencia de un TMB alto, fue de 11 pacientes (13,75 %), con un promedio de 19,43 Mut/Mb, siendo el menor valor de 10 Mut/Mb y el mayor de 50 mut/Mb; mientras que 64 pacientes se corresponden con un TMB bajo (80 %). Fue un paciente con cáncer de estómago el que presentó mayor valor de TMB, con 50 mut/Mb; y fue el cáncer de pulmón el que registró mayor incidencia de TMB alto (54,54 %); los otros tumores con TMB alto fueron mama, endometrio, melanoma y ovario. Por otro lado, fueron el glioblastoma multiforme, los sarcomas y el cáncer de glándulas salivales los que registraron menor TMB, con valores de 2 mut/Mb. Ningún paciente con diagnóstico de sarcoma ni de glioblastoma multiforme tuvo un TMB alto.
Se documentaron incidencias importantes de la mutación BRCA en 9 pacientes (11,25 %). La distribución según la localización del tumor fue 2 ovario (2,5 %), 1 vías biliares, 1 estómago, 1 pulmón, 1 rinofaringe, 1 endometrio, 1 vejiga y 1 tumor de primario desconocido (1,25 % cada uno). De esta incidencia de mutaciones BRCA coexisten con un TMB elevado 3 pacientes (33,3 %). Se registró una incidencia de mutación EGFR en 4 pacientes (5 %) con cáncer de pulmón; 9 mutaciones del gen KRAS (11,25 %), siendo 7 en pulmón (8,75 %) y 2 en cáncer de mama (2,5 %); y una mutación HRAS (1,25 %) en un paciente con cáncer de pulmón (Figura 2); de todos estos, solo 1 paciente con mutación KRAS coexiste con TMB alto (1,25 %). Sólo se registra 1 paciente con TMB alto (1,25 %) y una alta expresión de PDL-1 (> 1 %).
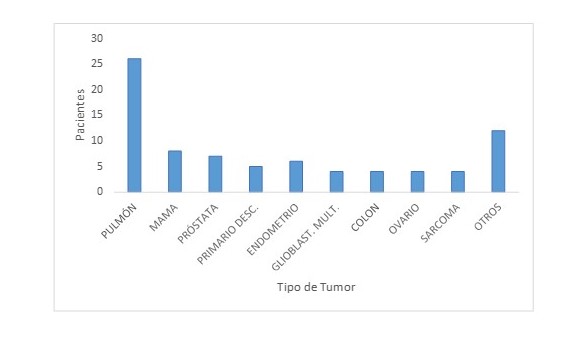
Figura 1
Distribución de pacientes con NGS según el tipo de patología oncológica.
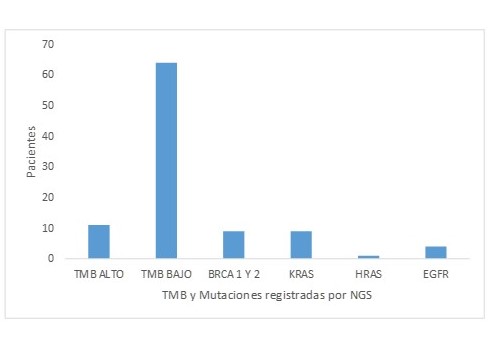
Figura 2.
Hallazgos moleculares en los estudios de NGS de los pacientes con patología oncológica.
Del total de pacientes incluidos, 21 recibieron tratamiento con inmunoterapia; de estos, 7 tenían TMB alto (33,3 %) y 14 tenían TMB bajo (66,7 %) (Figura 3). De los pacientes con TMB elevado, 5 (71,42 %) presentaron respuesta oncológica según RECIST 1.1. Por su parte, los pacientes con TMB bajo, 5 presentaron respuesta oncológica (35,71 %); mientras que 9 pacientes (64,29 %) tuvieron enfermedad progresiva (Figura 4 y 5). Se obtuvo un valor predictivo positivo de 0,71 y un valor predictivo negativo de 0,64; para la posibilidad de respuesta en pacientes con TMB alto que recibieron tratamiento con inmunoterapia. Se obtiene un valor de 2,38 para un α de 3,84 con un IC de 95 %; lo cual se corresponde con una P = 0,122, señalando que la diferencia no es estadísticamente significativa; sin embargo, estos hallazgos pueden ser consecuencia de lo pequeña de la muestra.
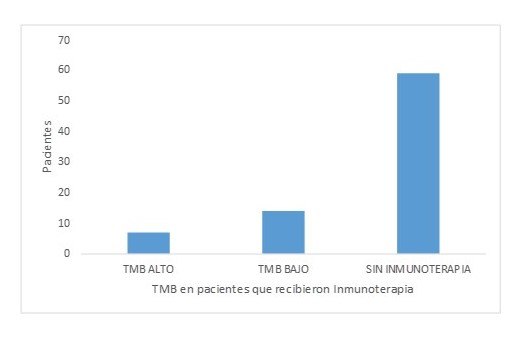
Figura 3.
¨¨Pacientes con patología oncológica que recibieron Inmunoterapia según el estatus del TM
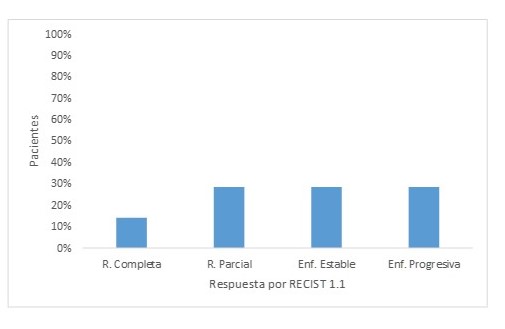
Figura 4.
Pacientes según respuesta oncológica (RECIST 1.1) que recibieron Inmunoterapia con un TMB alto.
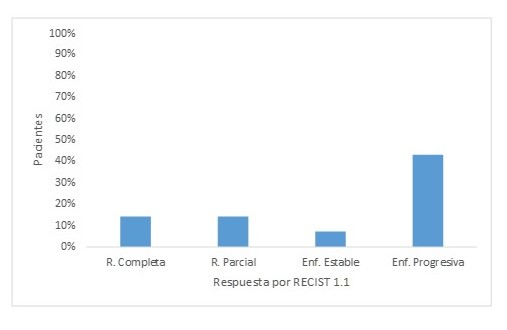
Figura 5.
Pacientes según respuesta oncológica (RECIST 1.1) que recibieron inmunoterapia con un TMB bajo.
DISCUSIÓN
En la bibliografía consultada, este es el primer estudio realizado en Venezuela sobre el análisis del TMB en tumores sólidos. Tampoco se consiguieron datos publicados de trabajos en Venezuela, que incluyan evidencia sobre pruebas de análisis mediante NGS de tejido tumoral. En los datos recolectados, se observó la presencia del TMB elevado en 11 pacientes (13,75 %) de la muestra, incluyendo todas las variedades de tumores. Se obtuvo una mayor muestra de cáncer de pulmón, probablemente debido a la importancia categórica que tiene el perfil molecular en el tratamiento de esta patología. Lo señalado por Bakenroth y col., es que el 10,8 % de su muestra tenía TMB alto; hecho el cual se compara con nuestra experiencia, donde se obtuvo un 13,75 % (15). Por otro lado, se identificó la mutación BRCA en 9 pacientes (11,25 %), de los cuales, 3 pacientes coexistieron con TMB alto (33,3 %); hecho el cual también es comparable con la bibliografía consultada (27). Al igual que Yarchoan y col., no se encontró asociación entre la presencia de TMB alto y la expresión de PDL-1, solo se obtuvo 1 paciente (1,25 %) con ambos hallazgos (19).
En el estudio, se registró un promedio de 19.43 Mut/Mb entre los pacientes con TMB alto. Para la respuesta oncológica, del total de pacientes con TMB alto, 5 (71,4 %) presentaron respuesta según criterios de RECIST v1.1. Este elemento es comparable con la bibliografía consultada; Marabelle y col., mencionan un 43 % de tasas de respuesta objetiva (12); por su parte, Yarchoan y col., obtuvieron una tasa de respuesta estimada de 40,1 % en pacientes con TMB alto que recibieron tratamiento con Inmunoterapia (19).
Es probable que, las sutiles diferencias, al menos en la evaluación de la respuesta oncológica se deba, primeramente, a que en el estudio se incluyeron pacientes que recibieron tratamiento con inmunoterapia sola o combinada, según la escogencia del oncólogo y basado en los diferentes tratamientos aprobados para cada tipo de tumor; esto definitivamente, podría reflejarse en un aumento de la tasa de respuesta y no necesariamente por acción de la inmunoterapia y el TMB elevado. Sería ideal contar con una mayor muestra y con mayor seguimiento, que le de mayor poder estadístico al estudio.
Concluimos que, hasta la fecha, no se encontraron otros estudios de similares características realizados en nuestra población. En nuestra experiencia, compartimos hallazgos con otros autores, donde la evidencia señala que un TMB alto se asocia con respuesta oncológica objetiva en aquellos pacientes que reciben inmunoterapia; aunque no contamos con una muestra de tamaño suficiente para poder establecer dicha asociación. Se requiere mayor seguimiento y una mayor muestra que permita hacer análisis de SG y poder evaluar si esta última, tiene relación estadísticamente significativa con la respuesta al tratamiento con inmunoterapia en pacientes con un TMB alto, lo que probablemente permita dar conclusiones más acertadas.
REFERENCIAS
1. Hodi F, O'Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen J, et al. Improved survival with Ipilimumab in patients with metastatic melanoma. N Engl J Med. 2010;363:711-723.
2. Powles T, O'Donnell P, Massard C, Arkenau HT, Terence W FriedlanderTW, et al. Efficacy and safety of durvalumab in locally advanced or metastatic urothelial carcinoma: Updated results from a phase 1/2 Open-label Study. JAMA Oncol. 2017;3(9):e172411.
3. Fehrenbacher L, Spira A, Ballinger M, Kowanetz M, Vansteenkiste J, Mazieres J, et al. Atezolizumab versus docetaxel for patients with previously treated non-small-cell lung cancer (POPLAR): A multicentre, open- label, phase 2 randomised controlled trial. Lancet. 2016;387(10030):1837-1846.
4. Wolchok JD, Kluger H, Callahan MK, Postow M Rizvi N, Lesokhinet A, et al. Nivolumab plus ipilimumab in advanced melanoma. N Engl J Med. 2013;369:122-133.
5.Robert C, Ribas A, Wolchok JD, Hodi F, Hamid O, Kefford R, et al. Anti-programmed-death-receptor-1 treatment with pembrolizumab in ipilimumab refractory advanced melanoma: A randomised dose-comparison cohort of a phase 1 trial. Lancet. 2014;384:1109-1117.
6.Ishida Y, Agata Y, Shibahara K, Honjo T. Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death. EMBO J. 1992;11(11):3887-3895.
7.Freeman GJ, Long AJ, Iwai Y, Bourque K, Chernova T, Nishimura H, et al. Engagement of the PD-1 immunoinhibitory receptor by a novel B7 family member leads to negative regulation of lymphocyte activation. J Exp Med. 2000;192(7);1027-1034.
8.Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, et al. Tumor-associated B7-H1 promotes T-cell apoptosis: A potential mechanism of immune evasion. Nat Med. 2002;8(8):793-800.
9.Rosenberg SA, Spiess P, Lafreniere R. A new approach to the adoptive immunotherapy of cancer with tumori nfiltrating lymphocytes. Science. 1986;233(4770):1318-1321.
10. Le DT, Uram JN, Wang H, Bartlett BR, Kemberling H, Eyring AD, et al. PD-1 blockade in tumors with mismatch-repair deficiency. N Engl J Med. 2015;372(26):2509-2520.
11. Overman MJ, McDermott R, Leach JL, Lonardi S, Lenz HJ, Morse MA, et al. Nivolumab in patients with metastatic DNA mismatch repair deficient or microsatellite instability-high colorectal cancer (CheckMate 142): An open-label, multicentre, phase 2 study. Lancet Oncol. 2017;18(9):1182-1191.
12. Marabelle A, Fakih M, Lopez J, Shah M, Shapira-Frommer R, Nakagawa K, et al. Association of tumour mutational burden with outcomes in patients with advanced solid tumours treated with pembrolizumab: Prospective biomarker analysis of the multicohort, open-label, phase 2 KEYNOTE-158 study. Lancet Oncol. 2020;21(10):1353-1365.
13.Yarchoan M, Albacker LA, Hopkins AC, Montesion M, Murugesan K, Vithayathil T, et al. PD-L1 expression and tumor mutational burden are independent biomarkers in most cancers. JCI Insight. 2019;4:e126908.
14. Fancello L, Gandini S, Pelicci PG, Mazzarella L. Tumor mutational burden quantification from targeted gene panels: Major advancements and challenges. J Immunother Cancer. 2019;7:183.
15. Backenroth D, Shao C, Li G, Huang L, Pruitt SK, CastellanosE, et al. Prevalence and prognostic effect of high tumor mutation burden (TMB-H) across multiple less common solid cancers using a real- world dataset. Ann Oncol. 2019;30 (suppl 5):v760-796.
16. Stenzinger A, Allen JD, Maas J, Stewart MD, Merino DM, Wempe M, et al. Tumor mutational burden standardization initiatives: recommendations for consistent tumor mutational burden assessment in clinical samples to guide immunotherapy treatment decisions. Genes Chromosomes Cancer. 2019;58:578-588.
17. Hellmann MD, Ciuleanu TE, Pluzanski A, Lee JS, Otterson G, Audigier-Valette C, et al. Nivolumab plus ipilimumab in lung cancer with a high tumor mutational burden. N Engl J Med. 2018;378: 2093-2104.
18. Ready N, Hellmann MD, Awad MM, Otterson G, Gutierrez M, Gainor JF, et al. First-line nivolumab plus ipilimumab in advanced non-small-cell lung cancer (CheckMate 568): Outcomes by programmed death ligand 1 and tumor mutational burden as biomarkers. J Clin Oncol. 2019;37:992-1000.
19. Yarchoan M, Hopkins A, Jaffee EM. Tumor mutational burden and response rate to PD-1 inhibition. N Engl J Med. 2017;377:2500-2501.
20. Lee M, Samstein RM, Valero C, Chan TA, Morris LGT. Tumor mutational burden as a predictive biomarker for checkpoint inhibitor immunotherapy. Hum Vaccin Immunother. 2020;16(1):112-115.
21. Hellmann M, Paz-Ares L, Reyes BC, Zurawski B, Kim SW, Carcereny CE, et al. Nivolumab plus Ipilimumab in advanced non–small-cell lung cancer. N Engl J Med. 2019;381:2020-2031.
22. Rizvi NA, Hellmann MD, Snyder A, Kvistborg P, Makarov V, Havel J, et al. Cancer immunology. Mutational landscape determines sensitivity to PD-1 blockade in non-small cell lung cancer. Science. 2015;348:124-128.
23. Herbst RS, Lopes G, Kowalski DM, NishioM, Wu YL, de Castro Junior G, et al. Association between tissue TMB (tTMB) and clinical outcomes with pembrolizumab monotherapy (pembro) in PD-L1-positive advanced NSCLC in the KEYNOTE-010 and -042 trials. Ann Oncol. 2019;30: v916-17.
24. Ott PA, Bang YJ, Piha-Paul SA, Abdul Razak A, Bennouna J, Soria JC, et al. T-cell-inflamed gene expression profile, programmed death ligand 1 expression, and tumor mutational burden predict efficacy in patients treated with pembrolizumab across 20 cancers: KEYNOTE-028. J Clin Oncol. 2019;37:318-327.
25. Van Allen EM, Miao D, Schilling B, Shukla SA, Blank C, Zimmer L, et al. Genomic correlates of response to CTLA-4 blockade in metastatic melanoma. Science. 2015;350:207-211.
26. Marabelle A, Le DT, Ascierto PA, Di Giacomo AM, Jesus-Acosta A, Delord JP, et al. Efficacy of pembrolizumab in patients with non- colorectal high microsatellite instability/ mismatch repair-deficient cancer: Results from the phase II KEYNOTE-158 study. J Clin Oncol. 2020;38:1-10.
27. Wen WX, Leong CO. Association of BRCA1- and BRCA2- deficiency with mutation burden, expression of PD-L1/ PD-1, immune infiltrates, and T cell-inflamed signature in breast cancer. PLoS One. 201925;14(4):e0215381.
28. Eisenhauer E, Therasse P, Bogaerts J, Schwartz LH, Sargent D, Ford SR, et al. New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1). Eur J Cancer. 2009;45(2):228 -247.
Notas de autor
borga@arsuve.com
Información adicional
TRABAJO GANADOR PREMIO “Dr. GUSTAVO ROJAS MARTÍNEZ”: 2022