ARTÍCULOS DE REVISIÓN
RADIOCIRUGÍA ESTEREOTÁCTICA EN EL TRATAMIENTO DE LAS METÁSTASIS CEREBRALES. EXPERIENCIA DE 20 AÑOS.
RADIOCIRUGÍA ESTEREOTÁCTICA EN EL TRATAMIENTO DE LAS METÁSTASIS CEREBRALES. EXPERIENCIA DE 20 AÑOS.
Revista Venezolana de Oncología, vol. 35, núm. 2, pp. 93-108, 2023
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 15 Noviembre 2022
Aprobación: 18 Marzo 2023
Resumen: OBJETIVO: Presentar nuestra experiencia de 20 años con radiocirugía estereotáctica en tratamiento de pacientes con metástasis cerebrales. METODO: Se realizó un estudio observacional 193 pacientes con metástasis cerebral sometidos a radiocirugía en el período 2000-2020, fueron divididos en 2 grupos: 1 Radiocirugía estereotáctica sin radioterapia holocraneana previa (92 pacientes) 2. Radiocirugía estereotáctica con radioterapia holocraneana previa (101 pacientes). Se describe la técnica empleada la cual fue evolucionando. Inicialmente utilizamos fracción única con dosis de 1 500-2 400 cGy de acuerdo al tamaño de la lesión, posteriormente régimen de hipofraccionamiento, 5 fracciones de 600 cGy. El régimen de radioterapia holocraneana más utilizado fue el de 3 000 cGy en 10 fracciones. RESULTADOS: La supervivencia global a 2 años para toda la población fue de 39,7 % y a 5 años de 13,9 %. La supervivencia global de acuerdo a los grupos de tratamiento se observó que a los 5 años en los pacientes del grupo 1 parece ser mejor (19,5 %), vs., el grupo 2 (10 %). En los pacientes con metástasis única se observó una aparente mejor supervivencia comparados con aquellos con metástasis múltiples. Se presentan cifras de supervivencia global de acuerdo a la evaluación pronostica por grados GPA. CONCLUSIÓN: La radiocirugía estereotáctica es una modalidad importante en el manejo de los pacientes que debe integrarse con otras modalidades terapéuticas como la cirugía y la radioterapia holocraneal, las indicaciones de esta ultima están cambiando en vista de sus efectos secundarios.
Palabras clave: Metástasis, radiocirugía, estereotáctica, radioterapia.
Abstract: OBJECTIVE: To present our 20 year experience with stereotactic radiosurgery in the treatment of patients with brain metastases). METHOD: An observational study conducted on 193 patients with brain metastases undergoing stereotactic radiosurgery from 2000-2020, they divided into 2 groups: 1. The stereotactic radiosurgery without previous holocranial radiotherapy (92 patients). 2. The stereotactic radiosurgery with previous holocraneal radiation therapy (101 patients). The stereotactic radiosurgery technique used is described, which evolved over time. Initially was used with a single fraction with doses of 1 500-2 400 cGy according to the size of the lesion, then a hypofractionation regimen, five fractions of 600 cGy. The most commonly used holocraneal radiation therapy regimen was 3 000 cGy in 10 fractions. RESULTS: The overall survival at 2 years for the entire population was 39.7 % and at 5 years was 13.9 %. The overall survival according to the treatment groups was observed to be better at 5 years in group 1 patients (19.5 %), versus group 2 (10 %). Patients with single brain metastases showed an apparent better overall survival compared to those with multiple brain metastases. Overall survival figures presented according to prognostic assessment by GPA grades. CONCLUSION: The stereotactic radiosurgery is an important modality in the management of patients with brain metastases, this technique be integrated, with other therapeutic modalities such as the surgery and the holocraneal radiation therapy; the indications of holocraneal radiation therapy are changing in view of its side effects.
Keywords: Metastases, radiosurgery, stereotactic, radiotherapy.
INTRODUCCIÓN
Las metástasis cerebrales (MC) constituyen un problema de gran importancia en la práctica oncológica dada su alta morbilidad y mortalidad asociada. El tratamiento primario continúa siendo la cirugía, la radioterapia holocraneana (RTH) y la radiocirugía estereotáctica (RCE), modalidad que está en continuo desarrollo y es uno de los pilares fundamentales en estas afecciones. Su verdadera incidencia ha sido difícil de determinar, sin embargo, se estima que aproximadamente del 10 % al 40 % de los pacientes con tumores sólidos van a desarrollar metástasis cerebrales. En los EE. UU se calcula una incidencia de 70 000 a 400 000 casos nuevos por año (1). En Venezuela en el registro central de cáncer del programa de oncología del MPPS no se encontraron cifras sobre la incidencia y mortalidad por MC (2).
La incidencia de MC se ha incrementado a través de los años debido al diagnóstico precoz de la enfermedad por el uso de modernos estudios de imágenes como tomografía computarizada y especialmente la resonancia magnética, y los avances en el tratamiento sistémico con una mayor supervivencia de los pacientes con neoplasias avanzadas (1).
La supervivencia de los pacientes con MC ha mejorado en las últimas décadas; en la era cuando el tratamiento con RTH era la modalidad terapéutica fundamental la supervivencia global (SG) media por lo general, era menor de 6 meses (3). En la época contemporánea con la incorporación de nuevas modalidades terapéuticas, la SG media estimada está en 13 meses con un rango de 5-29 meses, dependiendo del tipo del tumor primario (4).
Los tumores primarios que con mayor frecuencia producen MC son cáncer de pulmón 40 %-50 %, mama 15 %-20 %, melanoma 10 %-15 % y primarios desconocidos 10 %-15 %. Su localización está relacionada con el flujo sanguíneo cerebral, el 80 % de las lesiones se originan en los hemisferios cerebrales.
El término radiocirugía fue creado por Leksell en 1951, destacado neurocirujano reconocido como padre de la especialidad, como un método no invasivo para tratar lesiones cerebrales no accesibles a cirugía abierta, empleando un tubo de rayos X de 200 Kv, acoplado a un marco estereotáctico para tratar pacientes con dolor facial (5).
La RCE permite la administración de altas dosis de radiación al tumor, con alto grado de precisión, aproximadamente 1 mm, utilizando técnica estereotáctica, empleando 1-5 fracciones (6).
En la actualidad, la aplicación más frecuente de RCE craneal es en las MC. Inicialmente, esta modalidad terapéutica se utilizó en tumores cerebrales recurrentes y estos estudios sirvieron de base para determinar las dosis máximas tolerables de acuerdo al tamaño de la lesión (7). Posteriormente, se han realizado una serie de estudios aleatorios para evaluar el papel de la RCE como tratamiento adyuvante a la RTH en pacientes con oligometástasis concluyéndose que el tratamiento combinado puede mejorar la supervivencia y el control local (CL) en pacientes con metástasis únicas (8). Igualmente, se han comparado en otros protocolos el valor de la RCE con o sin RTH encontrándose que la RTH mejora el CL y disminuye la aparición de otras MC. Asimismo, se ha estudiado los resultados del tratamiento con cirugía más RTH vs. RCE y RTH, sin observarse una diferencia significativa entre ambos grupos (9).
Aunque es controversial, algunos estudios muestran que la RTH produce mayor déficit neurocognitivo comparado con RCE sola. Por tanto, sus indicaciones de rutina están en estudio y deben individualizarse (10,11,12).
El objetivo del presente trabajo es presentar nuestra experiencia de 20 años con el empleo de RCE en el tratamiento de pacientes con MC, por medio de un análisis de los datos clínicos y los resultados terapéuticos.
MÉTODO
Se realizó una revisión de las historias clínicas de los pacientes con MC tratados con RCE, en la Unidad de Radioterapia Oncológica GURVE del Instituto Médico La Floresta y en el Servicio de Radioterapia Dr. Enrique M. Gutiérrez del Centro Médico Docente La Trinidad, durante el período 2000-2020.
Se presenta una estadística descriptiva de la población en estudio, análisis de los aspectos clínicos, descripción y evaluación de la técnica de tratamiento, sobrevida actuarial y complicaciones del tratamiento radiante.
Los datos obtenidos de las 218 historias clínicas revisadas fueron registrados en una hoja de cálculo en Microsoft Office Excel. Se excluyeron 25 pacientes por no haber recibido tratamiento radiante o no haber finalizado el mismo.
En el presente trabajo se reportan los resultados de 193 pacientes tratados con RCE. Los pacientes se dividieron en 2 grupos: 1. RCE sin RTH previa. 2. RCE con RTH previa.
En nuestra organización se inicia la RCE craneal en el año 2000 en el Instituto Médico La Floresta, utilizando un acelerador lineal VARIAN 2100 C/D con fotones de 6 MV, empleando el sistema Brain Lab con conos de diversos tamaños y usando arcos no coplanares, usualmente se utilizaban 5 arcos con varios isocentros y la planificación se realizaba con el software de Brain Lab. La técnica de inmovilización usada fue el marco estereotáctico. En ese momento, la RCE se administraba en una sola fracción siguiendo, por lo general las pautas de la RTOG según las cuales las dosis máximas tolerables dependen del tamaño de la lesión oscilando de 1 500-2 400 cGy, para tumores de 2 cm - 4 cm. La prescripción se realizó a la periferia del tumor usualmente a la isodosis del 80 % (7). (Figura1).
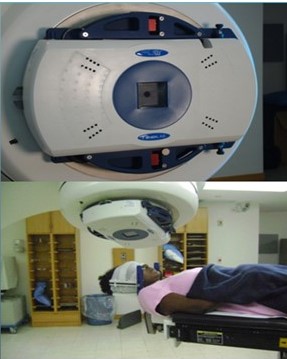
Figura 1
Sistema de conos con arcos no coplanares e inmovilización con marco estereotáct
Posteriormente, partir del año 2006 la RCE se comienza a realizar en el Servicio de Radioterapia Dr. Enrique M. Gutiérrez del Centro Médico Docente La Trinidad, igualmente en un acelerador lineal VARIAN 2100 C/D, para aquel momento se empezaron a emplear máscaras termoplásticas y el colimador micro-multiláminas, los cuales permitieron realizar la RCE no solo con fracción única, si no con régimen de hipofraccionamiento, siendo el esquema más empleado el de 5 fracciones de 600 cGy. El marco estereotáctico de ahí en adelante solo se ha utilizado en campos muy pequeños como es el caso del tratamiento de neuralgias del trigémino. La técnica fue evolucionando y desde entonces pasamos a la radioterapia de intensidad modulada con arcos volumétricos (TAVM) empleando un plan único con un solo isocentro y arcos no coplanares, pudiendo abarcar todas las lesiones metastásicas, utilizando para el posicionamiento las máscaras termoplásticas, manteniendo los controles de posicionamiento. El sistema de planificación de tratamiento ha sido el eclipse 10.0; esta técnica permitió una disminución significativa en el tiempo total de tratamiento y mejorar la conformación de la dosis y disminuir la dosis en los tejidos y órganos a riesgo. (Figura 2).
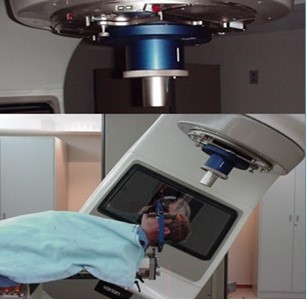
Figura 2
Colimador micro-multiláminas e inmovilización con máscaras termoplásticas.
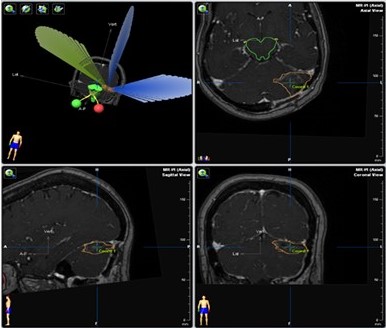
Figura 3
Plan de tratamiento de paciente con carcinoma de mama y MC solitaria resecada. Recibió RCE posoperatoria, fracción única, dosis de 2 000 cGy, empleando 3 arcos con colimador micro-multiláminas.
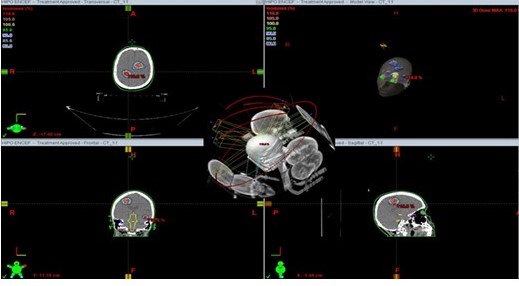
Figura 4.
Plan de tratamiento de un paciente con 4 MC tratadas con TAVM empleando 6 arcos. Recibió RCE con esquema de hipofraccionamiento, 5 fracciones de 600 cGy.
Para caracterizar la población se utilizaron datos como: media, mediana y desviación estándar. Para el análisis de sobrevida se utilizó el método de Kaplan Meier, a fin de obtener curvas de SG de toda la población y de acuerdo al tumor primario y a la evaluación pronóstico por grados (GPA) (4), igualmente se determinó el tiempo de sobrevida media. El método para comparación de los resultados de sobrevida y la respuesta fue el Long Rank Test (13).
Asimismo, se determinó la respuesta al tratamiento clínica y radiológica. Para el seguimiento se utilizaron los datos de la historia clínica de RT; y con los pacientes que no habían acudido a la consulta de RT, se realizó contacto directo con los médicos referentes y otros médicos tratantes, con los pacientes y/o familiares, por vía telefónica o personalmente.
RESULTADOS
En el presente trabajo se reportan los resultados de 193 pacientes tratados con RCE. La población fue dividida en 2 grupos: 1. RCE sin RTH previa, 92 pacientes y 2. RCE con RTH previa, 101 pacientes. En el Cuadro 1 se presenta las características de la población en estudio.
En los pacientes que recibieron RCE como tratamiento inicial (grupo 1) posteriormente en 17 fue necesario administrar RTH y 10 necesitaron de nuevo RCE por presentar nuevas lesiones. En el grupo 2, en 4 pacientes fue necesario administrar RTH de nuevo y en 9 tratamiento adicional con RCE por progresión de la enfermedad intracraneal.
En relación al estatus performance el 66 % de los pacientes tenían un puntaje >90 en la escala de Karnosfky.
En cuanto al número de lesiones, en el grupo 1 predominaron los pacientes con lesiones únicas vs. 38,6 % en el grupo 2. La enfermedad extra-craneal en el momento de la RCE estaba presente en el 54,3 % del grupo 1 y 43,6 % en el grupo 2. En relación al tumor primario, la mayoría de los pacientes presentaban carcinoma de pulmón seguido por carcinoma de la mama.
Se indica en el Cuadro 1, la evaluación pronostica por grados (GPA). Alrededor del 60 % de los pacientes de ambos grupos presentaban un puntaje entre 2-3. La mayoría de las lesiones metastásicas fueron de localización supratentorial. La mayoría de las MC tratadas eran ≤ 20-30 mm. La cirugía se practicó en un total de 19 pacientes, 12 del grupo 1 y 7 del grupo 2. En relación tratamiento sistémico, 16 pacientes del grupo 2 recibieron temozolamida en concurrencia con la RTH.
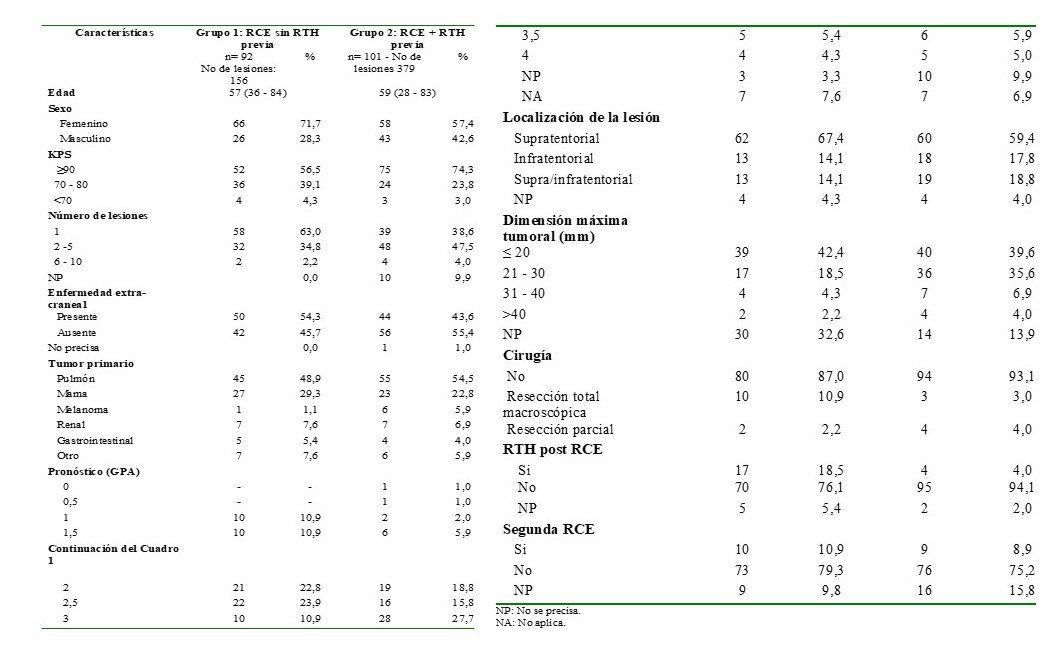
Cuadro 1
Características de la población de acuerdo al grupo de tratamiento.
El tiempo de seguimiento tuvo una mediana de 11,7 meses en el grupo 1 y de 8 meses en el grupo 2. Se evaluó la respuesta clínica, observándose que la mejoría de los síntomas se presentó con más frecuencia en el grupo 1 (sin RTH previa) 33,7 % vs. 22,8 % en el grupo 2. Alrededor del 40 % de los pacientes no se pudo obtener la respuesta clínica o radiológica y en cerca del 50 % de los casos en ambos grupos se observó respuesta radiológica de la enfermedad o estabilización de la misma. En 23 % de los pacientes se observó progresión a nivel del encéfalo (Cuadro 2).
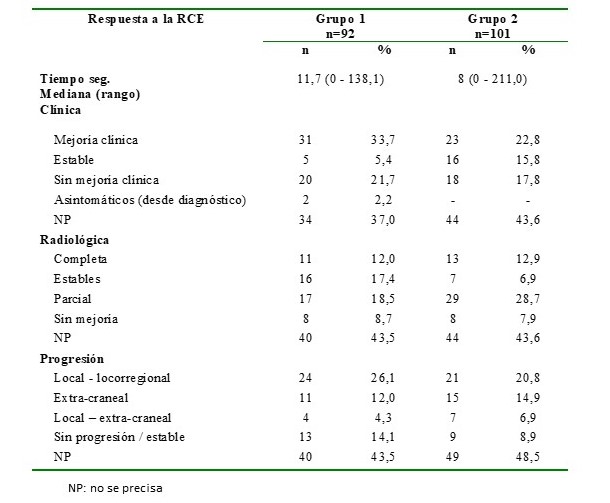
Cuadro 2
Respuesta a la RCE de acuerdo al grupo de tratamiento.
La SG de todos los pacientes tratados con una mediana de seguimiento de 10 meses fue de 39,7 % a los 2 años y 13,9 % a los 5 años (Figura 5).
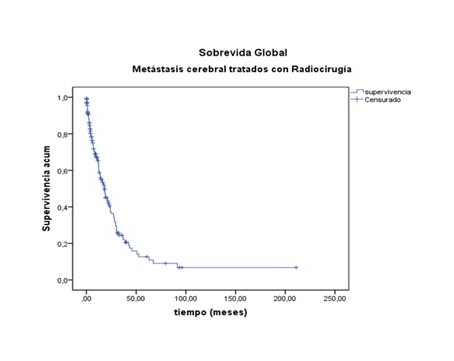
Figura 5
SG de pacientes con MC tratados con RCE
S(2años) = 39,7% ± 4,2 % S(5años) = 13,9% ± 3,9%
Al comparar los 2 grupos de tratamiento, se observó que la SG a los 60 meses en los pacientes sometidos a RCE como tratamiento inicial parece ser mejor 19,5 %, comparado con aquellos tratados con RTH previa 10 %. Esta diferencia probablemente se explica porque los pacientes sometidos a RTH previa presentaban MC más avanzadas que los sometidos a RCE inicial, sin embargo, no fue estadísticamente significativa (P=0,1) (Figura 6).
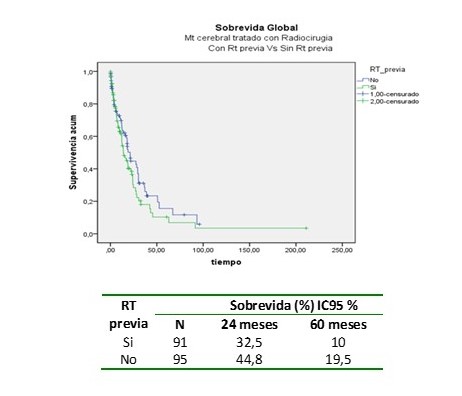
Figura 6
SG de pacientes tratados con RCE
Se analizó igualmente la SG de acuerdo al número de lesiones, encontrando que los pacientes con MC únicas presentaron una sobrevida más favorable a los 24 y 60 meses, en ambos grupos de tratamiento (Figura 7 y 8).
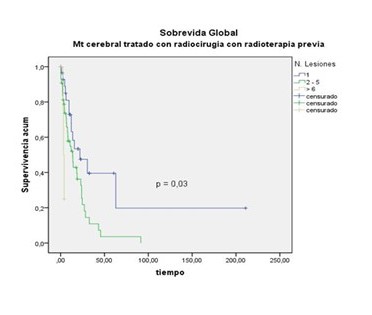
Figura 7.
Pacientes con MC únicas
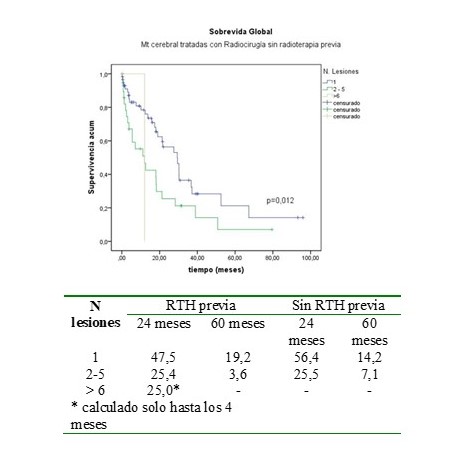
Figura 8.
SG
Por otra parte, se analizó la SG de acuerdo al tamaño de la lesión, encontrando que en el grupo que recibió RTH previa con MC < 20 mm la sobrevida aparentemente fue más favorable, no ocurrió lo mismo en los pacientes del grupo 2 tratados con RCE inicial (Figura 9 y 10).
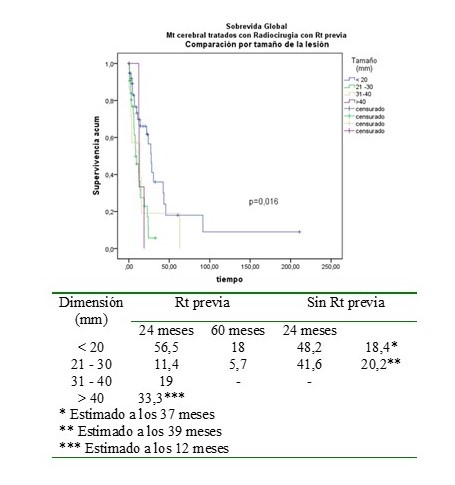
Figura 9
SG por tamaño de la lesión
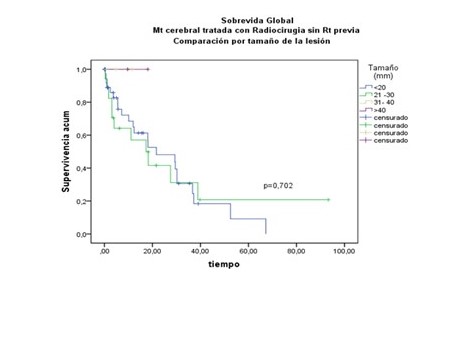
Figura 10.
Grupo 2
Se hizo un análisis de la SG igualmente según el tumor primario observando que en el carcinoma de mama los resultados fueron más favorables, seguido por carcinoma de pulmón, sin embargo, no hubo diferencias estadísticamente significativas. El número de pacientes con melanoma, tumores renales y gastrointestinales fue muy reducido (Cuadro 3).
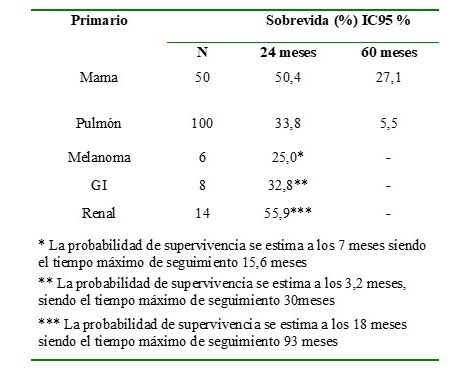
Cuadro 3
SG según el tumor primario.
La sobrevida media de acuerdo a la clasificación pronostica por grados (GPA) de acuerdo al puntaje se presenta en el Cuadro 4. Para los pacientes con carcinoma de mama y pulmón parece haber una relación del pronóstico acuerdo al puntaje de esta clasificación, los pacientes con GPA más altos presentaron tiempos de sobrevida más favorables. El grupo de los pacientes con melanoma, tumores renales y gastrointestinales fue muy reducido.
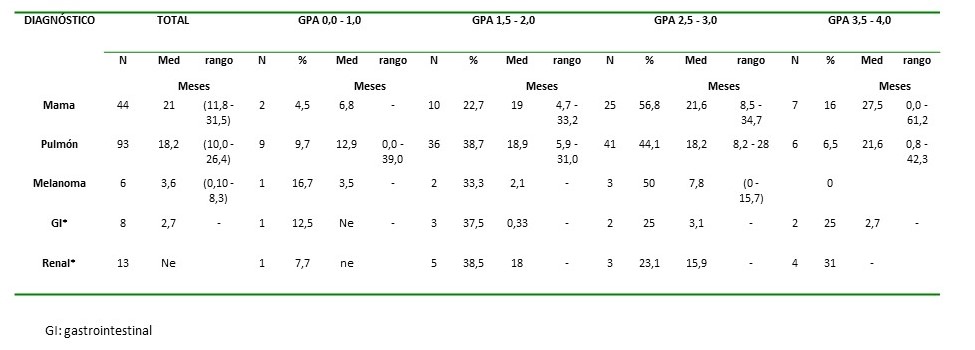
Cuadro 4.
Sobrevida media de acuerdo a la evaluación pronóstico por grados (GPA).
GI: gastrointestinal
En relación a las complicaciones, los pacientes que fueron sometidos a RTH desarrollan alopecia, dermatitis grado I-II, otitis y fatiga y problemas cognitivos como se explicará más adelante. Las complicaciones de RCE registradas en esta serie fueron pocas, solo se reportaron 4 casos de radio-necrosis en los pacientes sometidos a la RCE inicial. La RCE sobre la RTH tiene la ventaja de evitar la alopecia, dermatitis y disminuye la incidencia en los trastornos cognitivos. Probablemente, en esta serie existe sub-registro en cuanto a las complicaciones debido a la naturaleza de este estudio y a la falta de seguimiento.
DISCUSIÓN
El pronóstico de los pacientes con MC ha sido objeto de diversos estudios. En los estudios iniciales con el análisis de partición recursiva se estudiaron factores como el estado general por la escala de Karnosfky (KPS), la extensión de la enfermedad extra-craneal y la edad, que permitieron separar a los pacientes en 3 grupos pronóstico, este modelo fue de utilidad en el pasado (14).
Sin embargo, en la actualidad se han dividido los pacientes en 6 grupos de acuerdo al tumor primario: carcinoma del pulmón no células pequeñas (CNCP) tipo adenocarcinoma, CNCP del pulmón no adenocarcinoma, cáncer de mama, melanoma, carcinoma de células renales y canceres gastrointestinales. Incorporando en cada uno de estos grupos otros factores como el KPS, el número de MC, presencia de enfermedad extra-craneal, edad, y diagnóstico molecular. De acuerdo con este estudio que incluyó cerca de 7 000 pacientes se establecieron 4 grupos de riesgo en base a una evaluación pronóstico por grados (GPA) para cada uno de los 6 grupos de tumor primario. Esta escala ha sido de mayor utilidad para definir el pronóstico de la enfermedad, y en la selección de la terapéutica (4).
En el presente estudio de 193 pacientes se trató de clasificar los pacientes de acuerdo al GPA y se encontró una correlación entre el puntaje y el tiempo de sobrevida media en los pacientes con carcinoma de mama y pulmón.
Las indicaciones de la RCE en las MC se han venido modificando a medida que se acumula más experiencia clínica (15,16.17). En la actualidad en las pautas de la Sociedad Americana de Radioterapia Oncológica (ASTRO) se recomienda el uso de RCE como tratamiento único inicial en pacientes con 1 a 4 MC siempre que tengan adecuadas condiciones generales de acuerdo a la escala de Karnosfky (KPS), ya que la RTH adicional no ha demostrado mejorar la supervivencia y produce mayor deterioro neurocognitivo (17).
El tratamiento óptimo en individuos con 5 o más MC es más controversial pues no hay estudios aleatorios prospectivos en este grupo. Sin embargo, en un estudio prospectivo observacional, encontraron que en pacientes con 1 a 10 MC y un volumen acumulativo ≤ 15 cm³ tratados con RCE se observó que el tiempo de supervivencia posterior a la RCE no fue inferior al obtenido en aquellos con 1 a 4 MC. Además, no se observaron diferencias en el deterioro de la función neurológica, muerte por causas neurológicas, recidiva local, aparición de nuevas lesiones, tratamiento de rescate con RCE o RTH, diferencias en el test del estado mini-mental, y efectos adversos entre estas dos cohortes(18,19). En base a este estudio en las pautas de la ASTRO se recomienda con carácter condicional el empleo de RCE en pacientes con 5 a 10 MC, si su estado general de acuerdo con la clasificación de la ECOG (Eastern Cooperative Oncology Group) es grado de 2 o superior (17).
Los pacientes con 11 a 15 MC no se incluyen en las recomendaciones con carácter condicional de la ASTRO para tratamiento con RCE (17) ya que no existe evidencia suficiente en los estudios retrospectivos (17,18,19) y se esperan los resultados de un ensayo clínico prospectivo donde se está comparando la RTH con la RCE en pacientes con 5 a 15 MC (17).
En el presente estudio de los 193 pacientes tratados con RCE, el 50 % de los pacientes presentaban lesión única y 41 % de 2 a 5 lesiones. En cuanto a la supervivencia de acuerdo al número de lesiones, se encontró una diferencia significativa en favor de los pacientes con MC única en comparación con aquellos con MC múltiples. También se encontraron resultados más favorables de SG en lesiones < 20 mm solo en el grupo que recibió RTH previa.
En la selección de los pacientes con MC para tratamiento inicial con RCE, no solo hay que tener en cuenta el número de metástasis; existen otra serie de factores a considerar como: KPS, edad, localización del tumor primario y su histología, extensión de la enfermedad extra-craneal, diagnóstico molecular y otros señalados en la GPA (4) así como las posibilidades de realizar un control riguroso de la enfermedad craneal con resonancia magnética periódica cada 2 a 3 meses después de la RCE por 1 a 2 años y luego cada 4 a 6 meses indefinidamente, etc. (17). Es fundamental que las decisiones terapéuticas en este sentido sean tomadas por un equipo interdisciplinario que incluya neurocirujanos, neuroradiólogos, radioterapeutas oncólogos, oncólogos médicos, para ofrecer la mejor alternativa a estos pacientes.
En cuanto a la dosis óptima de RCE, el estudio de la RTOG 90-05 (en pacientes tratados con tratamiento focal o RTH previa) estableció las bases para el tratamiento con fracción única, según al tamaño de la lesión, se dividieron los tumores en 3 categorías de acuerdo al diámetro máximo: ≤ 2 cm, 2,1 cm-3 cm y 3,1cm-4 cm siendo las dosis máximas tolerables de 2 400, 1 800 y 1 500 cGy, respectivamente. En esta serie de 156 pacientes con tumores primarios cerebrales (36 %) y MC (64 %) se observó progresión tumoral local en 48 % después de la radiocirugía, siendo el riesgo de progresión casi 3 veces mayor en tumores primarios cerebrales comparados con MC y el riesgo de neurotoxicidad mayor en tumores de 21 mm a 40 mm comparado con tumores menores de 20 mm. La incidencia actuarial de radio-necrosis a los 2 años fue de 11 % (7).
En una revisión de más de 1 700 pacientes tratados con RCE (más de 2 700 lesiones) en 21 publicaciones, se encontró un CL promedio de 83 % con una sobrevida media de 9,6 meses estas cifras son comparables a los reportes quirúrgicos. Se encontró una relación dosis -respuesta con resultados más favorables en casos que recibieron dosis ≥ 1800 cGy (20).
En la actualidad en caso de lesiones mayores de 2 cm estamos utilizando técnicas de hipofraccionamiento (HF) que permiten la reparación del daño por radiación y recuperación de los tejidos normales con disminución de la toxicidad y permiten administrar dosis acumulativas al tumor mejorando las posibilidades de CL. Los regímenes más utilizados han sido 2 700 cGy en 3 fracciones de 900 cGy, el cual al compararse con regímenes de una sola fracción (UF) produjo cifras de CL de 91 % vs. 77 % con UF (21). Siendo la incidencia de radio-necrosis 8 % vs. 20 %, respectivamente. Resultados similares han sido reportados igualmente con regímenes de 3 000 cGy en 5 fracciones de 600 cGy cada una. En las series del Hospital Memorial de NY (MSKCC) de 195 pacientes tratados con este esquema se encontró CL de la enfermedad de 83 % y 64 % a los 12 y 24 meses respectivamente; el tamaño de la lesión fue el factor predictivo más importante; tumores ≥ 2,8 cm presentaron CL en 79 % vs. 87 % en aquellos < 2,8 cm (P=0,04) (22). Este último esquema lo hemos venido empleando con mayor frecuencia en los pacientes con MC > 2 cm.
En pacientes sometidos a resección quirúrgica por MC únicas existe un riesgo de recidiva local en el lecho quirúrgico de 50 % a 60 % en el primer año después de la cirugía (23,24). Por eso se ha empleado la RTH la cual reduce el riesgo de recidiva local y a distancia en otras áreas del cerebro en más del 50 %, pero no mejora la supervivencia (23). Sin embargo, existen complicaciones asociadas con la RTH como alopecia, fatiga y deterioro en las funciones neurocognitivas.
Por las razones antes mencionadas en los últimos años se ha venido utilizando la RCE posoperatoria a la cavidad de la resección quirúrgica como alternativa a la RTH. En un estudio fase III del Hospital MD Anderson (MDACC), en 131 pacientes con 1 a 3 lesiones cerebrales sometidos a cirugía se comparó la RCE posoperatoria al lecho quirúrgico con dosis de 1 200 a 1 600 cGy, vs., observación; observando una mejoría en el CL en 1 año con la RCE 72 % vs. 45 % con observación únicamente. No se presentaron complicaciones significativas con la RCE (25).
En otro ensayo clínico fase III multiinstitucional se comparó la RCE posoperatoria con (dosis 1 200 a 2 000 cGy en FU) vs. RTH (3 000cGy en 10 fracciones o 3 750 cGy en 15 fracciones), en pacientes con MC resecadas. Se observó que el CL a los 12 meses fue inferior en el grupo de RCE 61 % vs. 81 % con RTH al igual que el control intracraneal global 55 % vs. 81 % a los 6 meses, sin diferencias en la sobrevida media global 12,2 vs. 11,6 meses. El deterioro cognitivo a los 6 meses fue menor con RCE 55 % vs. 85 % con RTH (26).
En cuanto a las dosis utilizadas en RCE posoperatoria recomendadas varían de 1 200 cGy a 2 000 cGy con UF de acuerdo al volumen de la cavidad pos cirugía (26). En cavidades de mayor tamaño > 3 cm es preferible utilizar RCE con HF, esquemas de 2 700 cGy en 3 fracciones han producido resultados satisfactorios en estos casos (27).
En un meta-análisis reciente que incluyó 3 458 pacientes de 50 estudios tratados con RCE posoperatoria la cavidad quirúrgica se encontró que los regímenes de RCE con HF se asociaron con mejores cifras de CL 87,3 % vs. 80 % con aquellos de UF, la aparición de radio-necrosis fue solo de 6,9 % y la aparición de enfermedad leptomeníngea se observó en 13 % en todos los estudios analizados. El control de la enfermedad cerebral a distancia al año fue de 52,8 % (28).
Otra estrategia que está en estudio es el empleo de RCE preoperatoria focalizada en MC, para disminuir la incidencia de enfermedad leptomeníngea nodular, uno de los patrones de recaída observados en los pacientes tratados con RCE posoperatoria, la cual acarrea un pronóstico desfavorable. En un análisis retrospectivo se comparó la RCE preoperatoria vs. RCE posoperatoria, observándose una reducción en la aparición de enfermedad meníngea nodular de 16,6 % con RCE posoperatoria a 3,2 % con RCE preoperatoria, con una disminución igualmente de las cifras de radio-necrosis 16,4 % vs. 4,9 % (29).
En nuestra experiencia de 92 pacientes tratados con RCE inicialmente, 12 pacientes fueron sometidos a cirugía previa con resección parcial o total de la lesión y en el grupo de 101 pacientes que recibió RTH previa a la RCE, a 7 pacientes se les practicó cirugía para resección de la lesión. Este grupo será objeto de un análisis futuro cuando se acumulen mayor número de casos.
La RTH sigue teniendo un papel importante en las MC. Aunque sus indicaciones se han ido modificando, en la actualidad se considera que debe emplearse como tratamiento inicial en aquellos pacientes no elegibles para cirugía y o RCE. Entre ellos los individuos en malas condiciones con estado general funcional de acuerdo a la escala ECOG 3-4, todos aquellos con más de 10 MC salvo algunas excepciones, en las recaídas con enfermedad cerebral extensa después de RCE con o sin cirugía previa, asimismo, en los pacientes que no se puedan realizar un seguimiento riguroso después de la RCE con estudios de RM cada 2 a 3 meses. El empleo de RTH adyuvante en pacientes con pronóstico favorable y MC limitadas sometidos a RCE no se recomienda de rutina (17). Es importante clasificar a los pacientes de acuerdo con la evaluación pronóstico por GPA para orientar la terapéutica (4).
En cuanto a las dosis de RTH, el esquema más recomendado según un estudio fase 3 reciente es 3 000 cGy en 10 fracciones (30). En pacientes en muy malas condiciones se pueden emplear esquemas más cortos como 2 000 cGy en 5 fracciones (17).
En la presente serie de 193 pacientes tratados con RCE, el 52 % recibieron RTH previa, usualmente una dosis de 3 000 cGy en 2 semanas y luego recibieron RCE al haber progresión o persistencia de alguna lesión, el resto (92 pacientes) fueron sometidos a RCE inicial y posteriormente, 17 requirieron RTH por progresión de la enfermedad. La SG a los 2 años para toda la población (193 pacientes) fue de 39,7 % y a los 5 años de 13,9 %. Si se compara el grupo de pacientes tratados con RTH previa con aquellos sometidos a RCE como tratamiento inicial se encontró que la supervivencia aparentemente fue más favorable en este último grupo, a los 24 y 60 meses, estos resultados pueden explicarse por el hecho de que los pacientes sometidos a RTH presentaban enfermedad cerebral más avanzada, sin embargo, esta diferencia no fue estadísticamente significativa.
En vista de los efectos secundarios conocidos de la RTH se han venido estudiando una serie de estrategias para disminuir su toxicidad especialmente el deterioro cognitivo. En este sentido se han utilizado diversos agentes neuroprotectores. Entre ellos la Memantina ha sido una de las drogas con efectividad, como fue demostrado en el estudio RTOG 0614, donde los pacientes con MC tratados con RTH fueron divididos aleatoriamente, para recibir Memantina vs., placebo. El grupo tratado con Memantina presentó mejor función cognitiva a través del tiempo, específicamente esta droga retrasó el tiempo de aparición de problemas cognitivos, y de decaimiento de la memoria de reconocimiento, función ejecutiva y velocidad de procesamiento, en pacientes tratados con RTH (31).
Otra alternativa para mejorar el deterioro cognitivo ha sido la protección del hipocampo (PDH) durante la RTH, ya que esta región cerebral contiene células neurales primitivas responsables de la memoria. En un estudio fase II RTOG 0933 se demostró una reducción del deterioro neurológico en base al test de Hopkin de 4 % con PDH vs. 30 % en controles históricos (32). En otro trabajo fase III de la NRG se comparó la RTH con o sin PDH (en ambos grupos se empleó Memantina) observándose una reducción significativa del deterioro neurocognitivo, reducción relativa del riesgo 26 % en el grupo con PDH. En pacientes con lesiones cercanas al hipocampo o con enfermedad leptomeníngea no se recomienda la PDH (33). En base a estos resultados en la guía de la ASTRO (17) recomienda el empleo de Memantina y PDH en pacientes con pronóstico favorable sometidos a RTH.
REFERENCIAS
1. Aizer AA, Lamba N, Ahluwalia MS, Aldape K, Boire A, Brastianos PK, et al. Brain metastases: A Society for Neuro-Oncology (SNO) consensus review on current management and future directions. Neuro Oncol. 2022;24(10):1613-1646.
2. Capote L. Resumen del cáncer en Venezuela 2012. Rev Venez Oncol. 2015;27(4):256-268.
3. Borgelt B, Gelber R, Kramer S, Chang C, Davis LW, Perez CA, et al. The palliation of brain metastases: Final results of the first two studies by the Radiation Therapy Oncology Group. Int J Radiat Oncol Biol Phys. 1980;6:1-9.
4. Sperduto PW, Mesko S, Li J, Cagney D, Aizer A, Lin NU, et al. Survival in patients with brain metastases: Summary report on the updated diagnosis-specific graded prognostic assessment and definition of the eligibility quotient. J Clin Oncol. 2020; 38:3773-3784.
5. Leksell I. The stereotaxic method and radiosurgery of the brain. Acta Chir Scand. 1951;102(4):316-319.
6. ACR Practice parameters for performance of brain stereotactic radiosurgery, revised 2016 (resolution 41). Disponible en: URL: https://www.acr.org/-/media/ACR/Files/Practice-Parameters/stereobrain.pdf
7. Shaw E, Scott C, Souhami L, Dinapoli R, Kline R, Loeffler J, et al. Single dose radiosurgical treatment of recurrent previously irradiated primary brain tumors and brain metastases: Final report of RTOG protocol 90-05. Int J Radiat Oncol Biol Phys. 2000;47(2):291-298.
8. Andrews DW, Scott CB, Sperduto PW, Flanders AE, Gaspar LE, Schell MC, et al. Whole brain radiation therapy with or without stereotactic radiosurgery boost for patients with one to three brain metastases: Phase III results of the RTOG 9508 randomised trial. Lancet. 2004;363(9422):1665-1672.
9. Scoccianti S, Ricardi U. Treatment of brain metastases: Review of phase III randomized controlled trials. Radiother Oncol. 2012;102(2):168-179.
10. Brown PD, Jaeckle K, Ballman KV, Farace E, Cerhan J, Anderson SK, et al. Effect of radiosurgery alone vs. radiosurgery with whole brain radiation therapy on cognitive function in patients with 1 to 3 brain metastases: A randomized clinical trial. JAMA. 2016;316(4):401-409.
11. Mehta MP. The controversy surrounding the use of whole-brain radiotherapy in brain metastases patients. Neuro Oncol. 2015l;17(7):919-923.
12. Chang EL, Wefel JS, Hess KR, Allen PK, Lang F, Kornguth DG, et al. Neurocognition in patients with brain metastases treated with radiosurgery or radiosurgery plus whole-brain irradiation: A randomised controlled trial. Lancet Oncol. 2009;10(11):1037-1044.
13. Matthews DE, Farewel VT. Using and understanding medical statistics. 4. edición. Londres: Karger AG; 2007.
14. Gaspar L, Scott C, Rotman M, Asbell S, Phillips T, Wasserman T, et al. Recursive partitioning analysis (RPA) of prognostic factors in three Radiation Therapy Oncology Group (RTOG) brain metastases trials. Int J Radiat Oncol Biol Phys. 1997;37:745-751.
15. Mehta MP, Tsao MN, Whelan TJ, Morris D, Hayman JA, Flickinger JC, et al. The American Society for Therapeutic Radiology and Oncology (ASTRO) evidence-based review of the role of radiosurgery for brain metastases. Int J Radiat Oncol Biol Phys. 2005;63:37-46.
16. Tsao MN, Rades D, Wirth A, Lo S, Danielson B, Gaspar L, et al. Radiotherapeutic and surgical management for newly diagnosed brain metastasis (es): An American Society for Radiation Oncology evidence-based guideline. Prac Radiat Oncol. 2012;2:210-225.
17. Gondi V, Bauman G, Bradfield L, Burri SH, Cabrera A, Cunningham D, et al. Radiation therapy for brain metastases: An ASTRO Clinical Practice Guideline.
18. Hughes RT, Masters AH, McTyre ER, Farris M, Chung C, Page BR, et al. Initial SRS for patients with 5 to 15 brain metastases: Results of a multi-institutional experience. Int J Radiat Oncol Biol Phys. 2019;104:1091-1098.
19. Yamamoto M, Sato Y, Higuchi Y, Kasuya H, Barfod BE. A cohort study of stereotactic radiosurgery results for patients with 5 to 15 versus 2 to 4 brain metastatic tumors. Adva Radiat Oncol. 2020;5:358-368.
20. Boyd TS, Mehta MP. Radiosurgery for brain metastases. Neurosurg Clin N Am. 1999 ;10(2):337-350.
21. Minniti G, Scaringi C, Paolini S, Lanzetta G, Romano A, Cicone F, et al. Single-Fraction versus multifraction (3 Gy × 9 Gy) stereotactic radiosurgery for large (>2 cm) brain metastases: A comparative analysis of local control and risk of radiation-induced brain necrosis. Int J Radiat Oncol Biol Phys. 2016;95(4):1142-1148.
22. Lockney NA, Wang DG, Gutin PH, Brennan C, Tabar V, Ballangrud A, et al. Clinical outcomes of patients with limited brain metastases treated with hypofractionated (5 Gy × 6Gy) conformal radiotherapy. Radiother Oncol. 2017;123(2):203-208.
23. Patchell RA, Tibbs PA, Regine WF, Dempsey RJ, Mohiuddin M, Kryscio RJ, et al. Postoperative radiotherapy in the treatment of single metastases to the brain: A randomized trial. JAMA. 1998; 280:1485-1489.
24. Kocher M, Soffietti R, Abacioglu U, Villà S, Fauchon F, Baumertet BG al. Adjuvant whole-brain radiotherapy versus observation after radiosurgery or surgical resection of one to three cerebral metastases: Results of the EORTC 22952-26001 study. J Clin Oncol. 2011;29:134-141.
25. Mahajan A, Ahmed S, McAleer MF, Weinberg JS, Li J, Brown P, Settleet S, al. Post-operative stereotactic radiosurgery versus observation for completely resected brain metastases: A single-centre, randomised, controlled, phase 3 trial. Lancet Oncol. 2017;18:1040-1048.
26. Brown PD, Ballman KV, Cerhan JH, Anderson K, Carrero X, Whitton A, et al. Postoperative stereotactic radiosurgery compared with whole brain radiotherapy for resected metastatic brain disease (NCCTG N107C/CEC·3): A multicentre, randomised, controlled, phase 3 trial. Lancet Oncol. 2017;18:1049-1060
27. Minniti G, Esposito V, Clarke E, Scaringi C, Lanzetta G, Salvati M, et al. Multidose stereotactic radiosurgery (9 Gy x 3) of the postoperative resection cavity for treatment of large brain metastases. Int J Radiat Oncol Biol Phys. 2013;86: 623-629.
28. Akanda ZZ, Hong W, Nahavandi S, Haghighi N, Phillips C, Kok DL, et al. Post-operative stereotactic radiosurgery following excision of brain metastases: A systematic review and meta-analysis. Radiother Oncol. 2020;142:27-35.
29. Patel KR, Burri SH, Boselli D, Symanowski JT, Asher AL, Sumrall A, et al. Comparing pre-operative stereotactic Radiosurgery (SRS) to post-operative whole brain radiation therapy (WBRT) for resectable brain metastases: A multiinstitutional analysis. J Neuro-Oncol. 2017;131:611-618.
30. Trifiletti DM, Ballman KV, Brown PD, Anderson K, Carrero X, Cerhan JH, et al. Optimizing whole brain radiation therapy dose and fractionation: Results from a prospective phase 3 trial (NCCTG N107C [Alliance]/CEC.3). Int J Radiat Oncol Biol Phys. 2020;106:255-260.
31. Brown PD, Pugh S, Laack NN, Wefel JS, Khuntia D, Meyers C, et al. Memantine for the prevention of cognitive dysfunction in patients receiving whole-brain radio- therapy: A randomized, double-blind, placebo-controlled trial. Neuro-Oncol. 2013;15:1429-1437.
32. Gondi V, Pugh SL, Tome WA, Caine C, Corn B, Kanner A, et al. Preservation of memory with conformal avoidance of the hippocampal neural stem-cell compartment during whole-brain radiotherapy for brain metastases (RTOG 0933): A phase II multi-institutional trial. J Clin Oncol. 2014;32:3810-3816.
33. Brown PD, Gondi V, Pugh S, Tome W Wefel JS, Armstrong TS, et al. Hippocampal avoidance during whole-brain radiotherapy plus memantine for patients with brain metastases: Phase III trial NRG Oncology CC001. J Clin Oncol. 2020;38(10):1019-1029.
Notas de autor
rreyes@radioterapia.com.ve