CARACTERIZACIÓN CLÍNICA DE PACIENTES CON SÍNDROME MIELODISPLÁSICO Y EL USO DE ESCALAS PRONOSTICAS
CARACTERIZACIÓN CLÍNICA DE PACIENTES CON SÍNDROME MIELODISPLÁSICO Y EL USO DE ESCALAS PRONOSTICAS
Revista Venezolana de Oncología, vol. 35, núm. 4, pp. 225-231, 2023
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 12 Abril 2022
Aprobación: 10 Junio 2023
Resumen: OBJETIVO: Determinar las características clínicas de pacientes con síndrome mielodisplásico usando el sistema de puntaje pronóstico internacional revisado y el sistema de puntaje pronóstico basado en la clasificación de la Organización Mundial de la Salud. MÉTODO: Estudio observacional, descriptivo, retrospectivo, transversal, incluyó pacientes con síndrome mielodisplásico atendidos en tercer nivel de complejidad entre 2013 y 2018 con criterios de inclusión que fuera diagnóstico confirmado mediante extendido de sangre periférica, aspirado de médula ósea, hemoleucograma y/o cuadro clínico compatible con la enfermedad. RESULTADOS: Se incluyeron 86 pacientes, predominó el sexo masculino con 54,6 %, con una mediana de edad de 69 años. Los principales signos y síntomas asociados con el inicio de la enfermedad fueron astenia y adinamia con un 62,8 % ambas. El 40,7 % cursó con infecciones bacterianas recurrentes como patología asociada a síndrome, el 36 % presentó bicitopenia. El tipo de síndrome más común fue con exceso de blastos en 38,3 %. CONCLUSIÓNES: El síndrome mielodisplásico es una enfermedad hematológica relevante al tener relación con la susceptibilidad de infecciones bacterianas recurrentes, por lo que es necesario hacer uso de estas escalas pronósticas con el objetivo de precisar mejor el tratamiento de estos pacientes.
Palabras clave: Médula ósea, biopsia, pancitopenia, citometría de flujo.
Abstract: OBJECTIVE: To determine the clinical characteristics of patients with myelodysplastic syndromes using the revised international prognostic scoring system and the World Health Organization classification based prognostic scoring system. METHOD: An observational, descriptive, retrospective, transversal study that included patients with the myelodysplastic syndrome treated in high level of complexity between 2013 and 2018 with inclusion criteria that were a confirmed diagnostic through the blood smear, bone marrow aspirate, complete blood count and/or clinical presentation suitable with the disease. RESULTS: 86 patients were included, the male sex prevailed with 54.6 %, 69 years was the median age (min 0 max 96) and the median age of diagnosis was 66 years. The main signs and symptoms associated with the onset of the disease were asthenia and adynamia with 62.8 % each. 40.7 % of the patients had bacterial infections as a pathology associated with the syndrome, 36 % had bicytopenia. The most common type of syndrome was blast excess with 38.3 %. CONCLUSIONS: The myelodysplastic syndrome is a relevant hematologic disease as it is related to recurrent bacterial infections susceptibility, consequently it is necessary to use these prognostic scales aiming to precise a better treatment for these patients.
Keywords: Bone marrow, biopsy, pancytopenia, flow cytometry.
INTRODUCCIÓN
El síndrome mielodisplásico (SMD) es una enfermedad heterogénea causada por anormalidades en la maduración y diferenciación clonal de células madre hematopoyéticas y células multipotenciales presentes en la médula ósea, que se acompaña de displasia en uno o varios linajes celulares, hematopoyesis ineficaz, citopenia periférica y alto riesgo de progresión a leucemia mieloide aguda (LMA); generalmente su etiología es idiopática, sin embargo, se ha demostrado que factores ambientales pueden favorecer la acumulación de mutaciones oncogénicas que lleven a su desarrollo (1,2,3,4,5,6,7,8,9,10).
Entre sus manifestaciones clínicas se encuentran fatiga, palidez, infecciones recurrentes, sangrados, hemorragias y hematomas de acuerdo al tipo y número de citopenias con las que cursen(2, 4,11). El diagnóstico se establece haciendo estudios de médula ósea, los cuales abarcan el extendido de sangre periférica para visualizar grado de displasia, la biopsia medular para medición de porcentaje de blastos y los estudios citogenéticos con la finalidad de detectar anormalidades cromosómicas que ayuden en la sub-clasificación del síndrome (2).
Principalmente se ven afectados pacientes mayores de 60 años del sexo masculino, siendo una enfermedad de presentación rara en niños y jóvenes adultos; la tasa mundial de incidencia es de 4 por cada 100 000 habitantes anualmente en mayores de 60 años y de 30 por cada 100 000 habitantes en mayores de 70 años (2, 6, 7, 11). No obstante, esta incidencia podría ser mayor por el subregistro de casos (9).
El IPSS-R (sistema internacional de puntaje pronóstico revisado) y el WPPS ( sistema de puntaje pronóstico de la Organización Mundial de la Salud OMS), son herramientas útiles para el pronóstico del SMD al permitir la predicción de supervivencia y el riesgo de desarrollo de LMA; al tener en cuenta el número de citopenias, porcentaje de blastos en médula ósea y hallazgos citogenéticos, el IPSS-R es el más usado para clasificar a los pacientes en 5 categorías de riesgo (muy bajo, bajo, intermedio, alto y muy alto) que permiten definir la agresividad del tratamiento y expectativas (8, 9, 12, 13).
El objetivo del presente estudio fue determinar las características clínicas de los pacientes con síndromes mielodisplásicos usando los sistemas IPSS-R y WPPS.
MÉTODO
Se realizó un estudio observacional, descriptivo, retrospectivo, transversal en el que se incluyeron pacientes con diagnóstico de SMD atendidos en una institución de tercer nivel de complejidad en Medellín (Colombia) entre el 2013 y el 2018. Los criterios de inclusión fueron: pacientes con diagnóstico confirmado de SMD mediante extendido de sangre periférica, aspirado de médula ósea, hemoleucograma y/o cuadro clínico compatible con la enfermedad; fueron excluidos los pacientes con diagnóstico de anemia aplásica, mielofibrosis y leucemia mieloide aguda. Se realizó un muestreo no probabilístico de casos consecutivos.
La fuente de información fue secundaria a través de historias clínicas. La unidad de análisis fueron los pacientes con diagnóstico establecido de SMD. El instrumento de recolección que se utilizó fue un formulario estandarizado y diseñado por el grupo de investigación que incluía las variables establecidas en el protocolo del estudio. El análisis se llevó a cabo a través del programa SPSS, empleando un análisis univariado por medio de proporciones, frecuencias absolutas y relativas.
El trabajo de investigación contó con el aval ético correspondiente de las instituciones participantes. Según la Resolución 8430 de 1993 del Ministerio de Salud de la República de Colombia, se clasificó como una investigación sin riesgo ya que no se realizaron intervenciones en la población del estudio.
RESULTADOS
Se incluyeron 86 pacientes y predominó el sexo masculino con 54,6 % (47), la mediana de edad fue de 69 años (min 0 - máx 96) y la mediana de la edad de diagnóstico de SMD fue de 66 años (min 1- máx 96).
En cuanto a los antecedentes personales, el 34,8 % (30) según el reporte de la historia clínica consumía cigarrillos y el 19,7 % (17) tuvo exposición ambiental a hidrocarburos.
Los principales síntomas reportados en las historias clínicas de los pacientes con SMD fueron astenia y adinamia ambos con un 62,8 % (54). Cuadro 1.

Cuadro 1.
Signos y síntomas asociados
* No son excluyentes
Respecto a los antecedentes patológicos se encontraban registrados infecciones bacterianas recurrentes, artritis reumatoide y dermatosis neutrofílica febril aguda en un 40,7 % (35), 3,5 % (3) y 3,5 % (3) respectivamente.
El 36 % (31) de los pacientes con SMD habían sido tratados con quimioterapia y 8,1 % (7) con radioterapia.
En relación a los criterios de la OMS para la clasificación del SMD el 87,5 % (75) tenían alguna clase de citopenia y el 12,8 % (11) de los pacientes tenía presencia de células displásicas en médula ósea; en tanto, respecto a los criterios del IPSS-R el 7 % (6) tenía riesgo genético intermedio-bajo y el 39,5 % (34) cariotipo de clasificación bueno (Cuadro 2).
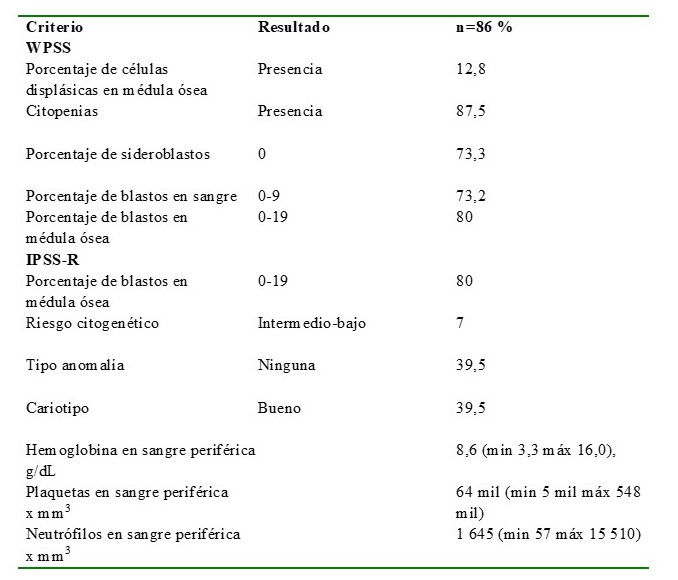
Cuadro 2
Resultados de escalas de clasificación
El reporte de alteraciones cromosómicas fue encontrado en la historia clínica del 84,8 % (73) de los pacientes, los resultados fueron: 9,3 % (8) del (5q) dato compartido para trisomía del 8, 8,1 % (7) mosaicismos, 2,3 % (2) del (17) mismo dato para del (7), monosomía del X y t (11,15); además, el 1,2 % (1) tenía trisomía del 21. Estas alteraciones fueron clasificadas en favorables, desfavorables o intermedias en un 25,6 % (22), 15 % (13) y 24,4 % (21) de los casos, respectivamente.
De acuerdo con el sistema de clasificación propuesto por la OMS, el 38,3 % (33) tenían SMD con exceso de blastos, 15,1 % (13) SMD con displasia multilinaje o unilinaje, 14 % (12) SMD no clasificable, 5 % (4) SMD con sideroblastos en anillo o SMD con del (5q) aislada.
El riesgo de progresión a LMA de acuerdo con el WPSS fue de 31,4 % (27), 19 % (16), 17,4 % (15) y 15,1 % (13) para riesgo alto, intermedio, bajo y muy bajo, mientras que el 13 % (11) de los pacientes tuvieron un resultado de la escala con riesgo muy alto.
Con la escala IPSS-R se calculó el riesgo de progresión del SMD a LMA y se obtuvo que 30 % (25), 24,4 % (21), 22,1 % (19), tenían un riesgo alto, intermedio y bajo respectivamente.
El 71 % (61) de los pacientes del estudio requirió transfusión de paquete de glóbulos rojos.
Respecto a los hallazgos del extendido de sangre periférica en la línea de glóbulos rojos se observó que el 30,2 % (26) de los pacientes tenía presencia de macrocitos, 16,2 % (14) microcitos y el 6 % (5) dacriocitos. En la línea de glóbulos blancos el 16,2 % (14) de los pacientes presentaron mieloblastos y el 8,1 % (7) neutrófilos displásicos, para estos datos en ambas líneas no son excluyentes.
El marcador citogenético más frecuente en los pacientes fue el CD34 con un 55 % (47) Cuadro 3.
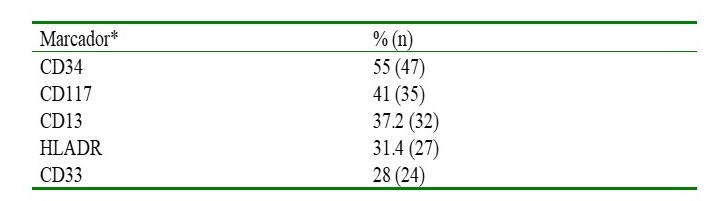
Cuadro 3.
Marcadores citogenéticos en la citometría de flujo
* No son excluyentes
En cuanto a la celularidad en la biopsia de medula ósea el 32,5 % (28) de los pacientes tenían un rango entre 70 % a 100 %. En el 15 % (13) se observó fibrosis en la médula ósea (Cuadro 4).
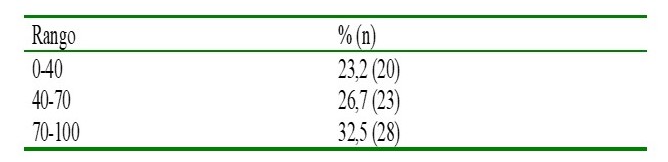
Cuadro 4.
Celularidad en médula ósea
DISCUSIÓN
El SMD es una enfermedad heterogénea con gran impacto en la calidad de vida de los pacientes, ya que su manifestación clínica predominante es la fatiga. Es causado por anormalidades en la maduración de las células madre hematopoyéticas y con el uso de puntajes pronósticos como el IPSS-R y el WPSS se puede predecir la supervivencia y el riesgo de desarrollo de LMA.
En un trabajo realizado por Wu y col., en pacientes con SMD se reportó que el 54,2 % era de sexo masculino con una mediana de edad de 61 años, datos similares a los del presente estudio en el cual predominó el sexo masculino con 54,6 % y la mediana de edad fue de 69 años (5). Por su parte en el estudio realizado por Azevedo y col., en pacientes con la misma condición se obtuvo una mediana de edad de 67 años y predominó el sexo femenino con un 70,7 % (14).
En el estudio realizado por de Swart y col., en 16 países de Europa e Israel en pacientes con SMD de bajo riesgo encontraron una mediana de edad de diagnóstico de 73, 0 años en contraste con la mediana de edad de diagnóstico encontrada en el presente estudio que fue de 66 años (15).
Los principales síntomas presentados por los pacientes con SMD fueron astenia y adinamia ambos con un 62,8 % datos comparables con lo reportado en el estudio realizado por Dhingra y col., en el que se reportaron como síntomas principales debilidad y fatigabilidad en el 81,8 % de los casos (16).
Respecto a los antecedentes personales en el presente estudio el 36 % de los pacientes recibió previamente quimioterapia y el 8,1 % recibió radioterapia, en comparación con el estudio realizado por Radhachandran y col., en EE. UU donde el 4,91 % y 2,57 % de los pacientes recibió quimioterapia y radioterapia respectivamente (2).
En el presente estudio el 87,5 % de los pacientes con SMD tenían alguna clase de citopenia mientras que en el estudio realizado por Majcherek y col., el 100 % de los pacientes la tenían (17).
En la investigación realizada por Wang y col., en China al aplicar la escala IPSS-R se obtuvo que el 32,6 % de los pacientes tenían un riesgo citogenético intermedio o bajo a diferencia de lo encontrado en el presente estudio donde el 7 % de los pacientes con SMD tenía este mismo riesgo (18).
En cuanto a los resultados del reporte de alteraciones cromosómicas en el 9,3 % de los pacientes se encontró del (5q), mientras que en el estudio realizado por Majcherek y col., solo el 2 % de los pacientes presentó esta misma alteración cromosómica (17). En el estudio realizado por Wang y col., se reportaron otras alteraciones en los pacientes donde el 11,3 % tenía trisomía del 8, el 4,1 % del (7), y el 1,2 % trisomía del 21, por su parte en el presente estudio para estas mismas alteraciones se reportaron 9,3 %, 2,3 % y 1,2 % respectivamente (18).
Majcherek y col., respecto al sistema de clasificación del SMD propuesto por la OMS reportaron que el 21 % tenía SMD con displasia unilinaje, el 4 % SMD no clasificable o SMD con exceso de blastos y el 1 % SMD con del (5q) aislada, en cambio, en el presente estudio el 38,3 % de los pacientes tenían SMD con exceso de blastos, el 15,1 % SMD con displasia unilinaje, el 14 % (12) SMD no clasificable y el 5 % SMD con del(5q) aislada (17).
Respecto a los requerimientos transfusionales en el presente estudio el 71 % de los pacientes del estudio requirió transfusión de paquete de glóbulos rojos mientras que en el estudio realizado por Azevedo y col., en Brasil y Argentina fueron requeridas transfusiones en el 62,5 % de los pacientes con SMD (14). A su vez, en el estudio realizado por Dhingra y col., en la India se realizaron transfusiones de paquetes de glóbulos rojos en el 23 % de los pacientes con diagnóstico de SMD (16).
Con relación a los marcadores citogenéticos en biopsia de médula ósea, en el estudio realizado por Azevedo y col., al menos el 2 % de los pacientes con SMD era CD34 positivo, mientras que en el realizado por Majcherek el 3 %, a diferencia del presente estudio en el cual el marcador citogenético más frecuente en los pacientes fue el CD34 con un 55 %(14, 17).
En el presente estudio el 32,5 % de los pacientes tenían un rango de celularidad en médula ósea entre 70 % a 100 % dato comparable con el estudio realizado por Azevedo y col., en el que el 48 % de los pacientes tenía hipercelularidad en médula ósea (14). Además, en el mismo estudio se describió fibrosis de la médula ósea en el 11,7 % a su vez en el presente estudio se observó fibrosis en el 15 % de estos pacientes (14).
El SMD afecta con mayor frecuencia a hombres entre la sexta y séptima década de la vida, y tiene gran impacto en el estado de salud, específicamente en la función medular ya que tienen alto riesgo de progresión a LMA. Es importante el uso de escalas pronosticas como el IPSS-R y el WPSS en la evaluación inicial de estos pacientes para identificar las complicaciones y el pronóstico de manera más eficaz y que esto pueda tener impacto en el manejo de los pacientes. La limitación del estudio es la falta de datos retrospectivos, por lo que se sugiere realizar nuevas investigaciones en la misma población para ampliar los conocimientos acerca del tema.
REFERENCIAS
1. Oster HS, Crouch S, Smith A, Yu G, Abu Shrkihe B, Baruch S, et al. A predictive algorithm using clinical and laboratory parameters may assist in ruling out and in diagnosing MDS. Blood Adv. 2021;5(16):3066-3075. doi: 10.1182/bloodadvances.2020004055.
2. Radhachandran A, Garikipati A, Iqbal Z, Siefkas A, Barnes G, Hoffman J, et al. A machine learning approach to predicting risk of myelodysplastic syndrome. Leuk Res. 2021;109:106639. doi: 10.1016/j.leukres.2021.106639.
3. Wang H, Niu H, Zhang T, Xing L, Shao Z, Fu R. Low- and intermediate-risk myelodysplastic syndrome with pure red cell aplasia. Hematology. 2021;26(1):444-446. doi: 10.1080/16078454.2021.1929694.
4. Petzer V, Theurl I, Weiss G, Wolf D. EnvIRONmental Aspects in Myelodysplastic Syndrome. Int J Mol Sci. 2021;22(10):5202. doi: 10.3390/ijms22105202.
5. Wu A, Gao P, Wu N, Shi C, Huang Z, Rong C, et al. Elevated mature monocytes in bone marrow accompanied with a higher IPSS-R score predicts a poor prognosis in myelodysplastic syndromes. BMC Cancer. 2021;21(1):546. doi: 10.1186/s12885-021-08303-8.
6. Rozo-Agudelo PA, Jaramillo-Arbelaez PE. Características citogenéticas de adultos con síndromes mielodisplásicos según criterios de clasificación de la OMS. Hematol Méx. 2020;21(2):103-114. https://doi.org/10.24245/rev_hematol.v21i2.3611.
7. Park M. Myelodysplastic syndrome with genetic predisposition. Blood Res. 2021;56(S1):S34-S38. doi: 10.5045/br.2021.2020327.
8. Papageorgiou SG, Kotsianidis I, Bouchla A, Symeonidis A, Galanopoulos A, Viniou NA, et al. Serum ferritin and ECOG performance status predict the response and improve the prognostic value of IPSS or IPSS-R in patients with high-risk myelodysplastic syndromes and oligoblastic acute myeloid leukemia treated with 5-azacytidine: A retrospective analysis of the Hellenic national registry of myelodysplastic and hypoplastic syndromes. Ther Adv Hematol. 2020;11: 2040620720966121.
9. Cazzola M. Myelodysplastic Syndromes. N Engl J Med. 2020;383:1358-1374. doi: 10.1056/NEJMra1904794.
10. Shreve J, Nazha A. The evolving landscape of Myelodysplastic Syndrome prognostication. Clin Hematol Int. 2020;2(2):43-48. doi: 10.2991/chi.d.200408.001.
11. Stauder R, Lambert J, Desruol-Allardin S, Savre I, Gaugler L, Stojkov I, et al. Patient-reported outcome measures in studies of myelodysplastic syndromes and acute myeloid leukemia: Literature review and landscape analysis. Eur J Haematol. 2020;104(5):476-487. doi: 10.1111/ejh.13389.
12. Bouchla A, Thomopoulos TP, Papageorgiou SG, Apostolopoulou C, Loucari C, Mpazani E, et al. Predicting outcome in higher-risk myelodysplastic syndrome patients treated with azacitidine. Epigenomics. 2021;13(14):1129-1143. doi: 10.2217/epi-2021-0124.
13. Chen-Liang TH. Prognosis in Myelodysplastic Syndromes: The clinical challenge of genomic integration. J Clin Med. 2021;10(10):2052. doi: 10.3390/jcm10102052.
14. Azevedo RS, Belli C, Bassolli L, Ferri L, Perusini MA, Enrico A, et al. Age, blasts, performance status and Lenalidomide therapy influence the outcome of Myelodysplastic Syndrome with isolated Del(5q): A study of 58 South American Patients. Clin Lymphoma Myeloma Leuk. 2022;22(1):e1-e6.
15. de Swart L, Crouch S, Hoeks M, Smith A, Langemeijer S, Fenaux P, et al. Impact of red blood cell transfusion dose density on progression-free survival in patients with lower-risk myelodysplastic syndromes. Haematologica. 2020;105(3):632-639. doi: 10.3324/haematol.2018.212217.
16. Dhingra G, Dass J, Arya V, Gupta N, Saraf A, Langer S, et al. Evaluation of multiparametric flow cytometry in diagnosis & prognosis of myelodysplastic syndrome in India. Indian J Med Res. 2020;152(3):254-262. doi: 10.4103/ijmr.IJMR_924_18.
17. Majcherek M, Kiernicka-Parulska J, Mierzwa A, Barańska M, Matuszak M, Lewandowski K, et al. The diagnostic and prognostic significance of flow cytometric bone marrow assessment in myelodysplastic syndromes according to the European LeukemiaNet recommendations in single-centre real-life experience. Scand J Immunol. 2021;94(2):e308.
18. Wang X, Liu W, Wang M, Fan T, Li Y, Guo X, et al. Cytogenetic characteristics of 665 patients with myelodysplastic syndrome in China: A single-center report. Oncol Lett. 2021;21(2):126. doi: 10.3892/ol.2020.12387.
Notas de autor
yulis.lobo@upb.edu.com
Información adicional
Agradecimiento: al Hospital Pablo Tobón Uribe por haber hecho posible la ejecución de esta investigación. Financiamiento: la presente investigación no ha recibido ninguna beca específica de agencias de los sectores públicos, comercial, o con ánimo de lucro. Conflicto de intereses:los autores declaran no conflicto de intereses