RADIOTERAPIA EXTERNA HIPOFRACCIONADA EN TRATAMIENTO DE CÁNCER DE MAMA ESTADIO PRECOZ Y LOCALMENTE AVANZADO
RADIOTERAPIA EXTERNA HIPOFRACCIONADA EN TRATAMIENTO DE CÁNCER DE MAMA ESTADIO PRECOZ Y LOCALMENTE AVANZADO
Revista Venezolana de Oncología, vol. 36, núm. 1, pp. 23-31, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 04 Agosto 2023
Corregido: 05 Septiembre 2023
Aprobación: 11 Noviembre 2023
Resumen: OBJETIVO: Actualización en tratamiento del cáncer de mama estadio precoz y localmente avanzado con radioterapia externa hipofraccionada. MÉTODO: Revisión retrospectiva 929 historias con cáncer de mama precoz y localmente avanzado con cirugía preservadora oncológica/mastectomía radical más radioterapia hipofraccionada adyuvante, entre 2009 - 2022; tratadas con radioterapia conformada 3D a la glándula mamaria/pared costal, dosis de 42,56 Gy en 16 fracciones con +/- boost al lecho tumoral. Radioterapia hipofraccionada a fosa supraclavicular en ganglios positivos. RESULTADOS: 879 pacientes. Mediana edad 60 años. 786 (89,41 %) cáncer precoz, más frecuente estadio IA (60,2 %) 93 (10,58 %) localmente avanzado. 779 (88,62 %) carcinoma infiltrante. Cirugía preservadora en 92,03 %, mastectomía parcial oncológica + ganglio centinela 65,1 % y mastectomía radical 7,73 %. 69,1 % de lesiones T1. Dermatitis aguda grado I 66,2 % 13,76 % dermatitis crónica grado I. Tiempo máximo de seguimiento >120 meses. Control locorregional mama precoz 5 y 10 años 98,8 %; localmente avanzado 90,7 %. Sobrevida causa específica mama precoz 5 y 10 años 97,6 % 96,4 % respectivamente; localmente avanzado 5- 10 años 79,26 % - 52,8 %. Sobrevida global para precoz 5 - 10 años 96,5 % 93,9 % avanzado 74,8 % 49,8 % respectivamente. CONCLUSIÓN: La radioterapia hipofraccionada adyuvante ha demostrado ser efectiva, con resultados comparables al fraccionamiento convencional. En 13 años de experiencia, demostraron que el control locorregional, sobrevida causa específica. global, complicaciones y resultados estéticos son excelentes y similares a la literatura internacional.
Palabras clave: Cáncer, mama, radioterapia, hipofraccionamiento, sobrevida.
Abstract: OBJECTIVE: Update on the treatment of early and locally advanced breast cancer with hypofractionated external radiotherapy. METHOD: It is a retrospective review of 929 histories with early and locally advanced breast cancer with oncological sparing surgery/radical mastectomy plus adjuvant hypofractionated radiotherapy, between 2009 - 2022; treated with 3D conformal radiotherapy to the mammary gland/costal wall, dose of 42.56 Gy in 16 fractions with +/- boost to tumor bed. Hypofractionated radiation therapy to supraclavicular fossa in positive nodes. RESULTS: 879 patients. Middle age 60 years. In 786 (89.41%) early cancer, more frequent stage IA (60.2%) 93 (10.58%) locally advanced. 779 (88.62%) infiltrating carcinoma. Preserving surgery in 92.03 %, oncological partial mastectomy + sentinel node 65.1 % and radical mastectomy 7.73 %. 69.1 % of T1 lesions. Acute dermatitis grade I 66.2 % 13.76 % chronic dermatitis grade I. Maximum follow-up time >120 months . Early breast locoregional control 5 and 10 years 98.8 %; locally advanced 90.7%. Early cause-specific breast survival 5 and 10 years 97.6 % 96.4 % respectively, locally advanced 5-10 years 79.26 % - 52.8 %. Overall survival for early 5 - 10 years 96.5 % 93.9 % advanced 74.8 % 49.8 % respectively. CONCLUSION: The adjuvant hypofractionated radiation therapy been shown to be effective, with results comparable to the conventional fractionation. In 13 years of experience, they demonstrated that locoregional control, survival causes specific. Overall, complications and aesthetic results are excellent and similar to the international literature.
Keywords: Cancer, breast, radiotherapy, hypofractionated, survival.
INTRODUCCIÓN
El cáncer de mama (CM) es la neoplasia más común a nivel mundial, una de cada doce mujeres será diagnosticada con esta patología a lo largo de su vida; según la Organización Mundial de la Salud (OMS) se identificaron más de dos millones de nuevos casos en el año 2020 con una mortalidad superior al 25 %. En mujeres jóvenes se ha descrito que 1 de cada 200 mujeres será diagnosticada con CM antes de los 40 años, siendo esto un indicador de pronóstico desfavorable (1,2) relacionada).
Lima SM, y col., realizaron un trabajo de investigación en 2021 en el que concluyeron que la tasa global de mortalidad por CM aumentó 0,23 % por año y la incidencia se incrementó un 1,44 % entre 1990 y 2017 (3).
El tratamiento del CM es multidisciplinario; la Sociedad Americana de Cirugía Oncológica (2021) (4) revisó 19 000 publicaciones de pacientes con CM, seleccionando 30 estudios encontrando que el 58,7 % de las mismas fueron tratadas con mastectomía parcial oncológica (MPO) y radioterapia (RT) vs. 41,3 % que se trataron solo con mastectomía radical (MR), concluyendo que el grupo de pacientes sometidas a tratamiento combinado de MPO y RT tuvo mejor sobrevida global (SG) que aquellas que se sometieron únicamente a mastectomía.
La RT como terapia adyuvante en el cáncer de mama precoz (CMP), convencionalmente se administró a dosis diarias de 1,8 Gy - 2 Gy durante 5 semanas, en 25 fracciones, alcanzando un total de dosis total de 50 Gy, con o sin dosis de refuerzo al lecho tumoral. Con la evolución de la tecnología en RT y la búsqueda de escalar tratamiento, se han propuesto los esquemas de radioterapia hipofraccionada (RT HF). Es decir, aumentar la dosis diaria de radiación, con disminución del número total de fracciones con acortamiento del tiempo de tratamiento. Ensayos clínicos aleatorizados fase III han demostrado la eficacia y seguridad de estos esquemas HF (5,6).
START Trial A (5) comparó el fraccionamiento de RT convencional, 2 Gy/día hasta 50 Gy vs. 41, 60 Gy o 39 Gy en 13 fracciones de 3,2 Gy/día o 3 Gy/día, con un seguimiento de 8 años, concluyendo que la sobrevida libre de enfermedad (SLE) y la SG fueron similares en ambos grupos. El START Trial B (6) encontró que el esquema de HF ofrecía tasas de recidiva tumoral locorregional, efectos adversos tardíos y cosméticos tan favorables como el fraccionamiento convencional
El grupo canadiense (7) comparó el esquema de hipofraccionamiento de 42,5 Gy en 16 fracciones a razón de 2,66 Gy/día vs., el fraccionamiento convencional de 50 Gy en 25 fracciones a razón de 2 Gy/día, en 1 234 pacientes con CMP evidenciando que la incidencia acumulada de recidiva local fue de 6,2 % y 6,7 % respectivamente, con un seguimiento de 10 años. Concluyen que el esquema de HF no es inferior al tratamiento estándar en pacientes con CMP posterior a MPO
López S y col., (8) realizaron una revisión retrospectiva de 449 casos de pacientes con diagnóstico de CMP, tratadas con esquema de HF 42,56 Gy en 16 fracciones, seguida de 3 dosis adicionales dirigidas al lecho tumoral, completando un total de 50,54 Gy, en el período 2009-2015, concluyeron que la SG a 5 años fue de 95,6 % y la SLE 94 %, control locorregional 99,6 % con pocas complicaciones cutáneas, determinando que la RT HF no es inferior a los esquemas de fraccionamiento convencional.
Debido a los excelentes resultados en cuanto a efecto radiobiológico de los esquemas HF, se ha extrapolado esta experiencia del uso de este fraccionamiento a los pacientes con cáncer de mama localmente avanzado (CMLA).
Cassidy RJ y col. (9) evaluaron 3 447 pacientes con CM T3N0 de las cuales el 47,8 % fueron tratadas con radioterapia posmastectomía (RTPM) vs., no RT, determinando que la SG a 5 años fue de 86,3 % RTPM vs. 66,4 % para no RTPM (P <0,01), estadísticamente significativa independientemente de la edad, grado histológico, tamaño del tumor, margen quirúrgico y administración de quimioterapia o terapia hormonal.
Maiti S y col. (10) evaluaron el uso de esquemas hipofraccionados post mastectomía en CMLA vs., el esquema convencional de 25 fracciones, en pacientes con quimioterapia neoadyuvante y/o adyuvante; La recurrencia a 3 años fue similar en los dos grupos, SLE media de 235 semanas para HF vs. 230 para tratamiento convencional, concluyendo que el HF era efectivo en este grupo de pacientes.
Investigadores de la Academia China de Ciencias Médicas presentaron en la Sociedad Americana de Radioterapia Oncológica (ASTRO) 2017 (11) el uso de HF en CM estadio III sin reconstrucción mamaria tratadas con HF vs., fraccionamiento convencional, no evidenciando diferencias significativas en la recurrencia locorregional a los 5 años, con toxicidad similar en ambos grupos.
En el presente trabajo, se expondrán los resultados actualizados de nuestra experiencia en los últimos 13 años, de las pacientes tratadas con esquema de hipofraccionamiento en el Servicio de Radioterapia “Dr. Enrique Gutiérrez” del Centro Médico Docente La Trinidad (CMDL) y la Unidad de Radioterapia Oncológica GURVE ubicada en el Instituto Médico La Floresta (IMLF).
MÉTODO
Se realizó una revisión retrospectiva de las historias de las pacientes con diagnóstico de CM, tratadas con RTHF en el período marzo 2009 - noviembre 2022.
Criterios de inclusión
Diagnóstico de cáncer de mama estadio precoz y localmente avanzado.
Pacientes tratadas con esquemas hipofraccionados
Ganglios negativos o positivos.
Criterios de exclusión
Paciente con enfermedad metastásica al momento del diagnóstico.
Paciente con enfermedades del colágeno.
Pacientes irradiadas previamente.
Se revisaron 929 historias clínicas de pacientes diagnosticadas con CM estadio precoz y CMLA que recibieron RT adyuvante con esquema HF de 2009 a 2022. Fueron excluidas 51 pacientes por tener enfermedad metastásica al momento del diagnóstico y haber sido tratadas con esquemas no hipofraccionados. Todas las pacientes fueron tratadas en acelerador lineal (AL) de energía dual, empleando fotones para irradiar la glándula mamaria/pared costal, áreas de drenaje y electrones o fotones para la dosis adicional al lecho del tumor (boost) en los pacientes que lo ameritaron.
Posterior a la cirugía, se administra RT con técnica conformada con planificación 3D (RTC3D). A todas las pacientes se les realizó tomografía computarizada (TC) de tórax con o sin contraste en inmovilizador de mama; se delimitaron los volúmenes blancos: glándula mamaria y lecho o pared costal, fosa supraclavicular (FSC) según fuera el caso y los órganos a riesgo (OAR): pulmones, corazón, médula espinal y esófago, en cada una de las pacientes. Para la planificación del tratamiento radiante posterior a cirugía preservadora, el volumen tumoral clínico (CTV) incluye toda la glándula mamaria, la cual se delimita mediante marcadores fiduciarios. El volumen de planificación (PTV) incluye el CTV más un margen de 2 cm en sentido cráneo caudal. En las pacientes posmastectomía el CTV incluye la pared costal y/o FSC y el PTV es el CTV más margen para corregir las incertidumbres del posicionamiento. Se emplearon campos tangenciales para el tratamiento de la mama/pared costal y campo directo para la FSC, los cuales se conforman a través del colimador multiláminas para disminuir la irradiación de los OAR (pulmón y corazón) (Figura 1 y 2). Por medio de histogramas dosis-volumen se evalúa la dosimetría, a nivel los volúmenes descritos. Las pacientes fueron tratadas en su mayoría en posición supina con uso de soporte de mama y en algunos casos de mamas péndulas y voluminosas se utilizó la posición prona, en un soporte en el cual la mama a tratar queda suspendida.
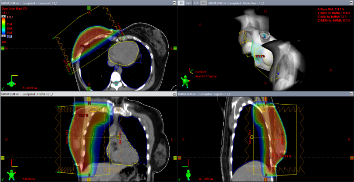
Figura 1
Tratamiento radiante con técnica conformada 3D
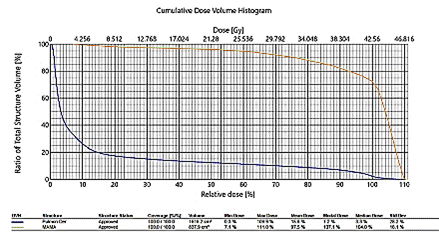
Figura 2.
Histograma dosis volumen
Utilizamos el esquema del grupo canadiense (7), administrando una dosis de 42,6 Gy en 16 fracciones de 2,66 Gy a toda la glándula mamaria; hicimos una modificación a dicho esquema administrando 3 fracciones adicionales al lecho tumoral para un total de 50,54 Gy. Para esta dosis de refuerzo o boost se utilizan electrones o fotones de acuerdo a la profundidad del lecho tumoral. En las pacientes mastectomizadas administramos una dosis de 42,6 Gy en 16 fracciones de 2,66 Gy con o sin boost.
El seguimiento de nuestras pacientes, se realizó con los datos de las historias médicas de los servicios de radioterapia, contacto vía telefónica / correo electrónico e información a través de los médicos referentes.
Se hizo análisis de los datos demográficos, clínicos y de la terapéutica administrada, presentando los resultados de control locorregional, SCE, SG y complicaciones agudas y crónicas del tratamiento.
Para el análisis descriptivo se utilizaron medidas de tendencia central como, promedio, mediana y rangos. La dispersión de datos se estimó con desviación estándar. Para las variables cualitativas se obtuvo frecuencias. Finalmente, para el análisis de SCE y SLE se utilizó el estadístico Kaplan- Meier y las comparaciones se realizaron con Long Rank Test.
La SCE y SLE se calcularon usando el estadístico de Kaplan- Meier. Se usó un programa de cálculo SPSS versión 22 y Microsoft Excel.
RESULTADOS
Se revisaron un total de 929 historias de pacientes tratadas con RT HF adyuvante en CM, se excluyeron 51 pacientes porque no cumplían con los criterios de inclusión. 809 (92,03 %) pacientes tratadas con cirugía preservadora, de las cuales 65,1 % fueron MPO más ganglio centinela (GC) y 68 (7,73 %) MR, entre el período marzo 2009 - noviembre 2022. La mediana de edad fue 60 años con un rango entre 28-91 años.
Se clasificaron por estadios según el sistema de estadificación la American Joint Committee on Cancer (AJCC) 8a edición (12), la mayoría de las pacientes fueron estadios precoces 89,41 % (786), siendo el estadio IA el más frecuente con 60,2 %, seguido del estadio IIA 18,2 %. Los estadios avanzados representan el 10,58 % (93).

Cuadro 1.
Clasificación por estadios.
El carcinoma infiltrante estuvo presente en 88,62 % de las pacientes. No se realizó revisión de la muestra histopatológica.
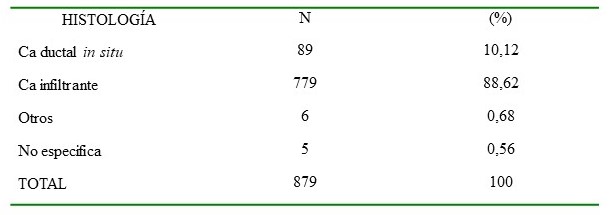
Cuadro 2.
Distribución histopatológica
El tiempo máximo de seguimiento fue superior a 120 meses en 168 pacientes (19,11 %). El tiempo promedio de seguimiento fue de 33,5 meses, con un rango de 0,40 – 163,10 meses, debido al aumento de la población en los últimos años, por lo que no existe el tiempo suficiente para lograr seguimientos más altos.
742 pacientes (84.41 %) se encuentran vivas sin enfermedad (VSE), de las cuales 206 (27,7 %) tienen un seguimiento < 6 meses. Se registraron 10 (1,1 3%) pacientes vivas con enfermedad a distancia (VCE), 13 (1,48 %) muertas con enfermedad (MCE) y 10 (1,14 %) muertas sin enfermedad (MSE).
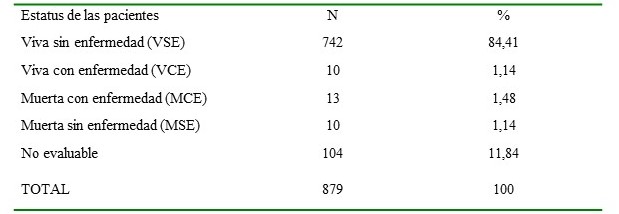
Cuadro 3.
Estatus de las pacientes
COMPLICACIONES
La toxicidad aguda y tardía fue clasificada según los criterios del Grupo de Radioterapia Oncológica (RTOG) (13), tanto para las pacientes CMP como para CMLA, 222 pacientes (25,3 %) no presentaron ningún tipo de complicación durante tratamiento. La complicación aguda más frecuente es la alteración en piel, la radiodermatitis grado I tipo eritema se observó en 582 pacientes (66,2 %), seguida de radiodermatitis grado II en 56 pacientes (6,4 %) y radiodermatitis grado III en 6 pacientes (0,7 %). En 5 pacientes (0,6 %) se presentó mastalgia, prurito e hipersensibilidad.

Cuadro 4.
Complicaciones agudas
376 pacientes (66,31 %) no presentaron complicaciones crónicas. 78 pacientes (13,7 %) presentaron con mayor frecuencia radiodermatitis grado I, asociada a resequedad y cambios de pigmentación a nivel de la piel de la mama; radiodermatitis grado II en un 0,18 % y fibrosis en 3,70 % de los casos; en 16,05 % de las pacientes no hubo registro de complicaciones en la historia. Debemos destacar, que luego de haber pasado 24 meses del tratamiento de RT, se observa que el número de pacientes con complicaciones en piel disminuye considerablemente.

Cuadro 5.
Complicaciones crónicas
El control locorregional en pacientes con estadio precoz fue del 98,8 % y en los estadios avanzados de 90,7 % (Figura 3). La SCE para estadio precoz tratadas con RT HF adyuvante a los 5 años y 10 años fue de 97,6 % y 96,4 % respectivamente, con un tiempo promedio de sobrevida de 159,3 meses IC: 95 %; para estadios avanzados la SCE a los 5 y 10 años fue de 79,2 % y 52,8 % respectivamente, con un tiempo promedio de sobrevida de 86,9 meses IC: 95 % (Figura 4).
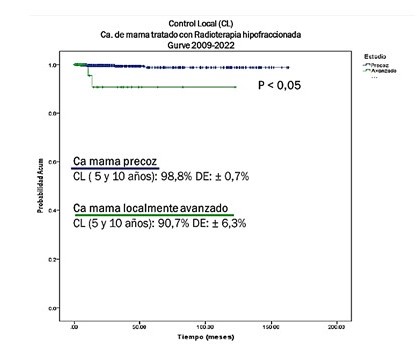
Figura 3
Control local
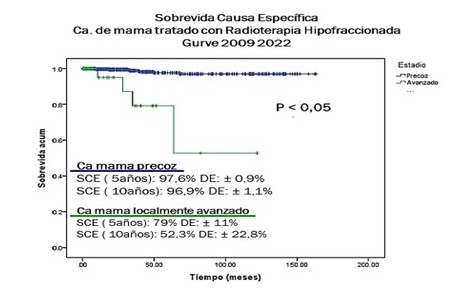
Figura 4
Sobrevida Causa Especifíca
Para el grupo de CMP, la SG a los 5 años y 10 años, luego de haber recibido RT HF fue de 96,5 % y 93,9 % respectivamente, siendo el tiempo medio de SG 154,9 meses IC: 95 % (150.9:158.8) (Figura 5). En las pacientes con CMLA, la SG a los 5 años y 10 años, luego de haber recibido RT HF fue de 74,8 % y 49,8 % respectivamente, con un tiempo medio de SG de 82,9 meses IC: 95 % (54,0: 111,8).
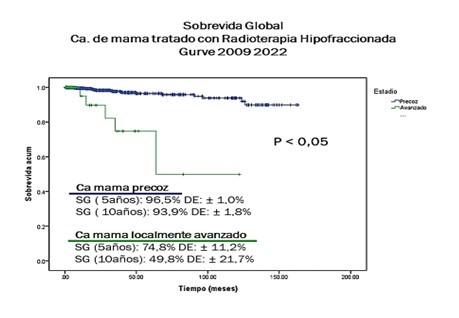
Figura 5
Sobrevida Global
DISCUSIÓN
Predecir la respuesta radiobiológica es un desafío en RT, el modelo lineal cuadrático ha sido validado por datos experimentales y clínicos, siendo utilizado principalmente para estimar dosis equivalentes y para predecir la probabilidad de control tumoral y de complicaciones sobre el tejido normal. El tejido mamario tiene una relación alfa/beta (α/β) baja, lo que lo hace sensible a la modificación de la dosis por fracción. Un incremento leve de la dosis diaria por fracción, disminuyendo la dosis total, es equivalente al fraccionamiento convencional con respecto al control local y las complicaciones tardías. Se debe destacar que independientemente del sitio de localización del tumor, histologías similares, muestran consistentemente valores similares de α/β (14).
START Trial A (5) evaluaron 2 236 pacientes con tumores pT1-T3, N0-N1 y compararon el fraccionamiento de RT convencional, 2 Gy/día hasta 50 Gy vs. 41,60 Gy o 39 Gy en 13 fracciones de 3,2 Gy/día o 3 Gy/día, con un seguimiento de 8 años, concluyeron que la SLE y la SG fueron similares en ambos grupos. En el START Trial B (6) se comparó el esquema convencional 50 Gy a razón de 2 Gy/día vs. 40 Gy a razón de 2,67 Gy/día, encontrando que el esquema de hipofraccionamiento ofrecía tasas de recidiva tumoral locorregional, efectos adversos tardíos y cosméticos tan favorables como el fraccionamiento convencional.
El grupo canadiense (7) comparando el esquema de hipofraccionamiento de 42,5 Gy en 16 fracciones a razón de 2,66 Gy/día vs., el fraccionamiento convencional de 50 Gy en 25 fracciones a razón de 2 Gy/día, evidenció que 10 años después del tratamiento la incidencia acumulada de recidiva local fue de 6,2 % y 6,7 % respectivamente, siendo los resultados obtenidos con RTHF no inferiores a la RT convencional. En cuanto a los resultados cosméticos el 71,3 % de las pacientes tratadas con RT convencional y 69,8 % de las pacientes tratadas con RTHF tuvieron un excelente resultado cosmético, concluyendo que la RTHF a toda la mama no es inferior que el tratamiento con RT convencional posterior a MPO.
Cante D y col., (15) analizaron el uso de HF con boost concomitante en carcinoma ductal in situ (CDIS), márgenes negativos y principalmente de bajo grado, en 82 pacientes, con una mediana de seguimiento que fue de 11,2 años (5-15 años) reportando una recurrencia local del 11 %, siendo el 78 % de las mismas carcinoma invasivo.
Maiti S y col., (10) compararon la RT convencional y el esquema hipofraccionado posterior a mastectomía, en pacientes con CM localmente avanzado. 222 mujeres tratadas aleatoriamente con RTHF (40 Gy en 15 fracciones) y RT convencional (50 GY en 25 fracciones) después de MRM junto con quimioterapia neoadyuvante y/o adyuvante. La mediana de seguimiento para las pacientes en el grupo convencional fue de 178 semanas, mientras que las tratadas con esquema hipofraccionado fue de 182 semanas. La recurrencia a tres años fue similar en los dos brazos, la SLE en las pacientes tratadas de forma convencional fue de 230 semanas y en las hipofraccionadas 235 semanas, con un cociente de riesgos instantáneos 1,01 (IC 95 % = 0,32 - 3,19; P= 0,987).
En ASTRO 2017 fue presentado un ensayo aleatorizado de la Academia de Ciencias Médicas de China (11) que comparó la RT posterior a mastectomía HF (43,5 Gy en 15 fracciones) con fraccionamiento convencional posmastectomía (50 Gy en 25 fracciones) en pacientes diagnosticadas con CM estadio III sin reconstrucción mamaria. No se evidenciaron diferencias significativas en la recurrencia locorregional a los 5 años, la toxicidad presentada fue similar en ambos grupos.
En nuestros resultados obtenidos en 879 con CMP y CMLA encontramos que los resultados en cuanto al control local SG, SCE y toxicidad, son comparables los esquemas de tratamiento convencional y los resultados encontrados en la literatura internacional. La SCE en CMP pos tratamiento preservador fue de a los 5 años y 10 años fue de 97,6 % y 96,4 % respectivamente, IC:95 % con un control local de 98,8 %. Para las pacientes con CMLA tratadas con RTHF la SCE a los 5 años y 10 años fue de 79,2,6 % y 52,8 % respectivamente, IC: 95 %, con un control local de 90,7 %. En cuanto a las complicaciones agudas, la más frecuente fue eritema grado I en un 66,2 % de los casos, con buenos resultados cosméticos.
Concluimos que en nuestra experiencia consideramos que el uso de esquemas de HF es seguro y eficaz en pacientes con CMP y CMLA; estos tratamientos ameritan el uso de RT guiada por imágenes con alta tecnología, así como un personal médico y físico médico capacitado para la planificación. En un futuro se presentarán los resultados de su uso en pacientes con reconstrucción mamaria. Los resultados obtenidos en las pacientes con CMLA promueven el uso de este esquema en dichas pacientes.
El HF es un tratamiento seguro en cuanto al control local, SCE, SG y toxicidad para las pacientes con CM, nos permite acortar el tiempo total de tratamiento y lo proponemos para los pacientes con CMLA.
REFERENCIAS
1.Organización Mundial de la Salud (2021) Cáncer de Mama, World Health Organization. World Health Organization. Disponible en: URL: https://www.who.int/es/news-room/fact-sheets/detail/breast-cancer.
2. Sopik, V. International variation in breast cancer incidence and mortality in young women Breast Cancer Res Treat. 2021;186(2):497-507. doi: 10.1007/s10549-020-06003-8.
3. Lima SM, Kehm RD, and Terry MB. Global Breast Cancer Incidence and mortality trends by region, age-groups, and fertility patterns. EClinicalMedicine. 2021;38:100985. doi: 10.1016/j.eclinm.2021.100985
4. De la Cruz Ku G, Karamchandani M, Chambergo-Michilot D, Narvaez-Rojas A, Jonczyk M, Príncipe-Meneses F, et al. Does breast-conserving surgery with radiotherapy have a better survival than mastectomy? A meta-analysis of more than 1,500,000 patients. Ann Surg Oncol. 2022;29(10):6163-6188.
5. START Trialists' Group, Bentzen SM, Agrawal RK, Aird EG, Barrett JM, Barrett-Lee PJ, et al. The UK standardization of breast radiotherapy (START) trial A of radiotherapy hypo-fractionation for treatment of early breast cancer: A randomized trial. Lancet Oncol. 2008;9(4):331-341.
6. START Trialists' Group, Bentzen SM, Agrawal RK, Aird EG, Barrett JM, Barrett-Lee PJ, et al. The UK standardization of breast radiotherapy (START) trial B of radiotherapy hypofractionation for treatment of early breast cancer: A randomized trial. Lancet Oncol. 2008;371(9618):1098-1107.
7. Whelan TJ, Pignol JP, Levine MN, Julian JA, MacKenzie R, Parpia S, et al. Long-term results of hypofractionated radiation therapy for breast cancer. N Engl J Med. 2010;362(6):513-520.
8. López V, Ott I S, Aguirre LP, Urdaneta LN, Vera G A, Ruan SL. Radioterapia hipofraccionada en tratamiento preservador del cáncer de mama estadio precoz experiencia de 6 años. Rev Venez Oncol. 2017;29(1):22-31.
9. Cassidy R, Liu Y, Kahn ST, Jegadeesh NK1, Liu X, Subhedar PD, et al. The role of postmastectomy radiotherapy in women with pathologic T3N0M0 breast cancer. Cancer. 2017;123(15):2829-2839.
10. Maiti S, Meyur S, Mandal BC, Lekshmi R, Susmita S, Biswas S, et al. Comparison of conventional and hypofractionated radiation after mastectomy in locally advanced breast cancer: A prospective randomised study on dosimetric evaluation and treatment outcome. Journal of Radiotherapy in Practice. 2020;(1):30-38.
11. Sayan M, Yehia ZA, Ohri N, Haffty B. Hypofractionated postmastectomy radiation therapy. Adv Radiat Oncol. 2020;6(1):100618.
12. Amin MB, Edge SB, Greene FL, Compton C, Gershenwald JE, Robert K Brookland RK, et al. The Eighth Edition AJCC Cancer Staging Manual: Continuing to build a bridge from a population-based to a more "personalized" approach to cancer staging. CA Cancer J Clin. 2017;67(2):93-99.
13. Cox JD, Stetz JA, Pajak TF. Toxicity criteria of the radiation therapy oncology group (RTOG) and the European Organization for Research and Treatment of Cancer (EORTC). Int J Radiat Oncol Biol Phys. 1995;31(5):1341-1346.
14. van Leeuwen CM, Oei AL, Crezee J, Bel A, Franken NA, Stalpers LJ, et al. The Alfa and beta of tumours: A review of parameters of the linear-quadratic model, derived from clinical radiotherapy studies. Radiat Oncol. 2018;13(1):96.
15. Cante D, Paolini M, Piva C, Petrucci E, Radici L, Ferrario S, et al. Hypofractionation and concomitant boost in ductal carcinoma in situ (DCIS): Analysis of a prospective case series with long-term follow-up. Life (Basel). 2022;12(6):889.