P16 COMO FACTOR PRONÓSTICO EN COMPORTAMIENTO CLÍNICO E HISTOLÓGICO DEL CARCINOMA ESCAMOSO DE CAVIDAD ORAL
P16 COMO FACTOR PRONÓSTICO EN COMPORTAMIENTO CLÍNICO E HISTOLÓGICO DEL CARCINOMA ESCAMOSO DE CAVIDAD ORAL
Revista Venezolana de Oncología, vol. 36, núm. 2, pp. 78-87, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 16 Junio 2023
Aprobación: 18 Diciembre 2023
Resumen: OBJETIVO: Los carcinomas de células escamosas de cavidad oral representan el 90 %95 %. El virus del papiloma humano, se indica como agente etiológico para el carcinoma de células escamosas. La inmunotinción p16 es precisa, disponible y fácil de interpretar en tejido. El propósito del siguiente estudio es evaluar el comportamiento biológico de los carcinomas escamosos de cavidad oral, para considerar el marcador p16, como una herramienta para la toma de decisiones y evaluar si esta condición, mejora o no, pronóstico, recurrencia y supervivencia libre de enfermedad. MÉTODO: Ensayo clínico no aleatorizado, se tomaron pacientes intervenidos por carcinoma escamoso de cavidad oral, desde enero 2015 a enero 2021. Se realizó inmunohistoquímica con p16INK4a. RESULTADOS: 12 pacientes, 6 eran masculinos (50 %) y 6 (50 %) femeninos, 8 (66,67 %) fumadores y 4 (33,33 %) no fumaban. El 50 % (6) fue en lengua derecha, 100 % carcinomas de células escamosas. El tamaño tumoral tuvo un promedio de 2,9 cm, 3 (25 %), tenían ganglios linfáticos positivos, 2 (16,67 %) tenían p16 nuclear positivo y 5 (41,66 %) p16 citoplasmático positivo. CONCLUSIONES: La asociación entre los p16 positivos fumadores y p16 negativos fumadores, es casi similar. El estado ganglionar positivo se relaciona con los p16 negativos. El tamaño tumoral es menor en p16 positivos. Existe tendencia hacia una mejor supervivencia general en los tumores que expresan p16.
Palabras clave: Carcinoma, células escamosas, cavidad oral, virus del papiloma humano.
Abstract: OBJECTIVE: Oral cavity squamous cell carcinomas represent the 90 %-95 %. The human papilloma virus is indicated as the etiologic agent for the squamous cell carcinoma. p16 immunostaining is accurate, available, and easy to interpret in tissue. The purpose of the following study is to evaluate the biological behavior of the oral cavity squamous cell carcinoma to consider the p16 marker as a decision-making tool and to evaluate whether this condition improves or not, the prognosis, recurrence and the disease- free survival. METHOD: It is a non-randomized clinical trial, of patients operated on for the oral cavity squamous cell carcinoma were taken from January 2015 to January 2021 and follow-up was performed. Immunohistochemistry was performed with p16INK4a. RESULTS: Of 12 patients, 6 were male (50 %) and 6 (50 %) were female, 8 (66.67 %) were smokers, and 4 (33.33 %) were non-smokers. In 50 % (6) were in the right tongue, 100 % squamous cell carcinomas. The tumor size averaged was 2.9 cm, 3 (25 %) had positive lymph nodes, 2 (16.67 %) had positive nuclear p16, and 5 (41.66 %) had positive cytoplasmic p16. CONCLUSIONS: The association between p16 positive smokers and p16 negative smokers is almost similar. The positive nodal status correlates with negative p16. Tumor size is smaller in p16 positives. There is a trend toward better overall survival in p16-expressing tumors.
Keywords: Carcinoma, squamous cell, oral cavity, human papilloma virus.
INTRODUCCIÓN
En 2012, 300 000 pacientes (2,1 % del total de casos de cáncer) sufrieron cáncer de cavidad oral, de los cuales 145 000 fallecieron (1). Recientemente, ya existen más de 377 713 nuevos casos, distribuidos en todo el mundo y 177 753 casos de mortalidad por cáncer oral en 2020 (2). Es la neoplasia maligna más común en el sudeste asiático (India, Sri Lanka, Pakistán, Bangladesh y Taiwán) y las regiones del Pacífico (Nueva Guinea y Melanesia) debido al hábito de masticar nuez de betel (3). En Latinoamérica, las prevalencias más altas se reportan en Argentina, sur de Brasil y Uruguay (4). Tiene mayor prevalencia en hombres que en mujeres, 5,8 frente a 2,3 por 100 000 (5). Se observa generalmente en personas mayores de 40 años en comparación con las más jóvenes (3). Representa una carga considerable para la salud pública (6). Las células escamosas constituyen el epitelio que reviste la cavidad oral, por lo tanto, los carcinomas de células escamosas representan el 90 %-95 %, seguido de neoplasias malignas mesenquimatosas, tumores hematológicos y melanomas (7). Los subsitios anatómicos involucrados son: mucosa yugal, piso de la boca, lengua móvil, reborde alveolar, trígono retromolar y paladar duro (5).
Biológicamente, los cánceres orales pueden desarrollarse a partir de lesiones displásicas premalignas, que están clínicamente presentes en eritroplasia, leucoplasia, liquen plano o combinaciones de estas condiciones con la exposición frecuente a carcinógenos bien establecidos como el alcohol, tabaco, nuez de betel e infección por el virus del papiloma humano (VPH) (7). Varios agentes relacionados con el tabaco, juegan un papel en el desarrollo de tumores, los potentes efectos de la 4-metilnitrosamino-1-3-piridil-1-butanona (NNK por sus siglas en inglés) y N'-nitrosonornicotine (NNN por sus siglas en inglés) son únicos. NNK metabólicamente activa y NNN, inducen mutaciones nocivas en oncogenes y genes supresores de tumores, al formar aductos de ADN, lo que podría considerarse como iniciación tumoral. Mientras tanto, la unión de NNK y NNN al receptor nicotínico de acetilcolina, promueve el crecimiento tumoral al potenciarlo y desregulando la proliferación, supervivencia, migración e invasión celular, por lo tanto, crea un microambiente para el crecimiento tumoral (8). El posible mecanismo de la carcinogénesis asociada con el alcohol, es que la enzima alcohol deshidrogenasa (ADH), oxida el etanol en acetaldehído, un metabolito intermedio que reacciona con el ADN y forma aductos de ADN. Estos aductos provocan mutaciones o inhiben la síntesis de ADN y, por lo tanto, inducen cáncer (3).
El VPH, se ha indicado como agente etiológico para el desarrollo de un subconjunto de carcinomas de células escamosas, especialmente en la base de la lengua y el área amigdalina en las personas más jóvenes, en comparación con la contraparte VPH negativa (1). Taxonómicamente este virus pertenece al Grupo I (virus ácido desoxirribonucleico ADN de doble cadena, covalentemente cerrado, con una talla de 7 500- 8 000 pb), es un virus eicosaédrico, sin cápside, que se transmite con alta fidelidad entre una copia y otra. Pertenece a la familia Papillomaviridae, al género Alphapapilloma virus (9). El genoma de los VPH puede ser dividido en tres segmentos de tallas diferentes. La región de control o región no codificadora, la región temprana y región tardía. La región de control regula el ciclo de vida del virus, la región temprana está compuesta por 6 genes: E1, E2, E4, E5, E6 y E7, los cuales están involucrados en la replicación y regulación viral, así como en su capacidad carcinogénica (E5, E6 y E7) y la región tardía está compuesta por dos genes que codifican para las proteínas L1 y L2, las cuales componen la cápside viral. Hasta el momento se han identificado más de 150 tipos de VPH, los más comunes son: 11, 16, 18, 31, 33, 35, 39, 45, 52, 56, 58 y 59 (10). Los subtipos 16 y 18 son los genotipos más frecuentemente relacionados con cáncer de cabeza y cuello.
El virus infecta las células del estrato basal en las membranas mucosas, entrando a la célula por endocitosis (11). El virus expresa la oncoproteína E6 y E7 que inactiva los genes supresores de tumores esenciales (GST) p53 y pRb, lo que resulta en una división agresiva de las células que condicionan el cáncer (12). La plausibilidad biológica del VPH como carcinógeno en el epitelio está bien establecida (13). La supervivencia a 5 años con el estándar de atención actual, independientemente de la terapia específica administrada, es de alrededor del 80 % al 85 % para los pacientes VPH positivos, pero solo del 30 % al 35 % para los pacientes con VPH negativos (5). En los carcinomas escamosos de cavidad oral el VPH es relativamente poco común (10 % a 15 %) (6). Una célula sana normal se encuentra bajo división celular, diferenciación y apoptosis controlada; por lo tanto, se mantiene la homeostasis de la célula, pero la célula cancerosa pierde su regulación, sufre una proliferación celular indefinida y escapa a la apoptosis por varios mecanismos, incluido el mantenimiento de la señalización proliferativa (3).
Los factores genéticos y epigenéticos en el cáncer oral, producen eventos que desencadenan la proliferación celular continúa, la inhibición de la apoptosis, mayor capacidad invasiva y en última instancia, tumorigénesis. Como mecanismo epigenético, las modificaciones de proteínas postraduccionales (PTM) juegan un papel crucial en la regulación de las funciones biológicas de proteínas. Hasta cierto punto, las proteínas modificadas controlan un "encendido" o estado "apagado" para regular varias funciones, como localización subcelular y transmisión de señales. La lisina 2-hidroxiisobutirila, es una PTM recién descubierta y se ha informado que está implicada en cada fase del proceso biológico de proteínas, desde la transcripción del ADN hasta degradación. Los resultados revelan que la proteína de expresión dentro de la vía reguladora del citoesqueleto de actina y los niveles de modificación de lisina, se alteran significativamente en los cánceres de cavidad oral (2).
Uno de los pilares del sistema de estadificación del American Joint Committee on Cancer (AJCC), por sus siglas en inglés, es la estratificación del pronóstico de los pacientes, en función de la presentación inicial para optimizar la selección del tratamiento. La AJCC publicó la octava edición en enero 2017 con criterios separados para la enfermedad positiva para p16 y negativa para p16, en orofaringe e incluyó la profundidad de invasión en los carcinomas escamosos de cavidad oral (14). Recientemente, el Colegio de Patólogos Americanos, basado en su revisión exhaustiva de la literatura médica, ha pedido pruebas obligatorias de todos los carcinomas escamosos de cabeza y cuello, en un presunto primario orofaríngeo y en metástasis de primario desconocido, y ha sido defendido por ellos y otras organizaciones influyentes, como el método de elección para determinar el estado del VPH. La inmunotinción de p16 es altamente precisa, ampliamente disponible para la mayoría de los laboratorios de diagnóstico y es fácil de interpretar en muestras de tejido (15). Por otro lado, los cánceres orales se caracterizan por una "cancerización de campo", lo que significa que el tracto aero-digestivo del paciente, es susceptible a lesiones premalignas o malignas. Estas características biológicas adversas fortalecen la recurrencia o aparición de otro primario de cabeza y cuello (7).
Aunque los pacientes con carcinoma de células escamosas de cavidad oral son susceptibles a tratamiento quirúrgico en la mayoría de los estadios, las opciones de tratamiento para los cuellos clínicamente negativo oscilan entre: la observación clínica, la disección ganglionar y la biopsia del ganglio centinela, debido a que la tasa de metástasis ganglionar oculta de los cN0, se ha estimado del 20 % al 30 % (16). Con el avance en el diagnóstico y la terapéutica, la tasa de supervivencia de cinco años ha mejorado, pero puede variar debido a la ubicación anatómica, el estadio, la edad al momento del diagnóstico, el tratamiento y las comorbilidades (3). El propósito del siguiente estudio es evaluar el comportamiento biológico de los carcinomas escamosos de cavidad oral, para poder considerar el marcador p16, como una nueva herramienta en este tipo de cáncer, permitiendo reforzar la toma de decisiones y evaluar si esta condición mejora o no, el pronóstico, la recurrencia y supervivencia libre de enfermedad.
MÉTODO
Tipo de estudio: Ensayo clínico no aleatorizado. Población y muestra: Se tomaron biopsias e información clínica de pacientes intervenidos quirúrgicamente por carcinoma escamoso de cavidad oral, en el período comprendido de enero 2015 hasta enero 2021, luego de haber aplicado los criterios de inclusión y exclusión.
Criterios de inclusión: pacientes mayores de 18 años, con carcinoma escamoso de cavidad oral, sin otro primario previo, que fueron intervenidos por el equipo de cabeza y cuello, cuyas historias de registro médico incluyeron la información pertinente, de los cuales se disponía de muestras histopatológicas en bloques intactos, que aceptaron que su información fuera utilizada para el estudio y que acudieron a su control para evaluación constante durante el tratamiento.
Criterios de exclusión: se excluyeron los pacientes con segundo primario de cabeza y cuello, con diagnóstico, recaída o recidiva de patología oncológica previa, que no estaban de acuerdo con el uso de su información médica, en los que no se recopiló la información médica necesaria y cuyos bloques de parafina en anatomía patológica estaban perdidos o deteriorados.
Procedimiento clínico y estadístico: para recolectar la información clínica se utilizó la historia del paciente e incluía: edad, sexo, presencia o no de hábitos tabáquicos, manifestaciones clínicas y estudios imagenológicos. Los resultados de las biopsias fueron aportados por el servicio de anatomía patológica y constó de: tipo histológico, tamaño tumoral, profundidad de invasión, enfermedad nodal y positividad p16. Todos los datos fueron recolectados hasta el año 2021, incluyendo la evaluación y seguimiento durante los 3, 6, 9 meses y al año. Para el procesamiento y análisis de los datos de este estudio, se utilizaron técnicas estadísticas descriptivas, Cuadros y representaciones gráficas (para las variables cualitativas). Se utilizaron métodos no paramétricos para distribuciones de probabilidad para los datos.
Patrones de tinción característicos: para la evaluación de la expresión de los marcadores celulares ensayados, se utilizó p16INK4a que es una proteína supresora de tumores. Este fue suministrado como anticuerpo purificado del sobrenadante del cultivo mediante cromatografía. El p16INK4a es un anticuerpo monoclonal de ratón, de Zeta Corporation USA® El inmunógeno utilizado es un péptido sintético del extremo C-terminal de p16INK4a humano, de la clase de IgG2. El vial se conservó a 4ºC. Se usaron secciones fijadas en formalina e incluidas en parafina. Se realizó desperafinizado con recuperación de epítopo inducida por calor en el tejido. La inmunotinción p16 se consideró positiva cuando se expresó en ≥70 % de las células tumorales con tinción. Se tomó en consideración las características para p16, como la tinción color ocre en el núcleo y en el citoplasma. Tanto la evaluación histopatológica como la observación de las reacciones inmunohistoquímicas, fueron realizadas por diferentes patólogos.
RESULTADOS
Se recolectó información clínica de 12 pacientes que cumplieron los criterios de inclusión y exclusión, se realizó la revisión de las biopsias y se realizó p16 a todas. La distribución de las características demográficas se muestra en el Cuadro 1.
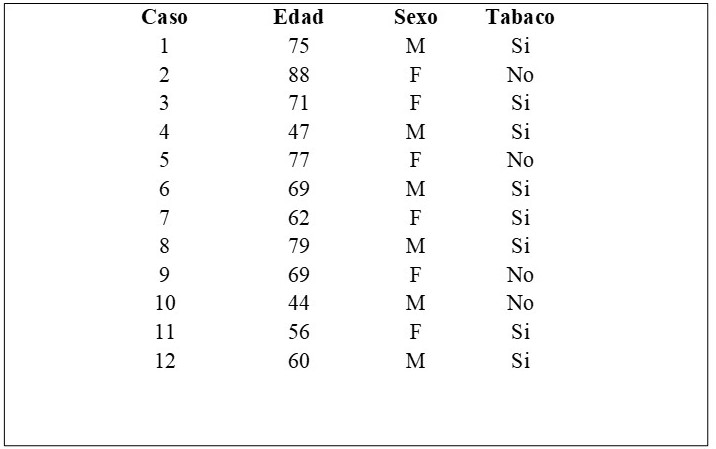
Cuadro 1
Distribución de las características demográficas de los pacientes
De los 12 pacientes evaluados, 6 eran del sexo masculino (50 %) y 6 (50 %) eran del sexo femenino, 8 pacientes (66,67 %) eran fumadores y 4 (33,33 %) no fumaban. La edad promedio fue de 66,41. El 50 % (6) se ubicaron en lengua móvil derecha, 16,67 % (2) tenían lesión en lengua móvil izquierda, 16,67 % (2) tenían lesión en reborde alveolar y 16,67 % (2) en mucosa yugal (Cuadro 2). El 100 % fueron carcinomas de células escamosas.
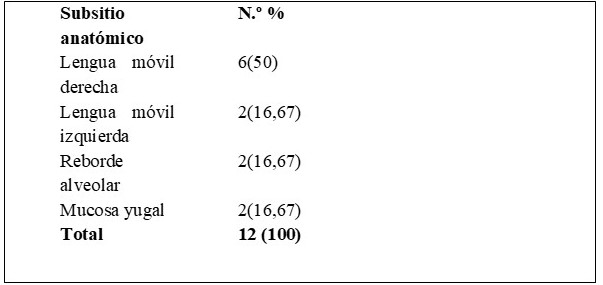
Cuadro 2.
Distribución de las características clínicas de los pacientes.
El 66,67 % (8) ameritaron glosectomía parcial y disección supraomohioidea ipsilateral, 8,33% (1) mandibulectomía marginal con colgajo platismal y disección supraomohioidea ipsilateral, 8,33% (1) mandibulectomía segmentaria con colgajo microquirúrgico radial de antebrazo y disección supraomohioidea ipsilateral, 8,33% (1) mandibulectomía marginal con colgajo de pectoral mayor y disección supraomohioidea ipsilateral, y 8,33 % (1) resección de mucosa yugal con colgajo miomucoso y disección supraomohioidea ipsilateral (Figura 1, Cuadro 3).
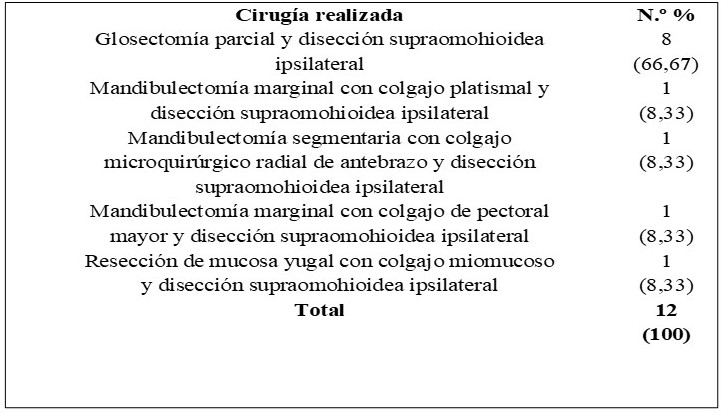
Cuadro 3.
Procedimientos quirúrgicos realizados.
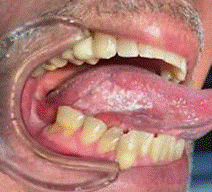
Figura 1
Carcinoma de células escamosas de lengua móvil derecha.
El tamaño tumoral tuvo un promedio de 2,9 cm. De los casos, 3 (25 %), tenían ganglios linfáticos positivos, que correspondían a los casos 1, 7 y 8, dos de los cuales fueron p16 negativos, todos los demás no tuvieron ganglios positivos. En la inmunohistoquímica, 2 (16,67 %) tenían p16 nuclear positivo y 5 (41,66 %) tenían p16 citoplasmático positivo. 5 (41,66 %) casos tenían una profundidad de invasión menor de 5 mm, 5 (41,66 %) casos tenían una profundidad de invasión mayor de 10 mm y 2 (16,66 %) casos tenían una profundidad de invasión de 5 mm a 10 mm.
En el seguimiento durante los 3, 6 y 9 meses, los 12 casos se mantuvieron libres de enfermedad en sus controles clínicos e imagenológicos. Al año de evaluación falleció el caso nº1 y 8, el primero, un masculino, fumador, con carcinoma escamoso de lengua que ameritó glosectomía con disección supraomohioidea ipsilateral, falleció a causa de recaída regional, era p16 negativo, y el caso 8, un masculino, fumador, con carcinoma escamoso de reborde alveolar que ameritó mandibulectomía marginal con colgajo de pectoral mayor y disección supraomohioidea ipsilateral, por causa diferente al cáncer. Hubo una recaída regional en el caso 6, masculino fumador, el cual era p16 negativo. Las características histológicas, inmunohistoquímicas y seguimiento se desglosan en el Cuadro 4.
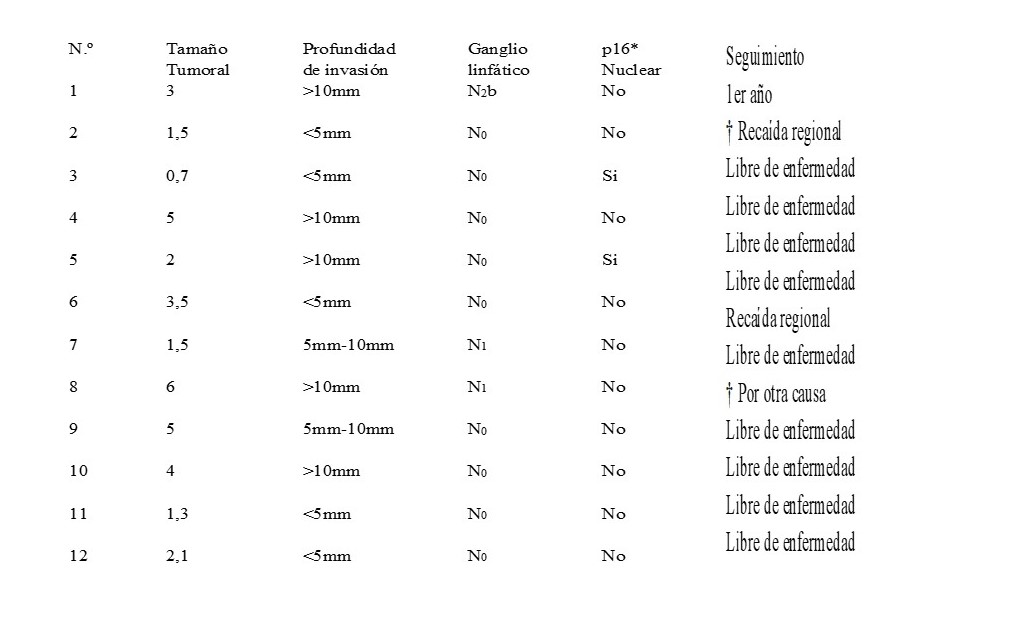
Cuadro 4
Distribución de las características histológicas.
*Marcador celular p16. † Caso que falleció.
DISCUSIÓN
Anteriormente, Liuzzi y col., en 2007, evaluaron 29 muestras de pacientes con carcinoma de células escamosas histológicamente confirmados en el servicio de cabeza y cuello del Hospital Oncológico “Padre Machado”. Se les realizó una toma de muestra del tumor la cual fue inicialmente congelada a - 80ºC, luego procesada a través de reacción en cadena de polimerasa y se determinó el tipo de virus que infecta al tejido muestreado. El 34,48 % resultó positivo para ADN del virus, siendo los de bajo riesgo los implicados (17). En este estudio se estudió la expresión de los marcadores celulares con la utilización de p16INK4a, que es un anticuerpo monoclonal de ratón, de Zeta Corporation USA® y la inmunorreacción evaluada fue nuclear y citoplasmática, siendo 2 (16,67 %) pacientes con p16 nuclear positivo y 5 (41,66 %) pacientes con p16 citoplasmático positivo, con un total de 5 casos positivos, a diferencia de los casos del estudio de Liuzzi y col., los cuales fueron 34,48 % y evaluados por PCR.
Por otra parte, D’Souza y col., en 2007, se enfocaron exclusivamente en el cáncer orofaríngeo y VPH. Como resultado, el cáncer orofaríngeo se asoció significativamente con la infección oral por VPH tipo 16 (Intervalo de confianza del 95 %, 6,3 a 36,6) y seropositividad para la proteína de la cápside L1 del VPH 16 (Intervalo de confianza del 95 %, 14,6 a 71,3). Se detectó ADN de VPH 16 en el 72 % (IC del 95 %, 62 a 81) de 100 especímenes de tumores incluidos en parafina y el 64 % de los pacientes con cáncer fueron seropositivo para la oncoproteína E6, E7 o ambas del VPH 16. Seropositividad de VPH 16 L1, estaba altamente asociado con el cáncer de orofaringe entre sujetos con antecedentes de consumo excesivo de tabaco y alcohol (IC del 95 %, 3,3 a 113,9) y entre aquellos sin dicha historia (IC del 95 %, 13,3 a 84,8). La asociación se incrementó de manera similar entre sujetos con infección oral por VPH 16, independientemente de su consumo de tabaco y alcohol (18). En este estudio 8 pacientes (66,67 %) eran fumadores. De los 5 (41,66 %) pacientes con p16 citoplasmático y/o nuclear positivo, solo dos casos estaban asociados con hábitos tabáquicos, casi similar a la asociación entre los p16 negativos y fumadores.
Reuschenbach M y col., en 2013, identificaron carcinoma oral atribuible al VPH en una cohorte de pacientes del sur de Alemania. Detectaron HPV-ADN por PCR en el 25,1 % (69/275) de los tumores. Se detectó una sobreexpresión difusa de p16INK4a en 11 tumores VPH PCR positivos, pero también en 6 tumores VPH PCR negativos. Ni el estado de VPH en PCR, ni el estado combinado de VPH en PCR/p16INK4a, ni el estado único de p16INK4a, se asociaron significativamente con la supervivencia libre de enfermedad o general, sin embargo, hubo una tendencia hacia una mejor supervivencia general, de los pacientes cuyo tumor expresó p16INK4a en un patrón focal en comparación con el que no expreso p16INK4a (P=0,09) (19). En este estudio fallecieron dos pacientes, caso nº1 y 8, el primero por enfermedad regional, no estaba asociado a VPH, el otro por causa diferente al cáncer y hubo una recaída regional en el caso 6, el cual no estaba asociado a VPH, por lo tanto, al igual que Reuschenbach y col., existe tendencia hacia una mejor supervivencia general, de los pacientes cuyo tumor expreso p16INK4a en comparación con el que no expreso p16INK4a.
Lingen y col., también en 2013, estimaron la fracción etiológica para el VPH entre los casos consecutivos e incidentes de carcinoma escamoso oral, evaluando la expresión de p16 por inmunohistoquímica. De 409 casos evaluables, 24 (5,9 %, IC del 95 % 3,6-8,2) fueron positivos para la expresión de VPH E6/7; 3,7 % (95 % IC 1.8-5,5) para VPH 16 y 2.2 % (95 % IC 0,8-3,6) para otros tipos de VPH. Surgieron tumores VPH positivos de toda la cavidad oral (piso de boca (9), lengua (6), proceso alveolar (4), paladar duro (3), encía (1) y labio (1) y se asociaron significativamente con el sexo masculino, el estadio tumoral pequeño, mala diferenciación tumoral e histopatología basaloide (20). A diferencia de Lingen y cpl., en este estudio el 50 % (6 casos) fueron en la lengua derecha, 16,6 7% (2) tenían lesión en lengua izquierda móvil, 16,67 % (2) en reborde alveolar y 16,67 % (2) en mucosa yugal.
Abd El-Azeem y col., en 2015, prepararon secciones de bloques histológicamente confirmados como carcinomas escamosos. Los tumores se clasificaron según el grado de queratinización y se realizó inmunohistoquímica. Como resultado p16 se sobre expresó en 27/44 casos (61,4 %) y se relacionó con un menor grado tumoral (P<0,001), un tamaño tumoral más pequeño (P=0,001), un estado ganglionar negativo (P<0,001), y una etapa temprana (P<0,001). p53 se expresó en 19/44 casos (43,2 %) y se relacionó con un grado alto (P<0,001), un tamaño tumoral más grande (P =0,005), un estado ganglionar positivo (P<0,001), y un tumor avanzado (P<0,001). p16 estaba inversamente relacionado con p53 (P<0,001) (21). En este estudio, 3 (25 %), tenían ganglios linfáticos positivos, que correspondían a los casos 1, 7 y 8, dos de los cuales fueron p16 negativos y 1 positivo, todos los demás no tuvieron ganglios positivos, es decir, el estado ganglionar positivo se podría relacionar con los VPH negativos, como en el estudio de Abd El-Azeem y col. En cuanto al tamaño tumoral, en los diagramas de caja 1, 2 y 3 (Figura 2), se puede observar diferencias entre los casos p16 positivos y p 16 negativos, donde los p16 positivos tenían menor tamaño tumoral, al igual que el estudio de Abd El-Azeem y col.
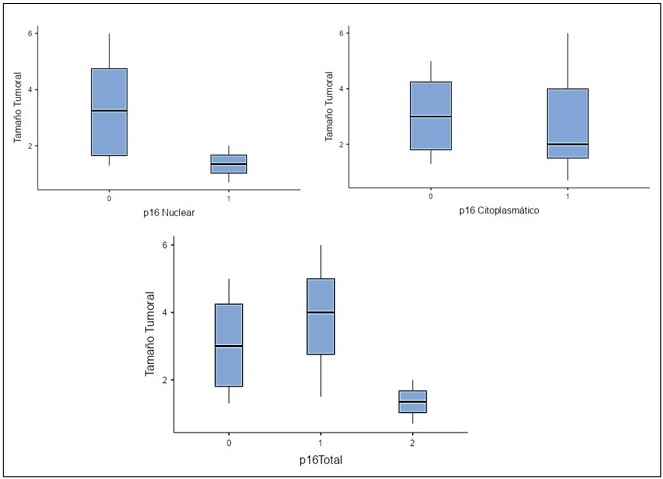
Figura 2.
Diagrama de caja 1, 2 y 3. Tamaño tumoral y p16 nuclear y citoplasmático.
Hernández y col., en 2019, investigaron el papel del VPH en los cánceres de la cavidad oral utilizando dos marcadores de exposición viral. Detectaron ADN del VPH en 38 de 122 (31 %) tumores de la cavidad oral. p16INK4a se expresó en el 30 % de los tumores. Ni el ADN del VPH, ni p16INK4a se asociaron con la supervivencia general (22). En este estudio, si existe tendencia hacia una mejor supervivencia general, de los pacientes cuyo tumor expreso p16 (Figura 3, 4, 5).
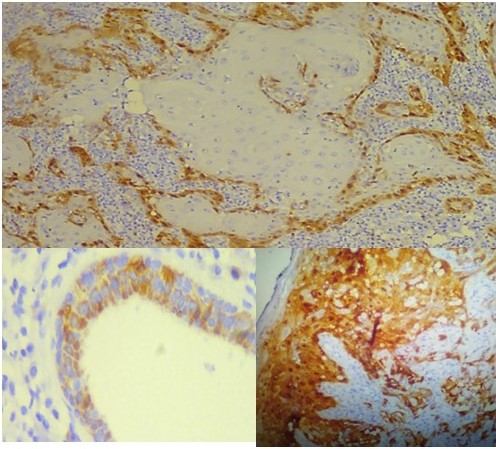
Figura 3, 4, 5.
p16 nuclear y citoplasmático.
Concluimos en que la asociación entre los p16 positivos fumadores y p16 negativos fumadores, es casi similar. EL estado ganglionar positivo se relaciona con los p16 negativos. El tamaño tumoral es menor en p16 positivos. Existe tendencia hacia una mejor supervivencia general en los tumores que expresan p16.
REFERENCIAS
1. Dhanuthai K, Rojanawatsirivej S, Thosaporn W, Kintarak S, Subarnbhesaj A, Darling M, et al. Oral cancer: A multicenter Study. Med Oral Patol Oral Cir Bucal. 2018;23(1):e23-e29.
2. Zhang Z, Xie H, Zuo W, Tang J, Zeng Z, Cai W, et al. Lysine 2-hydroxyisobutyrylation proteomics reveals protein modification alteration in the actin cytoskeleton pathway of oral squamous cell carcinoma. J Proteomics. 2021;249:104371.
3. Chamoli A, Gosavi A, Shirwadkar P, Wangdale K, Kumar S, Kumar N, et al. Overview of oral cavity squamous cell carcinoma: Risk factors, mechanisms, and diagnostics. Oral Oncology. 2021;121:105451.
4. Santelices M, Carcamo M, Brenner C, Montes R. Cáncer oral en Chile: Revisión de la literatura. Rev. Méd. Chile. 2016;144(6):766-770.
5. Bobdey S, Sathwara J, Jain A, Saoba S, Balasubramaniam G. Squamous cell carcinoma of buccal mucosa: An analysis of prognostic factors. South Asian J Cancer. 2018;7:49-54.
6. Chen C, Lohavanichbutr P, Zhang Y, Houck J, Upton M, Abedi-Ardekani B, et al. Prediction of survival of HPV16-negative, p16-negative oral cavity cancer patients using a 13-gene signature: A multicenter study using FFPE simples. Oral Oncology. 2020;100:104487.
7. Chen S, Hsiao S, Chang K, Chang J. New insights into oral squamous cell carcinoma: From Clinical aspects to molecular tumorigenesis. Int J Mol Sci. 2021;22(5):2252.
8. Xue J, Yang S, Seng S. Mechanisms of cancer induction by tobacco-specific NNK and NNN. Cancers (Basel). 2014;6:1138-1156.
9. Quijano R. Cáncer orofaríngeo y virus del papiloma humano en cabeza y cuello: Relaciones fisiopatológicas y epidemiológicas. Rev. Costarric. Salud Pública. 2018;27(1):16-23.
10. Domínguez S, Trujillo T, Aguilar K, Hernández M. Infección por el virus del papiloma humano en adolescentes y adultas jóvenes. Rev Cubana Obstet Ginecol. 2018;44(1):1-13.
11. Urbano S, Tovío E, Contreras N. Cáncer de cabeza y cuello asociado al Virus del papiloma humano. Presentación de caso. Rev Haban Cienc Méd. 2019;18(3):450-460.
12. Chamoli A, Gosavi A, Shirwadkar U, Wangdale K, Behera S, Kurrey N, et al. Overview of oral cavity squamous cell carcinoma: Risk factors, mechanisms, and diagnostics. Oral Oncology. 2021;121:105451.
13. Gillison M. Human papilloma virus associated head and neck cancer is a distinct epidemiologic, clinical, and molecular entity. Semin Oncol. 2004;31(6):744-754.
14. Salem F, Mansour M, Gitman M, Miles B, Posner M, Bakst R, et al. Real-time PCR HPV genotyping in fine needle aspirations of metastatic head and neck squamous cell carcinoma: Exposing the limitations of conventional p16 immunostaining. Oral Oncol. 2019;90:74-79.
15. Farquhar D, Coniglio A, Masood M, Lenze N, Brennan P, Anantharaman D, et al. Evaluation of pathologic staging using number of nodes in p16-negative head and neck cancer. Oral Oncol. 2020;180:104800.
16. Mijares A, Suarez C, Franco A. Confiabilidad del ganglio centinela en carcinoma de células escamosas de cavidad oral T1 / T2 N0. Revista Científica CMDLT. 2021;15(2):e-211022.
17. Liuzzi J, Estanga N, Castillo L, Correnti M, Mijares M, Gardie J. Tipificación del Virus del Papiloma Humano en carcinoma de células escamosas de cabeza y cuello. Rev Venez Oncol. 2007;19(3):210-218.
18. D’Souza G, Kreimer A, Viscidi R, Pawlita M, Fakhry C, Koch W, et al. Case–control study of human Papillomavirus and oropharyngeal. N Engl J Med. 2007;356 (19):1944-1956.
19. Reuschenbach M, Kansy K, Garbe K, Vinokurova S, Flechtenmacher C, Toth C, et al. Lack of evidence of human papillomavirus-induced squamous cell carcinomas of the oral cavity in southern Germany. Oral Oncol. 2013;49:937-942.
20. Lingen M, Xiao W, Schmitt A, Jiang B, Pickard R, Kreinbrink P, et al. Low etiologic fraction for high-risk human papillomavirus in oral cavity squamous cell carcinomas. Oral Oncol. 2013;49:1-8.
21. Abd El-Azeem M, Wasfy R, Shareef M. Immunohistochemical expression of p16 and p53 in oral and oropharyngeal squamous cell carcinoma: A pilot study in Egyptian patients. New Egyptian Journal of Pathology. 2015;35(1):81-86.
22. Hernandez B, Lynch C, Chan O, Goodman M, Unger E, Steinau M, et al. The HPV Typing of Cancer Workgroup. Human papillomavirus DNA detection, p16INK4a, and oral cavity cancer in a U.S. population. Oral Oncol. 2019;91:92-96.
Notas de autor
mibuenasalud@gmail.com.