CARCINOMA DUCTAL IN SITU: FACTORES DE RIESGO PARA RECURRENCIA. A PROPÓSITO DE UN CASO
CARCINOMA DUCTAL IN SITU: FACTORES DE RIESGO PARA RECURRENCIA. A PROPÓSITO DE UN CASO
Revista Venezolana de Oncología, vol. 36, núm. 2, pp. 110-115, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 10 Noviembre 2023
Aprobación: 15 Enero 2024
Resumen: OBJETIVO: Los factores de riesgo para recaída después de cirugía conservadora de mama en el carcinoma invasivo han sido bien establecido desde hace varios años. Sin embargo, al referirnos a carcinoma ductal in situ, estos factores de riesgo no se han identificado de manera precisa. El grado nuclear, lesión palpable, márgenes inadecuados luego de una cirugía preservadora, han sido descritos por algunos autores como factores de riesgo para recidiva. CASOCLÍNICO: Paciente femenina de 57 años de edad con antecedente de carcinoma ductal in situ tratada con mastectomía total izquierda más reconstrucción inmediata con colgajo miocutáneo del recto abdominal más biopsia de ganglio centinela quien posterior a 8 años de período libre de enfermedad presenta recaída local como carcinoma ductal infiltrante rpT2N0(gc)M0 estadio IIA Luminal A, recibe tratamiento multidisciplinario. CONCLUSIÓN: Los factores de riesgo de recurrencia posterior a diagnóstico de carcinoma ductal in situ no han sido bien establecidos hasta la fecha. El grado histológico, la raza negra y los márgenes estrechos son quizás los más estudiados, sin embargo, surge la necesidad de determinar marcadores biológicos y perfiles de expresión génica con el fin de identificar aquellos casos con mayor riesgo de recurrencia para individualizar su tratamiento y seguimiento. Son necesarios más estudios aleatorizados que permitan esclarecer este asunto.
Palabras clave: Carcinoma ductal, in situ, recurrencia, factores de riesgo.
Abstract: OBJECTIVE: The risk factors for relapse after the breast conserving surgery in the invasive carcinoma have been well established for several years. However, when referring to ductal carcinoma in situ, these risk factors have not been precisely identified. The nuclear grade, the palpable lesion or the inadequate margins after the sparing surgery have been described by some authors as risk factors for recurrence. CLINICAL CASE: A 57-year-old female patient with a history of ductal carcinoma in situ treated with left total mastectomy plus immediate reconstruction with myocutaneous flap of the rectus abdominis plus the sentinel lymph node biopsy who, after an 8-year of disease-free period, presented with a local relapse as an infiltrating ductal carcinoma rpT2N0(gc)M0 stage IIA Luminal A, she receives multidisciplinary treatment. CONCLUSION: The risk factors for the recurrence following a diagnosis of the ductal carcinoma in situ have not been well established to the date. The histological grade, the black race, and the narrow margins are perhaps the most studied, however; there is a need to determine the biological markers and the gene expression profiles in order to identify those cases with a higher risk of the recurrence in order to individualize their treatment and the follow-up. More randomized studies are needed to clarify this issue.
Keywords: Ductal carcinoma, in situ, recurrence, risk factors.
INTRODUCCIÓN
El carcinoma ductal in situ (CDIS) representa aproximadamente el 20 % de todos los casos diagnosticados en EE. UU y entre el 17 % y el 64 % de los casos detectados por mamografía en ausencia de una lesión palpable. Generalmente, 1 de cada 1 300 mamografías conduce al diagnóstico de CDIS, es por esto que durante años se planteó cierta incertidumbre en cuanto a la historia natural de la enfermedad de esta entidad nosológica. El tratamiento estándar para el CDIS se fundamenta en la cirugía con el mejor resultado estético posible, seguido de tratamiento adyuvante como radioterapia o terapia hormonal dependiendo de la opción quirúrgica ofrecida a la paciente y el perfil de inmunohistoquímica (1,2).
CASO CLÍNICO
Presentamos el caso de una paciente femenina de 57 años de edad con antecedente de CDIS de mama izquierda de bajo grado, patrón cribiforme estadio 0 /Luminal B HER2 +/RE 80%) (2013) tratado con mastectomía total izquierda más reconstrucción inmediata con colgajo miocutáneo del recto abdominal (TRAM, por sus siglas en inglés) más biopsia de ganglio centinela (negativo). Es evaluada por oncología médica, quienes indican Tamoxifeno, el cual no cumple.
La paciente no acude a sus controles regulares desde el año 2018, durante control por el servicio de Patología Mamaria en septiembre de 2021 se evidencia nódulo palpable en el cuadrante inferior de la cicatriz del colgajo TRAM, por lo cual se solicitan estudios de imagen y biopsia por aguja gruesa de dicha lesión, cuyo resultado histopatológico reporta positivo para carcinoma ductal infiltrante (CDI). Al examen físico se evidencia cicatriz hipocrómica a nivel de la mama izquierda en relación a colgajo autólogo, asociado a un nódulo de 3 cm x 3,5 cm en el cuadrante inferior interno, renitente y móvil, a nivel axilar y supraclavicular no se palpan adenopatías; el resto del examen físico se encontraba sin alteraciones (Figura 1).
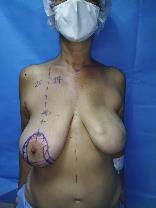
Figura 1
Paciente
Se solicita mamografía 2D (Figura 2 y 3) donde resalta la presencia de imagen nodular radiopaca, de bordes irregulares, espiculados e imprecisos a nivel del cuadrante inferior e interno de la mama izquierda. Se correlaciona dicho hallazgo con ultrasonido mamario donde se evidencia una masa de aspecto neoproliferativo de bordes espiculados, hipoecoica con sombra acústica posterior que mide 23 mm x 22 mm. Ecográficamente las axilas se encontraban sin alteración.
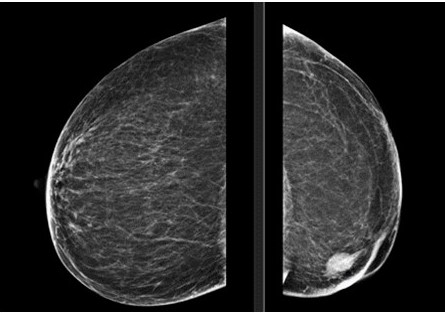
Figura 2.
Proyección céfalo caudal bilateral de la mamografía 2D.
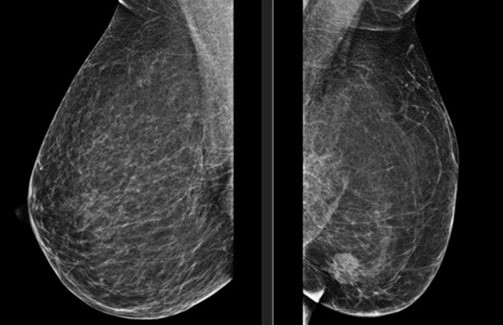
Figura 3.
Proyección medio lateral oblicua bilateral de la mamografía 2D.
En vista de estos hallazgos se solicita biopsia por aguja gruesa (BAG) la cual reporta infiltración al tejido conectivo denso y adiposo por carcinoma ductal moderadamente diferenciado cuya inmunohistoquímica reporta receptor de estrógeno (RE) positivo 90 %, receptor de progesterona (RP) positivo 5 %, HER2NEU negativo con un Ki67 en 4 % compatible con un subtipo molecular Luminal A. (Figura 4
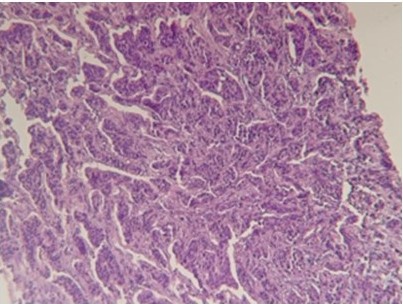
Figura 4
Infiltración al tejido adiposo por carcinoma ductal moderadamente diferenciado (40X)
Los estudios de extensión no demostraron la presencia de enfermedad a distancia. Se discute en reunión multidisciplinaria con posterior intervención quirúrgica (12/02/2022), realizando resección local amplia de la lesión + ganglio centinela (GC) axilar izquierdo + corte congelado + reconstrucción inmediata por cirugía plástica (colgajo local de avance). Como hallazgos se describe:
1. Tumor de 3 cm x 3 cm nivel del cuadrante inferior interno de la mama izquierda entre radiales 7 y 8.
2. Ganglio linfático teñido de azul a nivel axilar izquierdo con canalículo aferente también teñido en el nivel I de Berg.
3. Ganglio linfático no centinela (no teñido) de aproximadamente 1 cm de consistencia blanda, también en el nivel I de Berg.
El reporte tanto del corte congelado como de la biopsia definitiva de ambos ganglios linfáticos fue negativo para malignidad.
El reporte definitivo de la resección local amplia demostró la presencia de un carcinoma ductal infiltrante (CDI) moderadamente diferenciado con áreas de patrón micropapilar que mide 3,8 cm x 2 cm x 3 cm x 1,8 cm, sin evidencia de invasión vascular linfática ni perineural, CDIS presente de patrón cribiforme, piel y bordes de resección sin evidencia de tumor (Figura 5). Se discute en reunión de servicio y se concluye con diagnóstico de 1.CDIS pTisN0M0 estadio 0 (2013) 2. Carcinoma ductal infiltrante rpT2N0(gc)M0 estadio IIA Luminal A (2023).
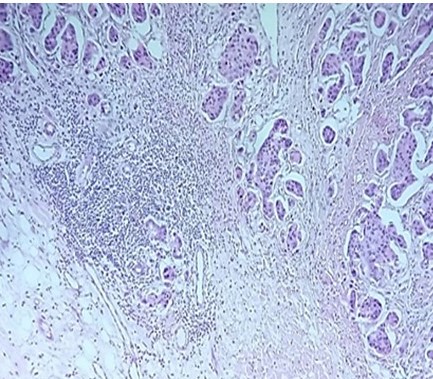
Figura 5.
Biopsia definitiva de resección local amplia que reporta carcinoma ductal infiltrante moderadamente diferenciado con áreas de patrón micropapilar. (40 X)
Se refiere al servicio de Oncología Médica y Radioterapia, controles posteriores por los servicios de Patología Mamaria, Cirugía Plástica y Reconstructiva y Oncología Médica. La paciente recibe quimioterapia a base de esquema CAF por 6 ciclos a título adyuvante, no recibe radioterapia (aunque fue referida) y actualmente se encuentra recibiendo exemestano 25 mg vía oral, sin evidencia de recaída locorregional hasta la fecha.
DISCUSIÓN
En pacientes que presentan diagnóstico de carcinoma invasor; el estado de los ganglios linfáticos, la edad, las características histológicas y la presencia de CDIS son quizás los factores pronósticos más importantes, los cuales pueden aumentar el riesgo de recurrencia (3).
Algunas publicaciones han tratado de identificar los factores más importantes en el CDIS para predecir el riesgo de recidiva, siendo el grado histológico, la edad, la raza negra y la enfermedad palpable, algunos de los más importantes. A la luz de estos hallazgos, O'Keefe y col. (4) sugiere que los factores de riesgo de recurrencia después de un diagnóstico de CDIS, difieren de los factores de riesgo de mortalidad por cáncer de mama invasor y del desarrollo de metástasis.
La mayoría de los estudios que han evaluado y tratado de predecir el riesgo de recurrencia en mujeres con CDIS se basan en series de casos no poblacionales de mujeres con este diagnóstico. Generalmente estos trabajos incluyen pequeños grupos de estudio con enfermedad recurrente y representan la experiencia individual de algunos centros, por esto se sugiere que hasta la fecha no han sido establecidos de forma contundente, los factores de riesgo que aumentan el riesgo de recidiva en CDIS (5).
Narod y col. (5) en un estudio observacional que incluyo más de 108 000 mujeres con diagnóstico de CDIS concluyen que el riesgo de muerte por cáncer de mama experimenta un incremento significativo al momento de presentar una recaída invasora ipsilateral, sin embargo, los factores que incrementan este riesgo no han sido dilucidados. Así como tampoco se ha definido hasta qué punto la mortalidad por cáncer de mama después del diagnóstico de CDIS es la consecuencia directa de una recurrencia invasiva o de si los casos mortales de CDIS tienen un alto potencial maligno desde el diagnóstico inicial(5,6).
En líneas generales, no ha sido demostrado que el tratamiento adyuvante con radioterapia o cirugías más extensas como la mastectomía total, reduzca el riesgo de mortalidad especifica por cáncer de mama, el cual se estima en 1,1 % (5,6).
Por estas razones, cada vez hay más evidencia que sustenta que el CDIS no es una entidad única, si no que abarca una gran variedad de lesiones que difieren entre sí en términos de presentación clínica, características mamográficas, extensión y distribución dentro de la glándula mamaria, características histológicas y comportamiento biológico, sin embargo, la comprensión de estas variables ha sido lenta, aunque constante (7,8).
Generalmente se afirma que el CDIS es una lesión neoplásica preinvasora, no letal, per se, sin embargo, algunos estudios sugieren que esta interpretación de la literatura debe ser analizada con mayor detalle. Por ejemplo, en población general con cáncer de mama invasivo se utilizan las firmas genéticas como el OncotypeDx para identificar a aquellas pacientes con bajo riesgo de muerte por cáncer de mama que podrían no beneficiarse de un tratamiento adyuvante con quimioterapia citotóxica; pero en la población con CDIS se ha propuesto que estas pruebas moleculares sean utilizadas para identificar a los pacientes que tienen un alto riesgo de recaída, que no necesariamente significa riesgo de muerte (5).
En la era de la medicina de precisión, la finalidad del manejo oncológico debe ser ofrecer el tratamiento preciso al paciente adecuado y evitar el tratamiento insuficiente o el sobretratamiento, individualizando cada caso. Adicionar la radioterapia (RT) a la cirugía conservadora ha demostrado que reduce la recurrencia local pero no influye la supervivencia global ni la supervivencia de cáncer especifica (9,10,11). Barrios y col. (12) opinan que el uso de RT adyuvante debe ser selectivo y reservarse para aquellos pacientes con mayor riesgo de recurrencia local y, por lo tanto, con más probabilidad de obtener un mayor beneficio de su uso, este procedimiento al igual que la cirugía no está exenta de complicaciones, sin embargo, los ensayos clínicos existentes hasta la fecha no han identificado cohortes de bajo riesgo, en las cuales se pueda omitir la RT.
En líneas generales pudiéramos decir que el CDIS sigue siendo una entidad nosológica ambigua ya que tanto la historia natural como la posibilidad de progresión hacia una lesión invasora no es predecible. El diagnóstico de nuestra paciente fue de recurrencia ipsilateral (CDI) con el antecedente de CDIS. No obstante; como lo reporta Lip y col. (13) en su investigación de la concordancia genómica y la relación clonal del CDIS puro y el CDI recurrente ipsilateral subsiguiente, veinte (20 %) de los CDI posteriores no estaban relacionados genéticamente con el primer CDIS. Esto significa que estos cánceres de mama invasivos eran nuevos y que el tratamiento del CDIS no redujo el riesgo de futuros cáncer de mama invasivo. Por esto, surge la necesidad de estudiar marcadores biológicos y perfiles de expresión génica con el fin de identificar aquellos casos con mayor riesgo de recurrencia y personalizar su tratamiento y seguimiento. Además de involucrar a los pacientes en la toma de decisiones a la luz de la evidencia científica publicada hasta la fecha (14,15).
Este artículo presenta el caso de una paciente con diagnóstico de CDIS que luego de 8 años tiene una recaída como una lesión infiltrante. Son varios los factores que se pudieran analizar entorno a este hecho; ya se sabe que el grado histológico, el estado de los márgenes y la forma de presentación de la lesión (lesión palpable vs., no palpable) pudieran estar relacionado con el riesgo de recaída. Quizás la omisión de alguno de los tratamientos adyuvantes como en nuestro caso, aumentan este riesgo, sin embargo, será necesario la realización de estudios prospectivos aleatorizados que permitan establecer formalmente los factores de riesgo para recidiva en estos casos.
REFERENCIAS
1. Kerlikowske K, Molinaro A, Cha I, Ljung BM, Ernster VL, Stewart K, et al. Characteristics associated with recurrence among women with ductal carcinoma in situ treated by lumpectomy. J Natl Cancer Inst. 2003;19;95(22):1692-1702.
2. Ernster VL, Ballard-Barbash R, Barlow WE, Zheng Y, Weaver DL, Cutter G, et al. Detection of ductal carcinoma in situ in women undergoing screening mammography. J Natl Cancer Inst. 2002;94(20):1546-1554.
3. van der Leij F, Elkhuizen PH, Bartelink H, van de Vijver MJ. Predictive factors for local recurrence in breast cancer. Semin Radiat Oncol. 2012;22(2):100-107.
4. O'Keefe TJ, Chau H, Harismendy O, Wallace AM. Risk factors for breast cancer mortality after ductal carcinoma in situ diagnosis differ from those for invasive recurrence. Surgery. 2023; 173(2):305-311.
5. Narod SA, Iqbal J, Giannakeas V,Sopik V, Sun P. 2015. Breast cancer mortality after a diagnosis of ductal carcinoma in situ. JAMA Oncol. 2015;1(7):888-896.
6. Mokbel K. Contemporary treatment of ductal carcinoma in situ of the breast. Med Sci Monit. 2005;11(3):RA86-93.
7. Sakorafas GH, Tsiotou AG. Ductal carcinoma in situ (DCIS) of the breast: Evolving perspectives. Cancer Treat Rev.2000;26(2):103-125.
8. Badve SS, Gökmen-Polar Y. Ductal carcinoma in situ of breast: Update 2019. Pathology. 2019 ;51(6):563-569.
9. Elshof LE, Schmidt MK, Rutgers EJT, Van Leeuwen FE, Wesseling J, Schaapveld M. Cause-specific mortality in a population-based cohort of 9799 women treated for ductal carcinoma in situ. Ann Surg. 2018; 267(5):952-958.
10. Early Breast Cancer Trialists' Collaborative Group (EBCTCG), Correa C, McGale P, Taylor C, Wang Y, Clarke M, Davies C, et al. Overview of the randomized trials of radiotherapy in ductal carcinoma in situ of the breast. J Natl Cancer Inst Monogr. 2010 (41):162-177.
11. Corradini S, Pazos M, Schönecker S, Reitz D, Niyazi M, Ganswindt U, et al. Role of postoperative radiotherapy in reducing ipsilateral recurrence in DCIS: An observational study of 1 048 cases. Radiat Oncol. 2018;13(1):25.
12. Barrio AV, Van Zee KJ. Ductal carcinoma in situ of the breast: Controversies and current management. Adv Surg. 2019;53:21-35.
13. Lips EH, Kumar T, Megalios A, Visser LL, Sheinman M, Fortunato A, et al. Genomic analysis defines clonal relationships of ductal carcinoma in situ and recurrent invasive breast cancer. Nat Genet. 2022;54(6):850-860.
14. Peltecu G. Ductal carcinoma in situ - Quo Vadis? Chirurgia (Bucur). 2021;116(5 Suppl):S5-6.
15. Wu M, Zhao H. Analysis of key genes and pathways in breast ductal carcinoma in situ. Oncol Lett. 2020;20(5):217.
Notas de autor
ljsolorzanop@gmail.com