CÁNCER DE MAMA OCULTO. REPORTE DE UN CASO CLÍNICO, ANALIZADO SEGÚN EL CONCEPTO ACTUAL.
CÁNCER DE MAMA OCULTO. REPORTE DE UN CASO CLÍNICO, ANALIZADO SEGÚN EL CONCEPTO ACTUAL.
Revista Venezolana de Oncología, vol. 36, núm. 3, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 14 Febrero 2024
Aprobación: 10 Abril 2024
Resumen: OBJETIVO: El cáncer de mama oculto suele presentarse como metástasis axilares sin afectación mamaria en los estudios de imagen y sin evidencia, de lesiones histológicas malignas en la glándula mamaria. Representa entre el 0,3 % y el 1 %, la incidencia no ha disminuido a pesar de los avances en las pruebas de imagen. CASO CLÍNICO: Paciente de 62 años, sin antecedentes personales ni familiares de riesgo, remitida en marzo de 2022, para evaluación por sospecha de enfermedad metastásica ganglionar. Ecografía axilar reveló plastrón ganglionar en axila izquierda, se practicó biopsia axilar guiada por ecografía, utilizando aguja cortante calibre 14, concluyó con diagnóstico histológico e inmunohistoquímico de metástasis de adenocarcinoma primario de mama. Estudios adicionales realizados, mamografía, ecografía mamaria, resonancia magnética, no revelaron la presencia de un tumor primario. Con diagnóstico de cáncer de mama oculto izquierdo cToN2Mo, estadio III A, luminal A, se programó tratamiento neoadyuvante con quimioterapia, finalizó en enero de 2022 y fue seguido de cirugía, consistió en disección axilar de los niveles I y II. Con los resultados de patología, concluimos con una impresión diagnóstica de cáncer de mama ypToN3Mo estadio III C, luminal A. Remitida al servicio de radioterapia, recibe radioterapia externa, a glándula mamaria izquierda y áreas drenaje linfático, finalizando en noviembre de 2023. Última evaluación en consulta, en febrero de 2024, no había evidencia clínica o de imagen de recurrencia local o a distancia. Actualmente recibe terapia sistémica adyuvante con anastrazol 1 mg.
Palabras clave: Cáncer de mama, oculto, mastectomía, disección axilar, resonancia magnética, ganglio, biopsia, inmunohistoquímica, adenopatía.
Abstract: OBJECTIVE: Occult breast cancer usually presents as axillary metastases without breast involvement in imaging studies and without evidence of malignant histological lesions in the mammary gland. New cases diagnosed each year represents between 0.3 %- 1 %; the incidence has not decreased despite advances in imaging tests. CLINICAL CASE: A 62-year-old patient, with no personal or family history of risk, was referred to us in March 2022, for evaluation for suspected lymph node metastatic disease. Axillary ultrasound was performed revealed lymph node plastron in the left axilla, for which ultrasound-guided axillary biopsy was performed, using a 14-gauge cutting needle, concluded with the histological and immunohistochemically diagnosis of metastasis of primary adenocarcinoma of the breast. Additional studies performed, mammography, breast ultrasound, breast magnetic resonance, not reveal the presence of primary tumor. With the diagnosis of cToN2Mo left occult breast cancer, stage III A, luminal A, neoadjuvant treatment with chemotherapy was scheduled, ended in January 2022 was followed by surgery, which consisted of axillary dissection of levels I and II. With the pathology results, we concluded with a diagnostic impression of ypToN3Mo stage III C, luminal A breast cancer. She was referred to the radiotherapy service, receive radiotherapy, to the left mammary gland and lymphatic drainage areas, completing treatment. in November 2023. Last evaluation in consultation, in February 2024, there was no clinical or imaging evidence of local or distant recurrence. She is currently receiving adjuvant systemic therapy with anastrazole 1 mg.
Keywords: Breast cancer, hidden, mastectomy, axilar disection, magnetic resonance, node, biopsy, immunohistochemestry, lymph.
INTRODUCCIÓN
El cáncer de mama es uno de los cánceres más comúnmente diagnosticados en el mundo, con una incidencia en rápido aumento, que afecta a una de cada ocho mujeres a lo largo de su vida (1,2). El cáncer de mama oculto es un tipo especial de cáncer de mama, y su tasa de detección en el cáncer de mama es muy baja. El cáncer oculto de la mama representa un reto para el clínico, la presencia de un ganglio axilar metastásico sin lesiones aparentes en la glándula mamaria plantea discusión y controversias en el tratamiento de esta enfermedad (3).
Representa el cáncer oculto de la glándula mamaria el 0,3 % al 1 % de los casos diagnosticados anualmente por carcinoma mamario, siendo la forma de presentación, la persistencia de un ganglio axilar no doloroso, de crecimiento lento de aproximadamente 2 cm x 3 cm. de diámetro, por lo general movible, en una paciente en la cual no hay evidencia clínica ni por imágenes de lesiones malignas en la glándula mamaria (3).
Importante que la paciente no presente tejido mamario ectópico en la axila, tampoco antecedentes de haber sido tratada por un cáncer de mama contralateral, y se haya descartado la presencia de enfermedad primaria maligna de otras localizaciones como pulmón, tiroides, melanomas, entre otras patologías (4).
En la literatura autores como Halsted (5), Cameron (6), Owen y col. (7) entre otros, ya habían publicado sus experiencias, pero no es sino a partir de las mejoras en las imágenes en patología mamaria que se establece en definitiva el concepto de cáncer oculto de mama, una vez que no hay evidencia de lesiones tanto en la mamografía, en el eco mamario, como tampoco en la resonancia magnética de mamas con contraste, clasificándose la enfermedad según la AJCC, según la clasificación TNM como cáncer de mama cToN1-2Mo correspondiendo a un estadio II-III .
Debido a que ésta es una patología poco frecuente, existe escasa experiencia al respecto y se plantea un dilema terapéutico, sin establecerse, el tratamiento óptimo de la enfermedad (8,9).
La disección axilar y el tratamiento sistémico neo y/o adyuvante siempre están indicados en el tratamiento del carcinoma de mama oculto, pero la mayor controversia es cómo tratar la glándula mamaria, ya sea con radioterapia externa o cirugía, y en ocasiones se plantea la observación y seguimiento (10 ,11, 12).
CASO CLÍNICO
Presentamos el caso de una paciente 53 años, quien consulta refiriendo aumento de volumen en región axilar izquierda de 1 año de evolución. Al examen físico sin evidencia a la palpación de lesiones mamarias, se aprecia en la axila izquierda plastrón ganglionar de 4 cm de diámetro movible, no fijo a estructuras vecinas. En los estudios realizados, como lo son mamografía, eco mamario y resonancia magnética de ambas mamas con gadolinio en marzo 2022, solo se observa, la presencia de lesión de ocupación de espacio en axila izquierda, sugestivo de plastrón ganglionar, sin lesiones subclínicas en las mamas (Figura1,2,3)
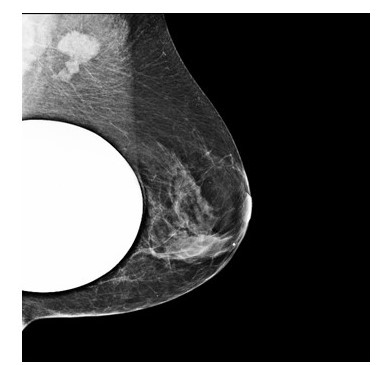
Figura 1
Mamografía medio lateral izquierda
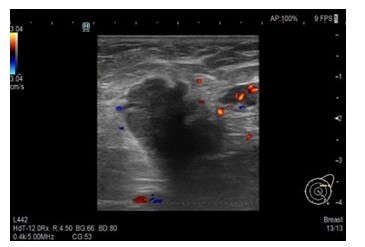
Figura 2
Ecografía axilar izquierda
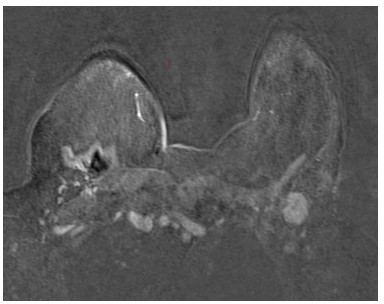
Figura 3
Resonancia magnética axila izquierda
Al examen físico mamas grandes asimétricas, presencia de cicatrices de mamoplastia de aumento, portadora de implantes mamarios, no se palpan tumores mamarios, y en la axila izquierda plastrón ganglionar de 4 cm. de diámetro duro movible que no infiltra piel. En vista de los hallazgos clínicos y de imágenes se procedió a realizar biopsia ecoguiada con aguja gruesa de corte, el 11/ 04/ 2022, reportando la anatomía patológica biopsia ap 3542 22, carcinoma ductal invasor grado II, ausencia de componente de carcinoma in situ, desmoplasia acentuada, con resultados para inmunohistoquímica biopsia ap. 3542 22 RE, + RP + ERB 2 neu negativo KI 67: 10 % subtipo molecular intrínseco tipo luminal A (Figura 4).
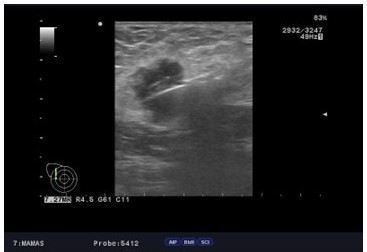
Figura 4
Biopsia ecoguiada aguja de corte
Los estudios de extensión realizados, tomografía axial computarizada de tórax sin contraste, ecosonograma abdominal, gammagrama óseo se reportan dentro de límites normales, y se concluye con el diagnóstico de cáncer de mama oculto izquierdo ct0N2Mo estadio IIIA.
La paciente inicia tratamiento neoadyuvante a base de quimioterapia, la culmina el 24 enero 2023, observándose al examen físico: ausencia de lesiones en la mama izquierda, en la axila izquierda, se palpa ganglio axilar, de menor tamaño, de aproximadamente 2 cm, consistencia dura y movible. Se realizan mamografía, ecosonograma mamario, resonancia magnética de ambas mamas con gadolinio 2023 los cuales están dentro de límites normales, y sin evidencia de lesiones en la glándula mamaria.
La conducta quirúrgica realizada, fue una disección axilar izquierda de nivel I - II, con los hallazgos, de múltiples adenopatías sospechosas de enfermedad metastásica, indicando el resultado de la anatomía patológica la presencia de 10 ganglios afectados por metástasis de 24 disecados. Los resultados del estudio de inmunohistoquímica informan se trata de enfermedad metastásica de un adenocarcinoma primario de la glándula mamaria, receptores estrógenos +, receptores progesterona +, ERB 2 neu negativo, CK 7 +CK 20 -, mamoglobina + RE y RP + Her 2 neu negativo. La conclusión es paciente femenina con el diagnóstico de cáncer oculto de mama izquierda pToN3Mo estadio III C. Como parte de su tratamiento adicional locorregional, la paciente recibió radioterapia a la glándula mamaria y a las áreas de drenaje, finalizando el tratamiento radiante en noviembre de 2023.
Durante el seguimiento, no se han presentado signos clínicos de una recaída locorregional y/o a distancia. En el examen físico realizado el 16 de febrero de 2024, no se detectaron lesiones en las glándulas mamarias y tampoco en las axilas. Las imágenes de mamografía y ecosonograma mamario de febrero de 2024 fueron normales. Se concluyó con un diagnóstico de BIRADS 2.
DISCUSIÓN
El cáncer de mama oculto constituye una patología poco frecuente del 0,3 al 1 % de los carcinomas mamarios diagnosticados anualmente. Se define actualmente, como aquella neoplasia que se manifiesta con un ganglio homolateral metastásico, de un adenocarcinoma mamario, histológicamente comprobado en ese ganglio axilar, sin evidencia clínica ni por imágenes de lesiones malignas en la glándula mamaria, a diferencia del antiguo concepto que lo definía como sólo a aquella lesión no palpable (3,4).
Esté término fue utilizado por primera vez por Halsted (5), en 1907, al reportar tres casos de pacientes con ganglios linfáticos metastásicos y glándulas mamarias normales por clínica. Les hizo seguimiento a las pacientes tras la resección axilar y a los pocos meses, se manifestó el cáncer de mama de manera evidente. Dos años más tarde, Cameron (6) reportó tres casos similares.
En 1954, Owen y col. (7) intentaron estimar la incidencia de cánceres ocultos y encontraron 25 casos en 5 451 pacientes (0,4 %). En estos casos, el método utilizado para el diagnóstico de los tumores de la mama fue tan solo la observación y la palpación.
Posterior a la introducción de la mamografía como método de elección para el diagnóstico del cáncer de mama, la definición cambió a la actualmente conocida (13).
De todas formas, a pesar de la mejora en las técnicas diagnósticas por imágenes de lesiones mamarias, la incidencia no ha cambiado. El encontrar una adenopatía axilar sospechosa, durante el examen físico, en el 90 % de los casos es de origen mamario, pero debe tenerse presente la posibilidad de que sea una metástasis de origen extra mamario como pulmón, tiroides, melanoma, linfoma, y páncreas entre otros (12).
El cáncer oculto de mama se presenta con más frecuencia en las mujeres, con una edad promedio de 50 años, la paciente consulta por la presencia de una masa axilar, sugestiva de ganglio, dura, no dolorosa, persistente, por lo general movible, en ausencia de tejido mamario ectópico y muy importante sin antecedentes personales de haber sido tratada la paciente por un cáncer de mama contralateral (4).
Dentro de la valoración diagnóstica se incluye la mamografía digital, la ecografía mamaria y la resonancia magnética con gadolinio, pasándose posteriormente a la realización de una punción con aguja fina o en su defecto, y más recomendable realizar una biopsia con aguja gruesa de corte, para así obtener material histológico que nos permita el diagnóstico anatomopatológico y en consecuencia también marcadores de inmunohistoquímica (13,14).
En este punto deben incluirse marcadores que orienten al clínico al diagnóstico de un carcinoma primario de glándula mamaria, no existiendo un tipo histológico de carcinoma mamario, más predominante o frecuente en los casos de cáncer de mama oculto (8,9).
El protocolo de trabajo en una situación de adenopatía axilar sospechosa sin lesión mamaria palpable, comienza con la historia clínica de la paciente, pasándose a la realización de mamografía bilateral digital, la cual tiene una sensibilidad para el tumor primario de la mama superior al 85 %, complementándose con el ultrasonido mamario, aumentando la sensibilidad por encima del 90 % (8,9,13,14,15,16).
El método más sensible para analizar la estructura anatómica en pacientes con adenopatía axilar de la mama es la resonancia magnética, que detecta el tumor primario entre un 43 % a 85 % de los casos, según los estudios revisados (17,18,19).
Los resultados de la ultrasonografía convencional son escasamente alentadores, con un elevado número de falsos positivos y falsos negativos (16). La poca rentabilidad diagnóstica de la mamografía ha elevado el empleo de la resonancia nuclear magnética. Ésta última ha demostrado una alta sensibilidad entorno al 85 %-100 %, pero con una baja especificidad, entorno del 35 %-90 %, oscilando el tamaño de las lesiones que se diagnostican, alrededor de 9 mm y 20 mm, definiendo lesiones malignas mamarias en un 75 % de los casos inicialmente clasificados como cáncer de mama oculto. La resonancia magnética bilateral mamaria, tiene que ser parte de la evaluación de las mujeres con cáncer de mama oculto (19).
Al analizar la literatura, paciente con diagnóstico de cáncer de mama oculto, al realizarse la resonancia magnética con gadolinio, en los 2/3 de los casos dejaron de serlo, debido al hallazgo imagenológico de la lesión primaria en la glándula mamaria. Parece definido en la bibliografía que el valor de la mamografía vs., la resonancia magnética, en la detección del cáncer de mama oculto es bajo con una sensibilidad del 29 % y una especificidad del 73 % (15,16).
Los estudios con radiofármacos, gammagrafía y tomografías de emisión de positrones no suelen estar indicados de manera rutinaria y no están incluidos en las guías de protocolo de cáncer de mama oculto. En los casos publicados que incluyeron el estudio de PET CT, se menciona que tiene una elevada sensibilidad, para diagnosticar enfermedad metastásica en la axila y a distancia superior al 90 % (20, 21 ,22,23).
El examen histopatológico es esencial para el diagnóstico, incluyendo pruebas para marcadores biológicos por inmunohistoquímica, ya que en más del 50 % de los casos, las células malignas en el ganglio expresan receptores hormonales. Las citoqueratinas como CK7, CK20, factor de crecimiento epidérmico y los marcadores Gata3 y Gcdpf-15 también se expresan lo que sugiere, un diagnóstico de una lesión primaria maligna primaria en la glándula mamaria.
Debido a la complejidad de esta enfermedad, un equipo multidisciplinario debe decidir el tratamiento. Todos los pacientes reciben tratamiento sistémico según el caso, ya sea neoadyuvante o adyuvante, basándose en el subtipo intrínseco molecular del tumor (24).
Desde la época de Cameron (6) y Halsted (5), la mastectomía radical modificada ha sido la cirugía tradicional en los casos de cáncer de mama oculto. La alternativa actualmente a la conducta anterior, es la linfadenectomía o disección axilar de dos o tres niveles, acompañada de la preservación de la glándula mamaria y de la aplicación de radioterapia externa a la misma. La cuadrantectomía, la mastectomía parcial del cuadrante supero externo de la mama correspondiente, ha sido abandonada por la mayoría de los autores (25 ,26).
El tiempo libre de enfermedad y la supervivencia global en pacientes con cáncer de mama oculto, suelen ser similares, al comparar las series de pacientes, a quienes se les realizó mastectomía radical vs linfadenectomía axilar más radioterapia externa a la glándula mamaria, y a las áreas de drenaje. Por eso la tendencia es a la conservación de la glándula mamaria y su consiguiente irradiación externa, más la irradiación a las áreas ganglionares de drenaje (27,28, 29,30 , 31).
Hay series que promueven la observación de la glándula mamaria, no realizar cirugía y tampoco irradiación externa, solo realizar la disección axilar más tratamiento sistémico. En estos casos las recaídas locales y regionales suelen ser mayores, cuando se comparan observación vs., radioterapia a la glándula mamaria, con un período libre de enfermedad y sobrevida superiores, cuando se indica radiaciones externas a la mama y a las áreas ganglionares de drenaje. Autores como Van Oijen y col., (30) promueven la actitud expectante, lo cual no es recomendable, debido a la elevada frecuencia con que los tumores primarios acaban apareciendo en la mama en más del 50 % de los casos (29).
La supervivencia fue mayor en aquellas pacientes que recibieron radioterapia externa a la glándula mamaria al comparar observación y recibir tratamiento. Se ha sugerido como método de tratamiento administrar radioterapia externa a la glándula mamaria, y se han publicado resultados de control local de la enfermedad en el 72 % al 100 % de los casos. Después de un seguimiento de 57 meses, Varadarajan (32) y col., trataron a 8 pacientes con cáncer oculto de la mama mediante radioterapia externa a la glándula mamaria sin cirugía. Ninguno de los pacientes presentó recaídas locorregionales ni metástasis a distancia.
Dado que en un alto porcentaje de las glándulas mamarias bien estudiadas no se encuentran tumores en la pieza operatoria, la cuadrantectomía está totalmente desaconsejada, no debemos realizar cirugías mamarias a ciegas, y también hay más resistencia a realizar mastectomías totales con vaciamiento axilar (8, 9, 11).
En caso de consultar con una adenopatía axilar metastásica de origen mamario, sin otro tumor primario maligno demostrado, el estándar actual indica que se debe realizar linfadenectomía
o disección axilar para obtener factores pronósticos (números de ganglios involucrados, estudios de inmunohistoquímica, entre otros) y así lograr control local de la enfermedad en la axila. Cuando se realiza una linfadenectomía axilar, es necesario irradiar las áreas de drenaje, como lo son la fosa supraclavicular, axilar y la cadena mamaria interna. El número de ganglios afectados en estos casos ayuda en el pronóstico. El 91 % de las personas sobreviven a los 5 años si solo hay 1 a 3 ganglios afectados y el 65 % si hay más de 4 ganglios afectados (33).
Incluir un tratamiento sistémico, como hormonoterapia, quimioterapia adicional y anticuerpos monoclonales, es fundamental. En algunos casos, el tratamiento sistémico será neoadyuvante, especialmente en los subtipos moleculares triple negativo, HER 2 neu positivos, con quimioterapia y terapias ANTIHER 2 neu, así como al presentarse la paciente con plastrón axilar o N2 al momento del diagnóstico, y en los casos de N3. Aunque hay pocos casos publicados, la predicción parece ser más favorable en comparación con pacientes en el mismo estado y con tumores palpables, estadios II, donde se registra una sobrevida del 50 % al 71 % a los 10 años (34,35).
REFERENCIAS
1. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136(8):E359-386. doi: 10.1002/ijc.29210
2. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 201868(9):394-424. doi: 10.3322/caac.21492
3. Walker GV, Smith GL, Perkins GH, Oh JL, Woodward W, Yu TK, et al. Population-based analysis of occult primary breast cancer with axillary lymph node metastasis. Cancer. 2010;116(17):4000-4006. doi: 10.1002/cncr.25197
4. Cisneros-Reig I, Laguna Sastre M, Sánchez AM, Guinot NJ, Gamón Giner JL, Sanchis JL, et al. Bilateral occult breast carcinoma: ¿A second primary tumour or contralateral tumour metastases? Eur J Surg. 2001;167:312-315.
5. Halsted W. The results of radical operations for the cure of the carcinoma of the Breast. Ann Surg. 1907;46 (1):1-19.
6. Cameron HC. An Address entitled Some clinical facts regarding mammary cancer. Br Med J. 1909;1:577-582.
7. Owen H K, Dockerty M B, Gray H K. Occult carcinoma of the breast. Surg Gynecol Obstet. 1954;98(3):302-308
8. Luna MA, Sánchez Méndez S, Mariscal A, Vizcaya V, Vallejos M, Solác M, et al. Cáncer oculto de la mama. Caso clínico y revisión de la literatura. Clínica e Investigación en Ginecología y Obstetricia. 2012;39(1) :21-28.
9. Yesika J. Dávila-Zablah*, Blanca K. Kanagusico-Elguezabal y Margarita L. Garza-Montemayor. Cáncer oculto de mama: reporte de un caso y revisión de la literatura. Anales de Radiología México. 2018;17:226-33
10. Walker GV, Smith GL, Perkins GH, Oh JL, Woodward W, Yu TK, et al. Population-based analysis of occult primary breast cancer with axillary lymph node metastasis. Cancer. 2010;116:4000-4006.
11. Brill KL, Brenin DR. Occult breast cancer and axillary mass. Curr Treat Options Oncol. 2001; 2:149-155.
12. Whillis D, Brown PW, Rodger A. Adenocarcinoma from an unknown primary presenting in women with an axillary mass. Clin Oncol(R Coll Radiol). 1990; 2:189-192.
13. Leibman AJ, Kossoff MB. Mammography in women with axillary lymphadenopathy and normal breast on clinical examination. Am J Roentgenol. 1992; 159:493-495.
14. Sibbering DM, Burrel AC, Evans DJ, Yeoman LJ, Wilson ARM, Robertson JFR, et al., On behalf of the breast team. Mammographic sensitivity in women under 50 years presenting symptomatically with breast cancer. The Breast. 1995;4:127-129.
15. Scoggins CR, Vitola JV, Sandler MP, Atkinson JB, Frexes-Steed M. Occult breast carcinoma presenting as axillary mass. Am Surg. 1999;65:1-5.
16. Jackson VP. What is the role of sonographic breast imaging for detecting occult cancer in a patient with a strong family history of breast cancer and mammographically dense breasts without obvious masses? AJR Am J Roentgenol. 1995; 165:1004.
17. Morris E, Schwartz L, Dershaw D, Van Zee K, Abransom A, Liberman L. MR imaging of the breast in patients with occult primary breast carcinoma. Radiology. 1997; 205:437-440.
18. Olson Jr JA, Morris EA, Van Zee KJ, Linehan DC, Borgen PI. Magnetic Resonance Imaging Facilitates Breast Conserva tion for Occult Breast Cancer. Ann Surg Oncol. 2000;7: 411-415.
19. Lieberman S, Sella T, Maly B, Sosna J, Uziely B, Sklair-Levy M. Breast magnetic resonance imaging characteristics in women with occult primary breast carcinoma. Isr Med Assoc J. 2008; 10:448-452.
20. Nieweg OE, Wong W, Singletary SE, Hortobagy GN, Kimm EE. Positron emission tomography with fluorine-18-deoxyglucose in the detection and staging of breast cancer. Cancer. 1993;71:3920-3925.
21. Avril N, Rose C, Schelling M, Dose J, Kuhn W, Bense S, et al. Breast imaging with positrón emission tomography and fluorine 18 fluorodesoxiglucose: Use and limitations. J Clin Oncol. 2000;18:3495-3502.
22. Ruiz G, Jiménez A, Pérez MJ, Montz R, González M, Carreras JL. PET-FDG en cáncer oculto de mama. Cir Esp. 2001;70 (2):105-107.
23. Taira N, Ohsumi S, Takabatake D, Hara F, Takashima S, Aogi K, et al. Contrast-enhanced CT evaluation of clinically and mammographically occult multiple breast tumors in women with unilateral early Breast cancer. Jpn J Clin Oncol. 2008; 38:419-425.
24. He M, Tang L-C, Yu K-D, Cao A-Y, Shen Z-Z, Shoa Z-M, et al. Treatment outcomes and unfavorable prognostic factors in patients with occult breast cancer. Eur J Surg Oncol. 2012;38:1022-1028.
25. Sohn G, Son BH, Lee SJ, Kang EY, Jung SH, Cho SH, et al. Treatment and survival of patients with occult breast cancer with axillary lymph node metastasis: A nationwide retrospective study. J Surg Oncol. 2014;110(3):270-274.
26. Shannon C, Walsh G, Sapunar F, AHern ´R, Smith I. Occult primary breast carcinoma presenting as axillary lymphadenopathy. Breast. 2002;11:414-418.
27. Masinghe SP, Faluyi OO, Kerr GR, Kunkler IH. Breast radiotherapy for occult breast cancer with axillary nodal metastases-does it reduce the local recurrence rate and increase overall survival? Clin Oncol (R Coll Radiol). 2011;23:95-100.
28. Kim BH, Kwon J, Kim K. Evaluation of the benefit of radiotherapy in patients with occult breast cancer: A population-based analysis of the SEER database. Cancer Res Treat. 2018;50(2):551-561. doi: 10.4143/crt.2017.189
29. Vlastos G, Jean ME, Mirza AN, Mirza NQ, Kuerer HN, Ames FC, et al. Feasibiliaty of breast preservation in the treatment of occult primary carcinoma presenting with axillary metastases. Ann Surg Oncol. 2001;8:425-431.
30. Van Ooijen B, Bontenbal M, Henzen-Logmang S C, Koper P C. Axillary nodal metastases from an occult primary consistent with breast carcinoma. Br J Surg. 1993;80(10):1299-300.
31. Ellerbroek N, Holmes F, Singletary E, Evans H, Oswald M, McNeese M. Treatment of patients with isolated axillary nodal metastases from an occult primary carcinoma consistent with breast origin. Cancer. 1990;1990(66):1461-1467.
32. Varadarajan R, Edge SB, Yu J, Watroba N, Janarthanan BR. Prognosis of occult breast carcinoma presenting as isolated axillary nodal metastasis. Oncology. 2006; 71:456-459.
33. Wang R, Chen J, Huang J J, Qing L V. Best Treatment options for Occult breast cancer. A meta-analysis. Front Oncol. 2023;13:1051232.
34. Arlow RL, Paddock LE, Niu XL, Kirstein L, Haffty BG, Goyal S, et al. Breast conservation therapy after neoadjuvant chemotherapy does not compromise 10-year breast cancer specific mortality. Am J Clin Oncol. 2018 41(12):1246-1251.
35. Cohen BL, Collier AL, Kelly KN, Goel N, Kesmodel SB, Yakoub D, et al. Surgical management of the axilla in patients with occult breast cancer (cT0 n+) after neoadjuvant chemotherapy. Ann Surg Oncol. 2020;27(10):1830-1841.
Notas de autor
gomezalvaro579@gmail.com