SARCOMA FIBROMIXOIDE DE BAJO GRADO DE MALIGNIDAD DE PARED TORÁCICA. REPORTE DE UN CASO
SARCOMA FIBROMIXOIDE DE BAJO GRADO DE MALIGNIDAD DE PARED TORÁCICA. REPORTE DE UN CASO
Revista Venezolana de Oncología, vol. 36, núm. 3, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 14 Octubre 2013
Aprobación: 17 Marzo 2024
Resumen: El fibrosarcoma mixoide de bajo grado de malignidad es un tumor raro, descrito por Evans en 1987, de curso clínico e histológico e inmunohistoquímico de apariencia benigna, pero con comportamiento local y a distancia agresivo, corresponde 0,7 % de todos los tumores de tejido blando. OBJETIVO. Presentación de caso de sarcoma fibromixoide de pared torácica de bajo grado de malignidad. MÉTODO: Descripción del caso, revisión bibliográfica. CASO CLÍNICO: Masculino 46 años de edad presenta masa palpable dolorosa en hemitórax anterolateral derecho de un año de evolución. Examen físico se precisa lesión ocupante de espacio pétrea, fija mal delimitada en hemitórax anterolateral derecho, de 12 cm x 10 cm x 8 cm aproximadamente. Estudios de imagen que evidencian lesión de partes blandas, que no infiltra arcos costales y se insinúa sobre músculo oblicuo lateral derecho. Llevado a mesa operatoria practicándose resección completa de lesión tumoral. Biopsia definitiva concluida como fibrosarcoma mixoide de bajo grado de malignidad de pared torácica con márgenes libres de tumor. CONCLUSIÓN: El fibrosarcoma mixoide de bajo grado de malignidad es una rara neoplasia, siendo la presentación costal menos frecuente, su manejo terapéutico representa un desafío para el médico debido a que el tratamiento de elección es quirúrgico y la mayoría de las veces conlleva resecciones amplias y deformantes.
Palabras clave: Tumor, fibrosarcoma, mixoide tejidos blandos, malignidad, pared costal.
Abstract: The low grade myxoid fibrosarcoma is a rare tumor, described by Evans in 1987, a benign-appearing clinical and histological and immunohistochemical, but with aggressive local and remote behavior, corresponding to 0.7 % of all tissue sokt tumors. OBJECTIVE. Presentation of a case of fibromyxoid sarcoma of the chest wall of low-grade malignancy. METHOD: Case description and the bibliographic review. CLINICAL CASE: 46 year old male who presented a palpable painful mass in one year history of the right antero lateral hemithorax. The physical examination requires a lesion occupying the stone space, which is poorly defined in the right anterolateral hemithorax, approximately 12 cm x 10 cm x 8 cm. The imaging studies that show soft tissue injury, which does not infiltrate the rib arches and is shown on the right lateral oblique muscle. He was taken to the operating table, performing a complete resection of the tumor lesion. The definitive biopsy concluded as low grade myxoid fibrosarcoma of the chest wall with tumor free margins. CONCLUSION: The low grade myxoid fibrosarcoma is a rare neoplasm, and the rib presentation is less frequent, the therapeutic management of which represents a challenge for the medical doctor because the treatment of choice is surgical and most of the time involves extensive and deforming resections. KEY WORD: Tumor, fibrosarcoma, soft tissue, myxoid, malignancy, rib wall.
Keywords: Tumor, fibrosarcoma, The low grade myxoid fibrosarcoma is a rare tumor, myxoid, malignancy, rib wall.
INTRODUCCIÓN
Las lesiones neoplásicas de la pared torácica son muy raras de encontrar, en estas se incluyen las de los tejidos óseos y/o tejidos blandos, que pueden ser de origen primario o secundario (metástasis). Estas lesiones tumorales primarias de la pared torácica representan aproximadamente entre el 2 % a un 5 % de todos los tumores del tórax, son de manejo difícil diagnóstico y terapéutico por lo que ameritan un estudio minucioso, detallado y exhaustivo para su abordaje su corrección (1).
El sarcoma fibromixoide de bajo grado (LGFMS) es un tumor infrecuente, con rasgos histológicos de bajo grado y curso clínico paradójicamente agresivo, conocido también como tumor de Evans quien lo describió en 1987 (2). Se trata de un tumor de partes blandas fibroblástico de apariencia histológica aparentemente benigna y un curso clínico indolente y maligno, con recidivas locales tardías y metástasis a distancia tardías, por lo que en la actualidad se puede afirmar que la evolución de este tumor es de predominio lento, pero frecuentemente implacable debido a su potencial metastatizante y al eventual desarrollo de recidivas locales con el paso de los años. A pesar de ello, se han descrito casos de supervivencia a los 50 años del diagnóstico inicial (3).
Afecta por lo general a la población adulta jóven, con un ligero predominio del sexo masculino. Son tumores malignos que pueden surgir de los tejidos mesodérmicos en diferentes localizaciones: extremidades (50 %), tronco y retroperitoneo (40 %), cabeza y cuello (10 %).
Asimismo, estos tumores pueden infiltrar a tejidos vecinos, en algunos casos el tumor está confinado a los músculos, aponeurosis o fascia (4).
Su origen etiológico es desconocido, pero se ha relacionado e involucrado con diversos factores como el genético como lo es la neurofibromatosis, síndrome de Gardner, síndrome de Wermer, esclerosis tuberosa, síndrome de nevus de células basales, síndrome de Li-Fraumeni, linfedema posquirúrgico o posirradiación, infección parasitaria, radiación ionizante, trauma en extremidades, exposición a químicos, entre otros (5).
Con respecto a su origen embriológico todavía no esta claro su mecanismo de aparición, aunque al parecer este se deriva de la hoja embriogénica del mesodermo, debido a esto es que su localización o situación se puede observar en los diferentes tejidos como: tejidos blandos, hueso, piel, órganos internos e incluso vaso y nervios. Los originados en partes blandas son en su gran mayoría benignos y cien veces más comunes que los malignos (6).
Su síntomatologia más frecuente es presentarse como una aparición de sensación de masa de aparición repentina indolora o con dolor local o referido, que muchas veces pasan desapercibidos ante la vista de los médicos tratantes, o son minimizados por el paciente, no obstante están presentes hasta en un 40 %. Asimismo, puede coexistir historia de trauma reciente, que se asocia incidentalmente, no causalmente con el hallazgo del tumor; la historia clínica, es fundamental, para establecer la duración de la masa, su velocidad de crecimiento, otra sintomatología asociada, ya sea esta local o lejana al sitio de la aparición de la lesión (7).
En cuanto a la estrategia diagnóstica esta basada en técnicas de imagen, esencialmente son la tomografía computarizada (TC) o la imagen de resonancia magnética (RMN) particularmente útil porque pueden dar dato más exacto en cuanto a su localización y extensión anatómica, asi como permite definir los límites tumorales para determinar su resecabilidad, pero son inespecíficas para la tipificación tumoral.
En la actualidad el único tratamiento viable es la cirugía, la escisión local amplia con un margen de tejido normal o bordes sanos de 2 cm - 3 cm, más allá de la lesión tumoral palpable, debería ser el tratamiento de elección (8).
La periferia de la lesión, usualmente se pierde en forma imperceptible en el tejido muscular vecino, dificultándole al cirujano y al patólogo precisar los límites de la lesión, sin embargo, la tasa de recurrencias locales varía y esto depende de la edad del paciente, de la localización de la lesión tumoral y de los márgenes de resección, es por ello que recurrencia después de la cirugía son de aproximadamente 35 % a 70 % (9).
En cuanto el tratamiento con radioterapia puede controlar lesiones irresecables y disminuir el riesgo de recurrencia local cuando el margen de resección está cerca del borde del tumor, cirugía y el uso de radioterapia como adyuvante de la cirugía, el índice de porcentaje de recurrencia son considerablemente bajos (0 % a 30 %) (10).
La tasa de supervivencia a cinco años se puede observar en el 92 % de los pacientes tratados con intentos curativos (cirugía o cirugía más radioterapia). No obstante muchos pacientes se presentan al inicio con enfermedad irresecable y debido a esto necesitarán otras modalidades terapéuticas (11).
Exiten otras alternativas terapéutica, done se están incluyendo el uso de drogas antiinflamatorias no esteroideas como la indometacina (que al actuar como inhibidores de las prostaglandinas pueden controlar la proliferación neoplásica), medicamentos antiestrógenos como el tamoxifeno y toremifeno, agentes progestacionales como la medroxiprogesterona o la administración de esteroides como la prednisona.
En la actualidad como complemento en la terapéutica de este tipo de neoplasia se empezó a recomendar el uso de la quimioterapia, la cual debe ser considerada en pacientes sintomáticos con lesiones tumorales irresecables, quienes no han respondido a regímenes menos tóxicos como los mencionados anteriormente (9,10,11,12).
El objetivo de este trabajo es el reporte de un caso de un paciente con fibrosarcoma mixoide de bajo grado de malignidad de pared torácica de poca frecuencia; es una neoplasia rara del tejido conectivo y de las aponeurosis de músculos esqueléticos, es una entidad tumoral benigna de origen fibroblástico bien diferenciado que se clasifica como tumor de partes blandas.
Estas lesiones presentan un comportamiento biológico intermedio entre los tumores fibroblásticos benignos y el fibrosarcoma, teniendo la capacidad de presentar recidiva local pero nunca metástasis.
CASO CLÍNICO
Motivo de consulta: “aumento de volumen en hemitórax derecho”. Enfermedad actual: paciente masculino de 46 años de edad, sin antecedentes patológicos, traumáticos ni personales previos de interés, quien refiere inicio de enfermedad actual hace 1 año caracterizado por aumento de volumen progresivo en tercio inferior anterolateral de hemitórax derecho, acompañado de dolor de leve a moderada intensidad sin irradiación, por lo que acude a facultativo quien solicita estudios de imágenes radiografia, ecosonograma y TC.
A la exploración fisica se aprecia y se palpaba una masa prominente aproximadamente de unos 12 cm x 10 cm x 8 cm de consistencia dura, no adherida a planos profundos y sin signos inflamatorios cutáneos, localizada en la pared costal anterolateral del tercio inferior del hemitórax derecho, resto del examen normal (Figura 1). La analítica de laboratorio realizada resultó normal incluyendo marcadores tumorales (alfafetoproteína, CA 125, CA19 9 y CEA).
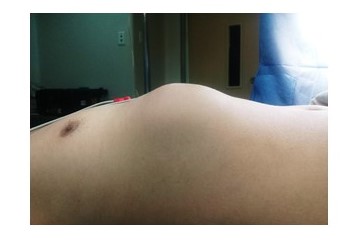
Figura 1.
Paciente con aumento de volumen en tercio inferior de hemitórax derecho, caracterizado por una masa no dolorosa en la pared costal anterolateral (interlineas blancas).
En la radiografía de tórax postero anterior y lateral derecha se aprecia una masa sobre la parrilla costal derecha, que no afecta a los arcos laterales de séptima, octava y novena costillas (Figura 2).
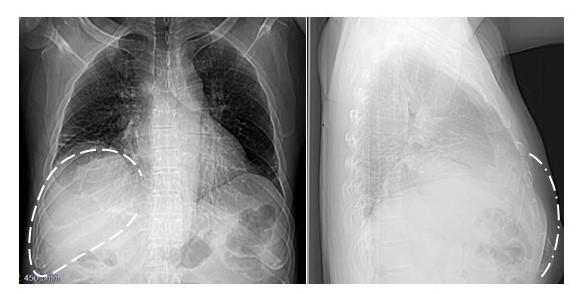
Figura 2
Radiografía PA y lateral derecha de tórax: se aprecia una masa sobre la parrilla costal derecha, que no afecta a los arcos laterales de séptima, octava y novena costillas.
Se solicitó TC de tórax de alta resolución hallazgos: se describe la presencia de una lesión hipodensa, homogénea torácica pélvica de unos 100 mm x 110 mm de diámetros transverso y anteroposterior, que se ubica a nivel de la pared antero lateral del hemitórax derecho inferior, que parecía depender del músculo oblicuo externo derecho, que no compromete plano óseo, ni intravisceral. Conclusión: lesión sólida de pared torácica anterior lateral derecha (Figura 3).
Se decide llevar a mesa quirúrgica practicando incisión de toracotomía anterolateral derecha sobre la zona tumoral, se aprecia una gran masa tumoral dura y con firme base de implantación sobre los arcos laterales de séptima, octava y novena costillas. Se realiza resección en bloque de partes blandas con resección oncológica de la masa que involucra músculo oblicuo externo con amplios márgenes (Figura 4).
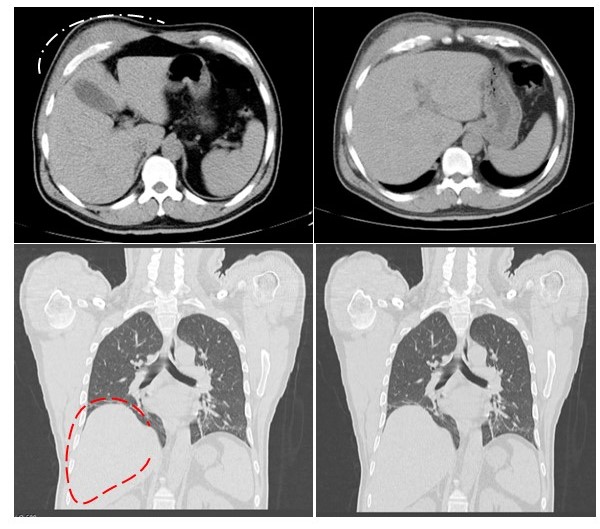
Figura 3.
Tomografía computada de tórax de alta resolución. Donde se aprecia una masa de partes blandas en la cara anterolateral del hemitórax derecho sin reacción perióstica de los arcos costales subyacentes.
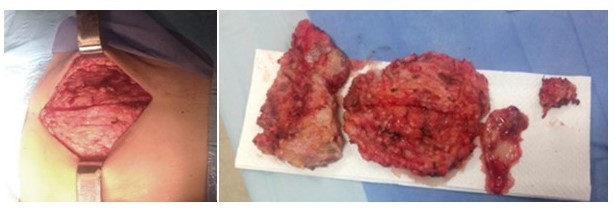
Figura 4.
Toracotomía antero lateral derecha a nivel del 9o espacio intercostal con resección quirúrgica de la lesión tumoral en su totalidad muestra patológica macroscópica.
La pieza quirúrgica fue enviada al laboratorio de patología, el estudio anatomopatológico: secciones biópsicas permiten evidenciar neoplasia de aspecto mesenquimal constituida por una baja densidad de células con núcleos ovoides con ligero pleomorfismo e hipercromatismo, sin figuras mitóticas, con citoplasma eosinofílico claro, en algunas células estrellada, que se disponen en haces paralelos (“espinas de pescado”), observándose tendencia a disponerse en forma arremolinada en áreas. Dichas células se evidencian inmersas en tejido fibrocolágeno denso, en algunas áreas mixoide, con escaso infiltrado linfoplasmocitario y vasos sanguíneos arciformes, dispuestos alrededor de las áreas mixoides.
Desde el punto de vista inmunohistoquímico las células tumorales mostraron positividad para vimentina (3+), actina de músculo en la pared de los vasos sanguíneos (3+), EMA (3+), el indicador de proliferación celular Ki-67 se expresó en el 8 % de los núcleos de las células tumorales. Negativas para citoqueratina, S-100, desmina, CD117, BCL2. Diagnóstico: hallazgos histopatológicos e inmunohistoquímicos compatibles con sarcoma fibromixoide de bajo grado tumor de Evans (Figura 5).
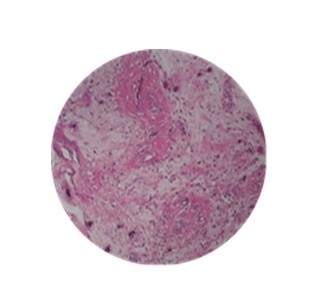
Figura 5.
Microfotografía. Corte histológico se evidencia neoplasia mesenquimal de células redondas y ovoides que proliferan de manera difusa con patrón mixoide, carecen de atipia y mitosis, alternando con abundantes haces de colágena hialina. La inmunohistoquímica mostró vimentina positiva y proteína S100 negativa.
La evolución posoperatoria es satisfactoria, y el paciente es dado de alta a los dos días de la intervención. Es remitido al servicio de oncología donde se decide el empleo de radioterapia externa. En la revisión practicada al año de la intervención no se aprecian signos clínicos ni radiológicos de recidiva.
DISCUSIÓN
Los tumores de tejido blando forman un gran grupo heterogéneo de neoplasias; histomorfológicamente e inmunohistoquímicamente, los datos experimentales sugieren que la mayoría de los sarcomas parten de células mesenquimales primitivas multipotenciales, que en el curso de su transformación neoplásica se diferencian en una o más líneas celulares. Los sarcomas de tejidos blandos (STB) representan aproximadamente el 1 % de todos los tumores en la población adulta y el 15 % en la edad pediátrica. El término "tejidos blandos" incluye músculo, tendones, tejido fibroso, graso, sinovial, vasos y nervios. Pueden invadir con frecuencia los territorios circundantes y a su vez pueden presentar metástasis a distancia. Estos tumores suelen aparecer en las extremidades proximales y el tronco, pero esporádicamente se pueden encontrar en lugares inusuales, como el retroperitoneo, la cabeza o la pared torácica (13).
El LGFMS es una variante distintiva del fibrosarcoma con un alto potencial de metástasis y, a veces, un largo intervalo entre la presentación del tumor y la metástasis, plantea un gran problema para los patólogos, radiólogos y cirujanos, es por ello que el seguimiento de larga data es el principio fundamental para el manejo del tumor.
La Clasificación Internacional de Enfermedades Oncológicas de la OMS (ICD-O), el LGFMS corresponde a una de las variedades de sarcoma de partes blandas incluidas dentro del grupo de los tumores fibroblásticos- miofibroblásticos, en el cual se incluyen igualmente el fibrosarcoma del adulto, el mixofibrosarcoma, el tumor de células especuladas hialinizante y el fibrosarcoma esclerosante. Corresponden a sarcomas de partes blandas situándose su frecuencia en 1 % de todos los tumores son de apariencia histológica benigna, pero con un alto potencial metastatizante, que se caracteriza de largos intervalos entre la aparición del tumor primario y sus metástasis (14).
La presentación clínica suele ser prolongada y está relacionada principalmente con la ubicación o localización anatómica de la masa tumoral. El LGFMS generalmente se presenta como una masa indolora de tejidos blandos con una duración previa a la biopsia de más de 5 años en el 15 % de los pacientes. En raras ocasiones pueden presentarse de la forma aguda de la enfermedad, como distress o dificultad respiratoria aguda y dolor torácico en caso de LGFMS en la pared torácica o actividad convulsiva en un paciente con LGFMS intracraneal (14). Como se presentó nuestro caso con poco o escaso dolor.
El diagnóstico de LGFMS generalmente no es difícil si el tumor se ha extirpado por completo y todas las características morfológicas e inmunofenotípicas características descritas anteriormente están presentes. El diagnóstico basado en técnicas de imagen, fundamentalmenteTC y RMN, permite definir los límites tumorales aunque son inespecíficas para la tipificación tumoral.
Sin embargo, los hallazgos en los estudios de imágenes de LGFMS suelen ser en muchos casos inespecíficos, por lo que se han descrito ciertos hallazgos en la TC y en la RMN. En las imágenes tomográficas sin contraste, el componente fibroso de estos tumores se ha descrito como isodenso al tejido muscular y el componente mixoide como hipodenso. Como sucedió en el caso que estamos describiendo (15).
Mientras que en las imágenes por RMN, el componente fibroso se caracteriza por ser hipointenso en las imágenes ponderadas en T1 y T2, y mejorar ligeramente en las imágenes ponderadas en T1 después de la administración de gadolinio.
Por otro lado, el componente mixoide se ha descrito como hipointenso en las imágenes ponderadas en T1 e hiperintenso en las imágenes ponderadas en T2, y realzando vívidamente en las imágenes ponderadas en T1 después de la administración de gadolinio. También se pueden encontrar calcificaciones dentro del tumor (16).
Una vez que se este con una alta sospecha de LGFMS y atendiendo a que existen cincuenta subtipos diferentes, dependiendo del tejido en el que se origine la lesión, algunos subtipos muy concretos poseen características específicas que determinan su terapéutica. Se debe determinar su grado histológico, que permite clasificar los sarcomas de menor (bajo grado) grado I, a mayor agresividad (alto grado) grados II-III, atendiendo sobre todo a la rapidez de división de las células y a su apariencia diferente de las células sanas. Los sarcomas de alto grado crecen rápidamente y poseen mayor tendencia a desarrollar metástasis en el curso de la enfermedad, mientras que en los de bajo grado el crecimiento es lento y se observa una mayor tendencia a la recidiva local que al desarrollo de metástasis a distancia.
Asimismo, se debe realizar su estadificación los SPB pueden clasificarse en dos estados diferentes: aquellos que se encuentran en fase localizada, y los que se encuentran diseminados, debido a la presencia de metástasis a distancia. La localización más frecuente de metástasis es el pulmón, excepto en los sarcomas intraabdominales, en los que predominan las metástasis hepáticas. La diseminación a los ganglios linfáticos regionales es rara en los sarcomas, y sólo se observa ocasionalmente en algunos subtipos determinados (sobre todo sarcoma epitelioide, sarcoma de células claras y sarcoma sinovial), y se asocia a pronóstico desfavorable. Dentro de los SPB localizados, la estadificación se establece tomando en consideración los siguientes factores: tamaño tumoral (mayor o menor de 5 cm), localización superficial o profunda, y grado histológico (bajo o alto). Nuestro paciente en cuanto al grado histológico, es de bajo grado (grado I) y con respecto a su estadificación puede clasificarse en fase localizada (17).
En el estudio histologico este se caracteriza por presentar una mezcla de zonas hipocelulares colagenizadas y más nódulos mixoides celulares. Las células tumorales suelen ser pequeñas, con escaso citoplasma eosinofílico, núcleos redondos a ovoides y nucleolos ausentes. Aunque se pueden encontrar áreas citológicamente atípicas focales de alta celularidad, aumento de la actividad mitótica, hipercromatismo nuclear y necrosis en aproximadamente el 10 % de los casos, las células tumorales generalmente se caracterizan por figuras mitóticas ausentes o escasas, anaplasia nuclear o necrosis
La tinción inmunohistoquímica es positiva para vimentina solamente y negativa con una variedad de anticuerpos, como desmina, queratina, proteína S100, antígeno de membrana epitelial, CD34 y CD31. La actina específica del músculo es positiva en la pared de los vasos pequeños dentro del tumor y muy positiva en la capa fibrosa periférica (14).
El tratamiento de los SPB es habitualmente multidisciplinario, incluyendo cirujanos especializados (cirujanos ortopédicos y/o cirujanos plásticos), oncólogos radioterapeutas y oncólogos médicos. Debido a la baja incidencia de estos tumores, a su gran heterogeneidad, y a su complejidad terapéutica, se recomienda que los pacientes deberían sean tratados por un equipo multidisciplinario. El tratamiento del sarcoma localizado es quirúrgico se debe conseguir la extirpación del tumor con tejido sano alrededor, asegurando unos márgenes de resección libres de afectación tumoral. Ello puede obtenerse mediante una cirugía amplia (con márgenes libres de tumor) o una cirugía radical (existen dos modalidades: amputación de la extremidad y cirugía compartimental, o resección de todo el compartimento muscular) (17).
La cirugía amplia es menos mutilante que la radical, y consigue unos resultados similares por lo que ha ido desplazando a ésta en la mayoría de casos, sin disminuir las probabilidades de curación. Sin embargo, en algunas localizaciones no siempre es posible obtener unos márgenes libres de tumor, y en esos casos puede ser necesario recurrir a la amputación para conseguir una extirpación adecuada. En los últimos años, se han incorporado al tratamiento quirúrgico, tratamiento complementario, como la radioterapia posoperatoria y las técnicas reconstructivas de la cirugía plástica, que han permitido reducir considerablemente el número de amputaciones sin comprometer la curación (18).
A nuestro paciente se le practicó una resección de todo el compartimento muscular del oblicuo externo con márgenes libres de lesión tumoral, con tratamiento complementario con radioterapia posoperatoria.
Se debe hacer un seguimiento periódico de estos pacientes puesto que un 15 %-20 % de los enfermos que recaen pueden ser curados con tratamientos de rescate. La mayoría de las recidivas se producen en los dos primeros años, aunque también existen recidivas muy tardías. El riesgo de recaída está influido por el grado de malignidad, la localización de la lesión primaria y el tratamiento correcto. El seguimiento se realiza habitualmente mediante exploración física y radiografía de tórax o TC de tórax, pero de forma más espaciada se realiza RMN del lecho tumoral, o TC de abdomen en caso de que se trate de un sarcoma retroperitoneal (17,18,19).
Concluimos en que el sarcoma fibromixoide de bajo grado es una neoplasia maligna citológicamente blanda con estroma fibroso y mixoide alternante de bajo grado y potencial maligno, se considera un tumor poco frecuente de tejidos blandos con un alto potencial de metástasis a distancia, a pesar de su aspecto histológico benigno, es probable que este paciente tenga un pronóstico favorable con un seguimiento cercano a largo plazo porque el tumor era solitario, bien encapsulado, confinado en el área localizada y no mostraba mitosis en la histología.
El reporte del caso presentado se llevó a cabo con la finalidad de enriquecer la literatura en cuanto a la información sobre el diagnóstico por imágenes, diagnóstico histológico e inmunohistoquímico, asi como el tratamiento quirúrgico de este tumor raro. Como no existe un protocolo específico con respecto a los exámenes de seguimiento y para diagnosticar tempranamente una posible metástasis, es importante informar a los pacientes sobre el potencial metastásico de larga data de la enfermedad.
REFERENCIAS
1. Araujo-Cuauro JC, Fernández F, Solarte J, Sánchez M. Mixofibrosarcoma: fibrohistiocitoma maligno de bajo grado en axila. Reporte de caso, revisión de la literatura. Rev Venez Oncol. 2018;30(1): 35-42.
2. Evans HL. Low-grade fibromyxoid sarcoma. A report of two metastasizing neoplasms having a deceptively benign appearance. Am J Clin Pathol. 1987;88(5):615-619. doi: 10.1093/ajcp/88.5.615.
3. Alfaro-Cervello C, Benavent Casanova O, Nieto G, Mares D, Francisco J. Sarcoma fibromixoide de bajo grado, un diagnóstico diferencial esencial en los tumores mixoides de apariencia benigna. Revista Española de Patología. 2018;51(3):178-182. DOI: 10.1016/j.patol.2017.05.004
4. Tinoco Téllez L, Aguirre Trigueros J, Domínguez Gasca L, Domínguez Carrillo L. Sarcoma fibromixoide de bajo grado. Acta méd. Grupo Angeles. 2016; 14(4):230-234. Disponible en: URL: Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1870-72032016000400230&lng=es.
5. Alfaro-Cervello C, Nieto G, Navarro S. Differential diagnosis of myxoid soft tissue tumors. Experience in the Clinical University Hospital of Valencia. Rev Esp Patol. 2017; 55(3): 185-191. Doi: 10.1016/j.patol.2019.07.005.
6. Citores PM, Tinoco CC, Arenal-VJ, Fernández CB, Torres NM, Zamora MT. Sarcoma fibromixoide de bajo grado: a propósito de 3 casos y revisión de la bibliografía. Cir Cir. 2013; 81(4): 33-339.
7. Lee E, HwangH, Kwon H, Park H, Choi HS. Low grade fibromyxoid sarcoma originating from the masseter muscle: A case report. Med Case Rep. 2015;9:176. https://doi.org/10.1186/s13256-015-0658-9.
8. Navarro DJ, Ferrer MM, Barrera CC, Campos M. Mixofibrosarcoma de bajo grado en la mama: una localización inusual Rev Senol Patol Mamar. 2014; 27(1):54-55. Doi: 10.1016/j.senol.2013.11.002
9. Ballesteros GJ, Casalots CA, Gols RM, Moreno P. Sarcoma fibromixoide de bajo grado intracraneal: a propósito de un caso. Radiología. 2011;53(2):171-174. doi: 10.1016 / j.rx.2010.04.009
10. Mike O, Seegenschmiedt MH. Radiation therapy for aggressive fibromatosis (desmoid tumors): Results of national patterns of care study. Int J Radiant Oncol Biol Phys. 2005; 61: 882-891: doi: 10.1016/j.ijrobp.2004.07.705.
11. Cruz-Benítez L, Cortés-Cárdenas S, Farías Alarcón M, Tenorio-Torres J, Ramírez-Heredia J, Conde-Vázquez E. Sarcoma fibromixoide de región sacra. Reporte de caso. GAMO. 2011;10 (5):319-325. Disponible en: URL: https://www.elsevier.es/es-revista-gaceta-mexicana-oncologia-305-articulo-sarcoma-fibromixoide-region-sacra-reporte-X1665920111894341
12. Bajpai J, Shukla S, Moazzam J, Singh AlokK, Goel Mohit, Mourya Amit, et al. Low‑grade fibromyxoid sarcoma around the knee involving the proximal end of the tibia and patella: A rare case report. Oncol Lett. 2014;7(4):1308-1312. doi.org/10.3892/ol.2014.1888
13. Ballestero-Pomar M, Fernandez-Samos R, Martin-Alvarez M, Barbas-Galindo J, Dominguez-Bahamonde J, Zarco-Castillo J. Extirpación de sarcoma fibromixoide de bajo grado con resección y reconstrucción de arteria femoral. Angiologia. 2005;57(4):345-351.
14.: Folpe A, Van den Berg E, Molenaar WM. Low-grade fibromyxoid tumor sarcoma. World Health Organization Classification of Tumours. Pathology and Genetics of Tumours of Soft Tissue and Bone. En: Fletcher CD, Unni KK, Mertens F, editores. Low grade fibromyxoid sarcoma. Lyon AND IARC Press; 2002. p.104-105.
15. Wu X, Petrovic V, Torode IP, Chow CW. Lowgrade fibromyxoid sarcoma: Problems in the diagnosis and management of a malignant tumour with bland histological appearance. Pathology 2009; 41(2):155-160. doi: 10.1080 / 00313020802579276.
16. Hwang S, Kelliher E, Hameed M. Imaging features of low-grade fibromyxoid sarcoma (Evans tumor). Skeletal Radiol. 2012;41(10):1263-72. doi: 10.1007/s00256-012-1417-
17. Olvia LG, González LM, Araujo SE. Diagnóstico histopatológico de tumores de tejidos blandos. Rev Hosp Niños Buenos Aires. 2011; 53(241): 94-100. Disponible en: URL: http://revistapediatria.com.ar/wp-content/uploads/2012/03/con379-94-101.Olvi_.pdf.
18. Vaquero M. Sarcoma fibroblástico mixoinflamatorio: presentación de un caso y revisión de la literatura. Rev Esp Patol 2008; 41 (3): 223-226. Disponible en: URL: http://www.patologia.es/volumen41/vol41-num3/pdf%20patologia%2041-3/41-03-11.pdf.
19. Sánchez GP, Soler GJF, Lozano R JA, Ruiz MJA. Tumor de Evans de la mano. Una localización excepcional. Rev Iberoam Cir Mano. 2007;35(01):043-047. DOI: 10.1055/s-0037-1606706.
Notas de autor
jcaraujoc_65@hotmail.com.
Información adicional
Consentimiento.: Se obtuvo el consentimiento legítimamente declarado o informado por escrito del paciente para la publicación del caso y las imágenes que lo acompañan.