INMUNOTERAPIA Y SUS CAMBIOS EN LAS IMÁGENES MULTIMODALES 18F FDG-PET/CT
INMUNOTERAPIA Y SUS CAMBIOS EN LAS IMÁGENES MULTIMODALES 18F FDG-PET/CT
Revista Venezolana de Oncología, vol. 36, núm. 3, pp. 182-207, 2024
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 28 Agosto 2023
Aprobación: 19 Abril 2024
Resumen: OBJETIVO: La interpretación adecuada de estudios morfo/metabólicos 18F FDG-PET/CT requiere conocimiento preciso sobre la distribución normal y anormal de la absorción del radiofármaco. A esto se suma que debemos estar atentos en la interpretación de las variantes fisiológicas y fisiopatológicas producto de procedimientos en el manejo de pacientes oncológicos que pueden modificar patrones imagenológicos preestablecidos. Comprender las posibles causas de mala interpretación aumenta la confianza en la interpretación de la imagen, reduce el número de estudios de seguimiento innecesarios, optimiza tratamiento y lo que es más importante, reduce la exposición a radiación del paciente. En estos últimos años la inmunoterapia específicamente los fármacos inhibidores de puntos de control inmunitario nos han dado un importante avance en el tratamiento oncológico, sin embargo, su uso no está exento de reacciones no deseadas denominadas efectos secundarios autoinmunes. MÉTODO: Estos efectos secundarios también nos han llevado a que las imágenes 18F FDG-PET/CT están presentando nuevos patrones imagenológicos de respuesta al tratamiento. Consideramos que el paciente posterior a inmunoterapia representa un cambio radical en la interpretación de un estudio 18F FDG-PET/CT. Revisamos los conceptos actuales sobre la inmunoterapia y sus patrones de efectos adversos relacionados con el sistema inmunitario con especial énfasis en las imágenes multimodal 18F-FDG-PET/CT. CONCLUSIÓN: El impacto de este artículo es ayudar a minimizar las malas interpretaciones, protocolizar descripciones de los estudios y disminuir diagnósticos erróneos que pueden afectar al manejo adecuado de los pacientes con consecuencias indeseables.
Palabras clave: Inmunoterapia, efectos secundarios autoinmunes, imagen multimodal 18FDG-PET/CT.
Abstract: OBJECTIVE: The proper interpretation of 18F FDG-PET/CT morphological and the metabolic studies requires accurate knowledge of the normal and the abnormal distribution of the radiopharmaceutical absorption. Added to this is the fact that we must be vigilant in interpreting the physiological and the pathophysiological variants resulting from procedures in the management of the cancer patients that can modify the pre-established imaging patterns. Understanding the possible causes of the misinterpretation increases confidence in the image interpretation, reduces the number of unnecessary follow-up studies, optimizes treatment, and the most importantly, reduces the radiation exposure to the patient. In recent years, the immunotherapy, specifically immune checkpoint inhibitor drugs, have given us an important advance in the cancer treatment; however, their use is not exempt from unwanted reactions called autoimmune side effects, also known as unwanted reactions called the autoimmune side effects METHOD: These side effects have also led us to the fact that 18F FDG-PET/CT images are presenting new imaging patterns of response to the treatment. We believe that posterior immunotherapy patients represent a radical change in the interpretation of an 18F FDG-PET/CT study. In this article we review the current concepts on the immunotherapy and its unwanted reactions called autoimmune side effects patterns with special emphasis on the multimodal 18F-FDG-PET/CT imaging. CONCLUSION: The impact of this article is to help minimize misinterpretations, standardize study descriptions, and reduce misdiagnoses that can affect proper the patient management with undesirable consequences.
Keywords: Immunotherapy, autoimmune side effects, multimodal 18F-FDG-PET/CT imaging.
El manejo terapéutico de los pacientes oncológicos consiste en cirugía, quimioterapia citotóxica y citostática y radioterapia. En otras palabras, al tumor primario lo cortamos, lo envenenamos y luego lo quemamos. Desde hace varios años nuevas técnicas de tratamiento como la inmunoterapia representan una alternativa y un enfoque diferente que ha proporcionado una forma de manejo de la enfermedad y ha permitido empezar a utilizar términos como cronificación o curación de la neoplasia, incluso en pacientes metastásicos. Sin embargo, estos tratamientos también se asocian con un espectro único de efectos secundarios denominados efectos adversos relacionados con el sistema inmunitario (irAE).
Este escenario nos lleva a definir que el acceso, disponibilidad e interpretación de las imágenes médicas en el paciente oncológico, se vuelve indispensable para la valoración de estos métodos, garantizando decisiones del manejo más precisas y resultados óptimos.
Es bien sabido que los sistemas de imágenes multimodalidad como la tomografía por emisión de positrones (PET)/tomografía computarizada (TC) puede reflejar la información biológica del cuerpo vivo de forma no invasiva y dinámica. Además de ser la más precisa en la valoración de muchos de los tipos de cáncer, sin importar en qué fase de la enfermedad esté el paciente (Cuadro 1).
Uno de los desafíos en el momento de la interpretación de las imágenes PET/CT utilizando su marcador 18 fluordeoxiglucosa (18F FDG) para la valoración del metabolismo de la glucosa, es la diferenciación correcta de la absorción anormal que es potencialmente patológica, de la absorción fisiológica o cambios metabólicos productos de otros factores. Un ejemplo de esto, son los de pacientes que toman metformina, ya que ha demostrado que este fármaco produce un retraso de la absorción intestinal de la glucosa, creando una mayor concentración del 18F FDG en la región intestinal disminuyendo la sensibilidad y especificidad de los estudios PET (1).
Por lo tanto, debemos estar conscientes de que cualquier cambio o modificación de conductas en relación al manejo terapéutico o no de un paciente oncológico, pueden alterar los patrones de interpretación de la imagen.
En esta revisión, nos centramos en mostrar una visión general sobre la inmunoterapia y sus patrones imagenológicos con especial énfasis en los cambios productos de los irAE y las imágenes 18F-FDG-PET/CT.
INMUNOTERAPIA QUE TENEMOS.
Epidemiologia, historia y mecanismo
La inmunoterapia no es quimioterapia. La Sociedad Americana de Oncología Clínica la define como un tipo de tratamiento contra el cáncer que estimula las defensas naturales del cuerpo para combatirlo. Utiliza sustancias producidas por el organismo o en un laboratorio para mejorar el funcionamiento de su sistema inmunológico y destruir las células cancerosas (4) Cuadro 2.
Sus inicios nos llevan a los años 1890, cuando el Dr. William Coley, un cirujano estadounidense del Hospital de Cáncer de Nueva York, ahora llamado Memorial Sloan Kettering, inyectó organismos estreptocócicos en un paciente con cáncer para causar erisipelas y estimular el sistema inmunitario. Así consiguió la regresión espontánea de múltiples tumores en más del 50 %. Coley hoy en día es considerado el “padre de la inmunoterapia” (6,7).
En estos últimos años debido a los avances que hemos tenido sobre inmunología, genética y cáncer, la inmunoterapia ha tomado un papel fundamental en el manejo de estos pacientes. En los EE. UU los pacientes candidatos a ser tratados con estas drogas aumentaron desde 1,5 % 2011 hasta el 43,6 % en el 2018 (8).
Esto se explica ya que la Food and Drug Administration (FDA) comenzó a aprobar estos tratamientos a partir de 2011. El primero fue ipilimumab (anti-CTLA-4). indicado para los melanomas metastásicos
Recientemente, la inmunoterapia basada en anticuerpos que inhiben a los puntos de control inmunitarios (ICI) también llamados check-point representa un importante paso adelante en la práctica clínica de los oncólogos médicos. Sin embargo, no es solo la eficacia de los ICI lo que los distingue de la quimioterapia (9).
INDICACIÓN
El manejo de los pacientes oncológicos basado en inmunoterapia, han comprobado ser efectivas contra el melanoma, cáncer de pulmón de células pequeñas y no pequeñas, cáncer de cabeza y cuello, cáncer de mama triple negativo, hepatocarcinoma, cáncer renal de células claras, cáncer de vejiga, tumores digestivos, entre otros (10).
MECANISMOS DE ACCIÓN
La inmunoterapia se refiere a una variedad de terapias que incluye cualquier tratamiento que modula la respuesta inmune. Se ha descrito que las respuestas a la inmunoterapia son más retrasadas con una disminución más lenta de la carga tumoral total, pero con una respuesta duradera(11,12). Aunque los ICI solo funcionan en un subgrupo o una minoría de pacientes, pueden inducir respuestas duraderas en el 10 %-20 % de los pacientes tratados, incluso después de la interrupción del tratamiento, proporcionando un beneficio para la supervivencia(13,14).
Hay que tener en cuenta que la ICI interviene en el equilibrio del sistema inmunitario lo cual puede conducir a una pérdida de auto tolerancia y a una activación inmune excesiva de los tejidos normales, lo que resulta en irAE (15).
EVENTOS ADVERSOS RELACIONADOS CON LA INMUNIDAD. (IRAE)
Aunque generalmente son toxicidades leves manejables, se estima que la incidencia de estos eventos adversos inmunomediados oscila entre el 30 % y el 40 % (16).
Otros autores han relacionado estos eventos con el tipo de agente utilizado para la terapia, en el caso de los agentes anti-CTLA4 las tasas reportadas son de hasta un 80 % en comparación con anti-PD1 (27 %) y anti-PDL1 (17 %), alcanzando hasta el 55 % con inmunoterapia combinada (17,18). Lo que lleva a nuevos perfiles de toxicidad que requieren un manejo diferente a los efectos tóxicos de las quimioterapias (19,20).
NO SE ENTIENDE CLARAMENTE LA FISIOPATOLOGÍA PRECISA QUE SUBYACE A LOS IRAE (21).
Se presume que el mecanismo de los irAE son efectos autoinmunes resultantes de una estimulación mal dirigida del sistema inmunitario durante la inmunoterapia (22).
Generalmente los irAE son condiciones autoinmunes o pseudo-autoinmunes que pueden afectar a cualquier órgano del cuerpo tras la administración de ICI.
Comúnmente la piel, el colon (tracto gastrointestinal), el hígado, los pulmones, glándulas endocrinas y las articulaciones. Otros sitios se ven afectados con menos frecuencia, como el sistema nervioso central, el sistema cardiovascular, el sistema hematológico, los riñones y el sistema ocular. Algunos de estos efectos tóxicos en órganos se diagnostican clínicamente y no requieren más análisis por imágenes (23,24).
INICIO Y DURACIÓN DE LOS IRAE.
Numerosos estudios relacionan estos efectos adversos con una mejor respuesta al tratamiento con inhibidores de ICI. Estos podrían ser un reflejo de la respuesta antitumoral y también suponer un beneficio en la supervivencia de los pacientes que las experimentan ( 25). Lo que sugiere que un inicio temprano de eventos adversos inmunorelacionados podría ser predictivo de una mejor respuesta al tratamiento con los inhibidores de check-points (26).
Los irAE comúnmente se manifiestan dentro de los primeros 3 meses de administración de la mayoría de los medicamentos, pero a veces mucho después de que se suspende la inmunoterapia.
Se ha determinado una tendencia a que un patrón temporal de efectos tóxicos se manifieste después del inicio de la terapia (21) (Cuadro 3).
Con los medicamentos anti-CTLA-4, tales manifestaciones tienden a ocurrir un poco antes que con otros IC. A pesar de tal patrón, varios autores afirman que los irAE pueden ocurrir en cualquier momento durante la terapia ICI (27,28).
En los casos de respuesta tumoral, los pacientes que están expuestos al tratamiento con ICI durante un período más prolongado, podrían aumentar la tasa de efectos tóxicos irAE con el tiempo (28,29).
MEDICAMENTOS DISPONIBLES
Actualmente existen tres fármacos aprobados por la FDA
Algunas de ellas son ipilimumab, que bloquea CTLA-4; pembrolizumab que bloquea PD-1. O, Atezolizumab, bloquea PD-L1. Sin embargo, al ser un campo relativamente nuevo, otros fármacos se van produciendo, van pasando las diferentes fases clínicas y llegan a ser aprobados, los cuales se resumen en el Cuadro 4.
Además, ya se están aprobando la combinación de estos anticuerpos inmunomoduladores que están dando buenos resultados clínicos (Cuadro 5).
Los efectos adversos de estos componentes por separado ya se están describiendo. Se ha observado que el ipilimumab, sus efectos parecen estar relacionados con dosis-dependientes, pudiendo aparecer de forma súbita o a largo plazo. Uno de los efectos descritos es la elevación de enzimas hepáticas. En referencia a los efectos adversos del nivolumab parece ser que son menos frecuentes que los observados con el anti-CTLA4. Estos efectos adversos no deseados son importantes a tener en cuenta una vez se empieza el tratamiento. Finalmente, es necesario conocer y anticiparse al conjunto de efectos secundarios asociados al uso de inhibidores de checkpoints, de forma que se afronte desde una perspectiva multidisciplinar para lograr un trato ideal y lo más personalizado para cada paciente (31).
IMÁGENES DE EVENTOS ADVERSOS RELACIONADOS CON EL SISTEMA INMUNOLÓGICO
irAE: el papel de la imagen 18F-FDG PET/TC
Las manifestaciones radiológicas de los irAE se pueden encontrar en hasta el 17 % de los pacientes que reciben inmunoterapia, y esto puede preceder a las manifestaciones clínicas (32,33).
La 18F-FDG PET está evolucionando con varios puntos fuertes en la evaluación de la respuesta a la inmunoterapia tumoral. Se ha descubierto que mejoran el rendimiento discriminatorio y pronóstico (34).
Esto no lleva a que la 18F-FDG PET además de sus indicaciones clínicas basadas en la caracterización del microambiente inmune tumoral, 18F-FDG PET puede determinar otras características o parámetros que permiten obtener mayor información fundamental en el manejo del paciente oncológico (35) Cuadro 6.
Recientemente, el informe del simposio sobre inmunoterapia de la Asociación Europea de Medicina Nuclear indicó que se deben informar los hallazgos incidentales relacionados con irAE. Aunque los irAE pueden no estar necesariamente asociados con síntomas clínicos, los médicos deben ser conscientes de su presencia y garantizar un seguimiento clínico que, sin embargo, podría conducir a una intervención clínica (35).
En la terapia celular CAR-T, sin embargo, hay otro conjunto de efectos adversos bastante inmediatos, como el síndrome de liberación de citoquinas, las toxicidades neurológicas relacionadas con las células CAR-T y la aplasia de células B, que no son directamente detectables usando 18F-FDG-PET (36,37). Además, los eventos adversos relacionados con las células CAR-T ocurren incluso antes que los irAE, incluso horas y días después de la primera solicitud imagenológica.
En la terapia celular CAR-T, sin embargo, hay otro conjunto de efectos adversos bastante inmediatos, como el síndrome de liberación de citoquinas, las toxicidades neurológicas relacionadas con las células CAR-T y la aplasia de células B, que no son directamente detectables usando 18F-FDG-PET (36,37). Además, los eventos adversos relacionados con las células CAR-T ocurren incluso antes que los irAE, incluso horas y días después de la primera solicitud imagenológica.
CABEZA Y CUELLO
Los irAE más frecuentes son la tiroiditis e hipofisitis. Estos efectos tóxicos endocrinos son quizás los irAE más difíciles, poco diagnosticados o mal diagnosticados asociados con la terapia ICI (37). Esto podría explicarse en parte porque son en su mayoría subclínicos u oligosintomáticos y también porque no están claramente clasificados en los Criterios Terminológicos Comunes para Eventos Adversos, como referencia estándar para los médicos. Sin embargo, es fácil representar estos irAE con la PET porque el proceso de inflamación de la glándula afectada aumenta la captación del FDG (24) (Cuadro 7).

Figura 2
Cabeza y cuello.
TÓRAX
Aunque es relativamente raro, la irAE más común en la región torácica es la inflamación pulmonar (neumonitis). A diferencia de otros irAE, es más frecuente con los medicamentos anti-PD-1 y con la terapia combinada (42). La neumonitis es muy variable en su inicio y gravedad: radioterapia pulmonar previa y la fibrosis son factores de riesgo para la neumonitis anti-PD-1 (27).
Los informes iniciales de neumonitis relacionadas con los inhibidores del punto de control inmunológico han descrito un espectro de manifestaciones radiológicas con diferentes patrones morfológicos de neumonías intersticiales (43,44).
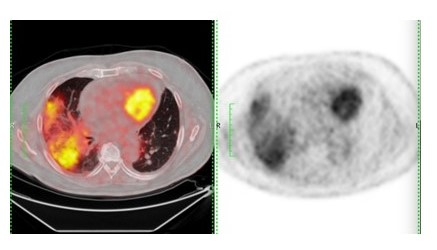
Figura 3.
Tórax
En el tórax también se pueden observar linfadenopatía y granulomatosis similares a los sarcoides también se reconocen como un irAE, más comúnmente observado en los ganglios linfáticos mediastínicos e hiliares, El tiempo medio desde el inicio de la terapia fue de 3,2 meses (rango, de 0,2 a 9,1 meses) en pacientes con melanoma tratados con ipilimumab.. También se pueden observar cambios parenquimatosos pulmonares con engrosamiento nodular de los haces peribroncovasculares y el tabique interlobular. El muestreo histológico de estos casos reveló una inflamación granulomatosa en una distribución interlobular, peribronquiolar y subpleural que se asemeja a la sarcoidosis. Un informe reciente demostró que esta entidad también puede ocurrir como un hallazgo aislado en el pulmón, con un foco de consolidación pulmonar en ausencia de linfadenopatía o síntomas. Estos hallazgos se resuelven después de que se retengan los inhibidores del punto de control inmunitario (46,47).
ABDOMEN
La colitis durante la terapia con inhibidores de puntos de control inmunológico es uno de los irAE específicos de órganos más comunes.
Estos están más fuertemente asociados con la terapia combinada (hasta el 50 %) o la terapia anti-CTLA-4 sola (hasta el 22 %) (27).
En pacientes tratados con ipilimumab, la colitis generalmente se desarrolla de 6 a 7 semanas después del inicio del tratamiento y se resuelve en un plazo de 6-8 semanas (46).
A pesar de que los pacientes a menudo no lo informan, la colitis es la razón principal por la que los pacientes sometidos a tratamiento con ICI llegan al departamento de emergencias (45).
Los casos graves probablemente requerirán la interrupción de la terapia con ICI, y las causas infecciosas (específicamente Clostridium difficile) deben descartarse con pruebas de heces(27,42).

Figura 4.
Abdomen.
HEPATITIS
Los efectos tóxicos hepáticos causados por la terapia ICI son relativamente comunes. El tiempo entre el inicio de la terapia y la hepatitis es de 5 semanas (rango, de 1 a 49 semanas) en pacientes tratados con monoterapia con inhibidor de PD-1/PD-L1 o CTLA-4 (50). La hepatitis tiene un espectro de manifestaciones. En el examen histológico, se observan dos patrones de lesión: un patrón de hepatitis aguda con lesiones predominantes en los hepatocitos y un patrón biliar con lesiones predominantes en los conductos biliares (51).
PANCREATITIS.
La pancreatitis también se puede ver en respuesta a la terapia con ICI, aunque con baja incidencia.
DISFUNCIÓN SUPRARRENAL.
La disfunción suprarrenal primaria relacionada con la terapia ICI es rara y puede manifestarse como insuficiencia suprarrenal primaria relacionada con la inflamación (adrenalitis). También podría poner en peligro la vida debido a la falta de cortisol (21).
EFECTOS MUSCULOESQUELÉTICOS Y REUMATOLÓGICOS
Los síntomas musculoesqueléticos son relativamente comunes durante la terapia con ICI. Los procesos musculoesqueléticos inflamatorios son irAE inusuales. También pueden ocurrir juntos en síndromes reumatológicos específicos (incluidas enfermedades del tejido conectivo), como la artritis reumatoide, la polimialgia reumática, el lupus eritematoso y el síndrome de Sjögren (54,55).
OTROS IRAE ESPECÍFICOS DE ÓRGANOS Y NECESIDADES CLÍNICAS NO SATISFECHAS
Se han descrito otros irAE específicos de órganos en pacientes tratados con inhibidores de puntos de control inmunológico, incluyendo encefalitis, mielitis, artritis, nefritis, dermatológicos, sarcoidosis o reacción similar a un sarcoide y miocarditis, por nombrar algunos.
El concepto y el conocimiento de los irAE siguen evolucionando a medida que experimentamos más casos en el entorno clínico. Muchos de los irAE requieren un enfoque multidisciplinario basado en hallazgos clínicos, imagenológico y a veces, histológicos para un diagnóstico y un manejo precisos. desarrollar métodos de diagnóstico precisos y establecer estrategias óptimas de gestión y monitoreo para tipos específicos de irAE. Los radiólogos están en primera línea para la detección, el diagnóstico y el monitoreo de muchos de estos nuevos irAE y pueden hacer contribuciones sustanciales como miembros clave de la atención multidisciplinaria del cáncer en la era de la inmuno oncología.
En resumen, solo hay una pequeña cantidad de literatura que describe toxicidades tardías diferentes de las irAE hasta ahora. Por lo tanto, se necesita más experiencia clínica y, en particular, literatura que evalúe el uso de imágenes de PET en la terapia celular CAR-T (56,
Concluimos en: una comprensión profunda de los mecanismos subyacentes de la inmunoterapia contra el cáncer es un desafío en la práctica clínica diaria que necesita un entrenamiento específico para poder ampliar los beneficios del tratamiento de ICI. Queda establecido que identificar los irAE, bajo la guía de las imágenes moleculares 18F-FDG PET/TC, complementa y define paradigma que pueden definir decisiones clínicas.
Por lo tanto, no solo los enfoques de diagnóstico serán prioritarios en la interpretación de las imágenes moleculares 18F-FDG PET/TC, estas deben desarrollarse con un enfoque amplio para ofrecer una valoración integral que oriente a identificar a los pacientes que podrían beneficiarse del tratamiento de ICI.
Podemos afirmar que, con la amplia disponibilidad de protocolos estandarizados, varios agentes de imagen asequibles y plataformas de análisis cuantitativos fáciles de usar con soporte de la inteligencia artificial, las imágenes 18F-FDG PET/TC desempeñarán un papel más importante en la era de la inmuno-oncología.
REFERENCIAS
1. Sancho Rodríguez L, Guillén Valderrama E, Pérez Pevida B, Escalada San Martín F, García GaB, Ribelles Segura M, et al. Estudio PET/CT con 18 F-FDG en pacientes con diabetes mellitus tipo 2: optimización de la pauta de metformina. Rev Esp Med Nucl Imagen Mol. 2015;34(Supl 1):S79.
2. Unterrainer M, Ruzicka M, Fabritius, MP, Mittlmeier K, Winkelmann M, Rübenthaler J, et al. PET/CT imaging for tumour response assessment to immunotherapy: Current status and future directions. Eur Radiol Exp. 2020; 4(1):63. https://doi.org/10.1186/s41747-020-00190-1
3. Kibrom BG, Rebaud L Cottereau A, Meignan M, Clerc J, Vercellino L, et al. 18F-FDG PET Maximum-Intensity Projections and Artificial Intelligence: A Win-Win Combination to Easily Measure Prognostic Biomarkers in DLBCL Patients. J Nucl Med. 2022;12:1925-1931.
4. ¿Que es la Inmunoterapia?. Disponible en: URL: https://www.cancer.net/es/desplazarse-por-atención-del-cáncer/cómo-se-trata-el-cáncer/inmunoterapia-y-vacunas/qué-es-la-inmunoterapia
5. ACS Reviewers/Subject Matter Experts. Disponible en: URL: www.cancer.org/cancer/acs-medical-content-and-news-staff.html
6. McCarthy EF. The toxins of William B. Coley and the treatment of bone and soft-tissue sarcomas. Iowa Orthop J. 2006;26:154-158.
7. Hoption Cann SA, van Netten JP, van Netten C. Dr William Coley and tumour regression: A place in history or in the future. Postgrad Med J. 2003;79(938):672-680.
8. Haslam A, Prasad V. Estimation of the percentage of US patients with cancer who are eligible for and respond to checkpoint inhibitor immunotherapy drugs. JAMA Netw Open 2019;2(5): e192535.
9. Pérez Gago M, Saavedra SG, de la Cruz-Merino. Advances in the immunobiological therapies for advanced melanoma. Actas Dermosifiliogr. 2017;108(8):721-728
10. Reyes SJ, González KB, Rodríguez C, Navarrete-Muñoz C, Salazar AP, Villagra A, et al. Actualización general de inmunoterapia en cáncer. Rev. méd. Chile. 2020;148(7): 970-982.
11. Wolchok JD, Hoos A, O'Day S, Weber JS, Hamid O, Lebbé C, et al. Guidelines for the evaluation of immune therapy activity in solid tumors: Immune-related response criteria. Clin Cancer Res. 2009;15:7412-7420.
12. Larkin J, Minor D, D'Angelo S, Neyns B, Smylie M, Miller WJr, et al. Overall survival in patients with advanced melanoma who received nivolumab versus investigator’s choice chemotherapy in CheckMate 037: A randomized, controlled, open-label phase III trial. J Clin Oncol. 2018;36:383-390.
13. Robert C, Ribas A, Hamid O, Daud A, Wolchok JD Joshuaet AM, et al. Durable complete response after discontinuation of pembrolizumab in patients with metastatic melanoma. J Clin Oncol . 2018;36:1668-1674.
14. Horn L, Spigel DR, Vokes EE, Holgado E, Ready N, Steins M, et al. Nivolumab versus docetaxel in previously treated patients with advanced non-small-cell lung cancer: two-year outcomes from two randomized, open-label, phase III trials (CheckMate 017 and CheckMate 057). J Clin Oncol. 2017;35:3924-3933.
15. Morad G, Helmink BA, Sharma P, Wargo JA. Hallmarks of response, resistance, and toxicity to immune checkpoint blockade. Cell. 2021;184:5309-5337. doi: 10.1016/j.cell.2021.09.020
16. Puzanov I, Diab A, Abdallah K, Bingham CO, Brogdon C, Dadu R, et al. Managing toxicities associated with immune checkpoint inhibitors: Consensus recommendations from the Society for Immunotherapy of Cancer (SITC) Toxicity Management Working Group. J Immunother Cancer. 2017;5(1):95.
17. Martins F, Sofiya L, Sykiotis GP, Lamine F, Maillard M, Fraga M, et al. Adverse effects of immune-checkpoint inhibitors: Epidemiology, management and surveillance. Nat Rev Clin Oncol. 2019;16:563-580.
18. Sun X, Roudi R, Dai T, Chen S, Fan B, Li H, et al. Immune-related adverse events associated with programmed cell death protein-1 and programmed cell death ligand 1 inhibitors for non-small cell lung cancer: A PRISMA systematic review and meta-analysis. BMC Cancer. 2019: 19:558.
19. Cousin S, Italiano A. Molecular pathways: Immune checkpoint antibodies and their toxicities. Clin Cancer Res. 2016; 22:4550-4555.
20. Nishijima TF, Shachar SS, Nyrop KA, Muss HB. Safety and tolerability of PD-1/PD-L1 inhibitors compared with chemotherapy in patients with advanced cancer: A meta-analysis. Oncologist. 2017;22:470-479.
21. Larissa BC, Queiroz MA, Barbosa FG, Nunes R, Zaniboni, Mazo RM, et al. RadioGraphics 2021;41(1):120-143.
22. Baxi S, Yang A, Gennarelli RL, Khan N, Wang Z, Boyce L, et al. Immune-related adverse events for anti-PD-1 and anti-PD-L1 drugs: Systematic review and meta-analysis. BMJ. 2018;360:k793.
23. Naidoo J, Page DB, Li BT, Connell L, Schindler K, Lacouture M, et al. Toxicities of the anti-PD-1 and anti-PD-L1 immune checkpoint antibodies. Ann Oncol. 2015;26(12):2375-2391. [Erratum in Ann Oncol. 2016;27(7):1362.]
24. Kottschade LA. Incidence and management of immune-related adverse events in patients undergoing treatment with immune checkpoint inhibitors. Curr Oncol Rep. 2018;20(3):24.
25. Teraoka S, Fujimoto D, Morimoto T, Kawachi H, Ito M, Sato Y, et al. Early immune-related adverse events and association with outcome in advanced non-small cell lung cancer patients treated with Nivolumab: A prospective cohort study. J Thorac Oncol. 2017;(12):1798-805.
26. Ricciuti B, Genova C, De Giglio A, Bassanelli M, Dal Bello MG, Metro G, et al. Impact of immune-related adverse events on survival in patients with advanced non-small cell lung cancer treated with nivolumab: Long-term outcomes from a multi-institutional analysis. J Cancer Res Clin Oncol. 2019;145 (2):479-485.
27. Chan KK, Bass AR. Autoimmune complications of immunotherapy: Pathophysiology and management. BMJ. 2020;369:m736.
28. Postow MA, Sidlow R, Hellmann MD. Immune-related adverse events associated with immune checkpoint blockade. N Engl J Med. 2018;378(2):158-168.
29. June CH, Warshauer JT, Bluestone JA. Is autoimmunity the Achilles’ heel of cancer immunotherapy? Nat Med. 2017;23(5):540-547. [Erratum in Nat Med. 2017;23(8):1004.]
30. [No Author´s list]. La inmunoterapia en algunos tipos de tumores es tratamiento de primera elección. Disponible en :URL: https://seom.org/seomcms/images/stories/recursos/NdP_HITOS_EN_InmunoOncologia_2018.pdf
31. Bartoló A. Doble toxicidad en paciente con melanoma tratada con nivolumab- ipilimumab Inmunología. 2022; 41(3):53-54.
32. Carter BW, Halpenny DF, Ginsberg MS, Papadimitrakopoulou VA, de Groot PM. Immunotherapy in non-small cell lung cancer treatment: Current status and the role of imaging. J Thorac Imaging. 2017;32:300-312.
33. Wang GX, Kurra V, Gainor JF, Sullivan R, Flaherty K, Lee S, et al. Immune checkpoint inhibitor cancer therapy: Spectrum of imaging findings. Radiographics. 2017;37:2132-2144.
34. Ito K, Teng R, Schöder H L Humm JL, Ni A, Michaud L, o Nakajima R, et al. 18F-FDG PET/CT for monitoring of Ipilimumab therapy in patients with metastatic melanoma. J Nucl Med. 2019;60(3):335-341.
35. Neelapu SS, Tummala S, Kebriaei P, Wierda W, Gutierrez C, Locke F, et al. Chimeric antigen receptor T-cell therapy assessment and management of toxicities. Nat Rev Clin Oncol. 2018;15:47-62.
36. Wang J, Hu Y, Yang S, Wei G, Zhao X, Wu W, et al. Role of fluorodeoxyglucose positron emission tomography/computed tomography in predicting the adverse effects of chimeric antigen receptor t cell therapy in patients with non-Hodgkin lymphoma. Biol Blood Marrow Transplant. 2019;25:1092-1098.
37. Sznol M, Postow MA, Davies MJ, Pavlick A, Plimack E, Shaheen M, et al. Endocrine-related adverse events associated with immune checkpoint blockade and expert insights on their management. Cancer Treat Rev. 2017;58:70-76.
38. Karantanis D, Bogsrud TV, Wiseman GA, Mullan B, Subramaniam R, Nathan M, et al. Clinical significance of diffusely increased 18FDG uptake in the thyroid gland. J Nucl Med. 2007;48(6):896-901.
39. Eshghi N, Garland LL, Nia E, Betancourt R, Krupinski E, Kuo PH. 18F-FDG PET/CT can predict development of thyroiditis due to immunotherapy for lung cancer. J Med Technol. 2018;46(3):260-264.
40. Sosa A, Lopez Cadena E, Simon Olive C, Karachaliou N, Rosell R. Clinical assessment of immune-related adverse events. Ther Adv Med Oncol. 2018;1758835918764628.
41. Kottschade LA. Incidence and management of immune-related adverse events in patients undergoing treatment with immune checkpoint inhibitors. Curr Oncol Rep. 2018;20(3):24.
42. Nishino M, Sholl LM, Hodi FS, Hatabu H, Ramaiya NH. Anti-PD-1-related pneumonitis during cancer immunotherapy. N Engl J Med. 2015;373(3):288-290.
43. Nishino M, Chambers ES, Chong CR, Ramaiya N, Gray S, l Marcoux J, et al. Anti-PD-1 inhibitor-related pneumonitis in non-small cell lung cancer. Cancer Immunol Res. 2016;4(4):289-293.
44. Cooksley T, Gupta A, Al-Sayed T, Lorigan P. Emergency presentations in patients treated with immune checkpoint inhibitors. Eur J Cancer. 2020;130:193-197.
45. Tirumani SH, Ramaiya NH, Keraliya A, Bailey N, Ott P, Hodi S, et al. Radiographic profiling of immune-related adverse events in advanced melanoma patients treated with ipilimumab. Cancer Immunol Res. 2015;3(10):1185-1192.
46. Berthod G, Lazor R, Letovanec I, Romano E, Noirez L, Mazza Stalder JM, et al. Pulmonary sarcoid-like granulomatosis induced by ipilimumab. J Clin Oncol. 2012;30(17):e156-e159.
47. Khunger M, Rakshit S, Pasupuleti V, Hernandez A, Mazzone P, Stevenson J, et al. Incidence of pneumonitis with use of programmed death 1 and programmed death-ligand 1 inhibitors in non-small cell lung cancer: A systematic review and meta-analysis of trials. Chest. 2017;152(2):271-281.
48. Kwak JJ, Tirumani SH, Van den Abbeele AD, Koo PJ, Jacene HA. Cancer immunotherapy: Imaging assessment of novel treatment response patterns and immune-related adverse events. RadioGraphics. 2015;35(2):424-437.
49. De Martin E, Michot JM, Papouin B, Champiat S, Mateus C, Lambotte O, et al. Characterization of liver injury induced by cancer immunotherapy using immune checkpoint inhibitors. J Hepatol. 2018;68(6):1181-1190.
50. Kim KW, Ramaiya NH, Krajewski KM, Jagannathan J, Tirumani S, h Srivastava A, et al. Ipilimumab associated hepatitis: Imaging and clinicopathologic findings. Invest New Drugs. 2013;31(4):1071-1077.
51. Okada H, Weller M, Huang R, Finocchiaro G, Gilbert M, Wick W, et al. Immunotherapy response assessment in neuro-oncology: a report of the RANO working group. Lancet Oncol. 2015.16(15):e534-e542.
52. Naidoo J, Wang X, Woo KM, Iyriboz T, Halpenny D, Cunningham J, et al. Pneumonitis in patients treated with anti-programmed death-1/programmed death ligand 1 therapy. J Clin Oncol. 2017;35(7):709-717.
53. Cappelli LC, Gutierrez AK, Bingham CO 3rd, Shah AA. Rheumatic and musculoskeletal immune-related adverse events due to immune checkpoint inhibitors: A systematic review of the literature. Arthritis Care Res (Hoboken). 2017;69(11):1751-1763.
54 Le Burel S, Champiat S, Mateus C, Marabelle A, Michot J, Robert C, et al. Prevalence of immune-related systemic adverse events in patients treated with anti-programmed cell death 1/anti-programmed cell death-ligand 1 agents: A single-centre pharmacovigilance database analysis. Eur J Cancer. 2017;82:34-44.
55. Hu Y, Wang J, Pu C, Zhao K, Cui Q, Wei G, et al. Delayed terminal ileal perforation in a relapsed/refractory B-cell lymphoma patient with rapid remission following chimeric antigen receptor T-cell therapy. Cancer Res Treat. 2018;50:1462-1466.
56. Wang Y, Zhang W-y, Han Q-w.,Liu L,Dai H, Gou Y, et al. Effective response and delayed toxicities of refractory advanced diffuse large B-cell lymphoma treated by CD20-directed chimeric antigen receptor-modified T cells. Clin Immunol. 2014; 155:160-175.
Notas de autor
luiscolmenter@hotmail.com















