MACROCITOSIS ERITROIDE: PREDICTOR DE EFICACIA EN PACIENTES CON ADENOCARCINOMA DE PULMÓN TRATADOS CON PEMETREXED
MACROCITOSIS ERITROIDE: PREDICTOR DE EFICACIA EN PACIENTES CON ADENOCARCINOMA DE PULMÓN TRATADOS CON PEMETREXED
Revista Venezolana de Oncología, vol. 37, núm. 1, pp. 59-70, 2025
Sociedad Venezolana de Oncología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 13 Octubre 2024
Aprobación: 12 Noviembre 2024
Resumen: Pemetrexed es una droga antifolato, la actividad antitumoral lo convierten en opción de tratamiento en ADC de pulmón, la presencia de polimorfismos de MTHFR genera baja actividad enzimática, afectando la eritropoyesis provocando aumento del VCM eritroide, identificando un subgrupo de pacientes sensibles a la actividad de Pemetrexed. Evaluamos macrocitosis eritroide como predictor de eficacia en pacientes con adenocarcinoma de pulmón tratados con Pemetrexed que acudieron a nuestra unidad desde enero 2011 a diciembre 2021. MÉTODO: Estudio descriptivo, retrospectivo, transversal. Población de 136 pacientes con diagnóstico de adenocarcinoma de pulmón que hubiesen recibido Pemetrexed. Muestra de 54 pacientes. Datos se vaciaron en Excel, presentados en cuadros y figuras, correlacionándose variables. RESULTADOS: 68,51 % fueron sexo femenino, edad promedio 67±10,69 años, 72,2 % estadio IV, 81,48 % recibieron Pemetrexed primera línea, VCM eritroide postratamiento promedió 98,60 fl. Se dividieron dos grupos según aumento de VCM, mayor 5 fl representó 70,37 %, VCM máximo alcanzó a 2 y 5 meses, el 86,4 % alcanzaron respuesta parcial, sobrevida global fue de 2 años 2 meses, libre de progresión 1 año y 7 meses. Siendo la correlación de estas variables de 0,80. Pruebas de sobrevida libre de progresión para VCM >5fl y VCM <5fl no fueron significativamente diferente (P-valor=0,13). CONCLUSIÓN: Se demostró 95 % de tasa de control de enfermedad en aquellos pacientes cuyo incremento en el volumen eritroide fue mayor posterior al inicio de la terapia; demostrando así su relación con una mayor eficacia.
Palabras clave: Macrocitosis eritroide, Pemetrexed, Adenocarcinoma, pulmón.
Abstract: The Pemetrexed is an antifolate drug, and its antitumor activity makes it a treatment option for the lung adenocarcinoma- The presence of MTHFR polymorphisms results in low enzymatic activity, affecting the erythropoiesis and causing an increase in erythroid MCV, identifying a subgroup of patients sensitive to pemetrexed activity. We evaluated the erythroid macrocytosis as a predictor of efficacy in patients with lung adenocarcinoma treated with pemetrexed who attended at our medical oncology unit from January 2011 to December 2021. METHOD: Descriptive, retrospective, cross- sectional study. The population consisted of 136 patients diagnosed with lung adenocarcinoma who had received pemetrexed. Sample consisted of 54 patients. The data were entered into Excel, presented in tables and graphs, correlating variables. RESULTS: 68.51 % were female, average age 67±10.69 years, 72.2 % stage IV, 81.48 % received first-line pemetrexed, post-treatment erythroid MCV averaged 98.60 fl. Two groups were divided according to MCV increase, greater than 5 fl represented the 70.37 %, maximum MCV was reached at 2 and 5 months, the 86.4 % achieved partial response, the overal survival was 2 years 2 month progression free survival 1 year 7 months. The correlation of these variables was 0.80. The progression free survivsl tests for MCV >5fl and MCV <5fl were not significantly different (P-value=0.13). CONCLUSION: A 95 % disease control rate was demonstrated in those patients whose increase in erythroid volume was greater after the start of therapy, demonstrating its relationship with greater efficacy.
Keywords: Erythroid macrocytosis, Pemetrexed, adenocarcinoma.lung.
INTRODUCCIÓN
Durante los últimos años el cáncer de pulmón se considera como la principal causa de muerte por cáncer, el 85 % de ellos son clasificados como cáncer de pulmón de células no pequeñas (CPNC) dividiéndose en 3 tipos histológicos: adenocarcinoma (ADC), carcinoma de células escamosas y carcinoma de células grandes(1). La mayoría de los pacientes con CPNC se encuentran en una etapa avanzada de la enfermedad en el momento del diagnóstico (3). El tratamiento incluye quimioterapia, radioterapia o cirugía solo o combinados; recientemente se dispone de terapias dirigidas a mutaciones específica y el uso de inhibidores de punto de control que han mejorado considerablemente la respuesta en estos pacientes (2).
Aunque los inhibidores de puntos de control inmunológico y los agentes dirigidos han demostrado una eficacia alentadora en el tratamiento, la quimioterapia con dos fármacos basada en platino es una parte integral del tratamiento estándar de primera línea para la mayoría de los pacientes con CPCN no escamoso avanzado (3,4). Dentro de los agentes quimioterapéuticos el Pemetrexed ha sido autorizado en pacientes con ADC como agente simple o en combinación con sales de platino con o sin Bevacizumab, como tratamiento de primera o segunda línea e incluso en mantenimiento (4). Se ha demostrado que ¨Pemetrexed, solo o en combinación, es superior a otros regímenes de quimioterapia en pacientes con enfermedad no escamosa.
El estudio de fase III PARAMOUNT, demostró que en pacientes con CPCN no escamoso avanzado que tenían enfermedad estable después de la inducción con 4 ciclos de Pemetrexed más cisplatino de primera línea dejar Pemetrexed como terapia de mantenimiento continuada mejoraba la sobrevida libre de progresión (SLP) (4,4 vs. 2,8 meses) y sobrevida global (SG) (13,9 vs. 11,0 meses) en comparación con placebo (3). El Pemetrexed ofrece una alta eficacia y baja toxicidad, por lo que se considera aún un buen agente de tratamiento (3).
Pemetrexed es una droga antifolato con diferentes puntos de acción, inhibe tres enzimas en la vía metabólica del folato, esenciales para la replicación celular: la timidilato sintasa (TS), dihidrofolato reductasa y ribonucleótido de glicinamida formil transferasa. También se dirige a otras enzimas, incluidas la aminoimidazol carboxamida ribonucleotido formiltransferasa, una enzima dependiente de folato implicada en la síntesis de purinas.
Las toxicidades más comúnmente asociadas con Pemetrexed son neutropenia, leucopenia, anemia, fatiga, náuseas y vómitos. La actividad antitumoral y la toxicidad leve del Pemetrexed lo convierten en una opción atractiva para combinar con terapias dirigidas en pacientes con ADC de pulmón (4,5). Para el año 2002, se identificó una correlación entre la mayor toxicidad del Pemetrexed en pacientes con deficiencia de folato, expresada indirectamente como hiperhomocisteinemia. Desde entonces, se recomienda la administración concomitante de ácido fólico y vitamina B12 durante el tratamiento con Pemetrexed, lo que demuestra que reduce la toxicidad sin comprometer la eficacia. La metilentetrahidrofolato reductasa (MTHFR) es otra enzima involucrada en el metabolismo del folato y cataliza la síntesis de 1-5- metiltetrahidrofolato, esencial en la síntesis de ADN y el metabolismo de la homocisteína (3,4,5,6).
En la literatura se han informado polimorfismos de MTHFR, lo que resulta en una baja actividad enzimática potencialmente capaz de predecir diferencias de supervivencia en el CPCN tratado con Pemetrexed. Los pacientes sometidos a tratamiento con Pemetrexed reciben suplementos vitamínicos con ácido fólico y vitamina B12 según lo indicado, por lo que se puede excluir una deficiencia de folato. Sin embargo, la conversión de la forma sintética del ácido fólico es inhibida por la actividad del Pemetrexed sobre la DHFR. Por lo tanto, a pesar de la suplementación, Pemetrexed podría reducir la cantidad de sustrato disponible para la actividad de MTHFR, revelando una posible condición de baja actividad enzimática, debido al polimorfismo. Finalmente, en la médula ósea, esto podría afectar la eritropoyesis normal y provocar un aumento del VCM de los glóbulos rojos. Por lo que el bloqueo de la acción de las misma conlleva a eritropoyesis ineficaz, con asincronía en la maduración núcleo/citoplasma que se traduce en glóbulos rojos con un volumen corpuscular medio mayor al habitual. Es por este mecanismo que el Pemetrexed induce macrocitosis eritroide. Por tanto, el aumento del VCM eritroide puede ser una expresión indirecta de la presencia de polimorfismos de MTHFR, identificando un subgrupo de pacientes principalmente sensibles y expuestos a la actividad de Pemetrexed, en los que Pemetrexed podría ser más tóxico, pero también más eficaz. Es por eso que, en este estudio, se evaluó la macrocitosis eritroide como predictor de eficacia en pacientes con ADC tratados con Pemetrexed que acudieron a la unidad de oncología médica ARSUVE desde enero 2011 a diciembre 2021. Se incluyeron pacientes con edad mayor o igual a 18 años que recibieron tratamiento con Pemetrexed como agente simple o en combinación con sales de platino con o sin Bevacizumab, como terapia de primera, segunda, tercera línea y/o mantenimiento, que tuviesen hematología con reporte del VCM eritroide previo a iniciado el tratamiento y al menos un mes después de finalizada.
La correlación entre VCM y fármacos antimetabolitos se informó previamente en un grupo de pacientes tratados con capecitabina. Además, algunos datos sugieren que, en mujeres con cáncer de mama metastásico, la elevación del VCM mientras toman capecitabina podría representar un factor predictivo de respuesta.
En el año 2021, Li Jeanji y col., publican un estudio sobre eficacia y seguridad de la quimioterapia de mantenimiento con Pemetrexed para cáncer de pulmón de células no pequeñas avanzado, de 69 pacientes en los que se pudo evaluar la eficacia, la tasa de respuesta objetiva (TRO) fue del 46,4 % y la tasa de control de enfermedad fue del 98,6 %. La TRO no mostró diferencias significativas entre los pacientes que recibieron Pemetrexed como tratamiento de primera línea y aquellos que recibieron Pemetrexed como tratamiento de segunda línea o superior. La mediana del ciclo de tratamiento para todos los pacientes fue de 8. La mediana de supervivencia libre de progresión (SLP) fue de 9,5 meses y la mediana de sobrevida global (SG) fue de 30,5 meses (3).
Hang W y col., en el 2022, describieron a través de un estudio retrospectivo en China la importancia clínica del volumen corpuscular medio eritroide como indicador pronóstico en pacientes con cáncer de pulmón localmente avanzado y radioterapia, De todos los pacientes, 89 eran hombres (79,5%), 23 eran mujeres (20,5 %), 46 (41,1 %) eran mayores de 65 años y 66 (58,9 %) eran menores de 65 años. Setenta y cuatro pacientes tenían VCM <93,65 fL, 38 pacientes tenían VCM ≥93,65 fL y la mediana del período de seguimiento fue de 24 meses. Los pacientes con estadio alto y el VCM alto tuvieron una SG más baja (P<0,05). Concluyeron que, en el tratamiento clínico de pacientes con cáncer de pulmón localmente avanzado, VCM se puede utilizar para predecir aproximadamente su tiempo de supervivencia (6).
En el 2015, Buti y col., estudian el papel predictivo de la macrocitosis de eritrocitos durante el tratamiento con Pemetrexed en pacientes con cáncer de pulmón de células no pequeñas avanzado atendidos en diferentes hospitales de Italia, se evaluaron 191 pacientes: la mediana de edad 62 años, 60 % hombres, 61 % estado funcional 0, 91 % estadio IV, 88 % adenocarcinoma, 25 % nunca fumador, 62 % recibió Pemetrexed como primera línea. El VCM medio aumentó significativamente desde el nivel basal (89 fL) hasta durante el tratamiento (94 fL), con un VCM medio = 4 fL. La mediana del tiempo desde el inicio del tratamiento hasta el VCM máximo fue de 2,2 meses. La mediana de SLP fue de 7 meses, y la mediana de supervivencia fue de 17 y 10 meses [ P = 0,02], en pacientes con VCM > 5 fL (n = 80) y VCM ≤ 5 fL (n = 111), respectivamente. El análisis multivariado identificó edad ≥ 62 años, PS 0, histología de adenocarcinoma y VCM > 5 fL como predictores independientes de SLP más prolongada. Concluyen que Pemetrexed induce macrocitosis. VCM > 5 fl en tratamiento con Pemetrexed se correlacionó con una mejor SLP y SG (4).
MÉTODO
Se trata de un estudio descriptivo, retrospectivo, transversal. Se realizó la revisión de historias médicas de 136 pacientes que fueron evaluados en el servicio de oncología médica ARSUVE entre enero 2011 y diciembre 2021, con diagnóstico de ADC que hubiesen recibido como parte de su tratamiento Pemetrexed como agente simple o en combinación con sales de platino con o sin Bevacizumab, como terapia de primera, segunda, tercera línea y/o mantenimiento, que tuviesen hematología con reporte del VCM eritroide previo a iniciado el tratamiento y al menos un mes después de finalizada. Se excluyeron aquellos pacientes con variedad histológica distinta al ADC, que los estudios de hematología no reportaran el VCM eritroide. La muestra estuvo 54 pacientes cumplieron criterios de inclusión para ser considerados, constituyendo así la muestra del estudio.
De la revisión de la historia clínica se obtuvieron los datos epidemiológicos, histología, parámetros de laboratorio, evolución clínica para cálculos de sobrevivida. Se consideró valor de referencia del VCM eritroide según la organización mundial de la salud entre 80 -100 fl como valor normal, de acuerdo al aumento del VCM eritroide con respecto a su valor basal posterior al inicio de tratamiento se dividieron en 2 grupos, los que aumentaron su VCM mayor a 5 fl y aquellos cuyo aumento fue menor a 5 fl.
La respuesta a la terapia fue tomada de acuerdo a los criterios de respuesta en tumores sólidos. Los datos se recogieron en una ficha de recolección de datos y posteriormente la información fue recopilada y vaciada en Excel.
Se presentan los datos en Cuadros (frecuencias y porcentajes) y Figuras de barras y circulares, que conducen al análisis de la muestra y a la discusión de los resultados. Además, se correlacionaron las variables de interés. Se correlacionaron las variables SG y SLP obteniéndose un valor de 0,80 y 0,68 en cada grupo respectivamente.
RESULTADOS
De las 136 historias revisadas se incluyeron 54 que cumplían con los criterios para este estudio, 37 (68,51 %) correspondían al sexo femenino y 17 (31,48 %) al sexo masculino. La edad mínima fue 33 años y la máxima 88 años, con una edad promedio de 67 ±10,69 años.
En cuanto al estadiaje, 39 (72,2 %) pacientes fueron estadio (St) IV, 7 pacientes (12,96%) St IIb, 5 pacientes (9,25 %) St IIIa y los St IIIb, IIa, IB representaron 1 paciente (1,85 %) cada uno de ellos, respectivamente (Figura 1).
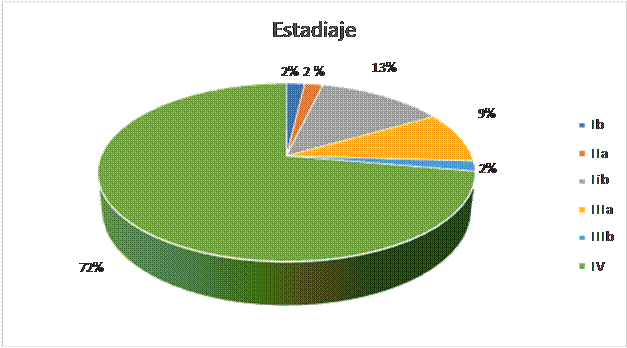
Figura 1.
Distribución según estadiaje de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed y macrocitosis eritroide.
Instrumento de recolección de datos.
El 100 % de los pacientes recibieron premedicación con ácido fólico y vitamina B 12 previo al inicio de tratamiento con Pemetrexed.
El Pemetrexed fue usado como tratamiento de primera línea en 44 (81,48 %) pacientes, 10 (18,5 %) pacientes lo recibieron como segunda línea, mientras que de los 54 pacientes incluidos en el estudio 30 (55,55 %) de ellos usaron Pemetrexed en mantenimiento (Figura 2).
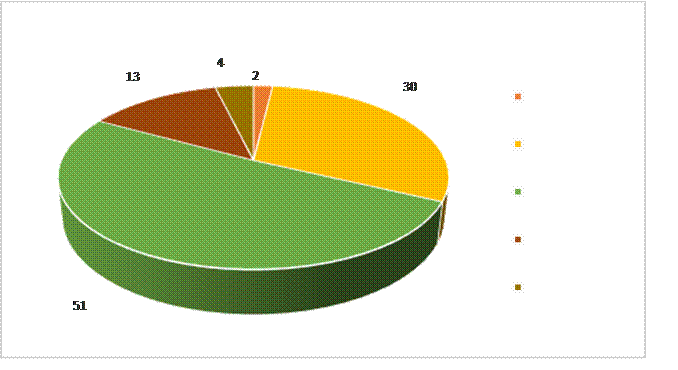
Figura 2
Distribución según la línea de tratamiento recibido de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed y macrocitosis eritroide
Instrumento de recolección de datos.
El VCM eritroide obtenido de las hematologías realizada por los pacientes previo al inicio de tratamiento tuvo un rango de (79,8-100,7) fl, con un promedio de 89,28 fl.
Al revisar los valores de VCM eritroide posterior al inicio de tratamiento con Pemetrexed encontramos que el valor mínimo fue de 81 fl y el valor máximo fue de 107,1 fl con un promedio de 98,60 fl.
Encontramos que en todos los pacientes hubo incremento de VCM eritroide posterior al inicio de tratamiento con Pemetrexed, sin embargo, fines de evaluar el cambio en el valor del VCM eritroide posterior al inicio de Pemetrexed se dividieron los pacientes en 2 g
El VCM eritroide obtenido de las hematologías realizada por los pacientes previo al inicio de tratamiento tuvo un rango de (79,8-100,7) fl, con un promedio de 89,28 fl.
Al revisar los valores de VCM eritroide posterior al inicio de tratamiento con Pemetrexed encontramos que el valor mínimo fue de 81 fl y el valor máximo fue de 107,1 fl con un promedio de 98,60 fl.
Encontramos que en todos los pacientes hubo incremento de VCM eritroide posterior al inicio de tratamiento con Pemetrexed, sin embargo, fines de evaluar el cambio en el valor del VCM eritroide posterior al inicio de Pemetrexed se dividieron los pacientes en 2 grupos, un grupo donde el VCM eritroide se incrementó más de 5 fl encontrando 38 (70,37 %) pacientes y otro grupo cuya variación fue menor a 5fl, representado por 16 (29,62 %) pacientes, respectivamente (Figura 3).
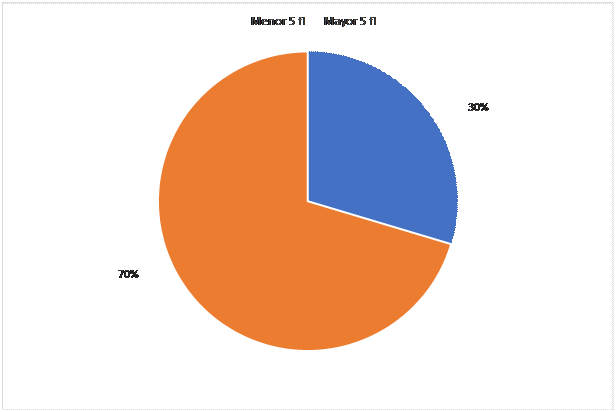
Figura 3
Distribución según la diferencia entre VCM de inicio y VCM máximo durante el tratamiento recibido en los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed.
Instrumento de recolección de datos.
El tiempo en alcanzar el VCM eritroide máximo posterior al inicio con Pemetrexed fue variable, siendo los más frecuente 2 meses por 11 (20,3 %) pacientes y 5 meses por 11 pacientes (20,3 %);
6 (11,11 %) lo alcanzaron a los 7 meses, 5 (9,25 %) lo alcanzaron a los 3 meses y 5 (9,25 %) a los
6 meses, al mes 3 (5,55 %), 1 paciente (1,85 %) a los 9 meses y después del primer año 4
(7,40 %) pacientes. El promedio fue de 5, 16 meses.
Al evaluar el tipo de respuesta alcanzada por los pacientes en tratamiento de los 54 pacientes, el 82% alcanzó respuesta parcial o enfermedad estable, 9 % respuesta completa y 9 % no respondió (Figura 4). Sin embargo, al evaluar el tipo de respuesta en cada grupo, encontramos que; de los 38 pacientes con un VCM eritroide que alcanzaron un diferencial mayor a 5 fl posterior a iniciar el tratamiento 33 (86,4 %) pacientes alcanzaron respuesta parcial o enfermedad estable, 3 (7,89 %) respuesta completa y 2 (5,26 %) no respondieron (Figura 5). En el grupo donde el diferencial del VCM eritroide fue menor a 5 fl encontramos 11 (68,75%) pacientes con respuesta parcial, 2 (12,50%) en respuesta completa 3 (18,75%). no respondieron (Figura 6).
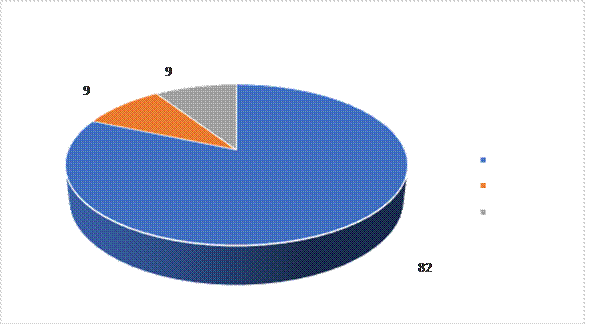
Figura 4.
Distribución según la respuesta al tratamiento de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed y macrocitosis eritroide. que acudieron a la consulta de oncología
Instrumento de recolección de datos.
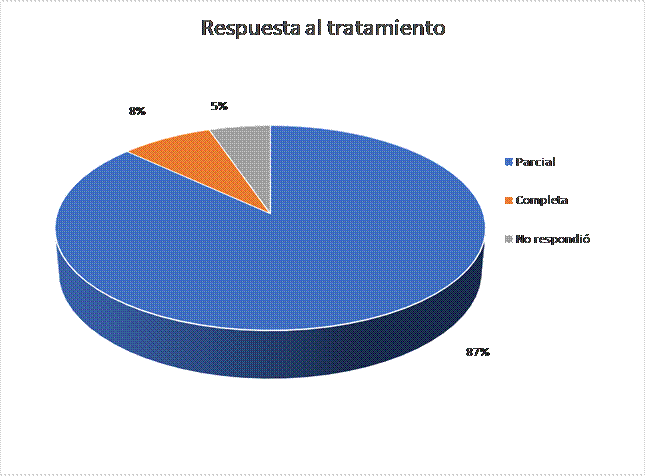
Figura 5
Distribución según la respuesta al tratamiento de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed con un diferencial en el VCM eritroide post tratamiento mayor a 5fl.
Instrumento de recolección de datos.
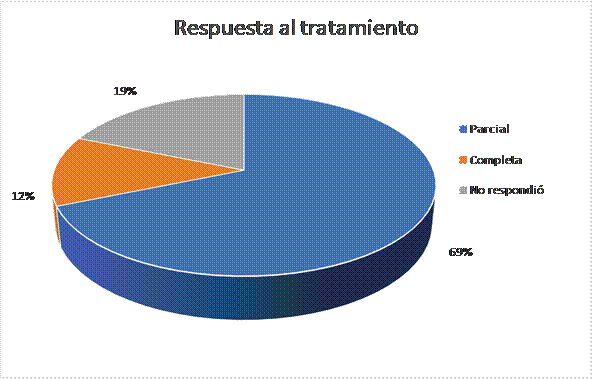
Figura 6.
Distribución según la respuesta al tratamiento de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed con un diferencial en el VCM eritroide post tratamiento menor a 5fl
Instrumento de recolección de datos
De acuerdo a los datos obtenidos la tasa de control de enfermedad en los pacientes cuyo aumento de VCM es mayor a 5fl es de 95 % vs. 81 % en el grupo con VCM menor a 5fl; en cuanto a las tasas de no respuesta encontramos 5 % vs. 19 % respectivamente.
En cuanto a la SG, en el grupo cuya diferencia de VCM eritroide fue mayor a 5 fl el promedio fue de 26 meses. En el grupo con un incremento de VCM eritroide menor a 5 fl la SG con un promedio de 24 meses. Para el grupo con diferencial de VCM eritroide mayor a 5 fl la sobrevida libre de progresión (SLP) con un promedio de 19 meses. En el grupo con VCM eritroide menor a 5 fl con un promedio de 14 meses. (Figura 7).
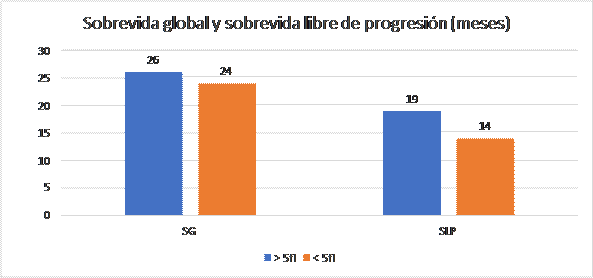
Figura 7
Distribución según la Sobrevida Global y Sobrevida Libre de progresión de los pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed con un diferencial en el VCM eritroide mayor o menor a 5fl.
Instrumento de recolección de datos.
En ambos grupos se correlacionaron las variables SG y SLP obteniéndose un valor de 0,80 (Anexo I) en aquellos cuya diferencia del VCM eritroide fue mayor de 5 fl, mientras que en el otro grupo el valor de la correlación fue de 0,68 (Figura 8)
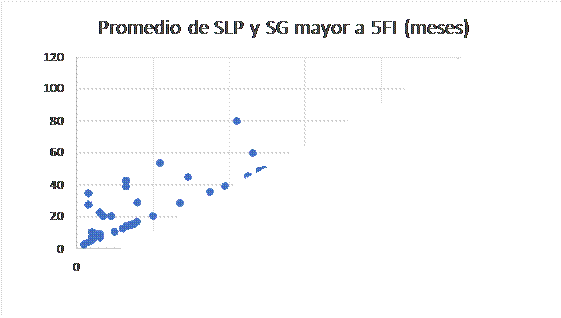
Figura 8
Correlación entre sobrevida global y sobrevida libre de progresión de pacientes con incremento de volumen corpuscular medio eritroide mayor a 5 fl desde el inicio de tratamiento de pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed.
Instrumento de recolección de datos.
Para comparar si existe diferencia significativa entre las pruebas de SLP para el grupo que alcanzó una diferencia VCM >5fl y <5fl, se realizó una prueba de normalidad en los datos, arrojando que no se distribuyen de forma normal, por lo que se procedió a realizar la prueba no paramétrica de Mann-Whitney, obteniéndose como resultado que las pruebas de sobrevida libre de progresión para VCM >5fl y VCM <5fl no son significativamente diferente (P- valor=0,13) (Figura 9).
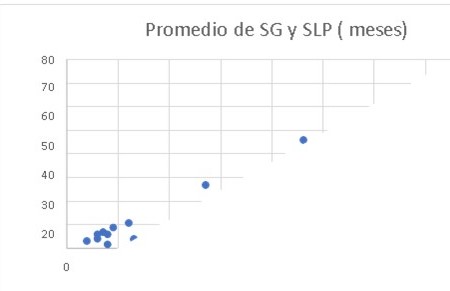
Figura 9
Correlación entre sobrevida global y sobrevida libre de progresión de pacientes con incremento de volumen corpuscular medio eritroide menor a 5 fl desde el inicio de tratamiento de pacientes con Adenocarcinoma de pulmón tratados con Pemetrexed.
Instrumento de recolección de datos.
DISCUSIÓN
El cáncer de pulmón sigue considerándose de alta mortalidad, el 85 % de ellos son de CPNC, dividiéndose en tres subtipos histológicos: adenocarcinoma, carcinoma de células escamosas y carcinoma de células grandes (2).
Una gran proporción de pacientes cursan con enfermedad localmente avanzada o metastásica ameritando el uso de terapia dirigida o específica, sin embargo, el uso de quimioterapia continúa siendo de importancia vital en estos pacientes. Los datos disponibles sugieren que varios regímenes basados en platino son igualmente eficaces.
Pemetrexed es estructuralmente similar a otros antifolatos como el metotrexato, pero a diferencia del metotrexato, que es principalmente un inhibidor de la dihidrofolato reductasa, el Pemetrexed se dirige principalmente a la timidilato sintasa (TS), lo que le confiere un espectro de actividad diferente, tiene un perfil farmacocinético favorable y su principal toxicidad ha sido la mielosupresión que se ha anulado con suplementos dietéticos de folato y vitamina B12 adicional (7).
Tradicionalmente, el subtipo histológico no condicionaba la elección de la quimioterapia. Sin embargo, datos recientes demuestran que la expresión de TS, el objetivo principal de Pemetrexed,
varía según el subtipo histológico de CPNC. Algunos datos clínicos sugieren una respuesta diferencial a los tratamientos basados en Pemetrexed basados en la modificación del VCM eritroide (8).
Es por eso que en esta oportunidad evaluamos si el uso de Pemetrexed condiciona macrocitosis eritroide y si este a su vez puede considerarse un predictor de eficacia en pacientes con ADC de pulmón. Pudimos encontrar que, de los 136 casos revisados, todos modificaban VCM eritroide, pero solo 54 cumplieron criterios de inclusión. De estos 54 pacientes el 70,3 % eran de sexo femenino, diferente a lo que encontramos en la literatura donde el predominio de los pacientes con ADC de pulmón que recibieron Pemetrexed en algunas de sus líneas de tratamiento eran de sexo masculino. Sebastiano y col., en un estudio italiano entre 2007 y 2012, Wang y col., entre 2012 y 2017 encontraron predominio de sexo masculino (4, 6)En relación a la edad, el promedio fue de 67 años, similar a lo descrito por Sebastiano y col.(4) donde la edad promedio fue de 62 años y el rango de edad estuvo comprendido entre 36 y 83 años. En el estudio de Li y col. (3), la edad promedio fue 60 años, con rango de 37 a 76 años.
La enfermedad avanzada (St IV) continúa siendo la más frecuente al momento del diagnóstico, manteniéndose en porcentajes mayores al 70 %, lo que hace pertinente iniciar tratamiento basado en regímenes de quimioterapia, siendo esto frecuente también en nuestro estudio donde el 72 % de los pacientes se encontraban en St IV, similar a lo reportado en el resto de los estudios a nivel mundial. (3,4,6)
Como agente de quimioterapia el Pemetrexed se ha utilizado en combinación con otras drogas como esquema de primera línea, en este estudio el 81,4 % de los pacientes lo usaron de primera línea, coincidiendo con lo reportado por Buti y col. (4) y Al- Saleh (7), concluyendo así que, comparado con otros regímenes terapéuticos, Pemetrexed es más efectivo para el tratamiento de ADC de pulmón.
En cuanto al VCM eritroide, este es un índice sanguíneo relativamente estable en personas sanas, que permite clasificar el tipo de anemia en los pacientes. Con la llegada de los recuentos sanguíneos automáticos, cada vez más se ha prestado atención a la importancia clínica de su aumento o disminución en la predicción de la progresión de la enfermedad y respuesta a distintos tratamientos. (5).
Excepto para ser utilizado para ayudar en el diagnóstico de enfermedades hematológicas, se ha reportado que el VCM eritroide es clínicamente asociado con enfermedades oncológicas no hematológicas como: tumores de cabeza y cuello, cáncer de esófago, cáncer colorrectal, cáncer de hígado, pulmón, entre otros. Su aumento puede estar inducido por el esquema de tratamiento, prediciendo respuesta al mismo y la mayor durabilidad de la respuesta. (6).
Encontramos que en pacientes con ADC de pulmón que fueron tratados con Pemetrexed, su VCM eritroide se incrementó durante la terapia, a pesar de todos estar pre medicados con ácido fólico y vitamina B12, encontrando un VCM máximo posterior al inicio de tratamiento de 107 fl, con un diferencial con respecto al inicio de tratamiento mayor a 5 fl. Siendo superior el valor de VCM encontrado en nuestro estudio que lo reportado en estudios similares donde evaluaron el VCM como predictor de sobrevida (4). El momento de alcanzar el VCM máximo posterior al inicio al tratamiento con Pemetrexed si fue similar al reportado en los estudios multicéntricos de alrededor de 2 meses desde el inicio de la terapia(3,4, 6).
Una diferencia de MCV > 5 fL en el tratamiento con Pemetrexed parece estar correlacionada con una mejor respuesta al tratamiento, SLP y SG. Vélez y col.. (9), informaron resultados similares en términos de aumento del MCV en una población similar (54 pacientes tratados con quimioterapia basada en Pemetrexed). Por su parte Buti y col. (4) tuvieron datos similares, pero en una población más grande.
La SLP fue mayor en ambos grupos al comparar con otros estudios, sin embargo, la tendencia es que en que en el grupo de pacientes donde el diferencial del VCM eritroide es mayor de 5 fl se mantenga la respuesta al tratamiento por más tiempo que en el grupo donde el diferencial es menor a 5 fl (3,4,6), resultado con el cual coincidimos, pudiendo así establecer mayor eficacia de Pemetrexed en cuanto a términos de SLP y SG aunque no haya sido estadísticamente significativo. Esto pudiese explicarse por un incremento en el metabolismo del Pemetrexed y un mayor tiempo de exposición al fármaco en este grupo de pacientes.
El Pemetrexed se mantiene como tratamiento fundamental en pacientes con ADC de pulmón, aunque actualmente se cuenten con líneas de tratamientos más específicas; su mecanismo de acción contempla la vía de la MTHFR que genera macrocitosis eritroide, pudiendo inducir mayor incremento del VCM en pacientes con uso del medicamento y estar en relación con mejoría de su sobrevida.
La macrocitosis eritroide inducida por el uso de pemetrexed en paciente con ADC de pulmón tiende a mejorar respuesta al tratamiento.
En nuestro estudio, se demostró una mejor tasa de control de enfermedad, con respuesta global al tratamiento de 95 % en aquellos pacientes cuyo incremento en el volumen eritroide fue mayor posterior al inicio de la terapia; demostrando así su relación con una mayor eficacia.
Hubo tendencia a mejorar respuesta al tratamiento, expresado en SLP y SG más prolongadas.
En aquellos pacientes con incremento de VCM eritroide mayor a 5 fl la tendencia es a mejorar SG y SLP, aunque no alcanzó significancia estadística.
En Venezuela hasta la fecha no contamos con estudios similares, por lo que pudiese ser la base para caracterizar estos pacientes sospechar la presencia de polimorfismos de la MTHFR que conllevan a mayor sensibilidad a pemetrexed y por ende mejor eficacia.
Consideramos que ampliar el estudio y su seguimiento prospectivo mejorará los datos en términos de eficacia y seguimiento de los pacientes.
REFERENCIAS
1. de Jong D, Das JP, Hong Ma, Valiplackal JP, Prendergast C, Roa T, et al. Novel targets, novel treatments: The changing landscape of non-small cell lung cancer. Cancer (Basell). 2023;15:2855. https://doi.org/10.3390/cancers15102855.
2. Zappa C, Mousa SA. Non-small cell lung cancer: Current treatment and future advances. Transl Lung Cancer Res. 2016;5(3):288-300.
3.Jianjie Li, Yujia Chi, Guang Cao, Jun Zhao, Tongtong An, Meina Wu, et al.. Efficacy and safety of pemetrexed maintenance chemotherapy for advanced non- small cell lung cancer in a real-world setting. J Thorac Dis. 2021;13(3):1813-1821. http://dx.doi.org/10.21037/jtd-21-337
4. Buti S, Bordi P, Tiseo M, Bria E, Sperduti I, Di Maio M, et al. Predictive role of erythrocyte macrocytosis during treatment with pemetrexed in advanced non-small cell lung cancer patients. Lung Cancer. 2015;88:319- 324.
5. Chih-Hsin Yang J, Mok T, Han B, Orlando M, Puri T, Park K. A Review of regimens combining Pemetrexed with an epidermal growth factor receptor Tyrosine Kinase Inhibitor in the treatment of advanced nonsquamous nonesmall-cell lung cancer. Clinical Lung Cancer. 2018;19(1): 27-34.
6. Wang H, Zhang J. Clinical significance of mean corpuscular volume as a prognostic indicator of radiotherapy for locally advanced lung cancer: A retrospective cohort study. J Thorac Dis 2022;14(12):4916-4924. https://dx.doi.org/10.21037/jtd-22- 1684
7. Al-Saleh K, Quinton C, Ellis PM. Role of pemetrexed in advanced non-small-cell lung cancer: meta-analysis of randomized controlled trials, with histology subgroup analysis. February 2012 Curr Oncol. 2012;19(1):e9-e15.
8. Velez M, Raez LE, Perez CA, Gomez JE, Mudad R, AM, et al. Abnormal elevation of erythrocyte mean corpuscular volume (MCV) in non-small cell lung cancer (NSCLC) patients treated with maintenance pemetrexed-based chemotherapy. J Clin Oncol.2012:30(Suppl 15):e17564-e17564.
9. Santos ES, Pérez CA, Gómez JE. Raez L. Increase in the erythrocyte mean corpuscular volume in non small lung cancer patients treat with pemetrexed - based chemotherapy. Disponible en: URL: https://ascopubs.org/doi/10.1200/jco.2010.28.15_suppl.1147
Notas de autor
Hh.arsuve@gmail.com.
Información adicional
Trabajo ganador “Premio Dr. Alejandro Calvo Lairet” 2024: premio
Información adicional
redalyc-journal-id: 3756
