Cartas científicas
18F-DOPA PET/TC para el diagnóstico del hiperinsulinismo congénito
18F-DOPA PET/CT for the diagnosis of congenital hyperinsulinism
18F-DOPA PET/TC para el diagnóstico del hiperinsulinismo congénito
Revista Argentina de Radiología, vol. 81, núm. 3, pp. 226-228, 2017
Sociedad Argentina de Radiología Asociación Civil
El hiperinsulinismo cong??nito (HIC) es una enfermedad poco frecuente, de causa gen??tica, que produce hipoglucemia debido a la secreci??n excesiva y/o desordenada de insulina. De no ser detectada tempranamente produce un severo da??o neurol??gico con un impacto importante en el desarrollo del ni??o. Se han descrito mutaciones en nueve genes como causa de HIC, aunque histol??gicamente se describen tres tipos mayores de esta entidad (difuso [50%], focal [40%] y at??pico [10%]), cuyo manejo difiere dr??sticamente1. Los pacientes con enfermedad focal requieren una pancreatectom??a parcial que remueva la zona de la lesi??n para proveer una cura completa sin las comorbilidades de la pancreatectom??a total. Esta intervenci??n queda restringida para la enfermedad difusa sin respuesta al tratamiento m??dico, cuya morbilidad es la diabetes mellitus iatrog??nica y la insuficiencia pancre??tica ex??crina2.
En Finlandia la incidencia del HIC se calcula en 1 por cada 50 000 reci??n nacidos en poblaci??n general, cifra que aumenta hasta 1 por cada 2500 reci??n nacidos en cohortes con consanguinidad, como las estudiadas en Arabia3. Hasta la fecha, en Argentina no existen estad??sticas ni publicaciones sobre el diagn??stico con 3,4-dihidroxi-6- 18 F-fluoro-L-fenilalanina (18F-DOPA) por tomograf??a computada por emisi??n de positrones (PET/TC) de esta enfermedad.
La 18F-DOPA es un radiotrazador an??logo de la L-DOPA, que ingresa a las c??lulas a trav??s del sistema transportador de amino??cidos, para posteriormente ser transformada en dopamina por la acci??n de la L-DOPA decarboxilasa. Se ha demostrado que las c??lulas neuroendocrinas y las c??lulas B de los islotes pancre??ticos expresan la enzima decarboxilasa, por lo que el radiotrazador es captado, decarboxilado y almacenado en el citoplasma para ser excretado mediante gr??nulos por las c??lulas ex??crinas y end??crinas del p??ncreas4. Por ello, el HIC puede ser diagnosticado mediante el estudio de 18F-DOPA PET/TC.
No obstante, la posibilidad de falsas interpretaciones debe ser considerada por m??ltiples factores. Entre ellos, la subestimaci??n de la captaci??n de lesiones de menor tama??o que la resoluci??n espacial del equipo, las im??genes no corregidas por el efecto del volumen parcial, la lesi??n focal amplia que puede confundirse con la variante difusa, la lesi??n localizada junto al ??rgano que capta fisiol??gicamente 18F-DOPA (como la v??a biliar y el sistema urinario) y la absorci??n insuficiente del radiotrazador en la lesi??n en relaci??n con las c??lulas ex??crinas adyacentes.
La imagen de PET/TC con 18F-DOPA dentro del algoritmo diagn??stico para la localizaci??n del tejido hiperpl??sico hiperfuncionante fue utilizado por primera vez en el a??o 2005 por Rivero et al.5 Desde entonces los diferentes centros del mundo dedicados al diagn??stico y tratamiento del HIC han mostrado su alto valor diagnostico (especificidad del 100%)2. En Latinoam??rica el primer estudio de 18F-DOPA PET/TC se realiz?? en Argentina en el a??o 2015 y hasta la fecha es el ??nico pa??s de la regi??n que ha implementado este m??todo, considerado actualmente como el de referencia para diferenciar entre el tipo difuso y focal.
Queremos compartir con usted y los lectores de la RAR nuestra experiencia inicial en el diagn??stico de HIC por medio de 18F-DOPA PET/TC mediante dos casos representativos, uno de la variante histol??gica focal y otro de la variante histol??gica difusa.
El primer paciente, que ten??a 12 d??as de vida, present?? hipoglucemia en la primera hora posterior al nacimiento (19 mg/dl) y fue tratado con suero dextrosado e hidrocortisona. El examen de insulinemia en hipoglucemia cr??tica (glucemia < 50 mg/dl) report?? 38 mUI/ml (valor de referencia insulinemia < 2) y se diagnostic?? hipoglicemia por hiperinsulinismo (relaci??n insulinemia/glucemia = 46 ([valor normal < 5]). Ante la sospecha de hiperplasia pancre??tica difusa, se solicit?? una tomograf??a computada (TC) de p??ncreas que result?? normal. Por este motivo, se deriv?? a nuestro hospital para ser estudiado mediante 18F-DOPA PET/TC. El equipo utilizado fue un Philips Gemini 64 TF. Las im??genes evidenciaron un foco hipermetab??lico a nivel de la porci??n cef??lica del p??ncreas, con un valor de captaci??n est??ndar m??ximo (SUV m??x) de 1,4. Esta cifra estaba 16% arriba del resto del par??nquima pancre??tico, lo cual fue compatible con foco de captaci??n focal (figs. 1 y 2).
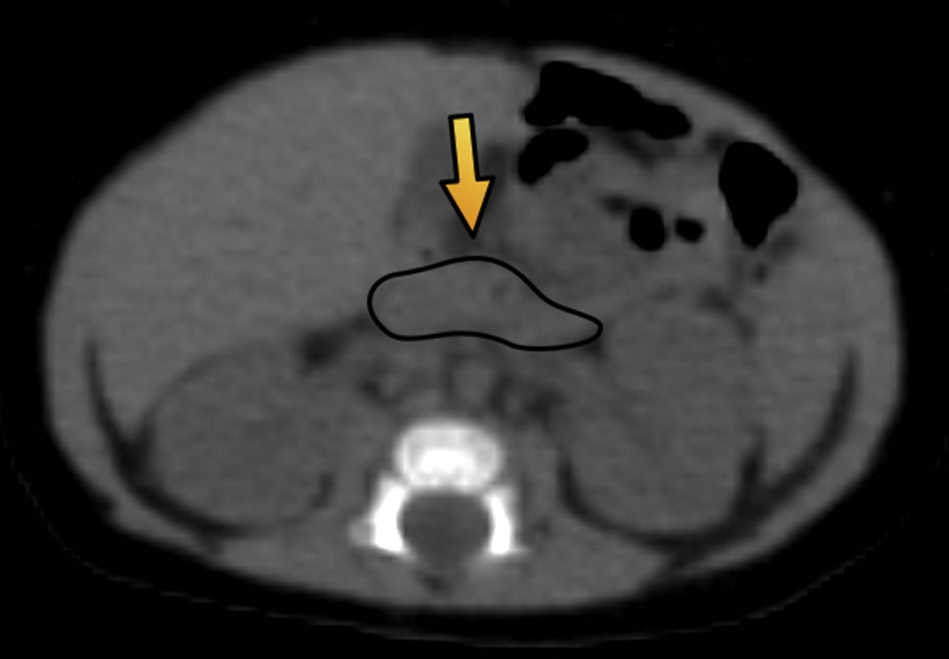
Figura 1
Tomografía computada de abdomen en plano axial muestra un parénquima pancreático delimitado por una línea negra (flecha) de configuración habitual, sin evidencia de lesiones focales.
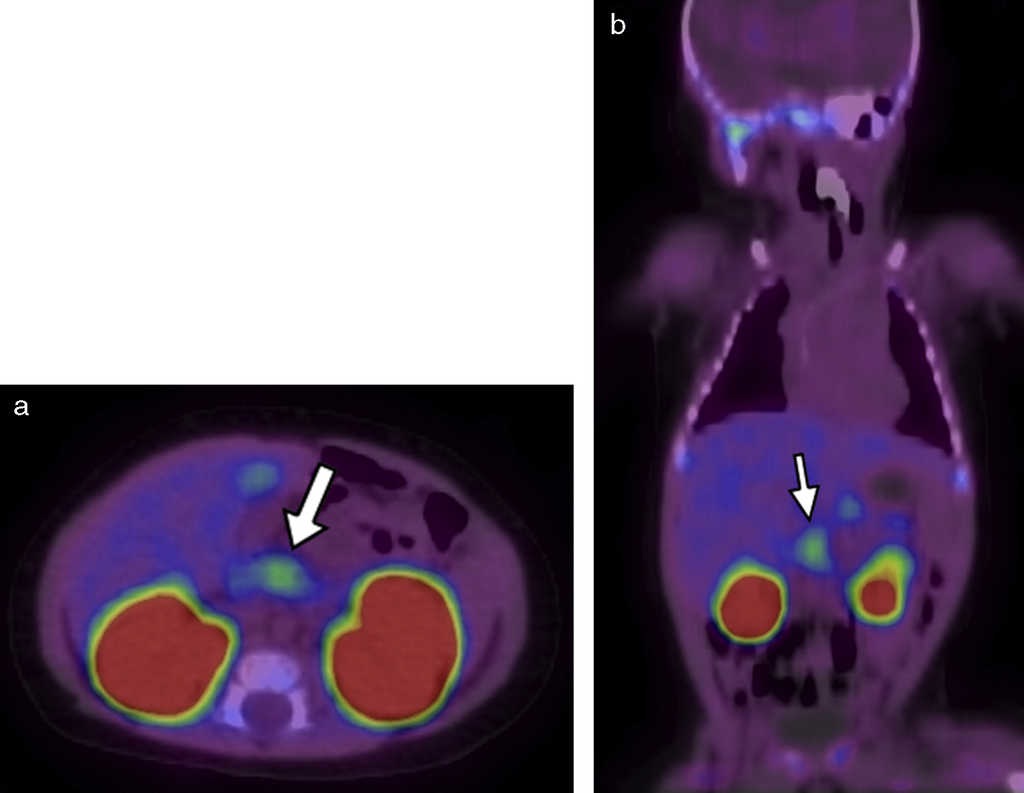
Figura 2
18F-DOPA PET/TC en (a) plano axial al mismo nivel que la y (b) en plano coronal evidencia una imagen focal de alta avidez por el radiotrazador (flechas blancas). También se destacan sitios de captación fisiológica de18F-DOPA, como la vesícula biliar y los riñones.
El segundo paciente de 3 d??as de vida present?? hipoglucemia de 12 mg/dl en las primeras horas posteriores al nacimiento. Fue ingresado a la unidad de terapia intensidad neonatal, donde se registraron hipoglucemias de hasta 20 mg/dl a pesar del tratamiento con suero dextrosado. Se realizaron muestras cr??ticas de hipoglucemias, valores de insulinemia de hasta 177, 223, 208 y 271 mUI/ml. Se descart?? hipoglucemia por d??ficit de hormona adrenocorticotropa (ACTH) y hormona de crecimiento (GH), y se plante?? como hip??tesis diagn??stica el HIC. Se inici?? tratamiento farmacol??gico con diazoxido y octreotide, pero el paciente continu?? con hipoglucemia. Por ello, se plante?? la necesidad de manejo quir??rgico y fue derivado a nuestra instituci??n para la realizaci??n del estudio 18F-DOPA PET/TC. Este identific?? una captaci??n difusa del radiotrazador con focos hipermetab??licos a lo largo de todo el ??rgano (cabeza, SUV m??x 3,8; cuerpo, SUV m??x 3,3; y cola, SUV m??x 3,8) (figs. 3 y 4).
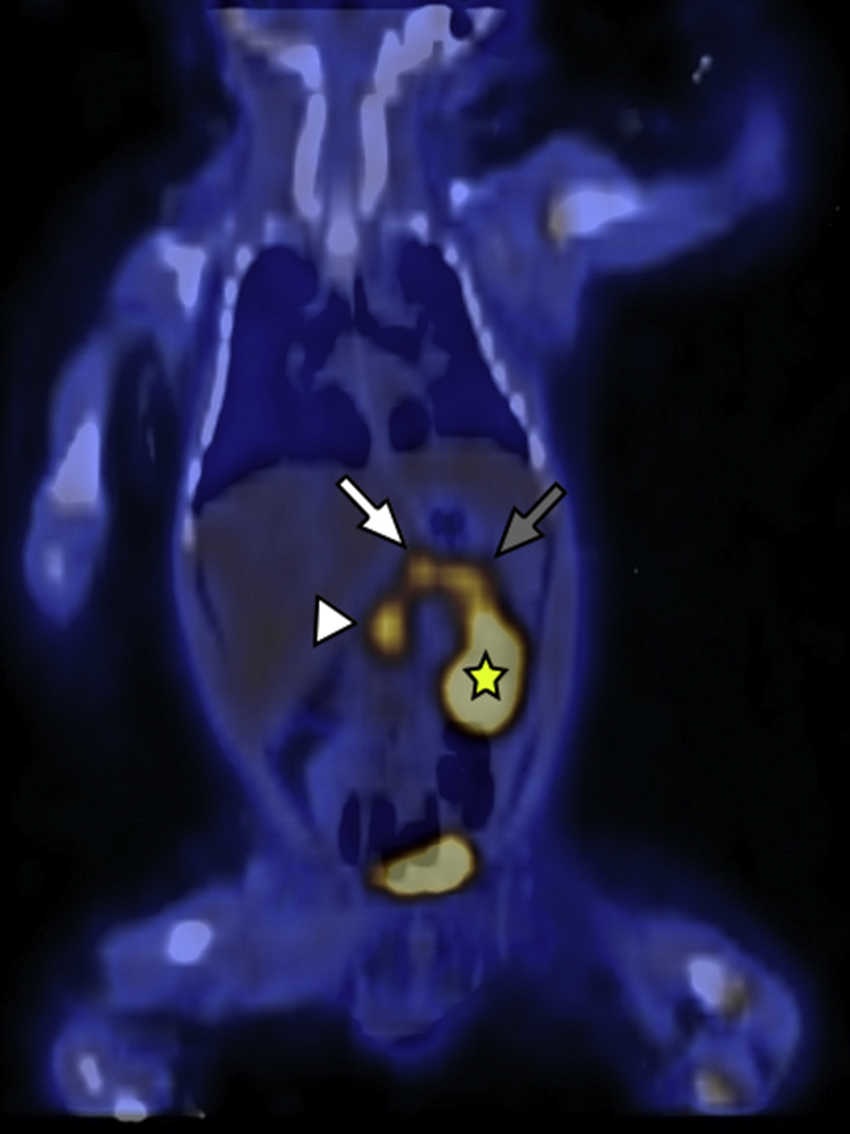
Figura 3
18F-DOPA PET/TC en plano coronal identifica a nivel del parénquima pancreático una acumulación difusa del radiotrazador y tres focos hipermetabólicos a nivel de la cabeza (cabeza de flecha), cuerpo (flecha blanca) y cola (flecha gris). Se señala, además, el riñón izquierdo (estrella amarilla) excretando el radiotrazador.
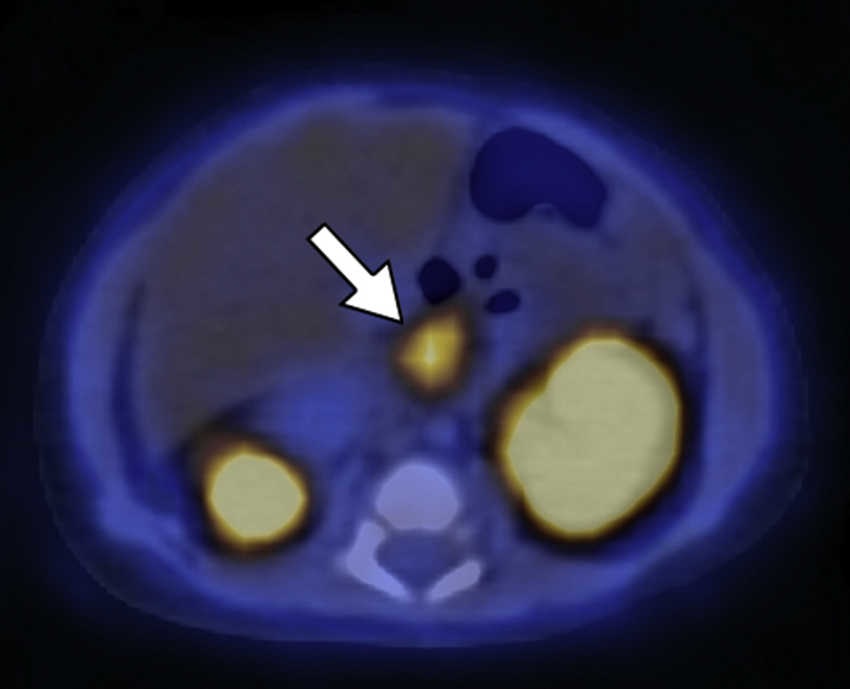
Figura 4
18F-DOPA PET/TC en plano axial del mismo paciente que la muestra una de las zonas de acumulación patológica del radiotrazador localizada en la cabeza pancreática.
Ambos pacientes fueron sometidos a tratamiento quir??rgico: en el primer caso se realiz?? pancreatectom??a parcial y en el segundo una total. El an??lisis histopatol??gico confirm?? el diagn??stico en los dos pacientes.
Confidencialidad de los datos
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicaci??n de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido informaci??n suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Conflicto de intereses
Los autores del trabajo declaran no tener ning??n conflicto de intereses.
Bibliografía
Palladino A.A, Stanley C.A. A specialized team approach to diagnosis and medical versus surgical treatment of infants with congenital hyperinsulinism. Semin Pediatr Surg. 2011; 20:32-7
Gopal-Kothandapani J.S, Hussain K. Congenital hyperinsulinism: role of fluorine-18L-3, 4 hydroxyphenylalanine positron emission tomography scanning. World J Radiol. 2014; 6:252
Glaser B, Thornton P, Otonkoski T, Junien C. Genetics of neonatal hyperinsulinism. Arch Dis Child-Fetal Neonatal Ed. 2000; 82:79-86
Seibyl J.P, Chen W, Silverman D. 3,4-dihydroxy-6-[18F]-fluoro-L-phenylalanine positron emission tomography in patients with central motor disorders and in evaluation of brain and other tumors. Semin Nucl Med. 2007; 37:440-50
Ribeiro M-J, De Lonlay P, Delzescaux T, Boddaert N, Jaubert F, Bourgeois S, et al. Characterization of hyperinsulinism in infancy assessed with PET and 18F-fluoro-L-DOPA. J Nucl Med. 2005; 46:560-6
Notas de autor
Autor para correspondencia. maria.bastianello@hotmail.com