Resumo:
Busca-se identificar a influência da política de regulação de preços da CMED para
medicamentos novos (novo, novo de referência, biológico novo) de contemplar os
interesses das empresas, nacionais e transnacionais, e favorecer o consumidor. A
metodologia emprega a criação de uma base de comparação entre os preços de
fábrica e máximo ao consumidor estipulados pela CMED, dos medicamentos novos da
classe terapêutica L da classificação Anatomical Therapeutic
Chemical, introduzidos no mercado entre abril de 2017 a agosto de
2020, confrontando-os com os preços praticados por farmácias, em janeiro 2021,
retirados do Consulta Remédios. A análise demonstrou que: (i) os princípios
novos, são majoritariamente introduzidos por transnacionais; (ii) os agentes do
setor possuem grande margem para comercialização; (iii) a regulação é
desrespeitada por parte dos varejistas; e (iv) tais políticas não fomentam as
empresas a investirem em P&D no Brasil. Há a necessidade de revisão da
política da CMED, por haver falhas no mercado.
JEL: D02, I18, L5.
Palavras-chave: Mercado farmacêutico, Regulação, Precificação de medicamentos novos, CMED.
Abstract: The research aims to identify the influence of CMED’s price regulation policy for new drugs (new, new reference, new biological) in considering the interests of national and transnational companies and favoring the consumer. The methodology employs the creation of a comparison base between the factory prices and the maximum consumer prices stipulated by CMED for new drugs from the therapeutic class L of the Anatomical Therapeutic Chemical classification, introduced in the market between April 2017 and August 2020, confronting them with the prices practiced by pharmacies in January 2021, taken from Consulta Remédios. The analysis showed that: (i) the new principles are predominantly introduced by transnationals; (ii) the sector’s agents have a large margin for commercialization; (iii) the regulation is disregarded by retailers; and (iv) such policies do not encourage companies to invest in R&D in Brazil. There is a need to review CMED’s policy due to market failures.
Keywords: Pharmaceutical market, Regulation, Pricing of new drugs, CMED.
Artigo original
A introdução de novos medicamentos no mercado farmacêutico brasileiro: exame em um cenário de precificação regulada*
The introduction of new drugs in the Brazilian pharmaceutical market: examination in a regulated pricing scenario
Received: 21 February 2023
Accepted: 11 September 2024
O estudo da indústria farmacêutica é uma missão complexa. Exige um entendimento profundo das características específicas do mercado farmacêutico global e nacional sobre as diversas etapas de sua cadeia produtiva, desde as empresas que produzem os medicamentos, as companhias que fornecem os insumos, até mesmo a prescrição dos medicamentos ao paciente feito pelos profissionais da saúde, além do papel do governo no monitoramento e na regulação do mercado (Hasenclever et al., 2002; Schweitzer; Lu, 2018).
Entre as características marcantes da indústria estão a essencialidade dos bens produzidos, a estrutura de mercado e, em particular, o fato de ser um segmento intensivo em ciência (Pavitt, 1984), que requer elevada soma de investimentos em P&D como porcentagem das receitas. No conjunto, esses atributos, entre outros, contribuem para uma estrutura de mercado oligopolizada, por vezes, acomodando monopólios por classes e subclasses terapêuticas (Rêgo, 2000; Moura, 2011).
Devido a importância do setor na saúde pública, constantemente o segmento farmacêutico é contemplado por políticas de estímulo industrial e de ciência, tecnologia e inovação (Mazzucato, 2013). Um dos instrumentos utilizados seria o financiamento público de P&D à saúde, como o realizado pelos Estados Unidos e pelo Reino Unido, mas muito incipiente no Brasil (Hasenclever et al., 2020, p. 95-96). Outro instrumento é a regulação na precificação dos medicamentos, utilizado pelo Governo Federal.
No Brasil, o controle estatal de preços, a partir de 2003, é realizado por meio da Câmara de Regulação do Mercado de Medicamentos (CMED). Este órgão interministerial possui a atribuição de regulação econômica do mercado farmacêutico, com a finalidade de promover a concorrência, estimular o acesso aos medicamentos e à inovação farmacêutica (Anvisa, 2019).
Entretanto, estudos realizados por Rocha (2019) e Santana (2019) destacam a insatisfação demonstrada por produtores de medicamentos nacionais com a política seguida pela CMED. No que tange à precificação de produtos novos sem patentes, chamados de inovadores (categoria II da Resolução CMED n. 02/2004), eles são valorados comparando-se os custos de tratamento com produtos alternativos já no mercado, enquanto os produtos novos com patentes (categoria I) são precificados contra o menor preço praticado em um rol de países definidos pela CMED.
A falta de isonomia na questão da precificação de produtos introduzidos no mercado pelas categorias I e II, que abrangem, respectivamente, os produtos novos e inovadores, pode levar ao desincentivo à introdução de produtos inéditos pelos produtores brasileiros que, em geral, introduzem inovações incrementais. Essa falta de isonomia é reforçada pela prática de análise de patentes pelo Instituto Nacional de Propriedade Industrial (INPI) que exclui o patenteamento de inovações incrementais, tais como inovações de segundo uso, apesar de que estas inovações implicam novos gastos em pesquisa e desenvolvimento (P&D). Há estudos em curso para a formação de preços da inovação incremental, que estimulariam a P&D no setor farmacêutico (Santana, 2019, p. 9).
Esta pesquisa busca subsidiar questões relevantes ao fortalecimento e consolidação do mercado farmacêutico brasileiro: a regulação e a precificação de medicamentos novos e inovadores. No cenário brasileiro, até os anos 2000, as empresas farmacêuticas nacionais se limitavam a produzir genéricos, mas, desde a segunda metade da década, têm ampliado progressivamente seus investimentos em P&D, ainda que direcionados para inovações incrementais (Paranhos et al., 2020).
Entretanto, a discussão sobre as inovações incrementais ou de segundo uso divide opiniões na área farmacêutica (Rocha, 2019, p. 67). Dentre os argumentos contrários a esse processo é que as inovações incrementais podem ser utilizadas pelas farmacêuticas como forma de estender ao máximo a exclusividade de mercado e o ciclo de vida de seus produtos. Isso seria prejudicial, pois atrasaria a entrada de genéricos e daria à empresa um aumento de seu portfólio de produtos e lucratividade adquiridos de forma artificial e sem qualquer ganho terapêutico (Rocha, 2019, p. 68).
Já entre os argumentos favoráveis a esse debate está o fato de que as empresas nacionais acessam recursos limitados para o financiamento do P&D, o que as obriga a uma decisão estratégica de acordo com os riscos que envolvem cada pesquisa. A ausência de recursos substantivos para realização de inovações radicais no Brasil, que exigem financiamentos capazes de reduzir as incertezas relacionadas ao seu desenvolvimento (Paranhos et al., 2020), faz com que as empresas nacionais escolham inovações incrementais, a opção muito mais segura e potencialmente menos custosa (Abbott, 2019).
Neste contexto, a pergunta de pesquisa que se quer responder é: A política adotada pelo governo brasileiro para definição dos preços dos medicamentos novos e inovadores, via CMED, está adequada para viabilizar, por um lado, o acesso dos consumidores aos medicamentos (preços mais baixos possíveis e inferiores ao preços máximos regulados) e, por outro, a remuneração isonômica para produtores nacionais (regulados, principalmente, pela categoria I) e multinacionais (regulados pela categoria II) no que diz respeito aos produtos novos?
O objetivo principal deste estudo é analisar o modelo de precificação para produto novo e/ou inovador praticado pela CMED a partir dos seguintes objetivos parciais ou específicos: a) descrever a política de precificação da CMED sobre o PF e PMC e os modelos de regulação seguidos por alguns países; b) analisar os preços praticados pelo comércio varejista e confrontá-los com os estabelecidos pela CMED - preço de fábrica (PF) e preço máximo ao consumidor (PMC); c) distinguir a nacionalidade das empresas que estão introduzindo medicamentos novos patenteados. As hipóteses e os critérios que delas emergem para responder à pergunta proposta pelo estudo, podem ser sintetizadas por: (i) se preço do varejo é superior ao preço máximo da CEMED, os consumidores não estão sendo beneficiados; (ii) se o preço de fábrica da CEMED é superior ao preço de mercado, o preço de fábrica está sendo marcado acima do que é necessário para os inovadores;
A justificativa principal do estudo é contribuir com evidências empíricas para subsidiar eventuais mudanças na regulação de preços, especialmente na regulação de produtos novos, que parece não acompanhar a evolução do mercado farmacêutico brasileiro, marcado pelo crescimento das inovações incrementais e pelo prejuízo às empresas nacionais. Em suma, o trabalho procura contribuir com a discussão sobre a validade da atual política de regulação dos preços dos medicamentos novos e, ao mesmo tempo, contribuir para melhorar as diretrizes da CMED nessa categoria de produtos. A análise destas questões pode fornecer elementos para a reflexão de opções de políticas e um desenvolvimento institucional mais adequado.
Para atingir os objetivos propostos, além desta Introdução, este estudo é composto por mais quatro etapas. O tópico 2 detalha a metodologia e as hipóteses que sustentam o estudo, bem como os critérios para responder à pergunta da pesquisa. O item 3 descreve os critérios de precificação na introdução dos medicamentos novos e/ou inovador pela CMED. O item 4 apresenta os dados coletados utilizando a metodologia de pesquisa, e realiza a análise comparativa dos preços dos medicamentos inovadores, entre abril de 2017 e agosto de 2020, com os preços dos medicamentos novos selecionados, praticados pelas drogarias, com preços base em janeiro de 2021. Por último, as considerações finais apresentam os principais resultados, as limitações do trabalho e sugestões para futuras pesquisas.
As hipóteses do estudo foram formuladas considerando pontos identificados nas políticas da CMED, sua comparação com outros sistemas regulatórios e insatisfações declaradas por agentes regulados acerca da precificação de produtos farmacêuticos novos, dividindo-se em:
Hipótese 1: Se a regulação de preços realizada pela CMED, aplicada no momento da entrada do produto novo e/ou inovador no mercado e corrigida anualmente, estimula a cadeia produtiva a seguir essa política, duas situações são possíveis: a) o preço de fábrica (PF) estabelecido pela CMED para produtos novos é significativamente maior que o preço praticado no mercado, ou seja, há forte indício que a margem de lucro, que já é considerada pela Câmara de regulação no momento da determinação desse preço, mais do que compensa os esforços em desenvolvimento de novos produtos - requer revisão da precificação para diminuir o valor ao consumidor final; b) o preço máximo ao consumidor (PMC) estabelecido pela CMED para produtos novos não é significativamente maior que o preço praticado no mercado - a precificação parece estar apropriada;
Hipótese 2: Se a regulação da CMED para produtos novos, mesmo considerando todos os custos e margem, aplica métodos que não induzem as empresas a investir em P&D no Brasil - tanto as nacionais, como as empresas transnacionais - há problemas na política de regulação econômica.
A metodologia proposta para o estudo de precificação de medicamentos novos está fundamentada no confronto entre o valor definido aos atacadistas/varejistas (PF) e preços aos consumidores finais (PMC) definidos pela CMED e aqueles praticados pelas redes de comércio (atacadistas e varejistas), ou seja, um exame do comportamento dos valores máximos e mínimos comercializados. A avaliação está baseada na estatística descritiva das diferenças de preços observados em fontes primárias e secundárias.
A pesquisa realizou-se em quatro etapas, não obrigatoriamente sem interseções entre elas. A primeira etapa, baseada na revisão de literatura, descreve os modelos de precificação de medicamentos no Brasil e em alguns países selecionados, onde os modelos tenham passado por algum tipo de análise. A segunda etapa diz respeito a coleta e sistematização dos dados sobre os medicamentos novos disponíveis no site da CMED/Anvisa e colocados no mercado brasileiro de medicamentos entre abril de 2017 e agosto de 2020, período em que a informação está disponível1. São considerados medicamentos novos aqueles classificados pela Anvisa como novo, novo de referência ou biológico novo2.
Segundo a Anvisa (Brasil, 2020), os medicamentos como novos, de referência e biológicos são definidos, respectivamente, como: (i) produtos inovadores comercializados cuja eficácia, segurança e qualidade foram comprovadas cientificamente junto ao órgão federal competente por ocasião do registro; (ii) medicamentos novos, com insumo farmacêutico ativo (IFA) que até o momento não havia sido registrado no país; e (iii) medicamento biológico é aquele que contém molécula com atividade biológica conhecida. Os dados publicados pela CMED com os valores dos medicamentos são divulgados mensalmente, porém as correções dos preços são feitas, em geral, em março de cada ano, seguindo a metodologia publicada por regras da câmara regulatória.
O Preço Fábrica (PF) é o preço máximo pelo qual um laboratório ou um distribuidor pode comercializar o medicamento. Nele estão considerados os custos, impostos (IPI), a margem de lucro dos laboratórios e dos distribuidores, além do percentual de distribuição. O Preço Máximo ao Consumidor (PMC) é o valor máximo permitido para venda ao consumidor final, incluindo os custos e impostos incidentes em cada Estado (ICMS). Assim, este seria o valor máximo autorizado a ser praticado por farmácias e drogarias, podendo tais varejistas praticar preços inferiores ao máximo, tendo em vista que este já contempla a margem de comercialização, lucro e os impostos. O Preço Máximo de Venda ao Governo (PMVG) resulta da aplicação do Coeficiente de Adequação de Preços (CAP) sobre o Preço Fábrica, quando for o caso. Quando a legislação não prevê a aplicação do CAP, o PMVG será igual ao PF (Anvisa, 2019).
A base de dados obtida a partir da CMED contém as seguintes informações: princípio ativo, Cadastro Nacional da Pessoa Jurídica (CNPJ), laboratório, registro, produto, apresentação, classe terapêutica, tipo de produto (status do produto), PF, PMC (impostos variando de 0% até 20%) e comercialização entre 2016 e 2020 (ano de entrada do medicamento no mercado brasileiro). Essas informações permitiram determinar o número de princípios ativos e de apresentações colocadas no mercado por ano e dos laboratórios proprietários dos registros.
A terceira etapa diz respeito à delimitação da base de dados e a coleta dos preços praticados. A etapa anterior selecionou 154.889 observações. Delas foram excluídos os princípios ativos com registros duplicados (decorrente da publicação ser mensal) - subamostra com 21.070 itens - e os registros de apresentações diferentes do mesmo medicamento (diferentes dosagens). Desses procedimentos restaram 2.639 observações que foram classificadas segundo os laboratórios responsáveis pela inovação, origem do capital (nacional/estrangeira) e preços definidos pela CMED.
Adicionalmente, os princípios ativos foram separados por Classe Terapêutica, conforme as Diretrizes para classificação ATC (Anatomical Therapeutic Chemical) e, para limitar a amostra e tornar o estudo factível, considerados apenas os medicamentos registrados como novos da Classe Terapêutica L. De acordo com a Diretrizes para classificação ATC e atribuição DDD (Defined Daily Dose) 2020 da Organização Mundial da Saúde, essa classe abrange os agentes antineoplásicos e imunomoduladores. Esses medicamentos são na maioria utilizados em tratamentos de alta complexidade e custos elevados - neoplasias (câncer); terapia endócrina; tratamento da esclerose múltipla (EM), doenças autoimunes e inflamatórias crônicas; auxiliar o sistema imunológico a combater infecções e doenças, na prevenção de rejeição de transplantes. Dessa seleção resultaram 138 princípios ativos para exame dos preços no varejo.
Segundo a Anvisa (2019), em 2018, a classe terapêutica L foi a que obteve o maior faturamento entre as classes ATC, com faturamento de R$ 12,47 bilhões ou 16,4% do mercado. Além disso, os produtos oncológicos lideraram as pesquisas clínicas no mundo, com 3.466 iniciativas (29%) em 2019. No Brasil, no mesmo ano, cerca de 68 estudos foram realizados, representando aproximadamente 2% das pesquisas mundiais dos últimos cinco anos (Interfarma, 2020).
Após a delimitação da base de princípios ativos (138), realizou-se uma pesquisa no site de algumas drogarias e farmácias utilizando a plataforma Consulta Remédios3, para determinar os preços praticados no mercado. Nessa coleta, realizada no período entre 02 de janeiro e 17 de janeiro de 2021, foram colhidos todos os preços disponíveis - sem considerar o valor do frete, por ser uma compra online, e descontos - para cada apresentação comercial (276)4. Essa busca foi bem-sucedida para 195 (66%) apresentações farmacêuticas e 96 princípios ativos (69%), relacionados a 38 redes de farmácias e drogarias presentes no site Consulta Remédios.
Por fim, foram necessários dois procedimentos adicionais: i) a eliminação dos medicamentos que apresentaram menos de dois registros de preços no varejo, impossibilitando a comparação com a base da CMED; ii) a exclusão dos produtos classificados como embalagens hospitalares e de uso restrito a hospitais e clínicas, que não podem ser comercializados pelo PMC. Por isso, foram definidos dois grupos de medicamentos: (1) princípios ativos “com restrição hospitalar”, que contempla 19 medicamentos em 26 apresentações e; (2) “sem restrição hospitalar”, que engloba 65 fármacos e suas 129 apresentações.
A última etapa foi a análise comparativa entre os preços praticados vis a vis o PF e o PMC, aplicada para a subamostra obtida após as hipóteses formuladas acima, e apresentada no item 4.
A CMED possui como objetivo institucional a regulação econômica do mercado de medicamentos para promover a assistência farmacêutica à população, estimulando a oferta de medicamentos e a competitividade do setor. Deve-se considerar que o controle direto dos preços dos medicamentos e lucros das farmacêuticas é considerado um fator importante na sustentabilidade fiscal dos sistemas de saúde (OCDE, 2015, p. 149), que são pressionados principalmente pela incorporação de novas tecnologias (OCDE, 2015, p. 24).
O fato de os valores dos medicamentos serem elevados em determinado país acaba sendo um grande obstáculo ao acesso a tratamento de doenças, independentemente do grau de desenvolvimento do que tenha essa nação. Nos últimos anos, a procura por produtos farmacêuticos novos aumentou drasticamente, impulsionada pelo envelhecimento da população, pela crescente prevalência de doenças crônicas e por mudanças nas práticas clínicas, como a introdução de tratamentos inovadores (Belloni; Morgan; Paris, 2016). Tais fatores são justificativos suficientes para o acompanhamento e análises de políticas voltadas ao acesso a medicamentos novos.
No mercado farmacêutico brasileiro, tanto as farmácias e drogarias, como laboratórios, distribuidores e importadores, devem respeitar os limites de preços determinados pela Câmara de Regulação do Mercado de Medicamentos (CMED)5. A CMED determina também o preço de entrada no mercado. Para essa definição a câmara usa dois procedimentos. Primeiro, toma como base os preços praticados em uma cesta de países (Austrália, Canadá, Espanha, Estados Unidos, França, Grécia, Itália, Nova Zelândia e Portugal), uma prática adotada por diversas nações na hora de precificar os produtos farmacêuticos. Segundo a CMED definiu que os produtos e apresentações novos são precificadas seguindo as categorias: I e II, que contemplam os novos produtos e; III, IV, V e VI para as novas apresentações. Neste estudo, os medicamentos analisados pertencem às duas primeiras classificações.
Na categoria I, se define como produto inovador que tenha molécula objeto de patente (ainda não registrada) no país e traga algum ganho em relação aos medicamentos já utilizados no tratamento para a mesma indicação terapêutica6. Já a categoria II é a classe dos medicamentos novos que não se enquadram na categoria anterior (inovação incremental). Assim, além de ser definida tendo com base nas opções terapêuticas disponíveis no Brasil, a precificação não pode ser superior ao menor preço internacional dos países de referência. Com a definição do PF de entrada, podem ser calculados o PMC e Preço Máximo de Venda ao Governo (PMVG).
O fabricante pode classificar o remédio por critérios de inovação e ganho terapêutico, ou também, como produtos que possam contribuir para aumentar a concorrência no mercado. Ademais, o produtor propõe à CMED um PF de entrada. Se o medicamento submetido não estiver sendo comercializado no país, este preço inicial não poderá superar ao que esteja sendo praticado em pelo menos três dentre os nove países considerados de referência.
A Resolução n. 1 de 01/06/2020 determina a maneira como a CMED define o PF e o PMC dos medicamentos, além de disciplinar a publicidade dos preços e estipular quais serão as margens de comercialização dos produtos farmacêuticos (Brasil, 2020a). A partir do segundo ano de comercialização, esta regra também se aplica ao reajuste aos produtos novos (CMAP, 2019, p. 20). O de cálculo do reajuste anual de preço é definido pelo índice chamado Variação Percentual do Preço (VPP). O VPP leva em conta a inflação acumulada entre março e fevereiro do ano subsequente, além dos ganhos de produtividade das empresas e o valor dos custos de produção (Anvisa, 2019), e é definido como (Brasil, 2020a):
, onde:
• IPCA: Índice Nacional de Preços ao Consumidor é calculado pelo IBGE;
• X: fator de produtividade repassado ao consumidor - procura captar redução de custos de produção para possibilitar redução dos preços; calculado com base no Índice de Produtividade do Setor Farmacêutico (razão entre Índice de Produção Física e total de horas trabalhadas);
• Y: fator de ajuste de preços entre setores - utilizado para captar possíveis aumentos nos custos de produção e elevações nos preços que precisam ser compensados; consideram-se as médias anuais de variação de custos com importação de insumos e variação das tarifas públicas;
• Z: fator de ajuste de preços intrassetor e calculado em função do fator X - considera-se a concentração do mercado para autorizar de reajuste de acordo com o Índice de Herfindahl-Hirschman (IHH), segundo níveis:
• Nível 1 - Sem evidências de concentração (IHH < 1.500): Fator Z = Fator X.
• Nível 2 - Moderadamente concentrado (1.500 < IHH < 2.500): Fator Z assume a metade do valor do Fator X.
• Nível 3 - Fortemente concentrado (IHH > 2.500): Fator Z = 0.
Os fatores X e Y são calculados pela Secretaria de Advocacia da Concorrência e da Competitividade do Ministério da Economia (SEAE/ME). O fator Z é estipulado pela Secretaria Executiva da CMED, Assim, a metodologia acaba por aplicar o menor reajuste para mercados com indicativo de menor concorrência e um maior reajuste para mercados com indicativo de maior concorrência.
Aqui são apresentados exemplos de precificação impostas por algumas nações, selecionadas após levantamento bibliográfico. Ao discutir as precificações existentes, Safatle (2017) destaca que a regulação de preços dos medicamentos é uma política largamente utilizada nos países da Organização para a Cooperação e Desenvolvimento Econômico (OCDE). Ademais, mesmo utilizando políticas de regulação, Dias, Santos e Pinto (2019) destacam que nos membros da OCDE, os governos chegam a financiar 60% dos medicamentos para a população, pois os valores podem comprometer uma considerável parte dos orçamentos das famílias, principalmente as de renda baixa.
Ao examinar a regulação internacional de medicamentos, Safatle (2017) aponta características como: (i) as políticas e ferramentas mais comuns nos países que adotam a regulação econômica do setor farmacêutico são a de price cap (preço máximo) e a de referenciamento externo de preços; (ii) comum em diversas localidades a comparação com preços de alternativas terapêuticas já existentes no mercado interno; (iii) estudos de farmacoeconomia são frequentemente realizados em boa parte dos países que regulam seus mercados. Em países da Europa, como Alemanha e Dinamarca, não há o estabelecimento de tetos de preços, mas os preços desses mercados são influenciados pela política de reembolso. Já o Reino Unido regula os custos e as margens de lucro do setor, com preços também influenciados pelas análises de custo-efetividade. Controles de custos e de margens de lucro já foram mais utilizados no passado, mas tal prática vem diminuindo, pois, segundo o autor, pode estimular empresas ineficientes ou custosas.
Para a Organização Pan-Americana da Saúde (2009), na América Latina há diversos critérios definidos para a regulação direta dos preços dos medicamentos, sendo que essas políticas seguem as experiências dos países em seus mercados e em outros considerados de referência. Assim, os principais critérios utilizados nas precificações podem estar baseados no custo de produção (como na Colômbia, Cuba e Equador), na sua utilidade terapêutica (Cuba e Brasil), em avaliação econômica (Brasil e Nicarágua), no preço de outros tratamentos disponíveis no mercado para a mesma patologia (Brasil e Cuba), e/ou nas comparações internacionais de preços (Brasil, Colômbia, Cuba, México e Nicarágua).
Dentro dos principais países da América Latina, a Argentina passou no início de 2018 a ter uma política nacional de medicamentos com a negociação e fixação de preços máximos. A política anterior era criticada porque, como principal consumidor, o governo não exercia um papel efetivo como regulador de preços, especialmente no caso de medicamentos oncológicos e de alto custo (Bisang; Luzuriaga; San Martín, 2017; Agência EFE, 2018).
O México, que não cobra impostos de medicamentos (Sindusfarma, 2019), aplica preço máximo apenas para medicamentos protegidos por patentes, ficando isentos da regulação os fármacos genéricos e os medicamentos de referência cujas patentes expiraram. Caso haja novos produtos sem comparadores, o fabricante pode definir o preço, que, no entanto, está sujeito a reavaliação três meses após o lançamento do produto (Moïse; Docteur, 2007).
Entre os países de referência para a CMED, França e Espanha são frequentemente escolhidos como base de comparação devido aos seus baixos preços, à transparência e ao acesso facilitado às informações sobre preços (Espin; Rovira; Labry, 2011, p. 13-14). Os Estados Unidos, o caso mais importante dentre as referências da CMED, são os maiores produtores de fármacos, líder em investimentos em P&D, o maior mercado consumidor de medicamentos e o que apresenta os mais altos preços de venda. Tais características já o fazem bem diferente da realidade brasileira. Além disso, dentro de sua cultura menos intervencionista, não praticam qualquer controle estatal quanto à formação de preços de medicamentos. Existe, no entanto, uma fiscalização rigorosa conduzida pela FDA (Food and Drug Administration) para a aprovação de medicamentos em termos de qualidade (Danzon; Keuffel, 2014; Monte, 2019).
Porém, Hyman e Silver (2020) consideram que o sistema americano para precificação e pagamento de medicamentos contra o câncer apresenta problemas. Há evidências de que em algumas terapias os preços seriam excessivamente altos para tratamentos introduzidos que oferecem apenas melhorias marginais em relação aos tratamentos já existentes. Outro fator seria a crescente inacessibilidade de copagamentos para alguns pacientes. Tais problemas seriam agravados por políticas que não levam em consideração as opções de tratamento concorrentes e são estruturadas de forma a distorcer os incentivos para a classe médica.
Já na Austrália, são as empresas farmacêuticas que definem o preço de seu medicamento no mercado, sem intervenção regulatória. Caso o medicamento seja indicado para integrar o Programa de Benefícios Farmacêuticos (PBF), que auxilia nos custos de medicamentos prescritos, o governo pode negar a inclusão no benefício. O governo e o fabricante devem concordar formalmente o preço de um produto antes de integrar o PBF, mas o fabricante não está obrigado a listar um produto. Além disso, o valor máximo de reembolso de um medicamento de um grupo terapêutico baseia-se no valor do menor preço do grupo e os pacientes pagam qualquer diferença entre o preço do medicamento adquirido e o preço de referência (Paris; Belloni, 2014).
Na Grécia há a fixação de preços máximos e de reembolso de produtos farmacêuticos. Os Boletins de Preços relevantes são revisados e emitidos semestralmente pelo Ministério da Saúde grego. O sistema é cofinanciado pelo Estado, contribuições para a seguridade social e pagamentos privados. Apesar das virtudes dessas políticas, existem críticas em relação aos aspectos de transparência, equidade e sustentabilidade de longo prazo (Yfantopoulos; Chantzarias, 2018).
Essas diferentes formas de regulações influenciam a política brasileira, pois alguns desses países servem como referência para os preços nacionais de novos fármacos introduzidos no mercado e dos que já são comercializados.
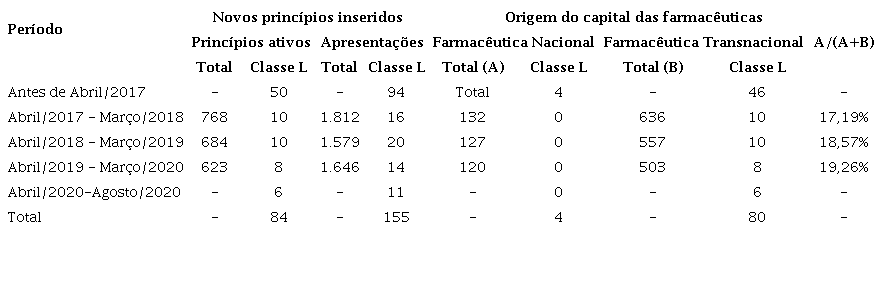
Mesmo que o período analisado seja curto (somente três ciclos), pode-se constatar uma pequena queda tanto no total quanto nos registros da Classe L. Além disso, os resultados confirmam a forte participação das empresas transnacionais (cerca de 80%) nos registros de novos produtos.
No período, foram colocados no mercado 84 novos medicamentos da classe L (em 155 apresentações). Deste valor, 50 (46 estrangeiros e 4 nacionais) medicamentos foram introduzidos antes da CMED começar a informar o tipo (status) do produto em suas publicações. Além disso, 6 medicamentos (em 11 apresentações) foram inseridos entre março de 2020 e agosto de 2020, completando a amostra em exame neste estudo.
A análise para os preços de todos os princípios ativos e suas apresentações é realizada após o agrupamento dos produtos que têm os preços de mercado marcados: a) acima (margem ou variação positiva) ou abaixo (negativa) do PF e PMC, e; b) essas variações são examinadas segundo três faixas: até 20%, entre 20,01% e 40% e acima de 40%. Dessa maneira, são analisadas as relações de preços mínimos e máximos praticados, confrontados entre si e com os PF e PMC definidos pela CMED, que apresentam as menores e maiores diferenças (%) - negativas e positivas - registradas em cada um desses três intervalos e as respectivas participações na amostra (%).
As faixas de variação (margem) dos preços foram selecionadas pelos seguintes motivos. Primeiramente, para os medicamentos “sem restrição”, os valores deveriam apresentar variação negativa, visto a regra da regulação da CMED ser do modelo de teto de preços (PMC). Ou seja, os valores das farmácias não poderiam exceder o determinado pela Câmara de Regulação. Por isso, é importante destacar a participação na amostra dos medicamentos que estão abaixo do teto e o número de fármacos encontrados acima do teto de preços. Para as variações negativas, pode-se intuir quais estão sendo os valores máximos de desconto em comparação ao teto de preços que a farmácia/drogaria está vendendo o fármaco. Essa informação permite ter uma ideia da margem de operação que as produtoras farmacêuticas, distribuidores e farmácias podem explorar e negociar entre si.
Em segundo lugar, essas faixas de percentuais de variações selecionadas foram definidas seguindo algumas características identificadas no mercado farmacêutico, tendo como base: a) variação do ICMS cobrado para estes produtos no PMC, pois o PF é um valor que não contempla o ICMS e sim o IPI. Assim, os valores do PMC contemplam os percentuais de ICMS que variam de 0% até 20% nos medicamentos em geral. Dentro da base dessa pesquisa, os valores dos medicamentos foram encontrados em farmácias e drogarias que operam em estados com ICMS de 17% (1 ocorrência), 18% (35 ocorrências) e 20% (2 ocorrências). Mesmo considerando que os valores de ICMS já estão inclusos nos preços analisados, tanto os da CMED para o PMC de 18% quanto nos valores retirados das farmácias e drogarias, a faixa percentual foi adotada como parâmetro de análise para possíveis diferenças tributárias; b) a faixa de valores entre 20% e 40% foi selecionada pois, pelo relato do CADE - Conselho Administrativo de Defesa Econômica, no caso do abuso cometido por estabelecimentos hospitalares, e detalhado adiante, foi evidenciado uma prática abusiva de aplicação aos valores pago pelas instituições nos medicamentos e utilizados nos tratamentos, um percentual a mais de 20% até 38%; c) o grupo acima de 40% seriam aqueles que utilizam uma margem acima dos intervalos citados anteriormente. Essa margem teve como um dos motivos de escolha o resultado de uma pesquisa realizada pelo Procon/SP, com 17 medicamentos de referência em seis drogarias e farmácias de São Paulo, de forma online entre os dias 31/03 e 04/05/2020. Nela se identificou que as maiores variações entre os preços mínimos e máximos desses medicamentos pesquisados foram de 41,2% em março e 40,6% em maio (Procon, 2020).
Importante destacar o motivo da análise descritiva do PF, com os preços encontrados e praticados pelo comércio varejista, para os medicamentos com e sem restrição hospitalar. O esperado é que PF seja menor que o preço de mercado, pois dentro do preço final, há o custo de comercialização das farmácias, o valor dos impostos e possíveis lucros. Na verdade, se considerarmos que o preço ao consumidor engloba até 20% de ICMS, percentuais abaixo desse valor merecem ser destacados.
A variação negativa entre preço CMED e de mercado pode indicar que o varejo consegue vender abaixo do máximo estipulado para os fabricantes/importadores/distribuidores. Nesse caso, poder-se-ia concluir que a precificação para o fabricante pode ter sido além do necessário, pois ele está conseguindo repassar ao comércio final, por meio de políticas de bonificação ou qualquer outra estratégia comercial, o que sugere uma política de desconto frente ao valor da regulação.
Os medicamentos com restrição são os fármacos de uso restrito a hospitais e clínicas ou que possuem embalagem hospitalares. Assim, através da Resolução CMED n. 03/2009 ficou definida a não publicação do PMC, em qualquer meio de divulgação, para medicamentos registrados como de “uso restrito a hospitais e clínicas”. A Orientação Interpretativa n. 5/2009 da CMED buscou indicar que os hospitais não devem lucrar com a venda de insumos hospitalares, mas apenas serem reembolsados pelo valor pago para os fornecedores de medicamentos e materiais hospitalares. Porém, práticas abusivas no segmento hospitalar foram identificadas pelo CADE7 ao investigar, em um inquérito administrativo, uma suposta prática de conduta anticoncorrencial por agentes do setor da saúde.
Havia indícios de que as tabelas de preços de medicamentos e materiais hospitalares utilizadas como referência nos contratos de prestação desses hospitais eram diferentes da CMED, cobrando tais valores de pacientes, de planos de saúdes com coparticipação, atendimentos privados e das operadoras de planos, que acabam repassando para os clientes. Dessa forma, apresentar e verificar o comportamento dos preços de fábrica em relação aos preços praticados se torna um ponto interessante para evidenciar este tipo de desvio de conduta
Na base de dados deste estudo, os princípios ativos classificados como “com restrição hospitalares” oriundos de farmacêuticas transnacionais somaram 18 (94,7%) e 1 medicamento foi registrado por uma empresa brasileira, totalizando 26 apresentações. De forma geral, o princípio ativo de maior valor financeiro foi o Plerixafor (produto: Mozobil) que apresentou valor máximo deR$ 24.887,34 e mínimo de R$ 21.490,00. Já a maior diferença encontrada entre o máximo e o mínimo, R$ 3.570,54, foi o Trastuzumabe (Herceptin - apresentação de 440 mg) com mínimo de R$ 11.870,00, dentre 8 observações. Essas diferenças de preços de mercado, com outras discutidas a seguir, permitem intuir a magnitude de gastos adicionais que podem recair sobre a população em tratamentos médicos, por vezes longos.
Entre os preços máximos e mínimos encontrados no comércio varejista, por apresentação farmacêutica, 1 fármaco não apresentou variação em seus preços e a maior variação foi de 55,7% (Rituximabe; produto: Mabthera; 9 observações). Considerando os intervalos de preços categorizados para a análise, 18 (69,2%) apresentações mostraram variação entre 0% e 20%, 5 (19,2%) estavam na faixa de 20,01% e 40% e 3 (11,5%) estavam acima de 40% de variação.
Como esses medicamentos não possuem seus PMC divulgados, os preços praticados pelos varejistas, por apresentação farmacêutica, foram comparados ao preço de fábrica definido pela CMED. Identificaram-se três apresentações com valores inferiores ao PF estipulado pela CMED (R$ 833,76). As três apresentações de cloridrato de gencitabina (produto: Gemzar) apresentaram variações negativas de -10,91%, -24,96% e -54,42%.
Já as demais 23 apresentações farmacêuticas dos princípios ativos “com restrição hospitalar” tiveram variação positiva de até 81,8% (Vinflunina; produto: Javlor; valores máximo e mínimo encontrados de R$ 940,50 e R$ 924,66, respectivamente). Dentro das faixas percentuais categorizadas neste estudo, sete fármacos (26,9%) apresentaram variações entre 0% e 20%, enquanto oito (30,8%) situaram-se em cada um dos intervalos seguintes: de 20,01% a 40% e acima de 40%.
O exame entre os preços máximos encontrados no comércio varejista e o preço fábrica definido pela CMED mostra variações significativas, entre -47,2% e 107,0%. A maior variação negativa de -47,23% foi observada para a apresentação farmacêutica, Cloridrato de Gencitabina (produto: Gemzar), o mesmo medicamento e a mesma composição que apresentou anteriormente a menor relação entre preços máximo e mínimo. Somente este fármaco apresentou variação negativa. As demais 25 apresentações obtiveram valores maiores que o estipulado no PF da CMED, sendo que 1 ficou na faixa de 0% até 20%, 7 medicamentos entre 20% e 40% de oscilação, e os demais, que representavam 65,4% dos preços observados (17 fórmulas farmacêuticas), estavam com valores que excedem o PF em mais de 40%. Nesses casos estão, por exemplo, as substâncias: i) Carfilzomibe (Produto: Kyprolis) 107,0% acima do PF e preços máximo e mínimo de R$ 8.910,00 e R$ 7.074,47, e; ii) Cladribina (Produto: Leustatin) com precificação de 93,7% acima do PF
Nesse item são confrontados os preços praticados pelas farmácias e drogarias com os preços definidos pela CMED - PF e PMC. Isso é importante para analisar se as políticas de regulação econômica estão sendo seguidas e os preços praticados não ultrapassam o estipulado. Esse exame mostra o comportamento dos agentes frente à regulação governamental.
Na base definida como “sem restrição hospitalar” obteve-se 66 princípios ativos e 129 apresentações farmacêuticas. O número de observações de preços no varejo para o mesmo fármaco variou entre 3 e 16 registros. De forma geral, os valores de aquisição das apresentações analisadas partem de um preço mínimo de R$ 31,75 até um máximo de R$ 109.176,73. Os três fármacos de maior valor financeiro foram: 1) Midostaurina (produto: Rydapt; valor máximo de R$ 109.176,73 e mínimo de R$ 87.330,00), caracterizado também como o medicamento com maior diferença entre todos os valores observados (R$ 21.846,73); 2) Ibrutinibe (produto: Imbruvica; preço máximo de R$ 75.615,10 e mínimo de R$ 56.077,99), sendo também a segunda maior variação em reais (diferença de R$ 19.537,11); 3) Acalabrutinibe (produto: Calquence; valor máximo de R$ 70.433,67 e mínimo de R$ 63.430,00).
A maioria dos princípios ativos (30) e apresentações (63) pertence à classe dos anticorpos monoclonais e inibidores antineoplásicos, todos registrados por farmacêuticas estrangeiras, distribuídas entre os seguintes países: África do Sul (cinco apresentações; 3,9%), Alemanha (oito; 6,2%), Estados Unidos (37; 28,7%), França (cinco; 3,9%), Japão (seis; 4,7%), Reino Unido (13; 10,1%), Suíça (47; 36,4%) e Uruguai (duas; 1,6%). Foram observados somente três medicamentos de origem nacional (4,5% da subamostra) em seis apresentações, sendo todos da subclasse terapêutica de terapia endócrina. O medicamento Dietilestilbestrol (produto: Destilbenol da Apsen Farmacêutica) apresentou, em sete observações, o menor preço de toda amostra (preço máximo de R$ 37,38 e o mínimo foi de R$ 31,75).
A análise entre os preços máximos e mínimos encontrados no comércio varejista (farmácia e drogarias) identificou que a menor variação entre esses valores foi de 0,0% e a maior de 150,3%. O fármaco que apresentou essa variação superior foi o Anastrozol (produto: Arimidex) e, dentre de 16 valores registrados, se obteve o valor máximo de R$ 1.237,09 e mínimo de R$ 494,35. Nos intervalos de análise considerados neste trabalho, 44,2% (57 das apresentações farmacêuticas) tinham variação dos valores entre 0% e 20%, outras 38,0 % (49) entre 20,01% e 40% e, por fim, 17,8% (23) acima de 40%.
Quanto às diferenças entre o PF e o menor preço praticado no varejo, 25 apresentações (19,4% da amostra) registraram variações negativas, indicando que o PF era superior ao menor preço praticado. O maior desconto sobre o preço fábrica foi de -76,8%, registrado pela sustância Hemitartarato de Vinorelbina (produto: Navelbine; quatro observações com valor mínimo de R$ 236,50 e máximo em R$ 245,04). Entre as 104 (80,6%) relações positivas das apresentações farmacêuticas. A maior variação foi de 86,9% do medicamento Venetoclax (produto: Venclexta; valores máximos de R$ 51.245,26 e mínimo de R$ 47.885,00).
Considerando as faixas percentuais estabelecidas para a análise, 21,7%, (28 apresentações), apresentaram variações entre 0% e 20% e 13,2% (17) estavam na faixa de 20,01% a 40%. Na faixa acima de 40% se encontravam a maioria das substâncias, 45,7%, que contemplam 59 medicamentos.
Por outro lado, os preços máximos em relação ao preço fábrica apresentam diferenças entre -75,9% até 118,7% nos valores. A substância que registrou diferença de -75,9% foi a apresentação farmacêutica Hemitartarato de Vinorelbina (produto: Navelbine), a mesma que obteve a menor relação entre os preços mínimos e PF, anteriormente. No total, sete apresentações estavam com um preço de mercado inferior ao PF definido pela CMED (5,4% da subamostra). As 122 apresentações restantes registraram valores superiores ao PF da CMED, sendo que 3 na faixa de 0% até 20%, 26 tinham variação de 20% a 40%, e 93 tinham preços com variações acima de 40% do PF. Neste último grupo está a substância Mesilato de Lenvatinibe (Produto: Lenvima) com uma relação superior de 118,7% e preços máximos e mínimos de R$ 13.533,08 e R$ 10.700,00. Além deste, em mais sete observações os preços máximos apresentaram uma variação superior a 100% do valor do PF.
As relações a seguir comparam os valores encontrados nas farmácias e drogarias contra os valores máximos ao consumidor (PMC) (i) sem imposto e (ii) com alíquota de 18% de ICMS. Inicia-se pela comparação entre os preços máximos e mínimos retirados dos sites das varejistas contra o PMCCMED sem imposto. É importante frisar dois pontos. Primeiramente, estamos comparando o PMC sem imposto com os preços praticados pelo comércio final, que está com o ICMS incluído. Há valores negativos que representam variações de mais de 20% em relação ao PMC, mesmo que o preço dos medicamentos esteja com o imposto embutido e o estipulado pela CMED não. Segundo ponto, uma oscilação positiva, poderia significar a não inclusão do ICMS. Ocorre que há medicamentos que já apresentam valores acima desse percentual, o que pode levantar a questão de sobrepreço em relação ao definido na regulação.
A comparação entre o PMC e o preço mínimo no varejo identifica uma variação entre -83,2% e 24,4%. Os índices negativos foram registrados em 77 apresentações farmacêuticas, ou seja, 59,7% da subamostra, sendo que a menor variação foi da substância Hemitartarato de Vinorelbina (produto: Navelbine), a mesma que registrou a menor variação na comparação entre o PF e os preços dos varejistas. Além dessa, outras cinco apresentações tinham preços marcados abaixo de -50% do PMC. Entre as flutuações positivas, 54 apresentações comerciais registraram diferenças acima de 20%. SOMA > 129
Dentro dos intervalos percentuais categorizadas para critério de análise, 49 fármacos ficaram distribuídos (38,0% da subamostra) com valores entre 0% e 20% e somente três (2,3%) das substâncias entre as apresentações na faixa de 20,01% e 40%. Nessa comparação, nenhum ficou acima de 40% de variação.
Já para a análise entre os preços máximos retirados dos sites das farmácias e drogarias em confronto com o PMC/CMED, sem impostos, vemos diferenças entre -82,60% e 45,58% dentro dos preços coletados. A maior relação negativa de -82,60% foi observada para a apresentação farmacêutica Hemitartarato de Vinorelbina, comentado anteriormente. Diferenças negativas ocorrem para 34 (26,4%) apresentações.
As demais 95 (73,6%) apresentações obtiveram valores maiores que o estipulado no PMC da CMED, sendo que 46 (35,7%) ficaram na faixa de 0% até 20%, 45 (34,9%) entre 20% e 40%, e quatro (3,1%) estavam com preços de venda no varejo em mais de 40% do que o definido pela regulação. Dentre as variações positivas se destacam as substâncias Mesilato de Lenvatinibe (Produto: Lenvima; diferença de 45,6% e preços máximo e mínimo de R$ 13.533,08 e R$ 10.700,00), Enzalutamida (Produto: Xtandi; 43,9%), o Citrato de Tamoxifeno (Produto: Nolvadex; 40,8%) e o medicamento Anastrozol (Produto: Arimidex; 40,8%).
Na análise da relação entre os preços máximos e mínimos encontrados no comércio varejista (farmácia e drogarias) em comparação com o PMC com 18% de ICMS definido pela CMED, vale destacar que foram considerados 119 apresentações farmacêuticas, pois 10 produtos da base não disponibilizaram os valores do PMC/CMED com impostos. Assim, essas 10 apresentações não estão incluídas.
Confrontando o PMC vis a vis o preço mínimo no varejo, encontrou-se uma variação de -86,2% e -0,03%, ou seja, todos os valores retornaram variações negativas. Isso era o esperado para uma análise deste tipo e que demonstraria uma adequação a regulação. Identifica-se que a menor diferença foi da substância Hemitartarato de Vinorelbina (produto: Navelbine), aquela que registrou em todas as comparações anteriores os maiores valores negativos.
Estes resultados demonstram que é possível para a farmácia vender os medicamentos dando descontos de até 80% do estabelecido pela CMED. Como mencionado anteriormente, isso pode ocorrer por políticas de bonificações das fabricantes para os comércios farmacêuticos que mais venderem seus produtos, descontos na compra em lotes maiores ou negociações melhores entre fabricante e varejista, entre outras políticas comerciais. Isso revela que há espaço para negociações e vendas com até 82% de desconto, mesmo com a incidência de 18% de ICMS.
Já na análise comparativa entre os preços máximos dos varejistas frente ao PMC/CMED com impostos, verifica-se um cenário similar ao anterior, com diferenças entre -85,7% e 17,0% nos valores. Ressalte-se, no entanto, que neste caso há preços burlando a regulamentação.
Das 38 soluções farmacêuticas (32,0% da base analisada) tiveram diferenças na faixa de 0% até 20%. Os registros de 0% até 2%, que somaram 11 medicamentos, poderiam ter como justificativa o percentual de ICMS que possui uma alíquota máxima de 20% (a análise utiliza 18%), ou seja, não se teria como afirmar que o teto de preços foi infringido. Porém, há outras 27 apresentações farmacêuticas que apresentam variações, entre o preço máximo encontrado nos sites das farmácias e drogarias e o PMC com 18% de ICMS, de 2,4% até 17,0%. Em resumo, o preço praticado estão acima do permitido pela regulação da CMED e estariam desrespeitando essas normas.
Safatle (2017) avalia que a regulação seguida pela CMED vem apresentando resultados favoráveis, dada a evolução dos preços dos produtos farmacêuticos entre janeiro de 1990 e fevereiro de 2017 (série deflacionada pelo Índice Nacional de Preços ao Consumidor - INPC/IBGE) - vide Gráfico 1. A política da CMED permitiu que os preços de medicamentos (aumento de 64,9% no período) se reduzissem em termos reais (elevação do IPCA de 82,3%). O autor também comenta que 87,5% das novas moléculas analisadas e consideradas inovadoras tiveram os preços pleiteados reduzidos e que a regulação garantiu uma redução média de 35% nos preços máximos de entrada dos novos medicamentos (Safatle, 2017).
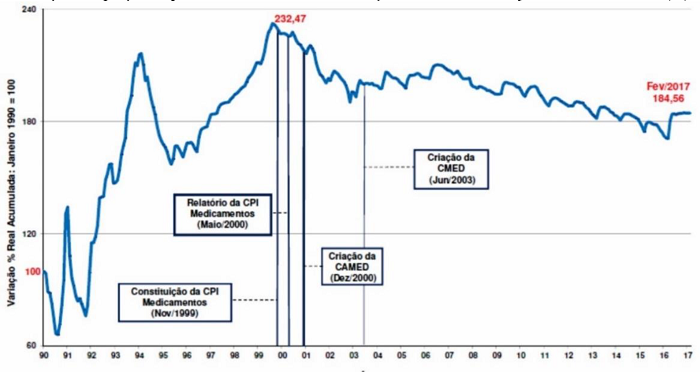
Contudo, nota-se no gráfico dois cenários. Antes da implementação da CMED as variações de preços cresceram vertiginosamente, chegando em seu pico antes da instauração da CPI dos medicamentos que, posteriormente, solicitou a criação de uma agência reguladora para o setor. O outro período de destaque seria posterior a 2003, com a implementação da Câmara de Regulação, marcando uma ligeira tendência de queda, embora sem uma ruptura significativa. Ou seja, a política da CMED controlou os preços dos medicamentos, mas não fez com que eles diminuíssem a ponto de amenizar o período de aumento abusivo (TCU, 2012). A política deveria ter corrigido essa inconsistência, fato que não manteria o padrão elevado por mais de 15 anos e que pode ter garantido aos agentes do setor uma certa lucratividade indevida.
Outra questão sobre o modelo de ajustes é que alguns países que utilizam o teto de preços, como o adotado no Brasil, não realizam reajustes anualmente, e pressupõem realinhamentos dos preços a cada dois ou até, no máximo, cinco anos (Maniadakis et al., 2017; Dias; Santos; Pinto, 2019). Esse já seria um ponto a ser discutido na atual política da CMED.
Outro ponto abordado no trabalho do TCU (2012), que também foi uma das recomendações da CPI dos Medicamentos em 2000, é a necessidade de desindexação dos preços dos fármacos em relação aos índices inflacionários. Isso não acontece na regulação atual, que utiliza o IPCA em três momentos na hora de definir os percentuais de reajuste. Esse fato prejudica tanto a população como o orçamento público. Pois, além dos medicamentos apresentarem variações positivas constantes com a utilização do índice inflacionário, outro fator discutível é que caso haja deflação, os índices não são utilizados no momento do cálculo dos ajustes dos preços, são zerados e não se considera um possível abatimento do valor negativo.
O mesmo ocorre com o fator de produção. Caso este índice resulte em um valor negativo, ele é zerado e não realiza o desconto nos valores dos medicamentos. A justificativa dessa decisão é de que não se pode dar reajuste negativo, pois, desestimularão o setor e as empresas menos produtivas serão beneficiadas em relação as mais produtivas (Brasil, 2020). Ou seja, o paciente não tem acesso ao desconto caso haja uma produtividade negativa, para proteção das empresas. Contudo, a política é para realizar uma precificação justa e promover o acesso aos medicamentos para a população.
Ainda na questão da metodologia, foram selecionados como países de referência, a Austrália, Canadá, Espanha, Estados Unidos, França, Grécia, Itália, Nova Zelândia e Portugal, países com diferenças sociodemográficas, macroeconômicas e no sistema de saúde, bem diferentes do Brasil. Maniadakis et al. (2017), ao estudarem as tendências mundiais em políticas farmacêuticas, consideraram que países desenvolvidos têm cobertura universal e utilizam em suas políticas o controle de produtos farmacêuticos com sistemas de referência de preços internos e externos, controles indiretos de preços e custos, além de realizar avaliações de tecnologia em saúde e controles de utilização de demanda. Porém, os países em desenvolvimento, como no caso do Brasil, apresentam um desempenho inferior em termos de cobertura e dependem principalmente de controles estatais restritivos para regular preços e despesas. E que existem disparidades significativas em todo o mundo no acesso aos produtos farmacêuticos, seu uso e reembolso de custos.
Para os autores, enquanto o desafio dos países de alta renda é manter o acesso aos cuidados, ao mesmo tempo lidam com as tendências em tecnologia e envelhecimento populacional, os países de renda baixa e média ainda fornecem à maioria de sua população apenas acesso precário a medicamentos, mostrando que há grandes diferenças nos objetivos finais das políticas desses dois grupos de países (Maniadakis et al., 2017). O que leva a se pensar o motivo que fez com que a regulação brasileira adotasse como referência, em sua maioria, países de alta renda com objetivos sociais diferentes, sendo que o cenário brasileiro é de grande desigualdade social e diferenças regionais visíveis.
Um exemplo claro é o caso de ter na cesta de países os Estados Unidos, onde os valores dos medicamentos são extremamente elevados, é o país onde grande parte das inovações farmacêuticas são realizadas (Interfarma, 2020, 2021) e não possui um sistema de saúde pública, como o Brasil. Já outros com estrutura macroeconômicas mais parecidas com a brasileira, ou que mesmo que apresentem uma renda mais elevada, como o Reino Unido, porém possui um sistema público de saúde e preços farmacêuticos mais controlados, não fazem parte da cesta de países referência.
Um exemplo de não considerar os fatores conjunturais e sociais do Brasil pode ser visualizado no caso do acesso aos fármacos. Há uma diferença nas distribuições dos medicamentos em localidades do Sul e Sudeste, mais desenvolvidas e com uma infraestrutura de acesso melhor, em relação a certas localidades do Norte do país, menos desenvolvidas e com infraestrutura mais precária. Isso gera uma elevação no custo de comercialização, e alguns medicamentos não são distribuídos em todos os pontos necessários (Drummond, Simões e Andrade, 2018). A metodologia não contempla esse tipo de situação e os reajustes anuais são iguais para ambos os casos, fazendo com que o distribuidor decida pelo mais compensatório, que é distribuir na região Sudeste, deixando os estados do Norte.
Também faz necessário a discussão sobre as mudanças que estão em curso na formação de preços no mercado farmacêutico, que seria a publicação de normas para a incorporação da inovação incremental, que automaticamente estimula o P&D no segmento de fármacos (Santana, 2019). É importante que nela haja métricas claras de como medir os ganhos terapêuticos de cada substância. Pois, atualmente alguns produtos antigos no exterior são considerados inovadores no Brasil, sem comprovação de ganhos clínicos. Ademais as resoluções atuais não estão calibradas adequadamente para medir os ganhos terapêuticos de inovação incremental, o que pode impedir a entrada de alguns medicamentos no mercado brasileiro (Safatle, 2017).
Relevante, também, seria uma melhor discussão sobre a discriminação de preços feita pela metodologia adotada, no momento de definir o valor de entrada do medicamento novo. Como já abordado anteriormente, a determinação de “preços premium”, para medicamentos com referência externa, e preços por custo de minimização, que em geral são produzidos por empresas brasileiras, favorecem as grandes multinacionais. Isso gera não só problemas na definição dos preços, mas também na decisão das farmacêuticas nacionais de investirem em inovações no país8.
Alguns pontos levantados na análise da relação dos preços CMED versus preços nas farmácias e drogarias foram que, ao pesquisar o número de medicamentos introduzidos como novos e a origem do capital da empresa farmacêutica que os registrou, foi possível encontrar que:
• No ano de 2017: foram colocados no mercado 768 princípios ativos e 1.812 apresentações farmacêuticas, sendo que 132 princípios eram oriundos de laboratório nacionais (17,2%) e 636 das soluções vinham de farmacêuticas transnacionais de origem externa (82,8%);
• No ano de 2018: inseriu-se cerca de 684 princípios ativos e 1.579 apresentações. Desses, 127 tinham origem nacional (18,6%) e os demais 557 medicamentos foram desenvolvidos e introduzidos por multinacionais de capital estrangeiro (81,4%);
• No ano de 2019: registrou-se 623 novos fármacos com 1.646 apresentações. Onde 120 tinham origem em companhias do Brasil (19,3%) e 503 foram registradas por farmacêuticas transnacionais (80,7%).
Com este pequeno exercício foi possível evidenciar uma leve queda na quantidade de princípios ativos registrados. Contudo, pela reduzida série de tempo, não se pode afirmar que é uma tendência para o setor no Brasil, nem para o pequeno aumento da participação das companhias brasileiras nesses registros. A Tabela 2 apresenta os principais dados encontrados na análise comparativa realizada.
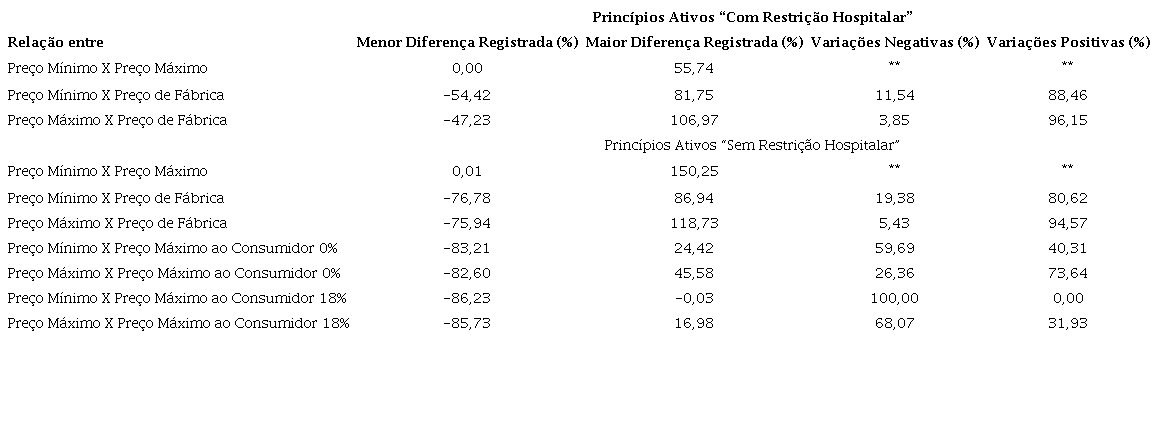
Primeiramente, nos medicamentos que são de uso hospitalar, um subamostra com menor quantidade de observações, a variação entre o preço mínimo e máximo encontrado fica entre 0,0% e 55,7%. Esses medicamentos não podem ser comercializados pelo PMC e não tem estes valores divulgados. Isso levanta a questão de como os pacientes saberão se estão pagando por um valor abaixo do PMC, no caso em que haja necessidade de comprar ou quando se deve realizar um pagamento aos hospitais por cobrança desses medicamentos em tratamentos no sistema privado, se seus preços não são de conhecimento da população.
Nas comparações entre os preços definidos pela CMED de preço fábrica em relação aos preços retirados dos sites das farmácias e drogarias, pode-se verificar que em ambos os grupos de análise, que há variações negativas. Na base “com restrição hospitalar” essa relação é de até -54,4% e no grupo “sem restrição hospitalar” chega a -76,8%. Isso nos revela que no mercado temos preços de venda nos varejistas abaixo do teto determinado pela Câmara de regulação para as farmacêuticas, importadoras e distribuidoras negociar seus produtos. Se esperava encontrar preços próximos ou acima da regulação, pois no valor ao consumidor estão incorporados os impostos, o custo de comercialização dos agentes do setor e seus lucros, apenas o ICMS não é computado.
Nesse mesmo grupo, sem restrição, por haver uma gama de observações maior, a variação dos preços mínimos e máximos apresenta uma oscilação considerável entre 0,01% e 150,25%. Na comparação entre os preços da regulação econômica e os preços cobrados ao consumidor, com impostos, verificam-se dois cenários. O primeiro é que o comércio final consegue vender os produtos com até 86,2% de desconto em relação ao preço regulado, o que é considerado um percentual elevado. O segundo ponto é que há produtos que excedem em até 17,0% os preços máximos definidos pela CMED, o que infringe a lei.
O primeiro fato acima nos remete aos preços definidos pela CMED e corrigido anualmente. Estes valores máximos permitem aos agentes do setor uma negociação que faça com que o preço de venda tenha um valor de mais de 80% abaixo do teto, mesmo que as farmácias tenham custos para cobrir e busquem lucro para se manterem. Assim, será que a política de preços não está definindo valores além do necessário? Ou a definição do preço de entrada e a correção anual está permitindo às farmacêuticas, aos distribuidores e as farmácias, obterem lucros iniciais que permitem negociações futuras bem abaixo do estipulado pela política, pois o faturamento obtido cobre os seus custos e dão suporte para essas estratégias comerciais.
O segundo ponto refere-se aos valores acima da regulação, o que fere o que foi definido por lei. Inicialmente, deve-se considerar que o agente que faz essa fiscalização dos sobrepreços são os pacientes. Como publicado na Orientação Interpretativa nº 08/2017, cabe ao consumidor exigir a lista de preços nas farmácias e drogarias para verificar o preço máximo permitido para o medicamento que deseja adquirir, considerando a alíquota de ICMS vigente no estado da federação em que se encontra. O consumidor pode, ainda, escolher entre as opções disponíveis no mercado o medicamento mais barato, sempre levando em consideração a prescrição médica. Nesse cenário, alguns aspectos devem ser considerados.
Primeiro, um dos grandes problemas no setor farmacêutico é a assimetria de informação, principalmente na relação com a população. Isso pode ocorrer devido ao grau de instrução dos pacientes, o seu conhecimento da legislação regulatória, de como visualizar o tabelamento dos medicamentos e como realizar uma troca de um medicamento por outro de igual aplicação terapêutica receitada pelos médicos, avaliando os preços.
Outra questão, como também comentado anteriormente, seriam as diferenças regionais. Em localidades onde há uma grande concentração de farmácia e drogarias, caso evidencie a cobrança indevida de valores de medicamentos, o paciente poderia simplesmente buscar em outra farmácia seu fármaco e registrar a denúncia de sobrepreço. Contudo, em localidades, principalmente do interior do país, onde há poucas farmácias (uma ou duas em cidades pequenas) como seria para um paciente que vê naquele único estabelecimento a possibilidade de encontrar o medicamento que poderá restabelecer sua saúde, e confirmando o sobrepreço, se recusar a comprar o fármaco necessário e até denunciar o comércio. Onde ele conseguiria o medicamento posteriormente? Será que sua condição permite tal ação?
Quando se trata de produtos essenciais, como o caso dos medicamentos, instituir um PMC que constantemente está num patamar bem mais elevado do que os valores praticados pela grande maioria do mercado, acaba por não garantir a regulação na ponta, ou seja, no preço final ao consumidor. Além disso, também se transfere para o paciente a função de ser o fiscalizador do mercado e o peso que isso implica, desconsiderando possíveis vulnerabilidades sociais e as relacionadas a sua condição de saúde.
Por fim, considerando todos os aspectos levantados nesta discussão, torna-se evidente que a política de preços necessita de uma revisão. Ela permanece há 18 anos em vigor, sem qualquer realinhamento ou revisão por iniciativa do poder público, a não ser quando houve a determinação pelo TCU. É claro que as regras regulatórias devem garantir segurança jurídica para os agentes do setor e mudanças regulares podem gerar atritos nesse quesito. Porém, o fato de não se analisar, em um período considerável, se as regras impostas estão alcançando os objetivos propostos pela regulação, também gera problemas e nesse caso, para a população.
Nesse sentido, em 2019, o governo federal instituiu a comissão de Análise de Impacto Regulatório (AIR), de acordo com as diretrizes da Casa Civil e do novo modelo regulatório da Anvisa. Essa AIR tem a função de analisar a Resolução CMED n. 2/2004, que aprova os critérios para definição de preços máximos permitidos para comercialização de medicamentos novos e novas apresentações (Brasil, 2020a).
Esta pesquisa teve como intuito analisar a influência e a metodologia da determinação de preços para medicamentos registrados como novos no mercado brasileiro. Essa precificação é realizada por um órgão interministerial do governo federal, que segue o modelo de teto de preços. Dentre os principais resultados, foi observado que o segmento farmacêutico de produtos novos é dominado por empresas transnacionais, que detém 80% de participação no lançamento desses produtos. Nessas condições, o modelo de precificação atual fomenta um preço melhor para os produtos trazidos de fora, dada a definição de um preço referenciado ao preço exterior mais elevado. Este resultado é ainda mais desfavorável para a Classe L, em que apenas 5% dos produtos novos é introduzido por empresas nacionais, demonstrando a dependência nacional da produção estrangeria de medicamentos em uma classe terapêutica de doenças de alta complexidade.
Os resultados indicam que a regulação não garante o menor preço e não gera um equilíbrio no acesso aos medicamentos. Os preços máximos de fármacos “sem restrição hospitalar” encontrados nos sites das farmácias e drogarias é superior ao PMC (com incidência de impostos) definido pela CMED. Neste grupo, foi possível identificar que alguns medicamentos têm seus preços definidos cerca de 150% superior ao menor preço encontrado no mercado.
Em relação às hipóteses levantadas, a primeira procurava considerar que se a regulação de preços realizada pela CMED, e aplicada no momento da entrada do novo fármaco no mercado, estimula a cadeia produtiva a seguir sua política, haveria duas possíveis situações. A inicial seria que se o preço CMED para produtos novos fosse significativamente maior que o preço praticado, haveria forte indício que a margem de lucro, que já é considerada pela CMED no momento da determinação de preço, mais do que compensa os esforços em desenvolvimento de novos produtos, daí a sugestão seria uma revisão da precificação.
Como houve casos em que a regulação definia preços que eram 80% superior ao praticado pelo mercado, conclui-se que essa hipótese está parcialmente confirmada. Além disso, ficou evidenciado que há agentes que não seguem a regulação, pois cobram valores até 16% superior ao do regulado. Logo, a segunda opção possível nessa situação em que se o preço CMED para produtos novos não é significativamente maior que o preço praticado, a precificação parece estar apropriada, foi rejeitada.
A segunda hipótese levantada para essa pesquisa foi que a regulação da CMED para produtos novos aplica métodos que não induzem as empresas a investir em P&D no Brasil, tanto as nacionais, como as empresas transnacionais, o que levantaria a discussão de que haja problemas na política de regulação econômica. Observou-se que 80% dos novos registros de princípios ativos da classe estudada são de origem estrangeira e há discussões levantadas por fabricantes nacionais de que a atual política favorece os produtos trazidos do exterior. Isso confirma parcialmente a hipótese levantada, já que a classe L está na fronteira do conhecimento e a tendência das empresas nacionais é, ainda, introduzirem preponderantemente inovações incrementais, que em geral não são patenteadas.
As principais limitações do trabalho foram: (i) utilizar uma classe terapêutica que apresenta características de alta concentração por empresas estrangeiras e que é fornecida, para a maioria dos pacientes que necessitam destes fármacos, pelo SUS. Isso gerou problemas na obtenção dos preços finais e nas comparações, pelo fato de haver produtos com restrição hospitalar que não possuem grande oferta e ainda tem seu PMC não divulgado; (ii) coletar apenas dados de preços finais de forma online e com grande concentração em um único ICMS, que pode apresentar variação em relação aos praticados nas lojas físicas; (iii) usar uma base de medicamentos divididas em dois grupos, que gera uma pequena amostra de fármacos para análise; (iv) usar como base somente três ciclos da regulação e ao retirar os dados dos sites das farmácias, os mesmos serem coletados em um único momento no tempo.
Os resultados encontrados revelam que a regulação econômica do setor farmacêutico não está alcançando seus objetivos institucionais de promover a concorrência, estimular o acesso aos medicamentos e inovação farmacêutica, principalmente para os medicamentos registrados como novos. Promover a concorrência no setor farmacêutico, torna-se essencial para a diminuição dos preços dos medicamentos em classes terapêuticas como a Classe L. Controlar o poder de mercado de alguns agentes do setor, que utilizam essa posição para obter lucros excessivos, via preços elevados e injustificáveis, fere os objetivos da implementação da Câmara de Regulação.
Espera-se que essa discussão possa levantar questões que gerem melhorias na definição das políticas públicas do setor farmacêutico, para que realmente se atinja o objetivo institucional da CMED. Ao longo de seu desenvolvimento e nas discussões realizadas neste trabalho ficou evidenciado que há diversas questões para serem analisadas na atual regulação econômica, principalmente na metodologia utilizada, que desconsidera as especificidades existentes no Brasil. Além disso, há a necessidade de se promover estudos regulares que verificam os impactos que as regulações exercem nos setores regulados, e possíveis atualizações a serem propostas para melhorar suas regras.


