Resumen: En las últimas décadas en Argentina se han incrementado notablemente los reportes de casos de erucismo, con algunos brotes de importancia epidemiológica. En diciembre de 2019, un vecino de la ciudad de Córdoba fue afectado por el contacto con orugas de una especie de Megalopyge Hübner, [1820] que se encontraban en un arbusto del arbolado urbano. Considerando la escasa información disponible sobre la familia en esta región del país y el riesgo sanitario potencial que podrían representar estas orugas, se propuso determinar la especie, describir su ciclo biológico y los estados inmaduros, y evaluar la potencialidad de utilización de especies hospedadoras alternativas. Los adultos y los estados inmaduros se asemejan más a los descriptos bajo el nombre de Megalopyge undulata vulpina Berg, 1882 que a cualquier otra especie del género. Sin embargo, algunas diferencias morfológicas y cromáticas conducen a proponer que se tratase de dos taxones afines pero diferentes. A la latitud de Córdoba la especie se comporta como bivoltina, con un tiempo promedio de embriogénesis de 6 días y 58 de desarrollo larval en la segunda generación. El tiempo de permanencia dentro del capullo fue muy variable. El escaso éxito en el intento de alimentar a las larvas con hospedadores alternativos indicaría que la especie no representaría, por el momento, un problema sanitario urbano emergente.
Palabras clave: Lepidoptera, Megalopyggidae, erucismo, fauna urbana, dermatitis, Argentina.
Abstract: During the last decades in Argentina, the cases of erucism have increased notably, with some outbreaks of epidemiological importance. In December 2019, a resident of the city of Córdoba reported a case of erucism caused by contact with caterpillars of Megalopyge Hübner, [1820] present in a shrub in the sidewalk. Taking into account the little information available in the literature about the family in general, and in this region of the country in particular, and the potential health risk that these caterpillars could represent, our goals were to know what species it is, to describe the immature stages and the development times of this species, and to evaluate the possibility of the caterpillars using some common tree species as alternative hosts. Adults and immatures reared in the laboratory are more similar to those described as Megalopyge undulatavulpina Berg, 1882 than any other species of the genus, but some morphological and chromatic differences lead to the proposition that these are two related but different taxa. According to our observations, at the latitude of Córdoba the species seems to be bivoltine, with an average embryogenesis time of 6 days and 58 days of larval development time for the second generation. The time spent inside the cocoon was highly variable. On the other hand, the limited success in the development of the larvae with the alternative hosts that we offered them would indicate that the species does not represent, at the moment, an emerging health problem.
Keywords: Lepidoptera, Megalopygidae, erucism, urban fauna, dermatitis, Argentina.
Artículos
Los estados inmaduros y el ciclo de vida de una Megalopyge Hübner, [1820] causante de dermatitis en la ciudad de Córdoba, Argentina (Lepidoptera: Megalopygidae)
Immature stages and life cycle of a Megalopyge Hübner, [1820] causing dermatitis in the city of Córdoba, Argentina (Lepidoptera: Megalopygidae)
Received: 15 September 2023
Accepted: 07 November 2023
Published: 30 June 2024
En las últimas décadas en Argentina, especialmente en las provincias de Misiones, Jujuy y Buenos Aires, se ha registrado un incremento en el reporte de casos de erucismo, hecho acompañado por el incremento de la población humana, la expansión de los centros poblados y la modificación de los ecosistemas silvestres (Gómez et al. 2018; Martínez et al. 2019). Los Lepidoptera responsables de la mayor parte de estos accidentes pertenecen a las familias Megalopygidae Herrich Schäffer, 1855, Saturniidae Boisduval, 1837 y Limacodidae Duponchel, 1844, con predominancia de las dos primeras (De Roodt et al. 2000; Martínez et al. 2019; Zapata, 2022).
La familia Megalopygidae, con más de 300 especies, constituye un grupo monofilético de distribución exclusivamente americana y mayor diversidad en la región Neotropical (Becker, 1995; Epstein et al. 1998; Heppner, 2008). Las orugas presentan una densa cubierta pilosa con dos tipos de cerdas. Las más largas, flexibles, a menudo pinnadas y de variados colores, les dan el aspecto velludo o cabelludo característico y son inofensivas. Las otras, cortas, rígidas y punzantes, con glándulas de veneno en la base y ocultas bajo las primeras, son las responsables de la acción urticante (Barth,1954; Stehr, 1987).
Si bien algunas especies de la familia Megalopygidae fueron descriptas a partir de material proveniente de Argentina entre fines del siglo XIX y principios del XX, los estudios realizados en el país sobre esta familia en los últimos 70 años son escasos. Las últimas sistematizaciones de información mencionan entre 10 y 15 especies incluidas en tres géneros: Megalopyge Hübner, [1820], Podalia Walker, 1856 y Norape Walker, 1855, algunas con determinación dudosa, cambios repetidos de género y muchas de biología desconocida (Cordo et al. 2004; Pastrana, 2004; Martínez et al. 2019). De los tres, Megalopyge es el de mayor riqueza, con entre seis y nueve especies (Cordo et al. 2004; Hayward, 1969; Pastrana, 2004).
Según la bibliografía, al menos ocho especies de Megalopyge serían polífagas, habiéndose encontrado orugas sobre diferentes especies de árboles y arbustos de una amplia variedad de familias (Cordo et al. 2004; Gómez, 2014; Hall, 2019; Hayward, 1969; Pastrana, 2004). Sin embargo, no siempre los registros reflejan las plantas hospedadoras de las que realmente se alimentan las orugas, sólo dónde ellas o sus capullos fueron encontrados (Hall, 2019). El conocimiento de los hábitos de vida y de las plantas hospederas espontáneas y potenciales de cada especie permitiría anticipar riesgos de encuentro y accidentes, y podría ser el punto de partida para la construcción de mapas epidemiológicos que sirvan para un programa de vigilancia en salud pública.
En diciembre de 2019, un vecino de la ciudad de Córdoba (Argentina) denunció por redes sociales el doloroso contacto accidental con unas orugas presentes en Punica granatum L. (Lythraceae), un arbusto del arbolado urbano conocido como granado. Las orugas fueron reconocidas por su aspecto como del género Megalopyge por A. Zapata, y los síntomas incluyeron una dermatitis ligera y una neuralgia aguda que se extendió por el miembro afectado, pero remitió espontáneamente a las pocas horas (Manuel Vázquez, com. pers).
De todas las especies y subespecies de Megalopyge, sólo de 12 son conocidos algunos de sus estados inmaduros y/o ciclos biológicos: M. albicollis (Walker, 1855) (Bourquin, 1941), M. amita (Schaus, 1900) (Bourquin, 1951, como M. lanceolata (Dognin, 1923)), M. braulio Schaus, 1924 (Diniz et al. 2013), M. chacona Schaus, 1920 (Bourquin, 1948; Orfila, 1967), M. dyari Hopp, 1935 (Martínez, 2022), M. hina (Dognin, 1911) (Sihezar, 2019), M. lanata (Cramer, 1780) (Bourquin, 1942), M. nuda (Stoll, 1780) (Dyar, 1928; Schreiter, 1943), M. opercularis (Smith, 1797) (Bishopp, 1923; Hall, 2019), M. undulata vulpina Berg, 1882 (Bourquin, 1945a, b), M. urens Berg, 1882 (Bourquin, 1936) y M. uruguayensis Berg, 1882 (Specht & Corseuil, 2008).
Considerando la importancia sanitaria que podría tener la especie de Megalopyge encontrada en Córdoba, se propuso indagar sobre su identidad, biología y su potencialidad de colonizar especies vegetales comunes del arbolado urbano.
Los adultos con los que se iniciaron los ensayos (Figura 1) se obtuvieron en febrero de 2020 a partir de orugas silvestres procedentes del sitio del incidente (31º 22’ 49’’ S, 64º 14’ 23’’O, 428 msnm), las que completaron su desarrollo en el laboratorio alimentadas con P. granatum. Las parejas se dispusieron en recipientes plásticos de 500 ml con tapa y papel tisú como sustrato para sujeción y oviposición. Los huevos (Figuras 2-3) fueron removidos diariamente, dispuestos dentro de cajas de Petri, y observados hasta la eclosión. En sendas cajas de Petri de 5 cm de diámetro con fondo de papel tisú, se dispusieron grupos de 10 orugas neonatas junto con hojas de P. granatum o de una de las cuatro especies vegetales alternativas en evaluación. La selección de estas se basó en especies de familias mencionadas como hospedadoras del género y que, a su vez, fueran especies frecuentes en el arbolado público de Córdoba (Plan Forestal de la Ciudad de Córdoba, 2018). Las elegidas fueron: Lagerstroemia indica (L.) Pers. (Lythraceae), Fraxinus pennsylvanica (Marshall) (Oleaceae), Ligustrum lucidum (L.) (Oleaceae) y Platanus x hispanica (Platanaceae). Se realizaron tres réplicas con cada una. Todas las cajas se mantuvieron a temperatura ambiente y fotoperiodo natural junto a un termómetro digital. Cada 48 horas se retiraron las mudas, se renovó el alimento y el papel, se contabilizó el número de orugas en cada estadio y se registraron las temperaturas máxima y mínima de los dos días previos. Cuando el desarrollo de los individuos lo requirió, se trasladó cada conjunto de larvas a contenedores plásticos de 500 cm3 para permitir el adecuado crecimiento y alimentación. Las mudas se almacenaron en seco en tubos Eppendorf y los individuos muertos fueron conservados en etanol al 70%. Los capullos se dispusieron en recipientes individuales rotulados por fecha de confección y con una tira de papel tisú que permitiera la sujeción de los adultos. Al emerger los imagos, se registró fecha y el sexo.

Las descripciones se realizaron a partir de ejemplares vivos y conservados con utilización de microscopio estereoscópico (Zeiss Stemi 508) y fotografías digitales (Nikon 5100, Axiocam ERc5s y Samsung Galaxy 2016). La nomenclatura utilizada es la propuesta por Stehr (1987) para las larvas y Mosher (1917) para las pupas. La longitud corporal de larvas (sin considerar los pelos) fue medida cuando éstas se disponían a mudar. Dimensiones inferiores a 5 mm fueron tomadas con ocular micrométrico, las mayores con regla. Los colores utilizados en la descripción se aproximan, por comparación visual a la codificacióm hexadecimal disponible en https://encycolorpedia.es (código entre paréntesis).
Huevo (Figuras 2-3): Color amarillo algo pálido (f3da0b), cilíndrico, con polos redondeados, adherido fuertemente al sustrato por un lateral o un polo con una sustancia cementicia ambarina. Corion con pequeñas depresiones dispersas sobre toda la superficie. Oviposturas unicapa de varias decenas de huevos, en general pegados en sentido longitudinal, uno al lado del otro, y cubiertos por escamas piliformes del abdomen de la hembra. Dimensiones: 1,21 ± 0,02 mm de longitud y 0,70 ± 0,02 mm de diámetro (n=10).
Larva: primer estadio (Figuras 4-5): tegumento beige amarillento (f3a505) uniforme, con una línea media dorsal longitudinal blanquecina entre T3 y A9. Forma general trapezoidal, con la región torácica notablemente más ancha que la caudal. En cada segmento, excepto en T1 y en A10, presenta verrugas dorsales, sub dorsales y laterales, del mismo color que el general, de las que emergen numerosas cerdas largas, pinnadas, flexibles y casi transparentes (pelos), y otras cortas, lisas, rígidas y más oscuras (espinas). T1 con dos verrugas dorsales aplanadas de las que emergen 6 pelos que se dirigen hacia anterior a modo de pestañas. Cabeza, patas torácicas y espuripedios del mismo color general. Cabeza siempre contra el sustrato, retraída dentro de T1 y ambos cubiertos por T2. A ventral de cada espiráculo se observa una protuberancia carnosa digitiforme. En A2 y A7 espuripedios inermes. Longitud: 2,68 ± 0,34 mm, rango: 2,2-3 mm (n=5).
Segundo estadio (Figura 6): similar al primero con mayor abundancia y longitud de las cerdas, especialmente los pelos en la zona media del cuerpo, cuyos extremos distales pueden doblarse hacia posterior. Longitud: 4,00 ± 0,14 mm; rango: 3,8-4,2 mm (n=5).
Tercer estadio (Figura 7): cubierta pilosa de color beige anaranjado algo apagado (ecd886), que cubre por completo el tegumento claro y oculta las espinas. Se destacan tres manojos de pelos más largos que el resto, flexibles y ondulados, uno dorsal y dos laterales, que surgen en la parte interna de las verrugas dorsales y subdorsales entre A3 y A5. Los manojos laterales se rizan hacia posterior. Cabeza castaña (804000) con stemmata y mandíbulas negras. Patas torácicas castañas. Longitud: 6,58 ± 0,43, rango: 6-7 mm (n=5).
Cuarto estadio (Figura 8): tegumento como en los estadios anteriores. Pelos de color como en el estadio anterio cerca del tegumento y más anaranjados en el ápice de los más largos. Los tres manojos de pelos largos observados en la etapa anterior se destacan aún más, con ápices curvados o enrulados. Presenta otros dos manojos largos, uno dirigido hacia anterior desde la zona media de T2 y otro dirigido hacia posterior desde la zona media de A9. En A5-A8 los pelos que surgen de las verrugas dorsales hacia la línea media y los dorsales de las verrugas subdorsales presentan sus extremos distales alineados y sus puntas blanquecinas comienzan a insinuar tres líneas longitudinales de guiones. Cabeza y patas torácicas como en el estadio anterior. Longitud: 8,40 ± 0,89; rango: 8-10 mm (n=5).
Quinto estadio (Figura 9): tegumento beige muy claro. Color de la cubierta pilosa muy variable entre individuos, desde un beige anaranjado algo apagado (ecd886), hasta un castaño cobrizo (a25e2a) y, en algunos ejemplares, con sectores o casi completamente negra. Los manojos de pelos largos se vuelven más rígidos y el dorsal, como una cresta, es más compacto y con las puntas dirigidas hacia posterior. Casi todas las puntas de los pelos son blancas, pero en los dorsales de las verrugas dorsales y subdorsales el sector blanco se extiende hasta casi la mitad por lo que las líneas de guiones dorsal y laterales observadas en el estadio anterior se vuelven más conspicuas. Longitud: 12,6 ± 0,55; rango: 12- 13 mm (n=5).
Sexto estadio: se observaron dos fenotipos, uno muy similar en aspecto al estadio anterior, con los pelos de la cresta dorsal curvados hacia posterior, y otros con los pelos completamente rectos (Figuras 10-12). Mientras las que presentaron el primero mudaron una vez más, las que presentaron el segundo tejieron su capullo al finalizar el desarrollo. Coloración muy variable desde beige anaranjado claro apagado (ecd886) marrón oscuro (5b3a29) o rojo ladrillo (9b111e), con las hileras de guiones blancos dorsal y laterales bien marcadas. En muchos ejemplares se observaron zonas de pelos negros en el margen de T2-T3 contra el sustrato, y en el manojo que se dirige hacia anterior. Longitud de los individuos que pasaron al estadio siguiente: 16,4 ± 2,19 mm; rango: 15-20 mm (n=5).

Séptimo estadio (último): similar en aspecto y variación de color que en el estadio anterior. Cresta dorsal sólo con pelos rectos. Longitud: 20,6 ± 2,19 mm; rango: 18-23 mm (n=5).
La oruga neonata se alimenta desde el mismo momento del nacimiento comenzando con el corion y continuando con las hojas. Durante los tres primeros estadios roe o raspa la superficie foliar, especialmente la inferior, mientras que a partir del cuarto estadio mastica completamente la lámina, comenzando por los bordes, sujetando a la hoja con los segmentos torácicos a modo de pinza. Se desplazan lentamente y la cabeza queda, casi todo el tiempo, protegida por los segmentos torácicos. La alimentación es solitaria. En ocasionales encuentros con sus congéneres no se observaron comportamientos de agresión o canibalismo. Cada proceso de ecdisis, en general, no supera las 24 horas. Al completar su desarrollo cada individuo busca un espacio protegido, preferentemente sobre alguna rama, en donde confecciona el capullo.
Capullo (Figuras 13-15): al finalizar su desarrollo, la larva de último estadio confecciona un capullo de color beige grisáceo (898176), forma ahusada y, en general, adosado a lo largo de una rama. En la parte media dorsal, a la altura de donde se encontraba la cresta dorsal, se destaca una protuberancia. Bajo la capa superficial y tenue, se encuentra una segunda capa de un tejido más denso y resistente, entretejido con los pelos de la oruga. Esta segunda capa es redondeada a posterior y roma en la parte anterior, zona que quedará obliterada por una tapa u opérculo de seda. Dicho opérculo será desplazado por el adulto y en él quedará retenida la exuvia pupal. Dimensiones: externa 20 ± 2 mm x 8 ± 0,1 mm; interna 15 ± 2 mm x 8 ± 0,2 mm (n=5).
Pupa (Figura 14): exarada. Color general beige amarillento (dc9d00), abdomen más claro. Segmentos abdominales 4-6 móviles. Tergos abdominales con bandas anteriores de espinas pequeñas. Cremáster reducido a un parche de ganchos en A10. Dimorfismo sexual en las ceratotecas y muescas genitales. Dimensiones: 11 ± 1,2 mm x 5 ± 0,2 mm (n=5).
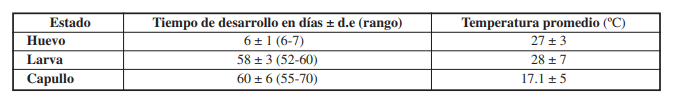
Los tiempos medios, mínimos y máximos de desarrollo de los estados inmaduros alimentados con granado y la temperatura diaria media promedio se resumen en la Tabla I. No se registraron diferencias entre los tiempos de permanencia en el capullo de individuos machos y hembras, por lo que se proporciona un valor único para el estado. No se verificó el momento exacto de la muda a pupa dentro del capullo, por lo que se informa el tiempo de permanencia dentro de capullo.
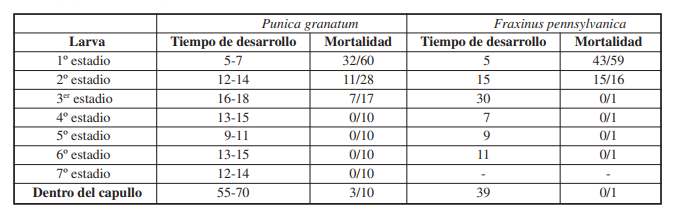
En la mayoría de los ensayos, a excepción de las alimentadas con P. granatum, al colocar las larvas de primer estadio sobre las hojas, éstas comenzaron a deambular de forma continua. En ocasiones, algunos individuos rasparon las hojas ofrecidas, pero la mayoría las evitaron y se desplazaron hacia la tapa del recipiente en un evidente comportamiento de huida. La mortalidad en todos los casos fue alta, produciéndose el deceso de la mayoría de los individuos en un rango de entre 7 y 15 días. En L. indica, P. x hispanica y L. lucidum el 100% de las larvas de primer estadio murieron por inanición. En P. granatum y F. pennsylvanica, algunas orugas lograron completar el desarrollo, con una temperatura promedio de 28ºC durante el estado larval (52-60 días en P. granatum y 77 días en F. pennsylvanica) y 17ºC durante el estado pupal. Los tiempos de desarrollo promedio y la mortalidad por estadio en los casos en los que el desarrollo se completó se resumen en la Tabla II. Al haberse producido una mortalidad elevada, las proporciones se indican sobre el total de individuos y no como promedio por grupo.
Los adultos de la especie de Megalopyge estudiada en el presente trabajo (Figura 1) son muy similares en envergadura alar, forma y patrón de diseño a los de M. undulata vulpina, M. opercularis y M amita (Bourquin, 1945b; Hopp,1934), pero más cercanos a los de la primera por los colores. Debido a que los adultos de este género en general son variables, se descaman fácilmente y las descripciones originales se basan principalmente en el diseño de las alas, sería necesario comparar en directo los tipos, o ejemplares de la misma procedencia, estudiar las estructuras genitales de todas y realizar análisis moleculares para dilucidar si todas son especies válidas y si la aquí estudiada es alguna de las ya descriptas. En Buenos Aires, Argentina, Bourquin describió el ciclo de una especie de Megalopyge a partir de huevos de un ejemplar capturado en El Tigre (Bourquin, 1945a, b). Esa especie fue inicialmente determinada por Köhler como M. uruguayensis Berg (Bourquin, 1945a) pero, posteriormente, Bourquin (1945b) publicó su ciclo de vida como M. undalata vulpina, con determinación de Schaus. Teniendo en cuenta las descripciones disponibles, así como la distribución, se consideró que la determinación como Megalopyge cf. undulata vulpina sería la más apropiada hasta que se revise la taxonomía del género.
El huevo (Figuras 2-3) es similar en aspecto, dimensiones y disposición durante la ovipostura que el de las otras especies del género de las que se conoce este estado (Bishopp, 1923; Bourquin, 1936, 1941, 1942, 1945b, 1951; Hall, 2019). El tiempo que demoró en promedio la embriogénesis de esta segunda generación en Córdoba (6 días, Tabla I), fue similar al tiempo reportado para M. opercularis (seis a ocho días, Bishopp, 1923) y M. undalata vulpina (seis días, Bourquin, 1945b), y aproximadamente la mitad que el de M. albicollis (13 días, Bourquin, 1941), M. lanata (14 días, Bourquin, 1942) y M. urens (14 días, Bourquin, 1936), mientras que M. amita tendría un valor intermedio (10 días, Bourquin, 1951). Diferentes factores podrían explicar estas diferencias, entre ellos, el número de generaciones anuales que puede desarrollar cada especie, la época del año en se realizaron los registros y la temperatura a la que se produjo el desarrollo. Así, mientras la mayoría de las especies con ciclo conocido serían bivoltinas, M. urens, quien presenta el tiempo de embriogénesis más prolongado, sólo tendría una generación anual. Por otra parte, en todas las especies en las que los tiempos fueron más prolongados, los registros se realizaron a fines de la primavera o comienzos del verano. Habría que conocer el tiempo de embriogénesis de la primera generación en las especies bivoltinas cuyo tiempo conocido es el de la segunda generación, para establecer si este fuese una característica propia de estas especies o las condiciones de fotoperíodo y/o temperaturas tendrían una influencia mayor en esta etapa del desarrollo.
Durante el desarrollo larval se registraron entre seis y siete estadios, con una morfología general similar a la de M. undalata vulpina (Bourquin, 1945a, b), aunque de ella sólo se informan entre cinco y seis estadios, igual que en M. opercularis (Bishopp, 1923). En los Lepidoptera no es inusual que el número de estadios larvales sea fluctuante, especialmente en camadas de larvas que se desarrollan durante otoño, llegando incluso a confundirse el número efectivo de estadios, como en M. opercularis (Bishopp, 1923). En general, se ha encontrado que las especies del género presentan entre cinco y nueve estadios larvales, con mayor número en aquellas con tiempo de desarrollo larval activo más prolongado y que presentan mayores dimensiones en el estado adulto, como M. albicollis (Bourquin, 1941) y M. urens (Bourquin, 1936).
Las larvas de la especie estudiada muestran características propias de la familia, como la presencia de espuripedios inermes en A2 y A7, y la retracción de la cabeza dentro del primer segmento torácico (Epstein, 1996). También la presencia de una protuberancia digitiforme glandular debajo de cada espiráculo (= sencilla digitada según Epstein, 1996). A semejanza de M. amita (Bourquin, 1951), M. opercularis (Bishopp, 1923; Hall, 2019) y M. undalata vulpina (Bourquin, 1945a, b), las orugas en los últimos estadios son cromáticamente variables (Figuras 9 a 12), lo que contrasta con la uniformidad de los primeros estadios (Figuras 4 a 8). Otra característica notable es la aparición de una cresta dorsal de pelos largos (Figuras 7 a 12), algo también observado en M. amita (Bourquin, 1951), M. opercularis (Bishopp, 1923; Hall, 2019) y M. undalata vulpina (Bourquin, 1945a, b). Sin embargo, mientras en M. opercularis la cresta es continua, incluyendo tórax y abdomen, en M. amita, M. undalata vulpina y las larvas estudiadas, dicha cresta se presenta solo en la región media (A2-A4). Por otra parte, si bien las orugas ilustradas y descriptas como de M. nuda por Stoll (1791) guardan cierta semejanza en cuanto a la presencia de cresta dorsal media elevada, en la misma no se observa el manojo de pelos largos hacia anterior y, por la descripción, parecería muy similar a la larva de M. uruguayensis cuya imagen aparece en Specht & Corseuil (2008). Un aspecto diferente muestra la oruga descripta por Dyar (1928), que se corresponde con la descripta e ilustrada por Schreiter (1943) bajo el nombre de M. nuda, y el de M. chacona (Bourquin, 1948; Orfila, 1967) que no presentan cresta dorsal, sino una densa cubierta de pelos claros aplanados sobre el cuerpo y dirigidos hacia posterior. Por su parte, las larvas de M. albicollis (Bourquin, 1941), M. braulio (Diniz et al., 2013) y M. dyari (Martínez, 2022) exhiben una densa cubierta pilosa con pelos muy largos y de aspecto esponjoso, que recubren todo el cuerpo y se unen en la línea media, mientras que las de M. hina serían más cortos, pero igualmente parejos y esponjosos (Sihezar, 2019). Realizando una comparación morfológica general de todo el estado larval, la especie estudiada se asemeja más a M. undalata vulpina (Bourquin, 1945a, b) que a cualquier otra especie del género con ciclo biológico conocido. A pesar de ello, es posible señalar algunas diferencias consistentes entre ambas. En primer lugar, y aunque puede ser subjetivo, el color de la larva de primer estadio, descripto como amarillo rojizo en M. undalata vulpina, mientras que las observadas durante el presente trabajo fueron siempre beige amarillento con una línea dorsal blancuzca (Figuras 4-5). Otra diferencia mucho más llamativa se documentó a partir del quinto estadio: las orugas estudiadas presentaron tres hileras de manchas blancas correspondientes a la mitad apical de los pelos de las verrugas dorsales A6-A9 y subdorsales A6-A8 (Figuras 10-12), mientras que en M. undalata vulpina se mencionan e ilustran sólo en los correspondientes a las de las verrugas subdorsales de tales segmentos (Bourquin, 1945b).
Si bien el tiempo de desarrollo larval total (Tabla I) fue similar al publicado sobre otras especies del género, fue notablemente más extenso que el reportado para la más semejante, M. undalata vulpina (35 días, Bourquin, 1945b). Quizás las condiciones artificiales de luz y temperatura a las que Bourquin sometió a sus larvas a fin de mantenerlas vivas pudieron modificar en el ritmo natural de desarrollo, ya que no estuvieron expuestas a las variaciones diarias naturales. Sin embargo, al haberlas mantenido a una temperatura media inferior respecto a la registrada en el presente trabajo (24,7 ºC vs. 28 ºC), se esperaría que el ciclo fuese más extenso y no más corto. En virtud de haber obtenido el desarrollo completo de una única larva en fresno, no es posible analizar la existencia de diferencias en el tiempo de desarrollo utilizando diferentes hospedadores. La elevada mortalidad de los primeros estadios larvales en crías en cautiverio es algo también mencionado en otras especies del género (Bishopp, 1923; Bourquin, 1936, 1942).
En lo que se refiere al comportamiento de alimentación, es habitual en las orugas del género que durante los primeros estadios las larvas sólo raspen la superficie foliar, mientras que los últimos mastican las hojas desde los bordes, ingiriéndolas en su totalidad o apenas respetando la nervadura central. Lo que varía según las especies es el estadio en el que la larva deja de raspar y comienza a masticar. Esto ocurriría más temprano en las especies con menor número de estadios larvales como M. opercularis (Bishopp, 1923), M. undalata vulpina (Bourquin, 1945b) y la aquí estudiada, que lo hicieron en cuarto, mientras que M. amita (Bourquin, 1951), M. lanata (Bourquin, 1942) y M. urens (Bourquin, 1936) con ocho estadios, lo hicieron en el quinto. Por su parte, en M. albicollis, que presenta nueve estadios, las orugas empiezan a masticar la hoja completa recién en el séptimo (Bourquin, 1941). Sin embargo, como las especies hospedadoras utilizadas en todos los casos fueron diferentes, no se puede descartar que características anatómicas de ellas, como dureza o pubescencia puedan también condicionar este comportamiento de alimentación.
En cuanto a la forma de construir el capullo, pegado a lo largo de una rama, y su aspecto general, con una región anterior roma y tapada con un opérculo, es similar a todas las especies del género en las que se lo conoce. Sin embargo, por su forma ahusada (Figura 13), se parece más a los de M. opercularis (Bishopp, 1923; Hall, 2019), M. undalata vulpina (Bourquin, 1945a, b), M. dyari (Martínez, 2022) y M. amita (Bourquin, 1951) que al resto, cuya forma es mucho más ovoide (Bourquin, 1936, 1941, 1948; Orfila 1967; Schreiter, 1943; Specht & Corseuil, 2008). Una característica llamativa en los capullos de la especie estudiada es una saliente en la parte media, correspondiente con la región más alta de la cresta en la oruga. Esta particularidad es compartida con los capullos de M. opercularis (Bishopp, 1923; Hall, 2019), M. undalata vulpina (Bourquin, 1945a, b) y M. dyari (Martínez, 2022), característica mucho más pronunciada en esta última.
La pupa de la especie estudiada también presenta las características típicas de la familia. Como indica Mosher (1917), podo, cerato y pterotecas se encuentran separadas entre sí y del resto del cuerpo, y los segmentos abdominales 4 a 6 son móviles. Cuando el imago emerge por la boca del capullo empujando el opérculo, la exuvia queda parcialmente retenida, observándose particularmente separadas las ceratotecas (Figura 15), como se ha ilustrado en otras especies del género (Bishopp, 1923; Bourquin, 1936, 1941, 1942, 1945b, 1951; Hall, 2019; Schreiter, 1943). Por otra parte, como en M. undalata vulpina (Bourquin, 1945b), la pieza vítrea del ojo es del mismo color beige amarillento del resto del tegumento, a diferencia de las pupas de M. albicollis (Bourquin, 1941), M. amita (Bourquin, 1951) y M. opercularis (Bishopp, 1923; Hall, 2019), en las que dicha pieza es de color negro. Sin embargo, a diferencia de M. u. vulpina, las pterotecas son castañas en lugar de pardinegras (Figura 14). En cuanto a la permanencia dentro del capullo, en la generación de otoño se observaron tanto individuos no invernantes como invernantes. El tiempo mínimo en los individuos no invernantes (55 días) fue algo superior que el registrado en pupas equivalentes de M. opercularis (41 días, Bishopp, 1923), mientras que el tiempo máximo (70 días) fue inferior al mínimo registrado para M. u. vulpina (88 días, Bourquin, 1945b). Asimismo, el tiempo mínimo de permanencia en el capullo de la especie estudiada fue aproximadamente el mismo que los de la primera generación de M. albicollis (43 días, Bourquin, 1941) y M. lanata (55 días, Bourquin, 1942), pero superior al mínimo de la primera generación de M. amita (30 días, Bourquin, 1951) y de M. opercularis (28 días, Bishopp, 1923). Sin dudas, las condiciones ambientales de temperatura y fotoperíodo, no siempre informadas en la bibliografía, condicionan la permanencia en este estado. Registros ocasionales de la primera generación de la especie encontrada en Córdoba (Zapata, obs. pers.), sugieren que el tiempo de permanencia dentro del capullo en ésta es inferior al mínimo registrado en la segunda generación.
En cuanto a la evaluación de utilización de hospedadoras alternativas, el éxito fue escaso. La imposibilidad de completar el ciclo con una de las especies hospedadoras espontáneas utilizada por Bourquin (1945a, b) para criar a M. undalata vulpina (Platanus x hispanica referido como P. orientalis) es otro de los aspectos en los que se diferencian. Esto sugiere que la especie en cuestión tiene una preferencia diferente a la criada por Bourquin y no sería ampliamente polífaga como M. opercularis, una de las especies del género con mayor registro incidentes dermatitógenos en el continente americano (Hall, 2019). Sin embargo, habría que identificar cuál o cuáles son sus hospedantes naturales, para considerar cuán amplia podría ser su dieta y, por extensión, cuál podría ser el riesgo potencial de encuentros con estas larvas.
En síntesis, la especie de Megalopyge encontrada en la ciudad de Córdoba, Argentina, cuyo ciclo y estados inmaduros se describen aquí, presenta dos generaciones anuales, con un período amplio de permanencia en estado de larva durante la época cálida (octubre-abril) y pasa el invierno como larva de último estadio y pupa dentro de un capullo sedoso y resistente. Por las características de los adultos es una especie próxima a M. undulata vulpina, M. opercularis y M. amita. Si bien parecería más semejante a la primera mencionada, existen diferencias consistentes entre las larvas y pupas que permiten diferenciarlas. Sería necesaria la realización de una revisión taxonómica del género. Respecto al aspecto sanitario, si bien las larvas permanecen en el ambiente durante la mayor parte de la estación cálida y su contacto puede producir cuadros de dermatitis local y neuralgia, esta especie mostró en laboratorio escasa afinidad por las especies comunes del arbolado urbano evaluadas. Además de indagar sobre cuál o cuáles podrían ser los hospedadores naturales, habría que considerar también la posibilidad de que otras especies arbóreas o arbustivas comunes pudieran servir como hospedantes alternativos y, en tal caso, la presencia de las orugas pudiera volverse un problema sanitario.
Al Sr. Manuel Vázquez, quien facilitó el acceso a los ejemplares con los que se inició el trabajo. A la cátedra de Introducción a la Biología (FCEFyN UNC) por el espacio físico e instrumental utilizado. Este trabajo fue subsidiado por SECyT- Universidad Nacional de Córdoba.
* Autor para la correspondencia / Corresponding author: E-mail: adrzapata@unc.edu.ar



