Artículos
Efectos del cambio climático antropogénico en la distribución potencial del género Pronophila Doubleday, [1849] en Colombia (Lepidoptera: Satyrinae, Pronophilina)
Effects of anthropogenic climate change on the potential distribution of the genus Pronophila Doubleday, [1849] in Colombia (Lepidoptera: Satyrinae, Pronophilina)
Efectos del cambio climático antropogénico en la distribución potencial del género Pronophila Doubleday, [1849] en Colombia (Lepidoptera: Satyrinae, Pronophilina)
Shilap Revista de Lepidopterología, vol. 52, no. 208, pp. 737-759, 2024
Sociedad Hispano-Luso-Americana de Lepidopterología
Received: 15 April 2021
Accepted: 20 January 2024
Published: 30 December 2024
Resumen: El género Pronophila Doubleday, [1849] pertenece a la subtribu Pronophilina (Nymphalidae: Satyrinae) y se encuentra distribuido desde el noroeste de Argentina hasta el extremo norte de Colombia y el noreste de Venezuela, y con tan solo un representante en Centroamérica. No obstante, aún se desconocen varias características sobre la historia natural del género. Adicionalmente, diferentes procesos de perturbación antrópica han ocasionado una variación climática acelerada en los últimos años, afectando los patrones de distribución y diversidad de diferentes taxones, como es el caso de las especies del género Pronophila en Colombia, dado a que la región Andina ha sido una de las zonas más afectadas por estas actividades antrópicas en las últimas décadas. Por esta razón, el objetivo del presente estudio fue generar un modelo de distribución potencial para las especies de Pronophila en el país ante diversos escenarios de cambio climático para los años 2050 y 2070, y realizar una comparación con un modelo de distribución potencial reciente, para poder evaluar el efecto del cambio climático en la distribución del género Pronophila en el país. La proyección de los diferentes modelos se realizó en el software R usando el algoritmo MaxEnt. Los resultados demostraron que las cuatro especies de Pronophila empleadas en el modelamiento experimentaron reducciones en sus áreas de distribución potencial en los años 2050 y 2070. Finalmente, los resultados de este estudio pueden usarse para desarrollar estrategias de conservación que mitiguen la disminución de la población y las extinciones locales predichas por el cambio climático antropogénico en Lepidoptera asociados con ecosistemas montañosos del país.
Palabras clave: Lepidoptera, Satyrinae, Pronophilina, distribución geográfica, MaxEnt, temperatura, Antropoceno, región Andina, Colombia.
Abstract: The Pronophila Doubleday, [1849] genus, belonging to the Pronophilina subtribe (Nymphalidae: Satyrinae), is distributed from northwest Argentina to the extreme north of Colombia and northeast Venezuela, with only one representative in Central America. However, much about the natural history of the genus is still unknown. Additionally, anthropogenic disturbances have caused accelerated climate change, affecting different taxa’s distribution and diversity patterns, including species of the Pronophila genus in Colombia due to the Andean region being one of the most affected areas by such activities in recent decades. Therefore, this study aimed to generate a potential distribution model for Pronophila species in the country under various climate change scenarios for the years 2050 and 2070. A comparison was also made with a recent potential distribution model to evaluate the effect of climate change on the genus’ distribution in the country. The R software was used with the MaxEnt algorithm to project different models. The results showed that the four Pronophila species used in the modeling experienced reductions in their potential ranges in the years 2050 and 2070. Lastly, the study’s results can be used to develop conservation strategies that mitigate population declines and local extinctions of Lepidoptera associated with the mountainous ecosystems of the country.
Keywords: Lepidoptera, Satyrinae, Pronophilina, geographic distribution, MaxEnt, temperature, Anthropocene, Andean region, Colombia.
Introducción
El Antropoceno, es considerada la época en donde se está evidenciando las mayores tasas de extinción de especies a nivel mundial ( Haraway, 2015; Equihua et al. 2016; Turvey & Crees, 2019; Cometti, 2020; Spalding & Hull, 2021). Las implicaciones de la pérdida de biodiversidad y la degradación de los ecosistemas son potencialmente tan graves para los seres humanos como para otras especies ( He & Silliman, 2019; Turvey & Crees, 2019). Adicionalmente, los diversos ecosistemas proporcionan una variedad de servicios ecosistémicos de regulación, y aprovisionamiento, incluido la captación de carbono, el reciclaje de nutrientes y la polinización, y representan la base de las economías, los medios de vida y la salud global, y millones de personas dependen directamente de sistemas naturales como ríos, bosques, mares, manglares, etc., para obtener alimentación, agua, recursos medicinales, culturales, y protección contra eventos ambientales extremos como lo es el cambio climático acelerado o antropogénico ( Turvey & Crees, 2019).
Por su parte, el cambio climático antropogénico, es considerado como uno de los principales fenómenos que genera efectos negativos en la biodiversidad ( Cheng & Bonebrake, 2017; Turvey & Crees, 2019). El cambio climático contemporáneo se reconoce en gran medida como un fenómeno antropogénico que comenzó y se sustenta en actividades industriales humanas que producen enormes cantidades de emisiones de gases de efecto invernadero (ej. CO2 y metano). A su vez, las crecientes concentraciones atmosféricas de gases de efecto invernadero han desencadenado una serie de rápidos cambios fisicoquímicos en el aire, la tierra y el mar ( He & Silliman, 2019), y se pronostica que el cambio climático antropogénico será la principal causa de extinción de especies en las próximas décadas ( Gaitán-Espitia & Hobday, 2020).
El cambio climático natural y antropogénico puede inducir a las especies a contraer o ampliar sus áreas de distribución, con evidencias del pasado histórico y reciente ( Carvalho et al. 2019; Gaitán-Espitia & Hobday, 2020), dado a que la alteración de los patrones de temperatura y precipitación pueden favorecer o restringir el área de distribución de una especie, puesto que el clima es uno de los principales factores que regulan el espacio geográfico de los individuos ( Russo & Kohlmann, 2013; Maciel-Mata et al. 2015; Carvalho et al. 2019). A su vez, se resalta que la temperatura y la precipitación pueden generar cambios adaptativos en las especies ( Uribe, 2015; Locatelli & Kanninen, 2010), puesto que, éstas tienden a adaptarse a la variación de las condiciones climáticas, y así pueden evitar la extinción respondiendo a los efectos del cambio climático como lo han hecho en el pasado (ej. migración, ajustes etológicos, morfológicos y fisiológicos). Sin embargo, no todas las especies responden de la misma manera ( Declerck & Decker, 2009; Gaitán-Espitia & Hobday, 2020), y los cambios en la idoneidad del hábitat junto con la velocidad sin precedentes de los cambios climáticos proyectados limitarán estas posibles respuestas, aumentando los riesgos de extinción ( Gaitán-Espitia & Hobday, 2020).
Por otra parte, las diferentes especies también pueden sufrir cambios de nicho, de modo que el nicho climático actual cambie para incorporar nuevas condiciones climáticas a través, por ejemplo, de la plasticidad fenotípica ( Gaitán-Espitia & Hobday, 2020). Estas respuestas plásticas son mecanismos importantes mediante los cuales los organismos maximizan su aptitud en ambientes heterogéneos, facilitando la persistencia de poblaciones naturales al ampliar la tolerancia a las condiciones ambientales ( Fox et al. 2017; Donelson et al. 2019). Aunque la plasticidad proporciona un mecanismo de adaptación al cambio climático, es poco probable que proporcione una solución a largo plazo a los desafíos que enfrentan las especies que experimentan cambios ambientales direccionales continuos, como lo es el caso del calentamiento global ( Gaitán-Espitia & Hobday, 2020).
Tanto la fauna como la flora de los Andes son muy vulnerables al cambio climático antropogénico ( Cuesta et al. 2012; Herzog et al. 2012; Gonda, 2020), y siendo una de las regiones biogeográficas que concentra una alta biodiversidad y endemismos a nivel mundial ( Särkinen et al. 2011; Mahecha et al. 2019), se hace necesario realizar estudios del impacto del cambio climático antropogénico en las diferentes especies que habitan en los Andes. Los lepidópteros son uno de los grupos más diversos, representando 157.424 especies descritas a nivel mundial, y son uno de los grupos de insectos más utilizados como bioindicadores ecológicos para medir los efectos de las actividades antropogénicas ( Miller et al. 2011). También se consideran vitales para los servicios ecosistémicos debido a diversas funciones, como plagas agrícolas, alimento para diversos organismos, polinizadores nocturnos y diurnos ( Dar & Jamal, 2021).
En ecosistemas Andinos de montaña, el grupo de lepidópteros dominante, en términos de riqueza y abundancia, son los Satyrinae (Nymphalidae), en especial los Pronophilina ( Mahecha et al. 2019; Olarte-Quiñones et al. 2021; Díaz-Suárez et al. 2022), los cuales presentan patrones de distribución altitudinales y geográficos muy específicos ( Pyrcz et al. 2007; Viloria, 2008). Se reconocen aproximadamente 45 géneros y más de 600 especies de las cuales el 95% se encuentran principalmente en los Andes tropicales entre Venezuela y el norte de Argentina ( Pyrcz et al. 2020; Olarte-Quiñones et al. 2021). Los Pronophilina exhiben diferentes patrones de distribución altitudinal en muchos casos restringidos a sistemas montañosos aislados que forman ‘islas continentales’, además de varios complejos de especies crípticas ( Pyrcz et al. 2016; Mahecha et al. 2019; Mahecha-J. et al. 2021). La mayoría de las especies de Pronophilina se encuentra relacionadas a ecosistemas templados húmedos o ecosistemas fríos como lo son los bosques andinos nublados, altoandinos y páramos, en donde se pueden encontrar las diferentes plantas hospederas y nutricias, como por ejemplo el género Chusquea Kunth (Poaceae), conocidas comúnmente como chusque o bambú de montaña y otras gramíneas ( Montero & Ortiz, 2013; Olarte-Quiñones et al. 2021; Díaz-Suárez et al. 2022).
El género Pronophila Doubleday, [1849], perteneciente a la subtribu Pronophilina, se distribuye desde el noroeste de Argentina (Tucumán) hasta el extremo norte de Colombia (Sierra Nevada de Santa Marta - SNSM) y el noreste de Venezuela (Turimiquire), con tan sólo un representante en las montañas de Centroamérica ( Pronophilatimanthes Salvin, 1871). Normalmente, las especies de Pronophila habitan los bosques montanos entre 1.000-3.000 msnm., registrando el máximo de diversidad alrededor de los 2.000 a 2.400 msnm. Para Colombia se registra una especie endémica para la SNSM ( Pronophila julianiAdams & Bernard, 1977) ( Pyrcz, 2000; Pyrcz, 2004). Los adultos de Pronophila presentan una amplia envergadura alar (8-10 cm) en comparación a otras especies de Pronophilina, y el dimorfismo sexual es poco marcado, siendo las hembras ligeramente más grandes que los machos, y con un diseño alar más claro. Los estadios larvales son aún desconocidos, pero se infiere que su planta hospedera podría tratarse del chusque de montaña, aunque se ha evidenciado en Ecuador, que Pronophila unifasciata Lathy, 1906 se puede alimentar de bambúes secundarios diferentes al chusque ( Pyrcz, 2004). El género Pronophila presenta una taxonomía estable y su sistemática es más conocida, a diferencia de otros géneros de Pronophilina como Pedaliodes Butler, [1867] ( Pyrcz, 2004; Pyrcz et al. 2019), reportándose para Colombia cinco (5) especies de las diecisiete (17) especies reportadas para el Neotrópico (Pyrcz, 2000, 2004) ( Figura 1). Por tal motivo, el género Pronophila es un buen modelo biológico para realizar estudios sobre los efectos del cambio climático antropogénico en ambientes de montaña, debido a que las especies de montaña a menudo ocupan nichos climáticos específicos, frecuentemente combinados con una alta especialización ecológica, lo que las hace altamente sensibles a los cambios ambientales ( Rödder et al. 2021).

Figura 1.
Especies que componen el género Pronophila para Colombia. A) P. juliani, B) P. unifasciata, C)P. epidipnis, D)P. orcus, E)P. intercidona. Fotos por Pyrcz.
Por lo tanto, el objetivo principal del presente estudio consistió en evaluar el efecto del cambio climático antropogénico en el género Pronophila, a través de modelos de distribución potencial. Para tal fin, se estableció la distribución potencial reciente de las especies pertenecientes al género Pronophila para Colombia, con base en la distribución actual. Posteriormente, a partir de los modelos de distribución potencial recientes, se proyectaron modelos de distribución en escenarios de cambio climático RCP 4,5, 6,0 y 8,5 para los años 2050 y 2070 respectivamente. Para la realización de los modelos de distribución de las especies, se utilizó el algoritmo MaxEnt, el cual presenta ventajas cuando sólo se tienen datos de presencia de la especie e incluso con una pequeña presencia de conjunto de datos, puede ofrecer resultados fiables y estables ( Elith et al. 2006; Phillips et al. 2006; Hijmans & Graham, 2006; Benito & Peñas, 2007; Romo et al. 2013; Anand et al. 2021). Además, para evaluar el efecto del cambio climático antropogénico sobre la idoneidad del hábitat de especies con hábitats estrechos, la predicción adecuada del hábitat y el mapeo de la distribución de las poblaciones son fundamentales ( Anand et al. 2021).
La predicción planteada en la presente investigación es que se espera que las especies del género Pronophila, exhiban una disminución en sus áreas de distribución potencial futura, observándose los efectos más severos bajo el escenario RCP 8.5 para ambos años 2050 y 2070, puesto que las emisiones y concentraciones de gases de efecto invernadero en este escenario aumentan exponencialmente con el tiempo ( Riahi et al. 2011; IPCC, 2013). En los resultados encontrados se evidenció una reducción de la distribución potencial en los diferentes escenarios de cambio climático tanto para el año 2050 y 2070 para las diferentes especies de Pronophila. Finalmente, el presente estudio permite contribuir al conocimiento de los patrones de distribución de este grupo de especies en los bosques Andinos en el país y el efecto del cambio climático antropogénico sobre estos patrones geográficos. Además, los resultados de este estudio pueden emplearse para desarrollar estrategias de conservación que mitiguen la disminución de la población y las extinciones locales predichas por el cambio climático antropogénico en lepidópteros asociados con ecosistemas montañosos del país.
Materiales y métodos
RECOPILACIÓN DE DATOS
La revisión taxonómica y recopilación de los datos asociados a las especies del género Pronophila se llevó a cabo en tres fases: La primera fase consistió en una revisión de las Colecciones Científicas Nacionales e Internacionales como: El Instituto de Ciencias Naturales ICN de la Universidad Nacional de Colombia; Museo Historia Natural de la Universidad de los Andes en Colombia (ANDES-E); Instituto Alexander von Humboldt IAVH en Colombia; Colección de Artrópodos y otros invertebrados (CAUD-216) de la Universidad Distrital Francisco José de Caldas (UDFJC) en Colombia; y la colección de Jagiellonian University, Kraków, Polonia (CEPUJ).
La segunda fase consistió en realizar salidas de campo a los lugares en los cuales no había reportes de las especies que componen al género pero que se presumía debería estar por las condiciones tanto altitudinales como bióticas. Los muestreos se realizaron entre los meses de enero a diciembre del año 2018-2019. Las recolectas se efectuaron empleando métodos activos y pasivos estandarizados para el estudio de lepidópteros ( Andrade et al. 2013; Freitas et al. 2021). En los métodos pasivos, se usaron trampas Van Someren Rydon (VSR) empleando como cebo pescado en descomposición y una mezcla de melaza, cerveza y fruta madura (banano, piña y papaya), los cuales son recomendados para mariposas Pronophilina ( Pyrcz et al. 2013; Díaz-Suárez et al. 2022)
En la tercera fase, se realizó una búsqueda en bases de datos especializadas en registros de biodiversidad tales como: el Fondo de información sobre biodiversidad global (GBIF, http://www.gbif.org) y SiB-Colombia ( https://biodiversidad.co/), como también se consultaron diversas publicaciones sobre Pronophila con el propósito de extraer los registros geográficos de las especies para Colombia.
ARREGLO SISTEMÁTICO
Para la determinación taxonómica de las diferentes especies que conforman el género Pronophila para Colombia, se emplearon caracteres autapomórficos de cada especie como lo son patrones alares, patrones de coloración, genitales de macho y hembra. Para la extracción de los genitales, se realizó lo propuesto por Andrade et al. (2013) y se siguió el arreglo sistemático propuesto por Pyrcz (2004). El proceso de determinación taxonómica se realizó en la Universidad Distrital Francisco José de Caldas, y los ejemplares se depositaron en la colección entomológica Museo de Historia Natural de la Universidad Distrital en la Colección de Artrópodos y otros invertebrados (CAUD-216) en Bogotá, Colombia.
MODELACIÓN DE LA DISTRIBUCIÓN POTENCIAL
El paquete dismo ( Hijmans et al. 2017), mediante el programa R versión 4.2.3 ( R Development Core Team, 2023), se utilizó para ejecutar el algoritmo MaxEnt versión 3.4.1 ( Phillips et al. 2006), el cual es ampliamente utilizado en investigaciones para predecir las distribuciones potenciales (SDM) de fauna y flora con gran precisión con un número mínimo de conjuntos de datos actuales para especies de rango limitado ( Phillips et al. 2006; Gebrewahid et al. 2020; Anand et al. 2021; Li et al. 2020).
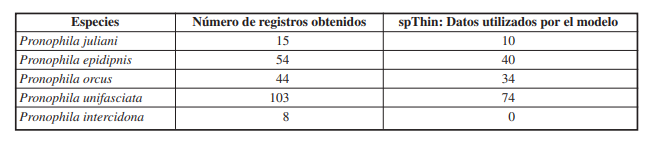
Los modelos de distribución potencial se proyectaron a partir de los datos de distribución geográfica recopilados para cada especie de Pronophila reportadas para Colombia ( Figura 2), los cuales se importaron a Microsoft Excel y se guardaron en formato “CSV”. Se uso el paquete spThin en R para realizar la reducción espacial de los registros de ocurrencia de las especies de Pronophila, para disminuir los problemas asociados con los sesgos de muestreo espacial, puesto que, la reducción elimina la menor cantidad de registros necesarios para disminuir sustancialmente los efectos del sesgo de muestreo y, al mismo tiempo, retiene la mayor cantidad de información útil ( Aiello-Lammens et al. 2015). Por tal razón, sólo se emplearon en el estudio cuatro de las cinco especies de Pronophila reportadas para Colombia ( P. unifasciata Lathy, 1906, P. juliani Adams & Bernard, 1977, P. epidipnis Thieme, 1906 y P. orcus (Latreille, [1813])), y no se consideró la especie P. intercidona Thieme, 1907 debido a la escasez de datos de presencia, lo cual no permitía realizar una buena proyección de la distribución potencial reciente y futura ( Tabla I).
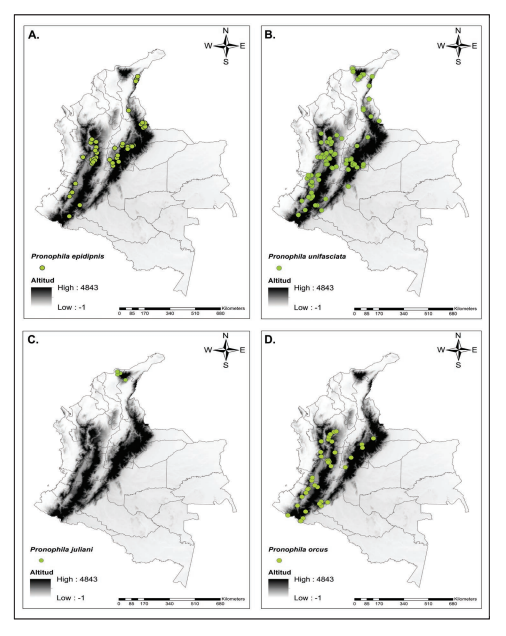
Figura 2.
Distribución de las especies del género Pronophila para Colombia a partir de los datos recopilados. a) P. epidipnis. b)P. unifasciata. c) P. juliani. d)P orcus. Círculos verdes representan la presencia de cada una de las especies para el país. No se incluye a P. intercidona.
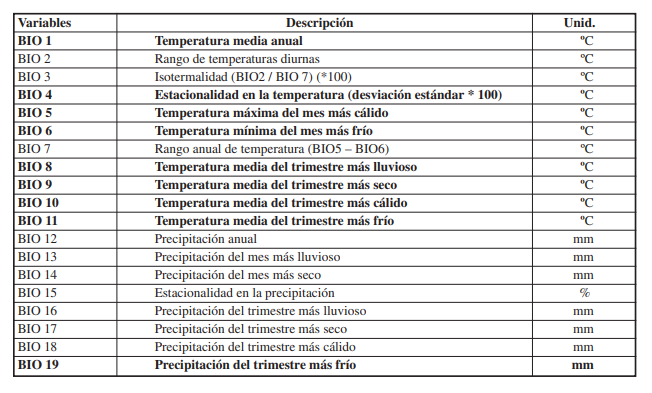
En la proyección de los modelos se emplearon las 19 variables bioclimáticas disponibles en WorldClim versión 2.1 ( Tabla II) ( Hijmans et al. 2005; www.worldclim.org), las cuales son el promedio de las precipitaciones y temperaturas para los años 1970 al 2000. Las capas con las variables bioclimáticas presentaron una resolución espacial de aproximadamente 1 km2 (30 segundos), con el propósito de tener datos con mejor resolución en la modelización (Varela et al. 2015; Gebrewahid et al. 2020). Posteriormente, se calculó el coeficiente de correlación de Pearson para examinar la correlación cruzada entre las 19 variables climáticas mediante el programa R versión 4.2.3 ( R Development Core Team, 2023), para evitar la multicolinealidad que puedan resultar en un sobreajuste del modelo ( Wang et al. 2018; Gebrewahid et al. 2020; Du et al. 2021). Por lo tanto, sólo se emplearon variables con correlaciones bajas (|r| < 0.8) para disminuir el fenómeno de sobreajuste y mejorar la precisión de las pruebas ( Elith et al. 2010; Gebrewahid et al. 2020). Acorde a los análisis de correlación entre las 19 variables, se seleccionaron solo nueve variables bioclimáticas para los análisis: BIO1, BIO4, BIO5, BIO6, BIO8, BIO9, BIO10, BIO11 y BIO19 ( Tabla II).
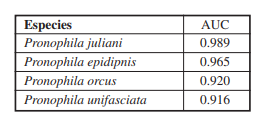
Para determinar la confiabilidad de los diferentes modelos obtenidos, se usó la prueba de AUC, que de acuerdo con Phillips et al. (2006), el grado de confiabilidad del modelo se evalúa teniendo en cuenta un AUC en donde 0 es el mínimo y 1 el máximo grado de confiabilidad ( Fielding & Bell, 1997). Las puntuaciones AUC pueden dividirse en cinco categorías ( Swets, 1988; Gebrewahid et al. 2020), un AUC < 0.5 describe modelos que son menos que aleatorios y rara vez ocurren en la realidad y un AUC de 0.5 es una suposición pura. Por lo tanto, el rendimiento del modelo se clasifica como fallido (0.5 a 0.6), malo (0.6 a 0.7), razonable (0.7 a 0.8), bueno (0.8 a 0.9) y excelente (0.9 a 1) ( Gebrewahid et al. 2020). Para los términos de este estudio, se manejó un valor de AUC por encima de 0.85, para considerar un modelo viable ( Quesada-Quirós et al. 2016; Gebrewahid et al. 2020). Se utilizó la prueba Jackknife (excluyendo sistemáticamente cada variable) para evaluar las variables ambientales dominantes que determinaron la distribución potencial de cada especie, siendo una variable influyente en el modelo cuando presenta un AUC > 0.8 ( Xianli et al. 2018). El modelo se parametrizó utilizando un número máximo de 10.000 puntos de fondo (background points), 500 iteraciones y un umbral de convergencia de 0.00001. Se utilizaron los tipos de características de bisagra, producto, lineal y cuadrática para abordar la complejidad del modelo, y el sobreajuste se controló utilizando el valor de regularización predeterminado de uno ( Rajpoot et al. 2020).
MODELAMIENTO EN ESCENARIOS DE CAMBIO CLIMÁTICO
El algoritmo MaxEnt se utilizó para predecir la distribución potencial en tres periodos: reciente, 2050 (2041-2060) y 2070 (2061-2080). Una vez obtenidos los mapas de distribución potencial recientes para cada especie de Pronophila, se realizaron las proyecciones futuras usando el modelo climático CMIP5 propuesta por la IPCC (2014), el cual se basa en los Modelos de Circulación General (GCM) el cual fue adoptado por la quinta evaluación del Panel Gubernamental para el Cambio Climático (IPCC, 2013; 2014). Estos modelos abarcan una gama de configuraciones ambientales, ciclo del carbono, condiciones atmosféricas, oceánicas y un sistema dinámico de la tierra con vegetación, el cual permite calibrar y corregir los modelos climáticos futuros ( Bellouin et al. 2011; Olson et al. 2021). El clima simulado por estos modelos depende en parte de la concentración atmosférica asumida de gases de efecto invernadero, y los “escenarios de emisiones” describen las concentraciones atmosféricas futuras proyectadas de gases de efecto invernadero ( Romero-Centeno et al. 2016). Por lo tanto, el clima proyectado para un período determinado en el futuro depende del modelo y el escenario de emisión utilizado, así como de la ejecución del modelo, debido a que cada ejecución es diferente ya que el clima es en parte un fenómeno estocástico ( Bellouin et al. 2011; Romero-Centeno et al. 2016).
Por lo tanto, se empleó el modelo HadGEM2-AO (Lee et al. 2010; Baek et al. 2013), perteneciente al modelo GCM. HadGEM2-AO incluye componentes ‘físicos’ que consisten en la atmósfera, el océano, el hielo marino con hidrología, un esquema de intercambio de superficie, el recorrido de los ríos y los procesos de aerosoles, además, tiene en cuenta las celdas de Hadley ( Martín et al. 2011; Baek et al. 2013; Rajpoot et al. 2020). Por tal motivo, se recomienda su uso para proyectar distribuciones futuras de especies en zonas tropicales (Duran et al. 2016). Dentro del modelo HadGEM2-AO, se encuentran las cuatro trayectorias RCPs, las cuales corresponden a escenarios prescritos para gases de efecto invernadero ( Baek et al. 2013; Jubb et al. 2013; Wei et al. 2018; Rajpoot et al. 2020). Consiguientemente, se modelaron los escenarios RCP 4.5, RCP 6.0 (escenarios intermedios) y RCP 8.5 (escenario extremo), con el fin de comparar el área de distribución potencial de las especies de Pronophila, y con ello determinar la variabilidad respecto a los diferentes escenarios RCPs ( Taylor et al. 2012; Baek et al. 2013; Jubb et al. 2013; Wei et al. 2018; Rajpoot et al. 2020).
COMPARACIÓN DISTRIBUCIÓN POTENCIAL RECIENTE VS. DISTRIBUCIÓN POTENCIAL FUTURA
La comparación del área potencial reciente con la distribución futura para cada una de las especies de Pronophila, se hizo mediante el programa ArcGIS versión 10.5 ( ESRI, 2016). La comparación se realizó tomando como base los mapas de distribución potencial reciente y el de los diferentes escenarios de cambio climático. Los resultados promedio de “Cloglog” se convirtieron en mapas binarios que muestran la idoneidad e inadecuación climática empleando una regla de umbral del percentil 10 de presencia de entrenamiento ( Rajpoot et al. 2020), y se proyectaron los cambios en los valores de distribución potencial con la finalidad de evaluar la reducción o ampliación en la distribución potencial ( Stranges et al. 2019) de las especies de Pronophila en Colombia.
Resultados
DISTRIBUCIÓN POTENCIAL RECIENTE
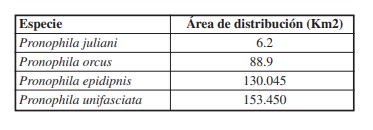
Se obtuvieron un total de 224 ocurrencias para las cuatro especies de Pronophila en Colombia, siendo las especies P. unifasciata, P. orcus y P. epidipnis las especies con mayor número de registros ( Tabla I). Adicionalmente, se corrobora la presencia de la especie P. intercidona para Colombia, en especial para la zona sur de la cordillera oriental. Se observó que P. epidipnis y P. unifasciata, presentaron un área de distribución potencial amplia a lo largo de las tres cordilleras del territorio colombiano (Figuras 3- 4), seguido de P. orcus ( Figura 5). Por su parte, P. juliani, exhibió un área de distribución potencial reducida, exclusiva para la SNSM ( Tabla III) ( Figura 6). Las diferentes proyecciones mostraron valores altos de AUC, que oscilan entre 0.91 y 0.98 ( Tabla IV).
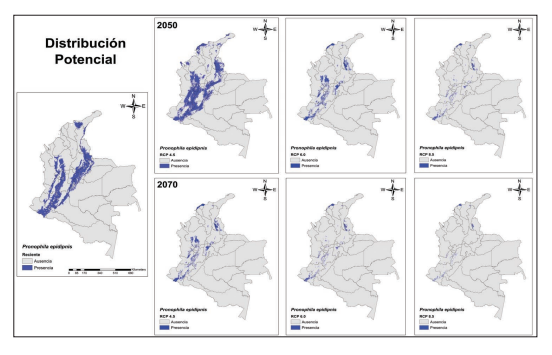
Figura 3.
Distribución potencial de la especie P. epidipnis en diferentes escenarios de cambio climático para Colombia.
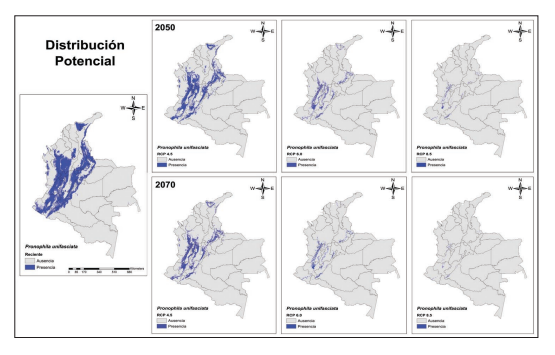
Figura 4.
Distribución potencial de la especie P. unifasciata en diferentes escenarios de cambio climático para Colombia.
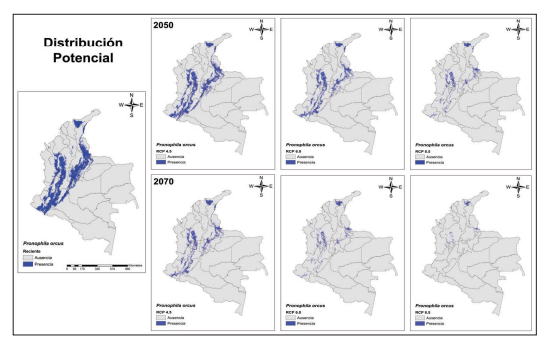
Figura 5.
Distribución potencial de la especie P. orcus en diferentes escenarios de cambio climático para Colombia.
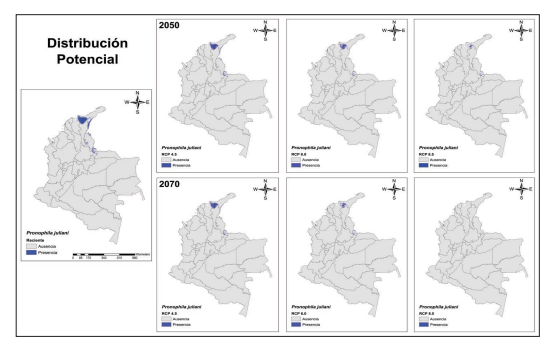
Figura 6.
Distribución potencial de la especie P. juliani en diferentes escenarios de cambio climático para Colombia.
DISTRIBUCIÓN POTENCIAL FUTURA
Los resultados muestran que las cuatro especies de Pronophila podrían experimentar una reducción sustancial en sus áreas de distribución potencial futura (2050-2070), puesto que, se aprecia una pérdida generalizada del área potencial de ocupación en relación con la distribución potencial reciente, siendo la especie P. juliani las más afectada ( Tabla V). A su vez, se evidenció que P. juliani presentó el mayor porcentaje de perdida de distribución potencial en todos los RCPs para los años 2050 y 2070 en comparación con las otras especies de Pronophila ( Tabla VI). Adicionalmente, se observa que para el RCP 8.5, tanto para el año 2050 y 2070, todas las especies de Pronophila tenderán a perder más del 92 % de la distribución potencial. Los resultados permiten inferir que, la distribución potencial de las especies de Pronophila empleadas se verán fuertemente afectadas por el cambio climático antropogénico en el año 2070, sin importar el escenario RCP ( Tabla VI). Por lo tanto, por medio de las proyecciones realizadas sobre la distribución potencial del género Pronophila para el año 2050 y 2070, se logra evidenciar el efecto negativo del cambio climático antropocéntrico sobre la distribución potencial de estas especies en el país.
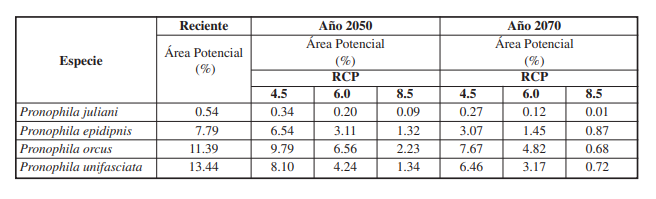
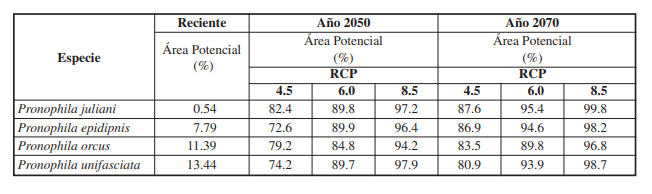
Porcentaje de pérdida de distribución potencial bajo los tres escenarios de cambio climático para los años 2050 y 2070 en las especies del género Pronophila en Colombia.
VARIABLES BIOCLIMÁTICAS
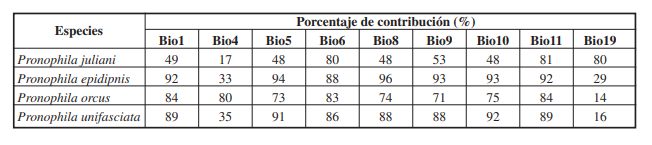
Las variables bioclimáticas empleadas en los modelos de distribución potencial reciente y futuro (2050-2070) para las cuatro especies de Pronophila, en su mayoría estaban asociadas a la temperatura. Adicionalmente, se evidencia que para P. juliani, las variables climáticas que influyeron en el modelo fueron BIO6, BIO11 y BIO19, siendo esta última, la única variable asociada a la precipitación. Para las especies P. epidipnis y P. unifasciata, las variables con mayor contribución fueron BIO1, BIO5, BIO6, BIO8, BIO9, BIO10, y BIO11, y para P. orcus fueron BIO1, BIO4, BIO6, y BIO11 ( Tabla VII).
Discusión
Los resultados encontrados en este estudio afirman la predicción planteada, en donde las especies del género Pronophila, se verían afectadas de manera negativa en su área de distribución potencial por efectos del cambio climático antropogénico. El estadístico de evaluación del modelo muestra que el AUC está por encima de 0.9 en todos los modelos, permitiendo inferir que las proyecciones son confiables y por ende viables ( Araujo et al. 2005; Laurente, 2015; Xianli et al. 2018). Para determinar el AUC, es preciso tener un número de presencias mínimas de hasta 15 individuos ( Mateo et al. 2011), este valor se ajustó para las especies P. orcus, P. unifasciata, P. epidipnis. Sin embargo, este número puede ser menor si se trata de una especie de distribución restringida ( Peterson et al. 2008), tal es el caso de P. juliani, considerada una especie endémica de la SNSM ( Pyrcz, 2004; Mahecha et al. 2019), y cuyos datos recopilados no fueron los suficientes, lo que puede explicar las sobreestimaciones o sobreajustes del modelo para esta especie (Elith et al. 2010; 2011; Gebrewahid et al. 2020). Además, esto se debe a que el modelo solo considera variables climáticas, pero no variables de estructura del paisaje como barreras biogeográficas, y teniendo en cuenta que las especies están restringidos a elevaciones específicas (Kattan, 2000), esto puede tener influencia en la predicción de la distribución futura de las especies ( Hickling et al. 2006; Romo et al. 2013).
La evaluación de los modelos permitió reafirmar la predicción de que las especies del género Pronophila, van a verse altamente perjudicadas debido a las variaciones en la temperatura y precipitación, conllevando a una disminución en las áreas de distribución potencial futuras ( Romo et al. 2013; Maciel-Mata et al. 2015). Las especies de Pronophila mostraron tener una ocupación espacial muy restringida, en especial P. juliani, asociada a la cordillera de los Andes, registrando su máxima frecuencia alrededor de los 2.000 a 2.400 msnm ( Pyrcz, 2004). Así mismo, estas zonas coinciden con áreas de mayor diversidad de especies de montaña para Colombia, donde a medida que aumenta la altitud, en las especies de Pronophilina suele aumentar la tasa de endemismo, a diferencia de otras especies de Nymphalidae ( Viloria et al. 2010; Pyrcz et al. 2009; Zenker et al. 2015; Mahecha et al. 2019).
Teniendo en cuenta la restricción ecológica de las especies de Pronophila (Pyrcz, 2004), la influencia de los RCPs, tuvieron una importante influencia en la distribución de las especies, pues como bien lo mencionan autores como Fleishman et al. (1999), Merrill et al. (2008), y Romo et al. (2013), al variar las condiciones climáticas, las distribuciones de las especies estudiadas pueden modificarse. En ese sentido, los aumentos de emisiones de CO 2 conllevarían al aumento de la temperatura promedio global ( Lovejoy, 2008), y al analizar cuáles fueron las variables que más inciden en la distribución futura de las especies, se encontró que en su mayoría son aquellas que están asociadas a la temperatura. La temperatura parece entonces el principal factor selectivo que actúa sobre la fisiología y etología de los Lepidoptera ( Clench, 1966; Wickman, 2009). Además, los efectos del cambio climático antropogénico sobre la biodiversidad son especialmente visibles en las zonas montañosas, donde las especies ocupan nichos climáticos específicos, frecuentemente combinados con una alta especialización ecológica, lo que las hace altamente sensibles a los cambios ambientales ( Rödder et al. 2021), conllevando posiblemente a extinciones locales ( Beniston et al. 1997; Hawkins et al. 2003; Mahecha-J. et al. 2011; Romo et al. 2013; Advani et al. 2019).
Los resultados aquí expuestos coinciden con lo propuesto por Romo et al. (2013), Nieto-Sánchez et al. (2015), Molina-Martínez et al. (2016), quienes evaluaron las respuestas de las comunidades de Lepidoptera a la variación climática, y destacan que la temperatura y la precipitación influencian la distribución de los Lepidoptera de alta montaña. Las variables climáticas de influencia para este estudio concuerdan con lo reportado por Romo et al. (2013), quienes evaluaron los efectos del cambio climático en Lepidoptera del género Boloria Moore, 1900 y priorizaron la influencia de la temperatura sobre este grupo, puesto que la variación en la temperatura puede modificar el ciclo de vida de los Lepidoptera, alternado su tasa de desarrollo, afectando la colonización de nichos, lo cual repercute en la distribución geográfica ( Kocsis & Hufnagel, 2011; Rödder et al. 2021), como bien se evidencia en los resultados obtenidos en el presente estudio. Lo anterior también coincide con lo propuesto por Peterson (2003), Lemoine et al. (2007), Laurente (2015), y Rödder et al. (2021), quienes mencionan que el cambio climático es determinante en la pérdida del hábitat, y por consiguiente puede afectar los patrones de distribución de las especies en general de flora y fauna.
Por otro lado, el aumento de la temperatura, también implica el estrés hídrico que vulnera la planta hospedera ( Chusquea spp.), en donde las especies, en su mayoría de Pronophilina, depende para su alimentación, metamorfosis y reproducción, y debido a su alta relación ecológica con dichas plantas pertenecientes a la familia Poaceae ( Pyrcz & Wojtusiak, 2002; Greeney et al. 2009; Mahecha-Jiménez et al. 2011; Montero & Ortiz, 2012; 2013), podrían estos Lepidoptera presentar afectación en su área de distribución. Cabe mencionar que el potencial hídrico foliar de las Poaceae depende de la disponibilidad del agua en el suelo y de la eficiencia de transporte del agua a través de su tejido vascular ( James et al. 2002), así mismo, dicha familia de plantas para Colombia se encuentra en rangos de temperatura que van desde los 14ºC ( Añazco, 2013). En ese sentido valdría la pena ahondar en el ciclo de vida de las especies de Pronophila, para analizar los efectos de los diferentes escenarios de cambio climático antropogénico junto con las plantas hospederas y así lograr un análisis holístico que explique la variación del área de distribución potencial de las especies.
De la misma manera, la pérdida del área de distribución de las especies del género Pronophila evidenciada en los resultados, puede deberse a que estos Lepidoptera presentan, como otras especies de elevaciones altas, melanismo térmico ( García-Pérez et al. 2007; Nevé & Després, 2020), y en la etapa de imago son activos cuando hace más calor (Robledo-García et al. 2002). Teniendo en cuenta lo anterior, las variables bioclimáticas constantes para las cuatro especies de Pronophila fueron: Temperatura mínima del mes más frio (BIO6) y Temperatura promedio del trimestre más frío (BIO11), las cuales son variables que están sujetas a temperaturas bajas, ello condiciona la actividad de vuelo de estas especies, ya que estas están fuertemente restringidas por la temperatura externa (Nevé & Després, 2020), puesto que los fuertes fríos y las corrientes heladas interfieren en el libre tránsito de los Lepidoptera, ya que los músculos torácicos de su tejido locomotor, presentan las tasas metabólicas de masa más altas que se conocen ( Dudley, 2000). Lo anterior coincide con lo propuesto por Cormont et al. (2011), con la especie de alta montaña de la subfamilia Satyrinae Coenonympha pamphilus (Linnaeus, 1758), donde el viento frio tuvo un efecto negativo en su locomoción.
Basados en los resultados obtenidos, otras de las variables con importante incidencia en las especies estudiadas fueron la temperatura máxima del mes más cálido (BIO5), temperatura promedio del trimestre más seco (BIO9) y temperatura promedio del trimestre más cálido (BIO10). Con base en esta información, se puede inferir que estas variables están relacionadas con la escasez de agua en época de calor, tiempo en el cual las especies del género Pronophila posiblemente se encuentren en etapa de reproducción, como sucede con Pedalidoes cocytia (C. Felder & R. Felder, [1867]) y Lymanopoda schmidti Adams, [1986], especies que habitan en alta montaña en Colombia ( Moreno & Ortiz-Pérez, 2012). A su vez, el agua es esencial para la reproducción de los Lepidoptera, ello podría afectar la posibilidad de intercambio de material genético entre los individuos que componen el género, puesto que la no disponibilidad del recurso hídrico puede ocasionar una reducción significativa de la fecundidad y fertilidad ( Torres-Vila et al. 1996). Por otro lado, la variable bioclimática precipitación del trimestre más frío (BIO19), tuvo únicamente influencia en la especie P. juliani, porque presenta un rango de distribución más estrecho que el resto de las especies, esto es porque hay pocos datos de presencia de la especie, por lo cual el software toma la variable, como un referente bioclimático único y se considera como un posible sesgo del modelo (Varela et al. 2014).
Las proyecciones realizadas para los años 2050 y 2070 bajo escenarios de cambio climático antropogénico para el género Pronophila, muestran algunas regiones habitables que coinciden con la distribución potencial reciente, aunque, se debe reconocer que es un grupo altamente sensible a los efectos del cambio climático, fenómeno que posiblemente genere cambios adaptativos a futuro. Basados en esto, se puede inferir que las variaciones climáticas pueden influenciar la aceleración del ciclo de vida de las especies por el aumento de la temperatura corporal, que a pesar de que puede aumentar la tasa de supervivencia, podría disminuir en los adultos la masa corporal y la tasa de fertilidad, disminuyendo el número de descendientes ( Kocsis & Hufnagel, 2011). Sin embargo, es importante destacar que los patrones de distribución de las especies asociadas a proyecciones bajo escenarios de cambio climático, deben ser interpretadas teniendo en cuenta la autoecología de los individuos/especies ( Laurente, 2015), ya que las predicciones en el tiempo pueden sobreestimar el comportamiento descendente de la distribución, al no considerar algunas variables ecológicas que quizá le permitan a las especies adaptarse a nuevas condiciones en las que han sido tradicionalmente observadas ( Lamont & Connell, 1996; Peterson, 2001; Mestres et al. 2015). Desde el punto de vista de la conservación es una situación preocupante, puesto que se predice que para el año 2070, habrá una reducción en la distribución de las especies de Pronophila en toda la región Andina colombiana. Por lo tanto, es importante determinar si esta reducción de las áreas potenciales de distribución predicha por los modelos, permiten plantear un plan de monitoreo enfocado al género Pronophila, y aplicar medidas de seguimiento de estas especies particularmente sensibles, y si estas tendencias se confirman, proceder con la implementación de procedimientos más drásticos a fin de prevenir la desaparición de estas especies, como por ejemplo la ubicación de áreas protegidas en los Andes que amortigüen el cambio climático antropogénico.
Con el fin de aumentar la posibilidad de predecir y prevenir los efectos del cambio climático antropogénico sobre los ecosistemas de montaña a corto y largo plazo, será necesario continuar realizando estudios que permitan conocer cada vez más y mejor la respuesta de las especies ante las variaciones climáticas. En este caso, valdría la pena, como ya se mencionó, realizar el estudio utilizando otras variables no consideradas en el presente trabajo como por ejemplo: el modelamiento de las plantas hospederas del género, o variables históricas, como barreras biogeográficas que puedan tener influencia sobre su distribución, también sería viable probar dichos modelos en campo, con el fin de validar la información contenida en la presente investigación. Así mismo, se debe reconocer que la mitigación de las variaciones de la temperatura y precipitación que devienen del cambio climático ya no es suficiente ( Locatelli et al. 2009), es necesaria la estructuración de estrategias de adaptación climática ( Gaitán-Espitia & Hobday, 2020; Rödder et al. 2021), que permitan generar incluso zonas de protección asociadas a mitigar los efectos de este fenómeno en las especies del género Pronophila, y que puedan servir como amortiguadores contra el cambio climático antropogénico ( Lobos, 2011). Además, debido a su distribución restringida, como el caso de P. juliani, y a su susceptibilidad a las variaciones de temperatura y precipitación, se hace necesario el seguimiento de las poblaciones del género Pronophila, con el fin de comprobar que no varíe drásticamente su área de distribución a lo largo del tiempo.
En términos generales, para ecosistemas del bosque Andino, el cambio climático antropogénico se considera como una amenaza para las especies de alta montaña, alterando sus patrones de distribución, por influencia de la variación de la temperatura y la precipitación, como se evidenció en el género Pronophila. Las cuatro especies estudiadas en la presente investigación del género Pronophila sufren una importante reducción de su área de distribución potencial, siendo la especie endémica P. juliani la de mayor afectación. Se determinó que las variables bioclimáticas de mayor influencia dentro de las diferentes proyecciones recientes y futuras son aquellas relacionadas con la temperatura, las cuales, acorde a nuestros resultados, restringen a futuro la distribución de las especies del género Pronophila en los Andes colombianos. Se evidencia así mismo, que bajo los tres escenarios de cambio climático (RCPs) utilizados en la presente investigación, existe una pérdida generalizada de la distribución potencial de las especies del género Pronophila, en proyección a los años 2050 y 2070, siendo sus efectos más severos en el escenario RCP 8.5. Finalmente, la información aquí presentada es de utilidad en términos de gestión de áreas protegidas, específicamente en la gestión y control del riesgo asociado a cambio climático antropogénico en ecosistemas de montaña, pues al puntualizar la posible extinción local de especies bioindicadores, es posible definir prioridades para un adecuado manejo y control. Por lo anterior, la gestión integral de emisiones de gases efecto invernadero, asociados al cambio climático antropogénico, debe enfocarse en la ampliación de áreas protegidas, que permitan la mitigación de éste en los hábitats de montaña en Colombia.
Agradecimientos
Al Proyecto “NCN grant Harmonia-10 2018/30/M/NZ8/00293 Evolutionary biogeography and diversification of the predominantly Andean butterfly subtribe Pronophilina (Nymphalidae, Satyrinae) based on phylogenetic data generated using modern molecular methods”, del Nature Education Centre de la Universidad Jagiellonian (Polonia) por el financiamiento del estudio. A todos los directores y conservadores de las diferentes colecciones revisadas a nivel nacional e internacional. A los docentes de la Maestría Manejo, Uso y Conservación del Bosque de la Universidad Distrital Francisco José de Caldas (Colombia), y a los familiares y amigos de la primera autora por su apoyo incondicional.
Referencias
Anand, V., Oinam, B., & Singh, I. H. (2021). Predicting the current and future potential spatial distribution of endangered Rucervus eldii eldii (Sangai) using MaxEnt model. Environmental Monitoring and Assessment, 193(3), 147.
Advani, N., Parmesan, C., & Singer, M. (2019). Takeoff temperatures in Melitaea cinxia butterflies from latitudinal and elevational range limits: a potential adaptation to solar irradiance. Ecological Entomology, 44(3), 389-396. https://doi.org/10.1111/een.12714
Aiello-Lammens, M., Boria, R., Radosavljevic, A., Vilela, B., & Anderson, R. (2015). spThin an R package for spatial thinning of species occurrence records for use in ecological niche models. Ecography, 38(5), 541-545. https://doi.org/10.1111/ecog.01132
Andrade-C., M. G., Henao-Bañol, E. R., & Triviño, P. (2013). Técnicas y procesamiento para la recolección, preservación y montaje de mariposas en estudios de biodiversidad y conservación (Lepidoptera: Hesperioidea - Papilionoidea). Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales, 37(144), 311325 https://doi.org/10.18257/raccefyn.12
Añazco, M. (2013). Estudio de vulnerabilidad del bambú (Guadua angustifolia) al cambio climático en la costa del Ecuador y norte Perú. Proyecto “Optimización de viviendas de bajo costo de bambú, una estrategia para adaptarse al cambio climático”. Unión Europea - Red Internacional del Bambú y Ratán.
Araujo, M. B., Thuiller, W, Williams P. H., & Reginster, I. (2005). Downscaling European species atlas distributions to a finer resolution: implications for conservation planning. Global Ecology and Biogeography, 14, 17-30. https://doi.org/10.1111/j.1466-822X.2004.00128.x
Baek, H. J., Lee, J., Lee, H. S., Hyun, Y. K., Cho, C., Kwon, W. T., & Lee, J. (2013). Climate change in the 21st century simulated by HadGEM2-AO under representative concentration pathways. Asia-Pacific Journal of Atmospheric Sciences, 49, 603-618. https://doi.org/10.1007/s13143-013-0053-7
Bellouin, N., Collins, W. J., Culverwell, I. D., Halloran, P. R., Hardiman, S. C., Hinton, T. J., & Roberts, M. J. (2011). The HadGEM2 family of met office unified model climate configurations. Geoscientific Model Development, 4(3), 723-757. https://doi.org/10.5194/gmd-4-723-2011
Beniston, M., Diaz, H. F., & Bradley, R. S. (1997). Climatic change at high elevation sites: an overview. Climatic Change, 36, 233-252. https://doi.org/10.1023/A:1005380714349
Benito, B., & Peñas, J. (2007). Aplicación de modelos de distribución de especies a la conservación de la biodiversidad en el sureste de la Península Ibérica. GeoFocus. Revista Internacional de Ciencia y Tecnología de la Información Geográfica, 7(7), 100-119.
Carvalho, S. B., Torres, J., Tarroso, P., & Velo-Antón, G. (2019). Genes on the edge: A framework to detect genetic diversity imperiled by climate change. Global Change Biology, 25(12), 4034-4047.
Cheng, W., & Bonebrake, T. C. (2017). Conservation effectiveness of protected areas for Hong Kong butterflies declines under climate change. Journal of Insect Conservation, 21(4), 599-606. https://doi.org/10.1007/s10841-017-9998-7
Clench, H. K. (1966). Behavioural thermoregulation in butterflies. Ecology, 47, 1021-1034. https://doi.org/10.2307/1935649
Cormont, A., Malinowska, A. H., Kostenko, O., Radchuk, V., Hemerik, L., Wallisdevries, M. F., & Verboom, J. (2011). Effect of local weather on butterfly flight behaviour, movement, and colonization: significance for dispersal under climate change. Biodiversity and Conservation, 20, 483-503. https://doi.org/10.1007/s10531010-9960-4
Cuesta, F., Muriel, P., Beck, S., Meneses, R. I., Halloy, S., Salgado, S., Ortiz, E., & Becerra, M. T. (2012). Biodiversidad y Cambio Climático en los Andes Tropicales - Conformación de una red de investigación para monitorear sus impactos y delinear acciones de adaptación. Red Gloria-Andes.
Cometti, G. (2020). El Antropoceno puesto a prueba en el campo: cambio climático y crisis de las relaciones de reciprocidad entre los q’ero de los Andes peruanos. Antipoda. Revista de Antropología y Arqueología, 38, 323. https://doi.org/10.7440/antipoda38.2020.01
Dar, A. A., & Jamal, K. (2021). Moths as ecological indicators: A review. Munis Entomology & Zoology Journal, 16, 830-836.
Declerck, F., & Decker, M. (2009). Integrando la adaptabilidad al cambio climático a través de la biodiversidad. In C. Sepúlveda & M. Ibrahim (eds). Políticas y sistemas de incentivos para el fomento y adopción de buenas prácticas agrícolas como una medida de adaptación al cambio climático en América Central (pp. 23-29). CATIE.
Díaz-Suárez, V., Mahecha-J., O., Andrade, M. G., & Pyrcz, T. W. (2022). Perturbación antrópica afectando a los patrones de diversidad en Satyrinae de montaña Pronophilina Reuter, 1896 en un bosque altoandino en Colombia (Lepidoptera: Nymphalidae). SHILAP Revista de lepidopterología, 50(200), 709-728. https://doi.org/10.57065/shilap.263
Donelson, J. M., Sunday, J. M., Figueira, W. F., Gaitán-Espitia, J. D., Hobday, A. J., Johnson, C. R., & Munday, P. L. (2019). Understanding interactions between plasticity, adaptation, and range shifts in response to marine environmental change. Philosophical Transactions of the Royal Society B, 374(1768), 20180186
Du, Z., He, Y., Wang, H., Wang, C., & Duan, Y. (2021). Potential geographical distribution and habitat shift of the genus Ammopiptanthus in China under current and future climate change based on the MaxEnt model. Journal of Arid Environments, 184, 104328. https://doi.org/10.1016/j.jaridenv.2020.104328
Dudley, R. (2000). The biomechanics of insect’s flight: Form, function, evolution. Princeton University Press. https://doi.org/10.1515/9780691186344
Elith, J., Graham, C. H., Anderson, R. P., Dudík, M., Ferrier, S., Guisan, A., Hijmans, R. J., Huettmann, F., Leathwick, J. R., Lehmann, A., Li, J., Lohmann, L. G., Loiselle, B. A., Manion, G., Moritz, C., Nakamura, M., Nakazawa, Y., Overton, J. Mcc., Peterson, A. T., Phillips, S. J., Richardson, K. S., Scachetti Pereira, R., Schapire, R. E., Soberón, J., Williams, S., Wisz, M. S., & Zimmermann, N. E. (2006). Novel methods improve prediction of species’ distributions from occurrence data. Ecography, 29, 129-151. https://doi.org/10.1111/j.2006.0906-7590.04596.x
Elith, J., Kearney, M., & Phillips, S. (2010). The art of modelling range-shifting species. Methods in ecology and evolution, 1(4), 330-342. https://doi:10.1111/j.2041-210X.2010.00036.x
Elith, J., Steven J., Hastie, T., Dudík, M., Yung, E., &Yates, C. (2011). A statistical explanation of MaxEnt for ecologists. Diversity and Distributions, 17, 43-57. https://doi.org/10.1111/j.1472-4642.2010.00725.x
Equihua, M., Hernández, A., Pérez, O., Benítez, G., & Ibañez, S. (2016). Cambio global: el Antropoceno. Universidad Autónoma del Estado de México Toluca, México. Ciencia Ergo Sum, 23(1), 67-75.
ESRI (2016). ArcGIS [software GIS]. Version 10.5. Redlands, CA: Environmental Systems Research Institute, Inc. Esri Press.
Fielding, A., & Bell, J. (1997). A review of methods for the assessment of prediction errors in conservation presence/absence models. Environmental Conservation, 24(1), 38-49. https://doi.org/10.1017/S0376892997000088
Fleishman, E., Austin, G. T., Bussard, P. F., & Murphy, D. D. (1999). A comparison of Butterfly communities in native and agricultural habitats in the Great Basin, USA. Biological Conservation, 89, 209-218. https://doi.org/10.1016/S0006-3207(98)00152-9
Fox, J. W., Vasseur, D., Cotroneo, M., Guan, L., & Simon, F. (2017). Population extinctions can increase metapopulation persistence. Nature ecology & evolution, 1(9), 1271-1278.
Gaitán-Espitia, J. D., & Hobday, A. J. (2021). Evolutionary principles and genetic considerations for guiding conservation interventions under climate change. Global Change Biology, 27(3), 475-488. https://doi.org/10.1111/gcb.15359
García-Pérez, J. F., Ospina-López, L. A., Villa-Navarro. F. A., & Reinoso-Flórez., G. (2007). Diversidad y distribución de mariposas Satyrinae (Lepidoptera: Nymphalidae) en la cuenca del río Coello, Colombia. Revista de Biología Tropical, 55, 645-653. https://doi.org/10.15517/rbt.v55i2.6039 PMid:19069774
Gebrewahid, Y., Abrehe, S., Meresa, E., Eyasu, G., Abay, K., Gebreab, G., & Darcha, G. (2020). Current and future predicting potential areas of Oxytenanthera abyssinica (A. Richard) using MaxEnt model under climate change in Northern Ethiopia. Ecological processes, 9(1), 1-15. https://doi.org/10.1186/s13717-019-0210-8
Greeney, H. F., Pyrcz, T. W., Devries, P. J. & Dyer, L. A. (2009). The early stages of Pedaliodes poesia (Hewitson, 1862) in Eastern Ecuador (Lepidoptera: Satyrinae: Pronophilini). Journal of Insect Science, 9, 1-8. https://doi.org/10.1673/031.009.3801 PMid:19619012 PMCid: PMC3011897
Gonda, C. (2020). Cambio Climático y Biodiversidad en los Andes Tropicales Fundación Ambiente y Recursos Naturales (FARN).
Haraway, D. (2015). Anthropocene, Capitalocene, Plantacionocene, Chthulucene: Making kin. Environmental Humanities, 6, 159-165. https://doi.org/10.1215/22011919-3615934
Hawkins, B. A., Field, R., Cornell, H. V., Currie, D. J., Guégan, J.-F., Kaufman, D. M., Kerr, J. T., Mittelbach, G. G., Oberdorff, T., O`Brien, E. M., Porter, E. E., & Turner, J. R. G. (2003). Energy, water, and broad-scale geographic patterns of species richness. Ecology, 84(12), 3105-3117. https://doi.org/10.1890/03-8006
He, Q., & Silliman, B. R. (2019). Climate change, human impacts, and coastal ecosystems in the Anthropocene. Current Biology, 29(19), R1021-R1035.
Herzog, S. K., Jorgensen, P., Martínez, S., & Tiessen, H. (2012). Patrones regionales de diversidad y endemismo en las plantas vasculares. In F. Cuesta, P. Muriel, S. Beck, R.I. Meneses, S. Halloy, S. Salgado, E. Ortiz & M.T. Becerra (ed.). Cambio Climático y Biodiversidad en los Andes Tropicales (pp. 180). Red Gloria-Andes.
Hijmans, R., Cameron, S., Parra, J., Jones, P., & Jarvis, A. (2005). Very high-resolution interpolated climate surfaces of global land areas. International Journal of Climatology, 25, 1965-1978. https://doi.org/10.1002/joc.1276
Hijmans, R., & Graham, C. (2006). The ability of climate envelope models to predict the effect of climate change on species distributions. Global Change Biology, 12, 2272-2281. https://doi.org/10.1111/j.1365-2486.2006.01256.x
Hijmans, R. J., Phillips, S., Leathwick, J., Elith, J., & Hijmans, M. R. J. (2017). Package ‘dismo’. Circles, 9(1), 1-68.
Hickling, R., Roy, D. B., Hill, J., Fox, R., & Thomas, C. (2006). The distributions of a wide range of taxonomic groups are expanding polewards. Global Change Biology, 12(3), 450-455. https://doi.org/10.1111/j.13652486.2006.01116.x
IPCC (2013). Summary for Policymakers. In T. F. Stocker, D. Qin, G.-K. Plattner, M. Tignor, S. Allen, J. Boschung, & P. Midgley (Eds.), Climate change 2013: The physical science basis. Contribution of Working Group I to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge University Press.
IPCC (2014). Climate change 2014: Mitigation of climate change. Contribution of working group 3 to the fifth assessment report of the intergovernmental panel on climate change. In O. Edenhofer,R. Pichs-Madruga, Y. Sokona, E. Farahani, S. Kadner, K., Seyboth, J. Minx (Eds.). Cambridge University Press
James, S. A., Clearwater, M. J., Meinzer, F. C., & Goldstein, G. (2002). Heat dissipation sensors of variable length for the measurements of sap flow in trees with deep sapwood. Tree Physiology, 22, 277-283. https://doi.org/10.1093/treephys/22.4.277 PMid:11874724
Jubb, I., Canadell, P., & Dix, M. (2013). Representative concentration pathways (RCPs). Australian Government.
Kocsis, M., & Hufnagel, L. (2011). Impacts of climate change on Lepidoptera species and communities. Applied Ecology and Environmental Research, 9, 43-72. https://doi.org/10.15666/aeer/0901_043072
Lamont, B. B., & Connell, S. W. (1996). Biogeography of Banksia in southwestern Australia. Journal of Biogeography, 23, 295-309. https://doi.org/10.1046/j.1365-2699.1996.00027.x
Laurente, M. (2015). Efectos del cambio climático en la distribución del Cedro ( Cedrela odorata L.) en la Amazonia Peruana. The Biologist, 13(2), 213-224.
Lemoine, N., Bauer, B., Peintinger, M., & Böhning-Gaese, K. (2007). Effects of Climate and Land-Use Change on Species Abundance in a Central European Bird Community. Conservation Biology, 21, 495-503. https://doi.org/10.1111/j.1523-1739.2006.00633.x PMid:17391199
Li, Y., Li, M., Li, C., & Liu, Z. (2020). Optimized maxent model predictions of climate change impacts on the suitable distribution of Cunninghamia lanceolata in China. Forests, 11(3), 302.
Lobo, J. M. (2011). Vulnerabilidad de las áreas protegidas y de zonas de interés para la biodiversidad ante el cambio climático. In P. Álvarez-Uría & J. L. De La Cruz (Coords.). Biodiversidad en España. Base de la Sostenibilidad ante el Cambio Global. Observatorio de la Sostenibilidad de España, Ministerio de Medio Ambiente y Medio Rural y Marino.
Locatelli, B., Kanninen, M., Brockhaus, M., Colfer, C. J. P., Murdiyarso, D., & Santoso, H. (2009). Ante un futuro incierto: cómo se pueden adaptar los bosques y las comunidades al cambio climático. Perspectivas forestales, 5, 1-92. CIFOR.
Locatelli, B. & Kanninen, M. (2010). Servicios ecosistémicos y adaptación al cambio climático. In R. Vignola, I. Pablo, C. Martínez-Alonso & B. Locatelli. Adaptación al cambio climático y servicios ecosistémicos en América Latina (11-20). Centro Agronómico Tropical de Investigación y Enseñanza (CATIE).
Lovejoy, T. D. (2008). Climate Change and Biodiversity. Revue scientifique et technique (International Office of Epizzotics), 27, 331-338. https://doi.org/10.20506/rst.27.2.1808
Maciel-Mata, C. A., Manríquez-Morán, N., Octavio-Aguilar, P., & Sánchez-Rojas, G. (2015). El área de distribución de las especies: revisión del concepto. Acta universitaria, 25(2), 3-19. https://doi.org/10.15174/au.2015.690
Mahecha-Jiménez, O. J., Dumar-Rodríguez, J. C., & Pyrcz, T. W. (2011). Efecto de la fragmentación del hábitat sobre las comunidades de Lepidoptera de la tribu Pronophilini a lo largo de un gradiente altitudinal en un bosque andino en Bogotá (Colombia) (Lepidoptera: Nymphalidae, Satyrina). SHILAP Revista de lepidopterología, 39(153), 117-126.
Mahecha, O., Garlacz, R., Andrade, M. G; Prieto, C., & Pyrcz, T. W. (2019). Island biogeography in continental areas: inferring dispersal based on distributional patterns of Pronophilina butterflies (Nymphalidae: Satyrinae) in the north Andean massifs. Revista mexicana de biodiversidad, 90, e902796. https://doi.org/10.22201/ib.20078706e.2019.90.2796
Mahecha-J, O., Triviño, P., Andrade-C, M. G., & Pyrcz, T. W. (2021). Two new species of Manerebia Staudinger from paramo habitat in the Colombian Eastern Cordillera of the Andes (Lepidoptera: Nymphalidae, Satyrinae, Pronophilina). Zootaxa, 4970(2), 293302
Martín J. L., Bethencourt, J., & Cuevas-Agulló, E. (2011). Evolución el calentamiento global en Tenerife. Tendencias desde 1944 en las temperaturas máximas y mínimas anuales. Proyecto ClimaImpacto del programa de Cooperación Translacional Madeira-Azores-Canarias 2007-2011.
Mateo, G. R., Felicísimo, A. M., & Muñoz, J. (2011). Modelos de distribución de las especies: una revisión sintética. Revista Chilena de Historia Natural, 84(2), 217-240. https://doi.org/10.4067/S0716-078X2011000200008
Merrill, R. M., Gutiérrez, D., Lewis, O. T., Gutiérrez, J., Díez, S. B., & Wilson, R. J. (2008). Combined effects of climate and biotic interactions on the elevational range of a phytophagous insect. Journal of Animal Ecology, 77, 145-155. https://doi.org/10.1111/j.1365-2656.2007.01303.x PMid:18177334
Mestres, F., Zivanovic, G., & Arenas, C. (2015). ¿Cómo se adaptan los organismos al cambio climático? las inversiones cromosómicas de “Drosophila subobscura”: el caso de las poblaciones de Serbia. Mètode Revista de difusión de la Investigación, 88, 36-43.
Miller, D. G., Lane, J., & Senock, R. (2011). Butterflies as potential bioindicators of primary rainforest and oil palm plantation habitats on New Britain, Papua New Guinea. Pacific Conservation Biology, 17, 149- 159. https://doi.org/10.1071/PC110149
Molina-Martínez, A., León-Cortes, J. L., Regan, M., Lewis, O. T., Navarrete, D., Caballero, U., & Luis-Martínez, A. (2016). Changes in butterfly distributions and species assemblages on a Neotropical Mountain range in response to global warming and anthropogenic land use. Diversity Distribution, 21, 1085-1098. https://doi.org/10.1111/ddi.12473
Montero, F. A., & Ortiz-Pérez, M. (2012). Estados inmaduros e historia natural de algunas especies de la subtribu Pronophilina (Nymphalidae: Satyrinae) presentes en el Páramo del Tablazo–Colombia. II. Lymanopoda schmidti Adams 1986. Tropical Lepidoptera Research, 22(1), 32-41.
Montero, F. A., & Ortiz-Pérez, M. (2013). Estados inmaduros e historia natural de algunas especies de la subtribu Pronophilina (Nymphalidae: Satyrinae) presentes en el páramo del tablazo–Colombia. ii. Neopedaliodes zipa (Adams 1986). Tropical Lepidoptera Research, 54-61.
Nieto-Sánchez, S., Gutiérrez, D., & Wilson, R. J. (2015). Long-term change and spatial variation in butterfly communities over an elevation gradient driven by climate, buffered by habitat. Diversity Distribution, 21, 950961. https://doi.org/10.1111/ddi.12316
Olarte-Quiñonez, C. A., Carrero-Sarmiento, D., Viloria, Á. L., & Ríos-Málaver, I. C. (2021). Patrones de diversidad de las mariposas de la subtribu Pronophilina (Lepidoptera: Nymphalidae: Satyrinae) en un gradiente altitudinal del Cerro de Tierra Negra, Cordillera Oriental, Norte de Santander, Colombia. Boletín Científico. Centro de Museos. Museo de Historia Natural, 25(2), 197-218.
Olson, S. K., Smithwick, E. A., Lucash, M. S., Scheller, R. M., Nicholas, R. E., Ruckert, K. L., & Caldwell, C. M. (2021). Landscape-scale Forest reorganization following insect invasion and harvest under future climate change scenarios. Ecosystems, 1-19.
Peterson, A. T. (2001). Predicting species geographic distributions based on ecological niche modeling. The Condor, 103(3), 599-605. https://doi.org/10.1093/condor/103.3.599
Peterson, A. T. (2003). Predicting the geography of species’ invasions via ecological niche modeling. Quarterly Review of Biology, 78, 419-433. https://doi.org/10.1086/378926 PMid:14737826
Peterson, D. P., Rieman, B. E., Dunham, J. B., Fausch, K. D., & Young, M. K. (2008). Analysis of trade-offs between the threat of invasion by nonnative brook trout ( Salvelinus fontinalis) and intentional isolation for native west slope cutthroat trout ( Oncorhynchus clarkiilewisi). Canadian Journal of Fisheries and Aquatic Sciences, 65(4), 557-573. https://doi.org/10.1139/f07-184
Phillips, S. J., Anderson, R. P., & Schapire, R. E. (2006). Maximum entropy modeling of species geographic distributions. Ecological Modeling, 190, 231-259. https://doi.org/10.1016/j.ecolmodel.2005.03.026
Pyrcz, T. W., & Wojtusiak, J. (1999). Mariposas de la tribu Pronophilini de la Reserva forestal Tambito, Cordillera occidental, Colombia. Segunda parte. Patrones de distribución altitudinal (Lepidoptera: Nymphalidae, Satyrinae). SHILAP Revista de lepidopterología, 27(106), 203-213.
Pyrcz, T. W. (2000). Contributions to the knowledge of Ecuadorian Pronophilini. Part IV. New taxa of Pronophila Doubleday (Lepidoptera: Nymphalidae: Satyrinae). Genus, 11(1), 69-86.
Pyrcz, T. W., & Wojtusiak, J. (2002). The vertical distribution of pronophiline butterflies (Nymphalidae, Satyrinae) along an elevational transect in Monte Zerpa (Cordillera de Mérida, Venezuela) with remarks on their diversity and parapatric distribution. Global Ecology and Biogeography, 11, 211-221. https://doi.org/10.1046/j.1466822X.2002.00285.x
Pyrcz, T. W. (2004). Notas taxonómicas sobre el género Pronophila Doubleday con la descripción de cuatro nuevas subespecies de Pronophila unifasciata Lathy (Nymphalidae: Satyrinae: Pronophilini). Boletín Museo de Historia Natural, 6(30), 233-244.
Pyrcz, T. W., & Viloria, A. L. (2007). Erebiine and Pronophiline Butterflies of the Serranía del Tama, VenezuelaColombia Border (Lepidoptera: Nymphalidae: Satyrinae). Tropical Lepidoptera, 15(1-2), 18-52.
Pyrcz, T. W., Wojtusiak, J., & Garlacz, R. (2009). Diversity and distribution patterns of Pronophilina butterflies (Lepidoptera: Nymphalidae: Satyrinae) along an altitudinal transect in northwestern Ecuador. Neotropical Entomology, 38, 716-726. https://doi.org/10.1590/S1519-566X2009000600003 PMid:20098916
Pyrcz T., Cerdeña, J., & Huamani, E. (2013). Systematics, bionomics, and zoogeography of high Andean pedaliodines. Part 14: Two new species of Pedaliodes Butler from the Huancabamba Deflection in southern Ecuador and northern Peru (Lepidoptera: Nymphalidae: Satyrinae). Genus, 24(2), 131-141.
Pyrcz, T. W., Clavijo, A., Uribe, S., Marín, M. A., Álvarez, C. F. y Zubek, A. (2016). Páramo de Belmira as an important centre of endemism in the northern Colombian Andes: New evidence from Pronophilina butterflies (Lepidoptera: Nymphalidae, Satyrinae, Satyrini). Zootaxa, 4179(1), 77-102. https://doi.org/10.11646/zootaxa.4179.1.3
Pyrcz, T. W., Lorenc-Brudecka, J., Zubek, A., Prieto, C., Boyer, P., Florczyk, K., & Lachowska-Cierlik, D. (2019). Considerations on the taxonomy of the genus Arhuaco Adams and Bernard 1977, and its relationships with the genus Pronophila Doubleday [1849] (Nymphalidae, Satyrinae). Neotropical entomology, 48, 302-313.
Pyrcz, T. W., Zubeck, A., Boyer, P., Nakamura, I., Waclawik, B., & Florczyk, K. (2020). Revisional notes on the cloud forest butterfly genus Oxeoschistus Butler in Central America (Lepidoptera: Nymphalidae: Satyrinae). Neotropical Entomology, 49, 392-411. http://dx.doi.org/10.1007/s13744-019-00757-7.
Quesada-Quirós, M., Acosta-Vargas, L. G., Arias-Aguilar, D., & Rodríguez-González, A. (2016). Modelación de nichos ecológicos basado en tres escenarios de cambio climático para cinco especies de plantas en zonas altas de Costa Rica. Revista Forestal Mesoamericana Kurú, 14(34), 1-12. https://doi.org/10.18845/rfmk.v14i34.2991
R Core Team (2023). R: A language and environment for statistical computing. R Foundation for Statistical Computing. https://www.R-project.org/
Rajpoot, R., Adhikari, D., Verma, S., Saikia, P., Kumar, A., Grant, K. R., & Khan, M. L. (2020). Climate models predict a divergent future for the medicinal tree Boswellia serrata Roxb. in India. Global Ecology and Conservation, 23, e01040. https://doi.org/10.1016/j.gecco.2020.e01040
Riahi, K., Rao, S., Krey, V., Cho, C., Chirkov, V., Fischer, G., Kindermann, G., Nakicenovic, N., & Rafaj, P. (2011). RCP 8.5: A scenario of comparatively high greenhouse gas emissions. Climatic Change, 109, 33-57. https://doi.org/10.1007/s10584-011-0149-y
Rödder, D., Schmitt, T., Gros, P., Ulrich, W., & Habel, J. C. (2021). Climate change drives mountain butterflies towards the summits. Scientific Reports, 11(1), 14382.
Romero-Centeno, R., Adams, D. K., Amador-Astúa, J. A., Castro, C. L., Cavazos-Pérez, M. T., Garduño-López, R., Lizarraga-Celaya, C., Mendoza-Castro, V. M., & Pavia-López, E. (2016). Fenómenos climáticos y su relevancia para el cambio climático regional futuro. In C. Gay García & J. C. Rueda Abad. Reporte Mexicano de Cambio Climático. Grupo I Bases científicas. Modelos y modelación (pp. 219-246). Universidad Nacional Autónoma de México.
Romo, H., Sanabria, P., & García-Barros, E. (2013). Predicción de los impactos del cambio climático en la distribución sobre las especies de Lepidoptera. El caso del género Boloria Moore, 1900 en la Península Ibérica (Lepidoptera: Nymphalidae). SHILAP Revista de lepidopterología, 41(162), 267-286.
Russo, R. O., & Kohlmann, B. (2013). Cambio Climático: efectos sobre la Biodiversidad. Universidad La Salle.
Särkinen, T., Toby, R., Lavin, M., Simon, M., & Hughes, C. (2011). Evolutionary islands in the Andes: persistence and isolation explain high endemism in Andean dry tropical forests. Journal of Biogeography, 39(5), 884-900. https://doi.org/10.1111/j.1365-2699.2011.02644.x
Stranges, S., Cuervo-Robayo, A. P., Martínez-Meyer, E., Morzaria-Luna, H. N., & Reyes-Bonilla, H. (2019). Distribución potencial bajo escenarios de cambio climático de corales del género Pocillopora (Anthozoa: Scleractinia) en el Pacífico oriental tropical. Revista mexicana de biodiversidad, 90, 1-16. https://doi.org/10.22201/ib.20078706e.2019.90.2696
Swets, J. A. (1988). Measuring the accuracy of diagnostic systems. Science, 240(4857), 1285-1293.
Taylor, K. E., Stouffer, R. J., & Meehl, G. A. (2012). An overview of CMIP5 and the experiment design. Bulletin of the American Meteorological Society, 93(4), 485-498. https://doi.org/10.1175/BAMS-D-11-00094.1
Torres-Vila, L., Stockel, J., & Rodríguez, M. (1996). Efecto de la indisponibilidad de agua sobre el potencial biótico de la polilla del racimo Lobesia botrana Den. y Schiff. (Lepidoptera: Tortricidae). Boletín de Sanidad Vegetal. Plagas, 22, 443-444.
Turvey, S. T., & Crees, J. J. (2019). Extinction in the Anthropocene. Current Biology, 29(19), R982-R986.
Uribe, E. (2015). El cambio climático y sus efectos en la biodiversidad en América Latina. Comisión Económica para América Latina y el Caribe (CEPAL).
Viloria, A. (2008). Mariposa blanca del páramo, Lymanopoda paramera. In J. P. Rodríguez & F. Rojas Suárez (Eds.). Libro Rojo de la Fauna Venezolana (p. 227). Provita y Shell Venezuela, S. A.
Viloria, A. L., Pyrcz, T. W., & Orellana, A. (2010). A survey of the Neotropical montane butterflies of the subtribe Pronophilina (Lepidoptera, Nymphalidae) in the Venezuelan Cordillera de la Costa. Zootaxa, 2622, 1-41. https://doi.org/10.11646/zootaxa.2622.1.1
Wei, B., Wang, R., Hou, K., Wang, X., & Wu, W. (2018). Predicting the current and future cultivation regions of Carthamus tinctorius L. using MaxEnt model under climate change in China. Global Ecology and Conservation, 16, e00477. https://doi.org/10.1016/j.gecco.2018.e00477
Wang, R., Li, Q., He, S., Liu, Y., Wang, M., & Jiang, G. (2018). Modeling and mapping the current and future distribution of Pseudomonas syringae pv. actinidiae under climate change in China. PloS one, 13(2), e0192153. https://doi.org/10.1371/journal.pone.0192153
Wickman, P. (2009). Thermoregulation and habitat use in butterflies. In J. Settele, T. Shreeve, M. Konvicka & H. Van Dyck, eds. Ecology of butterflies in Europe (pp. 55-61). Cambridge University Press.
Xianli, Z., Yingcun, X., & Howell, T. (2018). Jackknife approach to the estimation of mutual information. PNAS, 115(40), 9956-9961. https://doi.org/10.1073/pnas.1715593115 PMid:30224466 PMCid:PMC6176556
Zenker, M., De Vries, P., Penz, C., Teston, J., Freitas, A. V. L., & Pie, M. (2015). Diversity and composition of Arctiinae moth assemblages along elevational and spatial dimensions in Brazilian Atlantic Forest. Journal of Insect Conservation, 19(1), 129-140. https://doi.org/10.1007/s10841-015-9753-x
Author notes
a Autor para correspondencia: oscarmahecha23@gmail.com
