ARTÍCULOS
Recepción: 10 Julio 2018
Aprobación: 31 Octubre 2018
Resumen: La ganadería impacta los ecosistemas, particularmente a través del consumo y dispersión de especies introducidas que afectan la flora nativa. La dispersión de semillas de vegetación introducida por mamíferos exóticos es un ejemplo de facilitación entre especies exóticas. En este trabajo se abordaron tres aspectos (composición de la dieta, viabilidad y germinación de semillas) para evaluar el rol del ganado doméstico en la dispersión de Rosa rubiginosa, rosa mosqueta, en bordes de vegas de baja altura en la provincia de Mendoza. Se recolectaron heces frescas de ganado vacuno y equino (n=60), y se contabilizaron las semillas enteras de Rosa rubiginosa. La dieta de ambas especies estuvo conformada principalmente por flora nativa, sobre todo gramíneas (Poaceae). Tanto la vaca como el caballo aumentaron la tasa de germinación de las semillas enteras de rosa mosqueta en comparación con los controles establecidos. Ambos herbívoros introducidos utilizan la rosa mosqueta como un recurso importante y actúan como dispersores legítimos de sus semillas.
Palabras clave: Bos taurus, endozoocoria, Equus caballus, Rosa rubiginosa, vegas de baja altura.
Abstract: Livestock impacts ecosystems, particularly through the consumption and dispersion of introduced plant species that affect native flora. The dispersion of seeds introduced by exotic mammals is an example of facilitation among exotic species. In this work, three aspects (diet composition, viability and germination of seeds) were approached to evaluate the role of domestic livestock in the dispersion of Rosa rubiginosa, sweetbriar rose, on edges of low-altitude vegas in Mendoza province. Fresh feces were collected from cattle and horses (n = 60), and the intact seeds of Rosa rubiginosa were counted. The diet of both species was mainly made up of native flora, especially grasses (Poaceae). Both cows and horses increased the germination rate of intact sweetbriar rose’s seeds compared to established controls. We can highlight that both introduced herbivores use sweetbriar rose as an important resource and act as legitimate dispersers of their seeds.
Keywords: Bos taurus, endozoochory, Equus caballus, Rosa rubiginosa, low altitude vega.
INTRODUCCION
Las introducción de especies exóticas invasoras altera la composición de la flora, la fauna y el paisaje de una región (Macdonald et al. 1989; Vitousek et al. 1997), y es una de las principales causas de la pérdida de la biodiversidad. Cuanto más dramáticos son los cambios en el paisaje, mayor es la probabilidad de establecimiento exitoso para muchas de estas especies (Lockwood et al. 2007; Davis 2009).
Simberloff & Holle (1999) describen como facilitación, en inglés “invasional meltdown”, al proceso por el cual las especies exóticas favorecen el establecimiento y/o la invasión de otras especies exóticas. La invasión de plantas mediada por mamíferos exóticos puede facilitarse por dos mecanismos: por la alteración de los regímenes de disturbio y por la dispersión de sus semillas (Barrios-García & Simberloff 2013). La dispersión es un proceso clave para la invasión de plantas exóticas ya que permite su expansión hacia nuevos ambientes (Kot et al. 1996). Por ejemplo, el consumo de frutos por ungulados puede beneficiar a la planta si sus semillas son eliminadas en sitios adecuados para su germinación y supervivencia (dispersión por endozoocoria; Janzen 1984). Así, la dispersión favorece el flujo génico y la colonización, y permite evitar la competencia intraspecífica con la generación parental (Howe & Smallwood 1982). Además, la endozoocoria puede modificar la viabilidad y/o los patrones de germinación de las semillas (Traveset 1998). Cuando un animal ingiere semillas de una especie y las elimina en condiciones viables para su germinación se lo considera un dispersor legítimo de dicha especie (Herrera 1995).
Las especies silvestres del género Rosa son de origen europeo y asiático, y son consideradas como invasoras en diferentes regiones del mundo (Bran et al. 2003). La rosa mosqueta (Rosa rubiginosa) es una de las leñosas introducidas con mayor extensión en la región andino-patagónica de Argentina (Damascos & Gallopin 1992). Su introducción ocurrió cerca de 1910 en el Parque Nacional Nahuel Huapi, Provincia de Río Negro. En la actualidad se la encuentra en la región sur cordillerana de las provincias de Neuquén, Río Negro y Chubut, y en la zona de montaña de Mendoza, donde fue introducida para utilizarla como cerco vivo (Dalmasso et al. 2011). La rosa mosqueta tiene un conjunto de atributos característicos de las invasoras exitosas. Se reproduce asexualmente por propagación de sus raíces, y sexualmente con liberación gradual de sus semillas durante otoño-invierno, con alta viabilidad, dormición y longevidad de las mismas (Damascos et al. 2005). Se expande en áreas abiertas, asociada a cursos de agua y en quebradas húmedas en ambientes de precordillera (Dalmasso et al. 2011). Produce sustancias alelopáticas que inhiben e interfieren en la germinación, crecimiento o desarrollo de las plantas próximas (Whittaker & Feeny 1971; Liebman & Ohno 1998). En la región andino-patagónica, sus frutos constituyen un alimento nutritivo, accesible y abundante, especialmente durante el otoño y el invierno, cuando disminuye la disponibilidad de otros alimentos (Pelliza-Sbriller & Sepúlveda 2008). Sus frutos son coloridos y atractivos para los animales, los cuales eliminan sus semillas en condiciones viables (Parsons et al. 2003; Joublan et al. 1996; Martínez Carretero et al. 2006; Damascos 2008; Zimmermann et al. 2011). Su reproducción, establecimiento y/o el éxito de invasión están afectados tanto por las condiciones ambientales como por las especies que consumen sus frutos.
Las vegas son terrenos bajos, llanos y fértiles que se originan por cursos de agua temporarios y son importantes por sus características tanto florísticas y ecológicas como fitosociológicas (Méndez 2007). En los ambientes de montaña existen dos tipos de vegas: de baja altura (1200 a 2000 msnm) y de altura (por encima de los 2000 msnm). En ambos tipos de vegas existe un total de 104 especies vegetales, de las cuales 48 son exclusivas de vegas de baja altura y 40 de las de altura. Las especies autóctonas predominan en las vegas de altura mientras que en las de baja altura dominan las especies alóctonas (Méndez 2007). El aumento de plantas introducidas en las vegas de baja altura, como la rosa mosqueta, esta asociado a una mayor presión antrópica (Méndez 2007).
La ganadería no sólo impacta la demarcación territorial y el uso de los suelos, sino también la composición de las comunidades de plantas de las cuales se alimenta el ganado (Leege et al. 1981; Belsky & Gelbard 2000; Bartuszevige & Endress 2008). Tanto el ganado vacuno como el equino son dispersores por endozoocoria (Hatton 1989; Cosyns et al. 2005; Bartuszevige & Endress 2008; Chuong et al. 2016). En Estados Unidos, la vaca (Bos taurus) actúa como dispersor de especies tanto nativas como exóticas, principalmente gramíneas y herbáceas (Bartuszevige & Endress 2008). En Australia, el caballo (Equus caballus) come y dispersa semillas de rosa mosqueta en condiciones viables (Hatton 1989). Un estudio en los bosques patagónicos de Argentina muestra que las semillas de rosa mosqueta encontradas en las heces de ambos ungulados, exhibieron una viabilidad del 100% (Damascos et al. 2005).
En función de los antecedentes presentados, se espera que tanto el ganado equino como el vacuno dispersen semillas de rosa mosqueta, contribuyendo así al proceso de expansión de esta planta invasora al facilitar su establecimiento en los Andes áridos de Argentina. Para evaluar la interacción entre la rosa mosqueta y los ungulados domésticos en los bordes de vegas de baja altura en la región andina nos propusimos: a) determinar la composición de la dieta de ambas especies y analizar si existe variación estacional en el consumo de especies de plantas, y b) determinar el rol de cada especie de ungulado como dispersor legítimo de la rosa mosqueta.
MATERIALES Y MÉTODOS
Área de estudio
El estudio se desarrolló en la localidad de Las Vegas, Potrerillos, Mendoza (33° 00’S – 69° 16’O, 1860 m s.n.m.), una vega de baja altura en la región fitogeográfica Andina. La temperatura media es de 18.2°C en verano y 3.1°C en invierno (Méndez 2007). Está abastecida por dos arroyos, Las Mulas y Las Vacas, y en sus márgenes se encuentra una diversidad importante de flora nativa como Discaria trinervis (Chacay), Cortaderia rudiuscula (Cortadera), Ephedra breana (Solupe), Jarava sp. (Coirón), Denmoza rhodacantha (Cactus), Artemisia mendozana (Ajenjo), Spartium junceum (Retama), Berberis grevilleana (crucero), Ligaria cuneifolia (liga), Aldama gilliesii (botón de oro) (Méndez 2007). El ganado de la zona (equino y vacuno) es de pastoreo continuo, de tipo extensivo, con disponibilidad de vegetación estacional formada por una estepa graminosa (Gudiño De Muñoz 2002; Guevara et al. 2006).
Durante la estación húmeda (octubre-marzo) y seca (abril-septiembre) de 2011, y en la estación seca de 2014, se recolectaron a lo largo de las vegas 10 heces frescas de ganado equino y bovino por estación (60 muestras en total). Además, se tomaron muestras de plantas para ser identificadas y utilizadas como material de referencia. Durante la estación de maduración de los frutos (otoño) de 2014 también se recolectaron frutos maduros de rosa mosqueta para ser utilizados en los ensayos de viabilidad y germinación.
Dieta
Para determinar la dieta de ambos ungulados se utilizaron las muestras de 2011 de ambas estaciones, y se extrajeron 10 gramos de cada una para ser analizadas por la técnica microhistológica descripta en Dacar & Giannoni (2001). Se realizó la identificación de tejidos epidérmicos de hojas, tallos, tegumentos de semillas y frutos. Para cada muestra se observaron, de manera sistemática, 50 campos microscópicos a 40x para identificar especies presentes en la dieta, realizando un total de 1000 observaciones para el ganado bovino y 1000 para el ganado equino. Los ítems alimenticios fueron identificados a nivel de especie cuando fue posible. La presencia de cada ítem fue registrada y se calculó la frecuencia de ocurrencia relativa para cada uno (Holechek & Gross 1982). Para determinar si existen diferencias significativas entre la dieta del ganado vacuno y equino, se agruparon los ítems alimenticios en 6 categorías en función de la forma de vida: gramíneas, herbáceas, subarbustos (arbustos menores a 1 m de altura), arbustos, árboles y otros (pelos y artrópodos). Se evaluaron las diferencias en el consumo de frutos y hojas entre ambas especies de ungulados. Para cada análisis se realizó una prueba de Mann-Whitney (Zar 1999).
Viabilidad y germinación
Para evaluar la dispersión de semillas de rosa mosqueta se tomaron 10 gramos de cada muestra de la estación seca 2014. Estas muestras fueron secadas a temperatura ambiente y mediante análisis macroscópico se extrajeron y contabilizaron las semillas enteras de rosa mosqueta. Se agruparon por separado las semillas provenientes de caballos y de vacas, y se tomaron al azar 100 semillas de las muestras de cada especie para el ensayo de viabilidad y otras 100 semillas para el ensayo de germinación. También se extrajeron 200 semillas de los frutos colectados durante la estación seca 2014 como control para cada uno de los ensayos.
Para realizar el ensayo de viabilidad se cortaron longitudinalmente todas las semillas con un cúter. Las mitades se colocaron en frascos con solución de Tetrazolio (cloruro 2, 3, 5, trifenil tetrazolio Sigma) al 0.5% y se colocaron en estufa a 30°C (Pérez & Argüello 1997). Se realizaron observaciones durante 24 horas, registrando cada dos horas los cambios de coloración. Los embriones coloreados fueron observados a microscopio óptico 40x para determinar la viabilidad de las semillas (Moore 1985). Para evaluar las diferencias entre la viabilidad de las semillas de rosa mosqueta consumidas y las del control, se realizó una prueba de homogeneidad, utilizando el estadístico Chi-cuadrado (Zar 1999).
Se realizó un ensayo durante 8 meses para evaluar la capacidad de germinación de las semillas consumidas. Las 100 semillas de cada grupo (caballo, vaca y control) se sembraron individualmente a 2 cm de profundidad, en recipientes perforados, con sustrato proveniente del sitio de estudio, en condiciones de luz y temperatura ambiente, y regados periódicamente. Se observó cada 24 h el estado de las semillas y se removieron aquellas que presentaban protrusión de radícula. Se calculó el porcentaje de germinación (número de semillas germinadas sobre el total de semillas sembradas x 100), y la tasa de germinación (GR) de las semillas con la ecuación: GR = (5/6×P)/(T2−T1), donde P es el porcentaje final de germinación, T1 es el intervalo (en días) entre la siembra y la emergencia de 1/6 ×P de las plántulas, y T2 es el intervalo (en días) entre la siembra y la emergencia de 5/6 ×P plántulas (Izhaki & Ne’eman 1997). Para evaluar las diferencias entre las semillas consumidas y el control se realizó una prueba de homogeneidad, utilizando el estadístico Chi-cuadrado, χ2 (Zar 1999). No se evaluó la viabilidad de las semillas que no germinaron luego de 8 meses de ensayo.
RESULTADOS
Dieta
Los caballos consumieron principalmente gramíneas (56.3%), subarbustos (23.5%), arbustos (9.9%) y herbáceas (5.9%). Las gramíneas consumidas con mayor frecuencia fueron Festuca sp y Poa sp, tanto en la estación húmeda (28.0% y 23.4%, respectivamente), como en la seca (44.2% y 16.6%, respectivamente).
Entre los subarbustos, consumieron principalmente Senecio sp (8.2%) y Junellia sp (4.8%) en la estación húmeda; y Acantholippia seriphioides (8.8%), Ephedra sp (6.8%) y Lycium sp (6.2%) durante la estación seca. Dentro de las herbáceas, Medicago sp fue la especie más consumida durante la estación húmeda (6.8%). En cuanto a las especies arbustivas, Rosa rubiginosa fue la especie más consumida tanto en la estación húmeda (11.4%) como en la seca (7%); ver Tabla 1.
Media ± Error estándar de la frecuencia de ocurrencia de los ítems alimenticios presentes en la dieta de caballo y vaca en Las Vegas, Potrerillos, Mendoza, Argentina.
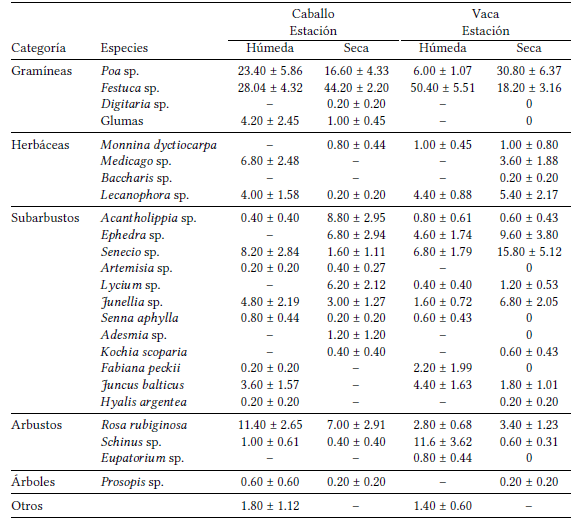
Las vacas tuvieron un consumo similar al de los caballos. Las vacas consumieron principalmente gramíneas (52.7%), subarbustos (29%), arbustos (9.6%) y herbáceas (7.8%). Durante la estación húmeda, las especies más consumidas fueron Festuca sp (50.4%), Schinus sp (11.6%), Senecio sp (6.8%), Poa sp (6.0%), Ephedra sp (4.6%), Lecanophora sp (4.4%) y Rosa rubiginosa (2.8%). Durante la estación seca consumieron principalmente Poa sp (30.8%), Festuca sp (18.2%), Senecio sp (15.8%), Ephedra sp (9.6%), Junellia sp (6.8%), Lecanophora sp (5.4%), Medicago sp (3.6%) y Rosa rubiginosa (3.4%); ver Tabla 1.
Comparando la variación estacional de las dietas entre ungulados, en función de la forma de vida de las plantas, vemos que las vacas consumen principal mente herbáceas durante la estación seca (Xvaca=10.2; Xcaballo=1.0; U=14; gl= 5; p<0.005; Fig. 1).
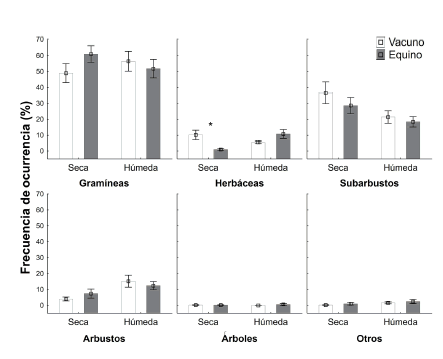
Fig. 1.
Variación estacional de la frecuencia de ocurrencia (Media ± Error estándar) de los ítems consumidos por vaca y caballo en función de la forma de vida de las plantas en Las Vegas, Potrerillos. El asterisco indica diferencias significativas p<0.05.
En relación a las partes de las plantas consumidas,durante la estación húmeda las vacas consumieron las hojas en mayor proporción que los caballos (Xvaca= 91.4; Xcaballo= 78.6; U= 18; gl= 1; p=0.015); en cambio los caballos consumieron mayor proporción de frutos que las vacas (Xvaca= 8.6; Xcaballo=21.4; U=18;gl=1; p=0.015; Fig. 2).
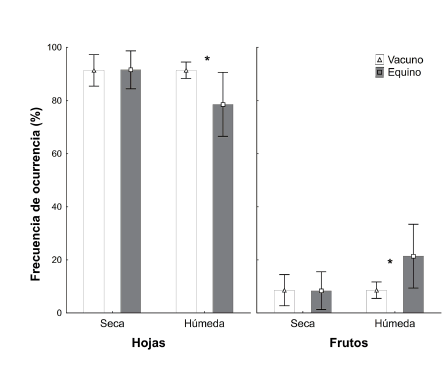
Fig. 2.
Variación estacional de la frecuencia de ocurrencia (Media ± Error estándar) de los ítems consumidos por vaca y caballo en función de las partes de plantas (hojas o frutos) en Las Vegas, Potrerillos. El asterisco indica diferencias significativas p<0.05.
Viabilidad y germinación
En los caballos se registró un promedio de 61±29 semillas de rosa mosqueta por muestra, y en las vacas se registró 10±4 semillas por muestra. En las heces de caballos se obtuvieron 138 semillas en la estación húmeda y 1713 semillas en la estación seca. En las heces de las vacas se obtuvieron 9 y 294 semillas; en la estación húmeda y en la estación seca, respectivamente. Se registraron 110 semillas dañadas en las muestras de caballos y 29 en las de vacas.
La viabilidad de las semillas consumidas tanto por las vacas (98%), como por los caballos (86%), fue mayor que la de las semillas recolectadas directamente de los frutos (79%, control); χ2=17.08; gl=2; p<0.05.
El porcentaje de germinación de las semillas consumidas por las vacas y los caballos fue mayor que el de las semillas del tratamiento (χ2=9.021; gl=2; p<0.05; Tabla 2).
Cantidad de semillas de rosa mosqueta enteras extraídas de las heces, n° de semillas germinadas sobre 100 sembradas (%), n° de semillas viables sobre 100 analizadas (%), comienzo de la germinación (T0) y tasa de germinación (TG) para cada uno de los tratamientos. T0 intervalo de días entre la siembra y la emergencia de 1/6 del porcentaje final de germinación (G); TG=5/6xG/(T-T0), donde T es el intervalo de días entre la siembra y la emergencia de 5/6xG.

La tasa de germinación para las semillas del control fue casi 4 veces menor que la de las semillas consumidas por los ungulados. Asimismo, las semillas consumidas por caballos demoran más en germinar que las semillas consumidas por las vacas (Tabla 2; Fig. 3).
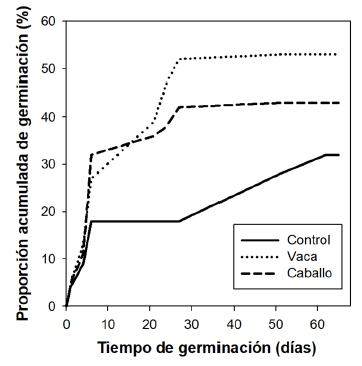
Fig. 3.
Porcentaje de germinación acumulado de las semillas de Rosa mosqueta a través del tiempo para los dos tratamientos y el control.
DISCUSIÓN
El estudio de los hábitos alimentarios de una especie, además de aportar información relacionada con la energía que necesitan los individuos para sobrevivir y reproducirse, nos permite tener una idea sobre la interacción de la especie con el ambiente físico y con las demás especies de la comunidad (Sih & Christensen 2001). Además, nos aporta información sobre la forma en que algunas comunidades vegetales pueden verse afectadas por el forrajeo de algunos animales (Wood & Roark 1980). En el caso del ganado doméstico, el conocimiento de sus hábitos alimentarios nos provee información para la toma de decisiones en el manejo del pastoreo; e.g. para el pastoreo rotativo (Provenza & Balph 1988).
En el área estudiada, caballos y vacas consumen principalmente flora nativa, sobre todo gramíneas predominantes en la zona como Poa sp y Festuca sp. En general, en los ambientes áridos y semiáridos, donde las condiciones son extremas (altas temperaturas, déficit hídrico y baja productividad), las especies responden a la variación estacional y espacial de los recursos (Van Horne et al. 1998). El agua controla por lo tanto el crecimiento vegetativo de la mayoría de las plantas leñosas y la germinación de las hierbas anuales y de las gramíneas (Rundel et al. 2007). La limitación de los recursos ocurre principalmente durante la estación seca, cuando la baja calidad del alimento genera una pérdida de peso en los animales (Danell et al. 2006).
La diferencia estacional en el consumo de herbáceas registrada durante la estación húmeda en este estudio puede resultar de los cambios en la disponibilidad o en la fenología de las plantas. Guevara et al. (2006) proponen para el desierto del Monte que, debido a estos cambios fenológicos en los pastos, la dieta de las vacas en particular, muestra un consumo mayor de especies leñosas durante la estación seca. Nuestros registros indican, coincidentemente, que las vacas consumieron menos especies leñosas en la estación húmeda que en la estación seca (36.6% y 40.8% respectivamente).
La producción extensiva de ganado depende de la habilidad del animal de seleccionar una dieta que contenga los nutrientes necesarios para el mantenimiento, crecimiento y reproducción (Gordon 1995). Según Heady & Child (1994) la elección de los ítems alimentarios está asociada a las reacciones del animal y a la palatabilidad de las plantas. El caballo consumió frutos de Rosa rubiginosa con mayor frecuencia que la vaca durante la estación húmeda. Durante la estación seca, que es el momento de menor productividad, el caballo mostró un consumo aún mayor de dichos frutos (21.4% en estación seca y 8.4% en estación húmeda). La vaca consumió un bajo porcentaje de frutos de rosa mosqueta en ambas estaciones (8.6%). El fruto de la rosa mosqueta es rico en azúcares, vitamina C, y con gran contenido proteico (Pelliza-Sbriller & Sepúlveda 2008). La ingesta de carbohidratos es esencial para la acumulación de reservas que se utilizan durante el o los periodos críticos de demanda energética (Abaigar 1993). Esto podría explicar el incremento del consumo de frutos de rosa mosqueta de los caballos durante la estación seca.
En otras experiencias realizadas con germinación de semillas, Campos & Ojeda (1997) encontraron que las semillas del algarrobo (Prosopis flexuosa) recolectadas de las heces de las vacas registraron una mayor capacidad germinativa, pero menor viabilidad, en comparación con las semillas recolectadas de las plantas. Sin embargo, registraron pocas semillas en las heces de los caballos, pero con mayor viabilidad y menor tasa de germinación. Nuestros resultados muestran que la carga de semillas/muestra fue mayor en los caballos que en las vacas para las dos estaciones analizadas. Coinciden además con los obtenidos en el noroeste de la provincia de Chubut, donde se registraron 86 000 semillas en las heces de los caballos y 23 000 en las de las vacas (Lloyd 2014). Estos autores reportaron que la viabilidad de las semillas, tanto de las consumidas como las del grupo control, fue superior al 75%. Las consumidas por las vacas alcanzaron casi el 100% con niveles similares a los registrados por Damascos et al. (2005) en los bosques de ciprés de Río Negro, Argentina. Como mencionan los mismos autores, Rosa rubiginosa presenta un conjunto de atributos, entre los que se encuentra una alta viabilidad de las semillas, que le permiten asegurar su propagación sexual durante un período extendido de aporte y dispersión de semillas. En nuestro trabajo, la mayor viabilidad de las semillas obtenidas de las heces de caballo y vaca en comparación con el grupo control, indicaría que las semillas no pierden la viabilidad al pasar por el tracto digestivo del ganado. Además, tanto el potencial de germinación como la tasa de germinación fueron mayores que el control. Por lo tanto, ambos ungulados actúan como dispersores legítimos de semillas de rosa mosqueta, ya que dispersan semillas viables y con mayor potencial y tasa de germinación. El aumento de la germinación se debe probablemente a la escarificación producida en su paso por del tracto digestivo, interrumpiendo la latencia de las semillas por la acción de las enzimas digestivas y de los microorganismos responsables de la fermentación (Gardener et al. 1993; Peco et al. 2006).
Es importante destacar que las especies del género Rosa necesitan largos períodos de exposición a condiciones húmedas y de baja temperatura para interrumpir su dormancia (Damascos et al. 2005). Este tratamiento no fue realizado en nuestro estudio, por lo que los porcentajes de viabilidad y germinación de las semillas consumidas y las del control pueden estar afectados por la dormición de las semillas Rosa rubiginosa.
En conclusión, nuestros resultados detectaron interacciones de facilitación entre plantas y mamíferos exóticos que posiblemente aumente la vulnerabilidad de las comunidades vegetales de las vegas de baja altura a la invasión por rosa mosqueta en los Andes áridos de Argentina. Ambos ungulados utilizan la rosa mosqueta como un recurso alimentario importante y actúan como dispersores legítimos de sus semillas. Futuros estudios deberían contemplar otros componentes como la carga ganadera, los patrones de movimiento y la disponibilidad de los recursos en el ambiente para determinar la utilización de los mismos (selección positiva o negativa); así como también la eficiencia y efectividad de la dispersión de sus semillas para comprender mejor el rol del ganado equino y vacuno en la invasión de la rosa mosqueta en los Andes áridos de Argentina.
Agradecimientos
A Juan Eduardo Cavaliere por la asistencia en los trabajos de campo y germinación. Al Dr. Ricardo Ojeda por su apoyo en el desarrollo de este estudio. A la Dra. Andrea Duplancic y Dra. Ana Mazzolari por el asesoramiento sobre el uso del Test de Tetrazolio y facilitar la bibliografía relacionada al tema.
REFERENCIAS
Abaigar, T. 1993. Régimen alimentario del jabalí (Sus scrofa) en el sureste Ibérico. Doñana, Acta Vertebrata 20:35-48.
Barrios-García, M. N., & D. Simberloff. 2013. Linking the pattern to the mechanism: How an introduced mammal facilitates plant invasions. Austral Ecology 38:884-890. https://doi.org/10.1111/aec.12027
Bartuszevige, A. M., & B. A. Endress. 2008. Do ungulates facilitate native and exotic plant spread? Seed dispersal by cattle, elk and deer in northeastern Oregon. Journal of Arid Environments 72:904-913. https://doi.org/10.1016/j.jaridenv.2007.11.007
Belsky, A. J., & J. L. Gelbard. 2000. Livestock grazing and weed invasions in the arid West. Oregon Natural Desert Association.
Bran, D., M. Damascos, C. López, J. Ayesa, F. Umaña, & H. Moraga. 2003. Distribución, abundancia y disponibilidad de frutos de rosa mosqueta en la Provincia de Neuquén. Patagonia Forestal 10:6-8.
Campos, M., & R. Ojeda. 1997. Dispersal and germination of Prosopis flexuosa (Fabaceae) seeds by desert mammals in Argentina. Journal of Arid Environment 35:707-714. https://doi.org/10.1006/jare.1996.0196
Chuong, J., J. Huxley, E. N. Spotswood, L. Nichols, P. Mariotte, & K. N. Suding. 2016. Cattle as dispersal vectors of invasive and introduced plants in a California annual grassland. Rangeland ecology & management 69:52-58. https://doi.org/10.1016/j.rama.2015.10.009
Cosyns, E., S. Claerbout, I. Lamoot, & M. Hoffmann. 2005. Endozoochorous seed dispersal by cattle and horse in a spatially heterogeneous landscape. Plant Ecology 178:149-162. https://doi.org/10.1007/s11258-004-2846-3
Dacar, M. A., & S. M. Giannoni 2001. Technical note: A simple method for preparing reference slides of seed. Journal of Range Management 54:1914-193. https://doi.org/10.2458/azu jrm v54i2 dacar
Dalmasso, A. D., M. Almirón, & N. Arroyo. 2011. Cerramientos vivos con especies nativas y exóticas rústicas. Experimentia 1:3-56.
Damascos, M. A., & G. G. Gallopin. 1992. Ecología de un arbusto introducido (Rosa rubiginosa L.= Rosa eglanteria L.): riesgo de invasión y efectos en las comunidades vegetales de la región andino-patagónica de Argentina. Revista Chilena de Historia Natural 65:395-407. https://doi.org/10.1127/phyto/16/1988/465
Damascos, M. A., A. H. Ladio, A. E. Rovere, & L. Ghermandi. 2005. Semillas de rosa mosqueta: dispersión y germinación en diferentes bosques nativos andino-patagónicos. Patagonia Forestal 11:1-6.
Damascos, M. A. 2008. La rosa mosqueta y otras rosas. 1ª ed.- Río Negro. Centro Regional Universitario Bariloche. Universidad Nacional del Comahue.
Danell, K., R. Bergström, P. Duncan, & J. Pastor. 2006. Large herbivore ecology, ecosystem dynamics and conservation. Cambridge University Press, UK. https://doi.org/10.1017/cbo9780511617461
Davis, M. A. 2009. Invasion biology. Oxford University Press, New York.
Gardener, C. J., J. G. Mcivor, & A. Jansen. 1993. Survival of seeds of tropical grassland species subjected to bovine digestion. Journal of Applied Ecology 30:75–85. https://doi.org/10.2307/2404272
Gordon, L. 1995. Animal based techniques for grazing ecology research. Small Ruminant Research 16:203-214. https://doi.org/10.1016/0921-4488(95)00635-x
Gudiño De Muñoz, M. E. 2002. Impacto de la obra Presa Potrerillos en los habitantes de la villa y su entorno inmediato. Revista Proyección Nº 2, editada por CIFOT, Facultad de Filosofía y Letras, Universidad Nacional de Cuyo, ISSN 1667-0876. https://doi.org/10.24310/analecta.2017.v39i1.5655
Guevara, J. C, O. R. Estévez, C. R. Stasi, & A. S. Monge. 1996. Botanical composition of the seasonal diet of cattle in the rangelands of the Monte Desert of Mendoza, Argentina. Journal of Arid Environments 32:387-394. https://doi.org/10.1006/jare.1996.0032
Guevara, J. C., M. B. Bertiller, O. R. Estevez, E. G. Grünwaldt, & L. Allegretti. 2006. Pastizales y producción animal en las zonas áridas de Argentina. Sécheresse 17:242-56.
Hatton, T. J. 1989. Spatial patterning of sweet briar (Rosa rubiginosa) by two vertebrate species. Australian Journal of Ecology 14:199-205. https://doi.org/10.1111/j.1442-9993.1989.tb01427.x
Heady, H. F., & R. D. Child. 1994. Rangeland Ecology & Management. Westwiew Press. Boulder, San Francisco, Oxford. 519 pp.
Herrera, C. M. 1995. Plant–vertebrate seed dispersal systems in the Mediterranean: ecological, evolutionary, and historical determinants. Annual Review of Ecology and Systematics 26:705–727. https://doi.org/10.1146/annurev.ecolsys.26.1.705
Holechek, J., & B. Gross. 1982. Evaluation of different calculation procedures for microhistological analysis. Journal of Range Management 35(6):721-726. https://doi.org/10.2307/3898248
Howe, H.f., & J. Smallwood. 1982. Ecology of seed dispersal. Annual Review of Ecology and Systematics 13:201–228. https://doi.org/10.1146/annurev.es.13.110182.001221
Izhaki, I., & G. Ne’eman. 1997. Hares (Lepus spp.) as seed dispersers of Retama raetam (Fabaceae) in a sandy landscape. Journal of Arid Environment 37:343-354. https://doi.org/10.1006/jare.1997.0273
Janzen, D. H. 1984. Dispersal of small seeds by big herbivores: foliage is the fruit. The American Naturalist 123(3):338-353. https://doi.org/10.1086/284208
Joublan, J. P., M. Berti, H. Serri, R. Wilckens, F. Hevia, & I. Figueroa. 1996. Wild rose germplasm evaluation in Chile. Progress in New Crops (J. Janick, ed.). American Society for Horticultural Science, Arlington, VA. p. 584-588.
Kot, M., M. A. Lewis, & P. Van Den Driessche. 1996. Dispersal data and the spread of invading organisms. Ecology 77:2027-2042. https://doi.org/10.2307/2265698
Leege, T. A., D. J. Herman, & B. Zamora. 1981. Effects of cattle grazing on mountain meadows in Idaho. Journal of Range Management 34:324-328. https://doi.org/10.2307/3897861
Liebman, M., & T. Ohno. 1998. Crop rotation and legume residue effects on weed emergence and growth: Applications for weed management. Integrated Weed and Soil Management (J. L. Hatfield, D. O. Buhler & B. A. Stewart, eds.). ANN ARBOR Press, Michigan. p. 181-221.
Lloyd, C. 2014. Avances en el control de rosa mosqueta. Medio Ambiente 23:103-106.
Lockwood, J. L., M. F. Hoopes, & M. P. Marchetti. 2007. Invasion Ecology. Blackwell Publishing, Oxford. 304 pp.
Macdonald, I. A. W., L. L. Loope, M. B. Usher, & O. Hamann. 1989. Wildlife conservation and the invasion of nature reserves by introduced species: a global perspective. Biological invasion: A global perspective p. 215-256.
Martínez Carretero, E., A. Dalmasso, C. Boccolini, R. Tobares, & C. Robledo. 2006. Evaluación de especies exóticas en la Reserva Natural Villavicencio, Precordillera Andina, Mendoza, Argentina. Manual para productores cercas vivas Nº 1 pág. 18.
Méndez, E. 2007. Pérdidas de biodiversidad vegetal en ambientes de cerrilladas pedemontanas de Mendoza, Argentina. Rev. FCA UNCuyo. Tomo XXXIX. N° 1, pp. 107-116.
Moore, R. P. 1985. Handbook on Tetrazolium Testing. Zurich: International Seed Testing Association.
Parsons, C. T., P. A. Momont, T. Delcurto, M. Mcinnis, & M. L. Porath. 2003. Cattle distribution patterns and vegetation use in mountain riparian areas. Journal of Range Management 56:334-341. https://doi.org/10.2307/4004036
Peco, B., L. López-merino, & M. Alvir. 2006. Survival and germination of Mediterranean grassland species after simulated sheep ingestion: ecological correlates with seed traits. Acta Oecologica 30:269–275. https://doi.org/10.1016/j.actao.2006.05.004
Pelliza-Sbriller, A., & L. Sepúlveda. 2008. La rosa mosqueta, el colilargo patagónico y el hantavirus. Desde la patagonia difundiendo saberes 5(6).
Pérez, M. A., & J. A. Argüello. 1997. Determinación del vigor por tetrazolio en semillas de maní (Arachis hypogaea L.) bajo distintas condiciones de almacenamiento. Agriscientia XIV:1924.
Provenza, F. D., & D. F. Balph. 1988. Development of dietary choice in livestock on rangelands and its implications for management. Journal of Animal Science 66:2356-2368. https://doi.org/10.2527/jas1988.6692356x
Rundel, P. W., P. E. Villagra, M. O. Dillon, S. Roig-juñent, & G. Debandi. 2007. Arid and semi-arid ecosystems. The physical Geography of South America (T.T. Veblen, K. Young & A. E. Ormeeds, eds.). Oxford University Press.
Sih, A., & B. Christensen. 2001. Optimal diet theory: when does it work, and when and why does it fail? Animal Behaviour 61:379-390. https://doi.org/10.1006/anbe.2000.1592
Simberloff, D., & B. Von Holle. 1999. Positive interactions of nonindigenous species: invasional meltdown? Biological Invasions 1:21–32.
Traveset, A. 1998. Effect of seed passage through vertebrate frugivores’ guts on germination: a review. Perspectives in Plant ecology, evolution and systematics 1:151-190. https://doi.org/10.1078/1433-8319-00057
Van Horne, B., R.l. Schooley, & P.b. Sharpe. 1998. Influence of habitat, age, and drought on the diet of Townsends ground squirrels. Journal of Mammalogy 79:521-537. https://doi.org/10.2307/1382983
Vitousek, P., C. D’antonio, L. Loope, M. Rejmanek, & R. Westbrooks. 1997. Introduced species: a significant component of human-caused global change. New Zealand Journal of Ecology 21:1-16.
Whittaker, R. H., & P. P. Feeny. 1971. Allelochemicals: Chemical interactions between species. Science 171:757-770. https://doi.org/10.1126/science.171.3973.757
Wood, G. W., & D. N. Roark. 1980. Food habits of feral hogs in coastal South Carolina. Journal of Wildlife Management 44:506–511. https://doi.org/10.2307/3807990
Zar, J. H. 1999. Biostatistical Analysis. Prentice-Hall, Upper Saddle River, New Jersey, USA. 636 pp.
Zimmermann, H. et al. 2011. Habitat invasion risk assessment based on Landsat 5 data, exemplified by the shrub Rosa rubiginosa in southern Argentina. Austral Ecology 36:870-880. https://doi.org/10.1111/j.1442-9993.2010.02230.x
Información adicional
Editor asociado: L. Guichón
