ARTÍCULO
EFECTO DE LOS REGÍMENES DE MANEJO EN LA OCUPACIÓN DE MAMÍFEROS EN UN CORREDOR DE CONSERVACIÓN EN EL SUDESTE DE LA AMAZONIA PERUANA
THE EFFECT OF MANAGEMENT REGIMES ON MAMMAL OCCUPANCY IN A CONSERVATION CORRIDOR IN THE SOUTHEASTERN PERUVIAN AMAZON
EFECTO DE LOS REGÍMENES DE MANEJO EN LA OCUPACIÓN DE MAMÍFEROS EN UN CORREDOR DE CONSERVACIÓN EN EL SUDESTE DE LA AMAZONIA PERUANA
Mastozoología Neotropical, vol. 28, núm. 1, p. 435, 2021
Sociedad Argentina para el Estudio de los Mamíferos
Recepción: 16 Marzo 2020
Aprobación: 19 Febrero 2021
Resumen: Los corredores de conservación constituyen una estrategia interesante ante la realidad de la conversión de bosque por áreas agrícolas. Con base en modelos bayesianos de ocupación multiespecies analizamos la ocupación de las especies de mamíferos a lo largo del corredor de conservación Manu-Tambopata (4 164.06 km2), ubicado en la Amazonia sur de Perú. Instalamos 102 cámaras trampa durante mayo y octubre del 2017 (8 104 días-cámara) en los regímenes de manejo que caracterizan al corredor: la concesión para la conservación Río Los Amigos, concesiones forestales (ACOMAT), la Reserva Nacional Tambopata y predios agrícolas. Se registraron 27 especies de mamíferos terrestres; sin embargo, el modelo no reveló diferencias significativas en la riqueza de especies en los cuatro regímenes de manejo, aunque sí se evidenció un efecto de la densidad de borde sobre la ocupación a escala de la comunidad. Ninguna de las especies comúnmente cazadas, con la excepción de la huangana (Tayassu pecari), evidenciaron diferencias en sus valores de ocupación en los regímenes de manejo; no obstante, la ocupación del perro de monte (Atelocynus microtis) y el jaguar (Panthera onca) fueron significativamente menores en los predios agrícolas. Nuestros resultados sugieren que en general los regímenes de manejo no tuvieron un efecto a escala de la comunidad, pero sí efectos específicos de las covariables (densidad de borde y distancia a vías) para algunas especies (e.g., A. microtis). El corredor MAT es aún un espacio en donde es factible mantener poblaciones saludables de mamíferos, aunque su viabilidad en el largo plazo requiere de asegurar conectividad tanto a nivel funcional como estructural.
Palabras clave: Amazonia peruana, cámaras-trampa, corredor de conservación, densidad de borde, modelo de ocupación multiespecies.
Abstract: Conservation corridors are an interesting strategy considering the increasing forest conversion by agricultural areas. We used Bayesian multispecies occupancy model in order to assess the occupancy of mammal species along the Manu-Tambopata conservation corridor (4 164.06 km2), located in the southern Peruvian Amazon. We installed 102 camera traps between May and October of 2017 (8 104 camera days), in four management regimes: Río Los Amigos conservation concession, forestry concessions (ACOMAT), Tambopata National Reserve and agricultural lands. Twenty-seven species of terrestrial mammals were recorded; however, models did not reveal significant differences in species richness among management regimes, although an effect of edge density on community-level occupancy was evident. Non-significant relationships were found between commonly hunted species and management regimes, apart from the white-lipped peccary; however, short-eared dog (Atelocynus microtis) and jaguar (Panthera onca) occupancy were significantly lower on agricultural lands. Our results suggested that, in general, the management regimes and covariables (edge density and distance to roads) did not have an effect at the community level but did have species-specific effects for some species (e.g., A. microtis). MAT corridor is still a space where it is feasible to maintain healthy populations of mammals, although its long-term viability requires ensuring connectivity at both a functional and structural levels.
Keywords: Camera traps, conservation corridor, edge density, multispecies occupancy model, Peruvian Amazon.
INTRODUCCIÓN
La pérdida y la fragmentación de los hábitats se encuentran entre las principales amenazas a la vida silvestre (Bennett & Saunders 2010; Olsoy et al. 2016; Tilman et al. 2017; Fletcher 2018). En el caso de la fragmentación, esta no solo disminuye el hábitat total disponible, sino que, además, aísla el hábitat remanente de forma simultánea, dificultando el movimiento de los organismos y la dinámica de los procesos ecológicos (Fahrig 2003, 2017). Desafortunadamente, la tendencia actual en los ecosistemas, particularmente en los bosques tropicales, está marcada por la fragmentación y pérdida de hábitat derivada de la conversión de los hábitats naturales a usos agrícolas o urbanos (Lewis & Maslin 2015; Monastersky 2015).
Los corredores han surgido como una de las estrategias para la conservación de la biodiversidad en los paisajes dominados por actividades humanas (Anderson & Jenkins 2012), los que, en los bosques tropicales, se caracterizan por la presencia de bosques continuos, bosques fragmentados y tierras agrícolas y ganaderas, entre otros tipos de usos. Estos corredores contribuyen a mantener la conectividad, concepto ampliamente utilizado en ecología del paisaje (Crooks & Sanjayan 2006; Turner & Gardner 2015; Hilty et al. 2019). En ese sentido, se han definido dos tipos principales de conectividad: la conectividad estructural, la cual explica el orden espacial de los distintos tipos de hábitats o elementos de un paisaje, y la conectividad funcional, la cual consiste en la respuesta conductual de los individuos, los taxones y los procesos ecológicos a la estructura física del paisaje (Turner & Gardner 2015; Hilty et al. 2019). En el caso particular de la conectividad estructural, para que esta sea efectiva, se requiere de la existencia de áreas con un alto estatus de conservación, tales como las áreas protegidas, así como áreas con sistemas productivos que son compatibles con la conservación de la biodiversidad, incrementando la calidad de hábitat y la coexistencia de las especies (Kremen & Merenlender 2018; Hilty et al. 2019; Shahnaseri et al. 2019).
El estudio de la pérdida de hábitat para la fauna requiere un enfoque a una mayor escala especial (i.e., escala de paisaje), y la identificación de grupos de especies que sean sensibles a la escala en la cual operan tanto la pérdida de hábitat y la fragmentación (i.e., escala de paisaje), así como a las distintas formas de uso de la tierra presentes (Khosravi & Hemami 2019). Así mismo, el análisis de la respuesta específica de las especies a las características del paisaje puede extenderse al análisis en la composición del paisaje a nivel de la comunidad, lo que es fácilmente integrado en un marco de modelación jerárquica (Guillera-Arroita et al. 2018). Precisamente, los modelos de ocupación son modelos jerárquicos útiles para evaluar el uso del espacio que hacen las especies a lo largo de un gradiente de calidad del hábitat y con una base probabilística (Royle & Dorazio 2008; Kéry & Royle 2016). En particular, los modelos de ocupación con múltiples especies que coexisten se conocen también como modelos de ocupación de comunidades, en los cuales se estima la variable de estado “riqueza de especies”; pero también se incluye el análisis a nivel especie-específico, en ambos casos incorporando covariables tanto a nivel de detección como de la ocupación, y bajo un enfoque bayesiano (Kéry 2011; Kéry & Royle 2016; Guillera-Arroita et al. 2018). Justamente, estas covariables pueden ser aquellas que tienen sentido a escala de paisaje, tales como la cobertura de bosque o la densidad de borde (Hilty et al. 2019; Presley et al. 2019). Igualmente, se puede incluir factores como el tipo de uso (regímenes de manejo), si esta es un área protegida, un área perturbada, o un área bajo manejo (Zipkin et al. 2010; Dechner et al. 2018), todas estas en el ámbito de corredores de conservación.
Los mamíferos son uno de los grupos taxonómicos más amenazados debido a la pérdida y degradación de sus hábitats (Schipper 2008; Alonso-F et al. 2017). Además, son un grupo que cumple roles críticos en los ecosistemas (Lacher 2019). No menos importante, debido a sus requerimientos de hábitat y de espacio, muchos de los mamíferos medianos y grandes requieren ser estudiados precisamente a una escala de paisaje (Crooks et al. 2011; Presley et al. 2019). El objetivo de este estudio fue, con base en modelos de ocupación de comunidades, analizar la ocupación de las especies de mamíferos a lo largo de un gradiente de perturbación en el paisaje de conservación denominado corredor Manu-Tambopata (en adelante MAT), ubicado en el sureste de la Amazonia peruana. Formulamos la hipótesis de que la riqueza de especies de mamíferos está afectada por los regímenes de manejo; en particular, se prevé una riqueza de mamíferos menor en áreas perturbadas en comparación a la de los otros regímenes de manejo en MAT. Así, predecimos que la ocupación de las especies estará relacionada positivamente con la distancia a las áreas perturbadas, especialmente para aquellas especies sensibles a la perturbación antropogénica (i.e. herbívoros y carnívoros grandes) (Bodmer et al. 1997; Naughton-Treves et al. 2003).
MATERIALES Y MÉTODOS
Área de estudio
El corredor MAT comprende un área de ∼ 4 164 km2 ubicado en el sur de la Amazonia peruana, en el departamento de Madre de Dios (Fig. 1). El corredor MAT presenta al menos cuatro regímenes de manejo representativos, los cuales cuentan con distintos niveles de protección (Tabla. 1, Fig. 1). La concesión para la conservación “Río los Amigos” (en adelante “Los Amigos”) es una concesión de conservación privada de 1 460 km2 creada en el 2001 con la finalidad de conservar una muestra representativa del ecosistema natural en la cual no se practican actividades tales como la tala o la cacería. Por otro lado, las concesiones forestales con fines de forestación o reforestación AGROFOCMA y la concesión con fines maderables EPEFOMGS SAC, las cuales forman parte de la Asociación de Concesionarios Forestales Maderables y no Maderables de las provincias del Manu y Tambopata (en adelante “ACOMAT”), constituyen una modalidad de derechos otorgados para la conservación y aprovechamiento de recursos naturales maderables y en donde además es posible desarrollar actividades de caza (∼ 1 890 km2). Los predios agrícolas (en adelante “predios”) a lo largo de la carretera Interoceánica constituyen una matriz heterogénea de cultivos agrícolas y agroforestales que conforman las áreas perturbadas (∼ 370 km2). Finalmente, el extremo norte de la Reserva Nacional Tambopata (2 747 km2), la cual constituye un área protegida por el Estado peruano que tiene permitido el uso directo de recursos de flora y fauna silvestre, a excepción de los recursos maderables, como parte de un aprovechamiento ancestral sostenible por las comunidades nativas aledañas (en adelante “RNT”) (Tabla. 1).
Colección de datos con cámaras trampa
El estudio se realizó en los regímenes de manejo más representativos del corredor MAT (ver Tabla. 1) entre el 3 de mayo y el 2 de octubre del 2017, con un total de 102 estaciones – cámara (27 en Los Amigos, 21 en ACOMAT, 19 en los predios y 35 en RNT) las que cubrieron un área de ∼ 450 km2 (Tabla. 1). En cada estación se instaló una cámara-trampa (Bushnell Trophy Cam HD), generalmente en un árbol o en una estaca a una altura de aproximadamente 40 cm del suelo. Por lo general, las estaciones fueron distanciadas a ∼ 2 km una de la otra siguiendo protocolos previos de otros estudios (Team 2011; Rovero & Zimmermann 2016).
Las fotografías fueron ingresadas a “cámera base“ (Tobler 2015), desde donde se obtuvieron los historiales de detección para cada especie. Agrupamos los datos de detecciones en cada sitio en períodos de muestreo de 14 días. El número mínimo de períodos fue de 1 para estaciones en dónde las cámaras estuvieron operativas ≤ 14 días, hasta un máximo de 11 períodos (Tabla. 1). Esta estrategia reduce el problema de la heterogeneidad causada por períodos cortos de gran actividad en algunas cámaras, además de mejorar el problema asociado a bajas detecciones (múltiples ceros en los historiales de detecciones) y sobre dispersión en los datos (Tobler 2015). Así, el historial de detección se elaboró con base en los períodos de muestreo de 14 días, siendo 0 si estuvo ausente y 1 si estuvo presente durante cada período de 14 días y por cada estación evaluada.
Covariables
Utilizamos covariables que potencialmente afectan la probabilidad de ocupación de los mamíferos presentes en el área de estudio (Material Suplementario, Tabla S1 y S2). Estas fueron la cobertura de bosque, la densidad de borde y la distancia a vías (distancia euclidiana). La cobertura de bosque y la densidad de borde son variables que describen la estructura del paisaje (Presley et al. 2019) y la distancia a vías fue usada como un indicador de perturbación (distancia euclidiana). Para la estimación de estas variables se delimitaron áreas circulares de radio a 200, 400 y 800 m, con centro en la ubicación de cada cámara, siguiendo un enfoque multiescalar, el cual es apropiado para evaluar la respuesta de las especies a la disponibilidad de hábitat (Laforge et al. 2016; Boyce et al. 2017), o en todo caso para conocer la escala en la cual es más evidente la respuesta de las especies a la variación en las características del paisaje. Estas tres áreas circulares reflejan un continuo de escalas, en el cual el radio mínimo (200 m) captura cuantitativamente la variación del hábitat con base en la resolución de la información espacial usada (Tabla S1, Material Suplementario) y el radio máximo (800 m) evita el traslape con los círculos alrededor de las estaciones cámara vecinas (Niedballa et al. 2015; Laforge et al. 2016), además de incluir el rango de hogar de varias de las especies registradas (Benchimol & Peres 2015).
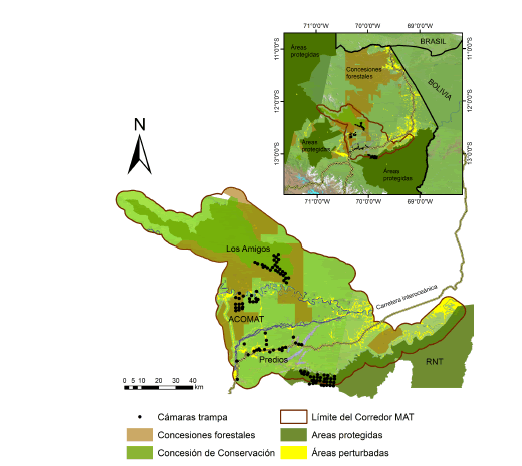
Fig. 1.
Ubicación de las cámaras trampas en el área de estudio en el corredor MAT.
Usando como base datos nacionales oficiales (Tabla S1, Material Suplementario), las estimaciones se realizaron utilizando mapas en formato ráster con un Sistema de información geográfica (ESRI*ArcGIS 10.5, Redlands, California-ESRI, 2018). La cobertura de bosque y la densidad de borde se calcularon usando Fragstat (Mcgarigal et al. 2012). Realizamos una prueba de colinealidad (Zuur et al. 2013; Kéry & Royle 2016), mediante el uso del factor de inflación de varianza (VIF) con el paquete HH (Heiberger & Holland 2015). Luego del análisis de colinealidad se descartó la cobertura de bosque debido a su alta correlación con la densidad de borde. Las variables se estandarizaron para tener promedio cero y una varianza de uno para facilitar la interpretación de los tamaños del efecto relativo de las variables en el modelo (Kéry & Royle 2016). Dos de las covariables (distancia a cuerpos de agua y distancia a vías) están relacionadas con la accesibilidad (por ejemplo, para la cacería), pero consideramos solo la distancia a vías como un indicador de perturbación en esos términos. En el caso de distancia a cuerpos de agua, esta se encuentra asociada, además, de acuerdo con la literatura, con las preferencias de hábitat de especies como los tapires (Tapirus terrestris) (Tobler et al. 2010; Ferreguetti et al. 2017) y las huanganas (Tayassu pecari) (Tobler et al. 2009; Reyna-Hurtado & Chapman 2019), y como un atrayente natural que afecta la detección (Burton 2015).
Modelo de ocupación multiespecies
Usamos un modelo bayesiano de ocupación multiespecies (Tobler 2015; Li et al. 2018) desarrollado con base en el modelo de ocupación de Royle Nichols (RN) (Royle & Nichols 2003). El modelo de RN ha sido recomendado previamente para datos que provienen de cámaras-trampa, las cuales se caracterizan por una gran heterogeneidad en la detección (Tobler 2015). Este modelo fue usado para analizar cómo los distintos regímenes de manejo presentes en MAT y las covariables afectan la ocupación a nivel de comunidades y a nivel de especies. Para algunas especies tales como el jaguar (Panthera onca), el jaguarundi (Puma yaguaroundi), el coatí (Nasua nasua) y la huangana (Tayassu peccari), entre otras, el distanciamiento entre cámaras fue menor que el diámetro del rango de hogar reportado para estas especies (De Oliveira 1998; Michalski et al. 2006; Guilherme Trovati et al. 2010; Morato 2016). En particular, los modelos de ocupación requieren que la distancia entre sitios sea igual o mayor que el rango de hogar; no obstante, cuando este requisito no se cumple, la interpretación que corresponde es la de probabilidad de uso de sitio en vez de la de ocupación (Mackenzie 2015; Mackenzie et al. 2018), lo cual aplica para la mayoría de las especies que se registraron en este estudio. Para propósitos del estudio, asumimos que el pool de especies permaneció constante durante la evaluación (i.e. criterio de población cerrada).
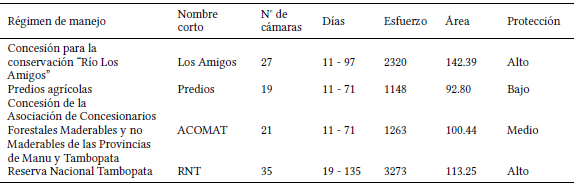
De acuerdo a lo propuesto por Li et al. (2018), el modelo define wil como una variable binaria latente en la cual wil = 1 si la especie i está presente en el régimen de manejo l, y 0 si la especie está ausente. En este caso wil es una variable aleatoria Bernoulli definida como wil∼ Bernoulli(Ωi), en donde Ωi es una proporción que varía entre 0 y 1, y puede ser interpretada como la probabilidad de ocupación al nivel del régimen de manejo. El modelo define zij como la variable binaria que indica el estado de ocurrencia de la especie i en la estación j, la cual se asume que es resultado de un proceso Bernoulli, definido como zij ∼ Bernoulli(wilxψij), en donde ψij es la probabilidad que la estación j sea usada por la especie i. El modelo estima la abundancia local de la especie i en la estación j(aij) usando una distribución Poisson con el parámetro λij y definida como aij ∼ Poisson(λij); siendo λij la abundancia local esperada de la especie i en la estación j. La probabilidad de ocupación en el modelo de RN es una variable derivada de la abundancia local (ψij = Pr(aij > 0) = 1 − eλij ), la cual puede ser usada sin necesidad de hacer alguna inferencia sobre la abundancia.
Las covariables asociadas a la ocupación como la densidad de borde (DB) y la distancia a vías (DV) fueron añadidas al modelo lineal como ENV (un agrupamiento operativo de las covariables), las cuales en su conjunto permiten estimar la abundancia esperada para la especie i en el sitio j:
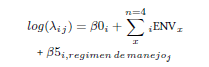
Para la variable régimen de manejo se utilizó a los predios como línea de base en el modelo siendo representado por el parámetro intercepto. β0i es el intercepto específico a la especie y βxi son los coeficientes de regresión especie – específicos para las covariables incluidas en ENV. En el caso de la detectabilidad, la probabilidad rij que un individuo de la especie i fuera detectado en la estación j se modeló en función de la distancia a cuerpos de agua y el régimen de manejo. De esta manera, nuestros datos de detección yij provienen de una distribución binomial yij ∼ Binomial(kj, 1 − (1 − rij)aij), en donde kj indica el número de ocasiones de muestreo (períodos) en que cada cámara estuvo activa:
log(rij) = α0i + α1i, distancia a cuerpos de agua x distancia a cuerpos de aguaj + α2i, regimen de manejoj
Se realizaron tres modelos, uno para cada escala (200, 400 y 800 m). Los modelos fueron conducidos bajo un enfoque bayesiano en JAGS (Plummer 2003) usando el paquete R2jags en R (R Core Team 2020). Usamos previas planas como ha sido recomendado para este tipo de modelos (Kéry & Royle 2016). El modelo corrió con tres cadenas paralelas con una longitud de 50 000 después de un burn-in de 20 000 iteraciones y un thinning rate de 10. Evaluamos la convergencia a través del estadístico de Gelman-Rubin, el cual debe ser cercano a 1 (Gelman et al. 2014). Así mismo, evaluamos la adecuación del modelo usando un P-valor bayesiano basado en la discrepancia X2 de Pearson (Kéry 2010). El P-valor bayesiano se define como la probabilidad Pr (X2obs < X2sims), la cual, si presenta valores mayors que 0.95 o menores a 0.05, es un indicativo de falta de ajuste (valores cercanos a 0.5 son indicativos de un modelo ajustado). Además, calculamos la carencia de ajuste estadístico X2obs/X2sims, la cual se espera que sea igual a 1 si el modelo se ajusta bien a los datos (Kéry & Schaub 2012; Tobler 2015). Los detalles del modelo para cada escala se muestran en el Material Suplementario
RESULTADOS
Con un esfuerzo total de 8 104 días-cámara registramos 27 especies de mamíferos (ver Material Suplementario, Tablas S4 – S9), de las cuales 26 fueron registradas en la Reserva Nacional Tambopata, 24 en los predios y 23 tanto en Los Amigos como en la concesión de conservación ACOMAT. Las especies con mayores detecciones fueron los venados (Mazama spp., 357 detecciones), seguidos del picuro (Cuniculus paca, 258), el sajino (Pecari tajacu, 247), y el tapir (Tapirus terrestris, 207). Especies con menos de 5 detecciones fueron el ronsoco (Hydrochoerus hydrochaeris), el mapache (Procyon cancrivorus) y el hurón (Galictis vittata).
Los modelos de comunidades tuvieron Pbayesiano de 0.86, 0.87 y 0.87 para las escalas de 200, 400 y 800 m respectivamente (con un ajuste de 1.08 en cada caso), lo cual revela que obtuvimos modelos aceptables (ver Material Suplementario, Fig. S1). La variación en la riqueza de especies posterior estimada para cada régimen fue muy similar en todas las escalas (Material Suplementario, Tabla S3). Por ejemplo, para la escala a 800 m, la riqueza fue ligeramente mayor en la Reserva Nacional Tambopata con 26.13 especies (intervalo creíble bayesiano del 95%, ICB: 26.11 – 26.15), y similar para los otros regímenes, siendo para ACOMAT 24.29 (95% ICB: 24.26 – 24.33), para Los Amigos 23.94 (95% ICB: 23.91 – 23.98) y para los predios 24.16 (95% ICB: 24.12 – 24.20) (Fig. 2).
Las distribuciones posteriores para los parámetros a nivel de la comunidad sugieren un efecto positivo de la densidad de borde (basado en los coeficientes beta, ICB del 95% no incluyó 0) (Fig. 3) que parece ser dependiente de la escala, ya que fue evidente solo a 800 m. No se encontró sustento para un efecto de la distancia a vías para la ocupación a escala de la comunidad, ni de la distancia a cuerpos de agua para la detectabilidad en ninguna de las escalas (el 95% y 90% ICB traslaparon con cero en ambos casos).
Los resultados del modelo a nivel especie-específico revelan efectos dependientes de la escala en la densidad de borde y la distancia a vías, aunque solo para algunas especies (Fig. 4). Por ejemplo, con base en los coeficientes beta, se encontró sustento para un efecto positivo (en todas las escalas) de la densidad de borde sobre la probabilidad de ocupación de la liebre amazónica Sylvilagus brasiliensis (sin traslape con cero al ICB del 95%). Por otro lado, se encontró sustento de un efecto negativo de la densidad de borde sobre la ocupación del perro de monte (Atelocynus microtis) a la escala de 800 m y marginal en la escala de 200 m (ICB del 95% incluyó 0, pero no al 90%); sobre la ocupación del añuje (Dasyoprocta variegata) a la escala de 400 y 800 m y marginal a la escala de 200 m; y marginal a 200 y 800 m para el margay (Leopardus wiedii). Similarmente, se encontró sustento para un efecto negativo de la distancia a vías sobre la probabilidad de ocupación de la zarigüeya común (Didelphis marsupialis) a 200 y 400 m, y del liebre (Sylvilagus brasiliensis) a 400 m; además de un efecto positivo pero marginal para el caso de los venados (Mazama spp.) en todas las escalas; y para el tapir (Tapirus terrestris) y el perro de monte tanto a 400 y 800 m. Por otro lado, se encontró sustento para un efecto positivo de la distancia a cuerpos de agua sobre la probabilidad de detección del majás (Cuniculus paca) y de los armadillos (Dasypus spp.) en las tres escalas.
La probabilidad de ocupación de las especies fue relativamente similar entre los diferentes regímenes de manejo y escalas analizados, con la excepción de la huangana, la cual tuvo su valor más bajo en Los Amigos (0.01 ± 0.08) en comparación a la de los otros regímenes (>0.50) en la escala a 800 m (similar en las otras escalas). Así mismo, la probabilidad de ocupación del perro de monte (0.13 ± 0.23), el jaguar (Panthera onca) (0.10 ± 0.23) y la punchana (Myoprocta pratti) (0.12 ± 0.15) fue notoriamente menor en los predios en comparación a la de los otros regímenes (>0.50, >0.56, y >0.25, respectivamente) (ver Material Suplementario, Tabla S4 – S9).
DISCUSIÓN
En el contexto actual de reemplazo del bosque tropical por tierras agrícolas y el incremento de los paisajes antropogénicos, iniciativas como los corredores de conservación requieren de una evaluación de sus contribuciones reales a la conservación de la biodiversidad. Uno de esos ejemplos es el corredor MAT, el cual constituye una propuesta oportuna considerando la continua pérdida de bosque en los últimos años, debido al incremento de la minería ilegal aurífera en Madre de Dios (Swenson et al. 2011) y los consecuentes impactos en el medioambiente (Kahhat et al. 2019). No obstante, los resultados encontrados parecen alentadores. En efecto, no encontramos diferencias en la riqueza de especies de los cuatro regímenes de manejo de la tierra analizados; inclusive, la riqueza encontrada en los predios es similar a la de áreas como Los Amigos que cuenta con un nivel de protección mayor y, a su vez, ligeramente menor al de la Reserva Nacional Tambopata. En ese sentido, los datos sugieren que no hay evidencias para apoyar la hipótesis propuesta. Varios estudios han sugerido que bajo ciertos niveles de perturbación y en paisajes que incluyen un mosaico de bosques y tierras bajo uso antropogénico, la riqueza de especies de mamíferos puede mantener niveles tan altos como aquella encontrada en los bosques originales (Medellín & Equihua 1998; Naughton-Treves et al. 2003). Los predios se encuentran colindantes a extensas áreas de bosque con mayor calidad de hábitat para la mayoría de las especies. Es probable que estos bosques tengan un rol clave en la dispersión de especies hacia los predios, siguiendo lo sugerido por uno de los paradigmas que explican la estructura de las metacomunidades: el efecto de masa (Leibold 2011; Leibold et al. 2018).
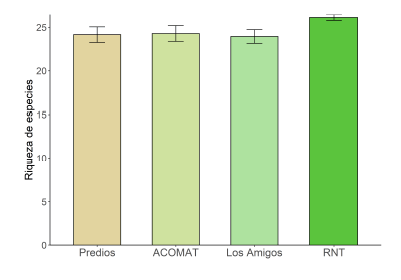
Fig. 2.
Riqueza de especies estimada en cada uno de los cuatro regímenes de manejo evaluados en el corredor Manu-Tambopata. Se muestra la desviación estándar respectiva en cada caso.
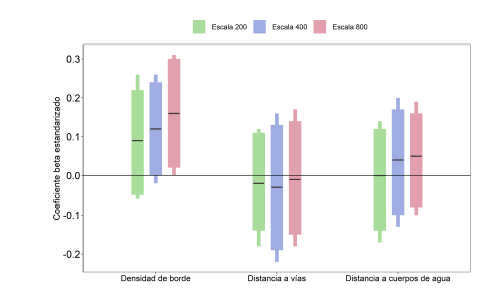
Fig. 3.
Respuesta de la probabilidad de ocupación promedio de la comunidad de mamíferos del corredor Manu-Tambopata a las covariables (densidad de borde y distancia a vías) y de la probabilidad de detección a la distancia a cuerpos de agua con base en los coeficientes de regresión (β). La línea horizontal dentro de las barras es el promedio, la barra angosta es el intervalo creíble al 95%, y la barra amplia el intervalo creíble al 90%.
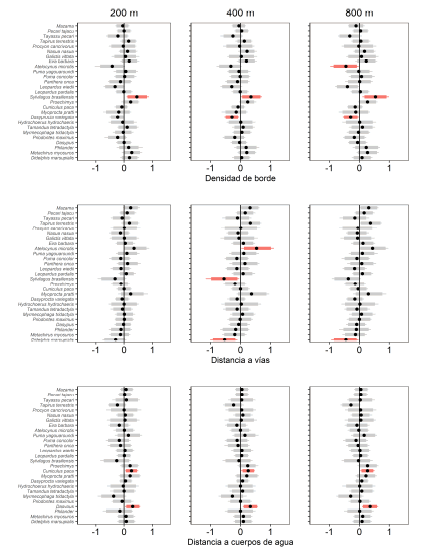
Fig. 4.
Respuesta de la probabilidad de ocupación (Ω) a las covariables de sitio (densidad de borde y distancia a vías) y de la probabilidad de detección (p) a la distancia a cuerpos de agua a nivel de especie. El punto indica la media, las barras anchas y delgadas indican los intervalos creíbles al 95% y 90% respectivamente. Efectos significativos en color rojo.
A pesar de que muchas especies de mamíferos medianos y grandes constituyen fuente de proteínas para las poblaciones locales, constituyendo uno de los servicios ecosistémicos más importantes en los bosques tropicales (Ohl-Schacherer et al. 2007; Endo 2009; Ramirez-Gomez 2015; Ripple 2016), en el presente estudio ninguna de las especies comúnmente cazadas en la Amazonia peruana (e.g. venados, sajinos, huangana, picuro, entre otras) (Loja et al. 2000; Hurtado-Gonzales & Bodmer 2004; Gavin 2007; Endo 2009; Mayor et al. 2015) evidenció diferencias significativas en sus valores de ocupación en los cuatro regímenes de manejo, desde aquellos con niveles altos o medios de protección hasta el nivel más bajo de protección (predios); ni con la distancia a vías, la cual es considerada como una covariable sustituta de la accesibilidad a caza. Desafortunadamente, no se logró obtener información de la población local respecto a la frecuencia e intensidad de la cacería; sin embargo, es importante mencionar que en las últimas décadas la migración hacia Madre de Dios, y en particular aquellos migrantes que colonizaron terrenos a lo largo de la carretera interoceánica, provienen de otras regiones del país en las cuales la cacería parece ser una actividad poco relevante (Urteaga 2003; Romero et al. 2005; De Echave et al. 2009; Rubio 2010). En todo caso, los resultados sugieren que podría existir una presión de caza mínima y que las especies en cuestión usan indistintamente los predios, haciendo uso de estas áreas de forma oportunista, lo cual ha sido también reportado en otros estudios y que, no menos importante, se encuentra obviamente condicionado a la existencia de áreas aledañas de bosque remanente (Naughton-Treves et al. 2003; Reyna-Hurtado & Tanner 2007; Tejeda-Cruz et al. 2009). De hecho, la deforestación presente en el área circundante a los predios podría ser considerada como menor, en comparación a la deforestación presente en la zona de uso por minería al noroeste del corredor y a lo largo de la carretera interoceánica (ver Fig. 1). Igualmente, no se podría descartar la dinámica fuente-sumidero como otra plausible explicación (Gilroy & Edwards 2017).
La probabilidad de ocupación de la huangana (T. pecari) en Los Amigos fue notablemente baja a diferencia del resto de áreas con niveles medios o bajos de protección. Esta especie fue anteriormente registrada como común en los Amigos (Tobler 2015). No obstante, aun cuando esta especie ha sido reportada como susceptible a la perturbación antropogénica y en particular a la presión de caza, las huanganas se caracterizan por patrones de movimiento y dispersión bastante dinámicos (Peres 1996; Keuroghlian et al. 2015; Reyna-Hurtado 2016), relacionados con sus amplios requerimiento de hábitat y patrones estacionales y anuales de movimiento (Fragoso 1998, 2004; Tobler et al. 2009; De Almeida Jácomo 2013; Hofman et al. 2016), lo cual podría explicar los bajos valores de probabilidad de ocupación durante el período de evaluación. Los resultados sugieren también que el perro de monte parece ser afectado negativamente por la calidad de hábitat (i.e., los predios, densidad de borde). De los pocos estudios realizados sobre el perro de monte, existe cierta evidencia que esta especie prefiere áreas de bosque lejos de las perturbaciones antropogénicas (Michalski 2010; Tobler 2015; Botelho et al. 2018), lo cual concuerda también con nuestros resultados. Por otro lado, los bajos valores en la ocupación del jaguar en los predios probablemente estén relacionados con una baja detección en este tipo de régimen, considerando que las cámaras no fueron ubicadas en trochas (caminos), los que son un atrayente natural para este felino (Sollmann 2011). De hecho, debido a su amplia plasticidad en el uso de hábitat, estos suelen usar también tierras agrícolas y ganaderas, sobre todo cuando sus presas naturales en el bosque son escasas (Foster et al. 2010; Morato 2016; Olsoy et al. 2016). Otra especie con bajos valores de ocupación en los predios fue M. pratti. Si bien no hay estudios sobre las preferencias de hábitat de esta especie (Patton et al. 2015), la menor ocupación encontrada en los predios coincide con lo reportado para M. acouchy, especie hermana que no frecuenta hábitats perturbados (Dubost 1988).
De acuerdo con los resultados y la disponibilidad de bosque en torno a los predios, es posible establecer corredores de vegetación que podrían ser sistemas productivos como parcelas agroforestales, que pueden servir además como vías para evitar el aislamiento de poblaciones de mamíferos a ambos lados de la carretera, y que además han demostrado ser efectivas en otras regiones (Pineda-Guerrero et al. 2015; Alonso-F et al. 2017; Piratelli et al. 2019). Otras opciones son pasos a desnivel o pasos para la fauna sobre la carretera, incluyendo puentes de dosel (Goosem et al. 2005; Teixeira et al. 2013; Gregory et al. 2017; Balbuena et al. 2019). Debido a que el presente estudio no consideró la evaluación del uso de la carretera como medio de paso de los mamíferos que habitan en el corredor, sería propicio conocer si esta representa una limitante en el uso de hábitat y dispersión de los mismos, tomando en consideración las diferencias en la resiliencia a la fragmentación entre los distintos gremios de la comunidad (Pinto et al. 2020).
Un mensaje que deja este estudio es que, a pesar de los niveles de perturbación de los predios, estos no afectan a gran parte de la comunidad de mamíferos medianos y grandes terrestres. No obstante, también es importante mencionar la importancia de áreas de gran cobertura forestal como aquellas presentes en los otros regímenes de manejo de la tierra (áreas protegidas o concesiones de conservación), las cuales constituyen áreas fuente para otras con menor calidad de hábitat. Así, el corredor MAT, a pesar de constituir un paisaje dominado por actividades humanas, es aún un espacio en donde es factible mantener poblaciones de mamíferos aunque su viabilidad en el largo plazo requiere de asegurar conectividad, tanto a nivel funcional como estructural, lo cual incluye, indudablemente, la disminución de la deforestación y la restauración de las áreas degradadas por la minería ilegal, asegurando así la coexistencia tanto para mamíferos silvestres como para seres humanos, y la provisión de servicios ecosistémicos.
Agradecimientos
Este trabajo no hubiera sido posible sin la colaboración de todas las entidades involucradas en la implementación de esta evaluación: el Servicio Nacional de Áreas Naturales Protegidas por el Estado (SERNANP), la Asociación para la Conservación de la Cuenca Amazónica (ACCA), a los concesionarios forestales de ACOMAT y la World Wildlife Fund, Perú. Así mismo, gracias a Luciano Huillca, Luis Villena, Vanessa Soto, Wilson Villa, Piero Rengifo y todos los colaboradores del equipo de ACCA que se involucraron en el desarrollo de este proyecto. Un agradecimiento especial a Ernesto Fernández, a los guardaparques de la Reserva Nacional de Tambopata y a los marinos de guerra del Perú por facilitarnos el ingreso a la reserva y a sus instalaciones. Finalmente, agradecer a Karla Ramos, Rubén Aviana y Juan Racua que participaron activamente en la instalación de cámaras trampa; y a Pamela Pastor que ayudó con el análisis espacial.
REFERENCIAS
Alonso-F, A. M., B. Finegan, C. Brenes, S. Günter, & X. Palomeque. 2017. Evaluación de la conectividad estructural y funcional en el corredor de conservación Podocarpus-Yacuambi, Ecuador. Caldasia 39:140-156. https://doi.org/10.15446/caldasia.v39n1.64324
Anderson, A. B., & C. N. Jenkins. 2012. Applying nature’s design: corridors as a strategy for biodiversity conservation. Columbia University Press, New York.
Balbuena, D., A. Alonso, M. Panta, A. Garcia, & T. Gregory. 2019. Mitigating Tropical Forest Fragmentation with Natural and Semi-Artificial Canopy Bridges. Diversity 11:66. https://doi.org/10.3390/d11040066
Benchimol, M., & C. A. Peres. 2015. Predicting local extinctions of Amazonian vertebrates in forest islands created by a mega dam. Biological Conservation 187:61-72. https://doi.org/10.1016/j.biocon.2015.04.005
Bennett, A. F., & D. A. Saunders. 2010. Habitat fragmentation and landscape change. Conservation Biology for All (N. S. Sodhi & P. R. Ehrlich, eds.). Oxford University Press.
Bodmer, R. E., J. F. Eisenberg, & K. H. Redford. 1997. Hunting and the likelihood of extinction of Amazonian mammals. Conservation Biology 11:460-466. https://doi.org/10.1046/j.1523-1739.1997.96022.x
Botelho, A. L. M., L. H. M. Borges, & B. McFarland. 2018. Abundance and composition of the medium to large-sized mammals in a private area of a REDD+ project in Acre, Brazil. Biota Neotropica 18. https://doi.org/10.1590/1676-0611-bn-2017-0487
Boyce, M. S., C. D. Mallory, A. T. Morehouse, C. M. Prokopenko, M. A. Scrafford, & C. H. Warbington. 2017. Defining Landscapes and Scales to Model Landscape–Organism Interactions. Current Landscape Ecology Reports 2:89-95. https://doi.org/10.1007/s40823-017-0027-z
Burton, A. C. et al. 2015. Wildlife camera trapping: a review and recommendations for linking surveys to ecological processes. Journal of Applied Ecology 52:675-685. https://doi.org/10.1111/1365-2664.12432
Crooks, K. R., C. L. Burdett, D. M. Theobald, C. Rondinini, & L. Boitani. 2011. Global patterns of fragmentation and connectivity of mammalian carnivore habitat. Philosophical Transactions of the Royal Society B: Biological Sciences 366:2642-2651. https://doi.org/10.1098/rstb.2011.0120
Crooks, K. R., & M. Sanjayan. 2006. Connectivity conservation. Cambridge University Press.
De Almeida Jácomo, A. T. et al. 2013. White-lipped peccary home-range size in a protected area and farmland in the central Brazilian grasslands. Journal of Mammalogy 94:137-145. https://doi.org/10.1644/11-mamm-a-411.1
De Echave, J., A. Diez, B. Revesz, L. Huber, M. Tanaka, & X. Ricard Lanata. 2009. Minería y conflicto social. Lima.
De Oliveira, T. G. 1998. Herpailurus yagouaroundi. Mammalian Species 578:1-6. https://doi.org/10.2307/3504500
Dechner, A., K. M. Flesher, C. Lindell, T. V. De Oliveira, & B. A. Maurer. 2018. Determining carnivore habitat use in a rubber/forest landscape in Brazil using multispecies occupancy models. PloS one 13:e0195311. https://doi.org/10.1371/journal.pone.0197397
Dubost, G. 1988. Ecology and social life of the red acouchy, Myoprocta exilis; comparison with the orange-rumped agouti, Dasyprocta leporina. Journal of Zoology 214:107-123. https://doi.org/10.1111/j.1469-7998.1988.tb04990.x
Endo, W. et al. 2009. Game vertebrate densities in hunted and nonhunted forest sites in Manu National Park, Peru. Biotropica 42:251-261. https://doi.org/10.1111/j.1744-7429.2009.00546.x
Fahrig, L. 2003. Effects of Habitat Fragmentation on Biodiversity. Annual Review of Ecology, Evolution, and Systematics 34:487- 515. https://doi.org/10.1146/annurev.ecolsys.34.011802.132419
Fahrig, L. 2017. Ecological Responses to Habitat Fragmentation Per Se. Annual Review of Ecology, Evolution, and Systematics 48:1-23. https://doi.org/10.1146/annurev-ecolsys-110316022612
Ferreguetti, Á. C., W. M. Tomás, & H. G. Bergallo. 2017. Density, occupancy, and detectability of lowland tapirs, Tapirus terrestris, in Vale Natural Reserve, southeastern Brazil. Journal of Mammalogy 98:114-123. https://doi.org/10.1093/jmammal/gyw118
Fletcher, R. J. et al. 2018. Is habitat fragmentation good for biodiversity? Biological Conservation 226:9-15.
Foster, R. J., B. J. Harmsen, & C. P. Doncaster. 2010. Habitat use by sympatric jaguars and pumas across a gradient of human disturbance in Belize. Biotropica 42:724-731. https://doi.org/10.1111/j.1744-7429.2010.00641.x
Fragoso, J. M. 1998. Home range and movement patterns of whitelipped peccary (Tayassu pecari) herds in the Northern Brazilian Amazon. Biotropica 30:458-469. https://doi.org/10.1111/j.1744-7429.1998.tb00080.x
Fragoso, J. M. V. 2004. A long-term study of white-lipped peccary (Tayassu pecari) population fluctuations in northern Amazonia: anthropogenic versus "naturalçauses. People in Nature: Wildlife Conservation in South and Central America (K. M. Silvius, R. E. Bodmer & J. M. V. Fragoso, eds.). Columbia University Press, New York, USA. https://doi.org/10.7312/silv12782-018
Gavin, M. C. 2007. Foraging in the fallows: Hunting patterns across a successional continuum in the Peruvian Amazon. Biological Conservation 134:64-72. https://doi.org/10.1016/j.biocon.2006.07.011
Gelman, A., J. B. Carlin, H. S. Stern, D. B. Dunson, A. Vehtari, & D. B. Rubin. 2014. Bayesian data analysis. Third ed. CRC Press. Taylor & Francis, Boca Raton, FL. 2. https://doi.org/10.1201/b16018
Gilroy, J. J., & D. P. Edwards. 2017. Source-sink dynamics: a neglected problem for landscape-scale biodiversity conservation in the tropics. Current Landscape Ecology Reports 2:51-60. https://doi.org/10.1007/s40823-017-0023-3
Goosem, M., N. Weston, & S. Bushnell. 2005. Effectiveness of rope bridge arboreal overpasses and faunal underpasses in providing connectivity for rainforest fauna.
Gregory, T., F. Carrasco-Rueda, A. Alonso, J. Kolowski, & J. L. Deichmann. 2017. Natural canopy bridges effectively mitigate tropical forest fragmentation for arboreal mammals. Scientific Reports 7:1-11. https://doi.org/10.1038/s41598-017-04112-x
Guilherme Trovati, R., B. Alves De Brito, & J. M. Barbanti Duarte. 2010. Habitat use and home range of brown-nosed coati, Nasua nasua (Carnivora: Procyonidae) in the Brazilian Cerrado biome. Revista de Biología Tropical 58:1069-1077. https://doi.org/10.15517/rbt.v58i2.5263
Guillera-Arroita, G., M. Kéry, & J. J. Lahoz-Monfort. 2018. Inferring species richness using multispecies occupancy modeling: Estimation performance and interpretation. Ecology and Evolution 9:780-792. https://doi.org/10.1002/ece3.4821
Heiberger, R. M., & B. Holland. 2015. Statistical analysis and data display: an intermediate course with examples in R. Second ed. Springer, New York.
Hilty, J. A., A. T. H. Keeley, W. Z. Lidicker Jr., & A. M. Merenlender. 2019. Corridor ecology: linking landscapes for biodiversity conservation and climate adaptation. Island Press. https://doi.org/10.1002/jwmg.21836
Hofman, M. P., J. Signer, M. W. Hayward, & N. Balkenhol. 2016. Spatial ecology of a herd of white-lipped peccaries (Tayassu pecari) in Belize using GPS telemetry: challenges and preliminary results. Therya 7:21-37. https://doi.org/10.12933/therya-16-335
Hurtado-Gonzales, J. L., & R. E. Bodmer. 2004. Assessing the sustainability of brocket deer hunting in the Tamshiyacu-Tahuayo Communal Reserve, northeastern Peru. Biological Conservation 116:1-7. https://doi.org/10.1016/s0006-3207(03)00167-8
Kahhat, R., E. Parodi, G. Larrea-Gallegos, C. Mesta, & I. Vázquez-Rowe. 2019. Environmental impacts of the life cycle of alluvial gold mining in the Peruvian Amazon rainforest. Science of the Total Environment 662:940-951. https://doi.org/10.1016/j.scitotenv.2019.01.246
Kéry, M. 2010. Introduction to WinBUGS for ecologists: A Bayesian approach to regression, ANOVA, mixed models and related analysis. Academic Press.
Kéry, M. 2011. Species Richness and Community Dynamics: A Conceptual Framework. Camera traps in animal ecology: methods and analyses (A. F. O’Connell, J. D. Nichols & K. U. Karanth, eds.). Springer. https://doi.org/10.1007/978-4-431-99495-412
Kéry, M., & J. A. Royle. 2016. Applied hierarchical modeling in ecology: Analysis of distribution, abundance and species richness in R and BUGS: Volume 1: Prelude and Static Models. Academic Press, Boston. https://doi.org/10.1016/b978-0-12-809585-0.00012-0
Kéry, M., & M. Schaub. 2012. Bayesian population analysis using WinBUGS. A hierarchical perspective. Elsevier. https://doi.org/10.1016/b978-0-12-387020-9.00014-6
Keuroghlian, A., M. D. C. A. Santos, & D. P. Eaton. 2015. The effects of deforestation on white-lipped peccary (Tayassu pecari) home range in the southern Pantanal. Mammalia 79:491-497. https://doi.org/10.1515/mammalia-2014-0094
Khosravi, R., & M.-R. Hemami. 2019. Identifying landscape species for ecological planning. Ecological Indicators 99:140-148. https://doi.org/10.1016/j.ecolind.2018.12.010
Kremen, C., & A. M. Merenlender. 2018. Landscapes that work for biodiversity and people. Science 362:eaau6020. https://doi.org/10.1126/science.aau6020
Lacher, T. E., Jr. et al. 2019. The functional roles of mammals in ecosystems. Journal of Mammalogy 100:942-964.
Laforge, M. P., R. K. Brook, F. M. Van Beest, E. M. Bayne, & P.D. Mcloughlin. 2016. Grain-dependent functional responses in habitat selection. Landscape Ecology 31:855-863. https://doi.org/10.1007/s10980-015-0298-x
Leibold, M. A. 2011. The metacommunity concept and its theoretical underpinnings. The Theory of Ecology (S. M. Scheiner & M. R. Willig, eds.). The University of Chicago Press, Chicago, IL, USA.
Leibold, M. A., J. M. Chase, S. A. Levin, & H. S. Horn. 2018. Metacommunity Ecology, Volume 59. Princeton University Press, Oxford. Volume 59. https://doi.org/10.1515/9781400889068
Lewis, S. L., & M. A. Maslin. 2015. Defining the Anthropocene. Nature 519:171.
Li, X., W. V. Bleisch, & X. Jiang. 2018. Using large spatial scale camera trap data and hierarchical occupancy models to evaluate species richness and occupancy of rare and elusive wildlife communities in southwest China. Diversity and Distributions 24:1560-1572. https://doi.org/10.1111/ddi.12792
Loja, J., A. Gironda, & L. Guerra. 2000. Biología y uso de la fauna silvestre en Tambopata: un caso de estudio. Conservación Internacional, Program Peru, Lima, Peru.
Mackenzie, D. I. 2015. Occupancy models. Introduction to ecological sampling (B. F. J. Manly & J. A. Navarro, eds.). CRC Press, New York, 200 pp.
Mackenzie, D. I., J. D. Nichols, J. A. Royle, K. H. Pollock, L. L. Bailey, & J. E. Hines. 2018. Occupancy estimation and modeling: inferring patterns and dynamics of species occurrence. 2nd Edition ed. Academic Press, Boston. https://doi.org/10.1016/b978-0-12-407197-1.00002-8
Mayor, P., P. Perez-Pena, M. Bowler, P. E. Puertas, M. Kirkland, & R. Bodmer. 2015. Effects of selective logging on large mammal populations in a remote indigenous territory in the northern Peruvian Amazon. Ecology and Society 20. https://doi.org/10.5751/es-08023-200436
Mcgarigal, K., S. A. Cushman, & E. Ene. 2012. FRAGSTATS v4: spatial pattern analysis program for categorical maps. Disponible en http://www.umass.edu/landeco/research/fragstats/fragstats.html. [acceso en septiembre del 2018]. https://doi.org/10.2737/pnw-gtr-351
Medellín, R. A., & M. Equihua. 1998. Mammal species richness and habitat use in rainforest and abandoned agricultural fields in Chiapas, Mexico. Journal of Applied Ecology 35:13-23. https://doi.org/10.1046/j.1365-2664.1998.00272.x
Michalski, F. 2010. The bush dog Speothos venaticus and short- eared dog Atelocynus microtis in a fragmented landscape in southern Amazonia. Oryx 44:300-303. https:/doi.org/10.1017/s0030605309990871
Michalski, F., P. G. Crawshaw, T. G. De Oliveira, & M. E. Fabián. 2006. Notes on home range and habitat use of three small carnivore species in a disturbed vegetation mosaic of southeastern Brazil. Mammalia 70:52-57. https://doi.org/10.1515/mamm.70.1-2.52
Monastersky, R. 2015. Anthropocene: the human age. Nature 519:144-147.
Morato, R. G. et al. 2016. Space use and movement of a Neotropical top predator: The endangered jaguar. PLOS ONE 11:e0168176.
Naughton-Treves, L., J. L. Mena, A. Treves, N. Alvarez, & V. C. Radeloff. 2003. Wildlife Survival Beyond Park Boundaries: the Impact of Slash-and-Burn Agriculture and Hunting on Mammals in Tambopata, Peru. Conservation Biology 17:1106-1117. https://doi.org/10.1046/j.1523-1739.2003.02045.x
Niedballa, J., R. Sollmann, A. B. Mohamed, J. Bender, & A. Wilting. 2015. Defining habitat covariates in camera-trap based occupancy studies. Scientific Reports 5:17041. https://doi.org/10.1038/srep17041
Ohl-Schacherer, J., G. H. Shepard, H. Kaplan, C. A. Peres, T. Levi, & D. W. Yu. 2007. The sustainability of subsistence hunting by Matsigenka native communities in Manu National Park, Peru. Conservation Biology 21:1174-1185. https://doi.org/10.1111/j.1523-1739.2007.00759.x
Olsoy, P. J., K. A. Zeller, J. A. Hicke, H. B. Qyigley, A. R. Rabinowitz, & D. H. Thornton. 2016. Quantifying the effects of deforestation and fragmentation on a range-wide conservation plan for jaguars. Biological Conservation 203:8-16. https://doi.org/10.1016/j.biocon.2016.08.037
Patton, J. L., U. F. J. Pardiñas, & G. D’Elia. 2015. Mammals of South America, Volume 2. Rodents. The University of Chicago Press, Chicago and London.
Peres, C. A. 1996. Population status of white-lipped Tayassu pecari and collared peccaries T. tajacu in hunted and unhunted Amazonian forests. Biological Conservation 77:115-123. https://doi.org/10.1016/0006-3207(96)00010-9
Pineda-Guerrero, A., F. González-Maya José, & J. Pérez-Torres. 2015. Conservation value of forest fragments for medium-sized carnivores in a silvopastoral system in Colombia. Mammalia 79(1): 115–119. https://doi.org/10.1515/mammalia-2013-0050
Pinto, F. A. S., A. P. Clevenger, & C. Grilo. 2020. Effects of roads on terrestrial vertebrate species in Latin America. Environmental Impact Assessment Review 81:106337. https://doi.org/10.1016/j.eiar.2019.106337
Piratelli, A. J., F. C. M. Piña-Rodrigues, & C. Raedig. 2019. Importar imagen Integrating biodiversity conservation into agroecosystem management: using birds to bring conservation and agricultural production together. Strategies and Tools for a Sustainable Rural Rio de Janeiro (U. Nehren, S. Schluter, C. Raedig, D. Sattler & H. Hissa, eds.). Springer. https://doi.org/10.1007/978-3-319-89644-110
Plummer, M. 2003. JAGS: A program for analysis of Bayesian graphical models using Gibbs samplingin Proceedings of the 3rd international workshop on distributed statistical computing (DSC 2003). Technische Unversität Wien, Vienna, Austria. https://www.rproject.org/conferences/DSC-2003/Proceedings/Plummer.pdf
Presley, S. J., L. M. Cisneros, B. T. Klingbeil, & M. R. Willig. 2019. Landscape ecology of mammals. Journal of Mammalogy 100:1044-1068. https://doi.org/10.1093/jmammal/gyy169
R Core Team. 2020. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org/
Ramirez-Gomez, S. O. et al. 2015. Analysis of ecosystem services provision in the Colombian Amazon using participatory research and mapping techniques. Ecosystem Services 13:93-107. https://doi.org/10.1016/j.ecoser.2014.12.009
Reyna-Hurtado, R., & C. A. Chapman. 2019. Next Moves: The Future of Neotropical Mammal Movement Ecology. Movement Ecology of Neotropical Forest Mammals (R. Reyna-Hurtado & Colin Chapman, eds.). Springer. https://doi.org/10.1007/978-3-030-03463-415
Reyna-Hurtado, R., & G. W. Tanner. 2007. Ungulate relative abundance in hunted and non-hunted sites in Calakmul Forest (Southern Mexico). Biodiversity and Conservation 16:743-756. https://doi.org/10.1007/s10531-005-6198-7
Reyna-Hurtado, R. et al. 2016. What ecological and anthropogenic factors affect group size in whitelipped peccaries (Tayassu pecari)? Biotropica 48:246-254. https://doi.org/10.1111/btp.12269
Ripple, W. J. et al. 2016. Bushmeat hunting and extinction risk to the world’s mammals. Royal Society Open Science 3:160498.
Romero, M. K., V. H. Pachas, G. Zambrano, & Y. Guarniz. 2005. Formalización de la minería en pequeña escala en América Latina y el Caribe: un análisis de experiencias en el Perú. https://doi.org/10.18356/29d2c8e2-es
Rovero, F., & F. Zimmermann. 2016. Camera trapping for wildlife research. Exeter: Pelagic Publishing, UK.
Royle, J. A., & R. M. Dorazio. 2008. Hierarchical modeling and inference in ecology. The analysis of data from population, metapopulations and communities. Academic Press, London.
Royle, J. A., & J. D. Nichols. 2003. Estimating abundance from repeated presence–absence data or point counts. Ecology 84:777-790. https://doi.org/10.1890/0012-9658(2003)084[0777:eafrpa]2.0.co;2
Rubio, C. J. 2010. El impacto de la minería aurífera en el Departamento de Madre de Dios (Peru)/The impact of mining gold in the Region of Madre de Dios (Peru). Observatorio Medioambiental 13:169. https://doi.org/10.5209/obmd.73177
Schipper, J. et al. 2008. The status of the world’s land and marine mammals: diversity, threat, and knowledge. Science 322:225-230.
Shahnaseri, G., M.-R. Hemami, R. Khosravi, S. Malakoutikhah, M. Omidi, & S. A. Cushman. 2019. Contrasting use of habitat, landscape elements, and corridors by grey wolf and golden jackal in central Iran. Landscape Ecology 34:1263–1277. https://doi.org/10.1007/s10980-019-00831-w
Sollmann, R. et al. 2011. Improving density estimates for elusive carnivores: Accounting for sex-specific detection and movements using spatial capture–recapture models for jaguars in central Brazil. Biological Conservation 144:1017-1024. https://doi.org/10.1016/j.biocon.2010.12.011
Swenson, J. J., C. E. Carter, J.-C. Domec, & C. I. Delgado. 2011. Gold Mining in the Peruvian Amazon: Global Prices, Deforestation, and Mercury Imports. PLOS ONE 6:e18875. https://doi.org/10.1371/journal.pone.0018875
Team. 2011. Terrestrial Vertebrate Protocol Implementation Manual, v. 3.1. Tropical Ecology, Assessment and Monitoring Network, Center for Applied Biodiversity Science, Conservation International, Arlington, VA, USA.
Teixeira, F. Z., R. C. Printes, J. C. G. Fagundes, A. C. Alonso, & A. Kindel. 2013. Canopy bridges as road overpasses for wildlife in urban fragmented landscapes. Biota Neotropica 13:117-123. https://doi.org/10.1590/s1676-06032013000100013
Tejeda-Cruz, C., J. Naranjo Eduardo, D. Cuarón Alfredo, H. Perales, & L. Cruz-Burguete Jorge. 2009. Habitat use of wild ungulates in fragmented landscapes of the Lacandon Forest, Southern Mexico. Mammalia 73:211. https://doi.org/10.1515/mamm.2009.044
Tilman, D., M. Clark, D. R. Williams, K. Kimmel, S. Polasky, & C. Packer. 2017. Future threats to biodiversity and pathways to their prevention. Nature 546:73-81. https://doi.org/10.1038/nature22900
Tobler, M. W. 2015. Camera base version 1.7. http://www.atriumbiodiversity.org/tools/camerabase
Tobler, M. W., S. E. Carrillo-Percastegui, & G. Powell. 2009. Habitat use, activity patterns and use of mineral licks by five species of ungulate in south-eastern Peru. Journal of Tropical Ecology 25:261-270. https://doi.org/10.1017/s0266467409005896
Tobler, M. W., J. P. Janovec, & F. Cornejo. 2010. Frugivory and Seed Dispersal by the Lowland Tapir Tapirus terrestris in the Peruvian Amazon. Biotropica 42:215-222. https://doi.org/10.1111/j.1744-7429.2009.00549.x
Tobler, M. W., A. Zúñiga, S. E. Carrillo-Percastegui, & G. V. N. Powell. 2015. Spatiotemporal hierarchical modelling of species richness and occupancy using camera trap data. Journal of Applied Ecology 52:413-421. https://doi.org/10.1111/1365-2664.12399
Turner, M. G., & R. H. Gardner. 2015. Landscape ecology in theory and practice: Pattern and Process. Second ed. Springer, New York.
Urteaga, P. 2003. La problemática minera y los pueblos indígenas en Madre de Dios, Perú. FENAMAD, OXFAM AMERICA. Lima, Perú.
Zipkin, E. F., J. A. Royle, D. K. Dawson, & S. Bates. 2010. Multi-species occurrence models to evaluate the effects of conservation and management actions. Biological Conservation 143:479-484. https://doi.org/10.1016/j.biocon.2009.11.016
Zuur, A. F., J. M. Hilbe, & E. N. Ieno. 2013. A Beginner’s Guide to GLM and GLMM with R: A Frequentist and Bayesian Perspective for Ecologists. Highland Statistics Newburgh, Newburgh, United Kingdom 256.
Información adicional
Editor asociado: Dr. Ariel Farías
Citar como: Mena, J., F. La Rosa-Camino, J. Loja-Aleman & Y. Apaza. 2021. Efecto de los regímenes de manejo en la ocupación de mamíferos en un corredor de conservación en el sudeste de la Amazonia peruana. Mastozoología Neotropical, 28(1):e0435. https://doi.org/10.31687/saremMN.21.28.1.0.28