SECCIÓN ESPECIAL - ARTÍCULO
Recepción: 01 Octubre 2020
Aprobación: 21 Febrero 2021
Resumen: Describimos una nueva especie del género Oxymycterus Waterhouse, 1837, de los altos Andes de Cusco en el sureste del Perú, basados en información molecular (Citocromo b), rasgos morfológicos y medidas. Esta especie es notablemente diferente de todas las otras formas peruanas y bolivianas estudiadas, en particular O. nigrifrons . O. paramensis. Los rasgos que la distinguen incluyen, entre otros, su tamaño corporal comparativamente mediano, coloración dorsal marrón amarillenta, ausencia de parche supranasal negruzco, foramen incisivo largo, expandido anteriormente y con el septo desarrollado ocupando la mitad a dos tercios del largo del foramen, fosa mesopterigoidea cuadrangular con los procesos hamulares del pterigoides aproximadamente paralelos y la porción dorsal del ectotimpánico expandida lateralmente. Hasta el momento, la nueva especie sólo se ha registrado en dos pequeñas cordilleras (Vilcabamba y Vilcanota) donde está aislada de otras formas, siendo así endémica y con el riesgo de vulnerabilidad asociado a una distribución restringida.
Palabras clave: Cordillera de Vilcabamba, Cusco, Machupicchu, sur del Perú, Yungas.
Abstract: We describe a new species of the genus Oxymycterus from the high Andes of Cusco in southeastern Peru, based on information provided by the analysis of molecular data (cytochrome .), morphology and measurements. This species is notably different from all other Peruvian and Bolivian forms studied, specially O. nigrifrons and O. paramensis. It distinguishing traits include a comparatively medium body size, dorsal coloration brown yellowish with black hairs, no blackish supranasal patch, a long, anteriorly expanded incisor foramen with a developed septum occupying half to two-thirds of the foramen length, a quadrangular mesopterygoid fossa with hamular process of pterygoid near parallels, and the dorsal portion of the ectotympanic laterally expanded. Currently, the new species is only known from two small mountain ranges (Vilcanota and Vilcabamba) being isolated from other forms, that define it as an endemic species, highlighting the vulnerability risk associated with its restricted distribution.
Keywords: Cordillera de Vilcabamba, Cusco, Machu Picchu, Southern Peru, Yungas.
INTRODUCCIÓN
Los roedores del género Oxymycterus Waterhouse, 1837 conforman un grupo de sigmodontinos caracterizados por una morfología altamente especializada, con uñas alargadas, hocico prolongado y estómago bilocular discoglandular (Carleton 1973; Hershkovitz 1962, 1994). Existe diversa evidencia que indica se trata de un grupo natural, diferenciado de otros géneros tanto por morfología (Carleton 1973; Hooper & Musser 1964; Vorontsov 1979; Voss & Linzey 1981; Oliveira 1998), datos electroforéticos (e.g., Hinojosa et al. 1987), moleculares (Smith & Patton 1993, 1999; Jayat et al. 2008) y cariotípicos (e.g., Vitullo et al. 1986). El género o parte de este ha sido revisado recientemente (Oliveira 1998; Hoffmann et al. 2002; Oliveira & Gonçalves 2015). Actualmente, se reconocen 16 especies (Oliveira & Gonçalves 2015; Peçanha et al. 2019). Sin embargo, existe consenso en que la diversidad de este género no está aún bien entendida (Hershkovitz 1994; Oliveira & Gonçalves 2015). Esta hipótesis se refuerza porque, en las últimas dos décadas, se han descrito tres especies nuevas (Hoffmann et al. 2002; Jayat et al. 2008; Peçanha et al. 2019).
En el Perú se reconocen cinco especies de Oxymycterus (Pacheco et al. 2011), cuatro de las cuales también se distribuyen en Bolivia y una en Brasil (Anderson 1997; De Abreu-Júnior et al. 2016). Oxymycterus hiska Hinojosa, Anderson & Patton, 1987, es conocida en su localidad típica en las Yungas del Departamento de Puno (Hinojosa et al. 1987) y en los departamentos de Cochabamba y La Paz de Bolivia, entre 600 y 3500 m (Anderson 1997); Oxymycterus incaThomas, 1900, habita el centro y sur del Perú (Departamento de Junín hasta el Departamento de Puno), norte de Bolivia (departamentos de La Paz y Pando) y al extremo suroeste de Brasil (Estado de Acre), en las vertientes orientales de los Andes y la Amazonía, siempre por debajo de 1200 m (Thomas 1900; Oliveira & Gonçalves 2015; De Abreu-Júnior et al. 2016); Oxymycterus juliacae J. A. Allen, 1900, endémica del Perú, habita en los departamentos de Cusco, Madre de Dios y Puno, en las vertientes orientales de los Andes entre 600 y 2700 m (Allen 1900; Thomas 1901; Oliveira & Gonçalves 2015); Oxymycterus nigrifronsOsgood, 1944, de las inmediaciones de la localidad tipo en el Departamento de Puno, en el sur del Perú y en el Departamento de La Paz, en Bolivia, entre 2000 y 3350 m (Osgood 1944; Oliveira & Gonçalves 2015); finalmente, Oxymycterus paramensis Thomas, 1912, que habita en los pastizales de altura y bosques adyacentes de los altos Andes del centro del Departamento de Cusco y desde el Departamento de La Paz en Bolivia hasta el noroeste en Argentina (Thomas 1902, 1920; Hershkovitz 1994; Oliveira 1998; Pacheco et al. 2009, 2011; Oliveira & Gonçalves 2015).
Entre las especies de Oxymycterus que colectamos en la región andina del Departamento del Cusco, se encuentra una forma corrientemente identificada como O. paramensis (Allen 1900; Thomas 1901; Hershkovitz 1994; Oliveira 1998; Oliveira & Gonçalves 2015). Es relativamente abundante en la zona de estudio, aunque llama la atención porque sus poblaciones tienen una distribución disjunta con respecto a la forma típica del Departamento de Cochabamba en Bolivia (Thomas 1902). Además, interpuesta entre ambas y a similar rango altitudinal se han registrado a O. hiska y O. nigrifrons (Oliveira & Gonçalves 2015). Asimismo, es destacable que esta región presenta elevada heterogeneidad geográfica y ambiental por el desarrollo de varias cordilleras (p. ej., Vilcabamba, Vilcanota, Carabaya y Real). Las mismas, con altitudes que superan los 6000 m, están separadas por profundos cañones y valles interandinos y podrían conformar barreras biogeográficas o condicionando barreras climáticas (Emck et al. 2006). Esto podría haber gatillado algunos procesos de especiación que se vienen descubriendo (Patton et al. 1990; Patton & Smith 1992; Patterson et al. 2012; Särkinen et al. 2012; Upham et al. 2013; Chazot et al. 2017; Hazzi et al. 2018; Pinto et al. 2018).
La evidencia molecular y los patrones de variación morfológica, a los que se suma su condición alopátrica, sugieren que la forma de Oxymycterus de Cusco corresponde a una especie nueva. La misma es aquí descripta enfatizando en sus notables diferencias con otras entidades conocidas para la región andina (Thomas 1925; Cabrera 1961; Anderson 1997; Oliveira 1998; Oliveira & Gonçalves 2015).
MATERIALES Y MÉTODOS
Especímenes, medidas y morfología
Este estudio se basa en la revisión de 112 especímenes de Oxymycterus obtenidos en el sur del Perú y oeste de Bolivia. Entre ellos 40 ejemplares corresponden a O. paramensis de Cusco, más un representante de la forma nominal de O. paramensis, un paratipo de O.hiska (MUSM 19881), 12 especímenes de Oxymycterus nigrifrons, cuatro de los cuales provienen del Perú y ocho de Bolivia y fotografías del cráneo del holotipo (FMNH 52629). Los especímenes revisados están depositados en el Museo de Historia Natural de la Universidad Nacional de San Agustín (MUSA), Arequipa, Perú, en el Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos (MUSM), Lima, Perú y en la Colección Boliviana de Fauna (CBF), La Paz, Bolivia (APÉNDICE 1).
Las medidas externas analizadas se obtuvieron de las etiquetas de los especímenes: longitud total (TL), longitud de la cola (LT), longitud de la pata posterior incluyendo la uña (HF), longitud de la oreja (EL) y la masa en gramos (W). La longitud de cabeza y cuerpo (HBL) se obtuvo restando LT a TL. Asimismo, se tomaron 22 medidas cráneodentarias mediante un pie de rey digital (0.01 mm) y siguiendo a Gonçalves & Oliveira (2004). Estas son: longitud máxima del cráneo (GSL), longitud cóndilo basal (CBL), longitud de los nasales (NAL), ancho de los nasales (NAB), longitud del tubo nasal (NTL), longitud del diastema superior (DIL), longitud de la hilera molar superior (MRL), longitud del foramen incisivo (IFL), longitud palatal (PAL), longitud palatal entre el foramen incisivo y la fosa mesopterigoidea (PBL), ancho máximo de rostral (ROB), ancho máximo anterorbital (AGB), ancho máximo del arco cigomático (ZAB), ancho de la placa cigomática (ZPB), ancho de la caja craneal (BCB), longitud máxima del interparietal (IPL), ancho máximo del interparietal (IPB), ancho mínimo del interorbital (LIB), ancho de la bulla auditiva (ABB), altura rostral (ROL), altura de la caja craneana (BCD) y longitud máxima de la mandíbula (GLM). Obtuvimos las medidas completas de O. hiska (n=1), O. inca (n=7), O. juliacae (n=13), O. nigrifrons (n=10), O. paramensis (1) y de O. paramensis del Cusco (n=14). Adicionalmente, obtuvimos medidas parciales de O. hucucha (3; Hinojosa et al. 1987), O. inca (3) y O. juliacae (4). Otras fueron tomadas de la literatura: O. hiska (2; Hinojosa et al. 1987), O. paramensis (3; Thomas 1902), O. paramensis de Cusco (17), y O. wayku (4; Jayat et al. 2008). Para las comparaciones morfométricas sólo se consideraron especímenes adultos o subadultos, con molares funcionales y desgastados.
Las medidas externas: LT, HBL, HF, EL, W y las craneanas: CBL, BCB y MRL de los Oxymycterus en este estudio se compararon con un Análisis de Varianza de una vía (ANOVA) y la prueba de Kruskal-Wallis, usamos la prueba de Tuckey para evaluar la significancia de la diferencia de medias; asimismo, comparamos estas variables entre las especies con la prueba de Mann-Whitney y aplicamos una corrección de Bonferroni a los valores de probabilidad. Los patrones de variación morfométrica en el espacio multivariado fueron explorados con un Análisis de Componentes Principales (PCA) implementado en el programa PAST (Hammer et al. 2001). Para tal efecto las medidas fueron transformadas a log10 y se usaron matrices de varianza-covarianza. Dado que no obtuvimos medidas completas de todas las especies, decidimos desarrollar dos PCA. Uno con medidas obtenidas por nosotros y de la literatura, que sólo analiza ocho variables (CBL, NAL, ZPB, ROB, ZAB, BCB, DIL y MRL), pero permitió comparar todas las especies andinas: O. hiska, O. hucucha, O. wayku, O. paramensis (típica, del sur de Bolivia y Argentina), O. nigrifrons y O. paramensis de Cusco. Otro PCA permitió incluir todas las variables pero solo sobre especies de Perú (O. inca, O. hiska, O. juliacae, O. nigrifrons y O. paramensis de Cusco) y O. nigrifrons de Bolivia.
La coloración es descrita de forma genérica y especificamos entre paréntesis los colores que se ajustan a los mostrados en la carta Ridgway (1912). Para la comparación morfológica de los rasgos craneanos seguimos a Carleton & Musser (1989) y Oliveira (1998), considerando todos los especímenes ya que los juveniles permiten apreciar mejor los caracteres de los molares. Para la asignación de la edad seguimos el modelo de Myers (1989) propuesto para el género Akodon. Para su descripción seguimos la nomenclatura presentada por Hershkovitz (1994, 1998). Para medir la convergencia de los molares calculamos el ángulo que forman la prolongación posterior de las líneas imaginaria que cruzan longitudinalmente las series dentarias.
Análisis filogenético
La filologenia molecular se hizo en base a las secuencias parciales del gen que codifican al citocromo b. Cuatro secuencias fueron obtenidas por nosotros: O. paramensis MSB 238408, BO: Tables Montes, Cochabamba (MZ322539); O. paramensis MUSA 4193, PE: Cusco (MZ322540); O. nigrifrons MUSA 4709, PE: Limbani, Puno (MZ322541); O. nigrifrons MUSA 4710, Limbani, Puno (MZ322542); O. nigrifrons AR 231, BO: Cochabamba (MZ322543), las que se sumaron a 37 obtenidas del GenBank, cuyos códigos se indican en los árboles filogenéticos elaborados. Elegimos cinco especies de akodontinos como grupos externos, a saber: Akodon juninensis, Blarinomys breviceps, Lenoxus apicalis, Juscelinomys huanchacae y Brucepattersonius iheringi (APÉNDICE 1).
Para la extracción de ADN usamos tejidos de músculo e hígado preservados en alcohol al 95% y seguimos la metodología de Bilton & Jaarola (1996). Amplificamos fragmentos del gen citocromo b usando las condiciones y cebadores descritos por Irwin et al. (1991). Amplificamos las secuencias con una mezcla master que contenía 2.5 µl de 5X PCR buffer, 1.5 µl de 50 mM MgCl2, 0.5 µl de 10 µM de cada primer, 0.5 µl de 10 mM dNTPs, 0.25 µl de Taq polimerasa (Invitrogen), 30 ng de DNA, y 18.25 µl de agua destilada; el volumen final fue de 25 µl. Las muestras fueron purificadas con ExoSAP-IT kit (ExoSAP-IT, GE Healthcare). Para visualizar los productos PCR, usamos geles de agarosa al 1% suspendida en un TBE buffer (Trisborato con EDTA). Las secuencias de ADN fueron obtenidas por la empresa Macrogen Inc. (Seoul, Korea).
La alineación de las secuencias se realizó con Muscle v3.8 (Edgar 2004) implementado en Mesquite v3.61 (Maddison & Maddison 2010), utilizando los valores predeterminados para todos los parámetros de alineación. Las secuencias alineadas y revisadas se sometieron a análisis filogenéticos utilizando los métodos de Máxima Verosimilitud (ML, Felsenstein 1981) e Inferencia Bayesiana (BI, Ronquist et al. 2012).
Los árboles de ML se calcularon utilizando IQ-TREE 1.6.12 (Trifinopoulos et al. 2016) empleando ModelFinder (Kalyaanamoorthy et al. 2017) para sugerir el modelo preferido de evolución por posición de codón y valores de arranque nodal ultrarrápidos (Hoang et al. 2018) para los análisis. ModelFinder seleccionó los siguientes modelos por posición de codón: TNe + I + G4 para la primera posición, TPM3u + F + I + G4 para la segunda y TIM2 + F + I + G4 para la tercera. Se realizaron pruebas de topología adicionales con ALHRT tipo SH con 10 000 réplicas y 126 iteraciones. Para el soporte nodal estimamos el SH-aLRT (LRTV) siguiendo a Guindon et al. (2010) y bootstrap ultra rápido (UFBV) implementado en IQ-TREE 1.6.12. Debido a que los valores de PP bayesianos tienden a ser una estimación menos conservadora de la confiabilidad del nodo que los valores de bootstrap no paramétricos, asumimos la inclusión de ambos valores de soporte en nuestros árboles representa los límites superior e inferior, respectivamente, de la confiabilidad del nodo (Douady et al. 2003).
Importar imagen Los análisis de BI se realizaron con MrBayes en el portal de enlace de CIPRES (Miller et al. 2010) e incluyeron la posición específica de los codones en los análisis, asumiendo intervalos uniformes previos para todos los parámetros excepto la composición de bases. Los datos se analizaron utilizando esquemas de partición y modelos de sustitución identificados por PartitionFinder (Lanfear et al. 2016). El modelo de evolución molecular seleccionado para la primera y segunda posición fue HKY + I + G, mientras que GTR + I + G se seleccionó para la tercera posición. Para BI se corrieron 10 millones de generaciones, muestreadas cada 1 000 generaciones; estos análisis se repitieron tres veces. El primer 25% de los árboles se descartó como “burn-in los árboles restantes se utilizaron para calcular un árbol de consenso utilizando la regla de la mayoría del 50%; las frecuencias se obtuvieron las estimaciones de probabilidad posterior (PP) para cada clado. Las ramas con probabilidad posterior (PP) con valores ≥ 0.95 se consideraron bien respaldadas. Todos los análisis fueron verificados ploteando los valores de log-likelihood contra el tiempo de cada generación para cada corrida, utilizando Tracer 1.7.1 (Rambaut et al. 2018). Después de cada una de las ejecuciones, confirmamos que todos los parámetros tenían tamaños de muestra efectivos >200.
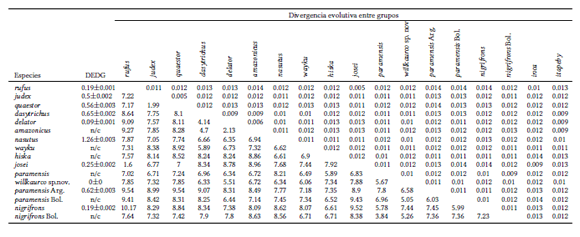
Estimamos el grado de divergencia en las secuencias de citocromo b calculando la distancia genética, entre especies y a nivel intraespecífico, usando el algoritmo de 2-parámetros de Kimura (K2P; Kimura 1983) implementado en el programa MEGA6 (Tamura et al. 2013), este último agrupado en base a los resultados del análisis filogenético. El grado de divergencia para ser usado en la determinación de especies es discutible; no obstante, nos permite tener una aproximación comparativa complementaria para comparar la distancia entre los subclados formados.
Descripción de nicho
Realizamos una comparación de datos ambientales que corresponden a los puntos de registro de O. paramensis de Cusco, O. nigrifrons de Perú, O. nigrifrons de Bolivia y O. paramensis típico, que se seleccionaron por su cercanía relativa. Esto permite establecer como estas variables se asocian a su distribución geográfica y brinda una idea de la segregación de los nichos. Usamos una aproximación de nicho basada en el análisis de 20 variables ambientales de cada una de las localidades de colecta, 19 variables fueron climáticas (BIO1-BIO19; 11 basadas en temperatura y 8 en precipitación) y además la elevación en m s.n.m. Estas fueron obtenidas de la base de datos WorldClim v.2 a 1 km de resolución (Fick & Hijmans 2017) y se estandarizaron para los análisis. Se efectuó un PCA para evaluar la amplitud del nicho y establecer cuáles son las variables mejor asociadas a su distribución. Adicionalmente, se graficó el perfil de elevación mediante una aplicación de GoogleEarth Pro en el área de distribución de O. paramensis de Cusco y de O. nigrifrons de Perú para de caracterizar y describir la complejidad de estos ambientes.
RESULTADOS
Análisis morfológico
En relación al tamaño encontramos que O. paramensis de Cusco es significativamente más pequeña que O. inca y O. juliacae, especies grandes en el contextodel género (Hershkovitz 1994); por otro lado, es significativamente más grande que O. hiska y O.hucucha, que son pequeñas. O. paramensis de Cusco comparten un tamaño intermedio con O. nigrifrons,O. paramensis sensu stricto, y O. wayku (Tabla 1). El ANOVA y la prueba de Kruskal-Wallis mostraron que existen diferencias altamente significativas en las variables analizadas entre todas las especies (Tabla 2), la prueba de Tuckey fue usada a posteriori con los resultados del ANOVA y la prueba de Mann-Whitney mostraron que el tamaño de las patas, el BCB y MTR muestran diferencias significativas entre O. paramensis de Cusco y las otras especies (Tabla 2). No obstante, la EL, W y CBL serían similares en promedio a O. hucucha, O. nigrifrons, O. paramesis sensu stricto y O. wayku (Tabla 2). Respecto de las diferencias morfológicas cualitativas que presentan estas especies, las mismas son sustanciales y se resumen en la Tabla S2).
Análisis de Componentes Principales: los primeros cuatro componentes principales explican el 93.35% de la varianza (Tabla S1); Fig. 1a). Los valores del primer componente principal discriminan los ejemplares analizados por efecto de ZPB (0.6763) y DIL (0.4072), mientras que en el segundo componente principal se generan dos grupos por efecto de DIL (-0.5204) y NAL (-0.4938). Uno de estos agrupa a las poblaciones de O. paramensis de Cusco y O. nigrifrons de Perú, mientras que el otro contiene a las restantes especies analizadas incluyendo O. nigrifrons de Bolivia. El tercer componente principal discrimina a O. wayku por el ROB (0.7162) y a O. nigrifrons de Bolivia y O. hucucha por el ZPB (- 0.5524).
El PCA sobre las formas de Perú y oeste de Bolivia, muestra que los cuatro primeros componentes principales explican el 87.48% de la varianza (Tabla S1); Fig. 1b). El primer componente discrimina a O. inca y O. juliacae en base al NTL (-0.3099), NAB (0.3915) y ZPB (0.3494); el segundo componente principal diferencia a O. nigrifrons de Bolivia influenciado por el NAB (-0.4941), IPL (0.6348) y, secundariamente, por el IPB (0.3395); el tercer componente principal solo muestra discriminación entre O. inca y O. juliacae, influenciado principalmente por IPB (-0.6466); el cuarto componente principal discrimina O. nigrifrons de Perú y O. paramensis de Cusco por las variables NAB (0.5419), NTL (0.5467) e IPL (0.4289). El conjunto combinado de los resultados nos permite discriminar a las especies de tamaño grande (O. inca y O. juliacae y las poblaciones de O. nigrifrons de Bolivia), mientras que la diferenciación de O. paramensis de Cusco es parcial y sólo en el cuarto componente principal definido por variables referidas al ancho del cráneo y el tubo rostral.
Medidas externas y craneanas (en milímetros) para muestras de especímenes (número entre paréntesis) de Oxymycterus andinos, incluyendo la nueva especie aquí descripta. * = medidas obtenidas de la literatura (Hinojosa et al. 1987; Anderson 1997; Jayat et al. 2008).
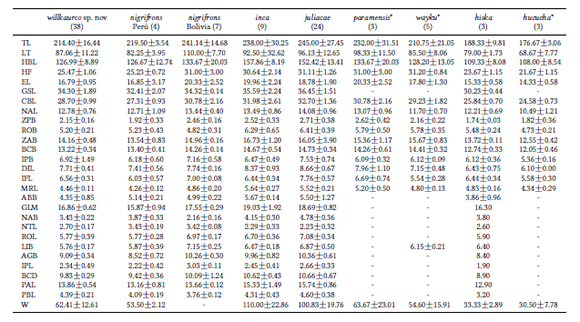
Comparaciones de las medidas externas: Longitud total (TL), longitud de cabeza y cuerpo (HBL), longitud de la pata posterior (HF), longitud de la oreja (EL), peso (W), y las craneales: longitud cóndilo basal (CBL), ancho del cráneo (BCB) y longitud de la hilera molar (MTR), con los Análisis de Varianza, prueba de Kruskal-Wallis, la prueba de Tuckey y la de Mann-Whitney. En esta última las indicadas en negrita corresponden a las que mantienen su significancia al aplicar la corrección de Bonferroni. Se presentan valores de probabilidad entre O. wilkaurco sp. nov. con las otras especies de Oxymycterus andinos.
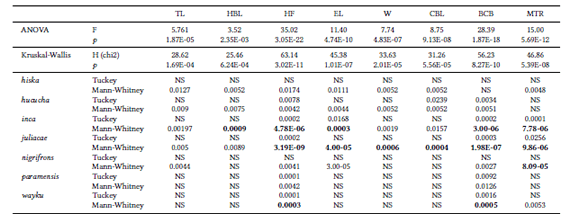
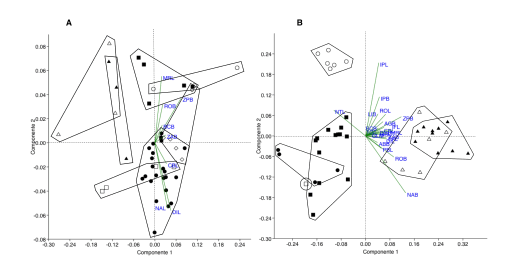
Fig. 1
Gráfico de los dos primeros componentes del PCA obtenido a partir de: A, 8 medidas craneanas para 7 especies de Oxymycterus (O. hiska [triángulo lleno], O. wayku [cuadrado lleno], O. nigrifrons de Perú [cuadrado], O. paramensis de Cusco [punto], O. nigrifrons de Bolivia [rombo], O. paramensis sensu stricto [círculo] y O. hucucha [triángulo]); y B, 22 medidas craneanas 7 especies de Oxymycterus (O. hiska [cuadrado], O. inca [triángulo], O. juliacae [triángulo lleno], O. nigrifrons de Perú [punto], O. nigrifrons de Bolivia [círculo] y O. paramensis de Cusco [cuadrado lleno]).
Análisis filogenético
En el análisis de ML se eligió el árbol que presentó el valor más alto de log-verosimilitud (-2 927.7240), con una distribución gamma discreta entre sitios (4 categorías [+G, parámetro=0.3626]). Los análisis de ML y BI resolvieron topologías prácticamente idénticas, con la excepción de que en BI hay dos clados que forman politomías: uno que incluye a O. nigrifrons, O. hiska y O. paramensis y otro a la base del árbol y que incluye O. itapeby, O. amazonicus y O. delator. En ambos análisis Oxymycterus es parafilético con respecto a Juscelinomys huanchacae. Sin embargo, las relaciones entre especies de Oxymycterus no cambian substancialmente si el análisis incluye a J. huanchacae como único grupo externo (Fig. S1). Todos los subclados que corresponden al nivel de especie presentan fuerte soporte nodal (>95/95, >0.95) y están altamente estructurados, con excepción del soporte de O. judex (que incluye a la forma nominal O. misionalis) en el análisis de ML (aLRTV=82.0, UFBV=81). Otro subclado contiene a O. dasytrichus (que incluye a O. hispidus), bien soportado con ambos métodos. El siguiente subclado agrupa a poblaciones de O. nasutus. El subclado más interno muestra a O. wayku muy bien sustentado con BI y ubicado en posición basal a dos subclados hermanos: el primero de ellos contiene dos grupos, uno bien sustentado por ambos métodos conformado por O. josei, O. rufus y O. inca y el otro integrado por O. judex (que incluye a O. misionalis) y O. quaestor; los dos grupos presentan amplio soporte en las topologías BI y ML. El siguiente subclado contiene las formas que corrientemente fueron asignadas a O. paramensis e incluye dos grupos, uno para poblaciones de Jujuy y Salta (Argentina), Cochabamba (Bolivia) y O. paramensis de Cusco (Perú), como taxones bien delimitados y soportados. El otro grupo incluye a O. hiska, basal a O. nigrifrons de la localidad típica, que a su vez resulta especie hermana de O. paramensis sensu stricto y de las poblaciones bolivianas referidas a O. nigrifrons (Fig. 2).
Los valores intraespecíficos varían de 0.09 a 1.26% (O. delator y O. nasutus, respectivamente); los valores de divergencia interespecíficos muestran a O. paramensis de Cusco con distancias genéticas >5.00% en todos los casos (Tabla 3), con un rango de variación desde 5.05% (con respecto a O. paramensis sensu stricto) hasta 8.16% (con respecto a O. inca).
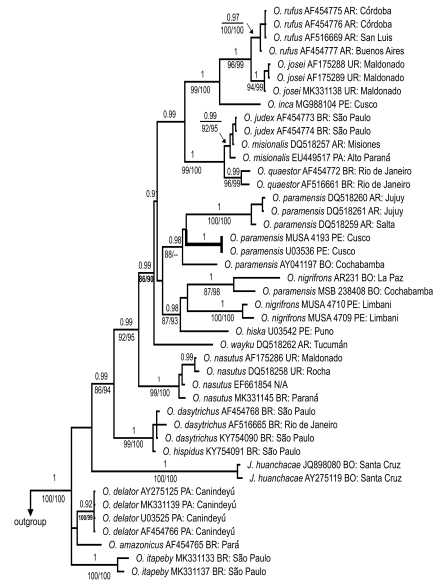
Fig. 2
Resultado del análisis filogenético del género Oxymycterus, basado en las primeras 801 bases del gen citocromo b. Filogenia construida mediante Inferencia Bayesiana implementado en el programa MrBayes en el portal CIPRES y el modelo de partición PartitionFinder. Se uso HKY + I + G para la primera y segunda posición y GTR + I + G para la tercera posición. Sobre la línea se indica el valor de la probabilidad posterior y debajo de la línea el soporte SH-aLRT (LRTv) / bootstrap ultra rápido (UFBv). Nótese que Juscelinomys huanchacae se recuperó dentro del grupo interno.
Análisis de nicho
La gráfica obtenida del PCA muestra que en el primer componente principal los nichos están superpuestos en todas las especies, teniendo casi todas las variables marcadas influencias, excepto BIO 13 y 14 (Fig. 3;Tabla S1). En el segundo componente principal se discriminan dos grupos con dos especies cada uno: el nicho de O. paramensis sensu stricto es más parecido al que usan las formas de O. nigrifrons de Perú, influenciado por las variables de temperatura (BIO 4, 8, 10) y de precipitación (BIO 12, 14 y 17). Los O. paramensis de Cusco se encuentran superpuestos con las formas de O. nigrifrons de Bolivia y están influenciados por las variables de precipitación BIO 13 y 16. Los primeros cuatro componentes principales dan cuenta del 95.95% de la varianza (Tabla S1). El perfil altitudinal muestra la alta complejidad orográfica en la región que corresponde al rango de distribución de O. paramensis de Cusco (Fig. 4), caracterizada por profundos cañones con 2000 m o menos y tierras altas que sobrepasan los 5000 m. En el caso de la cordillera de Carabaya, hábitat de O. nigrifrons de Perú se verifica una elevada pendiente, pero comparativamente con menor complejidad orográfica.
Distancias genéticas entre especies de Oxymycterus, obtenidas con el modelo de dos parámetros de Kimura; se presenta los valores (expresados en porcentajes) intra-grupo ± error estándar y entre pares de especies (debajo de la diagonal) y su error estándar (sobre la diagonal). Abreviaturas: Arg. = Argentina, Bol. = Bolivia. DDEG: divergencia evolutiva dentro de grupos.
Taxonomía
Basados en las evidencias previamente reseñadas, reconocemos a los O. paramensis de Cusco como una nueva especie del género. Ante la inexistencia de algún nombre disponible para estas poblaciones (Thomas 1920, 1925; Osgood 1944; Patton et al. 1990; Hershkovitz 1994; Wilson Reader 2005; Pacheco et al. 2011), seguidamente la nominamos y describimos:
Familia Cricetidae Fischer, 1817
Subfamilia Sigmodontinae Wagner, 1843
Tribu Akodontini Cockerell & Printz en Cockerell et al., 1914
Género Oxymycterus Waterhouse, 1837
Oxymycterus willkaurco, sp. nov.
Hocicudo del Cusco; Cusco’s hocicudo
LISD: urn:lsid:zoobank.org:pub:4D4F6013-FB82-464A-ABD4-EDA4540D95DD
Oxymycterus paramensis: Thomas 1920 (parte, no Oxymycterus paramensisThomas 1902).
Holotipo
MUSA 4192, hembra adulta (edad 3), coleccionada por Juvenal Silva el 12 de agosto de 2002 (número de campo QQC-8), conservada como piel disecada y cráneo (Fig. 1).
Paratipos
MUSA 4190, un macho adulto (edad 5) conservado como piel y cráneo, colectado por J. Silva el 12 de agosto de 2012 (número de campo QQC-1) en la localidad típica; MUSA 8095, un macho adulto (edad 4) conservado como piel y cráneo, colectado por C. Medina el 29 de marzo de 2009 (número de campo CMed 772) en Amparaes (13º 01’ 16.77"S, 72º 56’ 15.84"W, 4062 m), Distrito de Lares, Provincia de Calca, Perú; MUSA 8090, un macho juvenil (edad 2) conservado como piel y cráneo, colectado por C. Medina el 22 de marzo de 2009 (número de campo CMed 736) en la Comunidad de Coyllobamba (13º 57’ 12.89"S, 72º 59’ 06.03"W, 4022 m), Distrito de Lares, Provincia de Calca, Perú; y MUSA 16409, una hembra adulta (edad 4) conservada en fluido con el cráneo removido, colectado por J. P. Ludeña el 30 enero de 2014 (número de campo JPL 648) en Yanamayo (13º 05’ 02.87"S, 72º 16’ 58.18"W, 3754 m), Distrito de Ocobamba, Provincia de La Convención, Perú.
Localidad tipo
Perú: Departamento del Cusco, Provincia de Urubamba, Distrito de Urubamba, Chupani, 13º 05’ 03.94"S, 72º 07’ 17.30” W, 3850 m (Fig. 4).
Diagnosis
Una especie del género Oxymycterus que se diferencia de las demás por la siguiente combinación de caracteres: tamaño mediano (longitud de cabeza y cuerpo=115–150 mm; longitud de la cola=67–105 mm; longitud cóndilo basal=26.7–30.7 mm; longitud de la serie molar superior=4.2–4.7 mm; rangos basados en 38 individuos); coloración dorsal marrón amarillenta con abundantes pelos con puntas amarillas y con pelos negros uniformemente distribuidos; vientre más claro que dorso con tonos amarillentos; anillo periocular de pelos amarillo naranja claro; orejas pequeñas (15–18 mm), peludas, con abundantes pelos de color cremosos en su borde; sin mancha supranarinal; patas anteriores y posteriores dorsalmente grisáceas con ligeros tonos amarillentos; cola bicoloreada; cráneo delicado, alargado e inflado en vista lateral; nasales cortos que se extienden por delante de la sutura maxilo-frontal-lacrimal; foramen incisivo largo alcanza la parte media o posterior del procíngulo del M1, con septo es desarrollado ocupa la mitad del foramen en la mayoría de los especímenes y puede alcanzar hasta 2/3; borde anterior de la fosa mesopterigoidea no alcanza al M3; proceso medial redondeado en el borde posterior del palatino; fosa mesopterigoidea con márgenes externos paralelos; series molares superiores poco divergentes; bullas infladas, con borde superior del ectotimpánico expandido; proceso hamular del temporal en forma de hacha; hipoflexo ancho; anteroconúlidos m1 separados, juntos tienen un ancho similar al ancho molar; mesolófido del m1 largo y no fusionado al metalofúlido; anterolófido del m3 separado del paralofúlido; ectostílido del m3 presente.
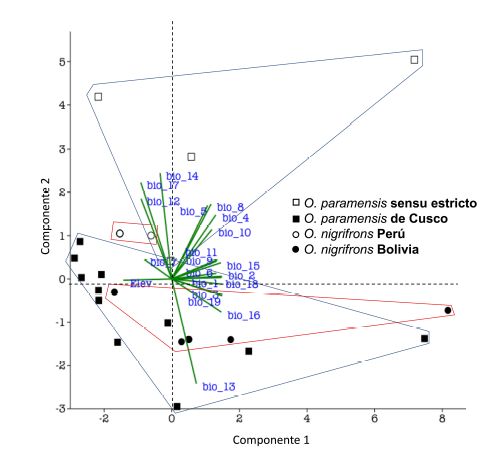
Fig. 3
Diagrama que describe la caracterización comparada del nicho de cuatro especies de Oxymycterus andinos, incluyendo la nueva especie aquí estudiada.
Medidas del holotipo (en mm)
HBL=115.5; LT=77.5; HF=24.8; EL=15; W =32.4; GSL=32.4; ZAB=14.6; BCB=13.7; LIB=5.7; MRL=4.5; NAL=12.7; NAB=5.4; DIL=7.7; IFL=6.5; ZPB=2.2.
Distribución
Oxymycterus willkaurco está distribuida en las vertientes orientales de los Andes del sur del Perú en el centro del Departamento del Cusco, entre 3200 y 4100 m, ocupando el sur de la Cordillera de Vilcabamba y la Cordillera de Vilcanota (Fig. 4). El hábitat de esta especie comprende formaciones de Puna Húmeda con pajonales y parches de bosque en quebradas y la parte más alta del bosque montano también llamado “elfin forest”.
Etimología
“Willkaurco” es una palabra compuesta derivada del idioma Quechua, “willka” significa sagrado y “urcu” significa montaña. Es tomada de los nombres de las cordilleras de Vilcabamba y Vilcanota donde se distribuye la especie, ya que “vilca” es una castellanización del vocablo quechua “willka”.
Descripción morfológica
Es una especie de tamaño mediano en el género (Tabla S2); el color dorsal es marrón grisáceo uniforme con abundantes pelos de puntas amarillentas (Pale Yellow-Orange, Chamois o Honey Yellow) y con numerosos pelos negros tanto en el dorso, cabeza y ancas, que le confieren un pelaje tipo agutí sin conformar una franja oscura media; el pelo dorsal es largo (x=11.93 mm, DE=0.66, rango=11.0-13.1 mm, n=20); presenta un anillo de pelos amarillo naranja claro alrededor de los ojos (Capucine Buff); Importar imagen la coloración ventral gris amarillento (Pale Yellow-Orange a Cream Buff), con las puntas de los pelos amarillentas, mientras que en la parte ventral del cuello se dan tintes rojizos (Capucine Buff); la base de los pelos dorsales y ventrales es de color gris uniforme; carece de parche supranarinal negruzco; las orejas son cortas (Tabla S2), muy peludas, con pelos amarillentos y negros en el borde; el mentón presenta un parche de pelos bancos de amplitud variable; puede prolongarse hasta el intraramal, inclusive como un parche aislado, aunque también puede estar ausente; carece de pelos blancos en labios o al costado del surco naso-labial (filtro); las manos y pies son dorsalmente de color grisáceo opaco con tonos amarillo pálido o blanco sucio (Pale Olive-Buff); las uñas de las manos son largas (x=5.1 mm, DE=0.31, rango=4.4-5.6 mm, n=25) con sus bordes unidos ventralmente hasta la mitad de la uña; la cola es corta (Tabla 1) y bicoloreada, con una delgada línea negruzca dorsal (Citrine-Drab) y el resto grisácea (Pale Olive-Buff); los pelos de la cola son largos, los dorsales cubren cuatro escamas y los ventrales, cuatro o cinco hileras.
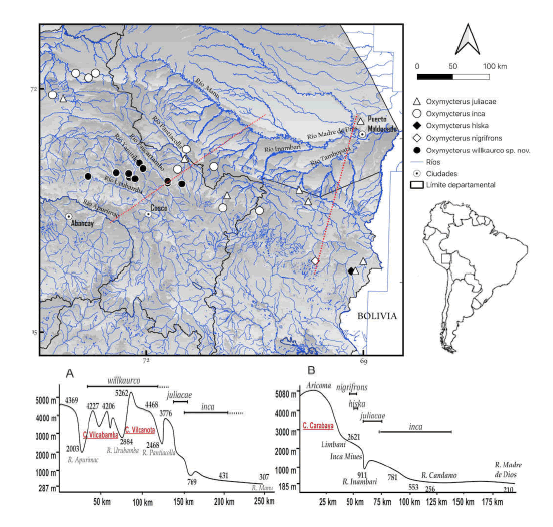
Fig. 4
Mapa de distribución de las especies de Oxymycterus registradas en Perú, incluyendo el nuevo taxón aquí descripto (arriba). Las líneas rojas muestran la dirección de los perfiles altitudinales que se detallan en A, entre Apurímac y el río Manu y B, entre Aricoma y Puerto Maldonado.
El rostro es agudo y alargado por la expansión anterior de los nasales y del premaxilar, que forman un tubo rostral; en vista dorsal resultan visibles los premaxilares; el margen lateral de los nasales es ligeramente convergente; el borde posterior de los nasales no alcanza la altura del borde posterior de la muesca cigomática y se ubican por delante de la sutura maxilo-fronto-lacrimal; los etmoturbinales son alargados, tres veces más largos que anchos; el arco cigomático expandido, es completo (jugal presente) y delgado; la región interorbitaria tiene forma de reloj de arena con bordes redondeados; el cráneo es delicado, alargado y curvado vista lateral; el foramen etmoideo se ubica detrás del M3; con la caja craneana redondeada y el seno frontal ligeramente inflado; la sutura frontoparietal tiene forma semicircular; el interparietal es largo en su parte media y suele expandirse a los costados con prolongaciones delgadas; el foramen incisivo penetra posteriormente hasta la parte media del procíngulo del M1 en adultos o hasta el borde anterior del protocono en juveniles; el septo del foramen incisivo abarca la mitad de este ocasionalmente puede ocupar 2/3; el puente palatino es largo, su borde posterior se prolonga más allá del borde posterior del M3; los surcos palatinos son poco notorios, pero con los forámenes palatinos posteriores bien desarrollados; los agujeros palatinos posterolaterales están poco desarrollados y se ubican a los lados de la fosa mesopterigoidea; la fosa mesopterigoidea presenta el proceso medio romo mientras que sus márgenes externos son paralelos; el borde anterior de la fosa mesopterigoidea no alcanza al borde posterior del M3; el foramen esfenopalatino es cerrado en vista lateral; bullas auditivas desarrolladas, con el borde superior del ectotimpánico expandido y la trompa de Eustaquio corta y delgada; el proceso hamular del escamoso expandido distalmente, en forma de hacha; la cápsula mastoidea es inflada; las fosas parapterigoideas son superficiales; la fisura petrotimpánica es más ancha que larga y el foramen oval está desarrollado.
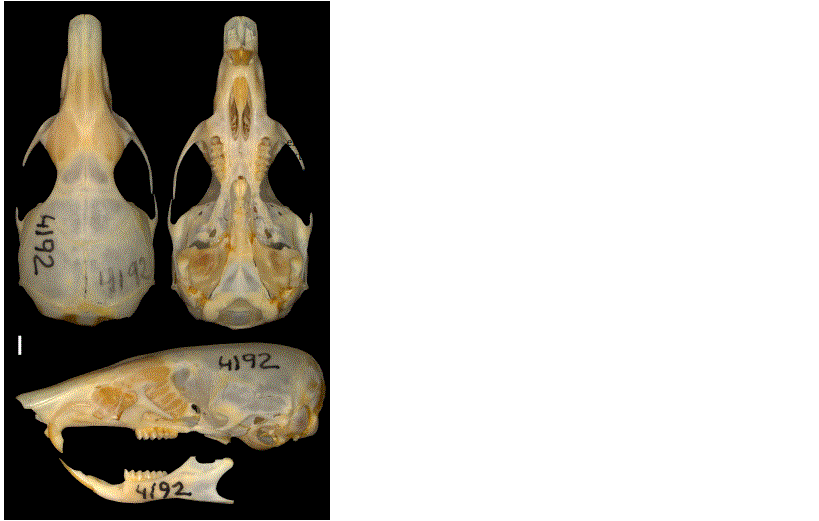
Fig. 5
Vista dorsal, ventral y lateral del cráneo del holotipo de Oxymycterus willkaurco sp. nov. (MUSA 4192) de Chupani, Provincia de Urubamba, Departamento del Cusco, Perú. Escala = 2 mm.
La mandíbula es baja y delicada con la proyección capsular no definida; la escotadura semilunar está excavada y es asimétrica; el proceso angular es delicado; la cresta masetérica es delicada; el foramen mental está desarrollado en posición supralateral; el proceso coronoides es grácil; el proceso ventromedial es redondeado.
Los incisivos maxilares son típicamente opistodontos; la superficie labial de los incisivos es color amarillo-anaranjado y en vista anterior puede presentar una delgada franja blanca hacia el borde medial; los incisivos inferiores son pálidos; las hileras molares ligeramente convergentes hacia atrás, en un ángulo de 10°; los molares presentan un patrón tetralofodonto, crestados y con cúspides ligeramente alternadas. El M1 con lófulos anterolabiales no separados por el proflexo; anterolofo separado del paracono y el lófulo anterolabial (visible en edad 2 y 3), protolofo ausente, mesolofo presente no fusionado al mesostilo que es muy reducido (sólo visible en edad 2 y 3); metalófulo ausente; psoterolofo y posterocónulo reducidos, e hipoflexo angosto sin enterolofo; el M2 con anterolófulo presente, mesolofo desarrollado, posteroflexo reducido a una pequeña invaginación, posterolofo reducido; el M3 con paracono redondeado, paraflexo reducido y corto y el mesoflexo ausente, en el m1 los anterocunúlidos separados por el prefléxido; m2 con labiolofúlido desarrollado, amplio y dirigido hacia adelante, mesofléxido desarrollado, mesolófido largo, carece de metalofúlido, protoflexo se prolonga profundamente pero muy es superficial, posteroconúlido desarrollado, distofléxido poco notorio en el m2, el labiolo- fúlido es delgado y dirigido hacia atrás bordeando el molar, ectolófido corto, mesofléxido profundo lo que hace un muro angosto; mesolófido definido y corto, posterofléxido profundo, y posteroconúlido alargado; en el m3 anterolofúlido y paralofúlido separados, labiolofúlido y ectofléxido poco desarrollados; ectostílido presente y posteroconúlido ausente.
Comparaciones
Ninguna otra especie de Oxymycterus habita en simpatría con O. willkaurco (Oliveira & Gonçalves 2015); en las tierras medias y bajas adyacentes habitan O. inca y O. juliacae, mientras que a una altura algo inferior, en los bosques montanos y las áreas abiertas al sureste, en la adyacente Cordillera de Carabaya, habita O. nigrifrons.
O. nigrifrons se diferencia externamente de O. willkaurco por su coloración ligeramente más oscura con tonalidades marrón rojizas; por presentar un parche supranarinal de color negruzco; por carecer de pelos blancos en el mentón; porque sus patas son grises y la cola amarronada y unicoloreada, con los pelos cortos que alcanzan a cubrir sólo tres escamas; su tamaño es ligeramente mayor aunque pesa menos (Tabla 1); su rostro es ligeramente más ancho en su extremo distal; sus nasales son largos y se extienden por detrás de la sutura maxilo-fronto-lacrimal; los etmoturbinales son más cortos, dos veces más largos que anchos; la muesca cigomática es más amplia en vista dorsal (Tabla S2); foramen esfenopalatino está abierto en vista lateral; el paladar tiene su margen posterior a la altura de la cara posterior de los M3, la fosa mesopterigoidea es redondeada y con los márgenes divergentes y más ancha que las fosas parapterigoideas, el proceso medial del margen posterior del palatino está presente pero poco desarrollado; los forámenes incisivos más cortos y no alcanza al protocono del M1; proceso hamular del escamoso recto; el septo maxilar ocupa aproximadamente la mitad del foramen incisivo; el palatino es corto, con el borde anterior de la fosa mesopterigoidea alcanzando el nivel medio de los M3s, los surcos palatinos están definidos; la bulla está menos desarrollada en vista ventral; la fisura petrotimpánica es semicircular; el estilo anteromedio ausente en el M1; los M3 tricuspidados y el anterolofo, cuando está presente, es muy pequeño.
O. paramensis sensu stricto se diferencia de O. willkaurco por su coloración dorsal compuesta de tonos más oscuros y rojizos, por tener abundantes pelos negros en el dorso que forman una franja dorsal, por la tonalidad en la cabeza que es marrón olivácea y por ser ventralmente más rojiza; por sus patas grisáceas con pelos marrones en el metatarso; por su pelaje dorsal ligeramente más largo (mayor de 13 mm); por ser en promedio ligeramente mayor en tamaño y peso aunque la cola, orejas y patas posteriores son significativamente más grandes (Tabla 1). Además, O. paramensis sensu stricto presenta la longitud del cráneo (CBL), el largo de la serie molar superior y el ancho del cráneo significativamente mayores (Tabla 1); los nasales son más largos y se prolongan más allá del borde posterior de la porción maxilar del arco cigomático; el proceso hamular del escamoso es recto; el septo del foramen de los incisivos es comparativamente angosto; los surcos palatinos están bien desarrollados; la fosa mesopterigoidea es redondeada con bordes divergentes; las bullas menos abultadas y con la porción dorsal del ectotimpánico menos desarrollada; las series molares convergentes, forman un ángulo de 20°; M1 con lófulos anterolabial y anterolingual separados por el proflexo; mesolofo y mesostilo fusionados; posterolofo más desarrollado y fusionado al paracono; mesolofo en M2 corto y grueso; M3 más complejo al ser tricuspidado con anterolofílido y anterolófido fusionados. mesolófido más corto que el metalofúlido; m3 desarrollado alcanza dos tercios del m2.
O. hiska y O. hucucha son de menor tamaño que O. willkaurco (Tabla 1); en ambos el rostro es más angosto y delicado y, en vista dorsal, no se aprecia el premaxilar; septo del foramen de los incisivos angosto; la fosa mesopterigoidea redondeada con forma de mazo; bulla no desarrollada; M3 tricuspidado. O. hiska, que habita en Puno y el oeste de Bolivia, tiene su pelaje más suave y grisáceo; tiene el cráneo comparativamente menos alargado y redondeado; el foramen de los incisivos es angosto con forma de paréntesis; paladar corto, con el borde anterior de la fosa mesopterigoidea penetrando hasta el hipocono del M3; M1 sin estilo anteromediano; anterolofo profundo y horizontal. O. hucucha, una especie del centro de Bolivia, tiene los nasales que sobrepasan el foramen infraorbital, la región interorbitaria más angosta y con bordes no redondeados; la placa cigomática ligeramente más reclinada; en el M1, el anterolofo está ausente o reducido; el mesolofo ausente; y las hileras molares son convergentes, con un ángulo de 19°.

Fig. 6
Series molar superior derecha (arriba) e inferior izquierda (abajo), en vistas oclusales, indicando grupos de, de izquierda a derecha: Oxymycterus nigrifrons edad 2 (MUSA 13532), Oxymycterus willkaurco sp. nov. edad 2 (MUSA 8090), edad 3 (MUSA 8095), edad 3 (MUSA 4192, holotipo), edad 4 (MUSA 16409) y edad 5 (MUSA 4190). Escala = 1 mm.
O. wayku se diferencia de O. willkaurco por su coloración más oscura; su tamaño comparativamente mayor (Tabla 1); el rostro es angosto y con una menor prolongación de los nasales; no se observan los premaxilares en vista dorsal; la región interorbitaria es más corta; su cráneo es más aplanado en vista lateral y menos alargado en vista dorsal; el foramen de los incisivos es corto, con forma de paréntesis; las bullas más reducidas y la región dorsal del ectotimpánico no desarrollada; el M1 sin estilo anteromedial y el anterolofo y mesostilo mejor desarrollados.
O. inca y O. juliacae son fácilmente distinguibles de O. willkaurco por su mayor tamaño en todas las medidas externas y craneanas (Tabla 1); sus colas son unicoloreadas con pelos cortos que alcanzan a cubrir tres escamas; los nasales robustos y largos que se extienden por detrás de la sutura maxilo-fronto-lacrimal; los etmoturbinales son más cortos, dos veces más largos que anchos; los cráneos son comparativamente más amplios; el foramen de los incisivos es desarrollado; el paladar corto; la fosa mesopterigoidea redondeada y carece del proceso medial del margen posterior. O. inca es de color pardo rojizo con vientre anaranjado; sin pelos blancos en el mentón; el foramen etmoides se ubica a la altura del M3; septo maxilar ocupa aproximadamente dos tercios del foramen incisivo; paladar largo con su margen posterior detrás de la cara posterior de los M3. O. juliacae es de color pardo rojizo, con puntas amarillentas, más amarillentas ventralmente; con pelos bancos que rodean el surco naso-labial; las uñas cerradas en su parte proximal hasta un tercio de su tamaño; con el foramen de los incisivos más largo, ubicándose a la altura o por delante del protoflexo del M1; septo maxilar ocupa aproximadamente tres cuartos del foramen incisivo; paladar corto con su margen posterior ubicado anteriormente a la cara posterior de los M3.
Historia Natural
O. willkaurco ocupa tres tipos de hábitats: el pajonal de puna, los parches de bosque con predominancia del género Polylepis y el bosque montano enano. Estas formaciones corresponden a la Puna Húmeda y a las Yungas Peruanas (Udvardy 1975; Brack 1986; Dinerstein et al. 1995; Fjeldsa & Kessler 1996). Su rango altitudinal registrado está entre 3000 a 4200 m. Su distribución, restringida a las cordilleras de Vilcabamba y Vilcanota, está separada de otras áreas por el río Apurímac (2003 m) al oeste y el río Pantiacolla (2468 m) al este, que colinda con la selva baja. Ambas cordilleras están divididas por el río Urubamba, también llamado Vilcanota (2884 m). Los pajonales de puna en esta zona pueden descender hasta 3000 m, presentan una densa cobertura herbácea con arbustos esparcidos; entre las herbáceas destacan Calamagrostis trichophylla, Festuca weberbaueri, Gentiana spp., Jarava inconspicua y, entre las leñosas, Astragalus garbancillo, Bomarea involucrosa, Cassia latipetiolata, Escallonia resinosa, Eupatorium spp. (Weberbauer 1945). Los parches de bosque aislados, rodeados por pajonales, presentan principalmente árboles de Polylepis besseri, P. incana, racemosa, P. sericea, P. subsericans y P. weberbaueri (Fjeldsa & Kessler 1996; Servat et al. 2002), con abundante acumulación de hojarasca, algunas veces de más de un metro de espesor. En el sotobosque predominan Baccharis spp., Cronquistianus volquensii, Fuschia spp. Luzula peruviana, Senecio tenuisagittatus (Servat et al. 2002). El bosque montano enano presenta árboles de pequeña talla y reducido desarrollo, destacándose Allnus jorullensis, Berberis spp., Cytharexylum spp., Escallonia spp., Gynoxys marcapatana, Gynoxys rugulosa, Weinmannia spp., (Weberbauer 1945; Fjeldsa & Kessler 1996; Servat et al. 2002; Kessler 2006; Young 2006); el suelo presenta abundante hojarasca y, en las ramas, hay numerosas plantas epífitas, musgos, bromelias y helechos (Kessler 2006).
Todas nuestras capturas de O. willkaurco fueron nocturnas en trampas acomodadas en el suelo. Los estómagos contuvieron insectos. Una de las hembras capturadas en el mes de julio estaba preñada y, en agosto, un macho presentó testículos escrotales; otros machos no reproductivos se colectaron en septiembre y marzo. Esto sugiere que la actividad reproductiva sería invernal, con nacimientos hacia la primavera. Otras especies de pequeños mamíferos capturados en simpatría con O. willkaurco fueron: el paucituberculado Lestoros inca y los roedores Akodon torques, Cavia tschudii Phyllotis osilae y Thomasomys aureus.
DISCUSIÓN
La diversidad de especies en Oxymycterus en los Andes ha sido subvalorada, planteándose que sus diferencias eran parte de la variación intraespecífica (Hershkovitz 1994). Sin embargo, este panorama ha ido cambiando en forma progresiva y la riqueza del género se ha incrementado de tres a ocho especies en la región oriental de los Andes Centrales (Hinojosa et al. 1987; Hershkovitz 1994; Oliveira 1998; Jayat et al. 2008; Oliveira & Gonçalves 2015; este estudio). La evidencia molecular y morfológica indica que se trata de un grupo bien diversificado. De su estudio pueden resultar claves valiosas no solo respecto de su ecología y evolución, sino también del impacto biótico de la orogenia andina, la variabilidad topográfica y la capacidad de estas especies para explotar un nicho altamente especializado y singular en los altos Andes.
Las filogenias, aunque aún pobres en marcadores moleculares y animales analizados, muestran grupos de especies bien estructurados y soportados (probabilidad posterior y bootstrap). Las distancias genéticas, aunque se trate de una medida no libre de controversia, nos muestra valores similares a otros trabajos que sustentan el nivel específico (Bradley & Baker 2001; Smith & Patton 1993; Schrago & Mello 2020). Nuestra evidencia también sugiere que las formas peruanas de O. nigrifrons corresponden a una especie plena, tal como fue sugerido a nivel morfológico (Oliveira 1998; Oliveira & Gonçalves 2015). Pero, nuestros resultados abren la necesidad de revisar con mayor detalle el estatus específico de las formas de O. nigrifrons de Bolivia que resultan parafiléticas con respecto a la forma típica y que estarían cercanamente emparentadas a O. paramensis sensu stricto. Asimismo, es necesario evaluar el estatus específico de las formas argentinas referidas a O. paramensis en el extremo austral de su distribución, en su momento ubicadas bajo el trinomio O. p. jacentiorThomas, 1925. Estos aspectos, también abordados desde un punto de vista morfológico y/o molecular (Oliveira 1998; Jayat et al. 2008), como así ambién la situación de las poblaciones asignadas a O. paramensis del sur de Cochabamba, resaltan una fuerte necesidad de un estudio integral de todos estostaxones y formas nominales.
La propuesta de que Oxymycterus willkaurco es una especie se sustenta en varios criterios que se han planteado para definir especies: 1) conforma una población geográficamente aislada de otras formas de Oxymycterus, que describen procesos ecológicos y evolutivos propios, lo que habría limitado efectivamente el flujo de genes (Coyne & Orr 2004; Wiens 2007); 2) por sus diferencias morfológicas, genéticas y de hábitat respecto de otras especies, se constituye en una unidad filogenética con rasgos autapomórficos y que ocupa una zona adaptativa diferente a la de otros linajes (Van Valen 1976; Schluter 2000); 3) por su distribución actual y el grado de divergencia genética, su especiación se habría dado en alopatría, por lo que su linaje mantendría una identidad propia (Wiley 1978); además, existe un porción de hábitat que en nuestros tiempos sería infranqueable (Frost & Kluge 1994); 4) filogenéticamente, conforma un subclado monofilético bien soportado (probabilidad posterior, bootstrap ultra rápido y SH-aLRT); además, la baja distancia genética intraespecífica, muestra una fuerte cohesividad genética que también se observa en todas las otras especies, y que describe una coalescencia recientemente entre ellas (de Queiroz 1988; Baum & Donoghue 1995); y 5) su morfología muestra una divergencia fenotípica que sería el resultado de la selección natural divergente por el uso de recursos y hábitats (Schluter 2000).
Oxymycterus willkaurco está confinada a las tierras altas de las cordilleras de Vilcabamba y Vilcanota y está separadas por las discontinuidades que configuran los cañones de los ríos Apurímac, Pantiacolla y Paucartambo. Las cabeceras de estos ríos, ubicadas sobre los 4 000 m, incluyen los hábitats preferidos de la especie; los mismos corresponden, biogeográficamente, a la unidad faunística y vegetacional referida como el Piso de las Quebradas Altas, también llamada Qheshwa Alta o Subpuna (Chávez-Chaparro 1950; Ceballos-Bendezú 1970, 1976). Es esperable la ausencia de esta especie en la parte norte de la Cordillera de Vilcabamba (Emmons et al. 2001; Solari et al. 2001). Esto se debería a la depression intermedia de esta cordillera, que desciende hasta los 1700 m y que potencialmente habría impedido su dispersión. Asimismo, registros no publicados demuestran que no habita al oeste del profundo cañón del río Apurímac (1500 a 2800 m a la altura de su área de distribución) y que las tierras bajas serían una barrera para la dispersión de esta especie. Por otro lado, su límite distribucional al sur en tierras altas, como en el valle del Cusco, estaría dado por una mayor aridez con cambio vegetacional (Weberbauer 1945; Emck et al. 2006). Notablemente, la especie tampoco tiene registros al suroeste de su rango, en territorios donde parece existir hábitat favorable. Allí aparece reemplazada por otras especies como O. nigritfrons y, un poco más al sureste, por O. hiska. Estas observaciones permiten abrir nuevas preguntas sobre el origen y colonización de O. willkaurco, en un área altamente compleja y con limitaciones dadas por la altitud (profundos cañones), vegetación y clima (aridez). Asimismo, en un género que parece tan especializado pero que ocupa un amplio rango de hábitats, desde el Bosque Atlántico hasta los Altos Andes, surge la necesidad de entender cómo funcionan los procesos de variación fenotípica, el grado de plasticidad de sus especies y los procesos adaptativos que le han permitido ocupar la extensa y variable área de distribución.
Oxymycterus willkaurco es una especie endémica de distribución restringida, que ocupa un área menor a 7000 km2. Aunque el estatus de sus poblaciones es desconocido, la cantidad de registros obtenidos sugiere que la especie es localmente abundante. Si bien en su área de distribución hay hasta 10 áreas protegidas (p. ej. Parque Nacional del Manu, Santuario Histórico de Machupicchu), en las cuales la actividad turística podría ser beneficiosa para la especie por la promoción de la conservación de la naturaleza, también ocurren problemas pretéritos, como la incursión de la agricultura y la ganadería y otros más recientes y no menos preocupantes, como la minería y la deforestación (Jameson & Ramsay 2007). En general, su restringida distribución aunada a problemas ambientales causados por la actividad humana sugiere que el estado de conservación de la especie debería ser considerada como vulnerable. Este es un ejemplo del estado de la biodiversidad actual, en el que la descripción de especies corre contra-reloj ante el impacto antrópico, siendo necesario emprender mayores esfuerzos en descubrir y describir nuestra riqueza biológica como primer paso para su conservación.
Materiales suplementarios
MATERIAL SUPLEMENTARIO EN LÍNEA (pdf) Suplemento 1
Tabla S1. Valor principal, porcentaje de varianza y valores de los cuatro primeros componentes principales de los Análisis de Componentes Principales a partir de: A) ocho medidas craneales transformadas a logaritmos de base 10 entre las siete formas de Oxymycterus andinos (O. hiska (triángulo lleno), O. wayku (cuadrado lleno), O. nigrifrons de Perú (cuadrado), O. paramensis de Cusco (punto), O. nigrifrons de Bolivia (rombo), O. paramensis sensu stricto (círculo), O. hucucha (triángulo); B) 22 medidas craneanas transformadas a logaritmos de base 10 que incluyen 6 formas de Oxymycterus andinos: O. hiska (cuadrado), O. inca, (triángulo) O. juliacae, (triángulo lleno) O. nigrifrons de Perú (punto), O. nigrifrons de Bolivia (círculo) y Oxymycterus de Cusco (cuadrado lleno; C) del PCA de las variables de nicho de cuatro especies O. nigrifrons de Perú (círculos), O. nigrifrons de Bolivia (puntos), O. paramensis sensu stricto (cuadrados) y O. paramensis de Cusco (cuadrados llenos).
Tabla S2. Matriz comparada de caracteres seleccionados entre las especies de Oxymycterus registradas en Perú y el oeste de Bolivia. En el caso de las estructuras de los molares se indica el grupo de edad en los que son visibles; si está entre paréntesis, es visible sólo en algunos de ese grupo de edad.
Fig. S1. Resultado del análisis filogenético del género Oxymycterus, basado en las primeras 801 bases del gen citocromo b. Filogenia construida con el método de Máxima Verosimilitud implementado en el programa IQ-TREE y el modelo de partición ModelFinder. Se uso TNe + I + G4 para la primera posición, TPM3n + F + I para la segunda posición y TIM2 + F + I para la tercera posición. El soporte nodal esta dado por SH-aLRT (LRTv)/ bootstrap ultra rápido (UFBv). Como grupo externo se usó a Juscelinomys huanchacae.
Agradecimientos
Agradecemos a las siguientes personas e instituciones por el apoyo desinteresado a este trabajo: Evaristo López Tejeda, director del Museo de Historia Natural de la Universidad Nacional de San Agustín (MUSA), Arequipa, Perú; Víctor R. Pacheco, curador del Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos (MUSM), Lima, Perú; Isabel Moya Díaz, en su momento, curadora de la colección de mamíferos de la Colección Boliviana de Fauna, La Paz, Bolivia; Bruce Patterson del Field Museum of Natural History (FMNH), Chicago, EE. UU., por las fotografías de un holotipo. Agradecemos al equipo editorial de la revista Mastozoología Neotropical, en especial a Ulyses F. J. Pardiñas que tuvo un paciente y riguroso trabajo y además porque sus aportes fueron fundamentales para mejorar el manuscrito. Asimismo, agradecemos a la Dirección General Forestal y de Fauna Silvestre y al Servicio Nacional de Áreas Naturales Protegidas por los permisos de colecta: RD 503-2011-AG-DGFFS, RJ 003-2013- SERNANP-ZRSD, RJSHM-No. 054-2012-SERNANP-JEF; al Centro de Estudios Avanzados de Ecología y Biodiversidad de la Pontifica Universidad Católica de Chile, que financió parcialmente algunas colectas, así como al Global Change Research Institute de la Academia Checa de Ciencias, por el financiamiento (a ARC), que facilitó el trabajo de campo en Bolivia, en particular a los proyectos GA CR 14-36098Gy MSMT Funding LO1415.
LITERATURA CITADA
Allen, J. A. 1900. On mammals collected in southeastern Peru, by Mr. H. H. Keays, with descriptions of new species. Bulletin of the American Museum of Natural History 13:219–227. http://hdl.handle.net/2246/557
Anderson, S. 1997. Mammals of Bolivia, taxonomy and distribution. Bulletin of the American Museum of Natural History 231:1–651. http://hdl.handle.net/2246/1620
Baum, D. A., & M. J. Donoghue. 1995. Choosing among Alternative “Phylogenetic” Species Concepts. Systematic Botany 20:560–573. https://doi.org/10.2307/2419810
Bilton, D. T., & M. Jaarola. 1996. Isolation and purification of vertebrate DNAs. Methods in Molecular Biology 50:25–37. https://doi.org/10.1385/0-89603-323-6:25
Brack, A. 1986. Las ecorregiones del Perú. Boletín de Lima 44:57–70. Bradley, R. D. & R. J. Baker. 2001. A test of the genetic species concept: cytochrome–b sequences and mammals. Journal of Mammalogy 82: 960–973. https://doi.org/10.1644/1545-1542(2001)082<0960:ATOTGS>2.0.CO;2
Bradley, R. D. & R. J. Baker. 2001. A test of the genetic species concept: cytochrome–b sequences and mammals. Journal of Mammalogy 82: 960–973. https://doi.org/10.1644/1545-1542(2001)082<0960:ATOTGS>2.0.CO;2
Cabrera, A. 1961. Catálogo de los Mamíferos de América del Sur. Revista del Museo Argentino de Ciencias Naturales “Bernardino Rivadavia”, Ciencias Zoológicas 4:xxii + 308–732.
Carleton, M. D. 1973. A survey of gross stomach morphology in New World Cricetinae (Rodentia. Muroidea) with comments on functional interpretations. Miscellaneous Publications, Museum of Zoology, University of Michigan 146:1–43. Handle: <http://hdl.handle.net/2027.42/56390>
Carleton, M. D., & G. M. Musser. 1989. Systematic studies of Oryzomyine rodents (Muridae, Sigmodontinae): A synopsis of Microryzomys. Bulletin of the American Museum of Natural History 191:1-83.
Ceballos-Bendezú, I. 1970. Los pisos zoogeográficos del Departamento del Cuzco. Publicaciones del Departamento Académico de Zoología y Entomología 1:1–26.
Ceballos-Bendezú, I. 1976. Nuevo esquema biogeográfico del Perú. Revista Universitaria, Universidad Nacional San Antonio Abad del Cusco LXIII(130):19–44.
Chávez-Chaparro, J. 1950. Distribución geográfica de los principales mamíferos peruanos. Revista Universitaria, Universidad Nacional San Antonio Abad del Cusco XXXIX(99): 233–321.
Chazot, N., D. L. De-Silva, K. R. Willmott, A. V. L. Freitas, G. Lamas, J. Mallet, C. E. Giraldo, S. Uribe & M. Elias. 2017. Contrasting patterns of Andean diversification among three diverse clades of Neotropical clearwing butterflies. Ecology and Evolution 8(8):3965–3982. https://doi.org/10.1002/ece3.3622
Coyne, J. A., & H. A. Orr. 2004. Speciation. Sinahuer Associates, Oxford University Press. Oxford.
De Abreu-Júnior, E. F., M. A. De Freitas, M. J. Lapenta, N. M. Venancio, D. P. F. De França & A. R. Percequillo. 2016. Marsupials and rodents (Didelphimorphia and Rodentia) of upper Rio Acre, with new data on Oxymycterus inca Thomas, 1900 from Brazil. Check List 12:1–16. http://dx.doi.org/10.15560/12.5.1956
de Queiroz, K. & M. J. Donoghue. 1988. Phylogenetic Systematics and the Species Problem. Cladistics 4:317-338. https://doi.org/10.1111/j.1096-0031.1988.tb00518.x
Dinerstein, E., D. M. Olson, D. J. Graham, A. L. Webster, S. A. Primm, M. P. Bookbinder & G. Ledec. 1995. Una Evaluación del Estado de Conservación de las Eco-regiones Terrestres de América Latina y el Caribe. Banco Internacional de Reconstrucción y Fomento, Banco Mundial y World Wildlife Fund, Washington D.C. Estados Unidos.
Douady, C. J., F. Delsuc, Y. Boucher, W. Ford Doolittle & E. J. P. Douzery. 2003. Comparison of Bayesian and maximum likelihood bootstrap measures of phylogenetic reliability. Molecular Biology and Evolution 20:248-254. https://doi.org/10.1093/molbev/msg042
Edgar, R. C. 2004. MUSCLE: a multiple sequence alignment method with reduced time and space complexity. BMC Bioinformatics 32:1792-1797. https://doi.org/10.1186/1471-2105-5-113
Emck, P., A. Moreira-Muñoz, & M. Richter. 2006. El clima y sus efectos en la vegetación. Botánica Económica de los Andes Centrales (M. Moraes R., B. Øllgaard, L. P. Kvist, F. Borchsenius & H. Balslev, eds.). Universidad Mayor de San Andrés, La Paz, Bolivia.
Emmons, L. H, L. Luna, & M. Romo. 2001. Mammals of the Northern Vilcabamba Mountain Range, Peru. Biological and Social Assessments of the Cordillera de Vilcabamba, Peru (A. L. E., Alonso, T. S. Schulenberg & F. Dallmeier, eds.). Conservation International, Washington, Estados Unidos.
Felsenstein, J. 1981. Evolutionary trees from DNA sequences: a maximum likelihood approach. Journal of Molecular Evolution 17:368–376. https://doi.org/10.1007/BF01734359
Fick, S. E., & R. J. Hijmans. 2017. WorldClim2: new 1 km spatial resolution climate surfaces for global land areas. International Journal of Climatology 37:4302–4315.
Fjeldsa, J., & M. Kessler. 1996. Conserving the biological diversity of Polylepis woodlands of the highland of Peru and Bolivia. A contribution to sustainable natural resources management in the Andes. NORDECO, Copenhage, Dinamarca.
Frost, D. R., & A. G. Kluge. 1994. A consideration of epistemology in systematic biology, with special reference to species. Cladistics 10:259–294. https://doi.org/10.1111/j.1096-0031.1994.tb00178.x
Gonçalves, P. R., & J. A. Oliveira. 2004. Morphological and genetic variation between two sympatric forms of Oxymycterus (Rodentia: Sigmodontinae): an evaluation of hypotheses of differentiation within the genus. Journal of Mammalogy 85(1):148–161. https://doi.org/10.1644/BER-012
Guindon, S., J. F. Dufayard, V. Lefort, M. Anisimova, W. Hordijk & O. Gascuel. 2010. New Algorithms and Methods to Estimate Maximum-Likelihood Phylogenies: Assessing the Performance of PhyML 3.0. Systematic Biology 59(3):307–321. https://doi.org/10.1093/sysbio/syq010
Hammer, Ø., D. A. T. Harper, & P. D. Ryan. 2001. PAST: Paleontological statistics software package for education and data analysis. Paleontologia Electrónica 4(1):1–9. http://palaeoelectronica.org/20011/past/issue101.htm
Hazzi, N. A., J. S. Moreno, C. Ortiz-Movliav, & R. D. Palacio. 2018. Biogeographic regions and events of isolation and diversification of the endemic biota of the tropical Andes. Proceedings of the National Academy of Sciences 115(31):7985–7990. https://doi.org/10.1073/pnas.1803908115
Hinojosa, F., S. Anderson, & J. L. Patton. 1987. Two new species of Oxymycterus (Rodentia) from Peru and Bolivia. American Museum Novitates, 2898:1–17. http://hdl.handle.net/2246/5182
Hershkovitz, P. 1962. Evolution of Neotropical cricetine rodents (Muridae) with special reference to the phyllotine group. Fieldiana: Zoology 46:1–524.
Hershkovitz, P. 1994. The description of a new species of South American hocicudo, or long-nose mouse, genus Oxymycterus (Sigmodontinae, Muroidea), with a critical review of the generic content. Fieldiana: Zoology n.s. 79:1–43.
Hershkovitz, P. 1998. Report on some sigmodontines rodents collected in southeastern Brazil with descriptions of a new genus and six new species. Bonner Zoologische Beiträge 47(3-4):193– 256.
Hoang, D. T., O, Chernomor, A. Von Haeseler, B. Q. Minh & L. S. Vinh. 2018. UFBoot2: Improving the Ultrafast Bootstrap Approximation. Molecular Biology and Evolution 35(2):518–522. https://doi.org/10.1093/molbev/msx281
Hoffmann, F. G., E. P. Lessa, & M. F. Smith. 2002. Systematics of Oxymycterus with description of a new species from Uruguay. Journal of Mammalogy 83:408–420. https://doi.org/10.1644/1545-1542(2002)083<0408:SOOWDO>2.0.CO;2
Hooper, E.T., & G. G. Musser. 1964. The glans penis in Neotropical cricetines (Muridae) with comments on classification of muroid rodents. Miscellaneous Publications, Museum of Zoology, University of Michigan 123:1–57. Handle: http://hdl.handle.net/2027.42/56367
Irwin, D. M., T. D. Kocher & A. C. Wilson. 1991. Evolution of the cytochrome b gene of mammals. Journal of Molecular Evolution 32:128–144. DOI https://doi.org/10.1007/BF02515385
Jameson, J. S., & P. M. Ramsay. 2007. Changes in high-altitude Polylepis forest cover and quality in the Cordillera de Vilcanota, Peru 1956-2005. Biological Conservation 138(1-2):38–46. https://doi.org/10.1016/j.biocon.2007.04.008
Jayat, J. P., G. D’Elía, U. F. J. Pardiñas, M. D. Miotti & P. E. Ortiz. 2008. A new species of the genus Oxymycterus (Mammalia: Rodentia: Cricetidae) from the vanishing Yungas of Argentina. Zootaxa 1911:31–51. https://doi.org/10.11646/zootaxa.1911.1.2
Kalyaanamoorthy, S., B. Q. Minh, T. K. F. Wong, A. Von Haeseler, & L. S. Jermiin. 2017. ModelFinder: fast model selection for accurate phylogenetic estimates. Nature Methods 14: 587-589. https://doi.org/10.1038/nmeth.4285
Kessler, M. 2006. Bosques de Polylepis. Botánica económica de los Andes Centrales (M. Moraes, B. Øllgaard, L. P. Kvist, F. Borchsenius & H. Balslev, eds.). Universidad Mayor de San Andrés. La Paz, Bolivia.
Kimura, M. 1983. The neutral theory of molecular evolution. Cambridge University Press, Cambridge. Inglaterra.
Lanfear, R., P. B. Frandsen, A. M. Wright, T. Senfeld, & B. Calcott. 2016. Partitionfinder 2: new methods for selecting partitioned models of evolution for molecular and morphological phylogenetic analyses. Molecular Biology and Evolution 34:772– 773 https://doi.org/10.1093/molbev/msw260
Maddison, W. P. & D. R. Maddison. 2010. Mesquite: A modularsystem for evolutionary analysis, version 2.73. <http://mesquiteproject.org>
Miller, M. A., W. T. Pfeiffer, & T. Schwartz. 2010. Creating the CIPRES Science Gateway for Inference of Large Phylogenetic Trees. Gateway Computing Environments Workshop (GCE). https://doi.org/10.1109/GCE.2010.5676129
Myers, P.1989. A preliminary revision of the varius group of Akodon (A. dayi, dolores, molinae, neocenus, simulator, toba, and varius). Advances in Neotropical Mammalogy (K. H. Redford & J. F. Eisenberg, eds. ). Sandhill Crane Press, Inc. Gainesville, Florida, Estados Unidos.
Oliveira, J. A. de. 1998. Morphometric assessment of species groups in the South American rodent genus Oxymycterus (Sigmodontinae), with taxonomic notes based on the analysis of type material. Tesis de Doctorado, Texas Tech University, Lubbock, Estados Unidos.
Oliveira, J. A. de, & P. R. Gonçalves. 2015. Genus Oxymycterus Waterhouse, 1837. Mammals of South America Vol. 2 Rodents (J.L. Patton, U.F.J. Pardiñas & G. D’Elía, eds.). The University of Chicago. Chicago, Illinois, Estados Unidos.
Osgood, W. H. 1944. Nine New South American Rodents. Field Museum Natural History Zool. Ser. 13:191–204.
Pacheco V., R. Cadenillas, E. Salas, C. Tello & H. Zeballos. 2009. Diversidad y endemismo de los mamíferos del Perú. Revista Peruana de Biología 16(1):5–32.
Pacheco, V., G. Márquez, E. Salas & O. Centty. 2011. Diversidad de mamíferos en la cuenca media del río Tambopata, Puno, Perú. Revista Peruana de Biología 18(2):231–244
Patterson, B. D., S. Solari, & P. M. Velazco. 2012. The role of the Andes in the diversification and biogeography of Neotropical mammals. Bones, clones, and biomes: the history and geography of Recent Neotropical mammals (B. D. Patterson & L. P. Costa, eds.). University of Chicago Press. Chicago. Estados Unidos.
Patton, J. L., P. Myers, & M. F. Smith. 1990. Vicariant versus gradient models of diversification: The small mammal fauna of eastern Andean slopes of Peru. Vertebrates in the tropics (G. Peters & R. Hutterer, eds.). Museum Alexander Koenig. Bonn. Alemania.
Patton, J. L., & M. F. Smith.1992. mtDNA Phylogeny of Andean mice: a test of diversification across ecological gradients. Evolution 46:174-183. https://doi.org/10.1111/j.1558-5646.1992.tb01992.x
Peçanha, W. T., F. Marques-Quintela, L. E. J. Ribas, S. L. Althoff, R. Maestri, G. Lopes-Gonçalves & T. R. O. De Freitas. 2019. A new species of Oxymycterus (Rodentia: Cricetidae: Sigmodontinae) from a transitional area of Cerrado – Atlantic Forest in southeastern Brazil. Journal of Mammalogy 100(2):578–598. https://doi.org/10.1093/jmammal/gyz060
Pinto, C. M., R. Ojala-Barbour, J. Brito, A. Menchaca, A. G. Carvalho, M. Weksler, G. Amato & T. E. Lee. 2018. Rodents of the eastern and western slopes of the Tropical Andes: phy- logenetic and taxonomic insights using DNA barcodes. Therya 9:15–27. https://doi.org/10.12933/therya-18-430ISSN2007-3364
Rambaut, A., A. J. Drummond, D. Xie, G. Baele, & M. A. Suchard. 2018. Posterior Summarization in Bayesian Phylogenetics Using Tracer 1.7. Systematic Biology 67: 901-904. https://doi.org/10.1093/sysbio/syy032
Ridgway, R. 1912. Color standards and color nomenclature. Reprint by Elibron Clasics, Washington. Estados Unidos.
Ronquist, F., M. Teslenko, P. Van Der Mark, D. L. Ayres, A. Darling, S. Hóhna, B. Larget, L. Liu, M. A. Suchard & J. P. Huelsenbeck. 2012. MrBayes 3.2: Eficient Bayesian Phylogenetic Inference and Model Choice Across a Large Model Space. Systematic Biology 61:539-542. https://doi.org/10.1093/sysbio/sys029
Ronquist, F. & J. P. Huelsenbeck. 2005. MrBayes v3.1. Bayesian Analysis Phylogeny. Florida: School for Computational Science, University of California, California. Estados Unidos.
Särkinen, T., R. T. Pennington, M. Lavin, M. F. Simon, & C. E. Hughes. 2012. Evolutionary islands in the Andes: persistence and isolation explain high endemism in Andean dry tropical forests. Journal of Biogeography 39:884–900. https://doi.org/10.1111/j.1365-2699.2011.02644.x
Schrago, C. G., & B. Mello. 2020. Employing statistical learning to derive species-level genetic diversity for mammalian species. Mammalian Review 50:1-12. https://doi.org/10.1111/mam.12192
Servat, G., W. Mendoza, & J. A. Ochoa. 2002. Flora y fauna de cuatro bosques de Polylepis (Rosaceae) en la Cordillera del Vilcanota (Cusco, Perú). Ecología Aplicada 1(1):25–35.
Schluter, D. 2000. The ecology of adaptive radiation. Oxford University Press INC, New York, Estados Unidos.
Smith, M. F., & J. L. Patton. 1993. The diversification of South American murid rodents: evidence from mitochondrial DNA sequence data for the Akodontine tribe. Biological Journal of the Linnean Society 50:149–177. https://doi.org/10.1111/j.1095-8312.1993.tb00924.x
Smith, M. F., & J. L. Patton. 1999. Phylogenetic relationships and the radiation of sigmodontine rodents in South America: evidence from cytochrome b. Journal of Mammalian Evolution 6:89–128. https://doi.org/10.1023/A:1020668004578
Solari, S., E. Vivar, P. Velazco & J. J. Rodriguez. 2001. Small mammals of Southern Vilcabamba Región, Perú. Biological and Social Assesments of the Cordillera de Vilcabamba, Peru (L. E. Alonso, A. Alonso, T. Schulenberg & F. Dallmeier, eds.). Rapid Assessment Program, Smithsonian Institution/Monitoring and Assessment Biodiversity Program. Conservation International 12:110-116.
Tamura, K., G. Stecher, D. Peterson, A. Filipski & S. Kumar. 2013. MEGA6: Molecular Evolutionary Genetics Analysis version 6.0. Molecular Biology and Evolution 30:2725-2729. https://doi.org/10.1093/molbev/mst197
Thomas, O. 1900. Descriptions of new rodents from Western South America. Annals and Magazine Natural History ser. 7, 6:294–302.
Thomas, O. 1900. Descriptions of new rodents from Western South America. Annals and Magazine Natural History ser. 7, 6:294–302. Thomas, O. 1901. New mammals from Peru and Bolivia, with a list of those recorded from the Inambari river, Upper Madre de Dios. Annals and Magazine Natural History ser. 7, 7:179–190.
Thomas, O. 1901. New mammals from Peru and Bolivia, with a list of those recorded from the Inambari river, Upper Madre de Dios. Annals and Magazine Natural History ser. 7, 7:179–190.
Thomas, O. 1902. On Mammals from Cochabamba, Bolivia, and the region north of that place. Annals and Magazine Natural History ser. 7, 9:125–143.
Thomas, O. 1920. Report on the Mammalia collected by Mr. Edmund Heller during the Peruvian expedition of 1915 under the auspices of Yale University and the National Geographic Society. Proceedings of United States National Museum 58(2333):217– 249.
Thomas, O. 1925. The Spedan Lewis South American Exploration. I.– On mammals from Southern Bolivia. Annals and Magazine Natural History ser. 9, 15:575–582.
Trifinopoulos, J., L. Nguyen, A. Von Haeseler & B. Q. Minh. 2016. W-IQ-TREE: a fast-online phylogenetic tool for maximum likelihood analysis. Nucleic Acids Research 44(Web Server issue): gkw256. https://doi.org/10.1093/nar/gkw256
Udvardy, M. 1975. A classification of the Biogeographical Provinces of the World. IUCN Occasional Papers Morges (Suiza) 18:1–48.
Upham, N. S., R. Ojala-Barbour, J. Brito, P. M. Velazco, & B. D. Patterson. 2013. Transitions between Andean and Amazonian centers of endemism in the radiation of some arboreal rodents. BMC Evolutionary Biology 13:1–24. http://www.biomedcentral.com/1471-2148/13/191
Van Valen, L. 1976. Ecological Species, Multispecies, and Oaks. Taxon 25(4):233–239. https://doi.org/10.2307/1219444
Vitullo, A. D., M. S. Merani, O. A. Reig, A. E. Kajon, O. Scaglia, M. B. Espinosa & A. PØrez-Zapata. 1986. Cytogenetics of South American akodont rodents (Cricetidae): new karyotypes and chromosomal banding patterns of Argentinean and Uruguayan forms. Journal of Mammalogy 67:69–80. https://doi.org/10.2307/1381003
Vorontsov, N. N. 1979. Evolution of the alimentary system of myomorph rodents [A translation of N. N. Vorontsov, 1967, Evolystsiya pischchevaritel’noi sistemy gryzunov mysheobraznye]. New Delhi (Indian National Scientific Documentation Centre), Published for the Smithsonian Institution and the National Science Foundation, Washington CD, Estados Unidos.
Voss, R. S., & A. V. Linzey. 1981. Comparative gross morphology of male accessory glands among Neotropical Muridae (Mammalia: Rodentia) with comments on systematic implications. Miscellaneous Publications, Museum of Zoology, University of Michigan 159:1–41. <http://hdl.handle.net/2027.42/56403>.
Weberbauer, A. 1945. El mundo vegetal de los Andes peruanos. Estación Experimental Agrícola de La Molina, Dirección de Agricultura, Ministerio de Agricultura. Lima, Perú.
Wiens, J. J. 2007. Species Delimitation: New Approaches for Discovering Diversity. Systematic Biology 56:875–878. doi:10.1080/10635150701748506.
Wiley, E.O. 1978. The Evolutionary Species Concept Reconsidered. Systematic Zoology 27:17–26. https://doi.org/10.2307/2412809
Wilson, D. E., & D. A. Reader. 2005. Mammal Species of the World. A Taxonomic and Geographic Reference. 3rd edition. Johns Hopkins University Press, Baltimore, Estados Unidos.
Young, K. R. 2006. Bosques húmedos. Botánica económica de los Andes Centrales (M. Moraes, B. Øllgaard, L. P. Kvist, F. Borchsenius & H. Balslev, eds.). Universidad Mayor de San Andrés, La Paz, Bolivia.
APÉNDICE 1
Especímenes examinados en este estudio conservados en las siguientes colecciones: Museo de Historia Natural, Universidad Nacional de San Agustín (MUSA; Perú), y Museo de Historia Natural, Universidad Mayor de San Marcos (MUSM; Perú). Los números de depósito en GenBank de las nuevas secuencias se brindan asociados a sus voucher entre corchetes.
Oxymycterus hiska: Perú, Puno, Sandia, Yanahuaya, 14 km W de Yanahuaya (MUSM 19881, paratipo).
Oxymycterus inca: Perú, Cusco, La Convención, Camisea, RC Machiguenga, Río Manitiari (MUSA 3020,3055-3057); Ashiriari 3 (MUSM 14396,14400); San Martín (MUSM 14404-14408); Cashiriari (MUSM 14396, 14400-14404); Paucartambo, Kosñipata, Consuelo 15.9 km SW, Pilcopata (MUSM 20006, 20008); Reserva Comunal Amarakaeri (MUSA 11893); Quispicanchi, Marcapata, Valle de Marcapata, Hda Cadena (MUSM 20254). Madre de Dios, Manu, Madre de Dios, Albergue Maskoitania 13.5km NW Atalaya (MUSM 20007); Tambopata, Tambopata, Estación Malinowski (MUSA 11057). Puno, Carabaya, San Gabán, Quebrada Sansari (MUSA 20694).
Oxymycterus juliacae: Perú, Puno, Carabaya, Coasa, PN Bahuaja Sonene, Línea Sísmica 102, HP 8 (MUSA 570-572,11057, HZP 1038, 1046, 1049, 1053, 1058, 1059, 1070); Parque Nacional Bahuaja Sonene, Línea Sísmica 103 (HZP 1252, 1255); Sandia, Limbani, Inca Mines-Juliaca (MUSA 21582, 21585); Yanahuaya, Yanahuaya (MUSM 35090); San Juan del Oro, Yanamayo, Putinapunku (MUSA 3152). Cusco, La Convención, Camisea, Reserva Comunal Machiguenga (MUSA 5715); Quispicanchi, Camanti, Soqtapata (MUSA 16314, 16316, 16317); Paucartambo, Kosñipata, Villa Carmen (MUSA 19853, 19858, 19878, 19880, 19881, 19891, 19895, 19896, 19899-10901, 19903). Madre de Dios, Tambopata, Tambopata, Sudadero. Línea Sísmica SAP07-10, LP 111 (MUSA 5599).
Oxymycterus nigrifrons: Perú, Puno, Sandia, Limbani, Alrededores de Limbani (MUSA 4709 [MZ322541], 4710 [MZ322542], 4711, 13532), (FMNH 52629, holotipo, foto). Bolivia, La Paz, Sud Yungas, Yancachi, Unduavi (ARC 49, 231 [MZ322543], 232, 353, 382, 384, 395, CBF 19891).
Oxymycterus paramensis: Bolivia, Cochabamba, 4.4. km por carretera al N de Tablas Montes, Río Jatún Mayu (238408 [MZ322539]).
Oxymycterus willkaurco: Perú, Cusco, Calca, Lares, Comunidad Coyllobamba (MUSA 8090); Amparaes (MUSA 8095, 20247), Quishuarani Hatun Queñua (MUSA 6422); Urubamba, Chupani (MUSA 4190-4192, 4193 [MZ322540], 4194); Paucartambo, Kcosñipata, Acjanaco (MUSA 4031, 4051), Acjanaco, Cerro Macho Cruz (MUSM 6720, 6721); Challabamba, Puesto de Vigilancia Acjanaco (MUSM 6723, 6724, 9299-9312, 9315-9320); La Convención, Ocobamba, Yanamayo (MUSA 16409, 16411-16413); Santa Teresa, Salcantay-Camino a Choquequirao (MUSA 20254).
Información adicional
Editor asociado: U. F. J. Pardiñas & C. A. Galliari
Citar como: Zeballos, H., C. E. Medina, A. Rico-Cernohorska & J. Salazar-Bravo. 2021. Una especie nueva de Oxymycterus (Cricetidae: Sigmodontinae: Akodontini) del sureste de Peru. Mastozoología Neotropical, 28(1):e0545. https://doi.org/10.31687/saremMN.21.28.1.0.26
