SECCIÓN ESPECIAL - ARTÍCULO
CÓDIGO DE BARRAS DE ADN PARA LA DELIMITACIÓN DE ESPECIES EN ROEDORES SIGMODONTINOS (CRICETIDAE) DEL NORTE ARGENTINO, CON ESPECIAL ÉNFASIS EN AQUELLAS DE LAS YUNGAS
Using DNA Barcoding for delimitation of species in sigmodontine rodents (Cricetidae) in north Argentina with special emphasis on those of the Yungas forest
CÓDIGO DE BARRAS DE ADN PARA LA DELIMITACIÓN DE ESPECIES EN ROEDORES SIGMODONTINOS (CRICETIDAE) DEL NORTE ARGENTINO, CON ESPECIAL ÉNFASIS EN AQUELLAS DE LAS YUNGAS
Mastozoología Neotropical, vol. 28, núm. 1, p. 541, 2021
Sociedad Argentina para el Estudio de los Mamíferos
Recepción: 29 Septiembre 2020
Aprobación: 26 Enero 2021
Resumen: En esta investigación usamos códigos de barras de ADN como una herramienta para el análisis de la diversidad específica y la variabilidad geográfica de roedores Sigmodontinae (Cricetidae) en el Norte de Argentina. Analizamos 162 individuos de 50 localidades pertenecientes a 31 especies originalmente determinadas mediante morfología. El 72% de las localidades estudiadas se encuentran en las Yungas mientras que el 71% de las especies analizadas habita en alguno de sus estratos altitudinales. Se realizaron dos análisis de delimitación de especies: la implementación bayesiana del método “Poisson Tree Processes” (bPTP) y el método “Automated Barcode Gap Discovery” (ABGD), este último bajo dos modelos de sustitución, K2P y JC69. El método bPTP evidenció linajes diferentes en algunas especies totalizando un recuento de 44 especies, 13 más que las 31 originalmente detectadas. El método ABGD resultó en 40 especies en promedio para todas las particiones recursivas de los dos modelos de sustitución utilizados. Las especies que presentaron más de un linaje genético (especies putativas) con respecto a su determinación original fueron las siguientes: Akodon budini, Akodon simulator, Akodon spegazzinii, Andinomys edax, Necromys lactens, Oligoryzomys chacoensis, Oligoryzomys flavescens . Phyllotis tucumanus. Los resultados obtenidos sugieren una diversidad de roedores sigmodontinos más elevada que la actualmente reconocida en la región de estudio y destacan la necesidad de relevamientos faunísticos más exhaustivos que permitan un apropiado inventario de la biodiversidad.
Palabras clave: bioinformática, COI, inferencia filogenética, inventario de especies, taxonomía.
Abstract: We used DNA barcodes to explore the species diversity and the geographic variability of Sigmodontinae (Cricetidae) rodents in North Argentina. We analyzed 162 individuals from 50 localities belonging to 31 species primarily determined by morphology. Most of the studied localities (72%) are from the Yungas forest while 71% of the analyzed species inhabit some of their altitudinal strata. We performed two species delimitation analyzes, the Bayesian Poisson Tree Processes (bPTP) method, and the Automated Barcode Gap Discovery (ABGD) method, the latter under two substitution models K2P and JC69. The bPTP method reported the presence of different lineages in some species totaling 44 species, 13 more than the 31 originally listed in our database. The ABGD method resulted in 40 species on average for all recursive partitions under the two substitution models. The following species presented more than one genetic lineage (putative species): Akodon budini, Akodon simulator, Akodon spegazzinii, Andinomys edax, Necromys lactens, Oligoryzomys chacoensis, Oligoryzomys flavescens and Phyllotis tucumanus. Our results suggest that the diversity of sigmodontine rodents in northwestern Argentina is higher than the currently recognized, and highlight the need for more exhaustive faunal surveys which allows a more accurate biodiversity inventory.
Keywords: bioinformatics, COI, phylogenetic inference, species inventory, taxonomy.
INTRODUCCIÓN
La delimitación de especies es una tarea crítica con implicancias en todos los campos de la biología. Por ejemplo, la identificación correcta de los organismos en los inventarios de especies es de gran importancia para la cuantificación de la biodiversidad y para responder preguntas en biología evolutiva, ecología, biología de la conservación y biogeografía (Dayrat 2005). En el marco de la actual crisis de la biodiversidad, la taxonomía resulta de gran utilidad para la generación de inventarios fiables de la composición de la diversidad biológica (Wheeler 1995, 2004; Mace 2004).
El Código de Barras de ADN (DNA barcoding) fue propuesto como una contribución a la sistemática, para lograr mayor evidencia en el proceso de identificación y discriminación de especies, además de resaltar casos que necesiten un análisis taxonómico más detallado (Borisenko et al. 2008). Se basa en el análisis de un fragmento del gen mitocondrial Citocromo Oxidasa Subunidad 1 (COI) con condiciones de secuenciación universalmente aceptadas y estandarizadas (Hebert et al. 2003a,b; Lanteri 2007). Este marcador se encuentra presente en todos los organismos, pero es suficientemente variable para determinaciones a nivel específico en animales y ha sido ampliamente aceptado para la identificación taxonómica (Hogg & Hebert 2004; Hebert et al. 2003a,b, 2004; Ward et al. 2005; Costa et al. 2007). Un proyecto de código de barras de ADN típicamente debe involucrar especímenes, análisis de laboratorio y de base de datos (Altamirano-Benavides & Yánez-Moretta 2016). El protocolo destaca la necesidad de relacionar esta información con ejemplares de referencia debidamente colectados, preservados y depositados en museos o colecciones científicas (Lanteri 2007).
En esta contribución, usamos códigos de barras de ADN como una herramienta para el análisis de la diversidad específica y la variabilidad geográfica de roedores sigmodontinos con énfasis en aquellos de los bosques montanos de las Yungas del noroeste de Argentina (NOA). En particular, la subfamilia Sigmodontinae (Cricetidae), con 87 géneros y 443 especies, comprenden más del 50% de la diversidad de especies de roedores de Sudamérica (Patton et al. 2015; Pardiñas et al. 2017). Además, son con frecuencia uno de los grupos más importantes en número de especies en comunidades de mamíferos de varias regiones del continente (Patterson 2000; Musser & Carleton 2005). A pesar de los numerosos avances en el estudio de los cricétidos neotropicales, estos se encuentran aún entre los micromamíferos con mayores vacíos de conocimiento, tanto en el NOA (Jayat et al. 2011) como en otras regiones, tal como lo demuestran las continuas revisiones taxonómicas y la descripción de especies nuevas para la ciencia (e.g., Díaz et al. 1999; Christoff et al. 2000; Jayat et al. 2008a; Percequillo et al. 2008; Bonvicino et al. 2010; Ferro 2010; Rocha et al. 2011; Pardiñas et al. 2013; Jayat et al. 2016a). La incorporación de evidencia molecular ha revelado, entre otros aspectos, la existencia de especies crípticas, naturalmente inadvertidas en estudios morfológicos (Baker & Bradley 2006; Pinto et al. 2018).
El NOA posee una marcada heterogeneidad fisiográfica y ambiental, con elevaciones que van desde 400 m hasta 5000 m s.n.m. y ambientes que incluyen desde selvas hasta desiertos. La variedad ambiental de la región se ve reflejada en la presencia de un tercio de las ecorregiones continentales reconocidas para el país (Burkart et al. 1999). A la par, es un área de alta diversidad biológica donde se puede encontrar el 48% de las especies de mamíferos terrestres de Argentina (Barquez et al. 2006). Las Yungas aunque comprenden menos de un 2% del área total de la Argentina, albergan, sin embargo, aproximadamente un 40% de la biodiversidad nacional (Malizia et al. 2012). No obstante, la diversidad de roedores sigmodontinos y los límites de distribución de las especies se mantienen, con frecuencia, como interrogantes, a tal punto que algunas especies son apenas conocidas por escasos ejemplares, en general procedentes de localidades típicas (Díaz et al. 1999; Pardiñas et al. 2005; Jayat et al. 2006). Todo esto sugiere que la diversidad actual de roedores sigmodontinos del NOA puede estar subestimada. Además, el contexto geográfico de la región, como parte austral de los Andes Centrales, la ubica en la zona con mayor riqueza de roedores en el continente (Maestri & Patterson 2016). Consecuentemente, el NOA constituye una región importante para una mejor comprensión de la evolución y biogeografía de estos mamíferos (Jayat et al. 2011; Formoso & Teta 2019).
El objetivo del presente estudio fue analizar la diversidad de especies de roedores sigmodontinos del NOA, por medio de reconstrucciones filogenéticas y el uso de métodos de delimitación de especies mediante la región “barcode” del COI. Estos resultados permitieron estimar el número de linajes en cada especie y determinar los patrones geográficos de distribución de los mismos, con especial énfasis en la ecorregión de las Yungas.
MATERIALES Y MÉTODOS
Extracción de ADN, amplificación y secuenciación
Para los análisis moleculares se utilizaron tejidos (corazón, hígado, riñón o músculo esquelético) correspondientes a 162 individuos de 50 localidades (Fig. 1), pertenecientes a 31 especies de roedores sigmodontinos, determinados sobre la base de morfología, siguiendo la sistemática propuesta en Barquez et al. (2006), Patton et al. (2015) y Teta et al. (2018). Las muestras fueron obtenidas en colectas de campo realizadas durante más de 10 años de relevamientos faunísticos, e incluye el análisis de ejemplares de siete localidades tipo. El principal repositorio de los ejemplares examinados es la Colección Mamíferos Lillo (CML), Facultad de Ciencias Naturales e Instituto Miguel Lillo, Universidad Nacional de Tucumán, Argentina. También se examinaron ejemplares pertenecientes a los catálogos de campo de Luis I. Ferro (LIF), Juan J. Martínez (JJM), del proyecto “Roedores sigmodontinos de Argentina: clarificación taxonómica, nomenclatural y sistemática a partir de series topotípicas” Localidades Tipo - Rubén Marcos Barquez (LT-RMB) y un ejemplar depositado en la Colección Nacional de Mastozoología (MACN-ma), Ciudad Autónoma de Buenos Aires, Argentina. Las localidades indicadas en la Fig. 1 se listan en el APÉNDICE 1. En este mismo se indican los nombres de los principales taxones específicos citados, a fin de no entorpecer la lectura del texto principal.
Todas las muestras de tejidos se conservaron en etanol al 96%. El ADN genómico se extrajo siguiendo el método de Ivanova et al. (2006), con modificaciones, utilizando columnas de giro individuales en lugar de placas (Martín et al. 2017). El fragmento del gen COI se amplificó mediante PCR y secuenció utilizando el cóctel de cebadores de vertebrados COI-2 (mamíferos): C_VF1LFt1 - C_VR1LRt1 (Ivanova et al. 2007). Las amplificaciones se realizaron en volumen de 12.5 µl que contenía: 1x buffer (Tris-HCl 1 mM [pH 8.3], KCl 5 mM), MgCl2 2.5 mM, la mitad de la mezcla estaba compuesta de trehalosa al 10%, dNTP 0.4 mM, 0.2 mM de cada cebador; 1 U Taq Polimerasa y 20-25 ng de ADN. Las condiciones de termociclado consistieron en una desnaturalización inicial a 94° C durante 2 minutos, 5 ciclos de 94° C durante 30 segundos, unión de los cebadores a 50° C durante 40 segundos y extensión a 72° C durante 1 minuto, seguido de 35 ciclos de 94° C durante 30 segundos, unión de los cebadores a 55° C durante 40 segundos y extensión a 72° C durante 1 min, con una extensión final a 72° C durante 10 min (Ivanova et al. 2007). Tanto las extracciones de ADN como las amplificaciones por PCR se realizaron en los laboratorios de códigos de barras genéticos del CONICET ubicado en el Museo Argentino de Ciencias Naturales “Bernardino Rivadavia” y de la Cátedra de Genética, Facultad de Ciencias Naturales e Instituto Miguel Lillo (IML) y Fundación Miguel Lillo (FML), Argentina. La secuenciación se realizó en el centro canadiense de códigos de barras de ADN del Centro de Genómica de la Biodiversidad, Universidad de Guelph, Canadá, en el marco del proyecto “Pequeños Mamíferos NOA” (MANOA).
Los cromatogramas fueron leídos en ambas direcciones y, posteriormente, se llevó a cabo el alineamiento múltiple de las secuencias utilizando los parámetros por defecto del programa Muscle v.3.6 (Edgar 2004). El mismo fue verificado manualmente en el programa DNAsp v.4.10 (Rozas et al. 2017). Las secuencias se encuentran depositadas en GenBank bajo los números de acceso: MW009859-MW010020. Se calcularon el número, frecuencia de haplotipos y la diversidad nucleotídica como medidas de caracterización de los polimorfismos de las secuencias de ADN mediante el programa DNAsp v.4.10 (Rozas et al. 2017). Adicionalmente, para enraizar los árboles filogenéticos se utilizaron secuencias obtenidas de GenBank pertenecientes a roedores de otros géneros de Cricetidae (Neusticomys sp., Rheomys thomasi, Sigmodon alstoni y Sigmodon hispidus). La selección de los taxones utilizados como grupo externo se basa en su posición filogenética, ya que forman parte de grupos basales dentro de la radiación de la subfamilia Sigmodontinae (Parada et al. 2013).
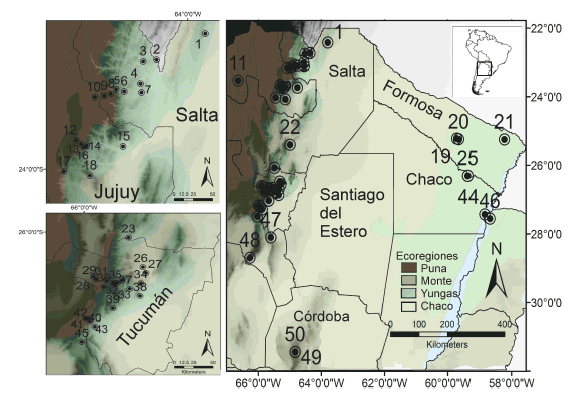
Fig. 1
Localidades de procedencia de los roedores analizados mediante el gen mitocondrial Citocromo Oxidasa Subunidad 1 (COI) en el norte argentino. Para la referencia de las localidades, véase el APÉNDICE 1.
Análisis de reconstrucción filogenética
Se utilizó la inferencia bayesiana como método de reconstrucción filogenética en MrBayes v. 3. 1. 2. (Ronquist et al. 2012) bajo el modelo de sustitución de nucleótidos HKY + I + G. El modelo fue seleccionado mediante el Criterio de Información de Akaike Corregido (AICc) (Akaike 1998) en el programa JModeltest v.2.1.3 (Darriba et al. 2012), utilizando ajustes por defecto. El análisis de inferencia bayesiana fue configurado en cuatro cadenas de Markov, 3 x 107 generaciones con un “burn-in” de 7 500 y los árboles fueron muestreados cada 1000 generaciones. Los árboles restantes fueron resumidos en un árbol de consenso de mayoría del 50%. El soporte de los grupos se obtuvo mediante los valores de probabilidad posterior. La convergencia de las corridas fue evaluada mediante tres parámetros: 1) que la desviación estándar de los cambios de frecuencia fuera suficientemente baja (<0,01), 2) que todos los valores de PSRF (“potential scale reduction factor”) fueron cercanos a 1 y 3) el examen del comportamiento de las cadenas frías mediante gráficos que relacionaron los valores de “log likelihood” a través de las generaciones. Se usó el programa Tracer v1.7.1 (Rambaut & Drummond 2003) para evaluar si los parámetros de interés tuvieron un muestreo adecuado: valores de ESS (“effective sample size”) >200.
Delimitación de especies
Para la detección estadística de los espacios (“gaps”) de divergencia genética en el conjunto de datos se usó el método ABGD (Automated Barcode Gap Discovery) (<https://bioinfo.mnhn.fr/abi/public/abgd/abgdweb.html>;).
Este método tiene como objetivo identificar el espacio entre dos distribuciones de frecuencias basadas en distancias genéticas. A partir de varios umbrales de distancias genéticas elegidos a priori, se calcula primero el límite máximo teórico (P máximo) de la diversidad intraespecífica (mediante modelos de coalescencia). Luego se identifica en toda la distribución de distancias genéticas entre pares de individuos qué distancia genética es superior al P máximo, la denominada “distancia de código de barras potencial”, es decir, un límite potencial entre la diversidad intra e interespecífica. La inferencia del límite y la detección de distancias se aplican de forma recursiva a los grupos obtenidos previamente, para obtener particiones más finas hasta que no haya más divisiones (Puillandre et al. 2012). Se utilizaron los valores de umbrales de distancias genéticas P por defecto, P mínimo=0.001 y P máximo=0.1 (umbrales de máxima y de mínima divergencia intraespecífica, respectivamente). Se establecieron sucesivos valores decrecientes de amplitud relativa de la distancia potencial del código de barras a partir del valor X=1.1 (máximo valor que logró dividir al conjunto de datos) variando en 0.2 unidades hasta X=0.3. Los demás parámetros del programa se mantuvieron bajo valores por defecto. Dado que este método se basa en la similitud entre pares de secuencias, es preciso definir los modelos de sustitución de pares de bases sobre los cuales se realizará la comparación. Se realizaron dos análisis usando los modelos de Kimura (1980; K2P) y de Jukes & Cantor (1969; JC69), para los cuales se registraron todos los resultados con umbrales de divergencia intraespecífica en el rango 0.001- 0.1 (Puillandre et al. 2012).
Alternativamente, se realizó un análisis de delimitación de especies mediante la implementación bayesiana del método PTP (Poisson Tree Processes), bPTP (Zhang et al. 2013) en el servidor web <https:/species.h-its.org/>. Este fue desarrollado como un criterio operacional del concepto filogenético de especie (Eldredge & Cracraft 1980) para inferir grupos basados en filogenias moleculares. El modelo PTP permite distinguir los procesos de especiación y eventos coalescentes a lo largo de las ramas de una topología dada; por lo tanto, requiere un árbol filogenético como entrada con las longitudes de las ramas que representan el número de mutaciones. El modelo PTP estima el número medio esperado de sustituciones por sitio entre dos eventos de ramificación, utilizando la información de longitud de la rama del árbol filogenético de entrada. Luego implementa dos clases independientes de procesos de Poisson (eventos de ramificación intra e interespecíficos) y agrupa el árbol filogenético en consecuencia. La implementación bayesiana del modelo PTP permite el cálculo de probabilidades posteriores como: (el número de apariciones de todos los descendientes bajo un nodo dado) / (el número de muestras). Esto representa la probabilidad a posteriori, bajo el modelo PTP, de que los taxones formen una especie. Los valores de soporte resultantes están fuertemente correlacionados con la precisión de la delimitación. En síntesis, el algoritmo de bPTP puede delimitar especies usando filogenias no ultramétricas, debido a que modela la tasa de especiación mediante el uso directo del número de sustituciones por sitio entre dos eventos de ramificación (Zhang et al. 2013).
Se utilizó el árbol no ultramétrico de consenso obtenido a partir del análisis bayesiano y se corrieron 500000 generaciones (“thinning”=500) con “burn-in” de 0.25 y los demás parámetros se mantuvieron por defecto.
Finalmente, se estimó la distancia genética promedio entre especies (y entre linajes, para aquellas especies cuyos resultados sobre delimitación de especies sugirieron la presencia de más de un linaje genético) mediante el modelo K2P y se estimó la varianza entre grupos mediante 1000 réplicas de bootstrap en el programa MEGA versión X (Kumar et al. 2018). Se construyeron gráficos de violines, cajas y bigotes para caracterizar la variación genética en cuatro categorías: entre linajes genéticos, entre especies de un género, entre especies dentro de una tribu y, finalmente, entre especies de diferentes tribus. Los diagramas de la variación genética entre categorías fueron construidos mediante la función geom_violin del paquete ggplot2 3.3.2 (Wickham 2016) para R 4.0.3 (R Core Team 2020).
RESULTADOS
Obtuvimos secuencias correspondientes a 162 individuos de 31 especies de roedores sigmodontinos (representando a 13 géneros y cinco tribus), distribuidas en 50 localidades del noroeste argentino (Fig. 1). De estas 50 localidades, 36 (72%) se encuentran en la ecorregión de Yungas, mientras que 22 de las 31 especies analizadas (70.97%) habitan alguno de sus estratos altitudinales. El alineamiento de las secuencias de COI para las 31 especies analizadas no reportó “gaps” internos y tuvo una longitud de 615 pb. La composición nucleotídica del fragmento del gen analizado indicó una proporción menor de G (16.6%), mientras para los demás nucleótidos fue similar entre sí: T (29.0%), A (27.7%) y C (26.7%). Se observó un total de 151 sitios polimórficos (S) y 100 haplotipos, con altos valores de diversidad haplotípica (Hd=0.9904±0.0021) y nucleotídica (π=0.13896±0.00329).
El análisis de inferencia bayesiana recuperó al grupo interno como monofilético, cuya composición genérica resultó consistente con las cinco tribus representadas en el conjunto de datos. Todas las especies originalmente establecidas mediante morfología fueron recuperadas como clados monofiléticos con elevados valores de soporte (Figs. 2-5). Sin embargo, un espécimen (CML 11116) determinado originalmente como Akodon budini, proveniente de la localidad de Cuesta Chica (departamento Orán, Salta) no se recuperó como perteneciente a ninguna otra especie analizada previamente tanto en este conjunto de secuencias, como en la base de GenBank mediante la herramienta de búsqueda BLAST (Basic Local Alignment Search Tool) (Fig. 4). Su análisis filogenético indicó una estrecha relación con A. spegazzinii con divergencias genéticas entre 1.8% con respecto al linaje C de A. spegazzinii (Tabla S1). Esta secuencia fue clasificada como una especie diferente mediante todos los métodos de delimitación utilizados (Fig. 4). El método bPTP mostró una delimitación específica coincidente, en general, con la determinación morfológica de las especies. Sin embargo, dividió algunas poblaciones como linajes diferentes, totalizando un recuento de 44 especies, 13 más que las 31 originalmente reconocidas en nuestra base de datos. Las especies que presentaron más de un linaje genético (especies putativas) con respecto a su determinación morfológica fueron: Akodon budini, Akodon simulator, Akodon spegazzinii, Andinomys edax, Necromys lactens, Oligoryzomys chacoensis, Oligoryzomys flavescens y Phyllotis tucumanus (Fig. 2-5).
Para la delimitación de especies mediante el método ABGD, se tuvo en cuenta el valor máximo de amplitud relativa del “gap” en el conjunto de datos (X=1.1) y las particiones recursivas, para ambos modelos de sustitución de pares de bases. El rango de especies delimitadas por ABGD para las particiones recursivas de todos los modelos resultó entre 36 y 43 especies usando el modelo K2P; mientras que para el modelo JC69 el recuento de especies fue entre 35 y 46 especies. El promedio, para todas las particiones recursivas de los dos modelos, resultó de 40 especies.
Las particiones más próximas al promedio de especies recuperadas mediante bPTP se presentaron para una amplitud relativa igual a X=1.1 y 0.9 entre los valores P mínimos comprendidos entre 0.00167 y 0.00278. Para la primera amplitud relativa, el modelo JC69 mostró dos particiones con número de especies igual al número de especies delimitadas por el método bPTP (44) con los valores Pmin=0.00167- 0.00278, mientras que el modelo K2P, reportó dos particiones de 43 especies.

Fig. 2
Árbol de consenso de mayoría obtenido mediante inferencia bayesiana: relaciones filogenéticas para los especímenes representantes de las tribus Andinomyini y Oryzomyini. La localidad de procedencia se indica entre paréntesis luego de la información del voucher. Las especies delimitadas por los métodos ABGD (modelos JC69 y K2P) y bPTP se encuentran representadas con barras de diferentes colores. Se indican los valores de soporte de probabilidad posterior.

Fig. 3
Árbol de consenso de mayoría obtenido mediante inferencia bayesiana: relaciones filogenéticas para los especímenes representantes de las tribus Phyllotini y Euneomyini. Para detalles adicionales, véase la Fig. 2.

Fig. 4
Árbol de consenso de mayoría obtenido mediante inferencia bayesiana: relaciones filogenéticas para parte de los especímenes representantes de la tribu Akodontini. Para detalles adicionales, véase la Fig. 2. La secuencia CML 11116 (Akodon sp.) proviene de un ejemplar perteneciente a Akodon budini.
Las dos medidas de distancia genética presentaron similitudes respecto a la delimitación de especies, a excepción de las siguientes: (1) Akodon boliviensis, que bajo el modelo K2P se recuperó como una única unidad taxonómica, mientras que fue dividida en cuatro especies putativas mediante el modelo JC69 (Fig. 4); (2) Oligoryzomys brendae, fue dividida en dos especies bajo el modelo K2P, si bien mediante el modelo JC69 se mantuvo como una única especie (Fig. 2); (3) O. chacoensis, que fue delimitada en dos linajes bajo el modelo K2P (CML 12123 constituyó una especie diferente), al igual que con el método bPTP, fue considerada como una sola especie bajo el modelo JC69 (Fig. 2); y (4) Necromys lactens, constituida por dos linajes bajo el modelo K2P, al igual que con el método bPTP, fue considerada como una sola especie bajo el modelo JC69 (Fig. 5).
Teniendo en cuenta el modelo K2P para una amplitud relativa del espacio igual a X=1.1 comprendido entre Pmin=0.00167 y Pmax=0.1, la composición de las especies delimitadas por el método ABGD resultó similar a la resultante del método bPTP: 43 y 44 especies, respectivamente. Las discrepancias ocurrieron en Akodon boliviensis, Necromys lactens Oligoryzomys brendae, O. chacoensis y O. flavescens y cuya delimitación resultó diferente entre los métodos ABGD y bPTP (Figs. 2-5). El modelo JC69, bajo los parámetros establecidos, coincidió únicamente con el modelo K2P en el caso de O. flavescens.
Las distancias genéticas bajo el modelo K2P se muestran en la Tabla S1. Para aquellas especies con más de un linaje genético, los valores de divergencia fueron los siguientes: Akodon budini (5.9%), A. simulator (3.0% a 4.1%) y A. spegazzinii (1.3% a 1.8%) Andinomys edax (1.9% a 4.2%), Necromys lactens (4%), Oligoryzomys chacoensis (0.8%), O. flavescens (2.1%), Phyllotis tucumanus (1.7% a 4.9%). El análisis de la variación de la divergencia genética indica que la distancia media entre linajes (o especies putativas) fue de 3.1% (rango: 0.8%- 5.9%), la distribución indica una aparente bimodalidad en la forma de la distribución (Fig. 6). La divergencia entre especies pertenecientes a un género tuvo un valor medio de 10.2% (rango: 3.4%-15.6%), la divergencia entre especies pertenecientes a una misma tribu mostró un valor medio de 15.9% (rango: 10.1%- 21.9%) y, finalmente, la divergencia entre especies pertenecientes a diferentes tribus indica un valor medio de 18.6% (rango: 12.4%- 26.5%; Fig. 6).

Fig. 5
Árbol de consenso de mayoría obtenido mediante inferencia bayesiana: relaciones filogenéticas para los especímenes de otros representantes de la tribu Akodontini. Para detalles adicionales, véase la Fig. 2.
DISCUSIÓN
El código barras de ADN fue diseñado como una técnica que analiza secuencias de uno o algunos genes de referencia a gran escala, para acelerar la asignación de especímenes a especies e incrementar el descubrimiento de nuevas especies (Hebert et al. 2003a; Stoeckle 2003). Sus proponentes previeron el desarrollo de bases de datos de secuencias asociadas a especímenes testigo (vouchers) representativas de especies descriptas con las cuales se pueden comparar secuencias de individuos colectados (Moritz & Cicero 2004). En el presente trabajo implementamos la técnica de código de barras de ADN haciendo uso del gen COI y esta demostró ser una herramienta de utilidad para la delimitación de especies de roedores sigmodontinos en el NOA. Para las especies aquí analizadas, los resultados indicaron una diversidad específica mayor a la originalmente listada en las últimas revisiones taxonómicas para la zona de estudio. Sin embargo, existieron algunas discrepancias entre los dos métodos de detección de especies, bPTP y ABGD y los modelos de sustitución (K2P y JC69), aplicados a este último.
El método ABGD detecta las rupturas en la distribución de distancias genéticas entre pares de individuos, denominada “brecha de código de barras” (Hebert et al. 2003a). La misma se basa en el supuesto que la distancia genética entre organismos de una misma especie será menor que la divergencia observada entre individuos de diferentes especies; por esto, es muy sensible a los parámetros de umbral de similitud e ignora las relaciones evolutivas. En este método se opera bajo el concepto genético de especie.

Fig. 6
Gráfico de violines, cajas y bigotes indicando la variación genética en cuatro categorías: linajes = entre linajes para aquellas especies que evidenciaron la presencia de más de un linaje, género = entre especies de un género, tribu = entre especies dentro de una tribu y entre tribus = entre especies pertenecientes a diferentes tribus. Se muestran los diagramas de densidad para resaltar la forma de la distribución de los datos. Las cajas delimitan el rango intercuartílico, la barra horizontal indica la mediana, y los bigotes muestran los valores extremos de la distribución. Los puntos indican valores atípicos de la distribución.
Los métodos de delimitación de especies basados en árboles, como PTP, se basan en el concepto filogenético de especie (Sites & Marshall 2004; Zhang et al. 2014), bajo el supuesto de monofilia recíproca. El método PTP implementa un enfoque basado en la filogenia sin necesidad de definir umbrales a priori. Sin embargo, su precisión se ve afectada cuando se aplica a grandes conjuntos de datos ya que no tiene en cuenta la variación intraespecífica divergente (Zhang et al. 2013).
A continuación, se discuten los resultados sobre la base del arreglo taxonómico por tribus con énfasis en aquellos casos en los cuales hubo delimitación de grupos dentro de especies nominales. Respecto de las implicancias taxonómicas del presente trabajo destacamos aquellos casos en que ambos métodos (bPTP y ABGD) fueron coincidentes en la delimitación de especies diferentes y relativizamos aquellos casos en que se detectaron diferencias entre métodos.
Tribu Oryzomyini (Fig. 2)
O. flavescens fue delimitada como dos especies diferentes mediante ambos modelos de sustitución del método ABGD (distancia K2P: 2.1%): una proveniente del Departamento Pirané, Formosa (zona transicional entre las ecorregiones Chaco Húmedo y Chaco Seco) y la otra de la Provincia de Tucumán. Una posible interpretación de este resultado es que la especie de Formosa sea, en realidad, Oligoryzomys fornesiMassoia, 1973, una forma presuntamente endémica del noreste argentino, cuyo estatus taxonómico permanece incierto dada la extrema similitud morfológica con O. flavescens (Massoia 1973; González Ittig et al. 2010). Alternativamente, este resultado es coincidente con reconstrucciones filo- genéticas realizadas a partir del gen mitocondrial Citocromo b (cyt b) por Rivera et al. (2018), quienes revelaron la existencia de dos linajes divergentes en 3.3%, sugiriendo que las poblaciones del oeste de Argentina fueran consideradas como una especie diferente (para la que quizás se podría aplicar el nombre previamente acuñado para Mendoza de O. occidentalis Contreras & Rosi 1980). Sin embargo, el método bPTP delimitó una única especie, incluyendo el espécimen formoseño (CML 12129) en el grupo de los especímenes de la Provincia de Tucumán.
En el caso de O. brendae, dos individuos (CML 11508 y CML 11509) de los bosques montanos de Jujuy, fueron reconocidos como una especie diferente por el método ABGD (modelo K2P), con mínimos valores de divergencia promedio (0.6%). Esta divergencia fue similar a la reportada por Teta et al. (2013), con valores de 0.9% para O. brendae. Cabe destacar que Oligoryzomys pachecoiHurtado y D’Elía, 2018, recientemente descripta para las Yungas de Bolivia (Hurtado & D’Elía 2018), podría encontrarse en el territorio argentino, dada la continuidad ambiental. Sin embargo, la distancia reportada entre O. pachecoi y O. brendae es de 5.3% para el gen mitocondrial Citocromo b (cyt b). Además, pese a la extensa cobertura en el muestreo y de las plausibles discontinuidades ambientales, no se evidencia la presencia de estructura filogeográfica en nuestros resultados. O. chacoensis, por su parte, fue dividida en dos especies por los métodos bPTP y ABGD (modelo K2P). Esta diferenciación se debe a un individuo colectado al norte de Tartagal, Departamento Gral. José de San Martín, Salta, que se diferencia con valores promedio de divergencia genética en 0.8%, similares en su valor máximo (1.39%) a los descriptos por González Ittig et al. (2010). Hurtado & D’Elía (2018), mediante una evaluación de la diversidad de especies de Oligoryzomys realizada con base a secuencias del gen cyt b, plantearon la división de O. chacoensis en dos especies candidatas. La primera de ellas se corresponde a la descripta por Myers & Carleton (1981), mientras que la otra forma fue referida como O. aff. O. chacoensis. La localidad de procedencia de esta última secuencia es Boquerón, oeste de Paraguay, que se encuentra relativamente cercana al sitio de colecta del espécimen aquí analizado (CML 12123). Di-Nizo (2018), mediante un análisis con el mismo gen, encontró un patrón similar donde el ejemplar referido a O. aff. O. chacoensis fue agrupado junto a O. chacoensis, con valores de divergencia del 3%.
Tribu Phyllotini (Fig. 3)
Los dos métodos de delimitación implementados, bPTP y ABGD (ambos modelos), distinguieron cuatro especies candidatas en Phyllotis tucumanus correspondientes a las provincias de Catamarca (1 especie), Tucumán (1 especie) y Salta/Jujuy (2 especies). Los valores de distancia genética promedio entre grupos, reportados por ABGD fueron de 3.2% para K2P y 3.1 % para JC69. Bradley & Baker (2001) propusieron que valores de distancia genética entre 2% y 10% podrían corresponder tanto a poblaciones conespecíficas como a especies plenas y que ameritarían estudios taxonómicos adicionales.
Jayat et al. (2016b) revalidaron las formas nominales P. nogalaris y P. tucumanus para poblaciones del NOA previamente referidas a P. osilae Allen, 1901. Estos autores proveen una diagnosis enmendada de P. nogalarisThomas, 1921 sobre la base de especímenes provenientes de dos localidades en pastizales a 3000 m de las Sierras de Zenta y que se encontraron en simpatría con la especie más extendida geográficamente, P. tucumanus. Nuestra delimitación de un único individuo (CML 11643; Abra de Volcán, 38.8 km al ENE de Humahuaca, 3150 m, Salta) como una especie diferente, sumado a que otro espécimen de la misma localidad (CML12310) es recuperado como perteneciente una especie más extendida en el NOA, nos sugiere que el CML 11643 podría corresponder a P. nogalaris (sensu Jayat et al. 2016b). Sin embargo, debemos notar aquí que la localidad tipo de P. nogalaris (Higuerilla, 2000 m), cuya ubicación geográfica ha permanecido como incógnita durante años (Pardiñas et al. 2007), se emplaza inmersa en los bosques montanos de los faldeos orientales de la Sierra de Tilcara, cuya composición específica difiriere marcadamente de los pastizales de los niveles altitudinales superiores (Ferro & Barquez 2014). En este sentido, la asignación del epíteto P. nogalaris a esta entidad, sin revisión del ejemplar tipo o al menos de material topotípico, podría ser prematura y requiere una adecuada exploración.
Por su parte, P. tucumanus presenta cuatro formas genéticas de acuerdo al gen mitocondrial cyt b, estructuradas geográficamente de norte a sur y con cierta diferenciación morfológica (Jayat et al. 2016b). Nuestros resultados indican la presencia de una especie candidata distribuida en la Cordillera Oriental de Salta y Jujuy, coincidente con la “forma 3” de P. tucumanus reconocida por Jayat et al. (2016b). En cambio, la “forma 1” (Phyllotis tucumanus sensu stricto) indicada por estos autores, cuya distribución abarcaría todo el extremo sur de las Yungas, es delimitada como dos especies diferentes por todos los métodos en nuestro análisis; una en la provincia de Tucumán (Phyllotis tucumanus sensu stricto) y una especie adicional en la provincia de Catamarca, con una divergencia de 1.7%.
Tribu Andinomyini (Fig. 2)
Nuestros resultados sobre la delimitación de especies en A. edax fueron congruentes entre sí. Se detectaron tres grupos genéticos, dos septentrionales en Salta y Jujuy y uno austral, en Tucumán. Se han reconocido dos subespecies para Andinomys edax (Yepes 1935; Salazar-Bravo & Jayat 2015): Andinomys edax edax (distribuida desde el sur de Perú hasta el extremo más septentrional del NOA) y Andinomys edax lineicaudatus (extremo más meridional del NOA). Esto coincide, a grandes rasgos, con nuestros hallazgos. Díaz & Barquez (2007), por su parte, trataron los taxones mencionados a nivel de especie: A. edax restringida a hábitats de Puna y Prepuna (entre 2000-4800 m) y A. lineicaudatus en Yungas (debajo de los 2500 m). La delimitación de CML 11801 como una especie diferente por todas las metodologías sugiere la existencia de más de una forma no descripta. Los valores de distancia genética promedio entre grupos resultaron de 1.9% a 4.2% (modelo K2P); por lo que el análisis podría estar detectando variabilidad asignable a taxa subespecíficos o bien especies de reciente separación, de acuerdo al criterio de Bradley & Baker (2001). Por su parte, Jayat et al. (2017) encontraron cuatro linajes mediante análisis de cyt b, pero consideraron a Andinomys como monotípico, dada la similitud morfológica y las proyecciones de modelos de distribución de espacies para estos linajes. Por el contrario, nuestros resultados sugieren la existencia de más de una forma en este género.
Tribu Akodontini (Figs. 4 y 5)
El método bPTP, al igual que ABGD bajo el modelo K2P, dividió a Necromys lactens en dos grupos genéticos bien estructurados geográficamente, uno en el norte de Salta y otro en Tucumán, con una divergencia de 2.5% para ambos modelos de sustitución. Resultados similares fueron reportados sobre la base del gen cyt b, con niveles de divergencia genética promedio de 3.3% (Jayat et al. 2020). No obstante, estos autores no encontraron diferencias morfométricas entre los linajes “Norte” y “Sur” y optaron por mantener la especie como monotípica. El género Akodon, por su parte, es uno de los más diversos y complejos de la radiación sigmodontina y actualmente se encuentra compuesto por unas 40 especies vivientes (Musser & Carleton 2005; Pardiñas et al. 2005, 2015). En nuestro conjunto de datos estuvo representado por 10 especies: A. albiventer, A. azarae, A. boliviensis, A. budini, A caenosus, A. fumeus, A. polopi, A. simulator, A. spegazzinii y A. toba.
Akodon simulator es una especie dominante en la ecorregión de las Yungas. Myers (1989) consideró la existencia de tres subespecies en el NOA: A. simulator tartareus Thomas 1919 al norte, A. simulator simulator al centro y A. simulator glaucinus Thomas 1919 al sur. El presente estudio abarca la totalidad del rango geográfico de la especie e incorpora material topotípico para las tres subespecies. Todos los métodos de delimitación aquí utilizados fueron coincidentes en delimitar tres especies en congruencia con las formas descriptas, con valores de divergencia genética entre linajes de 3.0% y 4.1% (K2P). Braun et al. (2008), al contrario, indicaron valores bajos de divergencia (2.33 - 3.44 %) y una clara estructuración geográfica sobre la base de cinco especímenes procedentes de los extremos de la distribución. Por esto, atendiendo al criterio de Baker & Bradley (2006), propusieron la elevación a especie de A. simulator, A. glaucinus y A. tartareus. La adición de ejemplares nos reveló que no existe una estructuración geográfica clara, encontrándose una especie restringida al norte, una al sur y una tercera ampliamente distribuida. Este patrón podría deberse a diferentes motivos, entre los que se cuentan la introgresión debida a hibridación y la separación incompleta de linajes, que crean confusión acerca de los límites de las especies entre las filogenias y discordancias entre las genealogías de genes y de especies. El uso de un único locus de ADNmt tiene limitaciones inherentes a su naturaleza, como la susceptibilidad a cuellos de botella y su herencia principalmente materna (Avise 2000; Freeland 2005). Esto dificulta dilucidar si el patrón aquí observado se debe a la existencia efectiva de tres especies diferentes, a dos especies y un híbrido, o a una única especie. Este problema se identifica como una limitante en el uso de ADNmt (Rubinoff 2006). Las relaciones entre taxones se pueden distinguir con mejor resolución cuando se estudia más de un marcador molecular (Feijoo et al. 2010; Teta et al. 2011; Martínez et al. 2012; Parada et al. 2015; Martínez & Gardenal 2016), para establecer así la congruencia de las reconstrucciones filogenéticas basadas en cada gen.
Akodon spegazzinii, tal como se considera actualmente, exhibe una variación morfológica intraespecífica considerable, principalmente expresada en la coloración del pelaje consistente con patrones de variación geográfica. Diversos autores han reflejado esta variación en sus revisiones taxonómicas, ya fuera como especies o subespecies: Akodon spegazzinii al oeste, en los valles Calchaquíes, Akodon tucumanensis Allen 1901 al este, en las planicies y selvas montanas y Akodon alterus Thomas, 1919 que se distribuye en los pastizales altomontanos (Myers et al. 1990; Díaz et al. 2000; Pardiñas et al. 2006; Jayat et al. 2008b). En este estudio los métodos de delimitación de especies ABGD y bPTP detectaron 3 grupos genéticos dentro de la especie. No obstante, no se encontró una estructura geográfica coincidente con la asignada tradicionalmente para cada subespecie. De hecho, los individuos provenientes de Otro Cerro (localidad tipo de A. alterus) fueron agrupados dentro de dos clados diferentes, ambos de las selvas y llanuras al este de Tucumán. Nuestros datos incluyen un único ejemplar procedente de los valles Calchaquíes, por lo que resulta necesaria más información sobre el área para dilucidar la diferenciación de esta forma geográfica. La matriz de distancias genéticas mostró valores de divergencia entre linajes de 1.3% y 1.8%. Valores similares se obtuvieron en un estudio basado en cyt b (Jayat et al. 2010, 2019), que indicarían escasa diferenciación entre los grupos genéticos encontrados, suponiendo linajes en vías de diferenciación.
En cuanto a Akodon budini, la presente investigación sugiere que esta especie está compuesta por dos grupos genéticos con elevados valores de soporte. Los métodos bPTP y ABGD (considerando ambos modelos de sustitución) coincidieron en delimitar estos grupos como especies diferentes, recíprocamente monofiléticos y con una marcada estructura geográfica, correspondientes a las provincias de Jujuy (sur) y Salta (norte). La distancia genética entre ambos linajes fue de 5.9%. Teniendo en cuenta esto último, dicha separación en dos grupos genéticos se podría deber a la existencia de, al menos, dos especies. Estudios morfológicos y morfométricos adicionales sobre los especímenes examinados, como el incremento del número de especímenes y localidades, resultan necesarios para decidir si estos hallazgos se traducen en cambios taxonómicos. A. budini es tradicionalmente considerada monotípica, pero incluye en su sinonimia a A. deceptorThomas, 1921, con localidad tipo en Higuerilla, Jujuy (Thomas 1918; Pardiñas et al. 2015).
Se destaca que una secuencia perteneciente al ejemplar CML 11116, cuya identidad no puedo ser determinada mediante el código de barras de ADN. La similitud genética de esta secuencia con A. spegazzinii (2.4%) y, en especial, respecto al linaje C de A. spegazzinii (1.8%), podría indicar conespecificidad, lo que implicaría una ampliación de rango de aproximadamente 250 km. Sin embargo, la revisión del ejemplar depositado en la Colección Mamíferos Lillo revela que se trata indudablemente de Akodon budini, como fuera originalmente mencionado (Ferro 2010), por lo que podría tratarse de una contaminación de la muestra durante el proceso de obtención de la secuencia. Estos resultados ponen de manifiesto la importancia del estudio de especímenes voucher, la diagnosis morfológica y evidencia de múltiples fuentes para el estudio de la diversidad biológica.
CONCLUSIONES
Como evidencian los resultados obtenidos, la taxonomía alfa de los roedores sigmodontinos, en una región fisiográfica y ambientalmente heterogénea como es el NOA, parece lejos de estar resuelta. El descubrimiento, descripción y frecuentes cambios nomenclatoriales de especies de roedores ponen en evidencia la necesidad de realizar muestreos más exhaustivos para varias formas y la aplicación de análisis bajo un enfoque integrativo, que incluya morfología y aspectos moleculares, como así también la inferencia filogenética a partir del uso de varios marcadores apropiados (nucleares y mitocondriales).
Las principales limitaciones que encontramos fueron: (1) el muestreo insuficiente para ciertas especies y géneros analizados cuya representatividad, basada principalmente en taxones de amplia distribución, limita la obtención de conclusiones acerca de la estructura geográfica y divergencia genética, (2) el uso de un único marcador que comprometería la resolución de las relaciones filogenéticas entre especie y géneros.
A pesar de estas limitaciones, el presente estudio es pionero en la aplicación del método de código de barras genético (DNA barcoding) en roedores del NOA y constituye un aporte importante al conocimiento de la biodiversidad en esta región.
Un enfoque integrativo de la taxonomía es necesario para acelerar y hacer más eficiente la delimitación de las especies. Dado que existen numerosas disciplinas que dependen de la fiabilidad de las delimitaciones específicas (ecología, conservación, biogeografía, etc.), se precisa del uso de herramientas complementarias para la delimitación de las especies. En el presente trabajo de investigación, el “DNA barcoding” demostró ser una herramienta eficiente para delimitar especies. A pesar de que no todas las unidades estudiadas estuvieron representadas por un tamaño elevado de muestras, las variaciones polimórficas del gen mitocondrial COI para el conjunto de datos resultaron suficientes para llevar a cabo los análisis de inferencia filogenética y de delimitación de especies. Un aspecto a destacar es que todas las especies para las cuales los dos enfoques utilizados sugieren la presencia de diferentes linajes genéticos habitan en la ecorregión de Yungas. Sobre la base de los resultados aquí obtenidos, se sugiere la presencia de 30 especies, en lugar de 22, que se distribuyen, al menos en parte, en las selvas de Yungas. Considerando que en este trabajo solo incluimos apenas una porción de las especies presentes en esta ecorregión y que continuamente se describen especies previamente desconocidas para la ciencia, podemos afirmar que tanto la profundización de los estudios sistemáticos como la exploración de campo, incrementarán el número de especies en esta región del país.
Materiales suplementarios
MATERIAL SUPLEMENTARIO ONLINE (pdf) Suplemento 1
Tabla S1. Distancias genéticas K2P entre especies/linajes de roedores sigmodontinos basadas en el gen COI. Diagonal inferior: valores medios de distancia genética. Diagonal superior: errores estándares estimados mediante 1000 réplicas de bootstrap. Las etiquetas indican las dos primeras letras del nombre genérico y las tres primeras del nombre específico (por ejemplo, Ho_cha = Holochilus chacarius). Los linajes se denominan de acuerdo a las Figs. 2-5.
Agradecimientos
Agradecemos al Fondo iBOL (International Barcode of Life) Argentina y a CONICET, por proporcionar los fondos para la preservación y secuenciación de los especímenes utilizados en la presente investigación (PIP 6179 2005-2006 “Roedores Sigmodontinos de Argentina: clarificación taxonómica, nomenclatural y sistemática a partir de series topotípicas” bajo la dirección de Ulyses Pardiñas y Ruben Barquez). Agradecemos a U. Pardiñas, C. Miguel Pinto y a un revisor anónimo, cuyas sugerencias ayudaron a mejorar el manuscrito. Al Consejo Interuniversitario Nacional (CIN) que otorgó una beca “Estimulo a las Vocaciones Científicas” para la realización de esta investigación. LDA le agradece a Emma Laura Alfaro Gómez por su ayuda y apoyo durante la realización de este trabajo.
REFERENCIAS
Akaike, H. 1998. Information Theory and an Extension of the Maximum Likelihood Principle. Selected Papers of Hirotugu Akaike. (E. Parzen, K. Tanabe & G. Kitagawa, eds.) Springer Series in Statistics (Perspectives in Statistics). Springer, New York, https://doi.org/10.1007/978-1-4612-1694-015
Altamirano-Benavides, M. & P. Yánez-Moretta. 2016. El código de barras de ADN (barcoding): una herramienta para la investigación y conservación de la diversidad biológica en Ecuador. La Granja: Revista de Ciencias de la Vida 23:5–13. https://doi.org/10.17163/lgr.n23.2016.01
Avise, J. C. 2000. Phylogeography. The history and formation of species. Harvard University Press, Cambridge, United Kingdom.
Baker, R. J., & R. D. Bradley. 2006. Speciation in mammals and the genetic species concept. Journal of Mammalogy 87:643–662. https://doi.org/10.1644/06-mamm-f-038r2.1
Barquez, R. M., M. M. Díaz, & R. A. Ojeda. 2006. Mamíferos de Argentina: sistemática y distribución. Sociedad Argentina para el Estudio de los Mamíferos (SAREM), Mendoza. https://doi.org/10.31687/saremlr.19.090
Bonvicino, C. R., J. A. De Oliveira, & R. Gentile. 2010. A new species of Calomys (Rodentia: Sigmodontinae) from eastern Brazil. Zootaxa 2336:19–35. https://doi.org/10.11646/zootaxa.2336.1.2
Borisenko, A. V., B. K. Lim, N. V. Ivanova, R. H. Hanner, & P. D. Hebert. 2008. DNA barcoding in surveys of small mammal communities: a field study in Suriname. Molecular Ecology Resources 8:471–479. https://doi.org/10.1111/j.1471-8286.2007.01998.x
Bradley, R. D., & R. J. Baker. 2001. A test of the genetic species concept: cytochrome-b sequences and mammals. Journal of Mammalogy 82:960-973. https://doi.org/10.1644/1545-1542(2001)082<0960:atotgs>2.0.co;2
Braun, J. K., B. S. Coyner, M. A. Mares & R. A. van Den Bussche. 2008. Phylogenetic relationships of South American grass mice of the Akodon varius group (Rodentia, Cricetidae, Sigmodontinae) in South America. Journal of Mammalogy 89:768–777. https://doi.org/10.1644/07-mamm-a-269r1.1
Burkart, R., N. O. Bárbaro, R. O. Sánchez & D. A. Gómez. 1999. Ecorregiones de la Argentina. Administración de Parques Nacionales y Secretaría de Recursos Naturales y Desarrollo Sustentable. Presidencia de la Nación. Buenos Aires. https://doi.org/10.1017/s0731126500017625
Christoff, A. U., V. Fagundes, I. J. Sbalqueiro, M. S. Mattevi & Y. Yonenaga-Yassuda. 2000. Description of a new species of Akodon (Rodentia: Sigmodontinae) from southern Brazil. Journal of Mammalogy 81:838–851. https://doi.org/10.1093/jmammal/81.3.838
Costa, F. O., J. R. Dewaard, J. Boutillier, S. Ratnasingham, R. T. Dooh, M. Hajibabaei & P. D. Hebert. 2007. Biological identifications through DNA barcodes: the case of the Crustacea. Canadian Journal of Fisheries and Aquatic Sciences 64:272–295. https://doi.org/10.1139/f07-008
Darriba, D., G. L. Taboada, R. Doallo & D. Posada. 2012. jModelTest 2: more models, new heuristics and parallel computing. Nature Methods 9:772. https://doi.org/10.1038/nmeth.2109
Dayrat, B. 2005. Towards integrative taxonomy. Biological Journal of the Linnean Society 85:407–417. https://doi.org/10.1111/j.1095-8312.2005.00503.x
Díaz, M. M., & R. M. Barquez. 2007. The wild mammals of Jujuy Province, Argentina: systematics and distribution. The quintessential naturalist: honoring the life and legacy of Oliver P. Pearson (D. A. Kelt, E. P. Lessa, J. Salazar-Bravo, & J. L. Patton, eds.). University of California Publications in Zoology 134. https://doi.org/10.1525/california/9780520098596.003.0016
Díaz, M. M., R. M. Barquez, J. K. Braun & M. A. Mares. 1999. A new species of Akodon (Muridae: Sigmodontinae) from northwestern Argentina. Journal of Mammalogy 80:786–798. https://doi.org/10.2307/1383248
Díaz, M.M., J. K. Braun, M. A. Mares & R. M. Barquez. 2000. An update of the taxonomy, systematics, and distribution of the mammals of Salta province, Argentina. Occasional Papers of the Oklahoma Museum of Natural History, 10:1–52.
Di-Nizo, C. B. 2018. Diversification and species limits in two genera of the tribe Oryzomyini (Rodentia: Cricetidae: Sigmodontinae) revealed by combined molecular and cytogenetic approaches (Doctoral dissertation, Universidade de São Paulo). https://doi.org/10.11606/t.41.2018.tde-26062018-084004
Edgar, R. C. 2004. MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Research 32:1792–1797. https://doi.org/10.1093/nar/gkh340
Eldredge, N., & J. Cracraft. 1980. Phylogenetic patterns and the evolutionary process. New York: Columbia University Press.
Feijoo, M., G. D’Elía, U. F. Pardiñas & E. P. Lessa. 2010. Systematics of the southern Patagonian-Fueguian endemic Abrothrix lanosus (Rodentia: Sigmodontinae): phylogenetic position, karyotypic and morphological data. Mammalian Biology 75:122–137. https://doi.org/10.1016/j.mambio.2008.10.004
Ferro, L. I. 2010. Micromamíferos del noroeste Argentino: Gradientes altitudinales y la transición bosque puna monte. Tesis de Doctorado. Universidad Nacional de Tucumán, Tucumán, Argentina.
Ferro, L. I., & R. M. Barquez. 2014. Patrones de distribución de micromamíferos en gradientes altitudinales del noroeste Argentino. Revista Mexicana de Biodiversidad 85:472–490. https://doi.org/10.7550/rmb.38029
Ferro, L. I., J. J. Martínez & R. M. Barquez. 2010. A new species of Phyllotis (Rodentia, Cricetidae, Sigmodontinae) from Tucumán province, Argentina. Mammalian Biology 75:523–537. https://doi.org/10.1016/j.mambio.2009.09.005
Formoso, A., & P. Teta. 2019. Richness, endemism and conservation of sigmodontine rodents in Argentina. Mastozoología Neotropical 26:99–117. https://doi.org/10.31687/saremmn.19.26.1.0.17
Freeland, J. R. 2005. Molecular Ecology. John Wiley & Sons Ltd. Chichester, London, United Kingdom.
González Ittig, R. E., J. Salazar Bravo, R. M. Barquez & C. N. Gardenal. 2010. Phylogenetic relationships among species of the genus Oligoryzomys (Rodentia, Cricetidae) from Central and South America. Zoologica Scripta 39:511–526. https://doi.org/10.1111/j.1463-6409.2010.00446.x
González Ittig, R. E., P. C. Rivera, S. C. Levis, G. E. Calderón & C. N. Gardenal. 2014. The molecular phylogenetics of the genus Oligoryzomys (Rodentia: Cricetidae) clarifies rodent host–hantavirus associations. Zoological Journal of the Linnean Society 171: 457–474. https://doi.org/10.1111/zoj.12133
Hebert, P. D., A. Cywinska, S. L. Ball, & J. R. Dewaard. 2003a. Biological identifications through DNA barcodes. Proceedings of the Royal Society of London B 270:313–321. https://doi.org/10.1098/rspb.2002.2218
Hebert, P. D., S. Ratnasingham, & J. R. Dewaard. 2003b. Barcoding animal life: cytochrome c oxidase subunit 1 divergences among closely related species. Proceedings of the Royal Society of London B. 270:96–99. https://doi.org/10.1098/rsbl.2003.0025
Hebert, P. D., E. H. Penton, J. M. Burns, D. H. Janzen & W. Hallwachs. 2004. Ten species in one: DNA barcoding reveals cryptic species in the neotropical skipper butterfly Astraptes fulgerator. Proceedings of the National Academy of Sciences USA 101:14812–14817. https://doi.org/10.1073/pnas.0406166101
Hogg, I. D., & P. D. Hebert. 2004. Biological identification of springtails (Hexapoda: Collembola) from the Canadian Arctic, using mitochondrial DNA barcodes. Canadian Journal of Zoology 82:749–754. https://doi.org/10.1139/z04-041
Hurtado, N., & G. D’Elía. 2018. A new species of long-tailed mouse, genus Oligoryzomys Bangs, 1900 (Rodentia: Cricetidae), from the Bolivian Yungas. Zootaxa 4500:341–362. https://doi.org/10.11646/zootaxa.4500.3.3
Hurtado, N. & G. D’Elía. 2019. An assessment of species limits of the South American mouse genus Oligoryzomys (Rodentia, Cricetidae) using unilocus delimitation methods. Zoologica Scripta 48:557–570. https://doi.org/10.1111/zsc.12365
Ivanova, N.V., J.R. Dewaard & P.D.N. Hebert. 2006. An inexpensive, automation-friendly protocol for recovering high-quality DNA. Molecular Ecology Notes 6:998–1002. https://doi.org/10.1111/j.1471-8286.2006.01428.x
Ivanova, N.V., T. S. Zemlak, R. H. Hanner & P. D. N. Hebert. 2007. Universal primer cocktails for fish DNA barcoding. Molecular Ecology Notes 7:544–548. https://doi.org/10.1111/j.1471-8286.2007.01748.x
Jayat, J. P., G. D’Elía, P. E. Ortiz & P. Teta. 2016a. A new species of the rodent genus Necromys Ameghino (Cricetidae: Sigmodontinae: Akodontini) from the Chaco Serrano grasslands of northwestern Argentina. Journal of Mammalogy 97:1321–1335. https://doi.org/10.1093/jmammal/gyw103
Jayat, J. P., G. D’Elía, R. Torres, S. E. Pacheco, P. E. Ortiz, J. Salazar-Bravo & B. D. Patterson. 2017. Integration of morphological, ecological, and genetic evidence suggests that the genus Andinomys (Rodentia, Cricetidae) is monospecific. Journal of Mammalogy 98:1060–1077. https://doi.org/10.1093/jmammal/gyx076
Jayat, J. P., G. D’Elía, U. F. Pardiñas, M. D. Miotti, & P. E. Ortiz. 2008a. A new species of the genus Oxymycterus (Mammalia: Rodentia: Cricetidae) from the vanishing Yungas of Argentina. Zootaxa 1911:31–51. https://doi.org/10.11646/zootaxa.1911.1.2
Jayat, J. P., P. E. Ortiz, & M. D. Miotti. 2008b. Distribución de roedores sigmodontinos (Rodentia: Cricetidae) en pastizales de neblina del noroeste de Argentina. Acta Zoológica Mexicana 24:137–177. https://doi.org/10.21829/azm.2008.243913
Jayat, J. P., P. E. Ortiz, F. R. González, & G. D’Elía. 2016b. Taxonomy of the Phyllotis osilae species group in Argentina; the status of the “Rata de los nogales” (Phyllotis nogalaris Thomas, 1921; Rodentia: Cricetidae). Zootaxa 4083:397–417. https://doi.org/10.11646/zootaxa.4083.3.5
Jayat, J. P., P. E. Ortiz, G. D’Elía, J. Salazar-Bravo & B. D Patterson. 2020. Taxonomic status of the nominal forms assigned to Necromys lactens (Rodentia, Cricetidae) as revealed by molecular and morphometric evidence. Journal of Mammalogy 101:24–35. https://doi.org/10.1093/jmammal/gyz187
Jayat, J. P., P. E. Ortiz, J. Salazar-Bravo, U. F. Pardiñas & G. D’Elía. 2010. The Akodon boliviensis species group (Rodentia: Cricetidae: Sigmodontinae) in Argentina: species limits and distribution, with the description of a new entity. Zootaxa 2744. https://doi.org/10.11646/zootaxa.2409.1.1
Jayat, J. P., P. E. Ortiz, P. Teta, U. F. Pardiñas & G. D’Elía. 2006. Nuevas localidades argentinas para algunos roedores sigmodontinos (Rodentia: Cricetidae). Mastozoología Neotropical 13:51– 67. https://doi.org/10.1525/california/9780520098596.003.0015
Jayat, J. P., P.E. Ortiz, S. Pacheco & R. González. 2011. Distribution of sigmodontine rodents in Northwestern Argentina: main gaps in information and new records. Mammalia 75:53–68. https://doi.org/10.1515/mamm.2010.067
Jayat, J.P., P. E. Ortiz, A. A. Ojeda, A. Novillo, P. Teta, G. D’Elía & R.A. Ojeda. 2019. Quantitative morphological characters of the skull suggest that Akodon oenos (Rodentia, Cricetidae, Sigmodontinae) is not a junior synonym of A. spegazzinii, Mammalia, 84:299–313. https://doi.org/10.1515/mammalia-2019-0043
Jukes, T. H., & C. R. Cantor. 1969. Evolution of protein molecules. Mammalian Protein Metabolism Academic Press, New York, USA.
Kimura, M., 1980. A simple method for estimating evolutionary rates of base substitutions through comparative studies of nucleotide sequences. Journal of Molecuar Evolution. 16:111–120. https://doi.org/10.1007/bf01731581
Kumar, S., G. Stecher, M. Li, C. Knyaz & K. Tamura. 2018. MEGA X: Molecular Evolutionary Genetics Analysis across Computing Platforms. Molecular Biology and Evolution 35:1547–1549. https://doi.org/10.1093/molbev/msy096
Lanteri, A. A. 2007. Código de barras del ADN y sus posibles aplicaciones en el campo de la Entomología. Revista de la Sociedad Argentina Entomológica 66:15–25.
Mace, G. M. 2004. The role of taxonomy in species conservation. Philosophical Transactions of the Royal Society London B: Biological Sciences 359:711–719.
Maestri, R., & B. P. Patterson. 2016. Patterns of species richness and turnover for the South American rodent fauna. PloS One 11: e0151895. https://doi.org/10.1371/journal.pone.0151895
Malizia, L., S. Pacheco, C. Blundo, & A. D. Brown. 2012. Caracterización altitudinal, uso y conservación de las Yungas Subtropicales de Argentina. Ecosistemas 21:53–73.
Martín, E., M. M. Moreno Ruiz Holgado, G. M. Silenzi Usandivaras & M. Bonano. 2017. Comparación de métodos de extracción de ADN para el género Astylus (Coleoptera: Melyridae). Acta Zoológica Lilloana 61:55–64.
Martínez, J. J., & C. N. Gardenal. 2016. Phylogenetic relationships among species of the Neotropical genus Graomys (Rodentia: Cricetidae): contrasting patterns of skull morphometric variation and genetic divergence. Biological Journal of the Linnean Society 118:648–667. https://doi.org/10.1111/bij.12767
Martínez, J. J., L. I. Ferro, M. I. Mollerach & R. M. Barquez. 2012. The phylogenetic relationships of the Andean swamp rat genus Neotomys (Rodentia, Cricetidae, Sigmodontinae) based on mitochondrial and nuclear markers. Acta Theriologica 57:277– 287. https://doi.org/10.1007/s13364-011-0070-9
Massoia E. 1973. Descripción de Oryzomys fornesi, nueva especie y nuevos datos sobre algunas especies y subespecies argentinas del subgénero Oryzomys (Oligroyzomys) (Mammalia-Rodentia-Cricetidae). Revista de Investigaciones Agropecuarias INTA Serie I Biología y Producción Animal 10:21–37.
Moritz, C., & C. Cicero. 2004. DNA barcoding: promise and pitfalls. PLoS Biology 2:1529–1531.
Musser, G. G., & M. D. Carleton. 2005. Superfamily Muroidea. Mammal species of the world: a taxonomic and geographic reference (D.E. Wilson & D.M. Reeder, eds.). 3rd ed. Johns Hopkins University Press, Baltimore, Maryland. https://doi.org/10.1108/09504120610673024
Myers, P., & M. D. Carleton. 1981. The species of Oryzomys (Oligoryzomys) in Paraguay and the identity of Azara’s Rat sixième ou Rat à tarse noir". Miscellaneous Publications of the Museum of Zoology, University of Michigan 161:1–41.
Myers, P. 1989. A preliminary revision of the varius group of Akodon (A. dayi, dolores, molinae, neocenus, simulator, toba and varius). Advances in Neotropical Mammalogy (K. Redford & J. F. Eisenberg, eds.). Sandhill Crane Press, Gainesville, Florida. https://doi.org/10.1140/epjc/s10052-019-7118-4
Myers, P., J. L. Patton, & M. F. Smith. 1990. A review of the boliviensis group of Akodon (Muridae: Sigmodontinae), with emphasis on Peru and Bolivia. Miscelaneous Publications, Museum of Zoology, University of Michigan 177:1–104.
Parada, A., G. D’Elía, & R. E. Palma. 2015. The influence of ecological and geographical context in the radiation of Neotropical sigmodontine rodents. BMC Evolutionary Biology 15:172. https://doi.org/10.1186/s12862-015-0440-z
Parada, A., U. F. Pardiñas, J. Salazar-Bravo, G. D’Elía & R. E Palma. 2013. Dating an impressive Neotropical radiation: molecular time estimates for the Sigmodontinae (Rodentia) provide insights into its historical biogeography. Molecular Phylogenetics and Evolution 66:960–968. https://doi.org/10.1016/j.ympev.2012.12.001
Pardiñas, U. F. J., G. D’Elía, P. Teta, P. E. Ortiz, P. J. Jayat, & S. Cirignoli. 2006 Subfamilia Sigmodontini, Tribu Akodontini. Mamíferos de Argentina, sistemática y distribución (R. M. Barquez, M. M. Díaz & R. A. Ojeda, eds.). Tucumán, Argentina.
Pardiñas, U. F. J. et al. 2017. Family Cricetidae (true hamsters, voles, lemmings and New World rats and mice). Handbook of the mammals of the world, volume 7. Rodents II (D. E. Wilson, T. E. Lacher, & R. A. Mittermeier, eds.). Lynx Edicions. Barcelona, Spain. https://doi.org/10.5040/9781472926937.part-0042
Pardiñas, U. F. J., G. D’Elía, S. Cirignoli, & P. Suarez. 2005. A new species of Akodon (Rodentia, Cricetidae) from the Northern Campos grasslands of Argentina. Journal of Mammalogy 86:462– 474. https://doi.org/10.1644/1545-1542(2005)86[462:ansoar]2.0.c o;2
Pardiñas, U. F. J., P. Teta, D. Voglino, & F. J. Fernández. 2013. Enlarging rodent diversity in west-central Argentina: a new species of the genus Holochilus (Cricetidae, Sigmodontinae). Journal of Mammalogy 94:231–240. https://doi.org/10.1644/12-mamm-a-216
Pardiñas, U.F.J., P. Teta, D. Alvarado-Serrano, L. Geise, J. P. Jayat, P. E. Ortiz, P. R. Gonçalves & G. D’Elía. 2015. Genus Akodon Meyen, 1833. Mammals of South America, Volume 2 -Rodents (L. L. Patton, U. F. J. Pardiñas, & G. D’Elía, eds.). The University of Chicago Press, Chicago, IL. https://doi.org/10.7208/chicago/9780226169606.001.0001
Pardiñas, U.F.J., P. Teta, G. D’Elia, S. Cirignoli, & P. Ortiz. 2007. Resolution of some problematic type localities for Sigmodontine rodents (Cricetidae, Sigmodontinae). The quintessential naturalist: honoring the life and legacy of Oliver P. Pearson (D. A. Kelt, E. Lessa, J. A. Salazar-Bravo, & J. L. Patton, eds.). University of California Publications in Zoology. https://doi.org/10.1525/california/9780520098596.003.0015
Patterson, B. D. 2000. Patterns and trends in the discovery of new Neotropical mammals. Diversity and Distributions 6:145–151.
Patton, J. L., U. F. Pardiñas & G. D’Elía. (eds.). 2015. Mammals of South America, volume 2: rodents. The University of Chicago Press, Chicago, IL. https://doi.org/10.7208/chicago/9780226169606.001.0001
Percequillo, A. R., E. Hingst-Zaher, & C. R. Bonvicino. 2008. Systematic review of genus Cerradomys Weksler, Percequillo and Voss, 2006 (Rodentia: Cricetidae: Sigmodontinae: Oryzomyini), with description of two new species from eastern Brazil. American Museum Novitates 2008:1–46. https://doi.org/10.1206/495.1
Pinto, C. M., R. Ojala-Barbour, A. Brito, J., Menchaca, A. L. G. Carvalho, M. Weksler, G. Amato & T. E. Lee. 2018. Rodents of the eastern and western slopes of the Tropical Andes: phylogenetic and taxonomic insights using DNA barcodes. Therya 9:15–27. https://doi.org/10.12933/therya-18-430
Puillandre, N., A. Lambert., S. Brouillet. & G. Achaz. 2012. ABGD, Automatic Barcode Gap Discovery for primary species delimitation. Molecular Ecology 21:1864–1877. https://doi.org/10.1111/j.1365-294x.2011.05239.x
Rambaut, A., & A. J. Drummond. 2003. Tracer. Disponible en: http://beast.community/
Rivera, P. C., R. E. González-Ittig, A. Robainas Barcia, L. I. Trimarchi, S. Levis, G. E. Calderón & C. N. Gardenal. 2018. Molecular phylogenetics and environmental niche modeling reveal a cryptic species in the Oligoryzomys flavescens complex (Rodentia, Cricetidae). Journal of Mammalogy 99:363–376. https://doi.org/10.1093/jmammal/gyx186
R Core Team. 2020. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org/
Rocha, R. G., E. Ferreira, B. Costa, I. Martins, Y. L. Leite, L. P. Costa & C. Fonseca. 2011. Small mammals of the mid-Araguaia River in central Brazil, with the description of a new species of climbing rat. Zootaxa 2789:1–34. https://doi.org/10.11646/zootaxa.2789.1.1
Ronquist, F., M. Teslenko, P. Van Der Mark, D. L. Ayres, A. Darling, S. Hohna, & J. P. Huelsenbeck. 2012. MrBayes 3.2: efficient Bayesian phylogenetic inference and model choice across a large model space. Systematic Biology 61:539–542. https://doi.org/10.1093/sysbio/sys029
Rozas, J., A. Ferrer-Mata, J. C. Sánchez-Delbarrio, S. Guirao-Rico, P. Librado, S.E. Ramos-Onsins & A. Sánchez-Gracia. 2017. DnaSP 6: DNA sequence polymorphism analysis of large data sets. Molecular Biology and Evolution 34:3299–3302. https://doi.org/10.1093/molbev/msx248
Rubinoff, D. 2006. Utility of mitochondrial DNA barcodes in species conservation. Conservation Biology 20:1026–1033. https://doi.org/10.1111/j.1523-1739.2006.00372.x
Salazar-Bravo, J., & J. P. Jayat. 2015. Cricetidae. Andinomys. En: Patton JL, Pardiñas UFJ, D’Elía G (eds) Mammals of South America. Vol. 2. Rodents. University of Chicago Press, Chicago.
Sites, J. W., & J. C. Marshall. 2004. Operational criteria for delimiting species. Annual Review of Ecology, Evolution, and Systematics 35:199–227. https://doi.org/10.1146/annurev.ecolsys.35.112202.130128
Stoeckle, M. 2003. Taxonomy, DNA, and the Bar Code of Life. BioScience 53:796–797. https://doi.org/10.1641/0006-3568(2003)053[0796:tdatbc]2.0.co;2
Teta, P. V., A. M. Abba, G. H. Cassini, D. A. Flores, C. A. Galliari, S. Lucero & M. A. Ramirez. 2018. Lista revisada de los mamíferos de Argentina. Mastozoología Neotropical 25:163–198. https://doi.org/10.31687/saremmn.18.25.1.0.15
Teta, P., G. D’Elía, U. F. Pardiñas, J. P. Jayat & P. E. Ortiz. 2011. Phylogenetic position and morphology of Abrothrix illutea Thomas, 1925, with comments on the incongruence between gene trees of Abrothrix (Rodentia, Cricetidae) and their implications for the delimitation of the genus. Zoosystematics and Evolution 87:227–241. https://doi.org/10.1002/zoos.201100005
Teta, P., J. P. Jayat, P. E. Ortiz & G. D’Elía. 2013. The taxonomic status of Oligoryzomys brendae Massoia, 1998 (Rodentia, Cricetidae), with comments on the availability of this name. Zootaxa 3641:433–447. https://doi.org/10.11646/zootaxa.3641.4.9
Thomas, O. 1918. On small mammals from Salta and Jujuy collected by Mr. E. Budin. Annals and Magazine of Natural History 1:186– 193. https://doi.org/10.1080/00222931808562299
Thomas O. 1921. On a further collection of mammals from Jujuy obtained by Sr. Budin. Annals and Magazine of Natural History 8:608-617. https://doi.org/10.1080/00222932108632625
Ward, R. D., T. S. Zemlak, B. H. Innes, P. R. Last & P. D. Hebert. 2005. DNA barcoding Australia’s fish species. Philosophical Transactions of the Royal Society B 360:1847–1857. https://doi.org/10.1098/rstb.2005.1716
Wheeler, Q. D. 1995. Systematics and biodiversity. BioScience 45:21–28.
Wheeler, Q. D. 2004. Taxonomic triage and the poverty of phylogeny. Philosophical transactions of the Royal Society of London. Series B, Biological sciences 359:571-583. https://doi.org/10.1098/rstb.2003.1452
Wickham, H. 2016. ggplot2: elegant graphics for data analysis. Springer-Verlag New York. ISBN 978-3-319-24277-4, https://ggplot2.tidyverse.org.
Yepes, J. 1935. Consideraciones sobre el género Andinomys (Cricetinae) y descripción de una forma nueva. Anales del Museo Nacional Buenos Aires 38:333–348.
Zhang, C., B. Rannala, & Z. H. Yang. 2014. Bayesian Species Delimitation Can Be Robust to Guide-Tree Inference Errors. Systematic Biology 63:993–1004. https://doi.org/10.1093/sysbio/syu052
Zhang, J., P. Kapli, P. Pavlidis & A. Stamatakis. 2013. A general species delimitation method with applications to phylogenetic placements. Bioinformatics 29:2869–2876. https://doi.org/10.1093/bioinformatics/btt499
APÉNDICE 1
Listado de especímenes analizados en este estudio. Acrónimos empleados: CML = Colección Mamíferos Lillo (Tucumán, Argentina); MACN-ma = Colección Nacional de Mastozoología, Museo Argentino de Ciencias Naturales “Bernardino Rivadavia” (Buenos Aires, Argentina); LT-RMB = Catálogo del proyecto de localidades tipo de Rubén Marcos Barquez; LIF = catálogo de campo de Luis Ignacio Ferro; JJM = catálogo de Juan José Martínez. Las localidades de procedencia se identifican con el número que se emplea en la Fig. 1. Números de acceso de GenBank entre [corchetes].
Akodon albiventer Thomas, 1897: 10) Jujuy, Humahuaca, Rincón de Zenta, 6 km al W del Abra de Zenta, sobre R.P. Nº 73. 4053 msnm, 23.161984º S; 65.081467º W (CML 11082; CML 11083) [MW009981, MW009982].
Akodon azarae (Fischer, 1829): 44) Chaco, San Fernando, 18 km al N del Pte. Gral. Belgrano camino a Isla del Cerrito, 27.43165° S; 58.845457° W (CML 11170) [MW009925].
Akodon boliviensis Meyen, 1833: 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés, 2057 msnm, 23.118908° S; 64.898032° W (CML 11105) [MW009943]. 10) Jujuy, Humahuaca, Rincón de Zenta, 6 km al W de Abrade Zenta, sobre R.P. Nº 73, 4053 msnm, 23.161984° S;65.081467° W (CML 11087; CML 11088) [MW009941,MW009942]. 13) Jujuy, Tilcara, Sierra de Tilcara, El Hueco, 21 km SE de Tilcara, 3100 msnm, 23.70764° S; 65.245586°W (CML 11093; CML 11094; CML 11095; CML 11096)[MW009944, MW009946, MW009945, MW009947].
Akodon budini (Thomas, 1918): 5) Salta, Orán, Cuesta Chica, 35 km O de El Oculto, 4 km E de San Andrés, 23.072365° S; 64.836874° W (CML 11117) [MW009979] (CML 11116) [MW009948]. 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés, 2057 msnm, 23.118907° S; 64.898032° W (CML 11118) [MW009980]. 14) Jujuy, Tilcara, Higuerilla, 23.729196° S; 65.178898° W (CML 12074; CML 12076) [MW009978, MW009976]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26,2 km al SE de Tilcara, 2500 msnm, 23.746714° S; 65.213489° W (CML 11106) [MW009977].
Akodon caenosus Thomas, 1918: 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés. 2057 msnm, 23.118907° S; 64898032° W (CML 11120; CML 11122; CML 11123) [MW009934, MW009933, MW009937]. 14) Jujuy, Tilcara, Higuerilla, -23.729196° S; 65.178898° W (CML 12084; CML 12085) [MW009936, MW009938]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26.2 km al SE de Tilcara. 2500 msnm, 23.746714° S; 65.213489° W (CML 9146; CML 11146) [MW009940, MW009939]. 37) Tucumán, Tafí Viejo, Río Grande, 5 km al S de El Siambón, 920 msnm, 26.768333° S, 65.468333° W (CML 9189) [MW009932]. 47) Catamarca, Paclín, El Durazno, 8 km al S de cruce de rutas 38 nueva y vieja, por ruta vieja. 762 msnm, 28.101373; 65.598771° W (CML 12187) [MW009935].
Akodon fumeus Thomas, 1902: 5) Salta, Orán, Cuesta Chica, 35 km O de El Oculto, 4 km E de San Andrés, 23.072365° S; 64.836874° W (CML 11134; CML 11135; CML 11136) [MW009928, MW009929, MW009927]. 6) Salta, Orán, Río Colorado, 25 km O de El Oculto (camino a San Andrés), 1008 msnm, 23.094257° S; 64.742311° W (CML 11144) [MW009926].
Akodon polopi Jayat, Ortiz, Salazar-Bravo, Pardiñas y D’Elía, 2010: 49) Córdoba, Punilla, Pampa de Achala, entre La posta y Los Gigantes, 2297 msnm, 31.441111° S; 64.826388° W (JJM005) [MW009931]. 50) Córdoba, Pampa de Achala, entre La posta y Los Gigantes, 2297 msnm 31.441666° S; 64.833333° W (JJM002) [MW009930].
Akodon simulator Thomas, 1916: 2) Salta, Orán, Estación de Aforo .Aguas Blancas", 2 km al N de Aguas Blancas, sobre ruta 52, 22.724073° S; 64.363847° W (CML 11157; CML 11158) [MW009985, MW009983]. 3) Salta, Orán, Quebrada de Vides, Puesto Viejo, 4 km SE de Angosto de Río Pescado, Parque Provincial Laguna de Pintascayo, 22.743886° S; 64.520953° W (CML 11159; CML 11161) [MW009998, MW010004]. 4) Salta, Orán, 43.7 km al NW del cruce de las rutas 50 y 18, camino a Isla de Cañas, sobre ruta 18, 23.002667° S; 64.552683° W (CML 9074) [MW010001]. 7) Salta, Orán, El Oculto, ruta prov. N 18 km 25 sobre Río Blanco (camino a San Andrés), 23.106169° S; 64.540388° W (CML 11149; CML 11150; CML 11151; CML 11152) [MW009986, MW009987, MW009984, MW010003]. 15) Jujuy, Ledesma, Peña Alta, 18 km O del cruce Río Ledesma, ruta 34, 23.73615° S; 64.756677° W (CML 9030) [MW009997]. 20) Salta, Metán, 15 km al N de Metán por ruta 9 y 5 km al W, 986 msnm, 25.3981° S; 64.987533° W (CML 12194) [MW010002]. 23) Salta, Candelaria, Rio Los Sauces, 12 Km NO de El Jardín, ruta 6 Km 110. 26.076° S; 65.483° W (LIF 192) [MW009868]. 26) Tucumán, Trancas, Tapia, cruce de ruta 9 y río Tapia. 612 msnm, 26.474321° S; 65.315061° W (CML 11169; CML 11168) [MW009996, MW010000]. 29) Tucumán, Tafí del Valle, El Remate, 8 km E de Amaicha. 2257 msnm, 26.638839° S; 65.859769° W (CML 11162) [MW009989]. 30) Tucumán, Tafí Viejo, Pie de la cuesta a Chasquivil, 5 km río arriba de la Hoyada sobre río Hoyada. 1700 msnm, 26.656427° S; 65.560341° W (CML 11164) [MW009995]. 38) Tucumán, Lules, Villa Nougués, 26.865739° S; 65.349155° W (CML 12090; CML 12091; CML 12092; CML 12093; CML 12094) [MW009990, MW009994, MW009992, MW009993, MW009991]. 48) Catamarca, Capayán, Otro Cerro, Rancho de los Crisho, 2160 msnm ± 9 m, 28.692863° S; 66.261849° W (CML 12088; CML 12089) [MW009988, MW009999].
Akodon spegazzinii Thomas, 1897: 27) Tucumán, Trancas, Cruce entre ruta 9 y arroyo India Muerta. 651 msnm, 26. 474321° S; 65. 315061° W (CML 11471) [MW009955]. 28) Tucumán, Tafí del Valle, Los Zazos, 4 km E de Amaicha.2105 msnm, 26.605587° S; 65.892333° W (CML 11365;CML 11366) [MW009952, MW009953]. 30) Tucumán, Tafí Viejo, Pie de la cuesta a Chasquivil, 5 Km río arriba de la Hoyada, 1700 msnm, 26.656427° S; 65.560341°W (CML 7282) [MW009949]. 32) Tucumán, Tafí Viejo, Ciénaga Grande, San José de Chasquivil, 26.685762° S;65.658555° W (CML 11371; CML 11375) [MW009964, MW009963]. 33) Tucumán, Tafí Viejo, La Sala de SanJosé de Chasquivil, 26.688484° S; 65.612299° W (CML4032; CML 11435) [MW009951, MW009961]. 34) Tucumán, Tafí Viejo, Las Agüitas, Parque Biológico Sierra de SanJavier. 1702 msnm, 26.695998° S; 65.339757° W (CML11828; CML 11829; CML 11839; CML 11847) [MW009969,MW009954, MW009966, MW009968]. 35) Tucumán, TafíViejo, Piedra Blanca, San José de Chaquivil, 26.709058° S;65.646161° W (CML 7276) [MW009950]. 37) Tucumán, Tafí Viejo, Río Grande, 5 km al S de El Siambón.920 msnm, 26.768333° S; 65.468333° W (CML 9188)[MW009965]. 40) Tucumán, Chicligasta, Parque Nacional Campo de Los Alisos, El Kenqueo. 3200 msnm, 27.172251°S; 65.979167° W (CML 11191) [MW009959]. 42) Tucumán, Chicligasta, Parque Nacional Campo de los Alisos, Puesto La Mesada 1679 msnm, -27,214911; -65,930088 (CML11288) [MW009962]. 43) Tucumán, Chicligasta, Santa Rosa, Parque Nacional Campo de los Alisos, 15 km Ode Alpachiri, 27.285066° S; 65.872948° W (CML 11330)[MW009960]. 45) Catamarca, Andalgalá, Alumbrera, 4km S de El Alamito, Las Estancias, 1663 msnm, 27.489907°S; 66.025433° W (CML 11178; CML 11179) [MW009957,MW009958].48) Catamarca, Capayán, Otro Cerro, Rancho de los Crisho, 2160 m ± 9 m, 28.692863° S; 66.261849°W (CML 12061; CML 12095; CML 12096) [MW009970,MW009967, MW009956].
Akodon toba Thomas, 1921: 19) Formosa, Patiño, Cruce entre ruta 95 y riacho Pilagá, 7 km N de cruce de rutas 81 y 95. 25.221153° S; 59.718669° W (CML 11171; CML 11172; CML 11173; CML 11472) [MW009975, MW009974,MW009972, MW009973]. 20) Formosa, Patiño, EstanciaPoguazú, 6 km E desde ruta 95, a 8 km N de cruce entrerutas 81 y 95, 25.239444° S; 59.658888° W (CML 11473)[MW009971].
Andinomys edax Thomas, 1902: 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés. 2057 msnm, 23.118907° S; 64.898032° W (CML 11801) [MW009902]. 9) Salta, Orán, Abra de Volcán, 38, 8 km al ENE de Humahuaca.3150 msnm, 23.145583° S; 64.975389° W (CML 11800)[MW009901]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26.2 km al SE de Tilcara. 2500 msnm, 23.746714°S; 65.213489° W (CML 8464) [MW009900]. 32) Tucumán, Tafí Viejo, Ciénaga Grande, San José de Chasquivil,26.685762° S; 65.658555°W(CML 11810) [MW009904]. 39)Tucumán, Monteros, Reserva Provincial Los Sosa. Ruta307 km 35, 27.031826° S; 65.665079° W. (CML 11806; CML11807; CML 11808) [MW009903, MW009905, MW009906].41) Tucumán, Chicligasta, Parque Nacional Campo de los Alisos, Puesto Los Nacimientos (La Cascada) 2700 msnm, 27.175042° S; 65.969353° W (CML 11805) [MW009907].
Auliscomys sublimis (Thomas, 1900): 12) Jujuy, Tilcara, Sierra de Tilcara, Toro Arita, 12 km ESE de Maimará, 14 km ESE de Tilcara, 4092 msnm, 23.665433° S; 65.298617° W (CML 8477; CML 12132) [MW010020, MW010019].
Calomys boliviae (Thomas, 1901): 7) Salta, Orán, El Oculto, RP 18 km 25 sobre Río Blanco (camino a San Andrés), 23.106169° S; 64.540388° W (CML 11614) [MW009892]. 23) Salta, Candelaria, Río Los Sauces, 12 km NW del jardín, ruta 6 km 110. 993 msnm, 26.076° S; 65.483° W (CML 11629; LIF 190) [MW009891, MW009893]. 26) Tucumán, Trancas, Cruce entre ruta 9 y arroyo India Muerta. 651 msnm,26.474321° S; 65.315061° W (CML 11616) [MW009895].37) Tucumán, Tafí Viejo, Río Grande, 5 km al S de El Siambón. 920 msnm, 26.768333° S; 65.468333° W (CML9254) [MW009894].
Calomys callosus (Rengger, 1830): 19) Formosa, Patiño, Cruce entre ruta 95 y riacho Pilagá a 7 km al N del cruce entre ruta 81 y 95, 25.221153° S; 59.718669° W (CML 9257; CML 9312) [MW009896, MW009897]. 24) Formosa, Pirané, El Colorado, Estación Experimental El Colorado INTA, 26.30888° S; 59.37222° W (CML 12136) [MW009898].
Calomys lepidus (Thomas, 1884): 31) Tucumán, Tafí Viejo, Laguna de Huaca Huasi, Cumbres Calchaquíes. 4210 msnm, 26.657879° S; 65.741977° W (CML 7501) [MW009889].
Calomys musculinus (Thomas, 1913): 24) Formosa, Pirané, El Colorado, Estación Experimental El Colorado INTA, 26.30888° S; 59.37222° W (CML 12137) [MW009890].
Eligmodontia puerulus (Philippi, 1896): 11) Jujuy, Susques, Bordo de Ecatón, ruta 52 km 165, salar de Olaroz. 3953 msnm, 23.530705° S; 66.639841° W (CML 11631; CML 11632) [MW009887, MW009888].
Euryoryzomys legatus (Thomas, 1925): 6) Salta, Orán, Río Colorado, 25 km O de El Oculto (camino a San Andrés) 1008 msnm, 23.094257° S; 64.742311° W (CML 11521) [MW009886]. 14) Jujuy, Tilcara, Higuerilla, 23.729196°S; 65.178898° W (LT-RMB 113) [MW009885].
Holochilus chacarius Thomas, 1906: 20) Formosa, Pirané, Estancia Poguazú, 8 KM N de cruce de rutas 81-95 y 6 Km E de R 95, 25.221153° S; 59.718669° W (LIF 120) [MW009859]. 24) Formosa, Pirané, El Colorado, Estación Experimental .El Colorado ÏNTA, 26.30888° S; 59.37222° W(LT- RMB 96; LT- RMB 97) [MW009860, MW009861].
Necromys lactens (Thomas, 1918): 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés. 2057 msnm, 23.118907° S; 64.898032° W (CML 11485) [MW009912]. 9) Salta, Orán, Abra de Volcán, 38, 8 km al ENE de Humahuaca.3150 msnm, 23.145583 ° S; 64.975389 ° W (CML 11484)[MW009913]. 32) Tucumán, Tafí Viejo, Ciénaga Grande, San José de Chasquivil, 2800 m, 26.685762° S; 65.658555°W (CML 8453) [MW009914]. 40) Tucumán, Chicligasta, Parque Nacional Campo de Los Alisos, El Kerqueo,3 200 msnm, 27.172251° S; 65.979167° W (CML 8454) [MW009915].
Necromys lasiurus (Lund, 1840): 21) Formosa, Pilcomayo, Ceibo 13, 8, 5 km SO de Naineck, 25.221153° S; 59.718669° W (CML 12067; CML 12105) [MW009911, MW009908]. 24) Formosa, Pirané, El Colorado, Estación Experimental INTA El Colorado, 26.30888° S; 59.37222° W (CML 12068) [MW009910]. 25) Formosa, Pirané, El Colorado, Estación Experimental El Colorado INTA, 26.309212° S; 59.375352° W (CML 12100) [MW009909].
Neotomys ebriosus Thomas, 1894: 12) Jujuy, Tilcara, Sierra de Tilcara, Toro Arita, 12 km ESE de Maimará, 14 km ESE de Tilcara. 4092 msnm, 23.665433° S; 65.298617° W (CML 7680) [MW009899].
Oligoryzomys brendae Massoia, 1998: 14) Jujuy, Tilcara, Higuerilla, 23.729196° S; 65.178898° W (CML 12116) [MW009864]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26, 2 km al SE de Tilcara. 2500 msnm, 23.746714° S; 65.213489° W (CML 11508; CML 11509) [MW009862, MW009863]. 17) Jujuy, Gral. Manuel Belgrano, León, 1 km río arriba, sobre Río León. 1708 m, 24.027383° S; 65.448517° W (CML 12112) [MW009865]. 26) Tucumán, Trancas, Tapia, cruce de ruta 9 y río Tapia. 612 msnm, 26.597672° S; 65,.267879° W (CML 11558) [MW009869]. 33) Tucumán, Tafí Viejo, La Sala de San José de Chasquivil. 2152 msnm,26.688484° S; 65.612299° W (CML 11597) [MW009867]. 38) Tucumán, Tafí Viejo, Pie de la cuesta a Chaquivil, 5 km rio arriba de la Hoyada, sobre río Hoyada, 1700msnm, 26.865739° S; 65.349155°W (LIF 146; CML 12121) [MW009870, MW009866].
Oligoryzomys chacoensis (Myers y Carleton, 1981): 1) Salta, Gral. José de San Martín, Virgen de la Peña. Km al W de ruta 34, al N de Tartagal, 22.420049° S; 63.794685° W (CML 12123) [MW009880]. 7) Salta, Orán, El Oculto, ruta provincial nº18 Km 25 sobre rio blanco (camino a San Andrés), 23.106169° S; 64.540388° W (CML 11564) [MW009883]. 19) Formosa, Patiño, Cruce entre ruta 95 y riacho Pilagá, 7 km N de cruce de rutas 81 y 95, 25.221153° S; 59.718669° W (CML 11561) [MW009881]. 21) Formosa, Pilcomayo, Ceibo 13, 8, 5 km SO de Naineck, 25.24371° S; 58.2267° W (CML 12111) [MW009882]. 24) Formosa, Pirané, El Colorado, Camping Municipal, cruce del Río Bermejo y ruta Nac. 90, 26.30888° S; 59.37222° W (CML 11562) [MW009884].
Oligoryzomys flavescens (Waterhouse, 1837): 24) Formosa, Pirané, El Colorado, Estación Experimental El Colorado INTA, 26.30888° S; 59.37222° W (CML 12129) [MW009871]. 33) Tucumán, Tafí Viejo, La Sala de San José de Chasquivil. 2152 m, 26.688483° S; 65.6123° W (CML 11578) [MW009874]. 41) Tucumán, Chicligasta, Parque Nacional Campo de los Alisos, Puesto Los Nascimientos (La Cascada). 2700 msnm, 27.175041° S; 65.969352° W (CML 11575; CML 11576) [MW009876, MW009875]. 42) Tucumán, Chicligasta, Parque Nacional Campo de los Alisos, Puesto La Mesada. 1679 msnm, 27.214911° S; 65.930088° W (CML 11546) [MW009872]. 43) Tucumán, Chicligasta, Santa Rosa, Parque Nacional Campo de los Alisos, 15 km O de Alpachiri, 27.285066° S; 65.872948° W (LIF 452) [MW009873].
Oligoryzomys nigripes (Olfers, 1818): 21) Formosa, Pilcomayo, Ceibo 13, 8, 5 km SO de Naineck, 25.243716° S; 58.2267° W (CML 12110) [MW009877]. 44) Chaco, San Fernando, 18 km al N del Pte. Gral. Belgrano camino a Isla del Cerrito, 27.43165° S; 58.845457° W (CML 11589;CML 11590) [MW009878, MW009879].
Oxymycterus paramensis Thomas, 1902: 5) Salta, Orán, Cuesta Chica, 35 km O de El Oculto, 4 km E de San Andrés, 23.072365° S; 64. 836874° W (CML 11497; CML 11498) [MW009922, MW009921]. 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés, 2057 msnm, 23.118907° S; 64.898032°W (CML 8467; CML 11501) [MW009923, MW009920]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26, 2 kmal SE de Tilcara, 2500 msnm, 23.746714° S; 65.213489°W (CML 11493; CML 11495; CML 11496) [MW009918,MW009919, MW009924].
Oxymycterus rufus (Fischer, 1814): 46) Corrientes, Capital, Estación biológica Corrientes, San Cayetano, 27.553110° S; 58.679494° W (MACN-maTC 242) [MW009916].
Oxymycterus wayku Jayat, D’Elía, Pardiñas, Miotti y Ortiz, 2008: 33) Tucumán, Tafí Viejo, La Sala de San José de Chasquivil. 2152 msnm,26.688484° S; 65.612299° W (CML 11504) [MW009917].
Phyllotis tucumanus (Thomas, 1912): 8) Salta, Orán, El Queñoal, 5 km al O de San Andrés. 2057 msnm, 23.118907° S; 64.898032° W (CML 11645; CML 11659) [MW010013, MW010014]. 9) Salta, Orán, Abra de Volcán, 38, 8 km al ENE de Humahuaca. 3150 msnm, 23.145583 ° S; 64.975389° W (CML 11643; CML 12310) [MW010012, MW010015].13) Jujuy, Tilcara, Sierra de Tilcara, El Hueco, 21 km SE de Tilcara, 3100 msnm, 23.70764° S; 65.245586° W(CML 12309) [MW010017]. 16) Jujuy, Tilcara, Sierra de Tilcara, El Matadero, 26, 2 km al SE de Tilcara. 2500 msnm,23.746714° S; 65.213489°W(CML 11639) [MW010016]. 30)Tucumán, Tafí Viejo, Pie de la Cuesta de Chasquivil, 5 km río arriba de la Hoyada sobre río Hoyada, 26.656427° S;65.560341°W(CML 8458) [MW010010]. 32) Tucumán, TafíViejo, Ciénaga Grande, San José de Chasquivil, 26.685762°S; 65.658555° W (CML 11693) [MW010008]. 36) Tucumán, Tafí del Valle, Rancho del Hombre Solo, El Infiernillo, 2800m, 26.741153° S; 65.769827° W (CML 8380) [MW010011].40) Tucumán, Chicligasta, Parque Nacional Campo de Los Alisos, El Kerqueo. 3200 m, 27.172251° S; 65.979167° W(CML 8465) [MW010009]. 48) Catamarca, Capayán, Otro Cerro, Rancho de los Crisho. 2160 msnm ± 9 m, 28.692863°S; 66.261849° W (CML 12141; CML 12142; CML 12145)[MW010005, MW010006, MW010007].
Tapecomys primus Anderson y Yates, 2000: 18) Jujuy, Doctor Manuel Belgrano, 7 km al N de Las Capillas, sobre ruta provincial 20. 1198 msnm, 24.075° S; 65.143333° W (CML 7080) [MW010018].
Grupo externo
Rheomys thomasi Dickey, 1928: El Salvador: Ahuachapán, El Imposible, San Francisco Menéndez, 13.85° N; 90.00° W [JF492335].
Neusticomys sp. : Ecuador: Orellana, Onkone Gare, 38 Km S de Pompeya Sur, 0.657° S; 76.454° W [JF491613; JF491614].
Sigmodon alstoni (Thomas, 1881): Suriname, Sipaliwini, Iconja Landing, Sipaliwini, River, savannah, 1.994° N; 56.092° W [HQ919654].
Sigmodon hispidus (Burmeister, 1854): México, Campeche, 27.5 Km S de Constitución, 27.5 Km S, 70 Km E de Escárcega, 18.383° N; 90.117° W [JF492688].
Información adicional
Editor asociado: U. F. J. Pardiñas & C. A. Galliari
Citar como: Andrade, L. D., J. J. Martínez, R. M. Barquez, E. Martín & I. Ferro. 2021. Código de barras de ADN para la delimitación de especies en roedores sigmodontinos (Cricetidae) del norte argentino, con especial énfasis en aquellas de las Yungas. Mastozoología Neotropical, 28(1):e0541. https://doi.org/10.31687/saremMN.21.28.1.0.22