ARTÍCULO
Recepción: 14 Diciembre 2020
Aprobación: 03 Abril 2021
Resumen: Colombia es uno de los países con mayor riqueza de primates en el mundo. Sin embargo, el número e identidad de las especies ha sido un tema debatido a lo largo de los años. Las primeras descripciones de primates colombianos se remontan a expediciones posteriores a la conquista española. A esto se sumaron las primeras revisiones taxonómicas de géneros y especies en la primera mitad del siglo XX, a partir de literatura y especímenes de museo. Con el objetivo de unificar la información taxonómica de los primates no humanos del país, realizamos una revisión de literatura enfocada en aquellos aportes que han llevado a cambios en los arreglos taxonómicos y nomenclaturales de los últimos 20 años. Además, reunimos información sobre los taxa con localidad tipo en Colombia a partir de revisiones de las descripciones originales. En total, reconocemos la presencia de 36 especies y 17 subespecies, donde los mayores cambios se han dado en los géneros Cebus y Aotus. Reportamos ocho especies endémicas, y 25 taxa con localidades tipo en el país. Consideramos que, de acuerdo con revisiones recientes, las poblaciones del género Cacajao en el país corresponden a C. ouakary (Spix 1823) y, ante la ausencia de evidencia molecular, barreras geográficas y diferenciación fenotípica, indicamos a Pithecia milleri como subpespecie de P. hirsuta (Spix 1823), y a Cheracebus lucifer y C. medemi como subespecies de C. torquatus (Hoffmannsegg, 1807. Finalmente, proponemos el uso de subgéneros para representar las relaciones evolutivas en Saguinus .Leontocebus) y Callicebus .Plecturocebus, Cheracebus).
Palabras clave: Endémica, primates neotropicales, primates no humanos, Suramérica, taxonomía.
Abstract: Colombia is among the countries with the greatest richness of primates in the world. However, the number and identity of species has been a debated topic over the years. The first descriptions of Colombian primates date back to expeditions after the Spanish conquest. Later, the first taxonomic reviews of genera and species were published in the first half of the 20th century, based on literature and museum specimens. To unify the taxonomic information of non-human primates of the country, we conducted a literature review focused on those contributions that have led to changes in the taxonomic and nomenclatural arrangements of the last 20 years. Also, we collected information on taxa with type locality in Colombia from revisions of the original descriptions. We recognize the presence of 36 species, and 17 subspecies, where the greatest changes have occurred in the genera Cebus and Aotus. We report 8 endemic species and 25 taxa with type localities in the country. Furthermore, we consider that, according to recent reviews, the populations of the genus Cacajao in the country correspond to C. ouakary (Spix 1823) and, in the absence of molecular evidence, geographic barriers, and phenotypic differentiation, we indicate Pithecia milleri as a subspecies of P. hirsuta (Spix, 1823), and Cheracebus lucifer and C. medemi as subspecies of C. torquatus (Hoffmannsegg, 1807). Finally, we propose the use of subgenera to represent the evolutionary relationships in Saguinus .Leontocebus) and Callicebus .Plecturocebus, Cheracebus).
Keywords: Endemic, Neotropical primates, non-human primates, South America, taxonomy.
INTRODUCCIÓN
Las primeras documentaciones y descripciones de los primates que ocupan el territorio colombiano corresponden a crónicas posteriores a la conquista española (Hernández-Camacho & Cooper 1976). Desde las primeras descripciones de Linneo en 1758, y con las realizadas por von Hoffmannsegg, von Humboldt, Etienne Geoffroy-St. Hilaire y von Spix, en 1823 se registraban 16 de las 38 especies reconocidas actualmente para Colombia (Hernández-Camacho & Cooper 1976; Ramírez-Chaves et al. 2016). Más adelante, a finales del siglo XIX y principios del siglo XX se comenzaron a establecer algunas de las colecciones biológicas modernas a partir de expediciones que tuvieron como referentes tanto a naturalistas británicos y norteamericanos, como a los hermanos lasallistas quienes documentaron extensamente la fauna colombiana, incluyendo a los primates (Defler 2010). Desde la década de 1940, P. Hershkovitz, a partir de numerosas recolectas en diversas expediciones, realizó descripciones de nuevas especies y subespecies, así como extensas revisiones de diferentes grupos aportando a la taxonomía y sistemática de los primates colombianos (Hershkovitz 1949, 1955, 1977, 1979, 1982, 1983, 1984, 1987a,b, 1988, 1990; Patterson 1987). Posteriormente, durante la segunda mitad del siglo XX, y la primera década del siglo XXI, los principales aportes taxonómicos en el país estuvieron liderados por Jorge Hernández-Camacho y T. R. Defler apoyados, en parte, por material depositado en colecciones biológicas nacionales como las del INDERENA (que pasaron al Instituto Alexander von Humboldt), el Instituto de Ciencias Naturales de la Universidad Nacional de Colombia, el Museo de Historia Natural de la Universidad del Valle y colecciones internacionales, incluyendo principalmente las del Field Museum of Chicago (Defler 2010; Mantilla-Meluk et al. 2014).
Los estudios relacionados con taxonomía de primates en Colombia han sido menos frecuentes en comparación con temas como ecología y anatomía, y con otros países del neotrópico como Brasil (Hernández-Camacho & Cooper 1976; Defler & Hernández-Camacho 2002; Defler 2003, 2010; Stevenson et al. 2010; Guzmán-Caro et al. 2018), a pesar de ser uno de los países con mayor riqueza de primates. En Colombia no existe un consenso en el número estimado de especies, lo que se ha derivado de complejos problemas taxonómicos (en grupos como Aotus, Callicebus, Cebus y Leontocebus) y la aceptación, o no, de diferentes hipótesis dependiendo del punto de vista de los autores (Defler 2010). Históricamente han existido diversas propuestas en cuanto al número de especies de primates en Colombia, las cuales van desde 27 hasta 40 especies, y un número variable de taxa endémicos, algunos con localidades tipo en el país (Groves 2006; Defler 2010; Guzmán-Caro et al. 2018). En el momento, la última propuesta sugiere la presencia de 38 especies y 14 subespecies, de las cuales nueve son endémicas (Anónimo 2020a,b).
La historia taxonómica de los primates colombianos está marcada por la antigüedad de las primeras descripciones, los aportes de diversos investigadores y recolectas durante los siglos XIX a XXI. La información histórica y actual permanece aislada y existen confusiones causadas por diferencias en el número e identidad de las especies en los listados nacionales. El objetivo de la presente contribución fue reunir la información taxonómica de los primates no humanos del país, con énfasis en aquellas investigaciones que han llevado a cambios en los arreglos taxonómicos y nomenclaturales para Colombia durante los últimos 20 años. De esta manera esperamos aportar al conocimiento y entendimiento de las principales modificaciones a nivel regional que han influenciado los listados de mamíferos en el país.
MÉTODOS
Se revisaron los listados de mamíferos de Colombia de los últimos veinte años: Alberico et al. (2000), Solari et al. (2013) y Ramírez-Chaves et al. (2016), con especial énfasis en las descripciones y comentarios de Defler (2003, 2010, 2020) y complementando con la revisión de Hernández-Camacho & Cooper (1976). Posteriormente, se revisó la siguiente bibliografía como punto de partida para cada grupo: Rylands & Mittermeier (2009), para primates del nuevo mundo en general; Rylands et al. (2016), Callitrichidae; Hershkovitz (1949, 1984), Cebus, Sapajus y Saimiri; Hershkovitz (1949, 1984), Aotus; Hershkovitz (1988, 1990), Callicebus; Hershkovitz (1979, 1987a), Pithecia; Hershkovitz (1987b), Cacajao; Lawrence (1933) y Stanyon et al. (1995), Alouatta; Kellogg & Goldman (1944), Ateles; y Fooden (1963), Lagothrix. Esta corresponde a literatura a la que se tuvo acceso y fue consultada directamente por los autores. Por otro lado, accedimos a recientes listados de mamíferos de países vecinos (Abreu et al. 2020; Pacheco et al. 2020; Quintela et al. 2020; Tirira 2020), para comparar los arreglos taxonómicos a nivel de género en busca de una estabilidad taxonómica en la región.
Adicionalmente, se reunió información acerca de las especies y subespecies cuya localidad tipo corresponde a territorio colombiano por medio de la revisión de las descripciones originales y con apoyo de los estudios citados anteriormente.
RESULTADOS Y DISCUSIÓN
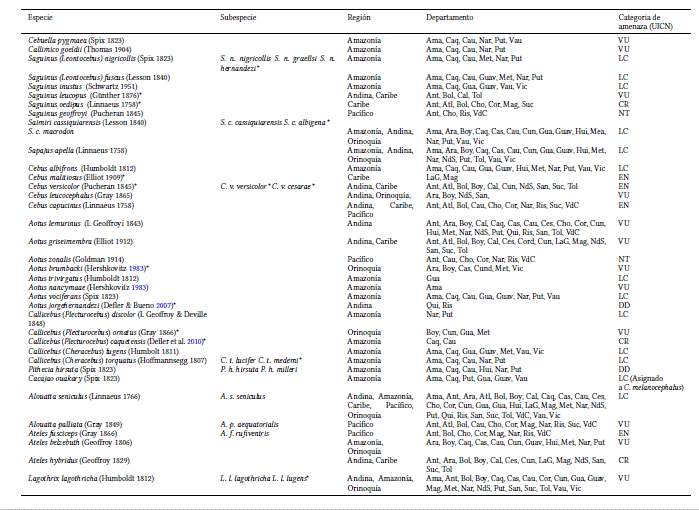
Según Defler (2003), aunque no es posible afirmar con certeza el número de especies de primates que habitan en Colombia, este podría encontrarse “entre 26-32 o quizá un poco más”. En total reconoce 29 especies, siete más que la revisión sobre primates no humanos de Colombia publicada por Hernández-Camacho & Cooper (1976). Posteriormente, Defler (2010) partió del sistema de Groves (2005), al cual agregó tres especies, reportando un total de 32. Una de las modificaciones de Defler (2010) es reconocer una especie de churuco (Lagothrix lagothricha) en lugar de dos (L. lagothricha y L. lugens). Por su parte, Solari et al. (2013) incluyeron 31 especies de primates en la lista de mamíferos de Colombia, cifra que se eleva a 38 en el trabajo de Ramírez-Chaves et al. (2016) (Fig. 1, Tabla S1). Otros listados nacionales, específicos para primates, han mantenido la cifra de 38 especies, aunque con algunas diferencias con respecto al trabajo de Ramírez-Chaves et al. (2016) (Anónimo 2020a,b). En la presente revisión reconocemos 36 especies y 17 subespecies (ocho y seis endémicas respectivamente), con algunos cambios a nivel de género con respecto a listados anteriores (Tabla 1 y Tabla S1). De estos taxa, al menos 25 fueron descritos en territorio nacional y, considerando que algunos carecen de ejemplares tipo, resulta importante realizar revisiones que evalúen la pertinencia de la definición de neotipos.
El incremento de siete especies desde el 2013 se debe a la descripción de nuevas especies, antes consideradas subespecies, donde se incluyen las del género Cheracebus (C. lucifer y C. medemi; Van Roosmalen et al. 2002; Rylands et al. 2012; Byrne et al. 2016), las del género Cebus (C. leucocephalus, C. malitiosus y C. versicolor; Boubli et al. 2012; Rylands et al. 2013) y Saimiri (S. macrodon; Lynch-Alfaro et al. 2015). Adicionalmente, dado que Saimiri sciurus fue restringida a la Amazonía de Brasil y Guayana, Ramírez-Chaves et al. (2016) reconocen la ocurrencia en Colombia de las especies S. cassiquiarensis y S. macrodon. La validez de esta última se discute más adelante en este trabajo. Tal aumento en el número de especies está fundamentado en un cambio de filosofía en cuanto al concepto de especie. Como en otros grupos, la taxonomía del orden Primates ha estado tradicionalmente basada en el concepto biológico que considera a las especies como conjuntos de poblaciones actual o potencialmente entrecruzadas que están aisladas reproductivamente (sin híbridos fértiles) de otros conjuntos similares (Mayr 1942, 1948). En el nuevo milenio, la obra de Groves (2001) impactó el sistema de clasificación en la primatología al recurrir al concepto filogenético de especie, descrito por Cracraft (1983) como el grupo más pequeño diagnosticable de organismos individuales dentro del cual existe un patrón parental de ascendencia y descendencia. La propuesta de Groves (2001) ha sido ampliamente adoptada por primatólogos neotropicales, aun así, muchos investigadores no están de acuerdo con el cambio del concepto que ha llevado a numerosas modificaciones, e incluso a una inflación taxonómica por medio de la descripción de nuevas especies y la elevación de subespecies al rango de especie (Matauschek et al. 2011; Rosenberger 2012; Ruiz-García et al. 2012b, 2015, 2016).
En cuanto a las clasificaciones propuestas a nivel de género de las últimas décadas (ver las secciones de Saguinus-Leontocebus, Sapajus-Cebus y Cheracebus-Plecturocebus), seguimos las consideraciones de Garbino (2015) sobre adoptar un método de “Focused monophyly”. Este propone asignar el rango de género a grupos monofiléticos de especies cuando están respaldados por múltiples fuentes de datos (i.e moleculares, osteológicos y de pelaje, ecológicos, vocalizaciones y cariotipos), por lo que las estimaciones de tiempos de divergencia no deberían considerarse como el único criterio para justificar nuevos arreglos taxonómicos a este nivel (Rosenberger 2012). En este sentido, resulta útil el uso de la categoría de subgénero dado que aporta a la estabilidad en la nomenclatura al representar la cercanía entre clados relacionados preservando el binomen usado tradicionalmente, permite una comunicación más eficiente entre científicos al evitar cambios de género innecesarios, y reemplaza el uso de nombres informales para clados dentro de taxa monofiléticos como, por ejemplo, “divisiones” o “grupos de especies” que no denotan relaciones jerárquicas y no están regulados por el Código Internacional de Nomenclatura Zoológica (Rosenberger 2012; Garbino 2015; Teta 2019).
Especies y subespecies de primates no-humanos de Colombia. La información de región y departamento fue tomada y modificada de Solari et al. (2013) y los modelos de distribución de Henao-Díaz (2020). *Endémica. Departamentos: Amazonas (Ama), Antioquia (Ant), Arauca (Ara), Atlántico (Atl), Bolívar (Bol), Boyacá (Boy), Caldas (Cal), Caquetá (Caq), Casanare (Cas), Cauca (Cau), Cesar (Ces), Córdoba (Cor), Cundinamarca (Cun), Chocó (Cho), Guainia (Gua), Guaviare (Guav), Huila (Hui), La Guajira (LaG), Magdalena (Mag), Meta (Met), Nariño (Nar), Norte de Santander (NdS), Putumayo (Put), Quindío (Qui), Risaralda (Ris), Santander (San), Sucre (Suc), Tolima (Tol), Valle del Cauca (VdC), Vaupés (Vau), Vichada (Vic).
1. Familia Callitrichidae
Cebuella Gray 1866 – Leoncito, tití pigmeo/ Pygmy marmoset Cebuella fue propuesto por Gray (1866) como subgénero de Hapale (más tarde Callithrix), luego considerado como un género aparte por Gray (1870), reforzado por Cabrera (1917) y Thomas (1922) basados en caracteres dentales y craneales (Van Roosmalen & Roosmalen 1997). Estudios sobre la afinidad filogenética entre Cebuella pygmaea y primates amazónicos del género Callithrix han indicado que podrían considerarse como congenéricos (Rosenberger 1981; Barroso et al. 1997; Porter et al. 1997; Tagliaro et al. 1997). A su vez, Groves (2001) consideró a Cebuella como subgénero de Callithrix, pero Rylands & Mittermeier (2009) consideraron que las diferencias en tamaño, morfología y hábitos eran suficientes para mantener a pygmaea en un género separado.
Tradicionalmente se consideraba la existencia de dos subespecies, Cebuella pygmaeapygmaea y C. p. niveiventris, separadas por el río Solimoes (Cruz Lima 1945, Napier 1976, ver Van Roosmalen & Roosmalen 1997; Rylands et al. 2009), las cuales no eran reconocidas por Hershkovitz (1977). Defler (2003, 2010) consideró válida la clasificación de subespecies y mencionó que la especie es bien conocida en la región amazónica al sur del río Caquetá, con observaciones cerca al río Caguán (Izawa 1975) y posibles registros en el alto río Guaviare y Guayabero. Revisiones recientes (Boubli et al. 2018; Garbino et al. 2019) coinciden en asignarles la categoría de especie, por lo que el género actualmente se encuentra conformado por C. pygmaea y C. niveiventris. Finalmente, al restringir la localidad tipo de C. pygmaea al norte del río Solimoes (Garbino et al. 2019) se confirma que este es el nombre correspondiente a las poblaciones de Colombia.
Callimico Miranda-Ribeiro 1912 – Diablillo, chichico negro/Goeldi’s monkey
Género monotípico, aunque se ha considerado la existencia de más de un taxón (Rylands & Mittermeier 2009).
Saguinus Hoffmannsegg 1807 y Leontocebus
Wagner 1840 – Titís, tamarinos/Tamarins
La historia de la clasificación y nomenclatura de los tamarinos es compleja; incluimos apartes de algunos arreglos taxonómicos, con énfasis en los taxa presentes en Colombia (se sugiere ver Rylands et al. 2016).
Elliot (1913) asignó el nombre Leontocebus a los tamarinos del grupo “nigricollis” (con los subgéneros Tamarinus y Marikina), y ubicó a oedipus y geoffroyi en el género Oedipomidas. Hershkovitz (1949) clasificó a los tamarinos en dos géneros, Marikina (subgéneros Tamarin, Marikina y Oedipomidas) con especies en Colombia y Leontocebus en el oriente de Brasil. Cabrera (1957) asignó a los tamarinos en el género Leontocebus con tres subgéneros: Leontocebus (grupos nigricollis, mystax y midas), Oedipomidas (grupo oedipus) y Marikina (leucopus y grupo bicolor). La clasificación de Hershkovitz (1958) comprendió los géneros Saguinus (con los subgéneros Saguinus, Oedipomidas y Marikina) y Leontideus; posteriormente Hershkovitz (1977) ubicó a todos los tamarinos en el género Saguinus evitando el uso de subgéneros y clasificándolos en seis grupos de especies.
Para Colombia se han listado entre seis y siete especies de Saguinus (Hernández-Camacho & Cooper 1976; Díaz et al. 1986; Alberico et al. 2000; Defler 2003, 2010; Solari et al. 2013) (Tabla S1 y S2). Análisis moleculares de las últimas décadas (Cropp et al. 1999; Boubli et al. 2015; Buckner et al. 2015) han apoyado los grupos de especies propuestos por Hershkovitz (1977) (Rylands et al. 2016). Matauschek et al. (2011), utilizando marcadores mitocondriales, encontraron evidencia de polifilia en los taxa S. fuscicollis y S. nigricollis y sugirieron que, de acuerdo con estudios anteriores (Moore & Cheverud 1992; Jacobs et al. 1999), S. f. fuscus era más similar a S. nigricollis que a otras subespecies de S. fuscicollis. Esto se vio reflejado en la elevación de fuscus a la categoría de especie, y fue listada como tal en Solari et al. (2013) (Tabla S1). Diferentes análisis han evidenciado la divergencia entre el grupo nigicollis y los demás tamarinos, estimada entre 11 a 8 m.a. (Rylands et al. 2016). Con base en esto, y apoyados en diferencias morfológicas y ecológicas, Rylands et al. (2016) propusieron elevar al grupo nigricollis al nivel de género apoyando lo propuesto por Buckner et al. (2015). Los autores argumentan que se ha propuesto que 11 a 7 m.a es una edad apropiada para considerar dos clados como géneros diferentes (Goodman et al. 1998), y que su propuesta sigue el mismo razonamiento que la división de los monos capuchinos en dos géneros (Cebus y Sapajus). Bajo esta clasificación, la nomenclatura correspondiente a los tamarinos presentes en Colombia sería Leontocebus fuscus, L. nigricollis (subespecies nigricollis, graellsi y hernandezi), Saguinus inustus, S. oedipus, S. geoffroyiy S. leucopus, y corresponde a lo reportado en ellistado nacional de Ramírez-Chaves et al. (2016).
Esta división ha sido discutida por Garbino & Martins-Junior (2018) argumentando que resulta innecesaria dado que se podría usar la figura de “sub-género”, la cual es aceptada y utilizada en muchos otros grupos taxonómicos (Garbino 2015; Teta 2019). A partir de evidencia genética, osteológica, de pelaje y vocalizaciones, proponen una clasificación que reconoce seis géneros en la subfamilia Callitrichinae: Callimico, Callithrix, Cebuella, Mico, Leontopithecus y Saguinus. Para reflejar la distinción fenotípica, y evitar el uso informal del término “grupo de especies”, subdividen a Saguinus en los subgéneros Leontocebus, Saguinus y Tamarinus (revalidado en ese trabajo). Esta propuesta es seguida por Garbino & Aquino (2018), así como por Abreu et al. (2020) y Quintela et al. (2020) en los recientes listados de mamíferos de Brasil, Pacheco et al. (2020) en Perú, y en la presente revisión para los primates de Colombia.
2. Familia Cebidae
Saimiri Voigt 1831 – Monos ardilla/ Squirrel monkeys
La clasificación más aceptada en las últimas décadas comprende cinco especies: S. boliviensis, S. sciurus, S. oerstedi, S. ustus y S. vanzolinii (Hershkovitz 1984; Ayres 1985). Este arreglo fue controvertido por Thorington Jr. (1985) y Costello et al. (1993) pero apoyado por análisis moleculares de Lavergne et al. (2010) y Chiou et al. (2011), y reconocido por Rylands et al. (2000), Groves (2001, 2005) y Rylands & Mittermeier (2009). Para Colombia, Defler (2003, 2010) reportó a S. sciurus, con tres subespecies (S. s. albigena, S. s. cassiquiarensis y S. s. macrodon), al igual que Solari et al. (2013).
Carretero-Pinzón et al. (2009), basados en una red de haplotipos construida a partir de 1140 pb del gen citocromo b (datos publicados posteriormente por Lavergne et al. 2010) sugirieron dos posibles arreglos para los taxa presentes en Colombia: a) Si S.s. albigena, S. s. cassiquiarensis y S. s. macrodon, de la región central y noroccidental de la Amazonía, son lo suficientemente cercanos entre sí para considerarse subespecies, pero constituyen un grupo separado de S. s. sciurus en la región amazónica oriental, entonces el nombre válido sería cassiquiarensis Lesson, 1840, pasando a clasificarse como subespecies de Saimiri cassiquiarensis; o b) Siguiendo el concepto filogenético de especie, sería apropiado considerarlas especies separadas: S. albigena, S. cassiquiarensis y S. macrodon. Por su parte, Lavergne et al. (2010) sugieren que, si se asume que S. ustus, S. oerstedii y S. boliviensis son especies diferentes (sensu Hershkovitz 1984), los taxa presentes en Colombia podrían asignarse a S. ustus, pero Chiou et al. (2011) reportó que cassiquiarensis Lesson, 1840 tiene prioridad sobre ustus Saint-Hilaire, 1843. Por su parte, Ruiz-García et al.(2015) coinciden con Costello et al. (1993) al proponer a S. oerstedii y S. sciurus como las dos especies válidas para el género, basándose en el concepto biológico de especie y apoyados en las bajas distancias genéticas y la extensa hibridación obtenidas en sus análisis con COI y COII. Su propuesta también señala que, sino se detectan casos de hibridación que impliquena S. vanzolinii, esta podría considerarse una tercera especie.
La clasificación de Rylands (2013) reconoce a los taxa de Colombia como S. c. cassiquiarensis, S. c. albigena y S. macrodon. Sin embargo, Lynch-Alfaro et al. (2015), por medio de análisis de D-Loop y Cyt b, encontraron que S. macrodon, S. c. albigena y S. c cassiquiarensis forman un clado, y no dos, como se esperaría con el arreglo taxonómico de Rylands et al. (2013). Considerando, además, que macrodon resulta ser un clado polifilético, Lynch-Alfaro et al. (2015) recomiendan considerar cinco subespecies de S. cassiquiarensis (reuniendo los clados cassiquiarensis, albigena, macrodon A, macrodon B y macrodon C) a la espera de mayor investigación morfológica que ayude a resolver las relaciones dentro del complejo S. cassiquiarensis y a evaluar la nomenclatura apropiada para los diferentes clados de macrodon. En el presente trabajo seguimos esta clasificación, que difiere de la lista nacional de Ramírez-Chaves et al. (2016) quienes incluyen a S. cassiquiarensis y S. macrodon como especies monotípicas (Tabla S1).
Sapajus Kerr 1792 y Cebus Erxleben 1777 – Maiceros, capuchinos, cariblancos/Capuchin monkeys
Elliot (1913) presentó una clave dicotómica donde dividió a los micos maiceros en “tufted” (con penachos) y “untufted” (sin penachos), siendo una distinción presente en revisiones posteriores, incluyendo las de Hershkovitz (1949, 1955), pero manteniendo a todas las especies y subespecies dentro del género Cebus. Una distinción adicional establecida por Hill (1960) fue señalar que los maiceros con penachos (tufted) son más compactos y robustos en sus extremidades, mandíbula y cráneo mientras que los maiceros sin penachos (untufted) son menos robustos, más esbeltos y con extremidades más largas. Por esto, se conocen también como robustos (tufted) y gráciles (untufted) Lynch-Alfaro et al. (2012b).
Diferentes investigaciones han apoyado esta clasificación, entre ellas la de Silva Jr. (2001) quien concluyó, a partir de análisis morfológicos (Lynch-Alfaro et al. 2012b), que estos taxa deberían dividirse en dos subgéneros: Sapajus Kerr 1792 y Cebus Erxleben 1777. Posteriormente, Lynch-Alfaro et al. (2012b), al reunir y analizar información morfológica, biogeográfica, ecológica y comportamental que distingue a los micos robustos y gráciles, propusieron su división en géneros. Allí incluyen evidencia obtenida por Lynch-Alfaro et al. (2012a) quienes, a partir de información del ARN ribosomal 12S y Cyt b, sugirieron a los taxa gráciles y robustos como recíprocos monofiléticamente y estimaron la divergencia entre ambos en aproximadamente 6.2 m.a. Los autores argumentaron que el tiempo de divergencia entre estos clados es similar al de humanos y chimpancés (estimado entre 5 a 7 m.a), y al de los géneros Lagothrix y Brachyteles (estimado entre 8 a 10.7 m.a), y lo interpretaron como un fuerte soporte para considerar los dos clados principales (Sapajus y Cebus) como géneros separados (Lynch-Alfaro et al. 2012a).
Ruiz-García et al. (2012a) consideraron que, aunque la propuesta de Lynch-Alfaro et al. (2012b) obtuvo un soporte filogenético a partir de evidencia morfológica, genética, comportamental, ecológica y biogeográfica, aún no había sido ampliamente aceptada y se requerían más pruebas antes de adoptar ese esquema taxonómico (por esta razón los autores optaron por mantener a los micos robustos (tufted) en el género Cebus). Posteriormente, Ruiz-García et al. (2016) estimaron el tiempo de divergencia entre 5.5 y 3.3 m.a dependiendo del procedimiento utilizado (indicando 3.3 m.a como el tiempo más probable) y consideraron que las evidencias no eran suficientes para apoyar el uso de Sapajus como género. Por su parte, Gutiérrez & Marinho-Filho (2017) propusieron que lo más adecuado, al menos provisionalmente, era el uso de subgéneros argumentando que: 1) elevar a Sapajus al nivel de género era innecesario, pues no aporta nada que el nombre a nivel de subgénero no pueda lograr; 2) usar los tiempos de divergencia como argumento para elevar a Sapajus al nivel de género es inadecuado, entre otras cosas, porque el tiempo estimado por Lynch-Alfaro et al. (2012a) fue inferido a partir de solo un locus, por lo que debería considerarse un resultado preliminar; y 3) podría plantear dificultades en la comunicación científica. Posteriormente, Lima et al. (2017), con un mayor número de muestras y utilizando los marcadores Cyt b, D-loop y COI, nuevamente sugieren la consideración de los clados de Sapajus y Cebus como géneros separados estimando su divergencia en 5.8 m.a, y Lima et al. (2018) encontraron nuevo soporte para la monofilia recíproca de ambos clados con un tiempo de divergencia de 6.6 m.a.
En el presente trabajo, considerando la literatura disponible acerca de las diferencias en términos morfológicos, genéticos, comportamentales, ecológicos y biogeográficos, seguimos la clasificación propuesta por Lynch-Alfaro et al. (2012b) al reconocer a los géneros Sapajus y Cebus como los presentes en Colombia. Esto coincide con Garbino & Aquino (2018) y con lo adoptado en los listados nacionales de mamíferos de Ecuador (Tirira 2020) y Brasil (Abreu et al. 2020; Quintela et al. 2020).
Sapajus Kerr 1792 – Micos maiceros/ Tufted capuchin monkeys
Hershkovitz (1949) agrupó a los maiceros robustos en Cebus apella (Linnaeus 1758). Cabrera (1957) y Hill (1960) también clasificaron a los primates de este grupo dentro de C. apella, pero reconociendo 11 y 16 subespecies respectivamente (Lima et al. 2018). De estas, el taxoón correspondiente a los bosques de Colombia ha sido identificado como C. apella apella por Hernández-Camacho & Cooper (1976) y Defler (2003), y como C. apella fatuellus por Defler (2010) y Ruiz-García et al. (2012b). La clasificación de Groves (2001) incluyó seis subespecies de C. apella, pero Silva Jr. (2001) no reconoció ninguna forma subespecífica, por lo que consideró a Cebus (subgénero Sapajus) apella como especie monotípica (Rylands & Mittermeier 2009). Posterior a la propuesta de Lynch-Alfaro et al. (2012b) (ver sección anterior), los listados nacionales de Solari et al. (2013) y Ramírez-Chaves et al. (2016) incluyeron a Sapajus apella (como especie monotípica).
Recientes investigaciones han sugerido que, mientras las poblaciones del bosque Atlántico podrían ser divididas en tres o cuatro especies, las formas de la Amazonía y biomas asociados hacen parte de un complejo de especies, o de una especie altamente polimórfica (Lima et al. 2018). Los análisis de Lima et al. (2018), agrupan a S. apella, S. macrocephalus y S. cay en dos clados geográficos del noreste y suroeste del Amazonas en lugar de agruparse en las morfoespecies tradicionalmente. De estas, apella seguiría siendo la denominación correspondiente a las poblaciones de Colombia considerando, además, que actualmente macrocephalus Spix 1823 es considerada sinónimo de S. apella (Boubli et al. 2020). Es importante señalar que estas investigaciones incluyen pocas muestras (y en algunos casos ninguna) de la región Amazonia y Orinoquia de Colombia. Además, recientemente se han reportado registros de S. apella (y C. albifrons) en el suroeste del país, en los Andes orientales del departamento de Nariño (Ramírez-Chaves et al. 2020) por lo que es evidente que muchas localidades de Colombia requieren mayores esfuerzos de muestreo para la toma de datos morfológicos y genéticos.
Cebus Erxleben 1777 – Micos capuchinos, cariblancos/ Untufted capuchin monkeys
Hershkovitz (1949) reconoció tres especies de cariblancos: C. albifrons (Humboldt 1811), C. capucinus (Linnaeus 1758) y C. nigrivittatus Wagner 1848 (=olivaceus Schomburgk 1848). A su vez, incluyó 13 subespecies de C. albifrons, la mayoría de ellas en Colombia. Hernández-Camacho & Cooper (1976) reconocieron seis para el país: C. a. malitiosus, C. a. cesarae, C. a. albifrons, C. a. unicolor, C. a. yuracus y C. a. versicolor considerada como un complejo de formas que incluía versicolor, leucocephalus y pleei (Hershkovitz 1949) y mencionaron que los especímenes del lado colombiano del río Arauca podrían ser variantes de C. a. adustus, conocida en la región del lago de Maracaibo en Venezuela. Allí mismo, los autores señalaron que en cercanías de Barrancabermeja (Santander), a partir de recolectas y observaciones de campo en 1957 y 1958, se encontraron evidencias de pleei y leucocephalus en localidades cercanas e, incluso, individuos de ambos taxa en los mismos grupos sociales. Esto se sugirió como evidencia de que leucocephalus (fase oscura) y pleei (fase clara) representaban extremos de la fase intermedia que correspondía a C. a. versicolor (Hernández-Camacho & Cooper 1976; Defler 2003). Defler (2003, 2010), basado en los análisis de Defler & Hernández-Camacho (2002), siguió el arreglo nomenclatural de cinco subespecies para Colombia: C. a. albifrons, C. a. cesarae, C. a. cuscinus (=C. a. yuracus), C. a. malitiosus, y C. a. versicolor (que incluye a leucocephalus y pleei), coincidiendo con Rylands & Mittermeier (2009) y manteniéndose en Solari et al. (2013).
Ruiz-García et al. (2010), por medio de análisis de COII, sugirieron la existencia de tres grupos en el norte de Colombia: malitiosus, versicolor –pleei -cesarae y leucocephalus; con albifrons formando varios clados en las regiones Amazonia y Orinoquia. A partir de esto, los autores refutaron la hipótesis de Groves (2001) quien agrupó todas las formas del norte de Colombia como un único grupo (C. a. versicolor). Posteriormente, análisis moleculares de Lynch-Alfaro et al. (2012a) identificaron dos clados principales: el primero incluyendo a C. olivaceus y muestras de C. albifrons de localidades amazónicas, y el segundo a C. capucinus y muestras de C. albifrons de localidades del norte de los Andes. De esta manera, C. albifrons, como se consideraba tradicionalmente, era un grupo parafilético. Esto fue apoyado por Boubli et al. (2012), utilizando segmentos de D-loopy Cyt b, y propusieron un arreglo taxonómico provisional de nueve especies, incluyendo cinco para Colombia: C. albifrons, C. capucinus, C. cesarae, C.adustus/leucocephalus y C. versicolor. Por su parte, el estudio de Lima et al. (2017) recuperó ocho clados, en donde se incluye la consideración de C. albifrons, C.capucinus, C. cesarae, C. leucocephalus y C. versicolorcomo especies monotípicas.
Es necesario mencionar que, aunque estas investigaciones han sugerido a versicolor y cesarae como especies hermanas, han incluido pocas muestras de localidades del valle del Magdalena y el Caribe. Además, sus límites geográficos no son claros, y también se necesitan estudios detallados sobre su distinción morfológica. Por su parte, la validez de C. malitiosus permanece sin resolver (Boubli et al. 2012). De manera provisional, consideramos un arreglo taxonómico que incluye a versicolor Pucheran, 1845 y cesaraeHershkovitz, 1949, como formas subespecíficas de Cebus versicolor y mantenemos a C. malitiosus, tal como fue listada para el país por Ramírez-Chaves et al. (2016), haciendo la claridad de que su estatus como especie debe ser reevaluado en futuras investigaciones.
En cuanto a C. capucinus, Hershkovitz (1949) listó cinco subespecies, aunque no las reconoció como válidas. De estas, C. c. capucinus, C. c. curtus y C. c. nigripectus correspondían a Colombia. Más adelante, Hernández-Camacho & Cooper (1976) listaron a C. c. capucinus, aunque tampoco reconocieron como válidas las subespecies propuestas argumentando que la gran variabilidad en caracteres dentro del grupo hacía imposible una designación subespecífica basada en el material disponible. Esta postura, mantenida por Defler (2003, 2010), concuerda con los resultados de Ruiz-García et al. (2012a) con análisis de COII, y fue seguida en los listados nacionales de Solari et al. (2013) y Ramírez-Chaves et al. (2016). En la presente revisión también consideramos a Cebus capucinus como una especie monotípica dado que no se ha encontrado evidencia de diferenciación morfológica de los individuos de la isla Gorgona con respecto a localidades continentales, ni de divergencia genética con análisis moleculares.
3. Familia Aotidae
Aotus (Illiger 1811) – Monos nocturnos/ Night monkeys
Fue descrito inicialmente como Nyctipithecus a partir de una sola especie, A. trivirgatus (Illiger 1811), con una amplia distribución en gran parte de Suramérica y el sur de Centroamérica. Más adelante se describieron algunas especies distribuidas en Colombia: A. vociferans (Spix 1823) y A. lemurinus (Geoffroyi 1843) aún bajo el género Nyctipithecus, y A. griseimembra Elliot 1912 y A. zonalis Goldman1914 que en varios momentos fueron consideradas subespecies de trivirgatus y de lemurinus hasta el 2001 (Defler et al. 2001).
Hershkovitz (1949) consideró a Aotus como un género monotípico compuesto por A. trivirgatus (Humboldt 1812) y varias subespecies que incluían a A. t. griseimembra y A. t. lemurinus. A partir dela década de 1970 inició un auge en estudios cariológicos, y varias investigaciones (Brumback et al.1971; Brumback 1973, 1974; Ma et al. 1976a,b, 1977,1978, 1980) reportaron cariotipos para poblaciones de diferentes áreas geográficas que sugerían la presencia de más de una especie de mono nocturno. Estas investigaciones fueron fundamentales para Hershkovitz (1983) quien cuestionó la monoespecificidad del género y sugirió la presencia de nueve especies diferenciadas por su cariotipo, coloración y patrón de pelaje. Allí, Hershkovitz describió dos de las nueve especies (A. brumbacki y A. nancymaae) y planteó la división del género en dos grupos, separados por el río Amazonas y diferenciados por el patrón de coloración del cuello (monos nocturnos de cuello gris y de cuello rojo). Las especies de cuello gris se reportaron al norte del río Amazonas caracterizadas por una coloración desde agutí grisáceo hasta marrón oscuro, mientras que las de cuello rojo, ubicadas al sur del Amazonas, presentaban una coloración rojiza, anaranjada o amarillenta. Aotus lemurinus (incluyendo las subespecies A. l. lemurinus, A. l. griseimembra y A. l. zonalis), A. vociferans, A. trivirgatus y A. brumbacki (anteriormente identificada erróneamente como A. azarae) se incluyeron en el grupo de cuello gris, mientras que A. miconax, A. nigriceps, A. infulatus y A. azarae se incluyeron dentro del grupo de cuello rojo (Hershkovitz 1983). Con esta propuesta, de las nueve especies de monos nocturnos reconocidas, cuatro (las de cuello gris) se encontraban distribuidas en Colombia (Hershkovitz 1983; Alberico et al. 2000).
En el año 2001, se adicionaron dos especies de monos nocturnos para Colombia al considerar a A. l. griseimembra y A. l. zonalis como especies independientes de A. lemurinus presentando diferencias principalmente cariológicas (Defler et al. 2001). En este sentido, A. lemurinus, A. griseimembra y A. zonalis se definieron como un complejo de especies gemelas con características morfológicas similares y prácticamente indistinguibles entre sí, pero con distribuciones geográficas separadas (Defler et al. 2001; Defler 2003, 2010). En la misma investigación se discutió el estatus taxonómico de A. hershkovitzi, una especie a la cual habían sido asignados algunos individuos del Cauca, y se sugirió como sinónima de A. lemurinus. Además, mencionaron la posibilidad de la existencia de una especie no descrita, con un cariotipo diferente (Defler et al. 2001). Defler & Bueno (2007) describieron esa especie como A. jorgehernandezii a partir de un único individuo, mantenido presuntamente en cautiverio, entre los departamentos del Quindío y Risaralda. Lamentablemente, el espécimen no fue encontrado nuevamente en la colección del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia (No. ICN 14023) donde fue depositado (Defler & Bueno 2007; Ramírez-Chaves 2011). En 2005, Ruiz- Herrera et al. (2005) registraron un cariotipo con las mismas caracteristicas del reportado para A. jorgehernandezii (Torres et al. 1998), a partir de un individuo de procedencia desconocida que permanecía cautivo en el zoológico de Barquisimeto, Venezuela. Hasta el momento, los únicos dos individuos con cariotipos asignados a A. jorgehernandezii han sido animales mantenidos en cautiverio, cuya procedencia exacta se desconoce. En este sentido, es de gran importancia realizar estudios que integren técnicas cariológicas que permitan reconocer individuos con el cariotipo de A. jorgehernandezii en vida silvestre para confirmar la presencia de la especie en el país y dilucidar su distribución.
Con la descripción de A. jorgehernandezii se listaron siete especies para Colombia, todas del grupo de cuello gris (Defler 2010). Sin embargo, en 2012 se registró en el extremo sur del país la presencia de varios individuos de A. nancymaae, especie del grupo de monos nocturnos de cuello rojo. La presencia de estos individuos puede deberse a dos factores no excluyentes: 1) introducciones antrópicas por miembros del Centro de Primates de la Fundación Instituto de Inmunología de Colombia (FIDIC) quienes liberaron en Colombia individuos capturados en Perú con los cuales realizaban experimentos biomédicos, y 2) cambios históricos en el curso del río Amazonas y la formación de “Madres Viejas” (IGUN et al. 2012). De esta manera, en Colombia se registran actualmente ocho especies de monos nocturnos, de las cuales siete son de cuello gris (A. lemurinus, A. griseimembra, A. zonalis, A. brumbacki, A. trivirgatus, A. jorgehernandezi y A. vociferans y una de cuello rojo (A. nancymaae). Cabe mencionar que Ruiz-García et al. (2011), a partir de analisis moleculares, no encuentran una base genética que permita separar a los monos nocturnos en los grupos de cuello gris y cuello rojo, principalmente al encontrar que A. nancymaae y A. nigriceps (incluidos dentro del grupo de cuello rojo), se encuentran más relacionados con los monos nocturnos de cuello gris.
Es importante mencionar que, aunque A. trivirgatus no se ha incluido en los listados de Solari et al. (2013) y Ramírez-Chaves et al. (2016) (Tabla S1) al no presentar individuos recolectados dentro de Colombia, se mantiene aquí como especie probable para el país dado que en límites con Brasil y Venezuela existen registros de individuos morfológicamente diferentes a los Aotus registrados en localidades al este de la Amazonia colombiana (Defler 1994, 2003). Adicionalmente, esta especie es incluida en los listados de mamíferos de países vecinos de Colombia, como Brasil y Venezuela en regiones biogeográficas compartidas (Sánchez & Lew 2012; Abreu et al. 2020). Sin embargo, hasta el momento, el cariotipo de A. trivirgatus no es claro y se hace necesario adelantar estudios cariológicos que confirmen la presencia de la especie en Colombia (Defler 2003, 2010).
4. Familia Pitheciidae
Cheracebus (Byrne et al. 2016) y Plecturocebus (Byrne et al. 2016) – Zogui-zoguis, tocones/ Titi monkeys
Hershkovitz (1990) reconoció 13 especies del género Callicebus clasificadas en cuatro grupos: C. modestus (con una sola especie), C. donacophilus (C. donacophilus, C. olallae, C. oenanthe), C. moloch (C. cinerascens, C. hoffmannsi, C, moloch, C. brunneus, C. cupreus, C. caligatus, C. dubius, C. personatus) y C. torquatus (con una especie). Posteriormente, Kobayashi (1995) modificó el anterior arreglo taxonómico al proponer cinco grupos, mientras que Groves (2001) reconoció 16 especies incluyendo el cambio de C. cupreus ornatus por C. ornatus y C. torquatus medemi por C. medemi. Un cambio importante tuvo lugar después de la revisión de Van Roosmalen et al. (2002), quienes ajustando la clasificación del género siguiendo a Groves (2001), pero sin aportar nueva evidencia genética, elevaron todas las subespecies al nivel de especie argumentando que el concepto de subespecie carece de valor para describir la diversidad de primates neotropicales (Van Roosmalen et al. 2002), lo que resultó en un total de 28 especies. Al respecto, siguiendo el concepto biológico de especie, Defler (2003) se adhiere a la propuesta de Hershkovitz (1990) reconociendo a C. cupreus y C. torquatus como las dos especies colombianas (Tabla S1), al igual que lo presentado en el listado de Alberico et al. (2000). Más tarde, siguiendo algunas consideraciones basadas en análisis cariológicos (Bueno et al. 2006), Defler (2010) adicionó como especies monotípicas a C. discolor y C. ornatus (antes subespecies de C. cupreus, la cual deja de incluirse para Colombia), C. lugens (antes subespecie de C. torquatus) y a la recién descrita C. caquetensis para un total de cinco especies (Tabla S1) (Defler 2010). Esta clasificación se mantuvo en Solari et al. (2013).
Byrne et al. (2016) realizaron análisis filogenéticos con 20 loci nucleares y dos mitocondriales en 15 de las 34 especies reconocidas y propusieron una nueva clasificación a nivel de género que comprende a Callicebus, Plecturocebus y Cheracebus. Este estudio no incluyó muestras de lucifer ni medemi, pero mantuvo su clasificación a nivel de especie siguiendo a Van Roosmalen et al. (2002) y Groves (2005). Por consiguiente, en el listado nacional de Ramírez-Chaves et al. (2016) se listaron siete especies clasificadas como: P. discolor, P. ornatus, P. caquetensis, Ch. torquatus, Ch. medemi, Ch. lucifer y Ch. lugens (Tabla S1). Los resultados de Byrne et al. (2016) fueron soportados por Byrne et al. (2018) (donde se incluyó una muestra de lucifer) quienes realizaron una reconstrucción de la historia biogeográfica de la subfamilia Callicebinae con 11 loci nucleares y dos mitocondriales. Sin embargo, esta clasificación ha sido controvertida por algunos autores quienes, en pro de una estabilidad taxonómica, y a la espera de otras fuentes de datos como evidencia (Garbino 2015), sugieren el uso de la clasificación a nivel de sub-género (Serrano-Villavicencio et al. 2017; Gutiérrez & Marinho-Filho 2017; Garbino & Aquino 2018). Esta propuesta ha sido adoptada en los listados nacionales de mamíferos de Brasil (Abreu et al. 2020) y Perú (Pacheco et al. 2020), así como en la presente revisión para Colombia.
Por otro lado, Carneiro et al. (2020) mencionan haber recuperado todas las especies de Cheracebus como grupos monofiléticos, a partir de 17 muestras de Brasil (incluyendo tres de lucifer). Byrne et al. (2020) evaluaron la identidad de C. torquatus restringiendo su distribución entre los ríos Juruá y Purús en Brasil (considerando a purinus Thomas 1927 como sinónimo junior de torquatus). También redefinieron lugens para representar a todos los Cheracebus encontrados al norte del río Japurá-Caquetá, desde las estribaciones de la cordillera oriental en Colombia hasta la margen izquierda del río Branco y bajo río Negro (Byrne et al. 2020; Fig. 21). Aunque el material revisado incluye especímenes de lucifer y medemi (consideradas allí como especies), no se discuten en detalle.
De lo anterior destaca la falta de evidencia molecular, a partir de muestras de los taxa de Colombia, que apoye a medemi y lucifer como especies diferentes. De acuerdo con Defler (2020), no existen barreras geográficas entre sus poblaciones, contrario a lo mencionado por Groves (2001) para elevarlas a la categoría de especie por lo que su diagnóstico se limita a diferencias en los patrones de coloración de las manos. Además, los análisis de Bueno et al. (2006) con un espécimen colombiano de C. torquatus (sensu Hershkovitz 1990) describieron un cariotipo 2n= 20, similar al de animales cercanos al norte de Brasil (Egozcue 1969; Benirschke & Bogart 1976) lo que implicaría que son poblaciones de la misma especie (C. torquatus) (Defler 2020). En cuanto a lugens, aunque no se cuenta con diferenciación fenotípica, la información sobre número de cromosomas, 2n= 16 (Bonvicino et al. 2003; Stanyon et al. 2003; Bueno et al. 2006) podría indicar que es una especie cariológicamente diferente de C. torquatus (Defler 2020). De esta manera, proponemos considerar para Colombia, de manera provisional, a C. lugens y C. torquatus (C. torquatus lucifer y C. torquatus medemi, sensu Hershkovitz 1990), separadas por el río Caquetá. Aun así, resaltamos la necesidad de incluir muestras de localidades en territorio nacional en futuras investigaciones sobre las relaciones filogenéticas del género.
Pithecia Desmarest 1804 – Mico volador/ Saki monkeys
Hershkovitz revisó el género dos veces (1979, 1987). En la primera revisión reconoció cuatro especies, P. pithecia, P. hirsuta, P. monachus y P. albicans; en la segunda adicionó a P. aequatorialis y consideró a hirsuta Wagner 1840 como sinónimo junior de monachus É. Geoffroy 1812 (Rylands et al. 2000) y consideró a milleri como una subespecie débilmente definida de P. monachus monachus. Por su parte, Defler (2003, 2010) indicó a P. monachus (con P. m. monachus y P. m. milleri) como la única distribuida en Colombia. Esta clasificación se mantuvo en Solari et al. (2013).
Recientemente, Marsh (2014) propuso una clasificación de 16 especies basada en patrones de coloración en el pelaje y recurriendo al concepto filogenético de especie. Según esto, la identidad de las especies que ocurren en Colombia corresponde a P. hirsuta y P. milleri. Sin embargo, algunos autores han considerado que la revisión de Marsh ha ocasionado confusión en la identificación de ciertas especies del género. Por ejemplo, Serrano-Villavicencio et al. (2019) discuten algunas imprecisiones taxonómicas en cuanto a la organización del grupo P. irrorata en Bolivia, Brasil y Perú, considerando tres de las especies descritas por Marsh (2014) como sinónimos junior de P. irrorata. Gusmão & Santos-Silva (2015) reportaron el avistamiento de individuos en Brasil que no fueron identificados con certeza siguiendo la revisión de Marsh (2014) y finalmente asignados tentativamente como Pithecia cf. mittermeieri. En Colombia, Acevedo-Charry et al. (2017) encontraron individuos en Leguízamo, Putumayo, una localidad que, según los mapas de distribución y registros conocidos, se encuentra en medio de P. hirsuta y P. milleri (sensu Marsh 2014). Dado que los límites en la distribución de estas especies no son claros (Defler 2010; García et al. 2017), sumado a la ausencia de barreras ambientales entre las localidades, y la variación en el pelaje por edad y dimorfismo sexual, los registros fueron presentados como Pithecia monachus (sensu Hershkovitz 1987) (Acevedo-Charry et al. 2017). Por su parte, García et al. (2017) reportaron que uno de los registros de Marsh (2014) al norte del río Caguán presenta información errónea de su procedencia. En la presente revisión, considerando la ausencia de barreras ambientales y de evidencia molecular, así como la débil diferenciación fenotípica, consideramos a las poblaciones en Colombia como P. hirsuta hirsuta y P. hirsuta milleri de acuerdo con Defler (2020) a la espera de análisis comparativos que ayuden a resolver sus relaciones e identidad taxonómica.
Cacajao Lesson 1840 – Colimochos/ Uacaries
Hershkovitz (1987) propuso dos especies, siendo Cacajao melanocephalus (C. m. ouakary) la única con distribución en el país. Análisis genéticos de C. m. ouakary y C. m. melanocephalus sugirieron que deberían considerarse especies diferentes (Figueiredo et al. 2006; Rylands & Mittermeier 2009), por lo que Defler (2010) reportó a Cacajao ouakary como la especie válida para Colombia (Tabla S1). Boubli et al. (2008), basados en análisis de Cyt b, consideraron a ouakary como sinónimo junior de melanocephalus y elevaron esta última a nivel de especie proponiendo un arreglo taxonómico de cuatro especies (C. ayresi, C. calvus, C. hosomi y C. melanocephalus). Posteriormente, incluyendo evidencia morfológica y zoogeográfica, así como la revisión de especímenes de colecciones omitidos por Boubli et al. (2008), Ferrari et al. (2014) propusieron un arreglo taxonómico más conservador del grupo C. melanocephalus: Incluyeron a C. melanocephalus (C. m. melanocephalus y C. m. ayresi) al norte del río Negro en Brasil y Venezuela, y a Cacajao ouakary al sur del río Negro en Brasil y Colombia (Ferrari et al. 2014; Fig. 1), aunque esta hipótesis no ha sido reconocida en la última actualización de la UICN donde aún se considera sinónimo de melanocephalus (Boubli 2020). Dado que los reportes de ocurrencia para Cacajao en Colombia (GBIF.Org 2021) coinciden con la distribución propuesta por Ferrari et al. (2014) para ouakary, consideramos a Cacajao ouakary (Spix 1823) como la especie distribuida en territorio colombiano, entre los ríos Guayabero-Guaviare y el bajo río Apaporis (Defler 2010).
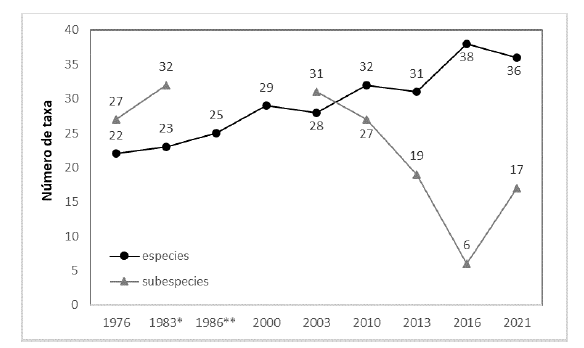
Fig. 1
Cambios en el número de especies y subespecies de primates no humanos en listas nacionales. *Corresponde al trabajo presentado por Hernández-Camacho y Defler en el Simposio de primatología (Arequipa, Perú, 1983) y publicado en 1989 en los anales del IX Congreso Latinoamericano de Zoologia. **Díaz et al. (1986)
5. Familia Atelidae
Alouatta Lacepede 1799 – Monos aulladores/ Howler monkeys
Rylands et al. (2000) y Cortés-Ortiz et al. (2015) reconocieron nueve especies, de las cuales A. palliata y A. seniculus se distribuyen en Colombia. Lawrence (1933) reportó siete subespecies de A. palliata, de las cuales cinco son aceptadas actualmente (Cortés-Ortiz et al. 2015). Las poblaciones de Colombia han sido referidas como A. p. aequatorialis (Defler 2003, 2010) aunque en los listados nacionales de Solari et al. (2013) y Ramírez-Chaves et al. (2016) se incluye la especie como monotípica Tabla S1. Recientemente, Doyle et al. (2020) realizaron análisis filogenéticos con muestras de siete de las nueve especies del género, pero no incluyeron ningún comentario sobre las formas subespecíficas para ninguna especie (al igual que los listados nacionales mencionados anteriormente). En este trabajo seguimos la clasificación presentada por Cortés-Ortiz et al. (2015) por lo que incluimos a A. p. aequatorialis.
Hill (1962) y Stanyon et al. (1995) reconocieron nueve subespecies de A. seniculus, que se redujeron a tres en la revisión de Cortés-Ortiz et al. (2015). Las poblaciones en Colombia se asignaban a la subespecie A. s. seniculus (Defler 2003, 2010) aunque en los listados nacionales de 2013 y 2016 se incluyó también como especie monotípica (Tabla S1) así como en Doyle et al. (2020). Aquí incluimos a A. s. seniculus siguiendo a Cortés-Ortiz et al. (2015). Por otra parte, los mapas de distribución presentados por Cortés-Ortiz et al. (2015) y Doyle et al. (2020), de acuerdo con los polígonos de la UICN (Urbani et al. 2018), sugieren la presencia de A. arctoidea en Colombia, en alrededores de Arauca y Casanare. Desafortunadamente, Doyle et al. (2020) no contaron con muestras de esta especie en sus análisis filogenéticos. Es necesario adelantar investigaciones en esta región para confirmar su presencia en Colombia.
Ateles Geoffroy 1806 – Monos araña/ Spider monkeys
Kellogg & Goldman (1944), a partir de caracteres morfológicos, propusieron la existencia de cuatro especies y múltiples subespecies. Tres de estas con presencia en Colombia: A. belzebuth belzebuth en los Llanos y la Amazonia, A. b. hybridus al oriente de los ríos Cauca y Magdalena, A. fusciceps robustus al norte, A. f. fusciceps en la costa pacífica y A. geoffroyi grisescens al noroccidente. Más tarde, Hernández-Camacho & Cooper (1976), basados en patrones de pelaje, sugirieron que el género Ateles es monotipico, compuesto únicamente por A. paniscus y varias subespecies. Esta clasificación fue modificada por Froehlich et al. (1991) a partir de análisis morfométricos, proponiendo la existencia de tres especies (A. paniscus, A. belzebuth, A. geoffroyi). Recientemente, a partir de análisis genéticos, se elevaron a nivel de especie varias de las subespecies propuestas por Kellogg & Goldman (1944) con un consenso de siete especies en el género, de las cuales tres se encontraban en territorio colombiano (A. belzebuth, geoffroyi, A. hybridus) (Collins & Dubach 2000; Groves 2001). Esto es consistente en los listados de Defler (2003); Defler et al. (2010), pero difiere de Alberico et al. (2000) quienes habían reportado, además, a A. fusciceps para Colombia (Tabla S1).
Solari et al. (2013) y Ramírez-Chaves et al. (2016) reportaron las mismas tres especies de Ateles para el país. Sin embargo, a partir de la revisión de Rylands et al. (2006), se sugiere que en lugar de las dos subespecies de A. geoffroyi consideradas para el país (A. g. grisescens y A. g. robustus), en Colombia habita la especie A. fusciceps, específicamente A. fusciceps rufiventris, con A. fusciceps fusciceps presente en Ecuador (Cepeda-Duque et al. 2018). Con respecto a A. hybridus, inicialmente se propuso que estaba compuesta por dos subespecies diferenciadas por su patrón de coloración y separadas por el río Magdalena en Colombia, ocurriendo A. h. brunneus en la orilla oeste y A. h. hybridus en la orilla este (Defler 2003). Esta clasificación subespecífica fue cuestionada por Link et al. (2015), por medio de análisis mitocondriales donde los haplotipos obtenidos se comparten entre las poblaciones de ambas orillas del río, sugiriendo que el río Magdalena no ha sido una barrera para la diferenciación de la especie. Al respecto, según diversos autores, el concepto de subespecie se basa en diferencias fenotípicas, y no genéticas, de dos poblaciones. Poblaciones conespecíficas que difieren morfológicamente entre sí se denominan subespecies (un dispositivo puramente taxonómico si estas son parte de una serie de poblaciones contiguas) (Simpson 1943; Mayr 1943, 1996). Hall (1943) menciona que si en la naturaleza ocurren cruces en zonas donde se encuentran los rangos geográficos de dos tipos de mamíferos, ambos deben tratarse como subespecies de una especie; y que, si en estas zonas no ocurren dichos cruces, entonces ambos tipos de mamíferos deben considerarse especies diferentes. De esta manera consideramos de suma importancia retomar la discusión sobre el estatus de las poblaciones de hybridus en Colombia realizando análisis que complementen las descripciones sobre su diferenciación morfológica descrita por autores como Defler (2003, 2010). En la presente revisión, reconocemos a A. belzebuth, A. hybridus y A. fusciceps (A. f. rufiventris) como los taxa presentes en Colombia.
Lagothrix Geoffroy 1812 – Churucos/ Woolly monkeys
Fooden (1963) reconoció dos especies, L. flavicauda y L. lagothricha. Esta última con cuatro subespecies, L. l. cana, L. l. lagothricha, L. l. lugens y L. l. poeppigii. Groves (2001, 2005) propuso elevar a la categoría de especie a cana, lugens y poeppigii considerando que las pieles examinadas eran marcadamente distintas (Defler 2003). Sin embargo, Defler (2003) consideró que la diferencia de coloración en las pieles no era un argumento definitivo para apoyar la designación de especies. También mencionó que, según un comentario personal de Ruiz-García, aunque lugens y lagothricha representan acervos genéticos diferentes, no se puede asegurar que sean especies distintas dada la falta de evidencia de aislamiento reproductivo. Así, Defler (2003, 2010) reconoció para Colombia a L. lagothricha con las subespecies L. l. lagothricha y L. l. lugens siguiendo a Fooden (1963). Esta clasificación se mantuvo en Solari et al. (2013).
Mantilla-Meluk (2013), basado en análisis morfométricos y del color del pelaje en especímenes de museo, sugirió la validez de L. lugens como especie incluyendo tres subespecies (L. l. defleri, L. l. lugens y L. l. sapiens). Sin embargo, investigaciones con COI, COII, D-loop, análisis cariológicos y revisiones de especímenes en colecciones biológicas (Botero et al. 2010; Ruiz-García & Pinedo-Castro 2010; Botero & Stevenson 2014; Defler 2014; Ruiz-García et al. 2014; Botero et al. 2015), no han encontrado soporte para la consideración de lagothricha y lugens como especies, y concuerdan con la clasificación de Fooden (1963). En la presente revisión incluimos a L. lagothricha con las subespecies L. l. lagothricha y L. l. lugens, lo que difiere del listado nacional de Ramírez-Chaves et al. (2016) quienes listaron a L. lagothricha sin mencionar formas subespecíficas (Tabla S1).
Taxa con localidad tipo en Colombia Abreviaciones:
AMNH: American Museum of Natural History
BM: British Museum
FMNH: Field Museum of Natural History
ICN: Instituto de Ciencias Naturales, Universidad Nacional de Colombia, Bogotá
MCZ: Museum of Comparative Zoology
MNHN: Museum National d’Histoire Naturelle de Paris
USNM: National Museum of Natural History, Smithsonian Institution, Washington, D.C.
ZMHB: Berlin Zoological Museum
Saguinus (Leontocebus) fuscus (Lesson 1840) Leontopitecus fuscus. Lesson R.P. 1840. Spec. Mamm. Bim. Quadrum., p. 202.
Localidad tipo: La descripción indica como hábitat de esta especie a las llanuras de Mocoa en la vertiente oriental de las cordilleras, a orillas de los ríos Putumayo y Caquetá, donde es nombrado “Leoncito” por los españoles.
Holotipo: No se indica en la descripción original.
Saguinus (Leontocebus) nigricollis hernandezi
Saguinus nigricollis hernandezi. Hershkovitz P. 1982.
Proc. Biol. Soc. Wash. 95(4), p. 649.
Localidad tipo: Río Peneya, pequeño tributario del río Caquetá, entrando por la izquierda (norte) unos 15 km arriba de la desembocadura del río Caguán y unos 50 km en línea recta abajo del pueblo de La Tagua. Intendencia de Caquetá, Colombia. Aproximadamente 150 m s.n.m.
Holotipo: Hembra adulta. Piel plana. FMNH, número de catálogo 123380. Recolectado en 1974 por Tsuyoshe Watanab (# original: 23).
Saguinus oedipus (Linnaeus 1758)
Simia oedipus. Linnaeus. 1758. Systema naturae, ed. 10, vol. 1, p. 28.
Localidad tipo: “America”. Restringida al bajo río Sinú, departamento de Córdoba, Colombia por Hershkovitz (1949).
Holotipo: No preservado. Nombrado según la descripción y placa coloreada de Edwards (1751) como “el pequeño mono león” Hershkovitz (1949). Comentarios: Según Edwards, se decía que el espécimen original había sido obtenido en “La Vera Cruz in New Spain [=México]”. Hershkovitz (1949) argumentó que la especie no ocurría naturalmente por fuera de Colombia y, apoyado en la descripción del hábitat realizada por Humboldt, restringió la localidad tipo al norte de Colombia.
Saguinus leucopus (Günther 1876) (no 1877) Hapale leucopus. Günther A. 1876. Proc. Zool. Soc. Lond. p. 743.
Localidad tipo: Medellín, Antioquia, U.S. of Columbia (=Colombia).
Holotipo: BM. No se indica número de catálogo. Recolectado por T.K. Salmon cerca a Medellín.
Saimiri cassiquiarensis albigena (Pusch 1941)
Cebus sciurus albigena. Pusch. 1941. p. 212. Localidad tipo: La descripción menciona a “Medina” con las coordenadas “N5, W73”. Hershkovitz (1984) hizo las siguientes precisiones: “Medina, ladera oriental de la Cordillera Oriental, aproximadamente a 50 km al noreste de Villavicencio, Cundinamarca, Colombia, 576 msnm”. Sin embargo, la interpretación puede resultar confusa por lo que hacemos la claridad de que la descripción corresponde al Municipio Medina, departamento de Cundinamarca, Colombia.
Holotipo: Macho. Piel y Cráneo. ZMHB, número de catálogo 33951. Recolectado por el hermano Nicéforo María (Hershkovitz 1984).
Comentarios: Von Pusch (1941) indica al hermano “Apolinar” como recolector del espécimen, pero Hershkovitz (1984) mencionó al hermano Nicéforo María.
Cebus albifrons (Humboldt 1812)
Simia albifrons. Humboldt A. von y Bonpland A. 1812.
Localidad tipo: Según Defler & Hernández-Camacho (2002), la descripción de Humboldt (1812) estuvo basada en un individuo cautivo reportado en Maipures, sobre la margen izquierda del río Orinoco (departamento de Vichada, Colombia), pero agregó que se observaron algunos individuos silvestres en los alrededores de la Misión de La Esmeralda en la margen derecha del alto río Orinoco (Venezuela). Más tarde, Humboldt (1824) mencionó que observó a Simia albifrons en la Misión Atures, 50 km al norte de Maipures, en el lado opuesto del río, contradiciendo su descripción original en 1812. La confusión surge porque el comentario de Humboldt (1824) se basa en el espécimen original, pero no se menciona a Maipures y tampoco había evidencia de la presencia de Cebus albifrons en cercanías de Atures, en la margen opuesta (derecha) del río Orinoco (correspondiente a Venezuela). Debido a la confusión, y lo que Defler & Hernández-Camacho (2002) consideraron errores en la descripción, que tampoco contaba con un espécimen tipo, se asignó una nueva localidad tipo basada en un neotipo recolectado 10 km al norte de Maipures, en el Parque Nacional Natural El Tuparro, departamento de Vichada, Colombia.
Holotipo: No preservado. Defler & Hernández-Camacho (2002) designaron un neotipo, depositado en la colección biológica del Instituto de Investigación de Recursos Biológicos Alexander von Humboldt en Villa de Leyva, Boyacá, Colombia. Macho adulto joven. Piel y cráneo. Número de catálogo 2844.
Cebus leucocephalus Gray 1865
Localidad tipo: “Columbia”. Hershkovitz (1949) restringió la localidad tipo a El Tambor, río Lebrija, 25 km noroeste de Bucaramanga, departamento de Santander, Colombia.
Holotipo: BM. comprado por Parzudaki (Hershkovitz 1949)
Comentarios: Gray (1865) mencionó que la especie puede ser una variedad de C. versicolor, aunque los distingue por la presencia de una línea en la frente.
Cebus versicolor Pucheran 1845
Localidad tipo: “Originaire de Colombie (Santa-Fé de Bogota)”. Hershkovitz (1949) mencionó que en cercanías de la ciudad de Bogotá no ocurren monos, y sugiere que el espécimen tipo provenía de algún lugar en el valle medio del río Magdalena en la vertiente occidental de la cordillera Oriental. Holotipo: Piel y cráneo. MNHN. Catálogo de tipos No. 86, número de catálogo 559 (479). Recibido de M. Jurgens en 1844 (Hershkovitz 1949).
Cebus versicolor cesarae (Hershkovitz 1949)
Cebus albifrons cesarae. Hershkovitz P. 1949. Proc. U. S. Natl. Mus vol. 98, No. 3232, p. 356.
Localidad tipo: Río Guaimaral, un canal del río Cesar, departamento del Magdalena, Colombia. 140 m s.n.m.
Holotipo: Macho adulto. USNM, número de catálogo 281588. Recolectado por P. Hershkovitz el 24 de agosto de 1942. Numero original: 525.
Cebus malitiosus Elliot 1909
Localidad tipo: “Vicinity of Bonda, Colombia, South America”. Hershkovitz (1949) la restringe a Bonda, esquina noroeste de la base de la Sierra Nevada de Santa Marta, departamento de Magdalena, Colombia.
Holotipo: Macho adulto. Piel y cráneo. AMNH, número de catálogo 14620. Recolectado por Herbert H. Smith.
Cebus capucinus capucinus. (Linnaeus 1758)
Simia capucina. Linnaeus. 1758. Systema naturae. ed. 10, p. 29.
Localidad tipo: Desconocida. Goldman (1914) fijó la localidad tipo de C. capucinus en la localidad tipo reconocida para C. hypoleucus. Según Hershkovitz (1949) esa localidad corresponde a la boca del río Sinú, al norte de Colombia, pero sugiere que hasta comprobar que capucinus ocurre en esa zona, la restricción aceptada debería ser la más amplia que corresponde al “norte de Colombia”.
Cebus capucinus curtus. Bangs 1905
Cebus curtus Bangs. 1905. Bull. Mus. Comp. Zool., vol. 46, p. 91.
Localidad tipo: Isla Gorgona, Colombia.
Holotipo: Macho adulto. MCZ, número de catálogo 10824. Recolectado el 2 de julio de 1904. Comentarios: Aunque la relaciona con Cebus hypoleucus, la define como una especie “bien marcada”, distinguiéndola de hypoleucus en el tamaño (extremidades más cortas, manos y pies más pequeños y un cráneo más pequeño y estrecho).
Aotus lemurinus (I. Geoffroy 1843)
Nyctipithecus lemurinus I. Geoffroy. 1843. Comptes Rendus Acad. Sci., Paris 16: 1151, p. 25.
Localidad tipo: Cercanías de Fusagasugá, “Santa Fe de Bogotá”, Cundinamarca (1700-2000 m s.n.m.) (Defler et al. 2001).
Holotipo: Macho adulto. MNHN, catálogo de tipos Nº 102a, número de catálogo 486 (545). Individuo comprado en 1842.
Comentarios: En la descripción se designó como localidad tipo a “Nueva Granada”. Más tarde, el mismo autor (Geoffroy-Saint Hilaire 1844) sugirió como localidad tipo “Santa Fe de Bogotá” ignorando algunos individuos recolectados en el “Paso de Quindío”, por lo que Hershkovitz (1949) designó esta localidad como tipo para la especie. Sin embargo, Defler et al. (2001) reafirmaron la posición de Geoffroy-Saint Hilaire (1844) proponiendo mantener a “Santa Fe de Bogotá” como localidad tipo y, específicamente, los alrededores de Fusagasugá (“neighborhood of Fusagasugá”).
Aotus griseimembra Elliot 1912
Localidad Tipo: Hacienda Cincinnati, Santa Marta, Colombia.
Holotipo: Macho adulto, AMNH, número de catálogo 32664. Colectado por M.A Carriker Jr., en Julio 20 de 1911.
Aotus brumbacki (Hershkovitz 1983)
Localidad Tipo: Villavicencio, Departamento de Meta, Colombia.
Holotipo: Macho adulto. FMNH, número de catálogo 123035. El individuo provenía de una colonia de la Escuela de Medicina de la Universidad de Washington, St. Louis, Mo.
Comentarios: Inicialmente el holotipo se había asignado a A. azarae y la localidad tipo correspondía al río Paraguay que atraviesa gran parte de Paraguay, Bolivia y Argentina. Sin embargo, el holotipo presenta características morfológicas y cariológicas de A. brumbacki y no de A. azarae. Por lo tanto, Hershkovitz (1983) asignó como localidad tipo a Villavicencio, Meta, en Colombia.
Aotus jorgehernandezi (Defler & Bueno 2007) Localidad Tipo: Incierta. Individuo encontrado en cautiverio en el Quindío. Posiblemente se distribuye en el Parque Nacional Natural de los Nevados, entre Quindío y Risaralda.
Holotipo: Hembra adulta. ICN, número de catálogo 14023. El espécimen no se encontró nuevamente en la colección.
Callicebus (Cheracebus) torquatus medemi Hershkovitz 1963
Callicebus torquatus medemi. Hershkovitz, P. 1963. Mammalia 27(1). Pág. 52.
Localidad tipo: Río Mecaya, en el banco derecho cerca a la boca del río Caquetá, departamento de Putumayo, este de Colombia. Elevación aproximada de 180 m s.n.m.
Holotipo: Macho adulto. Piel y cráneo. FMNH, número de catálogo 70699. Recolectado el 17 de marzo de 1952 por Philip Hershkovitz. Número original: 6144.
Callicebus (Plecturocebus)ornatus (Gray 1866) Callithrix ornata. Gray J. E. 1866. Ann. Mag. Nat. Hist., 3th ser., vol. 17, p. 57.
Localidad tipo: “New Granada”. Restringida por Hershkovitz (1963) a Villavicencio, en la región del alto río Meta, departamento del Meta, Colombia Holotipo: Piel y cráneo. BM. Comprado por M. Verreaux (Hershkovitz 1963).
Comentarios: La descripción menciona que el espécimen fue recibido a M. Verreaux como C. discolor.
Callicebus (Plecturocebus) caquetensis (Defler 2010) Callicebus caquetensis. Defler, T. R., Bueno. M. L., & García, J. 2010. Primate Conserv. (25):2.
Localidad tipo: Vereda El Jardín, 01° 8’ 24.61” N, 75° 32’ 34.04” W. Este de Valparaiso, municipalidad de Puerto Milán, departamento de Caquetá, Colombia. 251 m s.n.m.
Holotipo: Hembra juvenil. Piel, cráneo, esqueleto y tejidos en alcohol. ICN-MHN, número de catálogo 19439.
Pithecia hirsuta milleri Allen 1914
Pithecia milleri. Allen 1914. New South American monkeys. Bulletin of the American Museum of Natural History 33:647-655.
Localidad tipo: Morelia, en la cabecera del río Fragua, departamento de Caquetá, Colombia. Holotipo: Macho adulto. Piel y cráneo. AMNH, número de catálogo 33876 recolectado por Leo Miller, 8 de julio de 1912 (No. 878).
Alouatta seniculus (Linnaeus 1766)
Simia seniculus. Linnaeus. 1766. Systema naturae, ed. 12, p. 37.
Localidad tipo: “Carthagenae in silvis ad fluvium”, departamento de Bolívar, Colombia (Hershkovitz 1949).
Holotipo: No preservado.
Ateles hybridus I. Geoffroy 1828 (no 1829) Localidad tipo: Valle del río Magdalena, Colombia.
Restringido por Kellogg & Goldman (1944) a: “La Gloria” sobre el río Magdalena, sur del departamento de Magdalena, Colombia.
Holotipo: (Cotipos) 2 machos y 1 hembra. MNHN. Presentado por M. Plée en 1826.
Comentarios: Actualmente el término “Cotipo” no es reconocido por el Código Internacional de Nomenclatura Zoológica (ICZN 1999).
Ateles fusciceps rufiventris Scatler 1872
Ateles rufiventris. Scatler. 1872. Proc. Zool. Soc. London. pt. 2, p. 688.
Localidad tipo: “Columbia, in ripis fl. Atrato”. Restringido por Kellogg & Goldman (1944) a: río Atrato, Darién, Colombia.
Holotipo: Hembra. BM. No. desconocido. Comentarios: Sclater (1871) afirmó que el tipo de Ateles rufiventris fue obtenido en Colón, Panamá, por un oficial de la Royal West Indian Mail Co. el cual había sido llevado desde el río Atrato. Posteriormente, Sclater (1872) publicó una ilustración a color de este mono (Kellogg & Goldman 1944).
Lagothrix lagothricha lagothricha (Humboldt 1812) Simia lagothricha. Humboldt. 1812. Recuel d’observations de zoologie et d’anatomie comparée. Vol. 1: 354.
Localidad tipo: Al parecer el individuo fue observado cerca a San Fernando de Atabapo, una misión cerca a la desembocadura del río Guaviare (Fooden 1963). Holotipo: No preservado. El nombre y la descripción estuvo basada en un individuo cautivo, visto por Humboldt el 27 de mayo de 1800, en una cabaña indígena (Fooden 1963).
Comentarios: Actualmente la región donde se realizó la observación del individuo se ubica en alrededores de la frontera entre Colombia y Venezuela. San Fernando de Atabapo se ubica en la margen oriental del río Orinoco, al frente de la desembocadura del río Guaviare que se encuentra en la margen occidental (y que a su vez separa a los departamentos colombianos del Vichada y Guainía).
Lagothrix lagothricha lugens Elliot 1907
Lagothrix lugens. Elliot. 1907. Annals and Magazine of Natural History. series 7. p. 193.
Localidad tipo: “Mountains 2° 20’ north of Tolima, Colombia”. Fooden (1963) corrige la localidad e indica al departamento del Huila, en la región del valle alto del río Magdalena.
Holotipo: Macho adulto. Piel y cráneo. BM, número de catálogo 90.2.22.2. Fooden (1963) indicó el número No. 90.2.22.1.
CONCLUSIONES
Considerando la ubicación geográfica del país, que conecta la fauna de Centroamérica con el norte de los Andes, el Amazonas y las Guayanas (sumada a la presencia de ríos y cordilleras como potenciales barreras geográficas), la recopilación de datos sobre las relaciones filogenéticas de los primates que allí habitan representa un aporte a la comprensión de sus historias evolutivas a escala de la región neotropical. La lista de especies que presentamos aquí es una hipótesis basada en la información disponible. Esperamos que cambie con el surgimiento de evidencia de análisis genéticos, filogeográficos y filogenéticos, así como con estudios morfológicos en campo y con revisiones de especímenes de museos. En este sentido, es necesario promover colaboraciones nacionales e internacionales que contribuyan al aprendizaje y desarrollo de nuevos métodos de investigación, pero también incentivar el trabajo de nuevos investigadores en el campo de la taxonomía y la sistemática zoológica.
Agradecimientos
A los revisores que, con sus comentarios y sugerencias, aportaron a la mejora del manuscrito.
Dedicatoria: Los autores dedican este trabajo a la memoria de las personas fallecidas y violentadas durante las manifestaciones del paro nacional de 2021 en Colombia.
REFERENCIAS
Abreu, E. F. et al. 2020. Lista de Mamíferos do Brasil. Comitê de Taxonomia da Sociedade Brasileira de Mastozoologia (CT-SBMz). Disponível em: <https://www.sbmz.org/mamiferos-do-brasil/>. Acessado em: Noviembre 27 de 2020. https://doi.org/10.47749/t/unicamp.1994.74921
Acevedo-Charry, O. A., M. P. Henao-Rodríguez, & D. M. Morales-Martínez. 2017. Incidental records of mammals from Leguízamo, Putumayo, Amazon region at the southern border of Colombia. Mammalogy Notes 4:34-37. https://doi.org/10.47603/manovol4n2.34-37
Alberico, M., A. Cadena, J. Hernández-Camacho, & Y. Muñoz-Saba. 2000. Mamíferos (Synapsida: Theria) de Colombia. Biota colombiana 1:43-75.
Anónimo 2020a. Primates de Colombia. Asociación Primatológica Colombiana. Recuperado de https://drive.google.com/file/d/1LTbK-F4V5lGh1gJe3iMHvZqs3dlkrid/view
Anónimo 2020b Especies de primates colombianos. Guía de cambios taxonómicos (versión 4.0) de la Asociación Primatológica Colombiana. Recuperado de https://www.asoprimatologicacolombiana.org/uploads/1/1/4/7/11474090/gu/C3/ADa cambiostaxon/C3/B3micosprimates 4.0.pdf
Ayres, J. M. 1985. On a new species of squirrel monkey, genus Saimiri, from Brazilian Amazonia (Primates, Cebidae). Papéis Avulsos Zoologia, São Paulo 36:147-164. https://doi.org/10.1590/0031-1049.2014.54.32
Barroso, C. M. L. et al. 1997. Update on the phylogenetic systematics of New World monkeys: Further DNA evidence for placing the pygmy marmoset (Cebuella) within the genus Callithrix. International Journal of Primatology 18:651-674.
Benirschke, K., & M. H. Bogart. 1976. Chromosomes of the tanhanded Titi (Callicebus torquatus, Hoffmannsegg, 1807). Folia Primatologica 25:25-34. https://doi.org/10.1159/000155705
Bonvicino, C. R., H. N. Penna-Fieme, F. Do Nascimento, B. Lemos, R. Stanyon, & H. N. Seuánez. 2003. The lowest diploid number (2n=16) yet found in any primates: Callicebus lugens (Humboldt, 1819). Folia Primatologica 74:141-149. https://doi.org/10.1159/000070647
Botero, S., L. Y. Rengifo, M. L. Bueno, & P. R. Stevenson. 2010. How many species of woolly monkeys inhabit Colombian forests? American Journal of Primatology 72:1131-1140. https://doi.org/10.1002/ajp.20878
Botero, S., & P. R. Stevenson. 2014. Coat color is not an indicator of subspecies identity in Colombian woolly monkeys. The Woolly Monkey (T. Defler & P. R. Stevenson. eds.). Springer, New York, NY. https://doi.org/10.1007/978-1-4939-0697-02
Botero, S., P. R. Stevenson, & A. Di Fiore. 2015. A primer on the phylogeography of Lagothrix lagotricha (sensu Fooden) in northern South America. Molecular Phylogenetics and Evolution 82:511-517. https://doi.org/10.1016/j.ympev.2014.05.019
Boubli, J. 2020. Cacajao melanocephalus. The IUCN Red List of Threatened Species 2020: e.T160875418A160876028. https://dx.doi.org/10.2305/IUCN.UK.2020-2.RLTS.T160875418A160876028.en. Downloaded on 10 March 2021. https://doi.org/10.2305/iucn.uk.2020-2.rlts.t160875418a160876028.en
Boubli, J. P., M. N. F. Da Silva, M. V. Amado, T. Hrbek, F. B. Pontual, & I. P. Farias. 2008. A taxonomic reassessment of Cacajao melanocephalus Humboldt (1811), with the description of two new species. International Journal of Primatology 29:723- 741. https://doi.org/10.1007/s10764-008-9248-7
Boubli, J. P., A. B. Rylands, I. P. Farias, M. E. Alfaro, & J. Lynch-Alfaro. 2012. Cebus Phylogenetic Relationships: A Preliminary Reassessment of the Diversity of the Untufted Capuchin Monkeys. American Journal of Primatology 74:381- 393. https://doi.org/10.1002/ajp.21998
Boubli J. P. et al. 2015. Spatial and temporal patterns of diversification on the Amazon: a test of the riverine hypothesis for all diurnal primates of Rio Negro and Rio Branco in Brazil. Molecular Phylogenetics and Evolution 82:400-412. https://doi.org/10.1016/j.ympev.2014.09.005
Boubli, J. P. et al. 2018. How many pygmy marmoset (Cebuella Gray, 1870) species are there? A taxonomic re-appraisal based on new molecular evidence. Molecular Phylogenetics and Evolution 120:170-182. https://doi.org/10.1016/j.ympev.2017.11.010
Boubli, J. P. et al. 2020. Sapajus apella. The IUCN Red List of Threatened Species 2020: e.T172351505A172353050. https://dx.doi.org/10.2305/IUCN.UK.2020-2.RLTS.T172351505A172353050.en. Downloaded on 22 November 2020. https://doi.org/10.2305/iucn.uk.2021-1.rlts.t172351505a192594550.en
Brumback, R. A. 1973. Two distinctive types of owl monkeys (Aotus). Journal of Medical Primatology 2:284-289. https://doi.org/10.1159/000460336
Brumback, R. A. 1974. A third species of the owl monkes (Aotus). Journal of Heredity 65:321-323. https://doi.org/10.1093/oxfordjournals.jhered.a108540
Brumback, R. A., R. D. Staton, S. A. Benjamin, & C. M. Land. 1971. The chromosomes of Aotus trivirgatus Humboldt, 1812. Folia Primatologica 15:264-273. https://doi.org/10.1159/000155384
Buckner, J. C., J. W. Lynch-Alfaro, A. B. Rylands, & M. E. Alfaro. 2015. Biogeography of the marmosets and tamarins (Callitrichidae). Molecular Phylogenetics and Evolution 82:413-425. https://doi.org/10.1016/j.ympev.2014.04.031
Bueno, M. L., C. Ramírez-Orjuela, M. Leibovici, & O. M. Torres. 2006. Información cariológica del género Callicebus. Revista Academia Colombiana de Ciencia 30:109-115.
Byrne, H. et al. 2016. Phylogenetic relationships of the New World titi monkeys (Callicebus): first appraisal of taxonomy based on molecular evidence. Frontiers in Zoology 13:10.
Byrne, H. et al. 2018. Titi monkey biogeography: Parallel Pleistocene spread by Plecturocebus and Cheracebus into a post-Pebas Western Amazon. Zoologica Scripta 47:499-517. https://doi.org/10.1111/zsc.12300
Byrne, H., A. B. Rylands, S. D. Nash, & J. P. Boubli. 2020. On the Taxonomic History and True Identity of the Collared Titi, Cheracebus torquatus (Hoffmannsegg, 1807) (Platyrrhini, Callicebinae). Primate Conservation 34:13-52.
Cabrera, A. 1957. Catalogo de los mamíferos de América del Sur. Revista del Museo Argentino de Ciencias Naturales “Bernardino Rivadavia” 4(1):1-307. https://doi.org/10.22179/revmacn.13.214
Cepeda-Duque, J. C., A. Link, & H. Mantilla-Meluk. 2018. Incertidumbre taxonómica de un primate neotropical; el caso de Ateles fusciceps rufiventris Sclater, 1871 (Primates: Atelidae). Mastozoología Neotropical 25:455-461. https://doi.org/10.31687/saremmn.18.25.2.0.21
Chiou, K. L., L. Pozzi, J. W. Lynch-Alfaro, & A. Di Fiore. 2011. Pleistocene diversification in living squirrel monkeys (Saimiri spp.) inferred from complete mitochondrial sequence. Molecular Phylogenetics and Evolution 59:736-745. https://doi.org/10.1016/j.ympev.2011.03.025
Collins, A. C., & J. M. Dubach. 2000. Phylogenetic relationships of spider monkeys (Ateles) based on mitochondrial DNA variation. International Journal of Primatology 21:381-420.
Cortés-Ortiz, L. et al. 2015. The taxonomy of howler monkeys: integrating old and new knowledge from morphological and genetic studies. Howler monkeys: adaptive radiation, systematics, and morphology (M. M. Kowalewski, P. A. Garber, L. Cortés-Ortiz, B. Urbani & D. Youlatos, eds.). Springer, New York. https://doi.org/10.1007/978-1-4939-1957-43
Costello, R. K., C. Dickinson, A. L. Rosenberger, S. Boinski, & F. S. Szala. 1993. Squirrel monkey (genus Saimiri) taxonomy: A multidisciplinary study of the biology of the species. Species, Species Concepts, and Primate Evolution (W. H. Kimbel, & L. B. Martin, eds.). New York: Plenum Press. https://doi.org/10.1007/978-1-4899-3745-2 8
Cracraft, J.1983. Species concepts and speciation analysis. Current ornithology (R. J. Johnston, ed.). Plenum Press, New York.
Cropp, J. S., A. Larson, & J. M. Cheverud. 1999. Historical biogeography of tamarins, genus Saguinus: the molecular phylogenetic evidence. American Journal of Physical Anthropology 108:65-89. https://doi.org/10.1002/(sici)1096-8644(199901)108:1<65:aid-ajpa4>3.0.co;2-4
Defler, T. R. 1994. La conservación de los primates colombianos. Trianea 5:255-287.
Defler, T. R. 2003. Primates de Colombia. Conservación Internacional Colombia.
Defler, T. R. 2010. Historia natural de los primates colombianos. Bogotá D.C, Colombia: Universidad Nacional de Colombia.
Defler, T. R. 2014 Colombian Lagothrix: Analysis of their phenotypes and taxonomy. The Woolly Monkey. Developments in Primatology: Progress and Prospects (T. Defler & P. Stevenson, eds.). Springer, New York, NY.
Defler, T. R. 2020. Taxonomía de los primates colombianos. Disponible en: http://www.thomasdefler.net
Defler, T. R., M. L. Bueno, & J. I. Hernández-Camacho. 2001. Taxonomic Status of Aotus hershkovitzi: Its Relationship to Aotus lemurinus. Neotropical Primates 9:37.
Defler, T. R., M. L. Bueno, & J. García.2010. Callicebus caquetensis: A New and Critically Endangered Titi Monkey from Southern Caquetá, Colombia. Primate Conservation 25(1)1-9. https://doi.org/10.1896/052.025.0101
Defler, T. R., & J. I. Hernández-Camacho. 2002. The true identity and characteristics of Simia albifrons Humboldt, 1812: Description of neotype. Neotropical Primates 10:1-16.
Defler, T. R., & M. L. Bueno. 2007. Aotus diversity and the species problem. Primate Conservation 22:55-70. https://doi.org/10.1896/052.022.0104
Díaz, A. C., J. Hernández-Camacho, & G. A. Cadena. 1986. Lista actualizada de los mamíferos de Colombia. Anotaciones sobre su distribución. Caldasia 15:71-75.
Doyle, E. D. et al. 2020. Molecular phylogenetic inference of the howler monkey radiation (Primates: Alouatta). Primates 62:177-188. https://doi.org/10.1007/s10329-020-00854-x
Egozcue, J. 1969. Primates. Comparative Mammalian Cytogenetics (K. Benirschke, ed.). Springer-Verlag, New York.
Elliot, D. G. 1913. A review of the primates. Monograph series, Vol. 2. American Museum of Natural History, New York.
Ferrari, S. F., P. G. Guedes, W. M. Figuereido-Ready, & A. A. Barnett. 2014. Reconsidering the taxonomy of the Black-Faced Uacaris, Cacajao melanocephalus group (Mammalia: Pitheciidae), from the northern Amazon Basin. Zootaxa 3866:353-370. https://doi.org/10.11646/zootaxa.3866.3.3
Figueiredo, W. B., J. M. Silva, J. M. Bates, M. L. Harada, & J. S. Silva Jr. 2006. Conservation genetics and biogeography of pitheciins. International Journal of Primatology 27(suppl. 1): Abstract #510.
Fooden, J. 1963. A revision of the woolly monkeys (genus Lagothrix). Journal of Mammalogy 44:213-247. https://doi.org/10.2307/1377454
Froehlich, J. W., J. Supriatna, & P. H. Froehlich. 1991. Morphometric analyses of Ateles: systematic and biogeographic implications. American Journal of Primatology 25:1-22. https://doi.org/10.1002/ajp.1350250102
Garbino, G. S. T. 2015. Defining genera of New World monkeys: the need for a critical view in a necessarily arbitrary task. International Journal of Primatology 36:1049-1064. https://doi.org/10.1007/s10764-015-9882-9
Garbino, G. S. T., & C. C. de Aquino. 2018. Evolutionary significance of the entepicondylar foramen of the humerus in New World monkeys (Platyrrhini). Journal of Mammalian Evolution 25:141-151. https://doi.org/10.1007/s10914-016-9366-5
Garbino, G. S. T., & A. M. Martins-Junior. 2018. Phenotypic evolution in marmoset and tamarin monkeys (Cebidae, Callitrichinae) and a revised genus-level classification. Molecular Phylogenetics and Evolution 118:156-171. https://doi.org/10.1016/j.ympev.2017.10.002
Garbino, G. S. T, D. M. Casali, F. O. Nascimento, & J. E. Serrano-Villavicencio. 2019. Taxonomy of the pygmy marmoset (Cebuella Gray, 1866): Geographic variation, species delimitation, and nomenclatural notes. Mammalian Biology 95:135-142. https://doi.org/10.1016/j.mambio.2018.09.003
García, V. J., A. Paéz, & E. Palacios.2017. Aportes al conocimiento de la distribución del mico Volador Pithecia milleri (Allen, 1914) en el occidente Amazónico colombiano. Neotropical Primates 23:59-66.
GBIF.Org. 2021. GBIF Occurrence Download https://doi.org/10.15468/dl.vr97ad
Geoffroy-Saint Hilaire, I. 1844. Archives du Muséum d’Histoire Naturelle vol. 4, p.24, pl.2.
Goodman, M., et al. 1998. Toward a phylogenetic classification of primates based on DNA evidence complemented by fossil evidence. Molecular Phylogenetics and Evolution 9:585–598. https://doi.org/10.1006/mpev.1998.0495
Groves, C. P. 2001. Primate taxonomy. Smithsonian Institution Press, Washington, DC.
Groves, C. P. 2005. Order Primates. In: Mammal Species of the World (D. E. Wilson & D. M. Reeder, eds.). The Johns Hopkins University Press, Baltimore.
Groves, C. P. 2006. The primates Mammal species of the world: A taxonomic and geographic reference (D. E. Wilson & D. M. Reeder, eds.). 2006. Baltimore: The Johns Hopkins University Press.
Gusmão, A. C., & M. Santos-Silva. 2015. Ocorrência de parauacú Pithecia cf. mittermeieri Marsh, 2014 (Primates, Platyrrhini) na transição entre os biomas Pantanal, Amazônia e Cerrado, Mato Grosso, Brasil. Neotropical Primates 22:47-49.
Gutiérrez, E. E., & J. Marinho-Filho. 2017. The mammalian faunas endemic to the Cerrado and the Caatinga. ZooKeys 644:105-157. https://doi.org/10.3897/zookeys.644.10827.figure1
Guzmán-Caro, D. C., S. A. Vargas, S. Cárdenas, J. S. Castro, & P. R. Stevenson. 2018. Estudio y conservación de primates en Colombia: Avances, retos y el papel del Sistema de Parques Nacionales Naturales. La Primatología en Latinoamérica 2 - A primatologia na America Latina 2 (Tomo I) Argentina-Colombia (B. Urbani, M. Kowaleski, R. G. T. da Cunha, S. de la Torre & L. Cortés-Ortiz, eds.). Caracas, Venezuela: Ediciones IVIC. Instituto Venezolano de Investigaciones Científicas (IVIC). https://doi.org/10.22209/ic.v60n4a01
Hall, E. R. 1943. Criteria for vertebrate subspecies, species and genera: the mammals. Annals of the New York Academy of Sciences 44:141-144. https://doi.org/10.1111/j.17496632.1943.tb31300.x
Henao-Díaz, F. et al. 2020. Atlas de la biodiversidad de Colombia. Primates. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt. Bogotá D. C., Colombia. https://doi.org/10.21068/d100818oc
Hernández-Camacho, J., & R. W. Cooper. 1976. The nonhuman primates of Colombia. Neotropical Primates: Field Studies and Conservation (R. W. Thorington Jr. & P. G. Heltne, eds.). National Academy of Sciences, Washington D. C.
Hernández-Camacho, J., & T. R. Defler. 1989. Algunos aspectos de la conservación de primates no humanos en Colombia. La primatología en Latinoamérica, Anales del Simposio de Primatología del IX Congreso Latinoamericano de Zoologia, 9-5 Octubre 1983 (C. R. Saavedra, R. A. Mittermeier & I. Bastos Santos, eds.). Washington: World Wildlife Foundation. https://doi.org/10.5209/revcmpl.2012.v23.n1.39528
Hershkovitz, P. 1949. Mammals of northern Colombia: Preliminary report No. 4: Monkeys (Primates), with taxonomic revisions of some forms. Proceedings of the United States National Museum 98:323-427. https://doi.org/10.5479/si.00963801.98-3232.323
Hershkovitz, P. 1955. Notes on American monkeys of the genus Cebus. Journal of Mammalogy 36:449-452. https://doi.org/10.2307/1375688
Hershkovitz, P. 1977. Living New World monkeys (Platyrrhini) with an introduction to primates, vol 1. Chicago University Press, Chicago.
Hershkovitz, P. 1979. The species of sakis, genus Pithecia (Cebidae, Primates), with notes on sexual dichromatism. Folia Primatologica 31:1-22. https://doi.org/10.1159/000155871
Hershkovitz, P. 1982. Subspecies and geographic distribution of black-mantle tamarins Saguinus nigricollis Spix (Primates: Callitrichidae). Proceedings of the Biological Society of Washington 95:647-656.
Hershkovitz, P. 1983. Two new species of night monkeys, genus Aotus (Cebidae, Platyrrhini): a preliminary report on Aotus taxonomy. American Journal of Primatology 4:209-243. https://doi.org/10.1002/ajp.1350040302
Hershkovitz, P.1984. Taxonomy of squirrel monkeys genus Saimiri (Cebidae, Platyrrhini): a preliminary report with description of a hitherto unnamed form. American Journal of Primatology 7:155-210. https://doi.org/10.1002/ajp.1350070212
Hershkovitz, P. 1987a. The taxonomy of South American sakis, genus Pithecia (Cebidae, Platyrrhini): a preliminary report and critical review with the description of a new species and a new subspecies. American Journal of Primatology 12:387-468. https://doi.org/10.1002/ajp.1350120402
Hershkovitz, P. 1987b. Uacaries, new world monkeys of the genus Cacajao (Cebidae, Platyrrhini): a preliminary taxonomic review with the description of a new subspecies. American Journal of Primatology 12:1-53. https://doi.org/10.1002/ajp.1350120102
Hershkovitz, P. 1988. Origin, speciation, and distribution of South American titi monkeys, genus Callicebus (Family Cebidae, Platyrrhini). Proceedings of the Academy of Natural Sciences of Philadelphia 140:240-272. https://doi.org/10.5962/bhl.title.2843
Hershkovitz, P. 1990. Titis, new world monkeys of the genus Callicebus (Cebidae, Platyrrhini): a preliminary taxonomic review. Fieldiana, Zool. New Series, Field Museum of Natural History, Chicago. https://doi.org/10.5962/bhl.title.2843
Hill, W. C. O. 1960. Primates: comparative anatomy and taxonomy. Cebidae, Part A. Edinburgh: Edinburgh University Press. https://doi.org/10.1016/0160-9327(61)90022-9
Hill, W. C. O. 1962. Primates comparative anatomy and taxonomy Cebidae Part B. Edinburgh University Press, Edinburgh. https://doi.org/10.1016/0160-9327(63)90039-5
ICZN. 1999. International Code of Zoological Nomenclature. 4ta ed. Londres: The International Trust for Zoological Nomenclature. https://doi.org/10.5962/bhl.title.50608
IGUN, Fonam, Sinchi, Corpoamazonía. 2012. Informe final: Convenio de cooperación científica y tecnológica No. 10F del 15 de diciembre de 2011 entre el Fondo Nacional Ambienal - FONAM, la Universidad Nacional de Colombia - Instituto de Genética, el Instituto Amazónico de Investigaciones Científicas - SINCHI y la Corporación para el Desarrollo Sostenible del Sur de la Amazonía - CORPOAMAZONÍA. https://doi.org/10.3989/ic.1984.v35.i358.1933
Izawa, K.1975. Foods and feeding behavior of monkeys in the upper Amazon basin. Primates 16:295-316. https://doi.org/10.1007/bf02381557
Jacobs, S. C., A. Larson, & J. M. Cheverud. 1999. Historical biogeography of tamarins, genus Saguinus: the molecular phylogenetic evidence. American Journal of Physical Anthropology 108:65-89. https://doi.org/10.1002/(sici)1096-8644(199901)108:1<65:aid-ajpa4>3.0.co;2-4
Kellogg, R., & E. A. Goldman. 1944. Review of the spider monkeys. Proceedings of the United States National Museum 96:1-45. https://doi.org/10.5479/si.00963801.96-3186.1
Kobayashi, S. 1995. A phylogenetic study of titi monkeys, genus Callicebus, based on cranial measurements: I. Phyletic groups of Callicebus . Primates 36:101-120. https://doi.org/10.1007/bf02381918
Lavergne, A. et al. 2010. Phylogeny and phylogeography of squirrel monkeys (Genus Saimiri) based on cytochrome b genetic analysis. American Journal of Primatology: 72:242-253. https://doi.org/10.1002/ajp.20773
Lawrence, B. 1933. Howler monkeys of the palliata group. Bulletin of the Museum of Comparative Zoology at Harvard College LXXV 8:315-354.
Lima, M. G. et al. 2017. Capuchin monkey biogeography: understanding Sapajus Pleistocene range expansion and the current sympatry between Cebus and Sapajus. Journal of Biogeography 44:810-820. https://doi.org/10.1111/jbi.12945
Lima, M. G. et al. 2018. A phylogenomic perspective on the robust capuchin monkey (Sapajus) radiation: First evidence for extensive population admixture across South America. Molecular Phylogenetics and Evolution 124:137-150. https://doi.org/10.1016/j.ympev.2018.02.023
Link, A., L. M. Valencia, L. N. Céspedes, L. D. Duque, C. D. Cadena, & A. Di Fiore. 2015. Phylogeography of the critically endangered brown spider monkey (Ateles hybridus): Testing the riverine barrier hypothesis. International Journal of Primatology 36:530-547. https://doi.org/10.1007/s10764-015-9840-6
Lynch-Alfaro, J. W. et al. 2012a. Explosive Pleistocene range expansion leads to widespread Amazonian sympatry between robust and gracile capuchin monkeys. Journal of Biogeography 39:272-288. https://doi.org/10.1111/j.1365-2699.2011.02609.x
Lynch-Alfaro, J. W., J. D. S. E. Silva Jr., & A. B. Rylands. 2012b. How different are robust and gracile capuchin monkeys? An argument for the use of Sapajus and Cebus. American Journal of Primatology 74:273-286. https://doi.org/10.1002/ajp.22007
Lynch-Alfaro, J. W. et al.2015. Biogeography of squirrel monkeys (genus Saimiri): South-central Amazon origin and rapid pan-Amazonian diversification of a lowland primate. Molecular Phylogenetics and Evolution 82:436-454. https://doi.org/10.1016/j.ympev.2014.09.004
Ma, N. S. F., T. C. Jones, A. Miller, L. Morgan, & E. Adams. 1976a. Chromosome polymorphism and banding patterns in the owl monkey (Aotus). Laboratory Animal Science 26:1022-1036.
Ma, N. S. F., M. W. Elliott, L. M. Morgan, A. C. Miller, & T. C. Jones. 1976b. Translocation of Y chromosome to an autosome in the Bolivian owl monkey, Aotus. American Journal of Physical Anthropology 45:191-202. https://doi.org/10.1002/ajpa.1330450205
Ma, N. S. F., T. C. Jones, M. T. Bedard, A. C. Miller, L. M. Morgan, & E. A. Adams. 1977. The chromosome complement of an Aotus hybrid. Journal of Heredity 68:409-412.
Ma, N. S. F., R. N. Rossan, S. T. Kelley, J. S. Harper, M. T. Bedard, & T. C. Jones.1978. Banding patterns of the chromosomes of two new karyotypes of the owl monkey, Aotus, captured in Panama. Journal of Medical Primatology 7:146-155. https://doi.org/10.1159/000459804
Ma, N. S. F., D. M. Renquist, R. Hall, P. K. Sehgal, T. Simeone, & T. C. Jones. 1980. XX/“XO” sex determination system in a population of Peruvian owl monkeys, Aotus. Journal of Heredity 71:336-342. https://doi.org/10.1093/oxfordjournals.jhered.a109382
Mantilla-Meluk, H. 2013. Subspecific variation: an alternative biogeographic hypothesis explaining variation in coat color and cranial morphology in Lagothrix lugens (Primates: Atelidae). Primate Conservation 26:33-48. https://doi.org/10.1896/052.026.0102
Mantilla-Meluk, H., A. Cadena, & A. M. Jiménez-Ortega. 2014. Historia de la mastozoología en Colombia: Pasado, presente y perspectivas. Historia de la mastozoología en Latinoamérica, las Guayanas y el Caribe. Quito y México, DF: Editorial Murciélago Blanco y Asociación Ecuatoriana de Mastozoología 153-174. https://doi.org/10.22201/ie.20074484e.2011.1.1.12
Marsh, L. K. 2014. A taxonomic revision of the saki monkeys, Pithecia Desmarest, 1804. Neotropical Primates 21:1-165. https://doi.org/10.1896/044.021.0101
Matauschek, C., C. Roos, & E. W. Heymann. 2011. Mitochondrial phylogeny of tamarins (Saguinus, Hoffmannsegg 1807) with taxonomic and biogeographic implications for the S. nigricollis species group. American Journal of Physical Anthropology 144:564-574. https://doi.org/10.1002/ajpa.21445
Mayr, E. 1942. Systematics and the Origin of Species. Columbia University Press. New York, USA. Pp. 1-334.
Mayr, E. 1943. Criteria of subspecies, species and genera in ornithology. Annals of the New York Academy of Sciences 44:133-139. https://doi.org/10.1111/j.1749-6632.1943.tb31299.x
Mayr, E. 1948. The bearing of the new systematics on genetical problems the nature of species. Advances in genetics 2: 205-237. https://doi.org/10.1016/s0065-2660(08)60469-1
Mayr, E. 1996. What is a species, and what is not? Philosophy of Science 63:262-277.
Moore, A. J., & J. M. Cheverud. 1992. Systematics of the Saguinus oedipus group of the bare-face tamarins: evidence from facial morphology. American Journal of Physical Anthropology 89:73- 84. https://doi.org/10.1002/ajpa.1330890107
Pacheco, V. et al. 2020. Diversidad y distribución de los mamíferos del Perú I: Didelphimorphia, Paucituberculata, Sirenia, Cingulata, Pilosa, Primates, Lagomorpha, Eulipotyphla, Carnivora, Perissodactyla y Artiodactyla. Revista Peruana de Biología 27:289-328. https://doi.org/10.15381/rpb.v27i3.18356
Patterson, B. D. 1987. A biographical sketch of Philip Hershkovitz, with a complete scientific bibliography. Fieldiana Zoology 39:1-10.
Porter, C. A., J. Czelusniak, H. Schneider, M. P. C. Schneider, I., Sampaio, & M. Goodman. 1997. Sequences of the primate epsilon-globin gene: Implications for systematics of the marmosets and other New World primates. Gene 205:59-71. https://doi.org/10.1016/s0378-1119(97)00473-3
Von Pusch, B. 1941. Die Arten der Gattung Cebus. Zeitschrift fur Suaugetierkunde 16:183-237.
Quintela, F., C. A. Da Rosa, & A. Feijó. Updated And Annotated Checklist Of Recent Mammals From Brazil. Anais Da Academia Brasileira De Ciencias 2020. https://doi.org/10.1590/0001-3765202020191004
Ramírez-Chaves, H. E. 2011. Especímenes tipo de mamíferos en la colección del Instituto de Ciencias Naturales, Universidad Nacional de Colombia. Acta Biológica Colombiana 16:281-292. https://doi.org/10.47603/mano.v6n2.199
Ramírez-Chaves, H. E., A. F. Suárez-Castro, & J. F. González-Maya. 2016. Cambios recientes a la lista de los mamíferos de Colombia. Mammalogy Notes 3:1-9. https://doi.org/10.47603/manovol3n1.1-9
Ramírez-Chaves, H. E. et al. 2020. New records and confirmation of the presence of three species of primates (Mammalia, Primates) in southwestern Colombia. Check List 16:811. https://doi.org/10.15560/16.4.811
Rosenberger, A. L.1981. Systematics: The higher taxa. Ecology and Behavior of Neotropical Primates, Vol. 1 (A. F. Coimbra-Filho & R. A. Mittermeier, eds.). Rio de Janeiro: Academia Brasileira de Ciências. https://doi.org/10.1017/s0030605300017877
Rosenberger, A. L. 2012. New World monkey nightmares: science, art, use, and abuse (?) in platyrrhine taxonomic nomenclature. American Journal of Primatology 74:692-695. https://doi.org/10.1002/ajp.22037
Ruiz-García, M. et al. 2010. Molecular phylogenetics and phylogeography of the white-fronted capuchin (Cebus albifrons; Cebidae, Primates) by means of mtCOII gene sequences. Molecular Phylogenetics and Evolution 57:1049-1061. https://doi.org/10.1016/j.ympev.2010.09.002
Ruiz-García, M. & M. O. Pinedo-Castro. 2010. Molecular systematics and phylogeography of the genus Lagothrix (Atelidae, Primates) by means of the mitochondrial COII gene. Folia Primatologica 81:109-128. https://doi.org/10.1159/000315070
Ruiz-García, M. et al. 2011. Molecular phylogenetics of Aotus (Platyrrhini, Cebidae). International Journal of Primatology 32:1218.
Ruiz-García, M. et al.2012a. Molecular systematics and phylogeography of Cebus capucinus (Cebidae, Primates) in Colombia and Costa Rica by means of the mitochondrial COII gene. American Journal of Primatology 74:366-380. https://doi.org/10.1002/ajp.20940
Ruiz-García, M., M. I. Castillo, N. Lichilin-Ortiz, & M. Pinedo-Castro. 2012b. Molecular relationships and classification of several Tufted Capuchin lineages (Cebus apella, Cebus xanthosternos and Cebus nigritus, Cebidae), by means of mitochondrial cytochrome oxidase ii gene sequences. Folia Primatologica 83:100-125. https://doi.org/10.1159/000342832
Ruiz-García, M., M. Pinedo-Castro, & J. M. Shostell. 2014. How many genera and species of woolly monkeys (Atelidae, Platyrrhine, Primates) are there? The first molecular analysis of Lagothrix flavicauda, an endemic Peruvian primate species. Molecular Phylogenetics and Evolution 79:179-198. https://doi.org/10.1016/j.ympev.2014.05.034
Ruiz-García, M., K. Luengas-Villamil, N. Leguizamon, B. De Thoisy, & H. Gálvez. 2015. Molecular phylogenetics and phylogeography of all the Saimiri taxa (Cebidae, Primates) inferred from mt COI and COII gene sequences. Primates 56:145-161. https://doi.org/10.1007/s10329-014-0452-0
Ruiz-García, M., M. I. Castillo, & K. Luengas-Villamil. 2016. It is misleading to use Sapajus (robust capuchins) as a genus? A review of the evolution of the capuchins and suggestions on their systematics. Phylogeny, Molecular Population Genetics, Evolutionary Biology and Conservation of the Neotropical Primates (M. Ruiz-García & J. M. Shostell, eds.). Nova Science Publisher Inc., New York, USA.
Ruiz-Herrera, A., F, García, M. Aguilera, M. Garcia, & M. Ponsá. 2005. Comparative chromosome painting in Aotus reveals a highly derived evolution. American Journal of Primatology 65:73-85. https://doi.org/10.1002/ajp.20098
Rylands, A. B., H. Schneider, A. Langguth, R. A. Mittermeier, C. P. Groves, & E. Rodriguez-Luna. 2000. An assessment of the diversity of New World primates. Neotropical Primates 8:61-93.
Rylands, A. B., C. P. Groves, R. A. Mittermeier, L. Cortés-Ortiz, & J. J. Hines. 2006. Taxonomy and distributions of Mesoamerican primates. New perspectives in the study of Mesoamerican primates (A. Estrada, P. A. Garber, M. M. Pavelka & L. Luecke, eds.). Springer, United States. https://doi.org/10.1007/0-387-25872-83
Rylands, A. B., & R. A. Mittermeier. 2009. The diversity of the New World primates (Platyrrhini): an annotated taxonomy. South American Primates: Comparative Perspectives in the Study of Behavior, Ecology, and Conservation (Developments in Primatology: Progress and Prospects) (P. A. Garber, A. Estrada, J. C. Bicca-Marques, E. W. Heymann & K. B. Strier, eds.). Springer, New York, NY. https://doi.org/10.1007/978-0-387-78705-32
Rylands, A. B., A. F. Coimbra-Filho, & R. A. Mittermeier. 2009. The systematics and distributions of the marmosets (Callithrix, Callibella, Cebuella, and Mico) and callimico (Callimico) (Callitrichidae, Primates). The smallest anthropoids (S. M. Ford, L. M. Porter & L. C. Davis, eds.). Springer, Boston, MA. https://doi.org/10.1007/978-1-4419-0293-12
Rylands, A. B., R. A. Mittermeier, & J. S. Silva Jr. 2012. Neotropical primates: taxonomy and recently described species and subspecies. International Zoo Yearbook 46:11-24. https://doi.org/10.1111/j.1748-1090.2011.00152.x
Rylands, A. B. 2013. Handbook of the mammals of the world. Primates, Vol. 3 (R. A. Mittermeier, A. B. Rylands & D. E. Wilson, eds.). Barcelona: Lynx Edicions.
Rylands, A. B., R. A. Mittermeier, B. M. Bezerra, F. P. Paim, & H. L. Queiroz. 2013. Species accounts of Cebidae. Handbook of the Mammals of the World, vol. 3. Primates (R. A. Mittermeier, A. B. Rylands & D. E. Wilson, eds.). Lynx Edicions, Barcelona. https://doi.org/10.1644/14-mamm-r-059
Rylands, A. B. et al. 2016. Taxonomic review of the New World tamarins (primates: Callitrichidae). Zoological Journal of the Linnean Society 177:1003-1028. https://doi.org/10.1111/zoj.12386
Sánchez, H. J., & D. Lew. 2012. Lista actualizada y comentada de los mamíferos de Venezuela. Memoria de la Fundación La Salle de Ciencias Naturales 173:173-238.
Serrano-Villavicencio, J. E., R. L. Vendramel, & G. S. T. Garbino. 2017. Species, subspecies, or color morphs? Reconsidering the taxonomy of Callicebus Thomas, 1903 in the Purus–Madeira interfluvium. Primates 58:159-167. https://doi.org/10.1007/s10329-016-0555-x
Serrano-Villavicencio, J. E., C. M. Hurtado, R. L. Vendramel, & F. O. D. Nascimento. 2019. Reconsidering the taxonomy of the Pithecia irrorata species group (Primates: Pitheciidae). Journal of Mammalogy 100:130-141. https://doi.org/10.1093/jmammal/gyy167
Simpson, G. G. 1943. Criteria for genera, species, and subspecies in zoology and paleozoology. Annals of the New York Academy of Sciences 44:145-178. https://doi.org/10.1111/j.1749-6632.1943.tb31 301.x
Solari, S., Y. Muñoz-Saba, J. V Rodríguez-Mahecha, T. R. Defler, H. E. Ramírez-Chaves, & F. Trujillo. 2013. Riqueza, endemismo y conservación de los mamíferos de Colombia. Mastozoología Neotropical 20:301-365.
Stanyon, R., S. Tofanelli, M. A. Morescalchi, G. Agoramoorthy, O. A. Ryder, & J. Wienberg. 1995. Cytogenetic analysis shows extensive genomic rearrangements between red howler (Alouatta seniculus, Linnaeus) subspecies. American Journal of Primatology 35:171-183. https://doi.org/10.1002/ajp.1350350302
Stanyon, R., C. R. Bonvicino, M. Svartman, & H. N. Seuánez. 2003. Chromosome painting in Callicebus lugens, the species with the lowest diploid number (2n= 16) known in primates. Chromosoma 112:201-206. https://doi.org/10.1007/s00412-003-0261-5
Stevenson, P. R., D. C. Guzmán, & T. R. Defler.2010. Conservation of Colombian primates: an analysis of published research. Tropical Conservation Science 3:45-62. https://doi.org/10.1177/194008291000300105
Tagliaro, C. H, M. P. C. Schneider, H. Schneider, I. C. Sampaio, & M. J. Stanhope. 1997. Marmoset phylogenetics, conservation perspectives, and evolution of the mtDNA control region. Molecular Biology and Evolution 14:674-684. https://doi.org/10.1093/oxfordjournals.molbev.a025807
Teta, P. 2019. The usage of subgenera in mammalian taxonomy. Mammalia 83:209-211. https://doi.org/10.1515/mammalia-2018-0059
Tirira, D. G., J. Brito, S. F. Burneo, & Comisión de Diversidad de la Aem. 2020. Mamíferos del Ecuador: lista actualizada de especies Mammals of Ecuador: Updated checklist species. Versión 2020.2. Asociación Ecuatoriana de Mastozoología. Quito. https://aem.mamiferosdelecuador.com(actualización:2020-12-11)
Thorington Jr., R. W. 1985. The taxonomy and distribution of squirrel monkeys (Saimiri). Handbook of Squirrel Monkey Research (L. A. Rosenblum & C. L. Coe, eds.). New York: Plenum Press. https://doi.org/10.1007/978-1-4757-0812-71
Torres, O. M., S. Enciso, F. Ruiz, E. Silva, & I. Yunis. 1998. Chromosome diversity of the genus Aotus from Colombia. American Journal of Primatology 44:255-275.
Urbani, B., J. Boubli, & L. Cortes-Ortíz. 2018. Alouatta arctoidea. The IUCN Red List of Threatened Species 2018: e.T136486A17926227. Downloaded on 12 December 2020. https://doi.org/10.2305/iucn.uk.2018-2.rlts.t136486a17926227.en
Van Roosmalen, M. G. M., & T. Van Roosmalen. 1997. An eastern extension of the geographical range of the pygmy marmoset, Cebuella pygmaea. Neotropical Primates 5: 3-6.
Van Roosmalen, M. G. M., T. Van Roosmalen, & R. A. Mittermeier. 2002. A taxonomic review of the titi monkeys, genus Callicebus Thomas, 1903, with the description of two new species, Callicebus bernhardi and Callicebus stephennashi, from Brazilian Amazonia. Neotropical Primates 10(supplement):1-52. https://doi.org/10.1896/044.014.0201
Información adicional
Editor asociado: Dr. David Alfredo Flores
Citar como: García-Restrepo, S., S. O. Montilla 2021. Taxonomía de los primates de Colombia: cambios en los últimos veinte años (2000-2019) y anotaciones sobre localidades tipo. Mastozoología Neotropical, 28(2):e0584. https://doi.org/10.31687/saremMN.21.28.2.0.05.e0584
