ARTÍCULO
USO DE DOS MARCAS TEMPORALES EN DOS ESPECIES DE MURCIÉLAGOS: MYOTIS CHILOENSIS (CHIROPTERA: VESPERTILIONIDAE) Y TADARIDA BRASILIENSIS (CHIROPTERA: MOLOSSIDAE)
TEMPORARY MARKING OF TWO SPECIES OF BATS: MYOTIS CHILOENSIS (CHIROPTERA: VESPERTILIONIDAE) AND TADARIDA BRASILIENSIS (CHIROPTERA: MOLOSSIDAE)
USO DE DOS MARCAS TEMPORALES EN DOS ESPECIES DE MURCIÉLAGOS: MYOTIS CHILOENSIS (CHIROPTERA: VESPERTILIONIDAE) Y TADARIDA BRASILIENSIS (CHIROPTERA: MOLOSSIDAE)
Mastozoología Neotropical, vol. 28, núm. 2, p. 618, 2021
Sociedad Argentina para el Estudio de los Mamíferos
Recepción: 09 Junio 2021
Aprobación: 11 Noviembre 2021
Resumen: El uso de marcas inadecuadas en murciélagos ha sido frecuente y la aplicación de marcas no permanentes ha sido escasa. Medimos la permanencia de dos marcas temporales (perforación del patagio y tintura de pelo) en dos especies de murciélagos de pequeño tamaño en la zona mediterránea de Chile central. Ambas marcas presentaron similares resultados en tiempo de duración (40-42 días), aunque la perforación del patagio tuvo mayor duración en una mayor proporción de individuos marcados en ambas especies de murciélagos. Los resultados de nuestro estudio aportan a la identificación de técnicas apropiadas para el monitoreo y seguimiento poblacional de murciélagos.
Palabras clave: Chile central, perforación del patagio, semiárido, tintura de pelo, zona mediterránea.
Abstract: The selection of inappropriate marking methods for bats has been a common issue, and the use of non-permanent tags has been scarce. We measure the permanence of two temporary marks (patagium piercing and hair dyeing) in two species of small bats in the Mediterranean-climate area of central Chile. Both methods exhibited similar maximum duration (40-42 days), however, the patagium perforation lasted longer in a greater proportion of individuals than the hair dyeing for both bat species. Our results contribute to the identification of appropriate techniques for the monitoring and tracking of bat populations.
Keywords: Central Chile, hair dye, patagian piercing, semiarid, Mediterranean-climate zone.
El marcaje es una técnica utilizada en ecología de vida silvestre que permite el seguimiento de individuos (Braun 2005), además de evaluar parámetros poblacionales en el corto y largo plazo (Ellison et al. 2007). Por ejemplo, el método de marcaje y recaptura es comúnmente utilizado para estimar el tamaño de poblaciones animales (Braun 2005). No obstante, un inadecuado procedimiento de marcaje o el uso de materiales incorrectos pueden provocar lesiones e incluso la muerte de los individuos marcados (CCAC 2003). Para evitar dañar a los animales es necesaria evidencia que permita identificar las herramientas y metodologías apropiadas para el marcaje animal.
En murciélagos es frecuente el uso de métodos de marcaje inadecuados, cuya aplicación causa lesiones en los individuos (Rodríguez-Posada & Santa-Sepúlveda 2013). Por ejemplo, los anillos para aves fueron el método más común de marcaje en murciélagos durante el siglo pasado. Sin embargo, su uso evidenció irritación, desgarros, heridas e infecciones evidentes (Baker et al. 2001; O’Shea et al. 2004; Dietz et al. 2006). Actualmente, la inserción sub-dérmica de transpondedores integrados pasivos (PIT tag, por sus siglas en inglés) es de uso frecuente como marca permanente en murciélagos (e.g., Rigby et al. 2012; Van Harten 2019).
Las marcas temporales son una alternativa menos invasiva a las marcas permanentes, permitiendo la evaluación de parámetros poblacionales durante un período acotado de tiempo (Bonaccorso et al. 1976). El corte de pelo en pequeñas porciones del cuerpo se utiliza en pequeños mamíferos (Department of Environment and Conservation 2013). Sin embargo, en murciélagos el pelo puede ser especialmente importante para el mantenimiento de la temperatura (Canals & Cattan 2008), por lo que usar este tipo de marca podría ser perjudicial. El uso de tinturas también ha sido un método común de marcaje en especies de pequeños mamíferos (Department of Environment and Conservation 2013; Sack & Tripp 2020), sin embargo, en murciélagos son escasas sus aplicaciones (e.g., Montenegro & Romero-Ruz 1999; Sherwin et al. 2002).
La perforación del patagio se ha implementado como método de identificación individual (Faure et al. 2014). Aunque el uso de este método no ha sido frecuente en estudios de murciélagos, se recomienda para estudios de corto plazo (Barclay & Bell 1988). Bonaccorso & Smythe (1972) describen que esta marca temporal cicatriza en un período de alrededor de 10 días en Artibeus jamaicensis (Chiroptera: Phyllostomidae) y Saccopteryx bilineata (Chiroptera: Emballonuridae), dejando una pequeña cicatriz blanca que evidencia la secuencia de perforaciones que se hicieron días atrás.
Nuestro trabajo tiene como objetivo determinar la duración de dos marcas temporales (perforación del patagio y tintura de pelo) en dos especies de murciélagos de pequeño tamaño. Identificar una técnica de marcaje temporal efectiva aportará una herramienta útil para estimar el tamaño de las poblaciones de murciélagos y realizar estudios ecológicos a corto plazo.
Este estudio se realizó en el Parque Etnobotánico Quilapilún (33° 5’ 30.62” Sur, 70° 43’ 52.82” Oeste), ubicado en la Región Metropolitana a 30 kilómetros al norte de la ciudad de Santiago de Chile (Fig. 1). En este sitio existe una colonia mixta de las especies de murciélagos Myotis chiloensis (Vespertilionidae; 6-10 g) y Tadarida brasiliensis (Molossidae; 9-15 g) (Manque Bioexploraciones 2018). El área de estudio es parte de la Región del Matorral y del Bosque Esclerófilo (Gajardo 1994). El régimen climático del área es de tipo mediterráneo con una temperatura media anual de 13.9 ºC, con una máxima media de 29 ºC en el mes más cálido (enero) y una mínima de 2.8 ºC en el mes más frío (julio). Las precipitaciones se concentran en los meses de invierno y presentan una media anual de 380 mm (CGA 2015).
Para la captura y recaptura de individuos realizamos seis campañas de uno o dos días durante la estación estival (del 12 de enero al 4 de marzo de 2019), con un intervalo de ca. 10 días entre campañas. Para las capturas utilizamos 4 redes niebla (dos de 10 x 2.5 m, una de 6 x 2.5 m y una de 3 x 2.5 m) y 1 trampa arpa (de 4 x 2 m), que se activaron alrededor de las 20:00 h y se mantuvieron activas hasta las 03:00 h, con una revisión cada 20 minutos. Para manipular a los ejemplares seguimos el protocolo de bioseguridad establecido por el “Manual para el Monitoreo de Fauna Silvestre en Chile” (De La Maza & Bonacic 2013), incluyendo además la inmunización antirrábica de las personas que realizaron las actividades de captura y manipulación. Para la identificación de la especie usamos las descripciones de Rodríguez-San Pedro et al. (2014).
Para el marcaje de los individuos utilizamos dos marcas temporales: perforación del patagio y tintura de pelo. La perforación del patagio consistió en realizar pequeños orificios con una aguja de disección en la zona media inferior del patagio (Fig. 2A y 2C), realizando una secuencia única con un máximo de 10 perforaciones por ala, dispuestas en dos líneas paralelas de cinco perforaciones. Los códigos generados permitieron identificar a los animales a nivel individual. Para el marcaje con tintura de pelo utilizamos color naranjo marca L’Oreal® Colorista Washout, gel lavable y sin amoníaco (a diferencia de las tinturas permanentes) que no debería perjudicar la piel de los animales y cuya duración reportada por el fabricante es de 2 a 4 semanas. Esta tintura se aplicó con un guante de látex sobre la espalda desde el cuello hacia la zona lumbar (Fig. 2B y 2D). Si bien este método no permite una identificación a nivel individual, con el uso de distintos colores se podría determinar movimientos entre sitios de descanso o dispersión, entre otros.
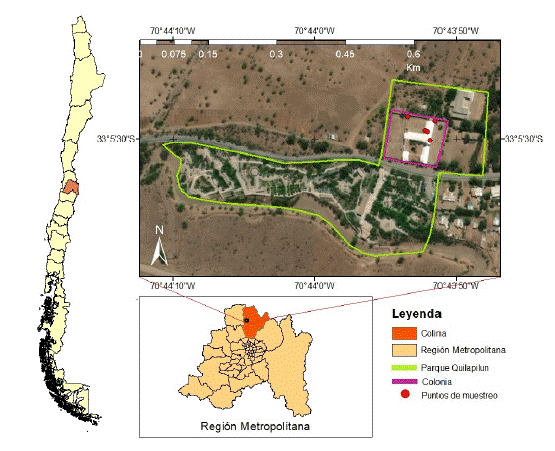
Fig. 1
Sitios de captura dentro del Parque Quilapilún, comuna de Colina, Región Metropolitana, Chile central.
Para evaluar la duración de las marcas, todos los individuos capturados en las primeras dos campañas fueron marcados con ambos métodos (perforación del patagio y tintura de pelo). Adicionalmente, como parte de un estudio de largo plazo, a estos individuos se les implantó un PIT tag (Biomark, Inc., modelo MiniHPT8, 8 mm, 30 mg), que permitió su identificación luego de que las marcas temporales no fueron visibles. Una vez marcados fueron liberados en el sitio de captura.
Durante las siguientes campañas registramos el número de individuos recapturados en los que fue visible cada tipo de marca temporal. Así, para cada marca en cada campaña se comparó el porcentaje de permanencia de la marca (número de individuos recapturados en que la marca fue visible/total de individuos recapturados que fueron marcados inicialmente). El porcentaje de permanencia de cada marca por campaña se graficó respecto a los días desde el marcaje inicial.
Capturamos y marcamos inicialmente un total de 102 individuos, correspondiendo 61 a Myotis chiloensis y 41 a Tadarida brasiliensis, con un total de 40 y 33 recapturas, respectivamente. La perforación del patagio y tintura de pelo en ambas especies de murciélagos no fueron visibles pasado los 50 días desde que el ejemplar fue marcado. La duración máxima en que se pudo observar ambas marcas fue de 42 días.
La perforación del patagio en ambas especies fue visible en un 100% de los individuos hasta los 42 días, mientras que la duración de la tintura de pelo varió por especie. En Myotis chiloensis se pudo ver en un 100% de los individuos recapturados hasta 30-32 días desde el marcaje original, pero en el intervalo de 40-42 días solo se pudo ver en el 50% de los individuos recapturados (Fig. 3A). En Tadarida brasiliensis la tintura de pelo fue visible en el 100% de los individuos recapturados hasta el intervalo de 20-22 días, luego bajó a 87.5% en el intervalo de 30- 32 días, y solo fue visible en un 25% de los individuos recapturados en el intervalo de 40-42 días (Fig. 3B). Esta diferencia entre especies podría deberse a características propias del pelaje (e.g., Fraser et al. 2013) o al acicalamiento de los individuos (e.g., Richards & Hall 2012).
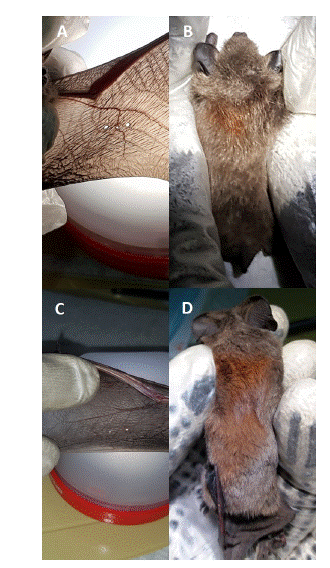
Fig. 2
Marcas temporales de Myotis chiloensis: (A) perforación del patagio (inicial) y (B) tintura de pelo (segunda recaptura); y Tadarida brasiliensis: (C) perforación del patagio (primera recaptura) y (D) tintura de pelo (inicial).
Nuestros resultados proveen evidencia sobre la permanencia de dos marcas temporales, en dos especies de murciélagos de tamaño pequeño en la zona mediterránea de Chile central. Tanto la perforación de patagio como la tintura de pelo serían útiles en estudios de corto plazo (e.g., Bonaccorso et al. 1976; Montenegro & Romero-Ruz 1999), siendo visibles en alrededor de un 100% de los individuos marcados por periodos de seis y tres semanas, respectivamente.
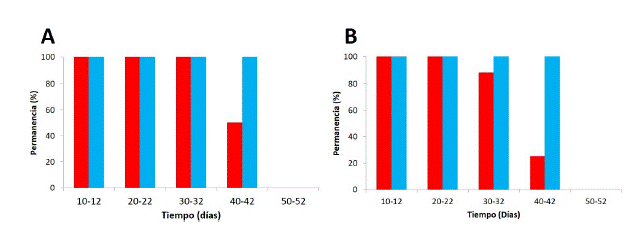
Fig. 3
Permanencia de marcas temporales (rojo: tintura; celeste: perforación del patagio) para las especies: (A) Myotis chiloensis y (B) Tadarida brasiliensis.
La perforación del patagio y la tintura de pelo presentaron una duración máxima similar. Sin embargo, los resultados muestran que la perforación del patagio fue visible por más tiempo en un mayor porcentaje de individuos marcados en comparación a la tintura de pelo, en ambas especies de murciélagos. No obstante, la duración de estos métodos de marcaje (ca. 6 semanas) fue menor a la registrada en otros estudios de murciélagos con marcas temporales (e.g., Bonaccorso et al. 1976; Amelon et al. 2017).
La permanencia de la perforación del patagio en todos los individuos recapturados alcanzó los 40-42 días, luego de esos días no fue visible de manera clara. Este período de duración fue menor a los 5 meses registrados por Bonaccorso et al. (1976) para Carollia perspicillata (Chiroptera: Phyllostomidae; 13.0-20.5 g). Sin embargo, esta especie de murciélago es de mayor tamaño que las nuestras y para la perforación del ala usaron un tatuador de oreja para ganado, herramienta que deja una perforación mucho más grande que la realizada en este estudio. Además, las diferencias en la visibilidad de este tipo de marcas pueden depender de la velocidad de cicatrización del patagio, ya que esta varía entre especies y temporadas (Ceballos-Vásquez et al. 2014). Si bien este método implica un daño temporal en el animal, alteraciones menores del patagio no influirían de manera importante en el comportamiento de los individuos (Voigt 2013). Además, en nuestro caso se produjo una rápida cicatrización de las perforaciones.
La permanencia de la tintura de pelo va disminuyendo con el transcurso de las semanas, siendo visible hasta por 30 días. Pasado este período de tiempo la intensidad del color es baja o no se ve. Esto indica que es un método útil en estudios de corto plazo en murciélagos. Nuestro resultado fue menor a las 15 semanas que registraron Wendeln et al. (1996) al usar tinturas repelentes al agua. No obstante, la tintura en el pelaje duró más tiempo de lo que el producto indicaba (2 semanas), probablemente debido a la ausencia de lavado del pelo. Sin embargo, como el producto es lavable, su durabilidad en zonas con mayor humedad debería validarse mediante otros estudios. Para zonas áridas y semiáridas sería un método adecuado y alternativo al uso de desinfectantes en spray como Larvispray® (e.g., Ossa et al. 2014), evitando así posibles efectos secundarios negativos que habitualmente produce el lindano (e.g., Sandu & Virsta 2015).
En conclusión, nuestros resultados permiten recomendar los métodos evaluados para estudios de corto plazo, como una alternativa más accesible y menos costosa que otros métodos de marcaje temporal, como por ejemplo las marcas para abejas (e.g., Kirkpatrick et al. 2019). Cuando se requiera la identificación a nivel individual, recomendamos el uso de la perforación del patagio como método de marcaje. En el caso de estudios que solo requieran identificar la procedencia del individuo (por ejemplo, movimiento entre dormideros o colonias), recomendamos el uso de tinturas, ya que es el método de marcaje menos invasivo, aunque su durabilidad debería validarse en climas más húmedos. Los resultados de nuestro trabajo contribuyen al desarrollo de métodos de monitoreo y seguimiento de las poblaciones de murciélagos en la zona central de Chile, área incluida dentro de un hotspot de biodiversidad del planeta.
Agradecimientos
Agradecemos a AngloAmerican-Los Bronces, al personal del Parque Etnobotánico Quilapilún y a todos los voluntarios que colaboraron en la toma de datos. La captura de animales se autorizó mediante la Res. Ex. 8152 del Servicio Agrícola y Ganadero.
REFERENCIAS
Amelon, S. K., S. E. Hooper, & K. M. Womack. 2017. Bat wing biometrics: using collagen–elastin bundles in bat wings as a unique individual identifier. Journal of Mammalogy 98(3): 744-751. https://doi.org/10.1093/jmammal/gyx018
Baker, G. B. et al. 2001. Wildlife Research 28(3):229.
Barclay, R. M., & G. P. Bell. 1988. Marking and observational techniques. Ecological and behavioral methods for the study of bats (eds.?). Smithsonian Institution Press, Washington DC, Estados Unidos.
Bonaccorso, F. J., & N. Smythe. 1972. Punch-marking bats: an alternative to banding. Journal of Mammalogy 53(2):389-390. https://doi.org/10.2307/1379186
Bonaccorso, F. J., N. Smythe, & S. R. Humphrey. 1976. Improved techniques for marking bats. Journal of Mammalogy 57:181-182. https://doi.org/10.2307/1379526
Braun, C. E. (ed.). 2005. Techniques for Wildlife Investigations and Management. Sixth Edition. The Wildlife Society, Bethesda, MD.
Canals, M., & P. E. Cattan. 2008. Radiografía a los murciélagos de Chile. Santiago de Chile: Universitaria.
CCAC (Canadian Council On Animal Care). 2003. CCAC species-specific recommendations on: BATS. Ottawa, Canada.
Ceballos-Vásquez, A., J. R. Caldwell, & P. A. Faure. 2014. Seasonal and reproductive effects on wound healing in the flight membranes of captive big brown bats. Biology Open 4(1):95-103. https://doi.org/10.1242/bio.201410264
CGA Ingenieros Consultores. 2015. Diagnóstico Comunal. Plan de Desarrollo Comunal 2015-2019. Ilustre Municipalidad de Colina, Colina, Chile.
De La Maza, M., & C. Bonacic. 2013. Manual para el monitoreo de fauna silvestre en Chile. Serie Fauna Australis, Facultad de Agronomía e Ingeniería Forestal. Pontificia Universidad Católica de Chile, San Joaquín, Chile. https://doi.org/10.7764/cdi.38.964
Department of Environment And Conservation. 2013. Standard Operating Procedure: Temporary Marking of Mammals, Reptiles and Birds. Perth, Australia.
Dietz, C., I. Dietz, T. Ivanova, & B. M. Siemers. 2006. Effects of forearm bands on horseshoe bats (Chiroptera: Rhinolophidae). Acta Chiropterologica 8(2):523-535. https://doi.org/10.3161/1733-5329(2006)8[523:eofboh]2.0.co;2
Ellison, L., T. O’shea, D. Neubaum, M. Neubaum, R. Pearce, & R. Bowen. 2007. A Comparison of conventional capture versus PIT reader techniques for estimating survival and capture probabilities of big brown bats Eptesicus fuscus. Acta Chiropterologica 9(1): 149-160. https://doi.org/10.3161/1733-5329(2007)9[149:acoccv]2.0.co;2
Faure, P. A., D. E. Re, & E. L. Clare. 2014. Wound healing in the flight membranes of big brown bats. Journal of Mammalogy 90:1148-1156. https://doi.org/10.1644/08-mamm-a-332.1
Fraser, E. E., F. J. Longstaffe, & M. B. Fenton. 2013. Moulting matters: the importance of understanding moulting cycles in bats when using fur for endogenous marker analysis. Canadian Journal of Zoology 91(8):533-544. https://doi.org/10.1139/cjz-2013-0072
Gajardo, R. 1994. La vegetación natural de Chile. Clasificación y distribución geográfica. Santiago, Chile.
Kirkpatrick, L., G. Apoznanski, L. De Bruyn, R. Gyselings, & T. Kokurewicz. 2019. Bee markers: a novel method for non-invasive short term marking of bats. Acta Chiropterologica 21(2):465-471. https://doi.org/10.3161/15081109acc2019.21.2.020
Manque Bioexploraciones. 2018. Informe de Línea Base Parque Etnobotánico Quilapilún, Los Bronces, Colina.
Montenegro, O., & M. Romero-Ruz. 1999. Murciélagos del sector sur de la Serranía de Chiribiquete, Caquetá, Colombia. Revista de la Academia Colombiana de Ciencias 23:641-649.
Ossa, G., C. Bonacic, & R. M. Barquez. 2014. First record of Histiotus laephotis (Thomas, 1916) from Chile and new distributional information for Histiotus montanus (Phillipi and Landbeck, 1861) (Chiroptera, Vespertilionidae). Mammalia https://doi.org/10.1515/mammalia-2014-0041.
O’Shea, T. J, L. E. Ellison, & T. R. Stanley. 2004. Survival estimation in bats: historical overview, critical appraisal, and suggestions for new approaches. Sampling Rare or Elusive Species (W. L. Thomson, ed.). Washington D.C, Estados Unidos: Island Press.
Richards, G. C., & L. S. Hall. 2012. A Natural History of Australian bats: working the night. CSIRO Publishing, Australia.
Rigby, E. L., J. Aegerter, M. Brash, & J. D. Altringham. 2012. Impact of PIT tagging on recapture rates, body condition and reproductive success of wild Daubenton’s bats (Myotis daubentonii). Veterinary Record 170:101. https://doi.org/10.1136/vr.100075
Rodríguez-Posada, M. E., & M. A. Santa-Sepúlveda. 2013. Reporte de lesiones en murciélagos causadas por el uso incorrecto de collares plásticos como método de marcaje. Therya 4(2):395-400. https://doi.org/10.12933/therya-13-124
Rodríguez-San Pedro, A., J. L. Allendes, P. Carrasco-Lagos, & R. A. Moreno. 2014. Murciélagos de la Región Metropolitana de Santiago, Chile. Seremi del Medio Ambiente Región Metropolitana de Santiago, Universidad Santo Tomás y Programa para la Conservación de los Murciélagos de Chile (PCMCh). https://doi.org/10.18273/revsal.v50n1-2018001
Sack, D. A., & D. W. Tripp. 2020. A comparison of Two Methods to Monitor Translocated Prairie Dogs. Wildlife Society Bulletin 44(2):416-423. https://doi.org/10.1002/wsb.1098
Sandu, M. A., & A. Virsta. 2015. Environmental toxicity of lindane and health effect. Journal of Environmental Protection and Ecology 16(3):933-944.
Sherwin, R. E., S. Haymond, D. Stricklan, & R. Olsen. 2002. Wildlife Capture and Monitoring-Freeze-branding to permanently mark bats. Wildlife Society Bulletin 30(1):97-100.
Van Harten, E. et al. 2019. High detectability with low impact: optimizing large PIT tracking systems for cavedwelling bats.Ecology and Evolution 9:10916-10928. https://doi.org/10.1002/ece3.5482
Voigt, C. C. 2013. Bat flight with bad wings: is flight metabolism affected by damaged wings? The Journal of Experimental Biology 216:1516-1521. https://doi.org/10.1242/jeb.079509
Wendeln, H., R. Nagel, & P. H. Becker. 1996. A Technique to Spray Dyes on Birds. Journal of Field Ornithology 67(3):442-446.
Información adicional
Editor asociado: Dra. Laura Guichón
Citar como: Puelma-Diez, F., N. R. Villaseñor & M. A. H. Escobar. 2021. Uso de dos marcas temporales en dos especies de murciélagos: Myotis chiloensis (Chiroptera: Vespertilionidae) y Tadarida brasiliensis (Chiroptera: Molossidae). Mastozoología Neotropical, 28(2):e0618. https://doi.org/10.31687/saremMN.21.28.2.14.e0618